LGR4/RSPO阻断剂与抗免疫检查点抑制剂联合用于肿瘤的免疫治疗的制作方法
本发明涉及免疫治疗领域,具体地涉及lgr4/rspo阻断剂与抗免疫检查点抑制剂联合用于肿瘤的免疫治疗。
背景技术:
恶性肿瘤,又称癌症,是当今严重危害人类健康的一类重大疾病。据世界卫生组织统计,全球每年恶性肿瘤发病超过800万例,且发病率总体仍然呈上升趋势。
在与恶性肿瘤的斗争历程中,人们开发和发展了多种应对恶性肿瘤的手段,从最初的手术切除,进一步发展到药物化疗,射线放疗,靶向治疗等方式,极大丰富了恶性肿瘤的治疗手段,也取得了显著的临床治疗效果,明显缓解了患者病症,改善其生活质量,延长存活时间。而近年来兴起的肿瘤免疫疗法,更是更新了人们的肿瘤治疗理念,该疗法的核心是唤起和调动机体自身的免疫系统来对抗、清除肿瘤细胞,最终抑制肿瘤的发生发展。
肿瘤微环境,尤其是其中发挥作用的免疫抑制性细胞和分子,成为制约当今众多免疫疗法疗效发挥的关键因素之一,自然成为人们关注以及试图改造的重点对象。存在于肿瘤微环境中的各类免疫细胞中,丰度最高,功能最为多样的是一类称作肿瘤相关巨噬细胞(tumorassociatedmacrophages,tam)的免疫细胞,这类细胞具有高度的异质性和可塑性,其多样的功能表型已经逐渐被揭示和证实,调节着肿瘤微环境的多种功能特性。tam可操控性的功能特性在肿瘤免疫疗法领域正日渐被人们所关注,并且已经有数种靶向于tam的药物进入临床前或临床试验。
tams是一类大量浸润于多种器官肿瘤组织中的单核巨噬细胞,大部分tam经由血液循环中的单核细胞迁移入肿瘤组织中而分化形成,经过与肿瘤组织内肿瘤细胞、内皮细胞及间质细胞的相互作用,即接受肿瘤内部环境的“re-education”,使tams表现为cd206表达显著升高,大量分泌il-10、tgf-β、vegf等细胞因子和生长因子的m2型巨噬细胞的表型,进而抑制抗肿瘤免疫应答,促进肿瘤组织内部的血管新生、上皮间质转换,最终促进了体内肿瘤的生长和转移
目前,美国食品与药品监督管理局(fda)已经批准了靶向的是细胞毒性t淋巴细胞抗原4(cytotoxict-lymphocyteantigen4)ctla-4以及程序性死亡受体1(programmeddeath1)pd-1及其配体pd-l1的单克隆抗体。上述免疫治疗手段采用单药或者联合用药方式,显示出惊人的临床效果。与传统抗肿瘤疗法中的化疗、放疗以及靶向治疗一样,作为新兴的治疗手段,免疫疗法也不可避免地存在一些局限性和有待完善的地方,主要体现在对于免疫疗法响应的恶性肿瘤还集中在白血病、黑素瘤、非小细胞肺癌(nsclc)等少数几种恶性肿瘤,且pd1抗体临床应答率仅在20~20%,大部分病人无效。
部分患者对于该类药物无响应或表现低响应,因此严重限制了该类药物对于特定类型肿瘤的广谱作用性。因而,本领域迫切希望找到提高该类药物临床响应率及治疗效果的可行性办法。
技术实现要素:
本发明的目的是提供一种lgr4/rspo阻断剂与抗免疫检查点抗体联合用于肿瘤的免疫治疗的方法。
本发明第一方面提供了一种产品组合,包括:
(i)第一药物组合物,所述第一药物组合物含有(a)第一活性成分,所述第一活性成分为lgr4/rspo阻断剂,以及药学上可接受的载体;和
(ii)第二药物组合物,所述第二药物组合物含有(b)第二活性成分,所述第二活性成分为抗免疫检查点的抑制剂,所述免疫检查点选自下组:pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb、或其组合;
以及药学上可接受的载体;
其中,所述的第一药物组合物和第二药物组合物为不同的药物组合物,或同一药物组合物。
在另一优选例中,所述lgr4/rspo阻断剂选自下组:
(a)特异性抑制lgr4表达和/或活性的拮抗剂;
(b)特异性抑制r-spondin表达和/或活性的拮抗剂;
(c)lgr4的结构类似物;
(d)r-spondin的结构类似物;
(e)上述各项的任意组合。
在另一优选例中,所述抑制剂选自下组:抗体、小分子化合物、或其组合。
在另一优选例中,所述的拮抗剂包括microrna、sirna、shrna、或其组合。
在另一优选例中,所述的拮抗剂包括抗体,较佳地为单克隆抗体。
在另一优选例中,所述的lgr4/rspo阻断剂为lgr4胞外段蛋白。
在另一优选例中,所述的lgr4胞外段蛋白包括胞外段蛋白全长蛋白、胞外段蛋白片段、包含lgr4胞外段蛋白的fc融合蛋白、包含lgr4胞外段蛋白的其他融合蛋白。
在另一优选例中,所述lgr4胞外段蛋白选自下组:ecd、包含ecd序列90%相似度的其他序列、或其组合。
在另一优选例中,所述的lgr4胞外段蛋白的氨基酸序列如seqidno.:1所示。
在另一优选例中,编码所述的lgr4胞外段蛋白的核苷酸序列如seqidno.:2所示。
在另一优选例中,所述的lgr4和r-spondin来源于人或非人哺乳动物。
在另一优选例中,所述lgr4/rspo阻断剂包括表达靶向rspondin的第一car和靶向肿瘤抗原的第二car的免疫细胞。
在另一优选例中,所述第一car和所述第二car的结构分别如式i和式ii所示:
l1-scfv1-z1-tm1-c1(i)
l2-scfv2-z2-tm2-c2-cd3ζ(ii)
式中,
各“-”独立地为连接肽或肽键;
l1和l2各自独立地为任选的信号肽序列;
scfv1和scfv2分别为靶向rspondin和肿瘤抗原的抗体单链可变区序列;和
z1和z2各自独立地为无或绞链区;
tm1和tm2各自独立地为跨膜结构域;
c1和c2各自独立地为共刺激信号分子;
cd3ζ为源于cd3ζ的胞浆信号传导序列。
在另一优选例中,所述的免疫细胞选自下组:
(i)嵌合抗原受体t细胞(car-t细胞);
(ii)嵌合抗原受体nk细胞(car-nk细胞);或
(iii)外源t细胞受体(tcr)t细胞(tcr-t细胞)。
在另一优选例中,所述第一car和第二car定位于所述免疫细胞的细胞膜。
在另一优选例中,所述免疫细胞的细胞膜上表达有所述第一car和所述第二car。
在另一优选例中,所述的l1和l2各自独立地为选自下组的蛋白的信号肽:cd8、cd28、gm-csf、cd4、cd137、或其组合。
在另一优选例中,所述的z1和z2各自独立地为选自下组的蛋白的铰链区:cd8、cd28、cd137、或其组合。
在另一优选例中,所述的tm1和tm2各自独立地为选自下组的蛋白的跨膜区:cd28、cd3epsilon、cd45、cd4、cd5、cd8、cd9、cd16、cd22、cd33、cd37、cd64、cd80、cd86、cd134、cd137、cd154、或其组合。
在另一优选例中,所述的c1和c2各自独立地为选自下组的蛋白的共刺激信号分子:ox40、cd2、cd7、cd27、cd28、cd30、cd40、cd70、cd134、4-1bb(cd137)、pd1、dap10、cds、icam-1、lfa-1(cd11a/cd18)、icos(cd278)、nkg2d、gitr、tlr2、或其组合。
在另一优选例中,所述组分(i)与组分(ii)的重量比为100:1-0.01:1,较佳地,10:1-0.1:1,更佳地,2:1-0.5:1。
在另一优选例中,所述产品组合中,所述lgr4/rspo阻断剂的含量为1%-99%,较佳地,10%-90%,更佳地,30%-70%。
在另一优选例中,所述产品组合中,所述抗免疫检查点的抗体的含量为1%-99%,较佳地,10%-90%,更佳地,30%-70%。
在另一优选例中,所述产品组合中,所述组分(i)和组分(ii)占所述产品组合总重的0.01-99.99wt%,较佳地0.1-90wt%,更佳地1-80wt%。
在另一优选例中,所述的药物组合物的剂型包括注射剂型、外用药物剂型和口服剂型。
在另一优选例中,所述药物组合物可以通过皮下注射、静脉注射、肌内注射的方式给药。
在另一优选例中,所述口服剂型包括片剂、胶囊剂、膜剂、和颗粒剂。
在另一优选例中,所述的药物组合物的剂型包括缓释型剂型、和非缓释型剂型。
本发明第二方面提供了一种组合物,包括:
(i)lgr4/rspo阻断剂;
(ii)抗免疫检查点的抑制剂,所述免疫检查点选自下组:pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb、或其组合;和
(iii)药学上可接受的载体。
在另一优选例中,所述抑制剂选自下组:抗体、小分子化合物、或其组合。
在另一优选例中,所述组合物中,所述组分(i)、组分(ii)占所述组合物总重的0.01-99.99wt%,较佳地0.1-90wt%,更佳地1-80wt%。
在另一优选例中,所述组合物还包括其他药物,所述其他药物用于(i)治疗肿瘤;(ii)抑制肿瘤生长;(iii)抑制肿瘤微环境中肿瘤相关巨噬细胞活性;和/或(iv)提高肿瘤对于抗免疫检查点疗法的敏感性。
在另一优选例中,所述其他药物选自下组:nivolumab、pembrolizumab、atezolizumab、avelumab、durvalumab、或其组合。
在另一优选例中,所述肿瘤包括实体瘤和血液瘤。
在另一优选例中,所述肿瘤选自下组:肺癌、黑色素瘤、结肠癌、肝癌、胃癌、非霍奇金淋巴瘤、前列腺癌、卵巢癌、乳腺癌、或其组合。
本发明第三方面提供了一种药盒,包括:
(a1)第一容器,以及位于所述第一容器中的lgr4/rspo阻断剂,或含有lgr4/rspo阻断剂的药物;
(a2)第二容器,以及位于所述第二容器中的抗免疫检查点的抑制剂,或含有抗免疫检查点的抑制剂的药物,其中,所述免疫检查点选自下组:pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb、或其组合。
在另一优选例中,所述药盒还含有(a3)第三容器,以及位于所述第三容器中的其他药物,所述其他药物用于(i)治疗肿瘤;(ii)抑制肿瘤生长;(iii)抑制肿瘤微环境中肿瘤相关巨噬细胞活性;和/或(iv)提高肿瘤对于抗免疫检查点疗法的敏感性。
在另一优选例中,所述的第一容器、第二容器和第三容器是相同或不同的容器。
在另一优选例中,所述的第一容器的药物是含lgr4/rspo阻断剂的单方制剂。
在另一优选例中,所述的第二容器的药物是含抗免疫检查点的抗体的单方制剂。
在另一优选例中,所述第三容器是含其他药物的单方制剂。
在另一优选例中,所述药物的剂型为口服剂型或注射剂型。
在另一优选例中,所述的试剂盒还含有说明书。
在另一优选例中,所述说明书记载了选自下组的一个或多个说明:
(a)将lgr4/rspo阻断剂和抗免疫检查点的抗体联用抑制肿瘤生长的方法;
(b)将lgr4/rspo阻断剂和抗免疫检查点的抗体联用抑制肿瘤相关巨噬细胞的促肿瘤功能的方法;
(c)将lgr4/rspo阻断剂和抗免疫检查点的抗体联用促进肿瘤微环境中cd8+t细胞的抗肿瘤活性的方法;
(d)将lgr4/rspo阻断剂和抗免疫检查点的抗体联用提高肿瘤对于抗免疫检查点疗法的敏感性的方法。
本发明第四方面提供了一种组合物的用途,所述组合物包括(i)lgr4/rspo阻断剂;和(ii)抗免疫检查点的抑制剂,所述免疫检查点选自下组:pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb、或其组合,用于制备一药物组合物或药盒,用于(i)治疗肿瘤;(ii)抑制肿瘤生长;(iii)抑制肿瘤微环境中肿瘤相关巨噬细胞的活性;和/或(iv)提高肿瘤对于抗免疫检查点疗法的敏感性。
在另一优选例中,所述lgr4/rspo阻断剂的作用浓度为1%-99%,较佳地,10%-90%,更佳地,30%-70%,以组合物的总浓度计。
在另一优选例中,所述抗免疫检查点的抗体的作用浓度为1%-99%,较佳地,10%-90%,更佳地,30%-70%,以组合物的总浓度计。
在另一优选例中,所述药物组合物或药盒包括(a)lgr4/rspo阻断剂和(b)抗免疫检查点的抗体;和(c)药学上可接受的载体;所述免疫检查点选自下组:pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb、或其组合。
在另一优选例中,所述药物组合物或药盒中,所述lgr4/rspo阻断剂占所述所述药物组合物或药盒总重的0.01-99.99wt%,较佳地0.1-90wt%,更佳地1-80wt%。
在另一优选例中,所述药物组合物或药盒中,所述抗免疫检查点的抗体占所述所述药物组合物或药盒总重的0.01-99.99wt%,较佳地0.1-90wt%,更佳地1-80wt%。
在另一优选例中,所述药盒还包括其他药物,所述其他药物用于(i)治疗肿瘤;(ii)抑制肿瘤生长;(iii)抑制肿瘤微环境中肿瘤相关巨噬细胞的活性;和/或(iv)提高肿瘤对于抗免疫检查点疗法的敏感性。
在另一优选例中,所述其他药物选自下组:nivolumab、pembrolizumab、atezolizumab、avelumab、durvalumab、或其组合。
本发明第五方面提供了一种(i)抑制肿瘤微环境中肿瘤相关巨噬细胞的活性;和/或(ii)提高肿瘤对于抗免疫检查点疗法的敏感性的方法,包括步骤:
给需要的对象施用(i)lgr4/rspo阻断剂;和(ii)抗免疫检查点的抑制剂,或本发明第一方面所述的产品组合或本发明第二方面所述的组合物或本发明第三方面所述的药盒,其中所述免疫检查点选自下组:pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb、或其组合。
在另一优选例中,所述对象包括人或非人哺乳动物。
在另一优选例中,所述非人哺乳动物包括啮齿动物和灵长目动物,优选小鼠、大鼠、兔、猴。
在另一优选例中,所述lgr4/rspo阻断剂抗免疫检查点的抗体同时或先后施用。
本发明第六方面提供了一种治疗肿瘤的方法,包括步骤:
给需要的对象施用(i)lgr4/rspo阻断剂;和(ii)抗免疫检查点的抑制剂,或本发明第一方面所述的产品组合或本发明第二方面所述的组合物或本发明第三方面所述的药盒,其中所述免疫检查点选自下组:pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb、或其组合。
在另一优选例中,所述对象包括人或非人哺乳动物。
在另一优选例中,所述非人哺乳动物包括啮齿动物和灵长目动物,优选小鼠、大鼠、兔、猴。
在另一优选例中,所述lgr4/rspo阻断剂抗免疫检查点的抗体同时或先后施用。
应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
附图说明
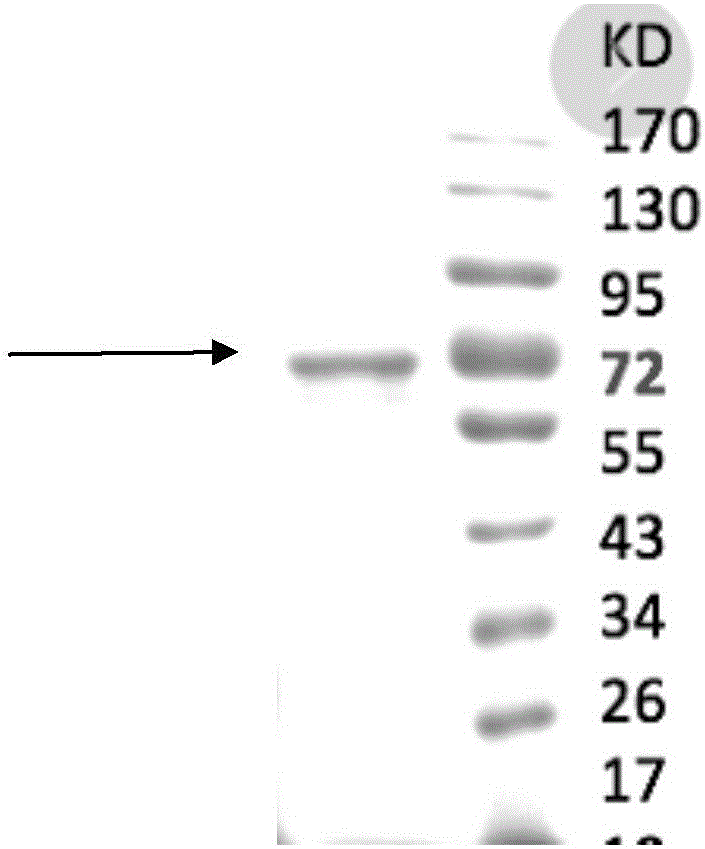
图1显示了lgr4ecd蛋白成功表达(请补充)。
图2显示了lgr4/rspo结合阻断剂lgr4ecd及rspo1抗体与pd1抗体联用能够更好的抑制肿瘤生长。
图3显示了lgr4/rspondin阻断剂lgr4-ecd和anti-rspondin1单抗协同anti-pd-1抗体改善小鼠b16f10黑色素瘤肿瘤微环境。
具体实施方式
本发明人经过广泛而深入地研究,首次意外地发现,联用lgr4/rspo阻断剂和抗免疫检查点抗体可有效用于(i)治疗肿瘤;(ii)抑制肿瘤生长;(iii)抑制肿瘤微环境中肿瘤相关巨噬细胞的活性;和/或(iv)提高肿瘤对于抗免疫检查点疗法的敏感性。在此基础上,本发明人完成了本发明。
本发明以car-t细胞为例,代表性地对本发明的工程化的免疫细胞进行详细说明。本发明的工程化的免疫细胞不限于上下文所述的car-t细胞,本发明的工程化的免疫细胞具有与上下文所述的car-t细胞相同或类似的技术特征和有益效果。具体地,当免疫细胞表达嵌合抗原受体car时,nk细胞等同于t细胞(或t细胞可替换nk细胞);当免疫细胞为t细胞时,tcr等同于car(或car可替换为tcr)。
术语
为了可以更容易地理解本公开,首先定义某些术语。如本申请中所使用的,除非本文另有明确规定,否则以下术语中的每一个应具有下面给出的含义。在整个申请中阐述了其它定义。
术语“约”可以是指在本领域普通技术人员确定的特定值或组成的可接受误差范围内的值或组成,其将部分地取决于如何测量或测定值或组成。
肿瘤相关巨噬细胞
肿瘤相关巨噬细胞(tumorassociatedmacrophages,tam)是一类被发现大量浸润于多种肿瘤发生部位的巨噬细胞,临床数据和动物实验都证明,肿瘤组织中的巨噬细胞与癌症患者或者荷瘤实验动物的存活率及预后情况密切相关。巨噬细胞根据其表型和功能可大致分为两个大类,即促炎抗肿瘤的m1型和抑炎促肿瘤的m2表型,且根据所接收刺激信号的不同,两型巨噬细胞之间可以相互转化,体现为巨噬细胞高度的异质性和可塑性。tam拥有大量与抗炎促肿瘤的m2型巨噬细胞相似的特征,能够抑制抗肿瘤的免疫应答,促进肿瘤细胞逃脱机体免疫监视;同时,通过分泌大量的il-10、tgf-β、vegf等细胞因子和生长因子,促进肿瘤组织内部的血管新生、纤维化、上皮间质转换等;tam还能够与周围的肿瘤细胞、基质细胞甚至其它的免疫细胞相互作用和通信,为肿瘤细胞的增殖、存活、侵袭、转移提供了良好的局部微环境。目前基于肿瘤相关巨噬细胞的肿瘤治疗方法已成为肿瘤免疫疗法领域极具吸引力的新方向,靶向肿瘤相关巨噬细胞的免疫疗法极具临床应用价值。
lgr4
lgr4全称为富含亮氨酸基序的g蛋白偶联受体4(leucine-richrepeat-containinggprotein-coupledreceptor4),也叫g蛋白偶联受体48(gproteincouplereceptor48),属于lgr类g蛋白偶联受体家族ⅱ,geneid:107515。
lgr4受体可以与r-spondin蛋白家族(r-spondin1-4)高特异性和高亲和力结合,其ic50仅为2-230nm,因而该分泌蛋白家族被视为lgr4的内源性配体。lgr4与r-spondin蛋白结合后可极大地增强经典的wnt/β-catenin信号通路,在成体干细胞和毛囊干细胞发育、骨骼细胞平衡、生殖道发育、眼睑发育甚至在巨噬细胞的模式识别过程中均发挥着重要的调节作用。然而,lgr4与r-spondin蛋白的结合并不能激活经典的g蛋白信号通路。已经证实,lgr4及其配体r-spondin蛋白在多种人类恶性肿瘤中异常表达,绝大多数情况下其表达均高于正常组织,包括肺癌,胃癌、结直肠癌、乳腺癌、前列腺癌等,lgr4/r-spondin通过wnt或者wnt相关信号通路促进肿瘤细胞的增殖生长。
申请人发现,相比于正常组织的巨噬细胞,lgr4在小鼠肺癌组织肿瘤相关巨噬细胞中也呈现上调表达,并且已经通过体内体外实验证实lgr4正调控巨噬细胞m2表型的功能极化,结合r-spondin在肺癌组织中以及lgr4在肺癌肿瘤相关巨噬细胞中的高度表达,预示着可以通过阻断肺癌组织中lgr4/r-spondin的相互作用,在直接作用于肿瘤细胞本身的同时通过调控肿瘤相关巨噬细胞的功能表型从而调控肿瘤细胞赖以生存的微环境,进而抑制肿瘤的发生发展,对于肿瘤的免疫治疗具有重大的应用价值和意义。
lgr4/rspo阻断剂
如本文所用,术语“lgr4/rspo阻断剂”指能够特异性抑制lgr4和r-spondin结合的制剂或组合物。所述lgr4/rspo阻断剂可以是小分子化合物,也可以是大分子物质(如抗体或可溶性蛋白),也可以是microrna、sirna、shrna等。代表性的lgr4/rspo阻断剂包括microrna、sirna、shrna、lgr4胞外蛋白ecd、抗r-spondin1抗体、r-spondin2抗体、r-spondin3抗体、r-spondin4抗体、抗lgr4抗体、特异性抑制lgr4和r-spondin的小分子化合物。
lgr4和r-spondin结合抑制剂
如本文所用,“lgr4和r-spondin结合抑制剂”、“抑制lgr4和r-spondin结合的抑制剂”可互换使用,是指能够特异性抑制lgr4和r-spondin结合的制剂或组合物。
在另一优选例中,所述的lgr4和r-spondin结合抑制剂为lgr4抑制剂、r-spondin抑制剂、lgr4结构类似物、和/或r-spondin结构类似物。
在另一优选例中,所述的lgr4和r-spondin结合抑制剂为seqidno.:1所示的lgr4胞外段蛋白。
在另一优选例中,所述的lgr4和r-spondin结合抑制剂为抗lgr4单克隆抗体和/或抗lgr4单克隆抗体。
rna干扰(rnai)
在本发明中,一类有效的lgr4和r-spondin结合抑制剂是干扰rna。
如本文所用,术语“rna干扰(rnainterference,rnai)”是指:一些小的双链rna可以高效、特异地阻断体内特定基因的表达,促使mrna降解,诱使细胞表现出特定基因缺失的表型,其也称为rna干预或者rna干涉。rna干扰是高度特异的在mrna水平上的基因沉默机制。
如本文所用,术语“小干扰rna(smallinterferingrna,sirna)”是指一种短片段双链rna分子,能够以同源互补序列的mrna为靶目标降解特定的mrna,这个过程就是rna干扰途径(rnainterferencepathway)。
在本发明中,干扰rna包括sirna、shrna以及相应的构建物。在本发明中,所述的干扰rna可以特异性地针对lgr4的干扰rna、和/或特异性针对r-spondin的干扰rna。优选地,所述的干扰rna可以特异性地针对lgr4与r-spondin的结合区域。
在本发明中,一种典型的shrna如式ii所示,
式中,
seq’正向为seq正向序列对应的rna序列或序列片段;
seq’反向为与seq’正向基本上互补的序列;
x’为无;或为位于seq’正向和seq’反向之间的间隔序列,并且所述间隔序列与seq’正向和seq’反向不互补,
||表示在seq正向和seq反向之间形成的氢键。
免疫检查点
免疫检查点是指免疫系统中存在的一些抑制性信号通路,通过调节外周组织中免疫反应的持续性和强度避免组织损伤,并参与维持对于自身抗原的耐受。利用免疫检查点的抑制性信号通路抑制t细胞活性是肿瘤逃避免疫杀伤的重要机制。因此,通过不同的策略增强t细胞的激活对肿瘤免疫治疗具有重要意义。本发明通过阻断(免疫检查点,如pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb等)信号来增强t细胞激活。
如本文使用,术语“pd-1”包括人pd-1(hpd-1),hpd-1的变体(突变的hpd-1)、同种型和物种同源物,以及与hpd-1具有至少80%、85%、90%、95%、96%、97%、98%、99%相同性的类似物。完整的hpd-1序列可以在genbank登录号u64863下找到。
在本发明中,代表性的抗免疫检查点的抗体包括抗pd-1抗体、pd-l1抗体、ctla-4抗体、tim3抗体、tigit抗体\icos抗体、lag3抗体、ox40抗体、cd47抗体、vista抗体、4-1bb抗体。
抗体
术语“抗体”(ab)应包括但不限于免疫球蛋白,其特异性结合抗原并包含通过二硫键互连的至少两条重(h)链和两条轻(l)链,或其抗原结合部分。每条h链包含重链可变区(本文缩写为vh)和重链恒定区。重链恒定区包含三个恒定结构域ch1、ch2和ch3。每条轻链包含轻链可变区(本文缩写为vl)和轻链恒定区。轻链恒定区包含一个恒定结构域cl。vh和vl区可以进一步细分为称为互补决定区(cdr)的高变区,其散布有更保守的称为框架区(fr)的区域。每个vh和vl包含三个cdr和四个fr,从氨基末端到羧基末端按照以下顺序排列:fr1,cdr1,fr2,cdr2,fr3,cdr3,fr4。重链和轻链的可变区含有与抗原相互作用的结合结构域。
抗体的制备
任何适于产生单克隆抗体的方法都可用于产生本发明的抗免疫检查点(如pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb)的抗体。例如,可以用连接或天然存在的免疫检查点(如pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb)同源二聚体或其片段免疫动物。可以使用合适的免疫接种方法,包括佐剂、免疫刺激剂、重复加强免疫接种,可以使用一种或多种途径。
任何合适形式的免疫检查点(如pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb)都可以作为免疫原(抗原),用于产生对免疫检查点(如pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb)特异的非人抗体,筛选所述抗体的生物学活性。激发免疫原可以是全长的成熟人免疫检查点(如pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb),包括天然的同源二聚体,或含单个/多个表位的肽。免疫原可以单独使用,或与本领域已知的一种或多种免疫原性增强剂组合使用。免疫原可以由天然来源纯化,或者在遗传修饰的细胞中产生。编码免疫原的dna在来源上可以是基因组或非基因组的(例如cdna)。可以使用合适的遗传载体表达编码免疫原的dna,所述载体包括但不限于腺病毒载体、腺相关病毒载体、杆状病毒载体、质粒和非病毒载体。
全人源化抗体可以选自任何种类的免疫球蛋白,包括igm、igd、igg、iga和ige。通过用下文实施例中描述的生物学测定筛选抗体易于实现必需恒定结构域序列的最优化,以产生所需生物学活性。
同样,任一类轻链都可以在本文的化合物和方法中使用。具体地说,κ、λ链或其变体在本发明的化合物和方法中是可以用的。
本发明抗体或其片段的dna分子的序列可以用常规技术,比如利用pcr扩增或基因组文库筛选等方法获得。此外,还可将轻链和重链的编码序列融合在一起,形成单链抗体。
一旦获得了有关的序列,就可以用重组法来大批量地获得有关序列。这通常是将其克隆入载体,再转入细胞,然后通过常规方法从增殖后的宿主细胞中分离得到有关序列。
此外,还可用人工合成的方法来合成有关序列,尤其是片段长度较短时。通常,通过先合成多个小片段,然后再进行连接可获得序列很长的片段。然后可将该dna序列引入本领域中已知的各种现有的dna分子(或如载体)和细胞中。
本发明还涉及包含上述的适当dna序列以及适当启动子或者控制序列的载体。这些载体可以用于转化适当的宿主细胞,以使其能够表达蛋白质。
宿主细胞为本领域常规的各种宿主细胞,只要能满足使上述重组表达载体稳定地自行复制,且所携带所述的核酸可被有效表达即可。具体地,宿主细胞可以是原核细胞,如细菌细胞;或是低等真核细胞,如酵母细胞;或是高等真核细胞,如哺乳动物细胞。优选的动物细胞包括(但并不限于):cho-s、cho-k1、hek-293细胞。
优选的宿主细胞包括e.colitg1或bl21细胞(表达单链抗体或fab抗体),或者cho-k1细胞(表达全长igg抗体)。
本发明中所述的用重组dna转化宿主细胞的步骤可用本领域熟知的技术进行。获得的转化子可用常规方法培养,转化子表达本发明的基因所编码的多肽。根据所用的宿主细胞,用常规培养基在合适的条件下培养。
通常,在适合本发明抗体表达的条件下,培养转化所得的宿主细胞。然后用常规的免疫球蛋白纯化步骤,如蛋白a-sepharose、羟基磷灰石层析、凝胶电泳、透析、离子交换层析、疏水层析、分子筛层析或亲和层析等本领域技术人员熟知的常规分离纯化手段纯化得到本发明的抗体。
所得单克隆抗体可用常规手段来鉴定。比如,单克隆抗体的结合特异性可用免疫沉淀或体外结合试验(如放射性免疫测定(ria)或酶联免疫吸附测定(elisa))来测定。
rspondin
rspondin是近年来新发现的蛋白家族,包括4个成员,分别为rspo1-4。rspo蛋白家族所有成员均为分泌性蛋白。
在本发明中首次发现,通过抑制rspo1-4与lgr4的结合,并同时与抗免疫检查点(如pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb)联用,从而有效(i)治疗肿瘤;(ii)抑制肿瘤生长;(iii)抑制肿瘤微环境中肿瘤相关巨噬细胞的活性;和/或(iv)提高肿瘤对于抗免疫检查点疗法的敏感性。
外源t细胞抗原受体
如本文所用,外源t细胞抗原受体(tcellreceptor,tcr)为通过基因转移技术从肿瘤反应性t细胞中克隆出tcr的α链和β链,通过基因工程的手段,以慢病毒或逆转录病毒为载体,外源性转入到t细胞内的tcr。
外源tcr修饰的t细胞能够特异性识别和杀伤肿瘤细胞,并通过优化tcr与肿瘤性特异性抗原的亲和力,可以提高t细胞与肿瘤的亲和力,提高抗肿瘤效果。
嵌合抗原受体(car)
嵌合免疫抗原受体(chimericantigenreceptors,cars)由胞外抗原识别区域,通常是scfv(single-chainvariablefragment),跨膜区以及胞内共刺激信号区域组成。cars的设计经历了以下过程:第一代car只有一个胞内信号组份cd3ζ或者fcγri分子,由于胞内只有一个活化结构域,因此它只能引起短暂的t细胞增殖和较少的细胞因子分泌,而并不能提供长时间的t细胞增殖信号和持续的体内抗肿瘤效应,所以并没有取得很好地临床疗效。第二代cars在原有结构基础上引入一个共刺激分子,如cd28、4-1bb、ox40、icos,与一代cars相比功能有很大提高,进一步加强car-t细胞的持续性和对肿瘤细胞的杀伤能力。在二代cars基础上串联一些新的免疫共刺激分子如cd27、cd134,发展成为三代和四代cars。
cars的胞外段可识别一个特异的抗原,随后通过胞内结构域转导该信号,引起细胞的活化增殖、细胞溶解毒性和分泌细胞因子,进而清除靶细胞。首先分离病人自体细胞(或者异源供体),激活并进行基因改造产生car的免疫细胞,随后注入同一病人体内。这种方式患移植物抗宿主病概率极低,抗原被免疫细胞以非mhc限制方式识别。
car-免疫细胞治疗在血液恶性肿瘤治疗中取得了非常高的临床反应率,这样的高反应率是以往任何一种治疗手段都无法达到的,在世界各引发了临床研究的热潮。
具体地,本发明的嵌合抗原受体(car)包括细胞外结构域、跨膜结构域、和细胞内结构域。胞外结构域包括靶-特异性结合元件(也称为抗原结合结构域)。细胞内结构域包括共刺激信号传导区和/或ζ链部分。共刺激信号传导区指包括共刺激分子的细胞内结构域的一部分。共刺激分子为淋巴细胞对抗原的有效应答所需要的细胞表面分子,而不是抗原受体或它们的配体。
在car的胞外结构域和跨膜结构域之间,或在car的胞浆结构域和跨膜结构域之间,可并入接头。如本文所用的,术语“接头”通常指起到将跨膜结构域连接至多肽链的胞外结构域或胞浆结构域作用的任何寡肽或多肽。接头可包括0-300个氨基酸,优选地2至100个氨基酸和最优选地3至50个氨基酸。
本发明的car当在t细胞中表达时,能够基于抗原结合特异性进行抗原识别。当其结合其关联抗原时,影响肿瘤细胞,导致肿瘤细胞不生长、被促使死亡或以其他方式被影响,并导致患者的肿瘤负荷缩小或消除。抗原结合结构域优选与来自共刺激分子和/或ζ链中的一个或多个的细胞内结构域融合。优选地,抗原结合结构域与4-1bb信号传导结构域和/或cd3ζ信号结构域组合的细胞内结构域融合。
如本文所用,“抗原结合结构域”“单链抗体片段”均指具有抗原结合活性的fab片段,fab’片段,f(ab’)2片段,或单一fv片段。fv抗体含有抗体重链可变区、轻链可变区,但没有恒定区,并具有全部抗原结合位点的最小抗体片段。一般的,fv抗体还包含vh和vl结构域之间的多肽接头,且能够形成抗原结合所需的结构。抗原结合结构域通常是scfv(single-chainvariablefragment)。scfv的大小一般是一个完整抗体的1/6。单链抗体优选是由一条核苷酸链编码的一条氨基酸链序列。作为本发明的优选方式,所述scfv包含特异性识别肿瘤高表达抗原cd47和msln的抗体,较佳地为单链抗体。
在本发明中,本发明的scfv还包括其保守性变异体,指与本发明scfv的氨基酸序列相比,有至多10个,较佳地至多8个,更佳地至多5个,最佳地至多3个氨基酸被性质相似或相近的氨基酸所替换而形成多肽。
在本发明中,所述添加、缺失、修饰和/或取代的氨基酸数量,优选为不超过初始氨基酸序列总氨基酸数量的40%,更优选为不超过35%,更优选为1-33%,更优选为5-30%,更优选为10-25%,更优选为15-20%。
在本发明中,所述添加、缺失、修饰和/或取代的氨基酸数量通常是1、2、3、4或5个,较佳地为1-3个,更佳地为1-2个,最佳地为1个。
对于绞链区和跨膜区(跨膜结构域),car可被设计以包括融合至car的胞外结构域的跨膜结构域。在一个实施方式中,使用天然与car中的结构域之一相关联的跨膜结构域。在一些例子中,可选择跨膜结构域,或通过氨基酸置换进行修饰,以避免将这样的结构域结合至相同或不同的表面膜蛋白的跨膜结构域,从而最小化与受体复合物的其他成员的相互作用。
本发明的car中的胞内结构域包括4-1bb的信号传导结构域和/或cd3ζ的信号传导结构域。
在本发明中,第一car和第二car的结构分别如式i和式ii所示:
l1-scfv1-z1-tm1-c1(i)
l2-scfv2-z2-tm2-c2-cd3ζ(ii)
式中,
各“-”独立地为连接肽或肽键;
l1和l2各自独立地为任选的信号肽序列;
scfv1和scfv2分别为靶向rspondin和肿瘤抗原的抗体单链可变区序列;和
z1和z2各自独立地为无或绞链区;
tm1和tm2各自独立地为跨膜结构域;
c1和c2各自独立地为共刺激信号分子;
cd3ζ为源于cd3ζ的胞浆信号传导序列。
嵌合抗原受体t细胞(car-t细胞)
如本文所用,术语“car-t细胞”、“car-t”、“本发明car-t细胞”均指本发明第一方面所述的car-t细胞,本发明car-t细胞可同时靶向rspondin和肿瘤抗原(如cd19、claudin18.2、egfr、her2、gpc3、nkg2d)。
本发明所述第一car和第二car表达后,会穿过细胞膜并定位在细胞膜上。
car-t细胞较其它基于t细胞的治疗方式存在以下优势:(1)car-t细胞的作用过程不受mhc的限制;(2)鉴于很多肿瘤细胞表达相同的肿瘤抗原,针对某一种肿瘤抗原的car基因构建一旦完成,便可以被广泛利用;(3)car既可以利用肿瘤蛋白质抗原,又可利用糖脂类非蛋白质抗原,扩大了肿瘤抗原的靶点范围;(4)使用患者自体细胞降低了排异反应的风险;(5)car-t细胞具有免疫记忆功能,可以长期在体内存活。
嵌合抗原受体nk细胞(car-nk细胞)
如本文所用,术语“car-nk细胞”、“car-nk”、“本发明car-nk细胞”均指本发明第一方面所述的car-nk细胞。本发明car-nk细胞可同时靶向rspondin和肿瘤抗原(如cd19、claudin18.2、egfr、her2、gpc3、nkg2d)。
自然杀伤(nk)细胞是一类主要的免疫效应细胞,通过非抗原特异性途径去保护机体免受病毒感染和肿瘤细胞的侵袭。通过工程化(基因修饰)的nk细胞可能获得新的功能,包括特异性识别肿瘤抗原的能力及具有增强的抗肿瘤细胞毒作用。
与自体car-t细胞相比,car-nk细胞还具有一下优点,例如:(1)通过释放穿孔素和颗粒酶直接杀伤肿瘤细胞,而对机体正常的细胞没有杀伤作用;(2)它们释放很少量的细胞因子从而降低了细胞因子风暴的危险;(3)体外极易扩增及发展为“现成的”产品。除此之外,与car-t细胞治疗类似。
外源t细胞抗原受体
如本文所用,外源t细胞抗原受体(tcellreceptor,tcr)为通过基因转移技术从肿瘤反应性t细胞中克隆出tcr的α链和β链,通过基因工程的手段,以慢病毒或逆转录病毒为载体,外源性转入到t细胞内的tcr。
外源tcr修饰的t细胞能够特异性识别和杀伤肿瘤细胞,并通过优化tcr与肿瘤性特异性抗原的亲和力,可以提高t细胞与肿瘤的亲和力,提高抗肿瘤效果。
复方药物组合物和药盒
本发明提供了含有活性成分(a)lgr4/rspo阻断剂;(b)为抗免疫检查点的抑制剂(包括抗体、小分子化合物等);以及(c)药学上可接受的载体的复方药物组合物。这类载体包括(但并不限于):盐水、缓冲液、葡萄糖、水、甘油、乙醇、粉剂、及其组合。药物制剂应与给药方式相匹配。本发明的药物组合物可以被制成针剂形式,例如用生理盐水或含有葡萄糖和其他辅剂的水溶液通过常规方法进行制备。诸如片剂和胶囊之类的药物组合物,可通过常规方法进行制备。药物组合物如针剂、溶液、片剂和胶囊宜在无菌条件下制造。本发明的药物组合也可以被制成粉剂用于雾化吸入。一种优选的剂型是注射制剂。此外,本发明药物组合物还可与其他治疗剂一起使用。
本发明还提供了一种可用于(i)治疗肿瘤;(ii)抑制肿瘤生长;(iii)抑制肿瘤微环境中肿瘤相关巨噬细胞的活性;和/或(iv)提高肿瘤对于抗免疫检查点疗法的敏感性的药盒,该药盒含有:
(a1)第一容器,以及位于所述第一容器中的lgr4/rspo阻断剂,或含有lgr4/rspo阻断剂的药物;和
(a2)第二容器,以及位于所述第二容器中的抗免疫检查点的抑制剂,或含有抗免疫检查点的抑制剂的药物,其中,所述免疫检查点选自下组:pd-1、pd-l1、ctla-4、tim3、tigit\icos、lag3、ox40、cd47、vista、4-1bb。
本发明的药物组合物和药盒适用于(i)治疗肿瘤;(ii)抑制肿瘤生长;(iii)抑制肿瘤微环境中肿瘤相关巨噬细胞的活性;和/或(iv)提高肿瘤对于抗免疫检查点疗法的敏感性。
本发明制剂可以每一天服用三次到每十天服用一次,或者以缓释方式每十天服用一次。优选的方式是每天服用一次,因为这样便于病人坚持,从而显著提高病人服药的顺应性。
服用时,极大多数病例一般每天应用的总剂量应低于(或少数病例等于或略大于)各个单药的每天常用剂量,当然,所用的活性成分的有效剂量可随给药的模式和待治疗的疾病的严重程度等而有所变化。
治疗方法
本发明还提供了用本发明的两种活性成分或相应的药物用于(i)治疗肿瘤;(ii)抑制肿瘤生长;(iii)抑制肿瘤微环境中肿瘤相关巨噬细胞的瘤活性;和/或(iv)提高肿瘤对于抗免疫检查点疗法的敏感性的方法。它包括给哺乳动物施用有效量的活性成分(a)lgr4/rspo阻断剂和活性成分(b)抗免疫检查点的抑制剂,或者施用含有所述活性成分(a)和活性成分(b)的药物组合物。
当本发明两种活性成分被用于上述用途时,可与一种或多种药学上可接受的载体或赋形剂混合,如溶剂、稀释剂等,而且可以用如下形式口服给药:片剂、丸剂、胶囊、可分散的粉末、颗粒或悬浮液(含有如约0.05-5%悬浮剂)、糖浆(含有如约10-50%糖)、和酏剂(含有约20-50%乙醇),或者以无菌可注射溶液或悬浮液形式(在等渗介质中含有约0.05-5%悬浮剂)进行非肠胃给药。例如,这些药物制剂可含有与载体混合的约0.01-99%,更佳地约为0.1%-90%(重量)的活性成分。
本发明的两种活性成分或药物组合物可以通过常规途径进行给药,其中包括(但并不限于):肌内、腹膜内、静脉内、皮下、皮内、口服、瘤内或局部给药。优选的给药途径包括口服给药、肌内给药或静脉内给药。
从易于给药的立场看,优选的药物组合物是液态组合物,尤其是注射剂。
此外,本发明的两种活性成分或药物还可与其他(i)治疗肿瘤;(ii)抑制肿瘤生长;(iii)抑制肿瘤微环境中肿瘤相关巨噬细胞的活性;和/或(iv)提高肿瘤对于抗免疫检查点疗法的敏感性的药物(如pd1/pd-l1抗体药物包括pembrolizumab、nivolumab、avelumab、atezolizumab、durvalumab等)联用。
本发明的主要优点包括:
(1)本发明首次发现,将lgr4/rspo阻断剂与抗免疫检查点抑制剂(如抗体)联用,可有效(i)治疗肿瘤;(ii)抑制肿瘤生长;(iii)抑制肿瘤微环境中肿瘤巨噬细胞的活性;和/或(iv)提高肿瘤对于抗免疫检查点疗法的敏感性。
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(newyork:coldspringharborlaboratorypress,1989)中所述的条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数是重量百分比和重量份数。
除非特别说明,否则本发明实施例中所用材料和试剂均为市售产品。
通用方法
小鼠b16f10黑色素瘤皮下移植模型及治疗实验
选取8周龄左右雄性c57bl/6小鼠分为7组,每组9-10只小鼠。戊巴比妥钠麻醉,用刮毛器除去背部毛发,随后每只小鼠经皮下在左侧背部注射2×105b16f10细胞。从注射肿瘤细胞后第二天开始,分别给以上7组小鼠右侧背部皮下或腹腔(anti-pd-1抗体)给药,每隔两天给药一次。连续给药5次,于注射肿瘤细胞后第十天开始用游标卡尺测量小鼠肿瘤体积,采用肿瘤体积=长×宽2,2的计算公式,绘制小鼠生存曲线。(详细剂量、单药、联药以及分组已在上文“实验结果”部分述及,此不再赘述)。lgr4-ecd和anti-rspondin1单抗协同增强anti-pd-1抗体的对小鼠b16f10黑色素瘤的治疗效果
我们将b16f10黑色素瘤模型的成瘤小鼠分为如下组别:
1、无菌pbs缓冲液组
2、无关igg对照组
3、lgr4-ecd单药组
4、anti-rspondin1抗体单药组
5、anti-pd-1单抗单药组
6、lgr4-ecd+anti-pd-1单抗联药组
7、anti-rspondin1单抗+anti-pd-1单抗联药组
随后施以相应的药物注射处理,其中lgr4-ecd和anti-rspondin1单抗采用皮下注射给药,而anti-pd-1抗体采取腹腔注射给药。药物剂量为lgr4-ecd:50μg/小鼠;anti-rspondin1:100μg/小鼠;anti-pd-1单抗:200mg/kg体重。每3天给药,总共给药5次。记录统计个组小鼠肿瘤体积大小情况及生存时间。如(图2)所示,无论是单药组还是联药做,阻断rspondin/lgr4同样会显著抑制b16f10黑色素瘤的生长。而相比于,anti-pd-1抗体单药组,与lgr4-ecd以及anti-rspondin1单抗的联合使用可以明显协同增强其抗肿瘤
实施例1lgr4原核表达载体的构建以及lgr4胞外段蛋白表达纯化
lgr4原核表达载体为申请人前期构建,所用表达载体骨架为pet28a(+),通过基因工程操作技术将lgr4基因的多核苷酸序列连入其多克隆位点,表达后,目的蛋白lgr4胞外段蛋白n端融合表达6×his标签蛋白。重组质粒转化bl21大肠杆菌,涂带卡那霉素抗性的lb琼脂糖培养板,过夜培养后,挑取单克隆阳性菌落,置于含卡那霉素抗性的lb液体培养基摇床培养过夜,将过夜菌液全部转入1l含卡那霉素抗性的新鲜lb液体培养基中,37℃,220rpm/min摇床摇菌。随时用分光光度计监测菌液od值,待菌液od值达到0.6-0.8时,加入1ml0.8m的iptg进行诱导表达。诱导前取1ml菌液2000rpm/min离心两分钟,弃上清,往菌体中加入100μl1×sdsloadingbuffer,100℃水浴锅煮样10分钟,作为未诱导对照组,iptg诱导表达时间为4小时。
菌体收集及裂解:诱导结束后,将菌液分批次以11000rpm/min离心15分钟,弃上清,挑取少量菌体加入100μl1×sdsloadingbuffer,100℃水浴锅煮样10分钟,作为诱导对照组。剩余菌体加入20ml的裂解缓冲液(相关配方见下文,以下所用试剂同),漩涡振荡器充分摇匀,与-80℃冰箱反复冻融3次后,将菌液置于冰上进行超声破碎,破碎条件为:400w,每次超声时间5秒钟,间歇5秒钟,次数为300次,超声破碎前,往菌液中加入1ml蛋白酶抑制剂cocktail(美国selleckchem公司,100×储液)。
蛋白收集及纯化:将经超声破碎后的菌液11000rpm/min离心10分钟,小心吸出上清,分别取少量沉淀及上清,加入100μl1×sdsloadingbuffer,100℃水浴锅煮样10分钟,留作电泳上样,分泌表达蛋白主要存在于上清,包涵体表达时蛋白则主要存在于沉淀中。
由于目的蛋白融合表达6×his标签蛋白,故可用镍柱亲和层析法纯化目的蛋白,所用镍柱为qiagen公司生产的ni-ntaagarose纯化beads。蛋白纯化前:
清洗镍柱:所用ni-ntaagarose以20%乙醇溶液浸泡于4℃条件保存。使用前往塑料柱中灌注4mlni-ntaagarosebeads,稍作沉降,再往柱子中加满双脱水过柱清洗2次,弃流出液,以上操作于4℃条件下进行。
平衡镍柱:往清洗后的镍柱中加满平衡缓冲液,弃流出液,以上操作于4℃条件下进行。
蛋白样过柱纯化:将样品液小心灌满柱子,分多次灌注,静置过柱,弃流出液,以上操作于4℃条件下进行。
洗涤镍柱:样品过柱结束后,往镍柱中加满洗涤缓冲液,静置过柱,重复两次,弃流出液,以上操作于4℃条件下进行。
洗脱蛋白:往洗涤后的镍柱中加2ml洗脱缓冲液,收集流出液,于4℃条件下进行。
蛋白浓缩及保存:选择7okd规格的浓缩超滤管(购自美国millipore公司),使用前以双脱水清洗两次,清洗过程:4℃离心,6000rpm/min,5分钟。
加入蛋白样品,6000rpm/min离心20分钟后,倒掉收集管底部废液,往超滤管中补加无菌的pbs缓冲液,加满为止,继续离心,如此重复2次,最终使pbs缓冲液替换掉洗脱液中的咪唑。
浓缩结束后,超滤管上层中剩余液即为浓缩的目的蛋白,bca法测定总蛋白浓度后,分装保存于-80摄氏度超低分冰箱,使用时避免反复冻融。
本实例中所使用相关试剂及其配方如下:
裂解缓冲液:50mmtris,300mmnacl,ph8.0
洗涤缓冲液:50mmnah2po4,300mmnacl,ph8.0
洗脱缓冲液:50mmnah2po4,300mmnacl,250mm咪唑,ph8.0
平衡缓冲液:50mmnah2po4,300mmnacl,20mm咪唑,ph8.0
如图1所示,表达出的lgr4-ecd蛋白分子量大小为72kd左右,纯度高(高达92%),无杂带。
实施例2lgr4/rspondin阻断剂协同pd-1抗体抗肿瘤作用
lgr4-ecd能够阻断lgr4与rspondin1、rspondin2、rspondin3、rspondin4的相互作用,rspondin1抗体能够阻断lgr4与rspondin1的相互作用。
本发明利用c57bl/6小鼠建立了b16f10的皮下黑色素瘤模型,并对肿瘤体积均一一致的成瘤小鼠分别施以lgr4-ecd、anti-rspondin1单克隆抗体,anti-pd-1单克隆抗体的单药及联合用药处理,以检测和评估rspondin/lgr4信号的阻断对于anti-pd-1单克隆抗体治疗效果的协同作用。
结果如图2所示。结果显示,lgr4/rspondin阻断剂lgr4-ecd能够显著增强免疫检查点pd-1抗体的抗肿瘤作用,延长荷瘤小鼠生存期;lgr4/rspondin阻断剂rspo1抗体也可以显著增强免疫检查点pd-1抗体的抗肿瘤作用,延长荷瘤小鼠生存期。
实施例3lgr4/rspondin阻断剂lgr4-ecd和anti-rspondin1单抗协同anti-pd-1抗体改善小鼠b16f10黑色素瘤肿瘤微环境
将各组小鼠肿瘤组织分离消化制成单细胞悬液后进行浸润免疫细胞的流式细胞分析,以评价经lgr4-ecd、anti-rspondin1单抗以及anti-pd-1单抗单药或者联药作用后,肿瘤组织中免疫细胞构成的变化。本发明发现,与前文已述及的作用一致,lgr4-ecd和anti-rspondin1单抗同样引起肿瘤微环境中tamm2比例降低,降了3.7-4.7倍,请补充(图3-a),并且明显协同增强了anti-pd-1单抗引起的肿瘤组织中干扰素伽马阳性ifn-γ(+)及颗粒酶b阳性(gzmb+)的激活型cd8t细胞浸润的增多,增多了1.7及5.2倍,(图3-c、d)。同样地,无论是单独用药还是与anti-pd-1单抗联合用药,lgr4-ecd以及anti-rspondin1单抗均明显减少了肿瘤组织中cd11b+ly6g+mdsc的浸润(图3、b),这充分说明了阻断rspondin/lgr4信号对肿瘤微环境的调节作用。
在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
序列表
<110>上海邦耀生物科技有限公司
<120>lgr4/rspo阻断剂与抗免疫检查点抑制剂联合用于肿瘤的免疫治疗
<130>p2018-0209
<160>2
<170>patentinversion3.5
<210>1
<211>501
<212>prt
<213>智人(homosapiens)
<400>1
leucysalaalaprocyssercysaspglyaspargargvalaspcys
151015
serglylysglyleuthralavalprogluglyleuseralaphethr
202530
glnalaleuaspilesermetasnasnilethrglnleuprogluasp
354045
alaphelysasnphepropheleuglugluleuglnleualaglyasn
505560
aspleuserpheilehisprolysalaleuserglyleulysgluleu
65707580
lysvalleuthrleuglnasnasnglnleulysthrvalproserglu
859095
alaileargglyleuseralaleuglnserleuargleuaspalaasn
100105110
hisilethrservalprogluaspserphegluglyleuvalglnleu
115120125
arghisleutrpleuaspaspasnileleuthrgluvalprovalarg
130135140
proleuserasnleuprothrleuglnalaleuthrleualaleuasn
145150155160
asnileserserileproaspphealaphethrasnleuserserleu
165170175
valvalleuhisleuhisasnasnlysilelysserleuserglnhis
180185190
cyspheaspglyleuaspasnleugluthrleuaspleuasntyrasn
195200205
asnleuaspglupheproglnalailelysalaleuproserleulys
210215220
gluleuglyphehisserasnserileservalileproaspglyala
225230235240
phealaglyasnproleuleuargthrilehisleutyraspasnpro
245250255
leuserphevalglyasnseralaphehisasnleuseraspleuhis
260265270
serleuvalileargglyalaserleuvalglntrppheproasnleu
275280285
alaglythrvalhisleugluserleuthrleuthrglythrlysile
290295300
serserileproaspaspleucysglnasnglnlysmetleuargthr
305310315320
leuaspleusertyrasnaspileargaspleuproserpheasngly
325330335
cysargalaleuglugluileserleuglnargasnglnileserleu
340345350
ilelysgluthrthrpheglnglyleuthrserleuargileleuasp
355360365
leuserargasnleuilearggluilehisserglyalaphealalys
370375380
leuglythrilethrasnleuaspvalserpheasngluleuthrser
385390395400
pheprothrgluglyleuasnglyleuasnglnleulysleuvalgly
405410415
asnpheglnleulysaspalaleualaalaargaspphealaasnleu
420425430
argserleuservalprotyralatyrglncyscysalaphetrpgly
435440445
cysaspsertyralaasnleuasnthrgluaspasnserproglnasp
450455460
hisservalthrlysglulysglyalathraspalaalaasnalathr
465470475480
serthralagluserglugluhisserglnileileilehiscysthr
485490495
proserthrglyala
500
<210>2
<211>1503
<212>dna
<213>智人(homosapiens)
<400>2
ctctgcgctgcgccctgcagctgcgacggcgaccgtcgggtggactgctccgggaagggg60
ttgacggcggtaccggaggggctcagcgccttcacccaagcactggatatcagtatgaac120
aatatcactcagttaccagaagatgcatttaagaattttccttttctagaggagctacaa180
ctggctggtaacgacctttcttttatccacccaaaagccttgtctgggttgaaagaactc240
aaagtcctaaccctccagaacaatcagttgaaaacagtacccagtgaagccattcgtgga300
ctgagtgctttgcagtctctacgcttagatgccaaccatattacctcagtcccggaggac360
agttttgaagggctcgttcagttgcggcatctgtggctggatgacaacatcttgacggaa420
gtgcctgtgcgtccgctcagcaacctgccaaccctgcaggcgctgaccttggctctcaac480
aacatctcaagcatccccgacttcgcattcaccaacctttcaagcttggtagtgctgcat540
cttcataacaataaaattaaaagcctcagtcaacactgttttgatggactagataacctg600
gaaaccctggacttgaattataataacttggatgaatttcctcaggctattaaagccctt660
cccagccttaaagagctgggatttcacagtaattctatttctgttatcccggatggagca720
tttgctggtaatccactgctaagaactatccatttgtatgataatcctctgtcttttgtg780
gggaactcagcatttcacaacctgtctgatctgcattccttagtcattcgtggtgcaagc840
ctggtgcagtggttccccaatctggccggaactgtccatctggagagtctaaccttgaca900
gggacaaaaataagcagcatacctgatgatctgtgccaaaaccaaaagatgctgcggact960
ctggacttatcttataacgatataagagaccttccaagttttaatggttgtcgtgcattg1020
gaagaaatttcattgcagcgtaatcaaatctccctgataaaggaaactacttttcaaggc1080
ctaacatccctaaggattctagatctgagtagaaacctgattcgtgaaattcacagtgga1140
gcttttgcgaagcttgggacaattactaacctggatgtgagtttcaatgaattaacctca1200
tttcctacggaaggcctgaatgggctcaatcaacttaaacttgtgggtaacttccagctg1260
aaagatgccttggcagccagagactttgccaatctcaggtctctatcagtaccatatgct1320
tatcagtgttgtgcattttgggggtgtgactcttatgcaaatttaaacacagaagataac1380
agcccccaagaccacagtgtgacaaaagagaaaggtgctacagatgcagcaaatgccacc1440
agcactgctgaaagtgaagaacatagccaaataatcatccattgtacaccttcaacaggt1500
gct1503
- 还没有人留言评论。精彩留言会获得点赞!
- SPNP‑I在制备Nav1.7通道工具试剂中的应用的制造方法与工艺
- SPNP‑I在制备Nav1.2通道工具试剂中的应用的制造方法与工艺
- SPNP‑IX在制备Nav1.3通道抑制剂中的应用的制造方法与工艺
- SPNP‑IX在制备Kv4.2通道工具试剂中的应用的制造方法与工艺
- SPNP‑IX在制备Kv4.3通道工具试剂中的应用的制造方法与工艺
- SPNP‑27在制备Nav1.5通道抑制剂中的应用的制造方法与工艺
- SPNP‑27在制备Nav1.3通道抑制剂中的应用的制造方法与工艺
- 一种多肽在制备Nav1.3钠通道工具试剂中的应用的制造方法与工艺
- SPKP‑XI在制备Kv4.2通道抑制剂中的应用的制造方法与工艺
- SGLT‑2糖尿病抑制剂及其中间体的制备方法与流程