一种化合物在制备抑制人类免疫缺陷病毒感染药物中的应用的制作方法
本发明属于医药技术领域,具体的涉及一种化合物在制备抑制人类免疫缺陷病毒感染的整合酶(integrase,in)-ledgf/p75相互作用药物应用。
背景技术:
人类免疫缺陷病毒(humanimmunodeficiencyvirus,hiv),是造成人类免疫系统缺陷的一种病毒,主要攻击人体的辅助t淋巴细胞系统,一旦侵入机体细胞,病毒将会和细胞整合在一起终生难以消除;广泛存在于感染者的血液、精液、阴道分泌物、乳汁、脑脊液、有神经症状的脑组织液中,其中以血液、精液、阴道分泌物中浓度最高;对外界环境的抵抗力较弱,感染者潜伏期长、死亡率高。hiv-1in是抗hiv-1药物研发的有效靶标。目前,临床上使用的3个in抑制剂雷特格韦(raltegravir,ral)、埃替格韦(elvitegravir,evg)和度鲁特韦(dolutegravir,dtg),均为in链转移反应抑制剂(integrasestrandtransferinhibitors,instis)。由于hiv-1的遗传多样性以及快速适应环境变化的能力,接受第一代整合酶抑制剂ral和evg治疗的患者,其体内很快就出现了耐药性突变病毒株。最近,宣称具有较高耐药基因屏障(geneticbarrierrtoresistance)的第二代in抑制剂dtg,其使用者体内也出现了耐药性突变病毒株。因此,寻找新的作用机制靶点以开发新的in抑制剂显得尤为迫切和重要。
hiv-1的基因组很小(约为10kb),病毒需要依赖宿主细胞蛋白及其信号通路完成自身复制。其中关键的一步是hiv-1rna逆转录后产生的cdna整合到宿主染色体形成前病毒,病毒的整合包含多个反应步骤,每一步反应的完成都需要宿主蛋白的辅助才能完成,这些参与整合的宿主蛋白称为整合辅因子(integrationcofactors,incfs)。研究认为,incfs具有以下功能:参与催化;核输入;整合位点定位;单链dna缺口的修复。目前,研究最为清楚的incf为晶状体上皮源性生长因子p75蛋白(lensepithelium-derivedgrowthfactor,ledgf/p75)。ledgf/p75是首个被发现的能与hiv-1in发生蛋白相互作用(protein-proteininteraction,ppi)的宿主蛋白。该ppi主要由ledgf/p75蛋白c端in结合区(integrase-bindingdomain,ibd)与hiv-1in催化核心区(catalyticcoredomain,ccd)作用形成,研究表明该蛋白相互作用是开发抗hiv药物的有效靶点。
目前国外许多医药公司和科研机构正在开发新的具有干扰in-ledgf/p75相互作用的抗hiv-1抑制剂,但目前还没有成功上市的该类抑制剂。因此,积极寻找和设计新的in-ledgf/p75相互作用抑制剂,具有重要的临床意义和广阔的应用前景。
技术实现要素:
本发明的目的在于提供一种化合物作为整合酶-ledgf/p75相互作用抑制剂用于抗hiv-1感染的应用。
本发明提供一种式i所示结构的化合物及其药学上可接受的盐在制备抑制人类免疫缺陷病毒感染相关疾病的整合酶与整合辅因子相互作用的药物中的应用,所述式i化合物结构中的r1为羟基或3,4,5-三羟基苯甲酰氧基;r2为顺式3,4-二羟基苯基、反式3,4-二羟基苯基、顺式3,4,5-二羟基苯基
式i所示化合物的结构为:
优选的本发明所述整合辅因子为人晶状体上皮源衍生因子p75蛋白。
优选的本发明所述的人类免疫缺陷病毒感染为1型人免疫缺陷病毒,相关疾病为获得性免疫缺陷综合征。
本发明所述药学上可接受的盐为式i合物与无机酸或有机酸形成的酸加成盐,所述无机酸为盐酸、磷酸或硫酸中的一种或多种,所述有机酸为醋酸、马来酸、枸橼酸、苯磺酸、甲基苯磺酸、富马酸或酒石酸中的一种或多种。
本发明所述药物为式i化合物或其药学可接受的盐和一种或多种药学上可接受的载体制成的药物,所述载体包括药学领域常规的稀释剂、赋形剂、填充剂、粘合剂、湿润剂、崩解剂、吸收促进剂、表面活性剂、吸附载体、润滑剂等。所述药物的剂型为片剂、胶囊剂、颗粒剂、丸剂或其他可制备的常规剂型,上述各种剂型的药物均可以按照药学领域的常规方法制备。
本发明的新颖之处和优点在于:
1)本发明首次将儿茶素、表儿茶素、表没食子儿茶素和表没食子儿茶素没食子酸酯作为整合酶-ledgf/p75相互作用抑制剂;
2)本发明测试了儿茶素类4个化合物,包括儿茶素、表儿茶素、表没食子儿茶素和表没食子儿茶素没食子酸酯,抑制整合酶与ledgf/p75相互作用的抑制活性,并且计算了他们各自对该相互作用抑制率达到50%的化合物浓度,抑制整合酶-ledgf/p75的活性实验,发现其具有较好的抑制活性。
3)儿茶素、表儿茶素、表没食子儿茶素和表没食子儿茶素没食子酸酯作为传统饮品中的成分,经过长时间的使用,安全性高适合制备安全、有效的用于人类免疫缺陷病毒感染相关疾病的治疗。
附图说明
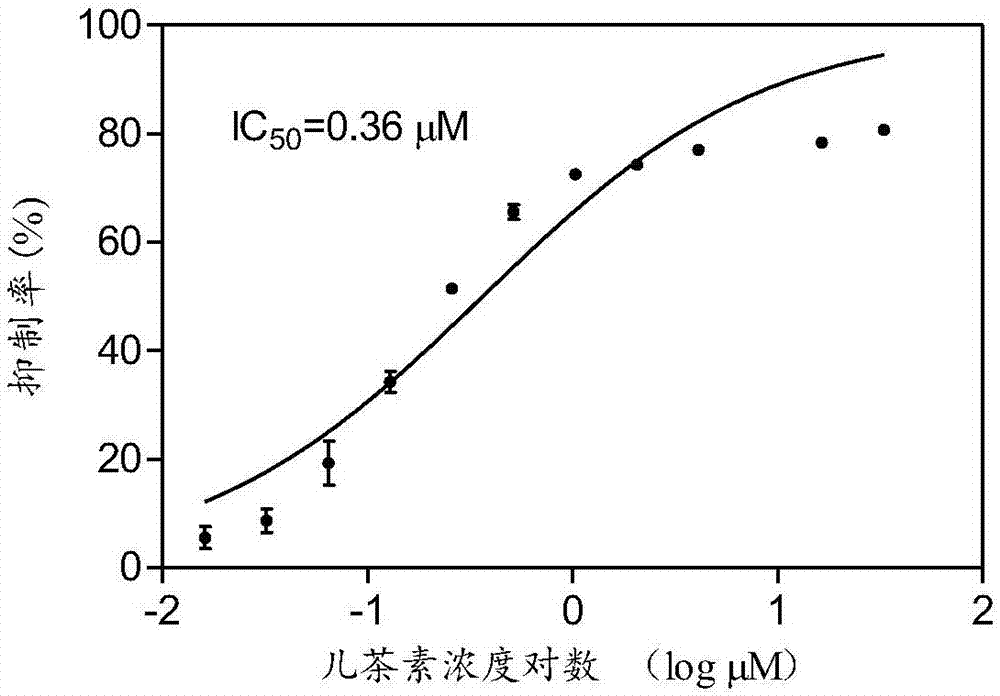
图1:儿茶素半数抑制浓度曲线图。
图2:表儿茶素半数抑制浓度曲线图。
图3:表没食子儿茶素半数抑制浓度曲线图。
图4:表没食子儿茶素没食子酸酯半数抑制浓度曲线图。
图5:儿茶素与in亲和力的测定。
图6:表儿茶素与in亲和力的测定。
图7:表没食子儿茶素与in亲和力的测定。
图8:表没食子儿茶素没食子酸酯与in亲和力的测定。
具体实施方式
为了证实本发明化合物的抑制整合酶与ledgf/p75相互作用的抑制活性,下面用儿茶素、表儿茶素、表没食子儿茶素和表没食子儿茶素没食子酸酯四种化合物(以下简称化合物)进行试验例,并结合附图对本发明做出进一步的描述。
试验例一、化合物对hiv-1整合酶-ledgf/p75相互作用的抑制活性测定
1、实验原理:当c端带有his标签的in蛋白和n端带有gst标签的ledgf/p75蛋白相互作用时(空间距离小于10nm),anti-6his-xl665受体磁珠和anti-gstcryptate供体磁珠也会相应靠近,从而发生共振能量转移(fret)现象。供体磁珠荧光分子的激发将诱发受体分子发出荧光,同时供体荧光分子自身的荧光强度衰减。当抑制剂分子阻断in分子间的二聚化作用时,fret现象减弱。因此,fret现象的强弱可以反映抑制剂分子对两个蛋白相互作用抑制作用的强弱。
2.实验材料:anti-6his-xl665微珠(cisbio,法国)、anti-gst-cryptate微珠(cisbio,法国)、384孔聚丙烯浅孔微孔板(perkinelmer,美国)
3、实验步骤
反应在384孔板中进行。将以下成分加入板孔中:30nmgst-in、30nmin-his6、化合物、反应buffer,混匀。室温,200rpm,反应1.5h。将用0.45nm的eu3+cryptateconjugatedmousemonoclonalantibodyanti-glutathiones-transferase和10nm的xl665-conjugatedmousemonoclonalantibodyanti-6histidine加入板孔,室温反应1.5小时。使用珀金埃尔默仪器有限公司(perkinelmerlifesciences)的多功能酶标仪envision2102multilabelreader,以320nm为激发光,读取665nm和620nm处的发射光。
4、数据处理
1)根据公式计算各孔665nm和620nm处荧光强度的比值(ration665/610);
2)根据公式计算各孔的相对抑制率
活性样品进行浓度稀释后检测的相对抑制率值,使用graphpad软件作图求算半数抑制浓度ic50值。
5、实验结果:化合物儿茶素、表儿茶素、表没食子儿茶素和表没食子儿茶素没食子酸酯的起始浓度为20μm,倍比稀释至0.01μm,进行抑制整合酶-ledgf/p75的活性实验,发现其具有较好的抑制活性,其半抑制浓度ic50分别为0.36μm,0.74μm,1.1μmand1.3μmrespectively.,曲线图参见图1-图4。
试验例二、化合物与in作用亲和力的测定。
1.实验原理:在光纤制成的生物传感器底端覆盖生物分子相容层,偶联in后形成生物膜层,进而用配体与小分子反应。小分子结合传感器底端偶联的配体时会导致生物膜层厚度增加,反射光干涉光谱曲线将产生迁移,仪器可以实时监测相位移的变化,并将其转化为可衡量分子间相互作用大小的参数。
2.实验步骤:生物膜干涉实验(bio-layerinterferometry,bli)在octetred96系统中完成。实验采用与仪器匹配的96孔板(fluotrace600,lote110103s),反应体积为200μl。将生物素化的in于固定到包被有链霉亲和素标的探针上,在缓冲液中浸泡10min。进行第一次基线扫描步骤,时间100s;将探针依次转移至含有不同终浓度的化合物中,结合,时间60s;最后将探针转移至缓冲液中进行解离步骤,时间40s。
3.数据处理:结合动力学参数利用dataanalysis(fortebio,7.1版)进行数据分析。
4、实验结果:化合物儿茶素、表儿茶素、表没食子儿茶素和表没食子儿茶素没食子酸酯与整合酶的亲和力分别为1.92μm,0.22μm,1.02μm和0.56μm。
- 还没有人留言评论。精彩留言会获得点赞!