一种海洋来源的二苯醚类活性成分在制备治疗Ⅱ糖尿病药物中的应用的制作方法
本发明涉及天然药物化学领域,具体涉及一类源于海洋真菌代谢的二苯醚类活性成分,在制备治疗ii糖尿病药物中的应用,属于天然药物领域。
背景技术:
ii糖尿病是一种严重危害人类健康的慢性非传染性疾病,文献报道糖尿病病程、高血压、高血糖、性别、年龄、高血脂、肥胖及人种均与糖尿病肾病的进展相关。随着社会经济的发展和人们生活方式的改变,糖尿病的发病率逐年迅速上升,己经成为继心脑血管疾病和肿瘤之后的第三大严重危害健康的疾病,我国已成为糖尿病患者第一大国。随着胰岛素、促胰岛素分泌药物、胰岛素增敏剂等药物的不断开发与应用,以及强化治疗方案的提出,糖尿病治疗领域不断进步。但是,而近年的多项调查表明,无论是欧美发达国家还是发展中国家,糖尿病控制状况均不容乐观,目前在临床上仍然缺乏有效的手段控制糖尿病及其并发症的发生与进展。
国际上对ii糖尿病药物的研发一直未停歇,但也一直未推出新的特效药能有效地治疗ii糖尿病,如果某种新药能缓解或治疗这种疾病,将是对人类的一大贡献。在我国,糖尿病发病率约9.8%,我国的糖尿病患者已超过1亿,给个人、家庭以及社会带来严重负担,已成为一个必须高度重视的公共卫生问题乃至社会问题,而在糖尿病患者中95%以上为ii糖尿病。现有的治疗ii糖尿病药物中,价格昂贵收效甚微,并多年未有特效药进入市场。进入老年人社会而导致的ii糖尿病的高发,还给家庭、社会带来沉重的经济负担。为了避免或减少当前药物的不良副作用或耐药性,同时提供更多候选药物和降低治疗ii糖尿病药物的成本,因此寻找新的ii糖尿病药物是迫切需要的。
文献(j.nat.prod.2015,78,844-849)公开了从海洋来源的真菌代谢产物中分离得到的如下结构的二苯醚类化合物,其报道有较强的抑菌活性。
技术实现要素:
本发明的目的提供上述从海洋来源的真菌代谢产物中分离得到的二苯醚类化合物的新药用用途。
本发明发现该二苯醚类化合物具有显著有效抑制a-葡萄糖苷酶活性的候选药物分子。
一种海洋来源的二苯醚类活性成分在制备治疗ii糖尿病药物中的应用;所述二苯醚类活性成分的结构式如下所示:
所述治疗ii糖尿病药物可以制备成目前适于人用临床应用的药物制剂,如片剂、胶囊、颗粒剂、注射剂等。
与现有技术相比,本发明具有如下有益效果:
1.本发明为目前ii糖尿病药物提供了一种海洋真菌代谢来源的药物小分子,拓宽了治疗ii糖尿病药物来源选择和技术参考,为该技术领域的发展作出了贡献。
2.本发明首次公开了ii糖尿病药物二苯醚类活性成分peniciaculinsa在制备治疗ii糖尿病药物中的用途,可显著有效抑制a-葡萄糖苷酶活性。
3.本发明中的ii糖尿病药物二苯醚类活性成分peniciaculinsa化合物来源于海洋真菌的代谢产物中,具有低毒、高效的特性。
附图说明:
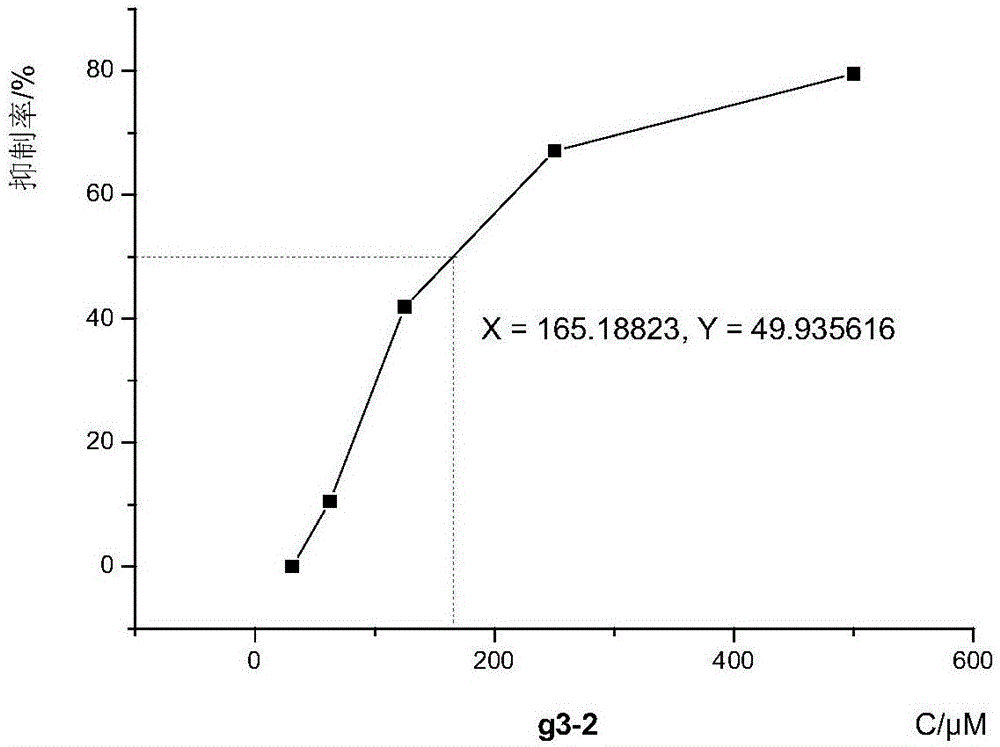
图1为实施例1中对治疗ii糖尿病药物二苯醚类活性成分peniciaculinsa在不同浓度抑制a-葡萄糖苷酶活性的作用;
图2为潜在治疗ii糖尿病药物二苯醚类活性成分peniciaculinsa的α-葡萄糖苷酶抑制作用的双倒数酶动力学曲线。
具体实施方式:
实施例1对ii糖尿病药物二苯醚类活性成分peniciaculinsa进行a-葡萄糖苷酶活性实验。
材料:
阳性对照:acarbose(阿卡波糖,文献中的ic50为(ic50=545±19μm,此次我们测出的值约为700-800μm);空白对照:dmso代替样品。葡萄糖苷酶(厂商阿拉丁,58units/mg,文献中配成的浓度是0.4units/ml,此次试验中,我们称0.58mg溶于10ml磷酸缓冲液,再从中取1ml稀释至10ml,再从稀释后的10ml取1ml稀释至2ml,最终浓度大概为0.2units/ml,现用现配);基质(即底物pnpg,配置的浓度为5mmol/l,用磷酸缓冲液溶解,现用现配);葡萄糖苷酶和基质一定要在冷藏室中保温。磷酸缓冲液(ph=7,100mmol/l,其中磷酸氢二钾占61.5%,磷酸二氢钾占31.5%,此次我们配制了500ml缓冲液。);样品(事先称量好,用dmso溶解);96孔板;2-20,20-200,100-1000μl的移液枪;5-50μl的移液排枪(8排);3种枪头。酶标仪。
注:只有中间白色区域测试用,灰色区域都空着不放任何东西。
步骤:60μl磷酸缓冲液+20μl葡萄糖苷酶溶液+10μl样品(最后一步混匀)——在37摄氏度的条件反应10min——加10μl基质(混匀)——在37摄氏度的条件反应20min——测量。(酶标仪:单波长405nm)前后顺序不能变,样品的终浓度为原来的十分之一。最后一步的20min根据情况调整。
1测阳性对照的值
根据文献的数据,配置acarbose的浓度为5000μm,6000μm,7000μm,8000μm,第一列,最后一步不加基质,用10μl磷酸缓冲液代替(此次我们只测了5000μm)。
抑制率:[1-((a样+b样+c样)/3-d样)/((a空+b空+c空)/3-d空)]*100%
2初筛
此次试验初筛的浓度是500μm,即要配成5000μm。先每个样平行两次测试,计算抑制率进行初筛。一般来说,抑制率在50%左右,其ic50大概也就在400-700之间,看情况估计。如果抑制率超过60%,尤其是〉80%就进行下一步梯度测试。
3梯度测试
将进一步测试的样品进行梯度稀释(逐一稀释2倍,则在前者中取50μl再加50μldmso,以此稀释5个梯度),平行三次,进行测试,分别计算5个梯度的抑制率(抑制率在50%上下都有点才合适),做出曲线,拟合,在曲线上找到抑制率50%对应的浓度就是ic50。
表1.ii糖尿病药物peniciaculinsa的a-葡萄糖苷酶活性实验
- 还没有人留言评论。精彩留言会获得点赞!