黄芩苷和黄芩苷衍生物在制备治疗牛病毒性腹泻病药物中的应用及黄芩苷衍生物的制作方法
本发明涉及医药技术领域,特别涉及芩苷及黄芩苷衍生物在制备治疗牛病毒性腹泻病药物中的应用、黄芩苷衍生物。
背景技术
牛病毒性腹泻病(bovineviraldiarrhea,bvd)是由bvdv感染牛引起的以发热、黏膜糜烂溃疡、腹泻及严重繁殖障碍为主要特征的一种病毒性传染病,传染性强,阳性检出率高达90%以上。一旦发生致死性粘膜病,死亡率达98%以上。目前,该病由于缺乏有效的防控技术,已呈世界性分布,约有70%~90%的牛群为bvd血清学反应阳性。由于尚无有效防治药物,宿主种群在不断扩大,如鹿、骆驼、野猪等。
因此对bvd的防治已成为十分迫切的社会与医学问题。目前,控制bvd的重要方法是疫苗接种,但是仍没有保护效果理想的疫苗。灭活bvdv苗对妊娠母牛安全,但需多次免疫。弱毒苗毒力不稳定,可诱发免疫抑制。接种疫苗时有可能感染bvdv野毒,持续感染(pi)牛后诱发粘膜病(md)等都可能使该病流行。另一方面,患病牲畜主要采用大剂量抗生素进行对症治疗,但其耐药性、毒性及药残等问题严重影响了防治效果。针对于目前bvdv感染尚无特异性的预防疫苗、治疗方法和抗病毒药物的现状,开发针对牛病毒性腹泻-黏膜病防治的新型有效药物及免疫佐剂十分必要。
技术实现要素:
本发明的目的在于提供芩苷及黄芩苷衍生物在制备治疗牛病毒性腹泻病药物中的应用、黄芩苷衍生物。本发明将黄芩苷和黄芩苷衍生物用于制备治疗牛病毒性腹泻病药物,具有较好的抗牛病毒性腹泻病毒的作用。
本发明提供了黄芩苷和黄芩苷衍生物在制备治疗牛病毒性腹泻病药物中的应用,所述黄芩苷衍生物具有式i所示的结构:
式i中r为-ch3、-c2h5、-c3h7、-c4h9、-c5h11、-c6h13或-c7h15。
本发明还提供了具有式ii所示的结构黄芩苷衍生物:
式ii中r’为-c6h13或-c7h15。
本发明还提供了具有式ii所示的结构黄芩苷衍生物的制备方法,包括以下步骤:
将黄芩苷与有机醇混合后,0℃下滴加氯化亚砜进行酯化反应,得到具有式ii所示的结构黄芩苷衍生物,所述有机醇为己醇或庚醇。
优选地,当r’为-c6h13时,酯化反应完成后,将所得酯化产物减压蒸干溶剂,加入无水乙醇后溶解后再次蒸干溶剂,加入乙醚,回流抽滤得到黄芩苷衍生物。
优选地,当r’为-c7h15时,酯化反应完成后,将所得酯化产物与乙醚混合后回流,然后放入冰箱,再将乙醚蒸干,加入石油醚抽滤得到黄芩苷衍生物。
优选地,所述黄芩苷与有机醇的用量比为222mg:16ml。
优选地,所述酯化反应的温度为40~60℃,所述酯化反应的时间为12~14h。
本发明提供了黄芩苷和黄芩苷衍生物在制备治疗牛病毒性腹泻病药物中的应用,将黄芩苷衍生物用于制备治疗牛病毒性腹泻病药物,具有较好的抗牛病毒性腹泻病毒的作用,经细胞试验证明,具有较好的抗牛病毒性腹泻病毒的作用,且一些衍生物的活性优于母体化合物黄芩苷,解决了目前bvdv感染尚无特异性的预防疫苗、治疗方法和抗病毒药物的问题。
附图说明
图1为黄芩苷己酯的1h-nmr;
图2为黄芩苷己酯的13c-nmr
图3为黄芩苷庚酯的1h-nmr;
图4为黄芩苷庚酯的13c-nmr;
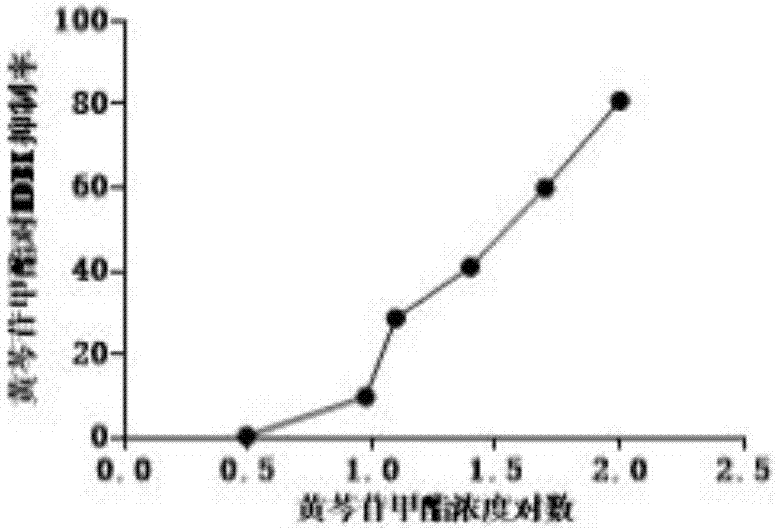
图5为黄芩苷甲酯对mdbk细胞作用的量效关系图;
图6为黄芩苷乙酯对mdbk细胞作用的量效关系图;
图7为黄芩苷丙酯对mdbk细胞作用的量效关系图;
图8为黄芩苷丁酯对mdbk细胞作用的量效关系图;
图9为黄芩苷戊酯对mdbk细胞作用的量效关系图;
图10为黄芩苷己酯对mdbk细胞作用的量效关系图;
图11为黄芩苷庚酯对mdbk细胞作用的量效关系图。
具体实施方式
本发明提供了黄芩苷和黄芩苷衍生物在制备治疗牛病毒性腹泻病药物中的应用,所述黄芩苷衍生物具有式i所示的结构:
式i中r为-ch3、-c2h5、-c3h7、-c4h9、-c5h11、-c6h13或-c7h15。
当所述r为-ch3、-c2h5、-c3h7、-c4h9或-c5h11时,本发明对所述黄芩苷衍生物的来源没有特殊的限定,采用本领域技术人员熟知的市售商品或常规的制备方法制得即可。
式i中r为-ch3、-c2h5、-c3h7、-c4h9、-c5h11、-c6h13或-c7h15时,对应的黄芩苷衍生物的名称依次为黄芩苷甲酯、黄芩苷乙酯、黄芩苷丙酯、黄芩苷丁酯、黄芩苷戊酯、黄芩苷己酯、黄芩苷庚酯。
在本发明中,所述具有式i所示结构的黄芩苷衍生物的结构如下式所示:
本发明还提供了具有式ii所示的结构黄芩苷衍生物:
式ii中r’为-c6h13或-c7h15。
本发明还提供了具有式ii所示的结构黄芩苷衍生物的制备方法,包括以下步骤:
将黄芩苷与有机醇混合后,0℃下滴加氯化亚砜进行酯化反应,得到具有式ii所示的结构黄芩苷衍生物,所述有机醇为己醇或庚醇。
在本发明中,所述黄芩苷与有机醇的用量比优选为222mg:16ml。
在本发明中,所述酯化反应的温度优选为40~60℃,所述酯化反应的时间优选为12~14h。
本发明对所述氯化亚砜的滴加速率没有特殊的限定,能够实现滴加即可。
在本发明中,当r’为-c6h13时,酯化反应完成后,优选将所得酯化产物减压蒸干溶剂,加入无水乙醇后溶解后再次蒸干溶剂,加入乙醚,回流抽滤得到黄芩苷衍生物。本发明对所述无水乙醇和乙醚的用量没有特殊的限定,采用本领域技术人员熟知的用量即可。
在本发明中,当r’为-c7h15时,酯化反应完成后,优选将所得酯化产物与乙醚混合后回流,然后放入冰箱,再将乙醚蒸干,加入石油醚抽滤得到黄芩苷衍生物。本发明对所述石油醚和乙醚的用量没有特殊的限定,采用本领域技术人员熟知的用量即可。
为了进一步说明本发明,下面结合实施例对本发明提供的黄芩苷和黄芩苷衍生物在制备治疗牛病毒性腹泻病药物中的应用及黄芩苷衍生物进行详细地描述,但不能将它们理解为对本发明保护范围的限定。
实施例1
称取黄芩苷111mg(0.25mmol)加入50ml单口瓶中,加入8ml甲醇,0℃搅拌下滴加氯化亚砜100μl,滴毕后室温搅拌14h,减压蒸干溶剂,加入10ml甲醇后溶解后再次蒸干溶剂,加入乙醚10ml,抽滤得黄色固体即为黄芩苷甲酯,在电子天平下称重,黄色固体为88.8mg。收率为80%。
实施例2
称取黄芩苷111mg(0.25mmol)加入50ml单口瓶中,加入10ml乙醇,0℃搅拌下滴加氯化亚砜100μl,滴毕后室温搅拌14h,减压蒸干溶剂,加入10ml乙醇后溶解后再次蒸干溶剂,加入乙醚10ml,抽滤得黄色固体即为黄芩苷乙酯,在电子天平下称重,黄色固体为84.36mg。收率为76%。
实施例3
取黄芩苷222mg(0.5mmol)加入100ml单口瓶中,加入16ml丙醇,0℃搅拌下滴加氯化亚砜300μl,滴毕后室温搅拌14h,减压蒸干溶剂,加入20ml无水乙醇后溶解后再次蒸干溶剂,加入乙醚20ml,回流抽滤得黄色固体即为黄芩苷丙酯,在电子天平下称重,黄色固体为157.62mg。收率为71%。
实施例4
取黄芩苷222mg(0.5mmol)加入100ml单口瓶中,加入16ml丁醇,0℃搅拌下滴加氯化亚砜300μl,滴毕后40℃搅拌14h,减压蒸干溶剂,加入20ml无水乙醇后溶解后再次蒸干溶剂,加入乙醚20ml,回流抽滤得橙黄色固体即为黄芩苷丁酯,在电子天平下称重,橙黄色固体为168.72mg。收率为77%。
实施例5
取黄芩苷222mg(0.5mmol)加入100ml单口瓶中,加入16ml戊醇,0℃搅拌下滴加氯化亚砜300μl,滴毕后40℃搅拌14h,减压蒸干溶剂,加入20ml无水乙醇后溶解后再次蒸干溶剂,加入乙醚20ml,回流抽滤得黄色固体即为黄芩苷戊酯,在电子天平下称重,黄色固体为86.58mg,收率为39%。
实施例6
取黄芩苷222mg(0.5mmol)加入100ml单口瓶中,加入16ml己醇,0℃搅拌下滴加氯化亚砜300μl,滴毕后40℃搅拌14h,减压蒸干溶剂,加入20ml无水乙醇后溶解后再次蒸干溶剂,加入乙醚20ml,回流抽滤得黄绿色固体即为黄芩苷己酯,在电子天平下称重,黄绿色固体为59.94mg,收率为27%。
对本实施例制得的黄芩苷己酯进行核磁谱图表征,结果如图1~2所示,图1为制得的黄芩苷己酯的1h-nmr,图2为制得的黄芩苷己酯的13c-nmr,1h-nmr(dmso-d6,600mhz,ppm):12.57(s,1h),8.68(s,1h),8.06(t,2h),7.59(d,3h),7.03(s,1h),7.01(s,1h),5.28(d,1h),4.19(d,1h),4.12(s,1h),4.06(s,1h),3.37-3.47(m,6h),1.55(t,2h),1.39(d,4h),1.13(d,2h),0.71(s,3h).13c-nmr(dmso-d6,150mhz,ppm):δ182.5,168.6,163.5,151.2,149.1,146.7,132.0,130.8,130.6,129.1,129.1,126.3,126.3,106.1,104.7,99.9,93.7,75.2,75.1,72.8,71.1,64.5,30.7,27.9,24.8,21.8,13.7。由图1~2可以看出,本实施例制得的产物为黄芩苷己酯。
实施例7
取黄芩苷222mg(0.5mmol)加入100ml单口瓶中,加入16ml庚醇,0℃搅拌下滴加氯化亚砜300μl,滴毕后60℃搅拌14h,得到粘稠状态,加入乙醚40ml回流,回流后放冰箱,后取出将乙醚蒸干,加石油醚抽滤得黄色固体即为黄芩苷庚酯,在电子天平下称重,黄绿色固体为144.3mg,收率为65%。
对本实施例制得的黄芩苷庚酯进行核磁谱图表征,结果如图3~4所示,图3为制得的黄芩苷庚酯的1h-nmr,图4为制得的黄芩苷庚酯的13c-nmr,1h-nmr(dmso-d6,600mhz,ppm):12.57(s,1h),8.68(s,1h),8.06(d,2h),7.60(d,3h),7.02(d,2h),5.28(d,1h),4.19(d,1h),4.13(s,1h),4.05(s,1h),3.35-3.47(m,6h),1.55(t,2h),1.24(s,6h),1.09(s,2h),0.72(t,3h).13c-nmr(dmso-d6,150mhz,ppm):δ182.5,168.5,163.5,151.2,149.1,146.7,132.0,130.8,130.6,129.1,129.1,126.3,126.3,106.1,104.7,100.0,93.7,75.2,75.1,72.8,71.1,64.5,31.1,28.2,28.0,25.1,21.9,13.8。由图3~4可以看出,本实施例制得的产物为黄芩苷庚酯。
黄芩苷及其衍生物的药理作用,是通过以下药效学实验得到证实的。
细胞牛肾原代细胞购买于中科院上海细胞库。
药品及试剂黄芩苷及其衍生物为实验室自制;牛病毒性腹泻病毒购买于中国兽医药品监察所。
1.黄芩苷及其衍生物体外抑制牛病毒性腹泻病毒活性试验
黄芩苷及其衍生物溶液的配制:
称取黄芩苷及其衍生物各20mg置2ml容量瓶中用dmso溶液溶解定容至2ml,所得浓度为10mg/ml。滤膜过滤除菌,4℃保存备用。采用二倍梯度稀释法,用细胞维持液将黄芩苷衍生物溶液稀释为不同浓度的溶液用于后续实验中。
bvdv毒力(tcid50)测定:
将该传代的细胞从细胞培养箱中取出,弃去原生长液。用高压灭菌过的pbs进行清洗干净。加入0.25%的乙酶进行消化。消化好的细胞,弃去乙酶。加入含有8%牛血清与1%双抗的营养液进行吹打,混匀。细胞进行10倍稀释后,取出10μl放置细胞计数板,在显微镜下计数。用营养液将细胞密度配制2.0×105的细胞悬液。用多孔道移液器将细胞悬液加入96孔细胞培养板中,100μl/孔。待细胞融合度达到80%以上时。用移液枪将原生长液弃掉,并用pbs清洗三次。接种用含3.5%马血清的维持液10倍梯度稀释的病毒液(10-1~10-10),100μl/孔。不同梯度的病毒液重复8孔。此外,实验设有阴性对照组(不加病毒与药物)、空白对照组。放置培养箱中培养,培养过程中,逐日记录细胞的状态与病变情况。五天后,用免疫过氧化物酶实验进行病毒毒力测定。
(1)弃去病毒生长液,用pbs洗三次,加入100μl80%丙酮pbs,4℃固定15min。
(2)弃去固定液,用pbs洗三次,拍打干净。
(3)用2%曲拉通pbs润洗一遍,弃去。加入100μl2%曲拉通pbs封闭液进行封闭,置37℃,5%co2孵育1h。
(4)弃去封闭液,加入用1%tween-80、5%马血清的pbs1:150稀释的一抗(bvdv阳性血清),置37℃,5%co2孵育1h。
(5)弃去一抗,用0.005%tween-20的pbs洗三遍。
(6)加入用1%tween-80、5%马血清的pbs1:1000稀释的二抗,孵育1h。
(7)弃去二抗,用0.005%tween-20的pbs洗三遍。
(8)加入aec染色液进行染色30min。阳性细胞呈现红色,阴性细胞不显色。
(9)观察并记录细胞病变程度和孔数。
记录细胞病变孔数,根据公式lgtcid50=l-d(s-0.5)计算bvdvtcid50值。
l:病毒最高稀释度的对数,d:病毒稀释度对数之间的差,s:细胞病变孔率总和。
黄芩苷衍生物对细胞毒性测定:
将细胞密度配制2.0×105的细胞悬液。用多孔道移液器将细胞悬液加入96孔细胞培养板中,100μl/孔。待细胞生长至单层时。用移液枪将原生长液弃掉,并用pbs清洗三次。将不同浓度的黄芩苷衍生物药物接种于细胞中,并将细胞放置细胞培养箱中培养。实验设有阴性对照组、空白对照组。逐日观察、记录细胞的生长状态。细胞培养48h后每孔加入10μlcck-8,孵育3h后在酶标仪下测od450值。根据od450值计算细胞的存活率与抑制率。确定黄芩苷衍生物对细胞的最大安全浓度。并根据黄芩苷衍生物对mdbk细胞作用的量效关系图5~11(图5~11依次为黄芩苷甲酯、黄芩苷乙酯、黄芩苷丙酯、黄芩苷丁酯、黄芩苷戊酯、黄芩苷己酯和黄芩苷庚酯对mdbk细胞作用的量效关系图)以及黄芩苷衍生物对mdbk细胞作用的量效关系方程(表1),计算黄芩苷衍生物对mdbk细胞的ic50值。
表1黄芩苷衍生物对mdbk细胞作用的量效关系方程
黄芩苷衍生物对病毒复制的抑制作用:
将细胞密度配制2.0×105的细胞悬液。用多孔道移液器将细胞悬液加入96孔细胞培养板中,100μl/孔。待细胞生长至单层时。用移液枪将原生长液弃掉,并用pbs清洗三次。每孔加入100μl100tcid50病毒液在37℃,5%co2培养箱孵育2h,弃去病毒液,加入不同浓度的黄芩苷衍生物药液,200μl/孔。将细胞放置培养箱中培养五天。培养过程中,逐日观察细胞的生长状态。记录细胞的cpe情况。五天后,取出细胞培养板,每孔加入20μlcck-8孵育3h,在酶标仪下测od450值。根据od450值计算不同浓度的黄芩苷衍生物抗bvdv有效率与黄芩苷衍生物的ic50。同时,实验另设有病毒对照组,阴性对照组及其空白对照组。每组实验设置8个平行孔。
黄芩苷衍生物对病毒的直接杀伤作用:
将细胞密度配制2.0×105的细胞悬液。用多孔道移液器将细胞悬液加入96孔细胞培养板中,100μl/孔。待细胞生长至单层时。用移液枪将原生长液弃掉,并用pbs清洗三次。加入100μl不同浓度的黄芩苷衍生物药液并在37℃,5%co2培养箱孵育4h后,直接加入100μl100tcid50病毒液孵育2h。弃去病毒液与药液。加入200μl维持液。将细胞放置培养箱中培养五天。培养过程中,逐日观察细胞的生长状态。记录细胞的cpe情况。五天后,取出细胞培养板,每孔加入20μlcck-8孵育3h,在酶标仪下测od450值。根据od450值计算不同浓度的黄芩苷衍生物抗bvdv有效率与黄芩苷衍生物的ic50。同时,实验另设有病毒对照组,阴性对照组及其空白对照组。每组实验设置8个平行孔。
黄芩苷衍生物对病毒的入侵阻断作用:
将细胞密度配制2.0×105的细胞悬液。用多孔道移液器将细胞悬液加入96孔细胞培养板中,100μl/孔。待细胞生长至单层时。用移液枪将原生长液弃掉,并用pbs清洗三次。加入100μl不同浓度的黄芩苷衍生物药液并在37℃,5%co2培养箱孵育4h后,弃去药液,加入100μl100tcid50病毒液孵育2h。弃去病毒液。加入200μl维持液。将细胞放置培养箱中培养五天。培养过程中,逐日观察细胞的生长状态。记录细胞的cpe情况。五天后,取出细胞培养板,每孔加入20μlcck-8孵育3h,在在酶标仪下测od450值。根据od450值计算不同浓度的黄芩苷衍生物抗bvdv有效率与黄芩苷衍生物的ic50。同时,实验另设有病毒对照组,阴性对照组及其空白对照组。每组实验设置8个平行孔。
黄芩苷衍生物对病毒的综合抑制作用:
将细胞密度配制2.0×105的细胞悬液。用多孔道移液器将细胞悬液加入96孔细胞培养板中,100μl/孔。待细胞生长至单层时。用移液枪将原生长液弃掉,并用pbs清洗三次。加入100μl不同浓度的黄芩苷衍生物药液与100μl100tcid50病毒液的混合液孵育4h,弃去混合液,加入不同浓度的黄芩苷衍生物药液,200μl/孔,将细胞放置培养箱中培养五天。培养过程中,逐日观察细胞的生长状态。记录细胞的cpe情况。五天后,取出细胞培养板,每孔加入20μlcck-8孵育3h,在在酶标仪下测od450值。根据od450值计算不同浓度的黄芩苷衍生物抗bvdv有效率与黄芩苷衍生物的ic50。同时,实验另设有病毒对照组,阴性对照组及其空白对照组。每组实验设置8个平行孔。
2.黄芩苷衍生物体外抑制牛病毒性腹泻病毒活性试验结果
2.1采用cpe法与免疫过氧化物酶实验测定bvdv毒力结果如表2。cpe法:细胞病变具有明显的脱落、聚堆现象,其细胞形态放生变化,变圆,细胞折光性差。经aec染色,病变的细胞核被染成红棕色。
表2不同稀释度的病毒接种细胞后的cpe情况
2.2黄芩苷及黄芩苷衍生物对细胞毒性测定
将细胞用不同浓度的黄芩苷及黄芩苷衍生物(200μg/ml~1.563μg/ml)进行处理,48h后观察细胞的形态,cpe结果发现,高浓度的黄芩苷及黄芩苷衍生物对细胞均有不同程度的毒性,随着药物浓度的降低,毒性降低,细胞的形态正常,同时发现,低浓度药物对细胞的增值具有一定的促进作用。但不同的药物对细胞的最大安全浓度具有差异性。从cck-8结果检测可知,黄芩苷及黄芩苷衍生物对细胞的最大安全浓度与对细胞的ic50值分别为表3。
表3黄芩苷及其衍生物对细胞的最大安全浓度与ic50值
2.3黄芩苷及其衍生物体外抗牛病毒性腹泻病毒活性作用
2.3.1黄芩苷及其衍生物抗bvdv复制抑制作用
除黄芩苷戊酯外,其它黄芩苷及其黄芩苷衍生物对bvdv都具有显著的复制抑制作用,在给予药物与病毒后,观察细胞的病变情况发现,药物组细胞与病毒对照组相比较,细胞脱落,聚堆现象较少。根据cck-8检测,黄芩苷及其黄芩苷衍生物对bvdv复制抑制作用由强到弱依次为:黄芩苷乙酯、黄芩苷丙酯、黄芩苷丁酯、黄芩苷甲酯、黄芩苷己酯、黄芩苷庚酯、黄芩苷、黄芩苷戊酯;其抗病毒最高有效率与ic50值如表4。
表4黄芩苷及其黄芩苷衍生物抗bvdv复制抑制作用最高有效率与ic50值
2.3.2黄芩苷及其黄芩苷衍生物抗bvdv直接杀伤作用
黄芩苷及其黄芩苷衍生物抗bvdv都具有显著的直接杀伤作用,在给予药物与病毒后,观察细胞的病变情况发现,药物组细胞与病毒对照组相比较,细胞脱落,聚堆,空泡现象较少。根据cck-8检测,黄芩苷及其黄芩苷衍生物对bvdv直接杀伤作用由强到弱依次为:黄芩苷、黄芩苷甲酯、黄芩苷庚酯、黄芩苷己酯、黄芩苷乙酯、黄芩苷丙酯、黄芩苷己酯、黄芩苷丁酯、黄芩苷戊酯;其抗病毒最高有效率与ic50值如表5。
表5黄芩苷及其黄芩苷衍生物抗bvdv直接杀伤作用最高有效率与ic50值
2.3.3黄芩苷及其黄芩苷衍生物抗bvdv入侵阻断作用
黄芩苷及其黄芩苷衍生物抗bvdv都具有显著的入侵阻断作用,在给予药物与病毒后,观察细胞的病变情况发现,药物组细胞与病毒对照组相比较,细胞脱落,聚堆,空泡现象较少。根据cck-8检测,黄芩苷及其黄芩苷衍生物对bvdv入侵阻断作用由强到弱依次为:黄芩苷、黄芩苷甲酯、黄芩苷丙酯、黄芩苷乙酯、黄芩苷丁酯、黄芩苷庚酯、黄芩苷己酯、黄芩苷戊酯;其抗病毒最高有效率与ic50值如表6。
表6黄芩苷及其黄芩苷衍生物抗bvdv入侵阻断作用最高有效率与ic50值
2.3.4黄芩苷及其黄芩苷衍生物抗bvdv综合抑制作用
黄芩苷及其黄芩苷衍生物抗bvdv都具有显著的综合抑制作用,在给予药物与病毒后,观察细胞的病变情况发现,药物组细胞与病毒对照组相比较,细胞脱落,聚堆,空泡现象较少。根据cck-8检测,黄芩苷及其黄芩苷衍生物对bvdv综合抑制作用由强到弱依次为:黄芩苷乙酯、黄芩苷、黄芩苷己酯、黄芩苷丙酯、黄芩苷丁酯、黄芩苷甲酯、黄芩苷庚酯、黄芩苷戊酯;其抗病毒最高有效率与ic50值如表7。
表7黄芩苷及其黄芩苷衍生物抗bvdv综合抑制作用最高有效率与ic50值
利用cck-8法与cpe法相结合,采用四种不同的给药方式研究表明黄芩苷及其衍生物体外抗bvdv活性作用显著,其发挥作用途径包括入侵阻断作用、直接杀伤作用、综合作用和抑制复制作用。
以上所述仅是本发明的优选实施方式,并非对本发明作任何形式上的限制。应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!