一种多组分骨粘合材料及使用方法与流程
本发明涉及医用材料领域,尤其涉及一种多组分骨粘合材料及使用方法。
背景技术:
医用骨粘合剂是一种新型骨折固定材料,常用于将细小的骨碎片、人造植入物附着到活骨,或用于骨骼的小面积修复和重建,具有操作方便、适用性强等优点,能够克服外固定或金属内固定手术复杂、易二次伤害和易发生感染的问题。
近年来,常用的医用骨粘合剂(也称骨粘合胶)分为有机骨粘合胶和无机骨粘合胶。其中有机骨粘合胶多由聚甲基丙烯酸甲酯(pmma)及其混合物形成,这种聚合物是由丙烯酸类单体,如甲基丙烯酸甲酯(mma),在引发剂存在下室温聚合而成。因其使用方便,在骨缺损、骨肿瘤、骨折、人工关节的粘接固定等方面都有应用。但是,这些基于pmma的传统有机骨粘合胶具有以下缺点:在骨粘合固化过程中,胶层释放热量较大可能会导致周围组织损伤;pmma通常不易降解或被人体吸收,这可能会引起该部位的炎症,增加感染的风险,还可能抑制断面新骨的生长。以钙、磷为主要成分的无机骨粘合胶具有无毒、无刺激、良好生物相容性和安全性、骨传导性等特点,但通常来说,这种胶较脆性,对断骨的粘接强度低,在实践中应用不广。
医用骨粘合剂应该满足以下要求:(1)安全可靠、无毒性、无三致(致癌、致畸、致突变);(2)具有良好的生物相容性,不妨碍人体组织的自身愈合;(3)在有血液和组织液的环境(水存在)中可以使用;(4)在常温、常压下可以实现快速粘合;(5)具有良好的粘合强度及持久性,粘合部分具有一定的弹性和韧性;(6)在使用过程中对人体组织无刺激性;(7)达到使用效果后能够逐渐降解、吸收、代谢;(8)本身无菌,能抑菌抗菌更佳。
早在上世纪50年代,聚氨酯已经被尝试用作一种有机骨粘合剂在临床上试验,因当时采用的聚氨酯胶与骨头的粘合性差,出现较高的感染率和并发症而被迫中止。到上世纪九十年代,有人开发出改性的聚氨酯粘合体系,如us5266608;此后,以提高骨粘合强度、减少临床不良反应为目标的聚氨酯骨粘合材料不断被改进,其中以美国食品及药物管理局批准的一种以蓖麻油多元醇为软段的聚氨酯骨水泥(kryptonitetm)最为突出。这种聚氨酯骨水泥包含基于蓖麻油改性的蓖麻油多元醇、异氰酸酯和β-磷酸钙等填料,在手术中混合形成粘合糊剂,同时可在封闭操作前形成刚性多孔聚合物。这种骨粘合剂已被临床用于胸骨闭合、头骨粘合等外科手术,如专利us8211458b2和us20050031578所示。
目前,在用作于人体骨粘合时,上述改性的聚氨酯骨水泥仍存在不小的挑战,这包括:由于人体应用的限制,聚氨酯骨水泥应用的温度为人体适应的温度,反应中发热不能超过50-60摄氏度,以免灼伤皮肤组织,造成人体伤害。同时,临床上在较短时间内(一般30分钟左右),骨粘合达到一定的初粘强度。此外,人体受伤创面往往会出现大量的血液和组织液,这种带水的环境对聚氨酯材料的性能有很大的负面影响。因为大量的水会消耗异氰酸基团,生成大量的脲键,一方面影响材料的粘合强度,另一方面会改变组分的反应配比,从而影响材料的最终粘合性能。
因此针对上述的问题,本领域的技术人员需要充分考虑医学使用环境的实际情况,从配方及工艺出发,设计出一种更适合人体体温环境的骨粘合材料,尽可能降低血液和组织液对骨粘合性能的影响,同时不对人体造成短期或长期的负面作用。
技术实现要素:
有鉴于现有技术的上述缺陷,本发明所要解决的技术问题是改进聚氨酯骨粘合剂的配方和工艺,适合人体体温环境使用,克服在带水的环境下对粘合剂性能的负面影响。
为实现上述目的,本发明提供了一种多组分骨粘合材料,包括异氰酸酯组合物、蓖麻油多元醇组合物、催化剂、粒径大小在10nm-100um之间的无机颗粒,且该无机颗粒含有吸水性硫酸盐和难溶性钙盐,其中吸水性硫酸盐分布于无机颗粒的表面。
骨骼的主要成分主要由含钙、磷的无机组分组成。在骨粘合材料中加入无机组分,可以制备接近人体内骨的结构,更利于断骨生长再生。本发明中无机颗粒含有至少两种无机组分,包括吸水性硫酸盐和难溶性钙盐,其中钙盐成分的作用在很多专利中已有解释,但是在骨粘合材料中,引入吸水性硫酸盐,在以前的报道中未见提及。
当骨粘合材料使用时,可能会遇到人体内血液和组织液的渗出,尽管此时异氰酸基团与水的反应速度很慢,但是,这些液体会稀释还未反应的聚氨酯的混合液,大大降低nco与羟基的反应速度,从而使得骨粘合材料的性能受到很大损害。在吸水性硫酸盐存在时,可以在一定时间内,将粘合材料周边的液体转化成固态,这可以在很大程度上保证中低温下聚氨酯反应的顺利进行。为实现这个作用,对无机颗粒的组成、形态、结构都有具体的要求。在本发明中发现无机颗粒的粒径大小在10nm-100um之间,且无机颗粒含有吸水性硫酸盐和难溶性钙盐,其中吸水性硫酸盐分布于无机颗粒的表面,能实现该作用。
在本发明的较佳实施方式中采用了无水硫酸镁,分布于难溶性碳酸钙的表面。无水硫酸镁具有很强的干燥能力,吸水后迅速生成含水的结晶化合物,在工业上常用来干燥有机化合物。一种可行的制备表面分布无水硫酸镁无机颗粒的方法是,通过将精制硫酸镁的饱和溶液过滤后,加入骨粘合材料的其它无机颗粒,搅拌下冷却结晶,离心分离,在200-250℃进行干燥脱水,制得表面复合无水硫酸镁的无机颗粒。
在本发明的具体实施方式中,根据使用的环境,出血量和组织液的多寡,选择适合的无水硫酸镁的用量。根据上述的原则,也可以采用类似的易吸水的物质,在不影响聚氨酯反应的前提下,达到类似的效果。
在本发明的多组分骨粘合材料中,难溶性钙盐可选自碳酸钙、β-磷酸三钙、羟基磷灰石等中一种或多种。
在本发明的具体实施例中,蓖麻油多元醇组合物为蓖麻油二元醇和蓖麻油三元醇。优选地,100重量份的所述蓖麻油三元醇还包括0.5-3重量份的水。蓖麻油酯化后的改性多元醇,与人体无害,在断骨形成时,相较于石油基聚酯多元醇和聚醚多元醇,更易于降解。本发明发现,在蓖麻油三元醇中加入微量的水分,有以下两点好处:1.水与异氰酸基团反应后,在骨粘合体系中形成微孔,通过控制开孔率和孔径大小,可以获得利于骨细胞生长的粘合层;2.该反应是放热反应,通过使用工艺的控制,使得一定程度上提高聚氨酯的反应温度,提高骨粘合材料的力学性能。当然,这里的水分量不宜过高,应避免造成骨粘合材料与人体接触的部位温度上升过高,超过人体可接受的范围。
在本发明的多组分骨粘合材料中,异氰酸酯组合物优选为含有二个或多个-nco基团的异氰酸酯组合物。异氰酸酯可选自脂肪族的、环脂族的和芳香族的异氰酸酯混合物,更优选氢化芳香族的异氰酸酯组合物。本发明发现异氰酸酯组合物为含有二个或多个-nco基团的氢化芳香族异氰酸酯组合物时,骨粘合材料的粘合效果更优。
满足异氰酸基团与羟基在常温下或人体温度附近快速反应,选择正确的催化剂体系很重要。通常这种缩聚反应被称为树脂化或凝胶化反应,反应后分子量会增大,会表现出高分子的粘合性、力学性能和成型特征。为使得骨粘合材料在人体内不成为人体骨组织生长的障碍,一种可选的方案是在成型的粘合结构中,构建细小、均匀的泡孔,这一点在专利us20050220771中已有说明。但是,由于催化目的的复杂和因在人体中使用的高标准要求,不同技术使用的催化体系只能通过实验来确定,且具有很强的新颖性和专用性。
在本发明的具体实施例中,催化剂是凝胶反应催化剂和发泡催化剂的组合物,优选对人体无毒或低毒的胺类催化剂,更优选1,2-二甲基咪唑溶液、三乙烯二胺溶液、五甲基二乙烯三胺、五甲基二丙烯三胺等中的一种或几种,或者选改性叔胺。
本发明的骨粘合材料具有粘合性强、力学强度高、骨传导性好、利于断骨生长再生、对人体安全等特点,适合人体体温环境使用,克服在带水的环境下对粘合剂性能的负面影响。在松质骨、硬骨组织粘合等人体骨修复中有很好的应用前景。
本发明还提供了多组分骨粘合材料具体使用方法,以下步骤:
步骤1、按官能团nco/oh摩尔比为1-1.3,将异氰酸酯小分子或低聚物与蓖麻油二元醇混合均匀,在60℃-90℃下反应合成异氰酸酯封端的聚氨酯预聚体;
步骤2、在蓖麻油三元醇、或者蓖麻油二元醇与蓖麻油三元醇的混合物中,加入催化剂溶解均匀,得到三元醇组合物;
步骤3、将上述聚氨酯预聚体、三元醇组合物和粒径大小在10nm-100um之间的无机颗粒按用量比例加料混匀:其中官能团nco/oh的摩尔比为1-1.1、无机颗粒占总重量的10-50wt.%;该无机颗粒含有吸水性硫酸盐和难溶性钙盐,其中吸水性硫酸盐分布于无机颗粒的表面;加料顺序为无机颗粒、聚氨酯预聚体和三元醇组合物;混合3-8分钟后涂覆使用,如涂覆到断骨的粘合面上,最好施加一定的压力于断骨,保持骨断面正常粘合,15-30分钟后骨粘合完成。
上述步骤1的合成方法,通过常规化学技术可以很容易得到长期保存的聚氨酯预聚体。步骤2中的蓖麻油三元醇中可以加入0.5-3重量份的水(以蓖麻油三元醇重量计算)。步骤2中若使用蓖麻油二元醇和蓖麻油三元醇的混合物,可以降低使用时液体的粘度,利于聚氨酯的双组分更混合均匀。步骤3中当无机颗粒的表面存在无水硫酸镁时,对本发明粘合材料的使用效果有很大影响,实验前,可以准备不同无水硫酸镁含量的无机颗粒,使用时根据具体的医学环境选择不同的无机颗粒。
以下将结合附图对本发明的构思、具体结构及产生的技术效果作进一步说明,以充分地了解本发明的目的、特征和效果。
附图说明
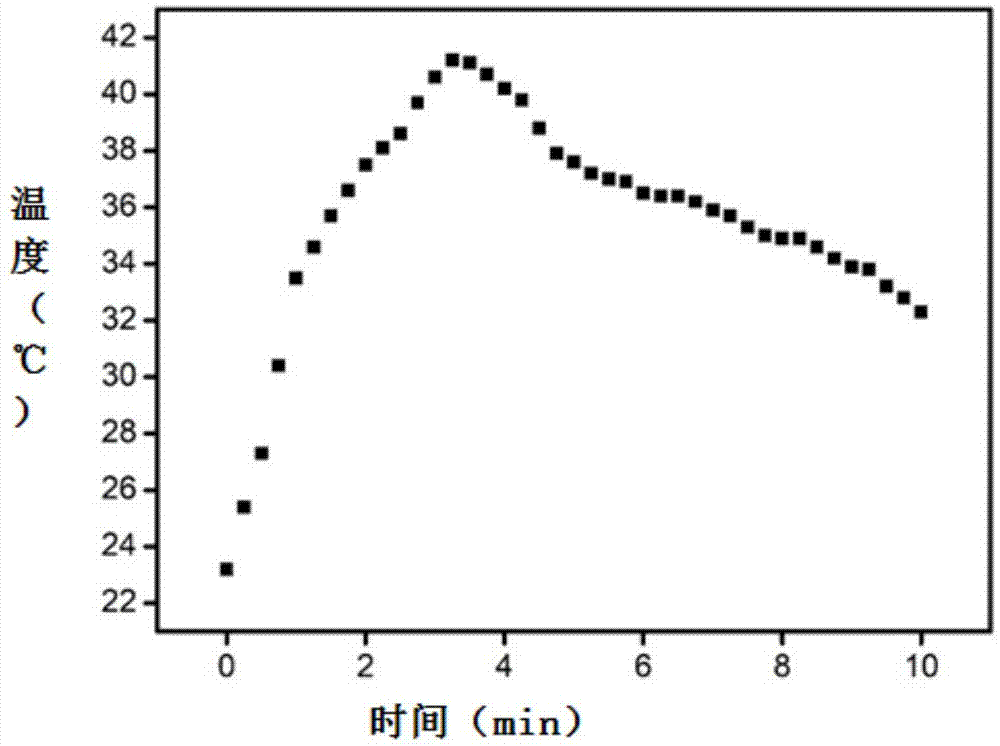
图1是本发明的一个较佳实施例的骨粘合材料外部温度变化图。
具体实施方式
以下参考说明书附图介绍本发明的多个优选实施例,使其技术内容更加清楚和便于理解。本发明可以通过许多不同形式的实施例来得以体现,本发明的保护范围并非仅限于文中提到的实施例。
所用试剂说明
以下未注明厂家的试剂,均购自sigma-aldrich公司,未经处理直接使用。
mdi:4,4'-二苯基甲烷二异氰酸酯;
hmdi:4,4-二异氰酸酯二环己基甲烷;
hxdi:氢化二亚甲基苯二异氰酸酯,日本三井化学株式会社;
m20s:聚mdi,nco含量30.74wt%,巴斯夫股份有限公司;
polycind290:蓖麻油二元醇,凡特鲁斯(上海)贸易有限公司;
polycint400:蓖麻油三元醇,凡特鲁斯(上海)贸易有限公司;
催化剂dm:东曹(上海)生物科技有限公司;
催化剂f:东曹(上海)生物科技有限公司;
五甲基二乙烯三胺:上海阿拉丁生化科技有限公司;
五甲基二丙烯三胺:上海阿拉丁生化科技有限公司;
碳酸钙:粒径3-5um;
β-磷酸三钙(tcp):粒径3um;
羟基磷灰石(ha):粒径10um;
无水硫酸镁:国药集团化学试剂上海有限公司;
消泡剂:db-100,陶氏化学有限公司;
表面活性剂:pluronicf108,巴斯夫化学有限公司。
聚氨酯预聚体中nco含量的测定
异氰酸酯小分子和低聚物与蓖麻油二元醇反应结束后得到聚氨酯预聚体,采用二正丁胺滴定法测定聚氨酯预聚体中的nco基团的含量,据此准确计算最终聚氨酯反应所需的蓖麻油三元醇组合物的用量。
含无水硫酸镁的无机颗粒的定量制备
将精制硫酸镁的饱和溶液过滤后,加入难溶性钙盐,如表面亲水的碳酸钙粉末,在缓慢搅拌下冷却结晶,经过离心分离,在200-250℃进行干燥脱水,可制得表面复合无水硫酸镁的无机颗粒,无机颗粒的粒径大小在10nm-100um之间。无机颗粒中无水硫酸镁的含量可以经多次洗涤、烘干至恒重后,计算残留物(难溶于水的无机组分)的质量求出。
分别准备含无水硫酸镁约20wt.%、50wt.%的无机颗粒。
体外骨粘合实验
实验前选取冷却保存的猪松质骨切割成小块,打磨成5×18×32mm3的长方体,分割成体积对等的两个长方块,横截面积为5×18mm2,断面打磨处理后,用棉花蘸取溶液擦拭待粘接的截面,保持待粘接面的湿润,均匀涂抹现配的聚氨酯粘合剂。待两块骨头粘好后,进行固定,分别置于三种不同的环境中,经后期养护24h后,取出进行样品的粘合性能测试。
这里三种不同的环境分别为:环境1,骨粘合后不直接接触水分;环境2,骨粘合后放在经pbs缓冲溶液浸泡的棉团中;环境3,骨粘合后放在pbs缓冲溶液中。
样品的粘合性能测试方法
(1)吸水率(质量百分数):在模具中将粘合材料混合后固化成型,在室温下放置24h后,在水中测量其吸水率,用来表征粘合层中的开孔程度。
(2)体外骨粘接强度:用instron4465型电子万能试验机,应力传感器2kn,拉伸速率5mm/min,室温下测试,测得体外骨粘合强度。
(3)压缩强度和压缩模量:用instron4465型电子万能试验机,应力传感器2kn,压缩速率2mm/min,压缩应变极限为50%,室温下测试。试样规格:
实施例1
在配有氮气、搅拌器的150ml三颈瓶中,将polycind290(蓖麻油二元醇)升温抽真空除水2h后,按照摩尔比nco/oh=1.05,加入摩尔比为7/3的mdi(4,4'-二苯基甲烷二异氰酸酯)和m20s(聚mdi),再升温至80℃,通氮气保护反应3h,得到浅褐色透明的聚氨酯预聚体。聚氨酯预聚体的合成反应结束后取样进行滴定,计算出异氰酸根的质量分数。
在polycint400中加入0.5wt.%的催化剂f和五甲基二乙烯三胺(质量比为9/1)混合物,以及1wt.%的纯水,均以polycint400重量计算,混合均匀备用得到三元醇组合物。
体外骨粘合性能的测试:按表1中实施例1的配方,在塑料容器中依次加入碳酸钙粉、聚氨酯预聚体和三元醇组合物,常温下搅拌约3-5min后,涂敷在断骨表面,在环境1中进行体外骨粘合实验,采用红外线感温枪检测胶层外部温度,得到图1。从图1可以得知,胶层放热的升温对人体组织基本上无影响,适合人体体温环境使用。
表1
备注:
1.根据骨粘合材料所处环境水分的多少,实验中选取三种典型的使用环境进行后期养护:环境1,骨粘合后不直接接触水分;环境2,骨粘合后放在经pbs缓冲溶液浸泡的棉团中;环境3,骨粘合后放在pbs缓冲溶液中;
2.表中的所有举例,聚氨酯预聚物按配比nco/oh=4合成,其中oh均由polycind290提供;
3.三元醇中含水量(%)以polycint400重量计算。
实施例2
与实施例1相比,除了将碳酸钙换成β-磷酸三钙,其它配方工艺不变。同样地,在环境1中进行体外骨粘合实验。
实施例3
与实施例1相比,除了将碳酸钙换成羟基磷灰石,其它配方工艺不变。同样地,在环境1中进行体外骨粘合实验。
实施例4
与实施例1相比,除了将在polycint400中换成加1wt.%的催化剂f和五甲基二乙烯三胺(质量比为9/1)混合物,以及2wt.%的纯水,其它配方工艺不变。同样地,在环境1中进行体外骨粘合实验。
实施例5
与实施例1相比,除了将mdi(4,4'-二苯基甲烷二异氰酸酯)换成hmdi(4,4-二异氰酸酯二环己基甲烷),其它配方工艺不变。同样地,在环境1中进行体外骨粘合实验。
实施例6
与实施例1相比,除了将mdi(4,4'-二苯基甲烷二异氰酸酯)换成hxdi(氢化二亚甲基苯二异氰酸酯),其它配方工艺不变。同样地,在环境1中进行体外骨粘合实验。
实施例7
与实施例1相比,除了将碳酸钙换成表面含20wt.%无水硫酸镁的碳酸钙,其它配方工艺不变,但在环境2中进行体外骨粘合实验。
实施例8
与实施例1相比,除了将碳酸钙换成表面含50wt.%无水硫酸镁的碳酸钙,其它配方工艺不变,但在环境3中进行体外骨粘合实验。
对比例1
与实施例1相比,三元醇组合物中不含水,其它配方工艺不变。同样地,在环境1中进行体外骨粘合实验。
对比例2
与实施例5相比,配方工艺不变,但在环境2中进行体外骨粘合实验。
对比例3
与实施例4相比,减少三元醇组合物中含水量至1wt.%,其它配方工艺不变,但在环境3中进行体外骨粘合实验。
实施例1-8和对比例1-3的体外骨粘合实验结果如表2所示。
表2
备注:*直接观察动物体内1-3月断骨生长情况,综合评价为较好++;好+;一般+-;差×。
本发明的效果将进一步通过以下的叙述来说明:
在实施例1中,在蓖麻油三元醇中添加了1wt.%的水,在聚氨酯反应时,起到微孔发泡的效果,利于骨细胞生长。相反,对比例1则不加人水,因粘合材料中开孔率较低,不利于骨组织修复。
在实施例2和实施例3中,采用不同的无机颗粒,在本发明确定的粒径范围内,同样可以得到较好的骨粘合效果。由于异氰酸酯小分子反应活性的差异,同样的施胶工艺在实施例5和实施例6中,测得的骨粘结强度要略低于mdi制得的骨粘合材料,但并不妨碍断骨的生长。
在实施例7和实施例8中,巧妙利用了无水硫酸镁能快速吸水的特性,在施胶过程中,能将胶层附近的组织液和血液中的水分迅速转化成结晶水,形成固态,利于聚氨酯的异氰酸基团与多元醇中的羟基反应,使得粘合性能不受环境中水分的影响。
而且,惊喜地发现,在实施例7和实施例8中,由于在无机颗粒表面引入无水硫酸镁,使得胶层中的开孔率较大,且对骨粘接强度没有造成不好的影响。这种影响在对比例2和对比例3中,直接造成骨粘结强度大幅下降。
以上详细描述了本发明的较佳具体实施例。应当理解,本领域的普通技术无需创造性劳动就可以根据本发明的构思作出诸多修改和变化。因此,凡本技术领域中技术人员依本发明的构思在现有技术的基础上通过逻辑分析、推理或者有限的实验可以得到的技术方案,皆应在由权利要求书所确定的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!