间充质干细胞外泌体抗皮肤表皮细胞氧化的特性及其制剂的制备方法与流程
本发明涉及一种干细胞外泌体的新用途,具体涉及一种间充质干细胞外泌体抗皮肤表皮细胞氧化的特性及其制剂的制备方法,尤其是人脐带间充质干细胞外泌体的新用途。属于干细胞及转化领域。
背景技术:
胞外囊泡(extracellularvesicle,evs)被认为是细胞间通讯的有效载体,这是由于它们能够传递蛋白质、脂质和核酸,从而影响受体和母体细胞的各种生理和病理功能。其中evs中的外泌体
间充质干细胞是一类具有自我更新及多向分化能力的细胞,我们通过研究人脐带间充质干细胞外泌体处理氧化应激模型,发现h2o2处理后的人表皮细胞总抗氧化能力、总超氧化物歧化酶(superoxidedismutase,sod)活性和谷胱甘肽过氧化物酶(glutathioneperoxidase,gsh-px)活性都显著下降(p<0.001),而加入了人脐带间充质干细胞外泌体的组别,跟h2o2组相比,这三种指标都显著上升(p<0.001),表明外泌体能够有效保护表皮细胞免受氧化损伤。人脐带间充质干细胞外泌体用于抗衰及修复是当前研究的热点,如利用人脐带间充质干细胞外泌体促进表皮细胞及成纤维细胞的增殖,调节皮肤胶原蛋白含量,改善皮肤缺水状态,使皮肤恢复弹性等。
尽管如此,目前人脐带间充质干细胞外泌体抗皮肤氧化或老化研究及应用领域尚有诸多缺点:
(1)目前人脐带间充质干细胞外泌体抗氧化或老化缺少客观的实验证据;
(2)个别发明提及人脐带间充质干细胞外泌体可改善细胞sod酶活性,但抗氧化应激作用太局限;
(3)干细胞外泌体作为生物学制剂,直接皮肤注射可能会产生皮肤二次损伤;
(4)外泌体主要成分为小分子物质,直接涂抹难以聚合,抗皮肤氧化或老化作用有限。
技术实现要素:
本发明的目的在于,提供人脐带间充质干细胞外泌体抗氧化的证据及抗氧化制剂的制备方法,以克服现有技术存在的上述缺点和不足。
鉴于此,本发明针对现有技术存在的问题,说明人脐带间充质干细胞外泌体在护肤品中的应用。
本发明所需要解决的技术问题,可以通过以下技术方案来实现:
作为本发明的第一方面,人脐带间充质干细胞外泌体的应用,其特征在于:所述人脐带间充质干细胞外泌体在抗皮肤表皮细胞氧化制剂中的应用。
其中,所述制剂为药品或护肤品。
作为本发明的第二方面,一种抗皮肤表皮细胞氧化制剂,其特征在于:所述制剂其成分包含人脐带间充质干细胞外泌体。
其中,所述人脐带间充质干细胞外泌体,制成人脐带间充质干细胞新鲜外泌体悬液。
其中,所述人脐带间充质干细胞外泌体的制备方法为:超速离心法提取的人脐带间充质干细胞外泌体,定性定量检测后加入生理盐水重悬,-80℃保存。
其中,所述制剂的剂型为外敷的水凝剂或乳液。
作为本发明的第三方面,一种抗皮肤表皮细胞氧化的人脐带间充质干细胞外泌体精华液,其特征在于:所述精华液的配方为:包括人脐带间充质干细胞外泌体和基质,所述基质包括溶剂、保湿剂、增稠剂、螯合剂、皮肤调理剂、皮肤调节剂和防腐剂的任意一种或组合。
其中,所述溶剂为水。
其中,所述保湿剂为丁二醇、透明质酸钠和糖类同分异构体的任意一种或组合。
其中,所述增稠剂为黄原胶。
其中,所述螯合剂为edta二钠。
其中,所述皮肤调理剂为聚二甲基硅氧烷和皮肤呼吸因子。
其中,所述皮肤调节剂为β-葡聚糖。
其中,所述防腐剂为明串球菌与萝卜根发酵产物滤液。
其中,所述的人脐带间充质干细胞外泌体精华液,由如下重量份原料制成:
作为本发明的第四方面,一种抗皮肤表皮细胞氧化的精华液的制备方法,包括如下步骤:
(1)将透明质酸钠在生产前用适量去离子无菌水溶解备用;
(2)将a组其他物料加入后加热至75~80℃,搅拌均匀并保持10分钟;加入b组物料均质3~5分钟保温10分钟;
(3)降温至50℃,加入c组物料,搅拌均匀并保温2分钟;
(4)降温至40℃,加入d组物料,搅拌均匀;
(5)冷却至35℃时加入e组物料(每种原料加入后搅拌均匀方能加入下一种物料),搅拌混合至均匀;
(6)在35℃检测、出料、静置、半成品检验、灌装及成品入库。
本发明的有益效果:
本发明提供了人脐带间充质干细胞外泌体的新用途,体外实验结果表明人脐带间充质干细胞外泌体可以促进表皮细胞的生长,保护表皮细胞免受氧化损伤,提高细胞内sod酶的活性,且无毒副作用,小鼠实验表明,人脐带间充质干细胞外泌体对动物皮肤无毒性。综上所述,人脐带间充质干细胞外泌体用于护肤品制剂,安全有效。
附图说明
为了更清楚地说明本发明实施例中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍。
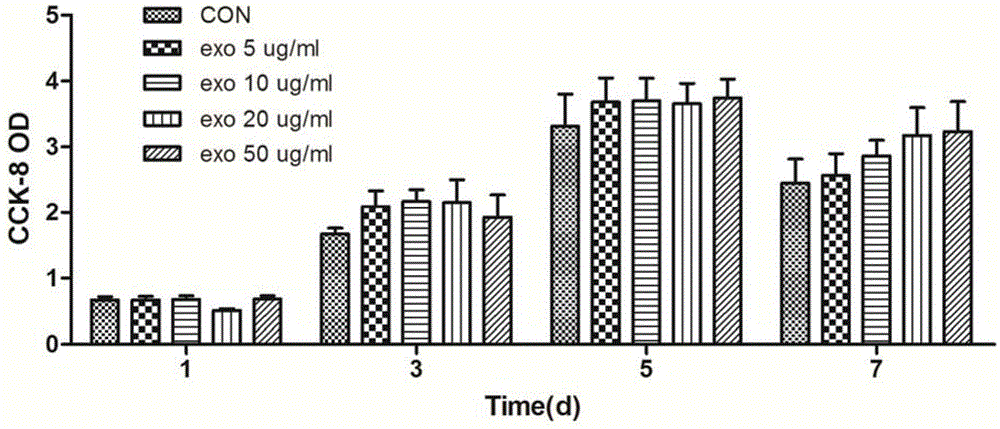
图1示实施例2,人脐带间充质干细胞外泌体体外安全性实验,cck-8法实验结果显示,外泌体对表皮细胞的生长没有毒性作用,第1、3、5d吸光值和对照组相比没有差异,第7d外泌体各组的吸光值高于对照组,表明外泌体有利于细胞的生长。横坐标为时间,纵坐标为od值。
图2示实施例3,人脐带间充质干细胞外泌体动物实验结果显示注射了外泌体的小鼠,背部没有出现异常。初步推断人脐带间充质干细胞外泌体对动物皮肤无毒性作用。a组为对照组,b组为生理盐水组,c组为外泌体组。
图3示实施例4,人脐带间充质干细胞外泌体能够保护表皮细胞免受氧化损伤,h2o2处理后,细胞的总抗氧化能力、总sod酶活性和gsh-px活性都显著下降(p<0.001),而加入了外泌体的组别,跟h2o2组相比,这三种指标都显著上升(p<0.001)。表明外泌体能够保护表皮细胞免受氧化损伤。a图纵坐标为总抗氧化能力,横坐标依次为正常组、h2o2组、外泌体组;b图纵坐标为总sod酶活性,横坐标依次为正常组、h2o2组、外泌体组;c图纵坐标为谷胱甘肽过氧化酶活性,横坐标依次为正常组、h2o2组、外泌体组。
图4示实施例4,8-ohdg为氧化损伤时,dna损伤的标志物,实验中发现正常人表皮细胞中8-ohdg表达量很少,而h2o2处理后,细胞中的表达量大幅增加,且核内表达显著,同时加入外泌体的组,与h2o2组相比,显著减少。sod2是抗氧化的关键分子,正常细胞中呈现高表达,h2o2处理后,sod2的表达显著下降,加入外泌体的组,表达量又显著回升,趋于正常。进一步说明外泌体具有抗氧化作用。图4a为人脐带间充质干细胞外泌体对人表皮细胞氧化损伤后8-ohdg表达的影响,图4b为人脐带间充质干细胞外泌体对人表皮细胞氧化损伤后sod2表达的影响。
图5示实施例5,人脐带间充质干细胞外泌体抗氧化精华液的制备工艺流程图。
图6示实施例6,人脐带间充质干细胞外泌体抗氧化精华液经过(45±1)℃、(-20±1)℃耐热耐寒交替进行,每48小时观察一次,随后更换温度,45天后观察外观(颜色,味道)无差别,肤感无明显差别,ph在误差允许范围内均达标,即与45天前的ph值相同,说明外泌体在室温时与该精华基质的配伍性良好。
具体实施方式
以下结合具体实施例,对本发明作进一步说明。对本发明实施例中的技术方案进行清楚、完整地描述。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1、人脐带间充质干细胞上清的收集与外泌体的提取
1.人脐带间充质干细胞的培养:
采集足月健康婴儿的脐带组织,放于装有pbs(含100u/ml的青链霉素)的无菌瓶中,4h内处理。剥离脐带的静脉和动脉,剥取华通氏胶,剪成2mm3大小,在培养瓶中均匀平铺,加入少量完全培养基保持湿润,培养基为dmem/f12加15%fbs,24h后补充足够的培养基,之后每3天换液一次,细胞长至融合后传代,,传代后培养基使用dmem/f12加10%fbs。
2.外泌体的提取:
用第3~5代的人脐带间充质干细胞上清提取外泌体,待细胞长至80%左右密度后,更换为无血清培养基,继续培养24h后,收集培养上清。
(1)、将培养上清4℃,300g,离心10min,保留上清液;
(2)、取上清4℃,2000g,离心10min,保留上清液;
(3)、取上清再4℃,10000g,离心30min,保留上清液;
(4)、离心后的上清4℃,100000g,离心70min,弃上清,收集沉淀即为外泌体,用pbs再将收集得到的外泌体离心洗涤一遍。
(5)、离心洗涤后的外泌体用生理盐水重悬。
实施例2、人脐带间充质干细胞外泌体体外安全性实验
cck-8法检测人脐带间充质干细胞外泌体对表皮细胞生长的影响。
检测样品:实施例1制备的人脐带间充质干细胞外泌体悬液。
受试生物体:人表皮细胞。
具体步骤:
(1)、将对数生长期的表皮细胞接种至96孔板,5000个/孔,分组为对照组和不同浓度外泌体组(1μg/ml,5μg/ml,10μg/ml,30μg/ml,50μg/ml)。
(2)、接种细胞24h后,按照分组加入不同量的外泌体,在之后的第1d、3d、5d和7d,吸弃培养板孔中旧培养基,加入含10%cck-8试剂的培养基,37℃继续孵育2h,然后用酶标仪在450nm波长处测吸光值,用cck-8法检测细胞的活力,分析外泌体是否对细胞生长有影响。
(3)、由图1可见,外泌体对人表皮细胞的生长没有毒性作用,第1d、3d、5d吸光值与对照组相比没显著差异,第7d的外泌体各组的吸光值高于对照组,表明外泌体有利于细胞的生长。
图1示实施例2,人脐带间充质干细胞外泌体体外安全性实验,cck-8法实验结果显示,外泌体对表皮细胞的生长没有毒性作用,第1d、3d、5d吸光值跟对照组相比没有差异,第7d外泌体各组的吸光值高于对照组,表明外泌体有利于细胞的生长。横坐标为时间(d),纵坐标为od值。
实施例3、人脐带间充质干细胞外泌体体内安全性实验
1.检测样品:实施例1制备的人脐带间充质干细胞外泌体悬液。
2.受试生物体:雄性昆明小鼠。
3.具体步骤:
(1)、选取体重在35~45g的雄性昆明小鼠12只,用脱毛剂除去背部毛发。
(2)、随机分为正常组、生理盐水组和不同剂量外泌体组(5~10μg/只/天,20~50μg/只/天),每组3只,外泌体组每日背部皮下注射一定量的外泌体,生理盐水组注射20μl生理盐水。
(3)、持续注射7d,同时每日观察背部皮肤变化。
(4)、由图2可见,注射了外泌体的小鼠,7天后观察,与正常组比较背部没有出现异常,初步推断对动物皮肤无毒性作用。
图2示实施例3,人脐带间充质干细胞外泌体动物实验结果显示注射了外泌体的小鼠,其背部没有出现异常。初步推断人脐带间充质干细胞外泌体对动物皮肤无毒性作用。a组为空白对照组,b组为生理盐水组,c组为外泌体组。
实施例4、人脐带间充质干细胞外泌体的抗氧化能力检测
1.检测样品:实施例1制备的人脐带间充质干细胞外泌体悬液。
2.受试生物体:人表皮细胞。
3.具体步骤:
(1)、人表皮细胞接种于10cm培养皿,随机分为正常组、h2o2组,h2o2+外泌体组。
(2)、细胞生长至融合后,统一更换为无血清培养基,同时外泌体组加入外泌体(10μg/ml)。
(3)、12h后,加入500μmh2o2,3h后收集细胞,超声破碎裂解。
(4)、根据试剂盒说明检测总抗氧化能力、总sod酶活性,谷胱甘肽过氧化物酶(gsh-px)的活性。
(5)、如图3所示,h2o2处理后,细胞的总抗氧化能力、总sod酶活性和gsh-px活性都显著下降(p<0.001),而加入了外泌体的组别,跟h2o2组相比,这三种指标都显著上升(p<0.001)。表明外泌体能够保护表皮细胞免受氧化损伤。
4免疫荧光检测:
(1)、将人表皮细胞接种于放有细胞爬片的24孔板中。
(2.)、密度达到60%时,更换为无血清培养基,分为正常组、h2o2组,h2o2+外泌体组,同时外泌体组加入外泌体(10μg/ml)。
(3)、12h后,加入500μmh2o2,3h后,4%多聚甲醛固定细胞,室温封闭2h。
(4)、孵育一抗过夜小鼠抗sod2(1:400),山羊抗8-ohdg(1:400),室温孵育二抗2h后,dapi孵育10min,每个步骤pbs洗涤3遍,每次3min,50%的甘油封片,荧光显微镜下观察。
(5)、如图4a所示8-ohdg是氧化损伤时,dna损伤的标志物,实验发现正常人表皮细胞中表达量很少,而h2o2处理后,细胞中的表达量大幅增加,且核内表达显著,同时加入外泌体的组,与h2o2组相比,显著减少。
(6)、如图4b所示sod2是抗氧化的关键分子,正常细胞中呈现高表达,h2o2处理后,sod2的表达显著下降,加入外泌体的组,表达量又显著回升,趋于正常。进一步说明外泌体具有抗氧化作用。
图3示实施例4,人脐带间充质干细胞外泌体能够保护表皮细胞免受氧化损伤,h2o2处理后,细胞的总抗氧化能力、总sod酶活性和gsh-px活性都显著下降(p<0.001),而加入了外泌体的组别,跟h2o2组相比,这三种指标都显著上升(p<0.001)。表明外泌体能够保护表皮细胞免受氧化损伤。a图纵坐标为总抗氧化能力,横坐标依次为正常组、h2o2组、外泌体组;b图纵坐标为总sod酶活性,横坐标依次为正常组、h2o2组、外泌体组;c图纵坐标为谷胱甘肽过氧化酶活性,横坐标依次为正常组、h2o2组、外泌体组。
图4示实施例4,8-ohdg为氧化损伤时,dna损伤的标志物,实验中发现正常人表皮细胞中8-ohdg表达量很少,而h2o2处理后,细胞中的表达量大幅增加,且核内表达显著,同时加入外泌体的组,与h2o2组相比,显著减少。sod2是抗氧化的关键分子,正常细胞中呈现高表达,h2o2处理后,sod2的表达显著下降,加入外泌体的组,表达量又显著回升,趋于正常。进一步说明外泌体具有抗氧化作用。图4a为人脐带间充质干细胞外泌体对人表皮细胞氧化损伤后8-ohdg表达的影响,图4b为人脐带间充质干细胞外泌体对人表皮细胞氧化损伤后sod2表达的影响。
实施例5、人脐带间充质干细胞外泌体抗氧化精华液
1.所述抗氧化精华液由如下重量份原料制成,见表1:
表1抗氧化精华液由如下重量份原料
2.抗氧化精华液的制备工艺包括如下步骤(图5):
(1)、将透明质酸钠在生产前用适量去离子无菌水溶解备用;
(2)、将a组其他物料加入后加热至75~80℃,搅拌均匀并保持10分钟;加入b组物料均质3~5分钟保温10分钟;
(3)、降温至50℃,加入c组物料,搅拌均匀并保温2分钟;
(4)、降温至40℃,加入d组物料,搅拌均匀;
(5)、冷却至35℃时加入e组物料(每种原料加入后搅拌均匀方能加入下一种物料),搅拌混合至均匀;
(6)、在35℃检测、出料、静置、半成品检验、灌装及成品入库。
图5示实施例5,人脐带间充质干细胞外泌体抗氧化精华液的工艺流程图。
实施例6、人脐带间充质干细胞外泌体精华液的稳定性测试
具体的实验步骤(图6):
(1)、a样品是未添加外泌体的精华基质,整个稳定性实验中室温保存,作为空白对照;
(2)、b样品是添加1000μg/100g外泌体的抗氧化精华,整个稳定性实验中室温保存;
(3)、c样品是添加1000μg/100g外泌体的抗氧化精华,将c样装入规格为10ml的离心管中,样品高度约8ml,塞上干净的玻璃塞。将其置于预先调节至(45±1)℃的恒温培养箱中,经48h后取出,待其恢复至室温后目测观察有无明显性状差异。
(4)、随后对其进行耐寒实验;将试样装入规格为10ml的离心管中,使样品高度约8ml,塞上干净的玻璃塞。
(5)、将高温处理48h后的样品置于预先调节至(-20±1)℃的冰箱中,经48h后取出,待其恢复至室温后目测有无明显性状差异。如此耐热耐寒交替进行45天。
(6)、45天后观察a样和b样外观(颜色,味道)无差别,肤感无明显差别,ph在误差允许范围内均达标,即与45天前的ph值相同,说明外泌体在室温时与该精华基质的配伍性良好;观察b样和c样外观(颜色,味道)无差别,肤感无明显差别,ph在误差允许范围内均达标,说明该外泌体精华的稳定性良好,稳定性实验记录如下表2:
表2实验记录
图6示实施例6,人脐带间充质干细胞外泌体抗氧化精华液经过(45±1)℃、(-20±1)℃耐热耐寒交替进行,每48小时观察一次,随后更换温度,45天后观察外观(颜色,味道)无差别,肤感无明显差别,ph在误差允许范围内均达标,即与45天前的ph值相同,说明外泌体在室温时与该精华基质的配伍性良好。
以上对本发明的具体实施方式进行了说明,但本发明并不以此为限,只要不脱离本发明的宗旨,本发明还可以有各种变化。
- 还没有人留言评论。精彩留言会获得点赞!