一种蛇毒蛋白局部用制剂及其制备方法与质量控制方法与流程
本发明属于药物制剂领域,特别涉及一种蛇毒蛋白局部用制剂及其制备方法与质量控制方法。
背景技术:
在两千多年前,西汉的《神农本草经》记载了用蛇来做为药的方法。李时珍的著《本草纲目》中也提到“蝮蛇能治平身枯死,手足脏腑间贡疾心腹痛”。蛇的毒腺可以分泌复杂的混合物,包括蛋白质、多肽、酶类和一些小分子物质,其具有一定的生物学活性。从20世纪初,蛇毒在疼痛方面的治疗就有了研究。1933年,robinson和chen探究到了眼镜蛇毒液有相当不错的镇痛作用。1934年,brazil也发现了蛇的毒液有良好止痛作用。近年来,有镇痛作用的蛇毒神经毒素更是备受关注,有研究团队发现舟山眼镜蛇毒毒素能与神经肌接头n-型乙酰胆碱受体结合,从而阻止神经递质乙酰胆碱和受体相结合。有实验证明短链的神经毒素是安全的,舟山眼镜蛇毒已在临床使用。蛇毒蛋白属于低分子多肽,主要由眼镜蛇毒中分离提纯的,由于其无成瘾、无耐受性、镇痛持久、使用便捷的优异性,在临床应用上有较好的镇痛效果,适用于慢性、顽固性、持续性疼痛治疗。有研究表明即蛇毒蛋白可以有效地治疗癌症患者晚期疼痛,并且具有明显减注射弱成瘾性的作用。蛇毒神经毒蛋白科博肽是从南眼镜蛇蛇毒中分离纯化得到《中国药典》记载,科博肽为白色粉末,按干燥品计算,含神经毒蛋白不得少于35%,具有较好的镇痛效果,可用于癌症止痛。科博肽的鉴别、检查、含量测定方法等药典上也有记载。
目前,市面上只有科博肽肠溶胶囊和注射剂。肠溶胶囊需口服,不适合不方便吞服的病人,如婴儿,而且药效成分可能遭到胃肠道消化酶与肝脏“首过效应”的破坏。而注射剂工艺复杂,价格昂贵,会使患者产生疼痛感,顺应性差。因此,有必要开发不同剂型的蛇毒蛋白制剂。
技术实现要素:
针对上述问题,本发明提供一种蛇毒蛋白局部用制剂,其包含蛇毒蛋白和水溶性基质。其中,蛇毒蛋白主要成分选自科博肽或科博肽的提纯物;水溶性基质可以是甘油、丙二醇、纤维素衍生物、卡波姆、海藻酸盐、西黄蓍胶、黄原胶、明胶、淀粉、改性淀粉、聚乙二醇、环糊精和/或β-环糊精。
作为优选,所述局部用制剂是凝胶剂、乳剂、乳膏剂、软膏剂、巴布剂、硬膏剂或栓剂,尤其是栓剂。
进一步优选,所述水溶性基质选自甘油明胶和/或聚乙二醇(peg)。
进一步优选,所述水溶性基质选自甘油明胶,且甘油与明胶的重量用量配比为3.5~0.5。
进一步优选,所述水溶性基质选自peg400、peg4000和/或peg6000。
进一步优选,所述水溶性基质选自peg400与peg4000的组合,二者重量用量配比为0.4~1.5。
进一步优选,所述peg400与peg4000的重量用量配比为0.4。
进一步优选,所述水溶性基质peg400与peg4000的重量用量之和是蛇毒蛋白的300~400倍,且以350倍为佳。
进一步优选,所述蛇毒蛋白局部用制剂还包含促渗剂。
进一步优选,所述促渗剂选自表面活性剂十二烷基硫酸钠、吐温80和/或泊洛沙姆,且以吐温80为佳。
进一步优选,所述吐温80的重量用量是栓剂总重的0.25%~2.5%,例如1%或2.5%。
本发明还提供蛇毒蛋白局部用制剂的制备方法,包括下述步骤:按比例称取水溶性基质peg,溶解或熔化,加入蛇毒蛋白,采用冷压法和热熔法制备成栓剂。
优选,加入蛇毒蛋白后,还加入促渗剂;所述促渗剂选自表面活性剂十二烷基硫酸钠、吐温80和/或泊洛沙姆,优选吐温80。
所述蛇毒蛋白局部用制剂的制备方法,优选采用热熔法制备成栓剂。
进一步优选,所述蛇毒蛋白栓剂的制备方法包括下述步骤:按比例称取水溶性基质peg4000、peg400,加热熔化;待温度降至36℃~50℃,加入蛇毒蛋白与吐温80,混匀;趁热注入栓模中,固化(温度为-2~2℃),脱模,即得。
进一步优选,所述蛇毒蛋白栓剂的制备方法包括下述步骤:按比例称取水溶性基质peg4000、peg400,加热熔化;待温度降至36℃~50℃,加入蛇毒蛋白与吐温80,搅拌均匀;趁热注入栓模中,固化(温度为-2~2℃),脱模,即得。
进一步优选,所述蛇毒蛋白栓剂的制备方法包括下述步骤:按比例称取水溶性基质peg4000、peg400,加热熔化;待温度降至36℃,加入蛇毒蛋白与吐温80,搅拌均匀;趁热注入栓模中,固化(温度为-2~2℃),脱模,即得。
本发明还提供蛇毒蛋白栓剂的质量控制方法,其特征在于包括有效成分蛇毒蛋白含量的检测。
作为优选,采用高效液相色谱法检测有效成分蛇毒蛋白的含量。
进一步优选,检测波长为277nm。
进一步优选,采用dikmaplastilods柱(4.6mm×150mm)
进一步优选,以0.1%三氟醋酸溶液为流动相a,三氟醋酸-50%乙腈溶液(1:1000)为流动相b;
进一步优选,采用梯度洗脱,具体条件为:洗脱初始状态流相b为8%,保持2min,在8min内流动相b增至100%,保持8min,再在6min内回到初始状态,保持10min。
进一步优选,柱温36℃;流速为每1ml.min-1。
前述蛇毒蛋白含量的检测方法同样适用于栓剂中蛇毒蛋白含量均匀度测定与溶出度测定。
进一步优选,所述蛇毒蛋白栓剂的质量控制方法还包括栓剂的外观检查、重量差异检查、融变时限检查中的一种或多种。
本发明的蛇毒蛋白局部用制剂工艺成本低、质量稳定、药效可靠,既能克服注射剂工艺复杂、价格昂贵、顺应性差等缺点,又能有效避免药物对胃的刺激,以及消化酶与肝脏“首过效应”对药效成分的破坏作用。与口服制剂相比较,本发明的蛇毒蛋白局部用制剂还具有吸收快、生物利用度高、起效快等特点,且适合不方便吞服的病人,如婴儿。本发明的蛇毒蛋白栓剂通过直肠或其他腔道给药,缓慢释药,还具有作用强而持久等优点。
本发明的蛇毒蛋白栓剂的质量控制方法稳定性高,可控性强,容易操作,能很好地保证蛇毒蛋白栓剂的质量。
本发明的其它特征和优点将在随后的说明书中阐述,并且,部分地从说明书中变得显而易见,或者通过实施本发明而了解。本发明的目的和其他优点可通过在说明书、权利要求书以及附图中所指出的结构来实现和获得。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作一简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
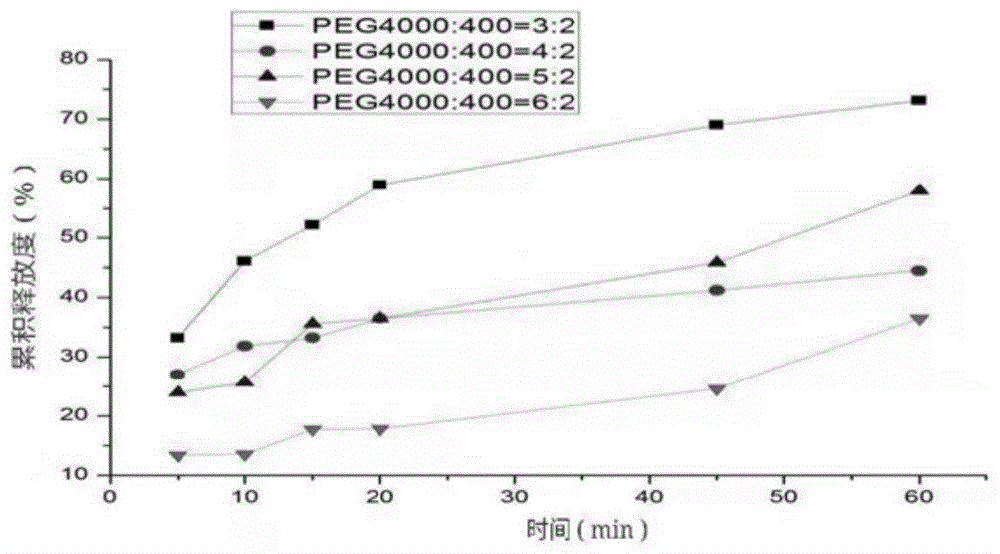
图1示出了不同用量peg4000对药物释放的影响;
图2示出了不同用量peg400对药物释放的影响;
图3示出了不同种类表面活性剂对药物释放的影响;
图4示出了不同用量吐温80对药物释放的影响;
图5示出了不同温度对药物释放的影响;
图6示出了蛇毒蛋白的hplc色谱图,其中a表示空白溶剂的hplc色谱图;b表示蛇毒蛋白溶液(87.5μg/ml)的hplc色谱图;c:蛇毒蛋白栓剂供试液(87.5μg/ml)的hplc色谱图;
图7示出了蛇毒蛋白栓剂的溶出度释放曲线;
图8示出了栓剂的外观要求。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地说明,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
一、蛇毒蛋白局部用制剂处方的选择
1.基质的选择
1.1peg基质的选择
取不同比例混合的各类型号的peg,于65℃温度下熔融,注入冷却模具中,冷却后,得空白基质栓。按《中华人民共和国药典》2015版四部通则0612“熔点测定法”第二法,测定不易粉碎的固体药品提供的方法,测定其熔点,经比较,在peg600:peg6000下的比例所测的熔点高(详见表1),为利于栓剂体温下在人体腔道融化或软化,故选择peg400:peg4000与peg400:peg6000较好。下一步实验即以甘油明胶、peg400:peg4000与peg400:peg6000进行比较。
表1不同比例peg的熔点
1.2甘油明胶与peg的选择
按照表2所列基质重量用量比例制备栓剂,具体为:
(1)取适量的明胶,加入与其比例为1:1的超纯水,将明胶静置1-2h充分溶胀。加入甘油于65℃浴上加热蒸发,沿着同一方向轻轻搅拌,避免产生大量气泡。待其温度降至36℃,加入适量蛇毒蛋白充分搅拌,迅速注入冷却的栓模中,固化,脱模。
(2)取不同比例混合的peg,于65℃温度下熔融,待温度降至适宜温度,加入蛇毒蛋白,充分搅拌,注入冷却模具中,固化,脱模。
(3)观察不同类型基质制备的栓剂的外观。
由实验现象及结果得出,加入peg6000会使溶液产生白色沉淀可能导致部分蛇毒蛋白失活,而且制得的栓剂容易脆,不适合作蛇毒蛋白的载体,而甘油明胶明显优于peg6000。因此,选择甘油明胶或者peg400:peg4000作为基质;但是由于含量测定时甘油明胶在277nm处的吸收波长干扰药物的吸收波长,故选用peg400:peg4000作为基质为佳。
表2不同类型基质的考察
1.3peg4000用量的选择
以6枚栓剂的处方用量为例,称取20mg蛇毒蛋白与2gpeg400,加入2g、3g、4g、5g、6gpeg4000,置于干燥的烧杯中,70℃水浴加热,待其完全熔化,搅拌均匀使基质全熔,温度降至36℃加入适量蛇毒蛋白,边加边搅拌。趁热注入已涂好润滑剂的栓模中,固化(温度为-2~2℃),用刀片切出溢出部分,脱模,制成6枚栓剂。对不同用量peg4000制备的栓剂的性能进行评分(详见表3),并测试蛇毒蛋白释放速度(详见图1)。
表3不同用量peg4000的考察
由表3和图1可知,随着peg4000用量增加,栓剂外观性状、完整均匀,硬度,累计溶出度逐渐变好,但是用量超过5.0g时,栓剂的栓剂外观性状、完整均匀,硬度,累计溶出度开始变差。可见peg4000用量过多会导致硬度过大,外观不美观。当用量在peg4000用量3.0~5.0g时,各项指标良好,因此确定其用量范围为3.0~5.0g。
1.4peg400用量的选择
以6枚栓剂的处方用量为例,称取20mg蛇毒蛋白与5gpeg4000,加入1g、2g、3g、4g、5g、peg400,置于干燥的烧杯中,70℃水浴加热,待其完全熔化,搅拌均匀使基质全熔,温度降至36℃加入适量蛇毒蛋白,边加边搅拌。趁热注入已涂好润滑剂的栓模中,固化(温度为-2~2℃),用刀片切出溢出部分,脱模,制成6枚栓剂。对不同用量peg4000制备的栓剂的性能进行评分(详见表4),并测试蛇毒蛋白释放速度(详见图2)。
表4不同用量peg400的考察
由表4和图2可知,随着peg400用量增加,栓剂外观性状、完整均匀,硬度,累计溶出度逐渐变好,但是用量超过4.0g时,栓剂的栓剂外观性状、完整均匀,硬度,累计溶出度开始变差。可见peg400用量过多会导致硬度不够,外观不美观。当用量在peg400用量2.0~4.0g时,各项指标良好,因此确定其用量范围为2.0~4.0g。
1.5促渗剂种类对药物释放的影响
本发明采用表面活性剂作为促渗剂。表面活性剂除了能显著减小溶液的表面张力外,还可用于增溶、乳化、润湿、去污、杀菌消泡和起泡等。本发明选取了几种有代表性的表面活性剂十二烷基硫酸钠(sds)(0.25%,指占栓剂总重的百分比)、吐温80(1%)、泊洛沙姆(polo)(2.5%)进行考察。对制得的栓剂的性能进行评分(详见表5),并测试蛇毒蛋白释放速度(详见图3)。
具体制备方法:按处方量称取peg4000、peg400,置于干燥的烧杯中,70℃水浴加热,使其完全熔化,混匀;待温度降至36℃,加入适量蛇毒蛋白,加入表面活性剂(十二烷基硫酸钠、吐温80或泊洛沙姆),边加边搅拌;趁热注入已涂好润滑剂的栓模中,固化(温度为-2~2℃),用刀片切出溢出部分,脱模,即得。
实验方法:采用溶出度第二法篮法进行测定(转速为50r.min-1,温度为37±0.5℃)。加入溶出介质ph为7.4的pbs,于5、10、15、20、45、60min分别取样,并补充相应量介质,用0.45μm微孔滤膜过。
表5不同种类的筛选结果
由表5和图3可知,选择表面活性剂0.25%十二烷基硫酸钠,1%吐温80,2.5%泊洛沙姆做促渗剂制得的栓剂的溶出度较好,其中吐温80优于泊洛沙姆,泊洛沙姆优于十二烷基硫酸钠。
1.6吐温80用量对药物释放的影响
按处方量称取peg4000、peg400,置于干燥的烧杯中,70℃水浴加热,待其完全熔化,搅拌均匀使基质全熔,温度分别降至36℃,加入适量蛇毒蛋白,加入不同量的吐温80表面活性剂边加边搅拌。趁热注入已涂好润滑剂的栓模中,固化(温度为-2~2℃),用刀片切出溢出部分,脱模,得样品。对制得的栓剂的性能进行评分(详见表6),并测试蛇毒蛋白释放速度(详见图4)
表6不同用量吐温80的考察
由表6和图4可知,1%吐温80和2.5%吐温80对蛇毒蛋白的促渗作用远远大于0.5%吐温80,当吐温80的浓度增大到一定数值时,会影响栓剂的硬度,故最高只选用2.5%吐温80。对蛇毒蛋白栓剂的促渗作用大小为:2.5%吐温80>1%吐温80>0.5%吐温80>0.25%吐温80;加入吐温80制备的栓剂外观性状、完整均匀,硬度均符合要求。因此,选择2.5%的吐温80作为促渗剂为佳。
2.栓剂处方的优化
选择栓剂中对蛇毒蛋白综合评分影响较大的四个因素进行正交实验对处方进行优化,分别为a:peg4000用量(g);b:反应温度;c:吐温80用量;d:peg400用量(g)(详见表7)。以制备6枚栓剂的用量为例。
表7正交实验因素水平表
表8正交试验方法与结果
表9方差分析结果
f0.05(2)=19.0
由表8、表9可见,各因素对蛇毒蛋白栓剂制备工艺的影响次序为:a>d>c>b,a(peg400)因素有显著影响确定筛选的最佳基本处方为a3b3c3d3,即:peg400用量为2g,peg4000用量为5g,温度为50℃,吐温含量为2.5%。
二、蛇毒蛋白局部用制剂的制备方法
1.温度对药物释放的影响
按处方量称取peg4000、peg400,置于干燥的烧杯中,70℃水浴加热,待其完全熔化,搅拌均匀使基质全熔,温度分别降至36℃,46℃,50℃,60℃加入适量蛇毒蛋白,边加边搅拌。趁热注入已涂好润滑剂的栓模中,固化(温度为-2~2℃),用刀片切出溢出部分,脱模,得样品。对制得的栓剂的性能进行评分(详见表10),并测试蛇毒蛋白释放速度(详见图5)。
表10不同温度的考察
由表10和图5可知,随着温度增加,溶出度逐渐增加,当温度大于50℃,可能会导致蛇毒蛋白失效,因此确定其温度范围为36℃~50℃。
2.栓剂冷却时间对药物释放的影响
按处方量称取peg4000、peg400,置于干燥的烧杯中,70℃水浴加热,待其完全熔化,搅拌均匀使基质全熔,温度分别降至36℃,加入适量蛇毒蛋白,加入处方量的吐温80表面活性剂边加边搅拌。趁热注入已涂好润滑剂的栓模中,固化(温度为-2~2℃)不同时间,用刀片切出溢出部分,脱模,得样品。对制得的栓剂的性能进行评分(详见表11)。
表11不同冷却时间的考察
由表11可知,冷却时间长短不会影响栓剂的外观性状、完整均匀,硬度均符合要求。
实施例1
处方(以6枚栓剂用量为例):
蛇毒蛋白原料药(科博肽)20mg;
peg4002g;
peg40005g;
超纯水少量;
制备方法:精密称取20mg蛇毒蛋白原料药于适量超纯水溶解成蛇毒蛋白溶液;按处方量称取peg4000、peg400,加热使其完全熔化、混匀;待温度降至36℃,加入制备好的蛇毒蛋白溶液,混匀;趁热注入已涂好润滑剂的栓模中,固化,脱模,即得。
实施例2
处方(以6枚栓剂用量为例):
蛇毒蛋白原料药(科博肽)20mg;
peg4002g;
peg40005g;
吐温180mg(含量百分数为2.5%);
超纯水少量;
制备方法:精密称取20mg蛇毒蛋白原料药于适量超纯水溶解成蛇毒蛋白溶液;按处方量称取peg4000、peg400,加热使其完全熔化、混匀;待温度降至36℃,加入制备好的蛇毒蛋白溶液,加入吐温80,混匀;趁热注入已涂好润滑剂的栓模中,固化,脱模,即得。
实施例3
处方(以6枚栓剂用量为例):
蛇毒蛋白原料药(科博肽)20mg;
peg4004.2g;
peg40002.8g;
吐温180mg(含量百分数为2.5%);
超纯水少量;
制备方法:精密称取20mg蛇毒蛋白原料药于适量超纯水溶解成蛇毒蛋白溶液;按处方量称取peg4000、peg400,置于干燥的烧杯中,水浴加热使其完全熔化、混匀;待温度降至46℃,加入制备好的蛇毒蛋白溶液,加入吐温80,边加边搅拌;趁热注入已涂好润滑剂的栓模中,固化(温度为-2~2℃),脱模,即得。
实施例4
处方(以6枚栓剂用量为例):
蛇毒蛋白原料药(科博肽)20mg;
peg4003g;
peg40004g;
吐温72mg(含量百分数为1%);
超纯水少量;
制备方法:精密称取20mg蛇毒蛋白原料药于适量超纯水溶解成蛇毒蛋白溶液;按处方量称取peg4000、peg400,置于干燥的烧杯中,70℃水浴加热使其完全熔化、混匀;待温度降至50℃,加入制备好的蛇毒蛋白溶液,加入吐温80,边加边搅拌;趁热注入已涂好润滑剂的栓模中,固化(温度为-2~2℃),用刀片切出溢出部分,脱模,即得。
实施例5
处方(以6枚栓剂用量为例):
蛇毒蛋白原料药(科博肽)20mg;
peg4004g;
peg40003g;
吐温18mg(含量百分数为0.25%);
超纯水少量;
制备方法:精密称取20mg蛇毒蛋白原料药于适量超纯水溶解成蛇毒蛋白溶液;按处方量称取peg4000、peg400,置于干燥的烧杯中,70℃水浴加热使其完全熔化,搅拌均匀;待温度降至50℃,加入制备好的蛇毒蛋白溶液,加入吐温80,边加边搅拌;趁热注入已涂好润滑剂的栓模中,固化(温度为-2~2℃),用刀片切出溢出部分,脱模,即得。
实施例6
处方(以6枚栓剂用量为例):
蛇毒蛋白原料药(科博肽)20mg;
甘油7g;
明胶2g;
超纯水少量;
制备方法:取处方量的明胶,加入与其比例为1:1的超纯水,静置1~2h充分溶胀;加入甘油,于65℃水浴加热蒸发,沿着同一方向轻轻搅拌,避免产生大量气泡;待其温度降至36℃,加入适量蛇毒蛋白,充分搅拌,迅速注入冷却的栓模中,固化,脱模,即得。
实施例7
处方(以6枚栓剂用量为例):
蛇毒蛋白原料药(科博肽)20mg;
甘油6g;
明胶2g;
超纯水少量;
制备方法:取处方量的明胶,加入与其比例为1:1的超纯水,静置1~2h充分溶胀;加入甘油,于65℃水浴加热蒸发,沿着同一方向轻轻搅拌,避免产生大量气泡;待其温度降至36℃,加入适量蛇毒蛋白,充分搅拌,迅速注入冷却的栓模中,固化,脱模,即得。
实施例8
处方(以6枚栓剂用量为例):
蛇毒蛋白原料药(科博肽)20mg;
peg4002g;
peg40005g;
泊洛沙姆180mg(含量百分数为2.5%);
超纯水少量;
制备方法:精密称取20mg蛇毒蛋白原料药于适量超纯水溶解成蛇毒蛋白溶液;按处方量称取peg4000、peg400,加热使其完全熔化、混匀;待温度降至36℃,加入制备好的蛇毒蛋白溶液,加入泊洛沙姆,混匀;趁热注入已涂好润滑剂的栓模中,固化,脱模,即得。
实施例9
处方(以6枚栓剂用量为例):
蛇毒蛋白原料药(科博肽)20mg;
peg4002g;
peg40005g;
十二烷基硫酸钠18mg(含量百分数为0.25%);
超纯水少量;
制备方法:精密称取20mg蛇毒蛋白原料药于适量超纯水溶解成蛇毒蛋白溶液;按处方量称取peg4000、peg400,加热使其完全熔化、混匀;待温度降至36℃,加入制备好的蛇毒蛋白溶液,加入十二烷基硫酸钠,混匀;趁热注入已涂好润滑剂的栓模中,固化,脱模,即得。
实施例10
处方(以6枚栓剂用量为例):
蛇毒蛋白原料药(科博肽)20mg;
peg4002g;
peg40005g;
超纯水少量;
制备方法:精密称取20mg蛇毒蛋白原料药于适量超纯水溶解成蛇毒蛋白溶液;按处方量称取peg4000、peg400,加热使其完全熔化、混匀;待温度降至36℃,加入制备好的蛇毒蛋白溶液,混匀;放冷后,采用冷压法制备成栓剂。
三、蛇毒蛋白局部用制剂的质量控制方法
1.样品含量测定条件的确定
1.1波长的选择
精密称取蛇毒蛋白适量,加入流动相溶解,配成质量浓度为35μg/ml的溶液作为对照品溶液。另取适量基质,加入适量流动相,置于水浴中(水浴温度为50℃)使基质溶解,充分混匀后冷却5min,过滤,取续滤液作为空白基质溶液。取以上两种溶液,进行200nm~600nm,结果表明蛇毒蛋白在277nm处有最大吸收,而空白基质溶液在277nm处紫外吸收较弱,不干扰蛇毒蛋白测定。
1.2色谱条件
dikmaplastilods柱(4.6mm×150mm);以0.1%三氟醋酸溶液为流动相a,三氟醋酸-50%乙腈溶液(1:1000)为流动相b;梯度洗脱条件:洗脱初始状态流相b为8%,保持2min,在8min内流动相b增至100%,保持8min,再在6min内回到初始状态,保持10min。柱温36℃;流速为每1ml.min-1;检测波长为277nm。理论板数以蛇毒蛋白的峰计算应大于3000。
1.3对照品溶液制备
精密称定蛇毒蛋白7mg,置20ml量瓶中,先加流动相定容为350μg/ml的标准液;临用前再将此标准液加乙腈,分别稀释为3.5、7、35、89.5、175、350μg/ml的供试品溶液。
1.4供试品溶液制备
取蛇毒蛋白栓剂10粒,将其剪碎,精密称定栓剂(含蛇毒蛋白约0.7mg),加入流动相溶液与栓剂碎屑,放于50℃水浴上加热直至栓剂碎片全部熔融,混匀后冷却约5min,取适量经0.45μm微孔滤膜过滤后,将滤液置于20ml容量瓶中。
1.5专属性实验
按“1.2”项色谱条件,按照处方量加入所有辅料稀释至刻度过滤进样,色谱图见图6-a。精密称取蛇毒蛋白3.5mg置20ml容量瓶中,流动相超声溶解并定容到刻度,混匀,即175μg/ml的储备液,过滤,按4.3.1进样,色谱图见图6-b。称取一定量栓剂(相当于含有0.7mg蛇毒蛋白),流动相超声溶解并定容到20ml,摇匀得蛇毒蛋白栓剂供试液,进样,色谱图见图6-c。实验表明:辅料对蛇毒蛋白测定不产生干扰,蛇毒蛋白色谱峰分离良好。分别精密吸取20μl对照品溶液液、供试品溶液和空白溶剂,进hplc检测。由图6可知,供试品和对照品溶液均在相应位置上出峰,而空白溶剂没有出峰,说明空白溶剂对蛇毒蛋白检测无干扰。
1.6标准曲线的绘制
取按“1.3”项下配制的蛇毒蛋白标准液10μl,加入流动相分别稀释为3.5、7、35、89.5、175、350μg/ml的供试品溶液,进样分析。其中,以蛇毒蛋白浓度作为横坐标(x),以蛇毒蛋白峰面积作为纵坐标(y),进行线性拟合。以色谱峰信噪比(s/n)为10时,作为定量下限。线性拟合得到蛇毒蛋白的标准曲线为y=1435.3x+862.22(r=0.997),线性范围为3.5-350μg/ml,定量下限为3.5μg/ml(n=5)。
1.7精密度实验
取“1.3”项下的对照品溶液35μg/ml,连续进样五次,按照以上色谱条件,记录峰面积,计算rsd(n=5)值分别为1.24%、表明精密度良好。
1.8样品日间稳定性实验
取样品适量,按“1.2”项色谱条件测定,分别于0、2、4、6、8、12h进样,记录样品峰面积并计算rsd为1.34%,表明样品在12h内稳定性良好。
1.9加样回收率实验
精密吸取蛇毒蛋白对照品,35、42、28μg/ml(100%,120%,80%)的低、中、高三个浓度的溶液,按处方比例加入空白基质,制备成高中低三个样品溶液,经0.45μm微孔滤膜过滤,取20μl上清液注入高效液相色谱仪,记录峰面积,计算回收率。结果说明方法回收率符合要求(详见表12)。
表12加样回收率实验结果(n=6)
实施例1:含量测定
分别取3批样品,每批10粒,剪碎混匀,精密称取1.2g,于10ml锥形瓶中,加入流动相稀释至刻度,水浴(50±2)℃加热使样品熔化,超声约5min,再精密移取5ml于10ml锥形瓶加流动相稀释至刻度,按照以上建立的高效液相含量测定方法进行含量分析3批样品中蛇毒蛋白标示量含量为85.09%,85.12%,86.03%(详见表13)。
表13蛇毒蛋白栓剂中蛇毒蛋白含量测定结果(
实施例2:含量均匀度测定
分别取3批样品,每批10粒,剪碎混匀,精密称取1.2g,于10ml锥形瓶中,加入流动相稀释至刻度,水浴(50±2)℃加热使样品熔化,超声约5min,再精密移取5ml于10ml锥形瓶加流动相稀释至刻度,按照以上建立的高效液相含量测定方法进行含量均匀度测定,结果详见表14。
表14蛇毒蛋白栓剂中蛇毒蛋白含量均匀度测定结果(
实施例3:溶出度测定
按2015版《中国药典》规定,选用ph7.0的磷酸盐缓冲溶液做溶出介质。取三批制剂,设定转速为50r·min-1,温度为37℃,分别在5,10,25,45,60,90,120,180min取样,在277nm处测定溶出液的溶出度,计算累积释放量。结果详见图7。
2.栓剂的外观检查
蛇毒蛋白peg栓剂呈白色半透明状,表面光滑,有一定硬度(详见图8)。
3.栓剂重量差异及融变时限检查
根据《中国药典》2015版二部附录规定操作,制备的三批栓剂批号:(20170915,20170916,20170917)的重量差异分别为±5.19%(如表15)、±5.14%和±5.13%;按照《中国药典》附录xb项下融变时限检查法取3枚蛇毒蛋白栓剂测定融变时限。融变时间分别为22min14s、20min23s和21min35s,结果均符合《中国药典》规定(详见表15)。
表15栓剂样品的重量差异
尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
- 还没有人留言评论。精彩留言会获得点赞!