一种具有抗卵巢癌活性的靶向纳米粒及制备和应用的制作方法
本发明属制药领域,涉及种具有抗卵巢癌活性的靶向纳米粒,及制备和在制备治疗卵巢癌疾病药物中的应用。
背景技术:
与其他妇科恶性肿瘤相比,卵巢癌的发病较为隐匿。有报道,75%以上的卵巢癌患者在确诊时已为晚期。近年来尽管卵巢癌的治疗手段在不断的改善,但其致死率仍旧是女性妇科肿瘤中最高的,卵巢癌患者的五年生存率从1975年的33.7%仅提高到2011年的45.6%。卵巢癌治疗的常规方案是通过手术切除肉眼可见的肿瘤和残留病灶并加以化疗,虽然卵巢癌对一线化疗药物(如紫杉醇)敏感,但效果短暂,很容易产生耐药性。据统计90%的iii-iv期卵巢癌患者死亡是因为多药耐药。因此,降低卵巢癌死亡率是临床重大的挑战,寻找有效的方法逆转卵巢癌-紫杉醇耐药具有重要意义。
姜黄素是一种天然多酚化合物,可用作功能性食品,药物和营养补充剂。它具有多种药理特性,如抗氧化,抗炎性,并已被证明可抑制肿瘤细胞的增殖。近年来,随着耐药性研究的深入,人们发现姜黄素可以通过调节多种信号通路,一定程度上提高药物的敏感性,逆转肿瘤耐药性。然而,姜黄素的应用受到其化学不稳定性,低水溶性和口服生物利用度差的限制。
纳米递送载体可通过改善溶解性和保护生物活性而大大提高治疗功效。此外,纳米粒还可以提高耐药细胞对药物的摄取,并向肿瘤组织提供精确的药物治疗,以减少全身毒性。卵巢癌组织表达较高水平的cd44,其为驱动肿瘤转移并且可能是肿瘤对化疗耐药的原因之一。当cd44被敲低时,增殖,侵袭活性和球状体形成被显著抑制,同时药物敏感性增强。因此,开发靶向cd44的策略可以预防卵巢癌的转移和耐药性。
透明质酸(ha)是一种聚阴离子多糖,具有低毒性,可生物降解和生物相容性,并且其产物诱导受体介导的细胞内信号传导。用ha修饰的纳米粒与癌细胞膜上过表达的cd44高度亲和,使其能靶向到卵巢癌细胞中。
技术实现要素:
本发明的一个目的是提供一种具有抗卵巢癌活性的靶向纳米粒,该纳米粒负载了紫杉醇和姜黄素,其纳米粒材料由硬脂酸(分子量为284.48da)、聚乙烯亚胺(分子量为10kda)和透明质酸(分子量为10kda)组成,其中硬脂酸与聚乙烯亚胺的质量比为2:1-2:5,透明质酸占硬脂酸、聚乙烯亚胺和透明质酸质量三者之和的10%,所负载的药物紫杉醇和姜黄素分别占总纳米粒的0.4%和0.4%。
本发明的另一个目的是提供所述靶向纳米粒的制备方法,是将碳二亚胺(edc)作为羧基的活化剂,将硬脂酸的羧基(sa)和聚乙烯亚胺(pei)的伯胺基脱水缩合,得到pei-sa。具体通过以下步骤实现:
(1)将199mg硬脂酸的羧基(sa)预先溶解在50ml热乙醇中,并将500mg聚乙烯亚胺(pei)分别溶解在40ml蒸馏水中,然后,在搅拌下将它们在80℃下混合,在300rpm搅拌下将750mg碳二亚胺(edc)加入混合物中,持续24小时,使用透析膜(mwco:3.5kda,spectrumlaboratories,lagunahills,ca)将反应溶液在10%乙醇溶液透析48小时以除去副产物,最后,用蒸馏水透析2小时,将透析的产物冻干,收集pei-sa,然后用5mg/ml浓度的ha涂覆pei-sa溶液,得到(pei-sa)ha冻干品。
(2)精密称取10mg(pei-sa)ha冻干品,加入适量的去离子水分散,制备得到浓度为1mg/ml的溶液,然后在室温下搅拌下将0.8ml紫杉醇和姜黄素(1mg/ml)乙醇溶液缓慢加入纳米溶液中,在冰浴中将混合物超声处理15分钟。之后,将混合物搅拌4小时,然后使用透析膜(mwco:7000da,usa)在纯水中透析过夜并经常更换纯净水。然后,将溶液以3500rpm离心15分钟以除去未加载的紫杉醇和姜黄素,用0.45μm孔径过滤器过滤并冻干,得到紫杉醇和姜黄素的(pei-sa)ha纳米粒(缩写为(pei-sa)ha/pc)。
本发明的再一个目的是提供所述的一种具有抗卵巢癌活性的靶向纳米粒在制备载抗卵巢癌活性靶向药物中的应用,所载药物为杉醇和姜黄素。研究报名载药纳米粒与游离药物相比(游离紫杉醇和姜黄素),可显著改善其在细胞水平的抗卵巢癌活性。
本发明利用sa的亲脂性和pei的亲水性,嫁接形成两亲型的纳米粒,同时利用ha的“受体-配体”特性,靶向卵巢癌细胞,以提高药物在靶标组织的富集,从而达到提高药物抗卵巢癌活性的目的,同时姜黄素的参与协同紫杉醇的抗肿瘤效果,并逆转其耐药性。
本发明的有益之处是:通过具有细胞摄取和细胞质滞留功能的高分子纳米材料,同时利用“受体-配体”特性,对靶标位于细胞内药物的包封,可大大增加卵巢癌细胞对药物的摄取。增加卵巢癌细胞对药物的摄取,有利于减少药物在正常组织的分布,降低药物的毒副作用;而姜黄素的联合协同了紫杉醇对卵巢癌细胞的毒性,增强紫杉醇的抗卵巢癌活性的同时逆转其耐药性。
附图说明
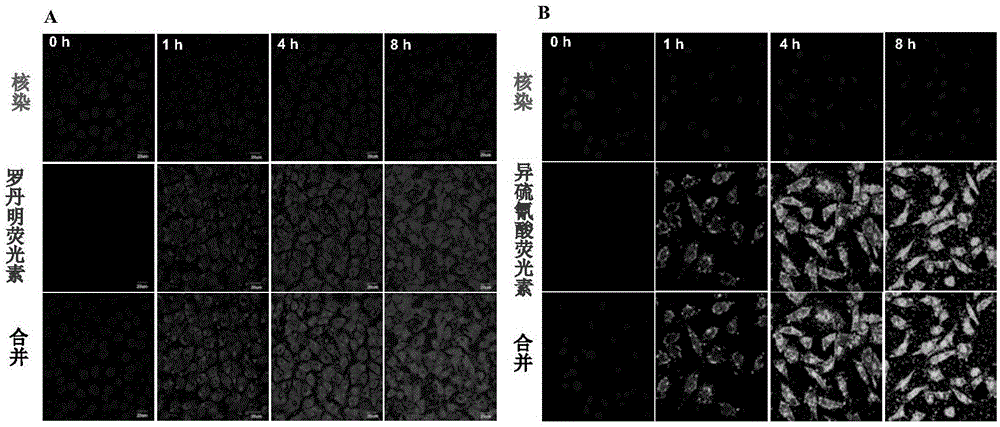
图1为共聚焦荧光显微镜观察(pei-sa)ha/pc在skov3的细胞摄取。
图2为纳米粒在卵巢癌组织微环境中的示意图。
具体实施方式
本发明结合附图和实施例做进一步的说明。
实施例1:抗卵巢癌活性纳米粒的制备
(1)抗卵巢癌活性纳米粒的制备
碳二亚胺(edc)作为羧基的活化剂,将硬脂酸的羧基(sa)和聚乙烯亚胺(pei)的伯胺基脱水缩合,得到pei-sa。将199mgsa预先溶解在50ml热乙醇中,并将100mgpei分别溶解在40ml蒸馏水中。然后,在搅拌下将它们在80℃下混合。在300rpm搅拌下将750mgedc加入混合物中,持续24小时。使用透析膜(mwco:3.5kda,spectrumlaboratories,lagunahills,ca)将反应溶液在10%乙醇溶液透析48小时以除去副产物。最后,用蒸馏水透析2小时,将透析的产物冻干,收集pei-sa。然后用5mg/mlha涂覆pei-sa溶液,得到(pei-sa)ha冻干品。
精密称取10mg(pei-sa)ha冻干品,加入适量的去离子水分散,制备得到浓度为1mg/ml的溶液,然后在室温下搅拌下将0.8ml紫杉醇和姜黄素(1mg/ml)乙醇溶液缓慢加入纳米溶液中,在冰浴中将混合物超声处理15分钟。之后,将混合物搅拌4小时,然后使用透析膜(mwco:7000da,usa)在纯水中透析过夜并经常更换新鲜水。然后,将溶液以3500rpm离心15分钟以除去未加载的紫杉醇和姜黄素,用0.45μm孔径过滤器过滤并冻干,得到紫杉醇和姜黄素的(pei-sa)ha纳米粒(缩写为(pei-sa)ha/pc)。
采用微粒粒度与表面电位测定仪,分别测定(pei-sa)ha/pc纳米粒的粒径大小、表面电位、药物包封率和载药量(表1)。表1为(pei-sa)ha/pc纳米粒的粒径大小和分布图(sa与pei的质量比为2:1)。
表1抗卵巢癌活性纳米粒的粒径、表面电位和药物包封率。
实施例2:抗卵巢癌活性纳米粒的制备
(1)抗卵巢癌活性纳米粒的制备
碳二亚胺(edc)作为羧基的活化剂,将硬脂酸的羧基(sa)和聚乙烯亚胺(pei)的伯胺基脱水缩合,得到pei-sa。将199mgsa预先溶解在50ml热乙醇中,并将300mgpei分别溶解在40ml蒸馏水中。然后,在搅拌下将它们在80℃下混合。在300rpm搅拌下将750mgedc加入混合物中,持续24小时。使用透析膜(mwco:3.5kda,spectrumlaboratories,lagunahills,ca)将反应溶液在10%乙醇溶液透析48小时以除去副产物。最后,用蒸馏水透析2小时,将透析的产物冻干,收集pei-sa。然后用5mg/mlha涂覆pei-sa溶液,得到(pei-sa)ha冻干品。
精密称取10mg(pei-sa)ha冻干品,加入适量的去离子水分散,制备得到浓度为1mg/ml的溶液,然后在室温下搅拌下将0.8ml紫杉醇和姜黄素(1mg/ml)乙醇溶液缓慢加入纳米溶液中,在冰浴中将混合物超声处理15分钟。之后,将混合物搅拌4小时,然后使用透析膜(mwco:7000da,usa)在纯水中透析过夜并经常更换新鲜水。然后,将溶液以3500rpm离心15分钟以除去未加载的紫杉醇和姜黄素,用0.45μm孔径过滤器过滤并冻干,得到紫杉醇和姜黄素的(pei-sa)ha纳米粒(缩写为(pei-sa)ha/pc)。
采用微粒粒度与表面电位测定仪,分别测定(pei-sa)ha/pc纳米粒的粒径大小、表面电位、药物包封率和载药量(表2)。表2为(pei-sa)ha/pc纳米粒的粒径大小和分布图(sa与pei的质量比为2:3)。
表2抗卵巢癌活性纳米粒的粒径、表面电位和药物包封率。
实施例3:抗卵巢癌活性纳米粒的制备
1)抗卵巢癌活性纳米粒的制备
碳二亚胺(edc)作为羧基的活化剂,将硬脂酸的羧基(sa)和聚乙烯亚胺(pei)的伯胺基脱水缩合,得到pei-sa。将199mgsa预先溶解在50ml热乙醇中,并将500mgpei分别溶解在40ml蒸馏水中。然后,在搅拌下将它们在80℃下混合。在300rpm搅拌下将750mgedc加入混合物中,持续24小时。使用透析膜(mwco:3.5kda,spectrumlaboratories,lagunahills,ca)将反应溶液在10%乙醇溶液透析48小时以除去副产物。最后,用蒸馏水透析2小时,将透析的产物冻干,收集pei-sa。然后用5mg/mlha涂覆pei-sa溶液,得到(pei-sa)ha冻干品。
精密称取10mg(pei-sa)ha冻干品,加入适量的去离子水分散,制备得到浓度为1mg/ml的溶液,然后在室温下搅拌下将0.8ml紫杉醇和姜黄素(1mg/ml)乙醇溶液缓慢加入纳米溶液中,在冰浴中将混合物超声处理15分钟。之后,将混合物搅拌4小时,然后使用透析膜(mwco:7000da,usa)在纯水中透析过夜并经常更换新鲜水。然后,将溶液以3500rpm离心15分钟以除去未加载的紫杉醇和姜黄素,用0.45μm孔径过滤器过滤并冻干,得到紫杉醇和姜黄素的(pei-sa)ha纳米粒(缩写为(pei-sa)ha/pc)。
采用微粒粒度与表面电位测定仪,分别测定(pei-sa)ha/pc纳米粒的粒径大小、表面电位、药物包封率和载药量(表3)。表3为(pei-sa)ha/pc纳米粒的粒径大小和分布图(sa与pei的质量比为2:5)。
表3抗卵巢癌活性纳米粒的粒径、表面电位和药物包封率。
实施例4:抗卵巢癌活性纳米粒的应用
(1)抗卵巢癌活性纳米粒的应用
(pei-sa)ha对skov3的ic50为478μg/ml,这表明(pei-sa)ha具有相对低的细胞毒性。
在skov3细胞中,游离ptx的ic50为1.35μg/ml,而(pei-sa)ha介导后ic50为0.11μg/ml(如表4所示)。游离姜黄素的ic50为2.49μg/ml,当(pei-sa)ha载体介导时,ic50为0.68μg/ml。(pei-sa)ha/姜黄素对耐药细胞的作用与敏感细胞相似。当ptx和姜黄素都装载在(pei-sa)ha载体((pei-sa)ha/pc)中时,ic50最小,表明这两种药物具有协同效应。在skov3-tr30细胞中,游离ptx的ic50为9.33μg/ml,而(pei-sa)ha中的ic50负载后为0.13μg/ml。当(pei-sa)ha载体介导时姜黄素ic50为0.70μg/ml,游离姜黄素的ic50为3.83μg/ml。在skov3-tr30细胞系中,(pei-sa)ha/pc显示出最佳细胞毒性。表4为ptx,(pei-sa)ha/ptx,姜黄素,(pei-sa)ha/姜黄素和(pei-sa)ha/pc对skov3/skov3-tr30细胞的ic50值。
游离ptx对耐药细胞的毒性显着降低。ptx由(pei-sa)ha介导后对敏感和耐药细胞都有效。在载体介导后,姜黄素对敏感细胞和耐药细胞具有相似的作用。这表明,一方面,(pei-sa)ha的功效可以有效地改善ptx对耐药细胞的作用。另一方面,姜黄素和ptx的组合对耐药细胞系具有更强的毒性作用。第三,姜黄素的参与逆转了ptx在耐药细胞系skov3-tr30中的作用。
表4ptx,(pei-sa)ha/ptx,姜黄素,(pei-sa)ha/姜黄素和(pei-sa)ha/pc对skov3/skov3-tr30细胞的ic50值。
实施例5:抗卵巢癌活性纳米粒的应用
(1)(pei-sa)ha/pc的细胞摄取
通过使用荧光标记的(pei-sa)ha/pc纳米粒测量在skov3细胞中的摄取。图1显示fitc标记的复合物和ritc标记的纳米粒分布与skov3细胞孵育0,1,2,4和8小时的荧光显微图像。从中可看出,随着孵育时间的增加,荧光强度逐渐增加。24小时后在所有细胞中检测到显着的荧光。值得注意的是,耐药细胞系skov3-tr30中荧光摄取与skov3中相似。另外,荧光标记的纳米粒的细胞内摄取也以定量方式进行。在孵育4小时后通过流式细胞术测量的(pei-sa)ha/pc的平均荧光强度结果与荧光照片的结果一致。图1为共聚焦荧光显微图像观察。其中a:skov3细胞孵育1小时,2小时,4小时和8小时的fitc标记的(pei-sa)ha/pc的荧光图像观察;b:skov3细胞孵育1小时,2小时,4小时和8小时的ritc标记的(pei-sa)ha/pc的荧光图像观察。缩写:fitc,异硫氰酸荧光素;ritc,罗丹明异硫氰酸酯;合并,结合核染色和荧光照片的组合。
实施例6
将生物相容性的硬脂酸(sa)修饰聚乙烯亚胺(pei)作为纳米粒的母核并用ha包裹,然后加载紫杉醇和姜黄素(图2),使其借助“抗体-受体”原理靶向卵巢癌组织。该纳米粒的使用可强烈协同增强紫杉醇的细胞毒性,并且可以改变紫杉醇信号传导途径以增强药物组合的协同效应,逆转紫杉醇耐药。
上述应用实例表明,本研究构建的载药纳米粒具有高效抗卵巢癌活性的作用。
- 还没有人留言评论。精彩留言会获得点赞!