人α防御素5改造肽在制备中和内毒素药物中的应用的制作方法
本发明涉及生物技术领域,具体涉及一种人α防御素5改造肽在制备中和内毒素药物中的应用。
背景技术:
内毒素,又被称为脂多糖(lipopolysaccharide,lps)是革兰氏阴性细菌细胞壁外膜的类脂多糖类物质,由脂质a、核心多糖和o-特异侧链3部分组成,是介导脓毒症发生发展的重要成分。细菌崩解产生的内毒素释放到血液中,通过识别免疫细胞表面的toll样受体4(tolllikereceptor4,tlr4)或进入到细胞内通过小鼠caspase11(人caspase4/5),激活下游信号通路,介导广泛的免疫炎症反应,进而导致多器官损伤和脓毒性休克。脓毒症患者血浆内毒素水平明显升高,而高水平的内毒素与更差的临床预后相关。因此,清除体内内毒素是脓毒症治疗的重要措施。然而,传统抗生素只能杀灭细菌而不具备中和内毒素的作用。
研究发现,某些天然或人工合成的阳离子抗菌肽(antimicrobialpeptides,amps)既可杀菌又具备中和内毒素的效果。例如,多黏菌素b是一种来源于多黏芽孢杆菌的环状阳离子抗菌肽,其已被证实可以中和内毒素。基于此研发的固定多黏菌素b纤维(pmx)灌流器是目前用于清除脓毒症血浆内毒素的装置,但仅限于日本、意大利等少数国家使用,我国尚未批准该装置应用于临床。此外,由于多黏菌素b的肾毒性和神经毒性较大,限制了其临床应用。所以,开发安全无毒的新型中和内毒素药物具有重要的临床意义。
人α防御素5(humandefensing5,hd5)表达于肠道黏膜潘氏细胞,具有三对二硫键(称之为氧化型hd5),表现为β折叠结构;hd5被还原后,二硫键消失,在水溶液中表现为无规则卷曲样结构,杀菌效果大大降低。既往研究证实,氧化型hd5可以中和某些外毒素,如霍乱弧菌的蛋白毒素(immunity.2014,41(5):709-21.),但却不能中和内毒素(scirep.2016,6:22875.)。本课题组前期研究对人α防御素5进行改造,在人α防御素5的c末端进行肉豆蔻酸修饰,显著增强其抗菌活性,尤其是针对耐甲氧西林金黄色葡萄球菌(专利文献cn106146643a),但是对于其是否在中和内毒素方面发挥作用尚未有报道。
技术实现要素:
本发明的目的在于提供一种人α防御素5改造肽的新用途,拓展其在临床实践中的应用。
为实现上述目的,本发明提供了人α防御素5改造肽在制备中和内毒素药物中的应用,所述人α防御素5改造肽由人α防御素5在c末端添加氨基酸残基并修饰连接肉豆蔻酸改造获得。
所述人α防御素5改造肽的肽链由34个氨基酸残基组成,其氨基酸序列为:
ala1-thr2-cys3-tyr4-cys5-arg6-thr7-gly8-arg9-cys10-ala11-thr12-arg13-glu14-ser15-leu16-ser17-gly18-val19-cys20-glu21-ile22-ser23-gly24-arg25-leu26-tyr27-arg28-leu29-cys30-cys31-arg32-gly33-lys34,其中cys3和cys31,cys5和cys20,cys10和cys30分别形成二硫键,第34位的lys的ε氨基上连接肉豆蔻酰基。
优选的,所述人α防御素5改造肽的c末端羧基酰胺化。
本发明研究表明,所述的人α防御素5改造肽可以中和内毒素进而抑制内毒素介导的炎症因子的释放,从而减轻因内毒素造成的组织脏器的损伤。分析其作用机制一方面在于其c端的肉豆蔻酸具有疏水性,能够与内毒素的脂质a结合;另一方面在于其所带的正电荷能与内毒素带负电荷的磷酸基团结合。同时,所述人α防御素5改造肽所形成的纳米胶束与内毒素胶束在体液环境中可以自组装成为纳米杂化胶束结构,增加了二者的结合,从而抑制了其生物活性。
进一步地,本发明还提供了所述人α防御素5改造肽在制备治疗脓毒症的药物中的应用。本发明提供的人α防御素5改造肽可用于清除脓毒症患者体内内毒素,达到治疗脓毒症的目的,因此,可将其应用于治疗脓毒症药物的开发中。
本发明具备的有益效果:
本发明研究发现人α防御素5改造肽hd5-myr在中和内毒素方面的新用途,通过中和内毒素,抑制其介导的炎症因子释放,减轻组织脏器损伤,对于治疗脓毒症具有重要价值。
附图说明
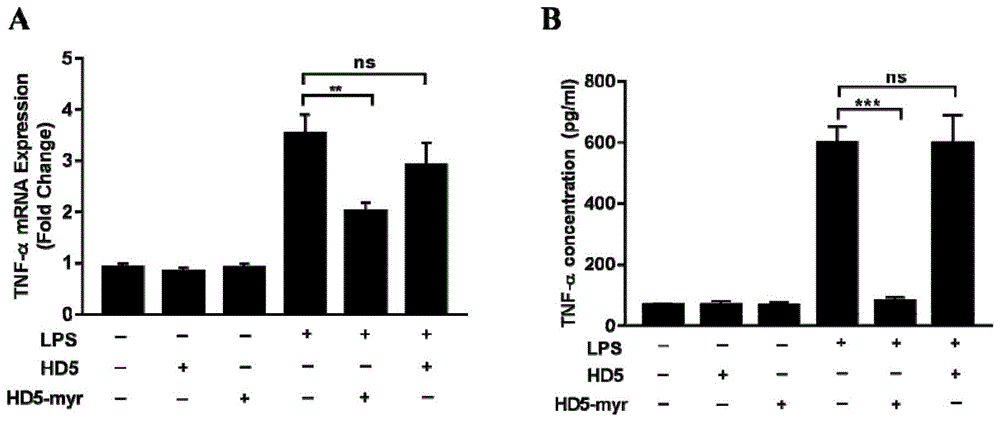
图1是hd5、hd5-myr对内毒素lps介导炎症反应的影响。a图表示raw264.7细胞tnf-αmrna表达;**p<0.01,ns表示差异无统计学意义。b图表示raw264.7细胞上清tnf-α蛋白表达;***p<0.001,ns表示差异无统计学意义。hd5-myr可以显著抑制内毒素lps引起的tnf-αmrna和蛋白的产生。
图2是hd5-myr治疗后,内毒素lps致脓毒症小鼠急性肺损伤情况(a)以及病理评分(b)。***p<0.001,ns表示差异无统计学意义。wt组表示小鼠未注射lps,仅注射磷酸盐缓冲液作为对照;vehicle组表示小鼠注射lps后给予溶剂水治疗;hd5组表示小鼠注射lps后给予hd5治疗;hd5-myr组表示小鼠注射lps后给予hd5-myr治疗。hd5-myr可以显著改善内毒素lps导致的急性肺损伤。
图3lps、lps和hd5混合液、lps和hd5-myr混合液的透射电子显微镜图。图中标尺表示100nm。
具体实施方式
为了更好地理解本发明,下面结合实施例和附图对本发明做进一步的详细说明,但下述实施例不是对本发明保护范围的限制,任何在本发明基础上做出的改变和变化,都在本发明的保护范围之内。
下述实施例中采用的hd5为天然氧化型hd5,其氨基酸序列为:
ala1-thr2-cys3-tyr4-cys5-arg6-thr7-gly8-arg9-cys10-ala11-thr12-arg13-glu14-ser15-leu16-ser17-gly18-val19-cys20-glu21-ile22-ser23-gly24-arg25-leu26-tyr27-arg28-leu29-cys30-cys31-arg32;
其中cys3和cys31,cys5和cys20,cys10和cys30分别形成二硫键,一个3个二硫键。
改造肽hd5-myr为本发明课题组前期研究改造获得,报道于专利文献cn106146643a。hd5-myr是在天然氧化型hd5的c端添加氨基酸残基并修饰连接一个肉豆蔻酸获得。
所述的hd5改造肽的氨基酸序列为:
ala1-thr2-cys3-tyr4-cys5-arg6-thr7-gly8-arg9-cys10-ala11-thr12-arg13-glu14-ser15-leu16-ser17-gly18-val19-cys20-glu21-ile22-ser23-gly24-arg25-leu26-tyr27-arg28-leu29-cys30-cys31-arg32-gly33-lys34;
其中cys3和cys31,cys5和cys20,cys10和cys30分别形成二硫键,一共3个二硫键。
上述序列第34位的lys的c末端酰胺化,且ε氨基上连接一个肉豆蔻酸(myristicacid,myr),故命名为hd5-myr。
实施例1
hd5-myr对内毒素lps介导炎症反应的影响
(1)将巨噬细胞系raw264.7种于24孔板,每孔5×105个细胞。
(2)将体积10μl、浓度为50ng/ml的lps与体积10μl、浓度为100μg/ml的hd5或hd5-myr混合,组成20μl体系,37℃孵育30分钟。
(3)将上述体系加入到24孔板内,使24孔板内的终体积为400μl。加样完毕后,将24孔板置于37℃、含5%co2的恒温细胞培养箱中,培养3h。
(4)3h后,采取如下操作:①吸取细胞上清于1.5mlep管,通过elisa方法检测细胞上清肿瘤坏死因子α(tumornecrosisfactorα,tnf-α)的含量;②24孔板内的细胞用磷酸盐缓冲液清洗3次,每孔加1mltrizol,吹打均匀后吸出置于1.5mlep管中,提取细胞中的核糖核酸(ribonucleicacid,rna),检测不同组别mrna水平tnf-α的表达情况。
结果如图1所示,hd5-myr可以显著减少tnf-αmrna和蛋白的表达,而hd5则不能。
通过细胞实验发现,人α防御素5改造肽可以抑制内毒素引起的炎症因子的释放。
实施例2
hd5-myr对内毒素lps致脓毒症小鼠急性肺损伤的改善作用
(1)取c57bl/6小鼠,体重21-23g,周龄6-8周。
(2)用pbs配置lps溶液,用超纯水配置hd5溶液、hd5-myr溶液。
(3)设计实验分组:wt组、vehicle组、hd5组、hd5-myr组。vehicle组、hd5组、hd5-myr组小鼠按10mg/kg的剂量腹腔注射lps,wt组小鼠腹腔注射相同体积的溶剂pbs。
(4)在lps致脓毒症模型建立后,hd5组、hd5-myr组小鼠分别注射60μg的hd5组、hd5-myr组、vehicle组小鼠注射相同体积的溶剂h2o。
(5)将小鼠饲养于适宜环境;24h后,取小鼠肺脏进行组织切片、苏木精-伊红染色,观察小鼠肺脏损伤情况。
结果如图2所示,注射lps后,小鼠肺脏出现明显损伤,可见呼吸膜增厚、肺泡间隔充血、肺泡内炎性细胞浸润。vehicle组和hd5组脓毒症小鼠肺脏没有改善;而hd5-myr治疗后,小鼠肺损伤明显好转,接近于正常肺脏。
通过动物实验发现,人α防御素5改造肽可以显著改善内毒素导致的急性肺损伤。
实施例3
lps和hd5-myr混合液的透射电子显微镜图
(1)将lps、hd5及hd5-myr溶解于超纯水中。
(2)配置lps、lps+hd5混合液、lps+hd5-myr混合液,上述溶液多肽(hd5和hd5-myr)终浓度为50μg/ml,lps终浓度为1μg/ml。
(3)用镀膜铜网蘸取少量样品,待充分浸润后,用滤纸吸掉多余液体,干燥30s后,滴加2%的醋酸双氧铀溶液,待充分染色后,用滤纸吸掉多余液体,于室温下干燥(尽量避免加热干燥以防铜网破裂)。
(4)干燥后用透射电子显微镜观察拍照。
结果如图3所示,lps和hd5-myr混合后,纳米杂化胶束形成,粒径明显变大;而lps和hd5混合后,粒径无明显变化。
透射电子显微镜发现,人α防御素5改造肽可以与内毒素形成纳米杂化胶束。
序列表
<110>浙江大学
<120>人α防御素5改造肽在制备中和内毒素药物中的应用
<160>2
<170>siposequencelisting1.0
<210>1
<211>34
<212>prt
<213>人工序列(artificialsequence)
<400>1
alathrcystyrcysargthrglyargcysalathrarggluserleu
151015
serglyvalcysgluileserglyargleutyrargleucyscysarg
202530
glylys
<210>2
<211>32
<212>prt
<213>人α防御素5(human)
<400>2
alathrcystyrcysargthrglyargcysalathrarggluserleu
151015
serglyvalcysgluileserglyargleutyrargleucyscysarg
202530
- 还没有人留言评论。精彩留言会获得点赞!