心脏瓣膜假体递送系统的制作方法
本公开涉及用于经皮递送和植入心脏瓣膜假体的装置和方法。瓣膜假体可以在护套内以压缩状态被递送到有缺陷的自体瓣膜并在原位释放。
背景技术:
人工心脏瓣膜用于置换受损或病变的心脏瓣膜。在脊锥动物中,心脏是具有四个泵室的肌肉器官:左心房、右心房、左心室和右心室,左心房、右心房、左心室和右心室中的每一个都设置有自己的单向瓣膜。自体心脏瓣膜被确定为主动脉瓣、僧帽瓣(或二尖瓣)、三尖瓣和肺动脉瓣。尽管主动脉瓣或二尖瓣的修复或置换更常见(因为它们位于心脏的压力最大的左侧),但是人工心脏瓣膜可用于置换任何这些自然形成的瓣膜。
常规的心脏瓣膜置换手术涉及通过胸部中的纵向切口访问患者胸腔内的心脏。例如,正中胸骨切开术需要切穿胸骨并迫使肋骨篮的两个相对半部分离,从而允许访问胸腔和心脏。然后将患者置于心肺转流术中,这涉及停止心脏以允许进入内部腔室。这种心脏直视手术特别具有侵入性,并且涉及漫长且困难的恢复期。
现有技术的前述实例及其相关的局限性旨在是说明性的而不是排他性的。在阅读了说明书和研究了附图之后,现有技术的其他局限性对于本领域技术人员将变得显而易见。
技术实现要素:
本公开涉及心脏瓣膜假体、以及能够有助于将心脏瓣膜假体递送到患者有缺陷的自体瓣膜结构(例如主动脉瓣)的递送装置和致动手柄。在一些实施例中,可以使用经导管(transcatheter)方法进行递送。
递送装置和致动手柄可使临床医生能够使用经血管方法(例如经股动脉方法)更容易地操纵和推进递送装置通过通向心脏的血管以及通过这些血管的曲折部。实际上,本文公开的一些实施例使得心脏瓣膜假体的构件能够作为轴向位移单元(构件之间部分重叠或完全重叠或不重叠)串联地前进,同时各构件仍然彼此可移动地连接,可移动地附接,柔性连接,可位移地连接,耦联或联接,从而最小化递送装置的通过轮廓或横截面。可选地,心脏瓣膜假体的构件可以连续位移的距离可以是可变的,使得各种构件相邻或可能相距数英寸或英尺。此外,心脏瓣膜假体的各构件的互连可以允许不同的移动程度,并且可以设置成提供有限移动范围的接合位置或保持位置。在一些实施例中,接合位置还可以提供心脏瓣膜假体的构件的预设相对定位,以便于心脏瓣膜假体的正确放置和释放。另外,一些实施例可以为临床医生提供高程度的控制,并且在将心脏瓣膜假体植入目标位置时增强心脏瓣膜假体的可操纵性。
根据一些实施例,提供了一种用于经导管主动脉瓣植入(tavi)和/或经导管主动脉瓣置换(tavr)的手术。例如,在tavi手术中,临床医生可以相对于主动脉瓣环锚固心脏瓣膜假体的锚固构件,以引导人工瓣叶结构的放置。瓣膜假体可包括人工瓣叶、锚固构件、瓣架(valveframe)构件和栓系构件,该栓系构件允许锚固构件和框架构件串联地放置在递送装置中,以减小递送装置的整体横断面。栓系构件可以联接到锚固构件和框架构件以允许一定范围的移动,并且在一些实施例中限制其他移动。栓系构件可以相对于锚固构件在释放位置和保持位置之间滑动。在保持位置,栓系构件可以允许瓣架构件的相对移动和瓣架构件相对于锚固构件最佳定位的预设或预定位置,这可以便于瓣膜假体的放置和释放。
例如,在一些实施例中,可以使用将栓系构件环绕锚固构件的“u形”部件的新颖方法来实现互连。栓系构件可以沿着锚固构件滑动,直到到达锚固构件上的行程的末端。临床医生可以对栓系构件施加张力,直到栓系构件安置在接合区域中。该动作可以使栓系构件松脱,并将其接合到锚固构件的接合区域。此后,仅基于临床医生将锚固构件放置到主动脉窦区域(临床医生可以通过荧光检查法看到并且可以“感觉”该放置)中,栓系构件建立瓣架构件相对于锚固构件的固定范围的纵向行程,并且随后建立瓣架构件在解剖结构中的适当位置。
因此,本文公开的一些实施例有利地提供了具有减小的通过轮廓或横截面的递送装置,从而能够以比常规方法更安全、侵入性更小的方式递送心脏瓣膜假体。因此,可以避免心脏直视手术,因为心脏瓣膜假体可以使用导管经由血管(例如股动脉)中的进入点前进到心脏。这为患者带来了巨大的好处,举例来说,包括对患者的创伤更小,更容易恢复,并且可能更低的手术风险。
此外,尽管锚固构件和瓣架构件的串联布置克服了创建低轮廓递送装置的挑战,但是互连的有利布置克服了另一个关键挑战:如何最佳地将瓣膜假体定位在自体瓣膜结构内并且可靠地将其锚固在适当位置。实际上,本文公开的一些实施例解决了该挑战,并且教导了在递送装置中使用栓系构件将锚固构件可操作地联接到瓣架构件的结构和方法。
递送装置可包括可以容纳锚固构件的至少一部分的近侧护套和可以容纳瓣架构件的至少一部分的远侧载体组件。当瓣膜假体装载到递送装置上时,栓系构件可以在锚固构件和瓣架构件之间延伸。瓣膜假体可以以逐个构件的方式从递送装置释放,这允许临床医生首先操纵和定位锚固构件,然后是瓣架构件。
在一些实施例中,锚固构件可以联接到递送装置的接合部件或抓紧件,接合部件或抓紧件允许临床医生推动或拉动锚固构件。当锚固构件相对于自体瓣环正确就位时,抓紧件可以从与锚固构件的接合中释放。
另外,在一些实施例中,递送装置的远侧载体组件可包括两个构件或称为两件式头锥组件。根据一些实施例,认识到如果使用单个管状部件或头锥来保护大部分瓣架构件,则由于在递送到目标瓣膜结构期间将瓣架构件保持在其压缩构造所需的扩展力和相应的压缩力,可能出现各种问题。因为递送装置可以非常长(例如,在一些实施例中,高达大约4到6英尺以上,尽管长度可以小于4英尺、3英尺或2英尺),这些力可以产生递送装置的更硬的远侧部分。此外,由于瓣膜植入的径向力引起的高摩擦力,这些力可能需要高程度的纵向力来释放瓣架构件。
因此,这种构造的径向力和摩擦力可能导致匹配手柄致动的问题,并且使得递送装置的远端的精确定位非常困难。例如,摩擦倾向于是可变摩擦,这使得临床医生难以将瓣膜假体的构件相对于彼此定位,这可能导致不可预测和/或不精确的构件定位或部署。因此,本文的一些实施例包括以下实现:通过将远侧载体或头锥组件分成两个构件(例如近侧外壳和远侧外壳),构件可以覆盖瓣架构件的较小表面区域,从而减小对单个构件施加的径向力以及为了致动或释放瓣架构件而需要克服的所产生的摩擦。因此,与单个管状部件相关的问题更易于管理。
另外,在一些实施例中,两件式远侧载体组件还可使临床医生能够以有利的顺序释放瓣架构件。例如,在本文公开的瓣膜假体、部署系统和手柄致动器的测试和开发期间,一些实施例通过在瓣架构件的近端部被释放之前允许瓣架构件的远端部首先打开来证明有利的特性。在一些实施例中,瓣架构件可在其远端部处具有一个或多个锚,其可补充向外的扩展力(由于瓣架构件的自扩展)及其所产生的摩擦接合。通过首先打开远端部(通过远侧头锥或外壳的致动),远端部可以如开花那样打开并与自体瓣膜结构接合,以确保瓣架构件相对于自体瓣膜结构的纵向位置。此后,瓣架构件的自扩展径向向外的力可以使瓣架构件的近端部变为与近侧头锥或外壳脱离接合并释放。
一些实施例还可以提供自对准特征,以允许递送组件的构件从释放状态(其中瓣膜假体的构件从与递送组件的接合释放)移动到嵌套或收起状态(其中递送组件的多个部分的外表面对准或在接缝处处于邻接位置)。这种对准、邻接或定位可以提供更平滑的外部轮廓,这可以降低在释放之后使递送组件钩住人工瓣膜或与人工瓣膜缠绕的可能性,或者降低当从患者的脉管系统取回递送组件时与其他脉管系统缠绕的可能性。
例如,在一些实施例中,远侧载体或头锥组件可包括内部柱塞或活塞机构。当瓣架构件装载到递送装置中时,柱塞机构可以被压缩。当瓣架构件被释放时,柱塞机构的弹簧可将柱塞头推动到相对于远侧载体组件的预定位置。根据一些实施例,在预定位置,柱塞头可以部分地从远侧外壳露出,并且被构造为与近侧外壳接合,以使近侧外壳和远侧外壳相对于彼此以邻接关系对准。因此,柱塞头可以与近侧外壳和远侧外壳接合,以减少在取回递送装置期间人工瓣膜或其他脉管系统卡住或钩住递送装置的可能性。另外,这些特征还可以帮助将递送装置近侧缩回到引导器护套中。此外,柱塞头还可以提供近侧表面,该近侧表面可以与瓣架构件的远端部接触,而不会与瓣架构件的复杂网状物接合或钩住,从而确保瓣架构件可以像开花那样打开,而不会卡在递送装置上。因此,一些实施例可以包括这些有利特征中的一个或多个,这些有利特征解决了使瓣膜假体和/或递送装置彼此卡住或钩住或围绕解剖结构的问题。
此外,由于递送装置的横截面轮廓减小,因此可以在降低对周围脉管系统创伤的风险的状态下实现瓣膜假体通过血管(例如经股动脉逆行方法中的股动脉)的逆行递送。例如,瓣膜假体通过股动脉的逆行递送与主动脉动脉(aortofemoralartery)损伤和/或破裂相关,并且当递送涉及穿过主动脉弓时具有潜在的中风风险。然而,使用本文公开的一些实施例实现的各种特征和优点提供了如下瓣膜假体和递送装置:其最小化沿着装置的递送路径的损伤,同时还最小化植入手术的侵入性质。
通过阅读以下描述、附图、实例和权利要求,本装置和方法等的其他实施例将变得清楚。根据前面和下面的描述可以认识到,本文描述的各个和每个特征以及这些特征中的两个或更多个的各个和每个组合包括在本公开的范围内,只要包括在这种组合中的特征不相互矛盾即可。另外,本公开的任意实施例可以不具体包括任意特征或这些特征的组合。特别是当结合所附实例和附图考虑时,在以下说明书和权利要求书中阐述了本公开的其他方面和优点。
本主题技术的其他特征和优点将在下面的描述中阐述,并且部分地将从描述中变得清楚,或者可以通过本主题技术的实践而学习到。
本主题技术的优点将通过在书面描述及其实施例以及附图中具体指出的结构来实现和获得。
应当理解,前面的整体描述和下面的详细描述都是示例性的和说明性的,并且旨在提供对本主题技术的进一步说明。
附图说明
下面参考附图描述本公开的说明性实施例的各种特征。所示实施例旨在说明本公开而非限制本公开。附图包括以下图:
图1示出了根据一些实施例的在经股动脉逆行方法中使用瓣膜递送装置进行的瓣膜假体的递送。
图2示出了根据一些实施例的瓣膜假体。
图3是根据一些实施例的装载到瓣膜递送装置上的图2的瓣膜假体的侧剖视图。
图4是根据一些实施例的图3的瓣膜递送装置的透视图,示出了用于接合瓣膜锚的抓紧机构。
图5a-5b是示出根据一些实施例的具有头锥保护器的图3的瓣膜递送装置的远侧载体组件的操作的侧剖视图。
图6示出了根据一些实施例的用于图2的瓣膜假体的耦联机构的实施例,其中瓣膜假体被装载到瓣膜递送装置上。
图7a-7d是示出了根据一些实施例的递送装置的远侧载体组件和近侧外壳的方面和操作的侧视图和端剖视图。
图7e是沿着图7d的剖面线7e-7e截取的剖视图,示出了根据一些实施例的图6的递送装置的远侧载体组件的近侧外壳的结构。
图8a是根据一些实施例的鼻锥保护器的透视图。
图8b-8f是示出了根据一些实施例的具有图8a的鼻锥保护器的递送装置的远侧载体组件的操作的侧剖视图。
图9a和9b是根据一些实施例的具有抓紧件机构和抓紧件对准毂的瓣膜递送装置的视图。
图9c是根据一些实施例的图9b的抓紧件对准毂组件的视图。
图10a和10b是示出根据一些实施例的图6的递送装置的近侧外壳的结构的透视图。
具体实施方式
在下述详细描述中,列举了许多具体的细节以提供对本主题技术的全面理解。应当理解,可以在没有这些具体细节中的一部分的情况下实施本主题技术。在其他情形中,没有详细示出公知的结构和技术,以避免影响对本主题技术的理解。
此外,尽管本公开列举了各个实施例的具体细节,应当认识到,该描述仅仅是示例性的,而不应以任何方式解释为限制。另外,可以设想的是,尽管可能在主动脉瓣假体的背景下披露或示出了本公开的特定实施例,但是这类实施例也可以用于其他心脏瓣膜假体的应用中。此外,本领域技术人员可以想到的对这类实施例及其变型的各种应用,也包含在本文描述的基本构思中。
现在将在下文中更全面地描述各个实施例。然而,这些实施例可以体现为多种不同的形式,并且不应解释为仅局限于在此列举的实施例;相反,提供这些实施例是为了使本公开完整和全面并且将本公开的范围充分地传达给本领域的技术人员。因此,在本文的一个实施例中示出或以其他方式披露的一个或多个特征可以互换使用或并入另一个可能未明确地示出或披露这个(这些)特征的实施例中。此外,除非明确指出,否则可以使用本领域的技术将为本文的一个实施例所示出或以其他方式披露的一个或多个特征从该实施例中排除。
与所有心脏瓣膜一样,健康的主动脉瓣将打开以允许血液流过以及闭合以防止血液回流。然而,瓣膜的疾病或功能不良会导致回流或血流减少(狭窄)。在这些情况下,必须使用置换的主动脉瓣假体来执行健康的主动脉瓣的功能。
微创手术技术正在发展,其中可以使用通过小切口引入的导管将瓣膜假体引入患者体内,该小切口提供进入例如股动脉或者直接进入心脏的通路。对于向不太适合开放性手术的患者提供治疗选择来说,这些植入技术已经显示出有前景的结果。然而,这种基于导管的人工瓣膜递送仍然存在挑战。
例如,根据在本文中披露的至少一个实施例的一方面认识到:常规的管道递送装置通过血管前进时对血管壁施加应力并且具有损坏血管壁的风险。此外,根据在本文中披露的至少一个实施例的一方面认识到:经导管的(transcatheter)人工瓣膜可能不能治疗主动脉回流(主动脉瓣关闭不全)的患者。另外,根据在本文中披露的至少一个实施例的一方面认识到:常规的人工瓣膜可能难以定位,可能需要快速的人工心室起搏,并且可能展开(expansion)有限。因此,常规的人工瓣膜的植入和使用可能导致并发问题,诸如血管损伤、中度至重度瓣膜周漏(paravalvularleakage)、瓣膜血栓/移位、冠状动脉阻塞以及由于过大的径向力引起的过大应力。
本公开描述了能够被递送到患者的有缺陷的心脏瓣膜处的心脏瓣膜假体的各个方面。瓣膜假体可包括至少一个瓣膜锚或扣紧件(clasper),所述瓣膜锚或扣紧件可移动地连接到、可移动地附接到、柔性地连接到、可位移地连接到、耦联到或联接到可径向扩张的瓣膜支撑件或瓣架(valveframe)。瓣架可包括人工瓣叶(假体瓣膜小叶)或尖瓣(cusps)并提供自体心脏瓣膜的功能。可由本公开中讨论的假体所实现的瓣膜假体的某些特征,还在例如美国专利no.8,366,768中进行了进一步描述,该美国专利的全部内容以引用的方式并入本文。
因此,本公开提供了多种可并入或排除于本文中明确讨论或示出的任何实施例的特征。可由本领域技术人员实施对这些特征的变型和组合,以实现本文所讨论的优点和益处。此外,尽管在本文中指出或建议了一些变型或组合,但可以预见到,本领域技术人员在开发合适的实施例或实施这些教导时,可以实施或排除在本文中披露的某些方面或特征。有利地,本文描述的各种实施例允许治疗患有主动脉回流的患者,允许瓣膜假体的精确的轴向、角向和径向定位,将瓣膜移位及瓣膜周漏最小化,同时避免对瓣环的损坏,将对起搏器的需要最小化,并且降低了阻塞冠状动脉的可能性。
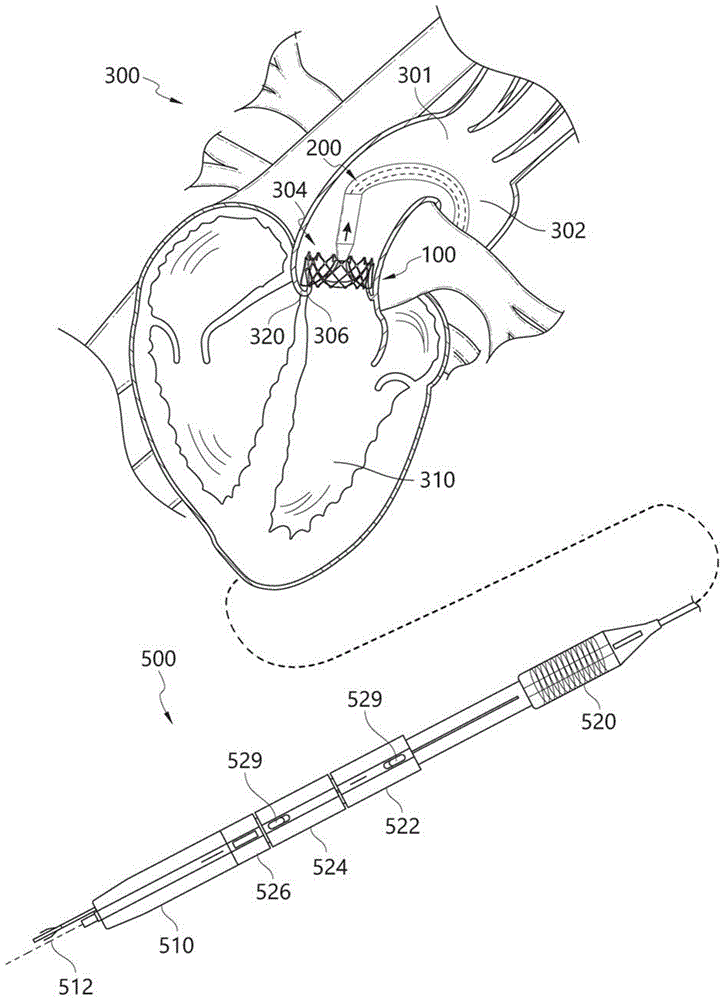
在图1至图5b中示出了心脏瓣膜假体的这些特征和益处中的一部分。图1示出了递送装置200在人类心脏300中的使用。心脏300可包括具有主动脉弓302和主动脉瓣304的主动脉301。主动脉瓣304可包括多个自体瓣叶306并且可将主动脉301与左心室310分离。根据一些实施例,递送装置200可以逆行通过主动脉301,直到到达主动脉瓣304的自体瓣叶306并通过自体瓣叶306而被定位。
参考图1和图2,在将瓣膜假体100递送到自体瓣膜部位期间,瓣膜锚104和支撑框架102可以串列(intandem)地布置,作为沿着递送装置200的纵轴线轴向移位的单元(锚与框架之间可部分或完全重叠,也可以不重叠)。与同心布置相比,这种构造可允许瓣膜假体100的构件的在径向上更紧凑的构造,从而形成更小的横截面,并有助于基于导管的递送。这可以提高递送装置200的灵活性(flexibility),使得递送装置200能够在导丝上行进通过循环系统(尤其是主动脉弓302)的曲折的几何形状。实际上,即使使用由导丝引导的递送装置,主动脉弓302也由于其突然且高度的弯曲而成为困难的障碍。通常,这是一些手术或递送装置的限制约束。然而,根据本文披露的一些实施例的各种益处和优点,如图1所示,递送装置200可以穿过主动脉弓302,前进到主动脉瓣304的区域中的目标位置处。
如图1所示,一旦瓣膜锚104处于期望的位置,支撑框架102就可以从远侧载体组件释放,并且扩张成与自体瓣叶306、以及瓣膜锚104的内部方面(internalaspects)并置(apposition),从而将自体瓣叶306夹在支撑框架102与瓣膜锚104之间。有利地,通过将自体瓣叶306夹在支撑框架与瓣膜锚之间,瓣膜假体100可以减少对径向力保持的依赖性。此外,通过将自体瓣叶306夹在支撑框架与瓣膜锚之间,减少了自体瓣叶306阻塞冠状动脉口的可能性,这可有益于冠状动脉口距离较短的患者,并可有益于已装有瓣膜假体,但可能在现有瓣膜假体内部需要新的瓣膜假体(“瓣膜内瓣膜”的应用)的患者。因此,支撑框架和瓣膜锚可以扩张成与主动脉瓣膜304接触,对自体瓣叶306和主动脉瓣环320施加慢性的向外的力。在此之后,假体100的人工瓣叶可以开始以期望的方式起作用,并且提供与自体瓣膜相同的操作。
根据一些实施例,本公开还提供了一种手柄致动器,该手柄致动器可用于控制本文所披露的递送装置的操作,并允许临床医生可靠且精确地控制瓣膜假体的递送。图1示出了根据一些实施例的手柄致动器的特征和操作,用于使用手柄致动器500来递送瓣膜假体。
图1示出了手柄致动器500,其可以控制用于瓣膜假体(例如,本文所讨论的心脏瓣膜假体100)的递送的递送装置(例如,本文所讨论的递送装置200)的一个或多个功能。手柄致动器500可包括多个致动器或可移动元件,诸如旋钮或按钮等。可移动元件可允许临床医生控制递送装置200的一种或多种操作。手柄致动器500可包括具有纵轴线512的控制手柄510。手柄致动器500也可被称为控制单元。在一些实施例中,手柄致动器500可联接到第二芯部件222(在例如图3和图5a、5b中示出)。控制手柄510可以支撑致动器并且在手术期间由临床医生握持。
在一些实施例中,如图1所示,手柄致动器500可包括第一可移动元件520、第二可移动元件522、第三可移动元件524和第四可移动元件526。第一可移动元件520可以用于操纵递送装置200,第二可移动元件522可用于释放瓣膜锚,第三可移动元件524可用于释放头锥(nosecone)或瓣架,第四可移动元件526可用作头锥肘杆锁定件(togglelock)。第一可移动元件520、第二可移动元件522、第三可移动元件524和第四可移动元件526也可以被称为第一控制元件520、第二控制元件522、第三控制元件524和第四控制元件526。
可选地,在一些实施例中,所述可移动元件中的一个或多个(例如第二可移动元件522和/或第三可移动元件524)可包括用于防止可移动元件的无意旋转的按钮或滑块式安全开关529。安全开关529可以构造为可被致动以将锁定件释放的弹性按钮或滑块机构,该锁定件向各个可移动元件的旋转或平移运动提供阻力。在一些实施例中,可移动元件可具有凸起特征,所述凸起特征为旋转提供视觉指示并且有助于由临床医生实施的凭触觉的接合和致动。在2018年12月18日提交的美国专利申请no.62/781,537的图13a至图13h中讨论和示出了手柄致动器500的其他特征以及操作手柄致动器500的方法,该美国专利申请的全文以引用的方式并入本文。
现在参考图2,其中以各种构造示出了瓣膜假体100及其构件。可以使用适当的递送装置(包括在本文中描述的递送装置)将瓣膜假体100递送到患者处。瓣膜假体100可包括:支撑框架102;以及锚固构件或瓣膜锚104,支撑框架102可移动地连接到、可移动地附接到、柔性地连接到、可位移地连接到、耦联到或联接到该锚固构件或瓣膜锚104。
瓣膜假体100可构造为使得瓣膜假体100的构件串列起来前进(advancedinseries),与此同时各构件彼此仍然可移动地连接、可移动地附接、柔性地连接、可位移地连接、耦联或联接,从而将递送系统的通过轮廓或横截面最小化。瓣膜假体100的构件之间的互连可允许不同程度的运动,并且可被设定在提供有限范围的运动的接合或保持位置。在一些实施例中,接合位置还可以提供对瓣膜假体100的构件的预设的相对定位,以有助于对瓣膜假体100进行正确放置和释放。另外,一些实施例可以为临床医生提供高程度的控制并且在将瓣膜假体100植入目标位置时增强瓣膜假体100的可操纵性。
在一些实施例中,在支撑框架102处于递送和展开之前的紧凑构造时,瓣膜锚104可以联接到支撑框架102。在一些实施例中,瓣膜锚104未固定于支撑框架102。此外,瓣膜锚104可以与支撑框架102分离,或者可以与支撑框架102分开形成并且后续联接到支撑框架102。因此,尽管瓣膜锚104的至少一部分(例如,锚固腿)可以与支撑框架102接触或以其他方式可逆地附接或连接到支撑框架102,但是瓣膜锚104的任何部分都未固定(例如,焊接或以其他方式不可逆地结合)于支撑框架102。换言之,瓣膜锚104可以接触或者以其他方式可逆地附接或连接到支撑框架102,而并非不可逆地固定到支撑框架102。
此外,一旦到达目标位置,瓣膜锚104可以以防止整个瓣膜锚104在初始扩张时从支撑框架102径向位移的方式,可移动地联接到支撑框架102。例如,在瓣膜锚104初始“着陆”到目标位置处的自体瓣膜结构的期间,瓣膜锚104的一部分可从支撑框架径向移位。在一些实施例中,支撑框架102可以在自体心脏瓣膜结构内展开或扩张,并且瓣膜锚104可变为置于支撑框架与自体瓣膜组织之间,变为至少部分地,并且可能是完全地不可动(immobilized)。瓣膜锚104可用于将扩张的支撑框架102在自体瓣膜结构内保持在位。
可选地,支撑框架102可以被称为瓣架或瓣膜支撑框架。图2示出了在当假体100被释放并且在自体瓣膜结构内扩张时所实现的构造中,与瓣膜锚104对准并且在瓣膜锚104内扩张的支撑框架102。自体瓣膜结构包括瓣环或瓣叶。该扩张构造用于通过接合自体瓣膜结构将瓣膜假体100固定在自体瓣环内。在一些实施例中,瓣膜假体100的扩张构造可减少对通过支撑框架102和瓣膜锚104施加的径向力来固定瓣膜假体100的依赖性,所述径向力是通过将自体瓣叶夹在或压缩在瓣膜假体100的支撑框架102与瓣膜锚104之间来实现的。此外,如本文中进一步所讨论,在瓣膜假体100的植入期间,支撑框架102和瓣膜锚104可以在扩张和/或压缩状态下相对于彼此移动,以有助于相对于自体瓣环及其周围结构对假体100进行正确的定位。实际上,通过本文公开的假体100和递送装置获得的各种优点允许临床医生实现更高的放置假体100的精确度,以及使得这种精确度的提高更加容易实现。
参考图2,支撑框架102可包括外侧表面(或外表面),并且限定了围绕纵轴线120的中央穿孔。纵轴线120与假体100的流入-流出轴线对应。在一些实施例中,瓣膜假体100还包括与支撑框架102联接的多个人工瓣叶或尖瓣106。支撑框架102可以为瓣叶106提供结构支撑。瓣叶106可具有限定了能够可逆地密封的开口的表面,该开口用于液体单向流过假体100。假体100可包括用于三叶(tri-leaflet)构造的三个瓣叶106。可以理解,单叶、双叶和/或多叶构造也是可行的。例如,瓣叶可以与支撑框架102联接,以横跨流体并且控制流体流过假体100的管腔。人工瓣叶106可包含一种或多种合成材料、工程化生物组织、生物瓣叶组织、心包组织、交联心包组织、主动脉根组织、经化学或生物加工/处理的组织,或它们的组合。在一些实施例中,心包组织选自但不限于由牛、马、猪、绵羊及人的组织或它们组合所组成的群组。
此外,在一些实施例中,瓣膜假体100可包括密封构件或膜108,所述密封构件或膜108可附接到支撑框架102的内侧面、外侧面和/或包围支撑框架102(例如通过层叠到支撑框架102的内表面和外表面上)。从而,瓣叶106可以联接到支撑框架102和/或膜108。在一些实施例中,膜108可以限制瓣叶106周围的区域中的血液流动,从而血液流动仅在瓣叶106之间、穿过假体100的管腔发生,如同在健康的自体心脏瓣膜中那样。
如图2所示,支撑框架102和/或瓣膜锚104可包括编织框架、线框架或激光切割框架(例如,激光切割的管状网)。在一些实施例中,支撑框架102和/或瓣膜锚104可包含形状记忆金属,该形状记忆金属可在指定的温度或温度范围下改变形状,或通过诱导应力改变形状。作为替代,自膨胀框架可包括具有弹簧偏压件的框架。制造支撑框架102和/或瓣膜锚104的材料既可允许支撑框架102和/或瓣膜锚104在展开时自动扩张到其功能尺寸和形状,而且也允许支撑框架102和/或瓣膜锚104被径向压缩到较小的轮廓,以便通过患者的脉管系统而被递送。用于本文所述的自膨胀构件(例如,支撑框架、瓣膜锚、锁定部件)的合适材料的实例包括但不限于医用级镍钛合金、钽、铂合金、铌合金、钴合金、藻酸盐、或它们的组合。基本上由镍和钛按比例制成,通常被称为镍钛诺的具有超弹性的形状记忆合金是优选的材料。在一些实施例中,本文所描述的自膨胀构件可以包含这样的材料,所述材料包括但不限于在人体内呈惰性的热塑性材料、形状记忆塑料及聚合物。在替代性实施例中,支撑框架102和/或瓣膜锚104不是自膨胀型的,而是例如如本领域公知的那样使用球囊导管来扩张。用于本文所描述的构件的适当的材料的实例包括但不限于不锈钢和钛。可选地,支撑框架102和/或瓣膜锚104可包括不透射线材料,以允许在荧光检查或其他成像技术下的可视化。
可选地,支撑框架102可包括一个或多个钩109,当支撑框架102在自体瓣环内扩张时,所述钩109可与自体瓣环、主动脉根或者自体瓣膜的任何其他部分接合。钩109可与自体瓣环接合,以便在手术期间固定假体100并减少假体100的任何朝下游或顺行的移位。
支撑框架102可包括第一端部110和第二端部112。当假体100在自体瓣环内释放时,第一端部110可位于第二端部112的上游。如图2所示,支撑框架102的第一端部110可以成形为圆柱的大致平坦的端部,其中支撑框架102的各第一顶点114基本上处于同一平面中,该平面可相对于假体100的纵轴线120大致垂直地取向。此外,第二端部112可以成形为包括一系列峰130和谷132,其中支撑框架102的第二顶点或副峰136共同地形成峰130和谷132的轮廓。当假体在自体瓣环内就位时,第二端部112的峰130和谷132可位于第一端部110的下游。
根据一些实施例,如图2所示,人工瓣叶106可以在与第二端部112的峰130周向对齐的位置处相对于支撑框架102联接。在一些实施例中,可以使用超高分子量聚乙烯缝线(sutures)将人工瓣叶106连接到膜108。这种独特的构造可有利地使假体100能够更完全地接近自体瓣膜结构,允许更自然的血液流动,而不限制或以其他方式约束瓣叶106的移动,并且使假体100更加无缝地与心脏的周围结构一体化。在一些实施例中,人工瓣叶106可包括这样的特征,所述特征包括但不限于平面特征、扁平特征、三维特征、贝塞尔曲线或其他合适的形状。可选地,人工瓣叶106可以通过固定在小叶状心轴上而成形。
瓣膜锚104可包括至少一个u形部件、瓣膜扣紧件、窦定位器、瓣膜定位器、或围绕瓣膜锚104的纵轴线延伸的瓣膜钩140。如图2所示,瓣膜锚104可包括多个凸部(lobes)或u形部件140,例如包括三个u形部件140,但也可以包括更少或更多个u形部件140。在一些实施例中,u形部件140可构造为与自体主动脉瓣的后主动脉窦、左主动脉窦和右主动脉窦接合,或者配合在自体主动脉瓣的后主动脉窦、左主动脉窦和右主动脉窦内。每个u形部件140可具有峰部分142和基体部分144。每个u形部件140可包括第一腿部146和第二腿部148。相邻的u形部件140的第一腿部146和第二腿部148可以在其峰部分142处互联。此外,u形部件140可以包括除u形以外的形状,诸如波浪形、v形、w形或者之字形等。可选地,多个瓣膜锚104可各自包括一个或多个u形部件140,其中所述多个瓣膜锚104协同地与主动脉窦接合,以便锚固本文所描述的瓣膜假体。
瓣膜假体100可包括使支撑框架102与瓣膜锚104互连的耦联机构(linkmechanism)。该耦联机构可包括将支撑框架102与瓣膜锚104互连的单个连续的材料线束或者多个彼此独立的材料线束。此外,耦联机构可以以滑动、接合或固定的方式附接到支撑框架102上和/或瓣膜锚104上的一个或多个位置。
根据一些实施例,瓣膜锚104可选的在瓣膜锚104的一个或多个部分中限定一个或多个接合区域,其中耦联机构可与一个或多个接合区域接合以限制支撑框架102与瓣膜锚104之间的相对运动。
例如,在各个峰部的互连处,瓣膜锚104可以限定接合区域150。接合区域150也可以被称为峰部接合区域。
如图2所示,支撑框架102可以经由一个或多个拴构件或耦联机构160柔性地耦合至瓣膜锚104。耦联机构160可以耦合到支撑框架102和瓣膜锚104,允许支撑框架102与瓣膜锚104之间的相对运动。然而,耦联机构160可以构造为限制支撑框架102与瓣膜锚104之间的相对移动。在一些实施例中,如本文所讨论的,当耦联机构160接合于接合区域150中时,瓣膜锚104的接合区域150可以用于进一步限制支撑框架102相对于瓣膜锚104的相对运动。
因此,瓣膜锚104可以耦合至支撑框架102,以允许瓣膜锚104相对于支撑框架102轴向或纵向移动,同时仍然保持耦合至支撑框架102。一些实施例的这种有利特征可以允许临床医生将瓣膜锚104相对于支撑框架102独立定位。例如,在经导管主动脉瓣置换中,临床医生可以独立地定位瓣膜锚104,以便将瓣膜锚104的基体部分144装配到主动脉窦中。主动脉窦的部分可包括自体主动脉瓣的后主动脉窦、左主动脉窦和/或右主动脉窦。在一些实施例中,瓣膜锚104可以旋转以在相应的主动脉窦中对准。在一些实施例中,瓣膜锚104与支撑框架102的互连可以允许瓣膜锚104自转以在主动脉窦中对准。此后,在瓣膜锚104“落在”相应的主动脉窦中的情况下,瓣膜锚104与支撑框架102的互连进一步使得支撑框架102能够沿着瓣膜假体100的纵向轴线120平移。在一些实施例中,在输送过程中,瓣膜锚104可以至少轴向地从相对于支撑框架102的近端位置移动到相对于支撑框架102的远端位置,或者从这些位置中的任一个移动到如下位置:支撑框架102与瓣膜锚104至少部分地纵向重叠的位置或支撑框架102与瓣膜锚104同心的位置。例如,在2018年12月18日提交的美国专利申请no.62/781,537的图11a至图11f中示出了各种位置的范围,其全部内容通过引用并入本文。
例如,如图2所示,当支撑框架102嵌套在瓣膜锚104内时,瓣膜锚104的基体部分144可沿纵向轴线120与支撑框架102的第一端部110纵向间隔开,间隔的距离为支撑框架102的长度的约10%至约100%、约25%至约75%、约33%至约100%、约33%至约66%、约25%至约75%、约50%至约75%、约60%至约70%。在一些实施例中,支撑框架102可以包含于瓣膜锚104或与瓣膜锚104完全重叠。在一些实施例中,支撑框架102可以与瓣膜锚104具有最小的重叠或没有重叠。支撑框架102可沿纵向轴线120移动以与瓣膜锚104重叠为支撑框架102的长度的约10%至约100%、约25%至约75%、约33%至约100%、约33%至约66%、约25%至约75%、或约50%至约75%。根据一些实施例,瓣膜锚104的u形部件140可以处于主动脉窦内的嵌套位置中,并且瓣膜锚104的基体部分144可以与支撑框架102的第一端部110纵向邻接、共面或间隔开。例如,当瓣膜锚104的至少一个基体部分144与自体主动脉瓣小叶的基体部分附件接触或相邻时,瓣膜锚104可以处于嵌套位置。此外,支撑框架102的第一端部110可以与自体瓣膜结构(或由自体主动脉瓣小叶的基体部分附件形成的虚拟环)或与心室-主动脉交叉点纵向邻接、共面或间隔开。
耦联机构160可以允许瓣膜锚104相对于支撑框架102的旋转和纵向移动。因此,尽管存在耦联机构160,瓣膜锚104也可以相对于支撑框架102旋转地移动。此外,在一些实施例中,耦联机构160可以固定地附接或耦合至支撑框架102并且固定地或可滑动地附接至瓣膜锚104。当支撑框架102相对于瓣膜锚104移动时,耦联机构160可以沿着u形部件140滑动。在一些实施例中,u形部件140具有大致弓形或凸形形状(如图2中的u形部件所示),其允许耦联机构160沿u形部件140的第一腿146和第二腿148的几何形状不受限制地移动。当耦联机构160被允许沿着u形部件140的第一腿146和第二腿148滑动时,瓣膜假体100可以处于被称为“可滑动”状态的位置。在可滑动状态下,支撑框架102相对于瓣膜锚104的纵向和/或旋转移动的范围是可变的并且可以是其最大的,因为耦联机构160可以沿着u形部件140的第一腿146和第二腿148移动。
在一些实施例中,耦联机构160可以固定地附接或耦合至支撑框架102并且固定地附接至瓣膜锚104。当支撑框架102相对于瓣膜锚104移动时,耦联机构160可以弹性地和/或可塑性地伸展、弯曲、变形。当耦联机构160变形时,支撑框架102相对于瓣膜锚104的纵向和/或旋转移动的范围是可变的,这是耦联机构160的变形所允许的。
在一些实施例中,耦联机构160可具有多个连接构件,其中每个连接构件耦合至支撑框架102的圆周并且沿支撑框架102的圆周间断地间隔开。每个连接构件可以可滑动地耦合至u形部件140中的相应一个。此外,耦联机构160可以具有以端对端方式耦合在一起的多个连接构件。此外,耦联机构160可以具有多个连接构件,这些连接构件在一端单独地耦合至支撑框架102以及在另一端单独地耦合至瓣膜锚104。如同本文类似地公开的那样,每个连接构件可以沿着瓣膜锚104可滑动,这里为了简洁起见不再描述。
然而,如上面所注意到的,瓣膜锚104还可包括接合区域150,接合区域150能与耦联机构160接合,以限制支撑框架102与瓣膜锚104间的相对运动。接合区域150可包括一个或多个局部凹面或其他几何形状,一旦耦联机构160进入接合区域150,所述局部凹面或其他几何形状就可以与耦联机构160接合或捕捉耦联结构160。接合区域150的各个实施例(诸如在上文提及的美国专利申请no.62/781,537的图2a至图2g中披露的那些)可用于:允许可滑动的耦联机构160进入接合区域150,但限制耦联机构160离开接合区域150。
现在参考图3,其提供了根据一些实施例的装载到递送装置200上的瓣膜假体100的侧剖视图。在图3中所示出的许多特征当中,图3示出了递送装置200的近侧外壳210可在瓣膜锚104和支撑框架102二者上延伸。因此,根据一些实施例,在图3所示的压缩或递送构造中,耦联机构(未示出)可以在瓣膜锚104与支撑框架102之间延伸,并且被至少部分地封入近侧外壳210内(取决于耦联机构与支撑框架102的连接点以及近侧外壳210的纵向范围)。
另外,图3示出了瓣膜锚104可包括耦联移动限制器240。耦联移动限制器240可以提供瓣膜锚104的线框结构的放大轮廓,以便在耦联机构沿着瓣膜锚104的u形部件滑动时限制或阻止耦联机构的移动。
在递送装置200的替代实施例中,在释放瓣膜锚104之前和期间,瓣膜锚104和支撑框架102都可以封闭在近侧护套构件204内。例如,在一些实施例中,瓣膜锚104可以在支撑框架102的远侧,其中瓣膜锚104靠近近侧护套构件204的远端,并且支撑框架102可以大致邻近瓣锚104(处于串联构造)且靠近瓣膜锚104。在递送装置200的一些实施例中,瓣膜锚104和支撑框架102都可以封闭在近侧护套构件204内,其中支撑框架102靠近近侧护套构件204的远端,并且瓣膜锚104大致邻近支撑框架102且位于支撑框架102的近侧。
此外,在递送装置200的替代实施例中,瓣膜锚104可以封闭在远侧载体组件206内,并且支撑框架102可以在瓣膜假体的递送之前和期间封闭在近侧护套构件204内。例如,在递送装置200的一些实施例中,瓣膜锚104和支撑框架102都可以封闭在远侧载体组件206内,并且支撑框架102可以在瓣膜假体的递送之前和期间封闭在近侧护套构件204内。在该构造中,瓣膜锚104和支撑框架102可以彼此大致相邻(处于串联构造),并且瓣膜锚104可以定位在支撑框架102的近侧。递送装置和假体的其他细节在上面提到的美国专利申请no.62/781,537中提供,并且以引用的方式并入本文。
此外,图3示出了锚保持部件170可用于使瓣膜锚104的接合区域150与控制部件或抓紧件224接合,以便于在递送期间移动和控制瓣膜锚104的定位。如关于上面提到的美国专利申请no.62/781,537的图7g至图7i所讨论的,这种接合可以将接合区域150保持在共同的平面152中,该平面152相对于递送装置200的纵轴线大致垂直地取向。
图4示出了根据至少一个实施例的递送装置200a的各方面。这些图未示出可以结合到实施例中的递送装置的所有构件。然而,这些图中所示的特征可以结合到递送装置的实施例中,以便于与瓣膜锚的接合,和/或在瓣膜锚在目标位置处的植入和释放期间便于瓣膜锚的递送和控制。
例如,图4示出了包括抓紧机构的递送装置200a的实施例。抓紧机构可用于将瓣膜锚的一部分与递送装置牢固地连接,以允许临床医生控制瓣膜锚的移动、操作和展开。抓紧机构可以使用各种联接机构接合瓣膜锚的一个或多个部分或结构,联接机构可以使用包括机械接合的附接装置、可溶解结构、化学反应性可降解结构、可电解降解结构等。
在一些实施例中,抓紧机构可以是管状抓紧机构。如图4所示的递送装置200a可包括抓紧件224a,抓紧件224a可与瓣膜锚104a的纵向位置接合并控制该纵向位置。递送装置200a的抓紧件224a可包括能够在管状外壳的管腔内移动的接合线。瓣膜锚104a可构造为包括从瓣膜锚104a的接合区域150d或150d'延伸的扣紧件柄脚(claspertang)。接合线可包括远端部,该远端部包括可在瓣膜锚104a的接合区域处联接到扣紧件柄脚的接合结构的销、脊或突起。当接合在一起时,接合线和扣紧件柄脚可以向近侧拉入管状外壳的管腔中,这在径向和纵向方向上将接合线和扣紧件柄脚相对于彼此固定。然而,当接合线和扣紧件柄脚移动到管状外壳的管腔之外时,随着瓣膜锚104a和扣紧件柄脚径向扩展,接合线和扣紧件柄脚可以脱离接合,从而使扣紧件柄脚从接合线脱开。这些和其它特征在上面提到的美国专利申请no.62/781,537中讨论,并且以引用的方式并入本文。
在使用期间,在瓣膜锚已从近侧护套内释放并且在瓣膜锚和瓣架已从递送装置释放之后,递送装置可构造为紧凑地重新组装并撤回到导引护套中,以便最小化对递送装置前进穿过的血管的任何损害。
例如,在至少一个实施例中,如图5a所示,近侧外壳210可包括近侧部分250,以便近侧护套构件204的远端部208与近侧外壳210的重新对准(例如,径向重新对准)。
如图5a所示,近侧部分250可以联接到芯部件220。此外,近侧部分250能够可选地在近侧方向上是锥形的或逐渐变细的,和/或近侧部分250具有圆周凸部(node)252和/或圆周腔254,这可便于近侧护套构件204相对于近侧外壳210沿着递送装置200的纵轴线的重新对准。近侧部分250的逐渐变细可以允许近侧护套构件204的远端部208在近侧部分250上向远侧平稳地前进,并且当远端部208接近近侧抵接表面214时,圆周凸部252可以接触近侧护套构件204的远端部208的内表面。
例如,如图5a所示,圆周凸部252可以在近侧方向上从近侧抵接表面214逐渐变细。利用这样的构造,当近侧护套构件204朝向近侧外壳210向远侧滑动时,圆周凸部252可以有利地朝向近侧外壳210的近侧抵接表面214向远侧引导近侧护套构件204的远端部208,使得近侧护套构件204的外表面与近侧外壳210的外表面对准。因此,近侧外壳210的外表面和近侧护套构件204的外表面可为递送装置200提供平滑的外部轮廓,当递送装置200在体腔内移动时,平滑的外部轮廓可以有利地降低递送装置200卡住或以其他方式损坏体腔内的组织的可能性。
可选地,近侧部分250可包括三个圆周凸部252和三个圆周腔254。圆周凸部252可从近端抵接表面214向近侧延伸。三个圆周腔254可以对应于瓣膜锚的u形部件的数量,所述u形部件容纳在近侧护套构件204和近侧外壳210的近侧部分250之间的近侧护套构件204内。
一些实施例的该有利特征可以允许远侧外壳212沿着递送装置200适当地定位,以确保远侧外壳212在取回递送装置200期间不会钩住或卡在任何结构上。
还如图5a和图5b所示,近侧外壳210和远侧外壳212可以共同容纳支撑框架102。可以致动第一芯部件220和第二芯部件222以分离近侧外壳210和远侧外壳212,从而允许支撑框架102在瓣膜锚104内就位时自扩展。
例如,通过沿着递送装置200的纵轴线相对于彼此推动或拉动第一芯部件220、第二芯部件222和/或近侧护套构件204,临床医生可以控制这些部件中的每一个的纵向移动,以允许释放瓣膜假体100的支撑框架102和瓣膜锚104。
此外,在一些实施例中,为了便于将递送装置200递送到目标位置,如图5a和5b所示,第二芯部件222可包括管腔218,以允许递送装置200沿着可以延伸穿过第二芯部件222的管腔218的导丝移动。
图5a和5b进一步示出了在支撑框架102释放期间近侧外壳210和远侧外壳212的位置。在将近侧外壳210和远侧外壳212从图5a中所示的位置分离到图5b中所示的位置之后,支撑框架102的第一端部110可以开始从压缩构造扩展到扩展构造。在一些实施例中,支撑框架102可在其第一端部110处具有一个或多个锚109(也参见图2),当锚109与自体瓣膜结构接合时,锚109可补充向外的扩展力(由于支撑框架102的自扩展)及其所产生的摩擦接合,以减轻支撑框架102相对于自体瓣膜结构的下游移动。因此,通过首先打开第一端部110(在第二端部112之前,并且经由近侧外壳210和远侧外壳212的相对移动),第一端部110可以如开花那样打开,以便于支撑框架的释放和/或与自体解剖结构(例如瓣膜结构本身)接合,以确保支撑框架102相对于自体瓣膜结构的纵向位置。此后,可以控制和释放支撑框架102的第二端部112,以使第二端部112从近侧外壳210脱离接合并释放。
在一些实施例中,第一端部110和第二端部112可以以相同或不同的速率同时打开。例如,在一些实施例中,第一端部110和第二端部112可以同时打开,但是第一端部110以比第二端部112更快的速率打开。
有利地,近侧外壳210和远侧外壳212的使用允许框架102的更大控制和增强操作。例如,通过控制近侧外壳210和远侧外壳212的分离位置和速率,可以控制支撑框架102在第一端部110和第二端部112处的打开。此外,通过控制远侧外壳212的移动,可以相对于第二端部112的打开的定时和速率(其可以通过近侧外壳210的移动来控制)来控制第一端部110的打开的定时和速率。
另外且有利地,通过具有单独的近侧外壳210和远侧外壳212,递送装置200所受的摩擦力可以减小,并使外壳210、212相对于支撑框架102的行程最小化。
特别地,根据一些实施例,远侧载体组件206可包括柱塞机构260,柱塞机构260可促进支撑框架102的扩展。柱塞机构260可从压缩状态(如图5a所示)扩展到扩展状态(如图5b所示)。柱塞机构260可以由弹簧或其他装置偏压,以便自动地从压缩状态移动到扩展状态。然而,在一些实施例中,柱塞机构260也可由临床医生手动致动。
如所示的,柱塞机构260可包括柱塞头262和偏压装置264。柱塞头262可包括圆锥形或逐渐变细的近侧部分286。锥形近侧部分286可以构造为在递送期间不仅接触支撑框架102的第一端部,而且还可以帮助使近侧外壳210的管状部分282的远端部290相对于递送装置200的纵轴线居中,并帮助将远端部290与远侧外壳212的管状部分272的近端部292对准。柱塞头262还可以包括外周表面294,外周表面294不仅可以接触管状部分272的内表面296,而且当管状部分282在柱塞头262的锥形近侧部分286上向远侧前进时,可以接触管状部分282的内表面298。
此外,柱塞机构260可以容纳在远侧外壳212的管状部分272的远侧管腔270内。例如,偏压装置264可以是弹簧。偏压装置264可以插入在远侧管腔270的内部结构或壁274与柱塞头262的远侧表面或结构276之间。柱塞头262可在远侧管腔270内向近侧移动,以便继续对支撑框架102的第一端部110施加朝向近侧取向的力,直到支撑框架102离开远侧管腔270。此后,根据一些实施例,支撑框架102可以自扩展,直到随着支撑框架102继续扩展,第二端部112从近侧外壳210的管状部分282的近侧管腔280被拉出。支撑框架102的扩展状态在上面讨论的图1和图2中示出。
本公开还描述了用于例如经股动脉递送瓣膜假体的递送装置的各方面。递送装置可以支撑瓣膜假体,诸如上面讨论的假体100。递送装置可包括近侧护套构件、远侧载体组件和控制单元,其中远侧载体组件在近侧护套构件的远侧,并且近侧护套构件在控制单元的远侧。在一些实施例中,远侧载体组件可包括圆锥形或锥形端部。近侧护套构件和远侧载体组件可在瓣膜假体的递送之前和期间至少部分地包围瓣膜假体的支撑框架和瓣膜锚。相对于近侧护套部件和远侧载体组件、支撑框架和瓣膜锚,递送装置的构造可使得瓣膜锚和支撑框架在紧凑状态下沿纵轴线连续地装载或定位,因此,使得递送装置能够实现最小的交叉轮廓,以减少将递送装置推进到患者体内的目标位置的任何困难。瓣膜锚可以从支撑框架连续移位的距离是可大幅变化的。这可以允许使用者将必须通过例如动脉和静脉推进的递送装置的半径最小化。此外,在定位和释放支撑框架之前,瓣膜锚可以独立于支撑框架而展开和定位,如下面更详细地描述的。另外,将瓣膜锚互连到支撑框架的耦联机构可有利地有助于支撑框架相对于瓣膜锚的可靠定位。
现在参考图6-7d,假体100被示出装载到递送装置200上。使用递送装置200,可以将瓣膜假体100逐个构件地递送和展开,以实现图2中所示的展开构造。在这个逐个构件展开过程期间(在上面提到的2018年12月18日提交的美国专利申请no.62/781,537的图11a-11f的递送阶段中所示的),耦联机构160沿着瓣膜锚104的u形部件移动的能力提供了几个明显的益处。例如,图6中示出了这些益处中的一个,即在瓣膜假体100的递送期间,使瓣膜锚104与支撑框架102连续定位以便实现递送装置最小的外部轮廓是有利的。该连续定位使得递送装置200具有最小化的外径,这可以使得递送装置200更容易地通过血管推进。
如图6所示,递送装置可以承载瓣膜假体的支撑框架、瓣膜锚和耦联机构。例如,图6显示递送装置200可以承载瓣膜假体100的支撑框架102、瓣膜锚104和耦联机构160。递送装置200可包括一个或更多个沿着递送装置200的纵轴线延伸的细长的芯部件。
递送装置200还可包括近侧护套构件204(在图6中以虚线示出以示出假体100和递送装置200的下面构件和特征)和远侧载体组件206(在图6中也以虚线示出以示出假体100和递送装置200的下面构件和特征)。近侧护套构件204可以耦联到控制单元并且远离控制单元延伸(在上面提到的2018年12月18日提交的美国专利申请no.62/781,537的图13a-13h中示出),临床医生可以通过该控制单元控制递送装置200的各构件的移动。
远侧载体组件206可以是构造成容纳瓣膜锚或支撑框架中的至少一个的两件式构件。远侧载体组件206包括近侧外壳210(以虚线示出)和远侧外壳212(以虚线示出)。近侧外壳210可以耦联到第一芯部件220,并且远侧外壳212可以藕联到第二芯部件222。在一些实施例中,远侧外壳212可以螺纹耦联和/或粘接耦联或结合到第二芯部件222。例如,第二芯部件222可包括中空轴。第一和第二芯部件220、222可以使得临床医生操纵近侧和远侧外壳210、212的相对位置。在将瓣膜假体100递送到体内的目标位置(例如,在此讨论的为主动脉瓣环)期间,近侧护套构件204和远侧载体组件206可以分别一起共同容纳瓣膜锚104和支撑框架102,并且由临床医生致动近侧护套构件204和远侧载体组件206以定位和释放瓣膜假体100。此外,远侧外壳212可包括圆锥形或锥形的前部或远侧部,以有助于通过脉管系统的移动。在一些实施例中,远侧载体组件206可被称为两件式远侧外壳或分叉式鼻锥组件。可选地,远侧外壳212可包含、或由其形成、或包括以下特征:含有诸如铂的不透射线材料。
图6示出了在装载构造中,在递送假体100之前的递送装置200。如所示的,第一和第二芯部件220、222延伸穿过递送装置200并且在其远端处分别耦联到远侧载体组件206的近侧外壳210和远侧外壳212。如这些图中所示,第二芯部件222可以设置在第一芯部件220的管腔内并可在其内滑动。因此,远侧载体组件206的近侧外壳210以及近侧护套构件204可相对于第二芯部件222和远侧外壳212为可滑动。
还如所示,近侧护套构件204可以在瓣膜锚104上方向远侧延伸,以将瓣膜锚104封闭在近侧护套构件204的管腔内,并将瓣膜锚104保持在压缩状态。近侧护套构件204的管腔也可称为近侧护套管腔。近侧护套部件204可相对于瓣膜锚104缩回,以允许瓣膜锚104的u形构件的基体部分随后展开并稍后被调遣到主动脉窦内的位置中。
还如图6中所示(也参见上文提到的2018年12月18日提交的美国专利申请no.62/781,537的图3a-3c),递送装置200可包括至少一个抓紧件224,抓紧件224可接合瓣膜锚104并控制瓣膜锚104的定位。抓紧件224可在可耦联到瓣膜锚104的u形构件的峰部的远侧包括远端、夹钳或钩226。例如,抓紧件224的夹钳226可以在瓣膜锚104的接合区域处耦联到锚保持构件170,以使抓紧件224与瓣膜锚104接合。抓紧件224的数量优选地等于瓣膜锚104的接合区域150或u形部件140的数量。每个抓紧件224可包括管状外壳228,终止于夹钳或钩226中的一对线材穿过管状外壳228。可以相对于容纳有线材的管状外壳228向近侧拉动线材,以便将夹钳226紧固在锚保持构件170周围,从而接合瓣膜锚104。为了释放夹钳226,线材可以相对于管状外壳228向远侧转移,从而使得夹钳226径向弹开并释放锚保持构件170。每个抓紧件224的远端可以封闭或耦联到瓣膜锚104的钩上。
抓紧件224的远端、夹钳或钩226与瓣膜锚104之间的互连可允许支撑框架102的瓣膜锚104相对于近侧护套构件204或在其内保持在静止和/或压缩位置。如下面进一步讨论的,例如,关于图9a-9c,这种接合可以将接合区域150保持在共平面152中,该平面152相对于递送装置200的纵轴线大致垂直的方向定向。另外,当近侧护套构件204相对于抓紧件224的远端向近侧缩回时,瓣膜锚104可以开始展开;然而,抓紧件224和接合区域150之间的接合可以使得临床医生在完全释放瓣膜锚104与递送装置200的接合之前相对于递送装置200推动、拉动或旋转瓣膜锚。例如,如上所述的,这可以使得临床医生将瓣膜锚104的基体部分144旋转或推入主动脉窦内的嵌套位置。此后,一旦处于嵌套位置,瓣膜锚104的接合区域150可以从抓紧件224的夹钳226释放,并且瓣膜锚104可以完全展开并且释放成与自体瓣环并置。
因此,在至少一个实施例中,临床医生可以通过将抓紧件的接合部或突起与瓣膜锚的扣紧件柄脚接合或耦联来操纵瓣膜锚。通过将接合部和扣紧件柄脚封闭在管状外壳内,可以限制接合部和扣紧件柄脚的相对径向移动(从而保持纵向接合并相对于彼此固定)。为了使接合部和扣紧件柄脚脱离,临床医生可以使接合部向远侧相对地推进超过管状外壳的端部。一旦处于该位置,当瓣膜锚径向展开时,扣紧件柄脚趋向于径向向外拉动,从而使扣紧件柄脚脱离接合部。此后,接合部可以缩回或撤回到管状外壳中。在一些实施例中,接合部与扣紧件柄脚的窗口或突起接合。在一些实施例中,接合部是销或槽。在一些实施例中,每个抓紧件可包括多个接合部或突起。
在使用期间,在瓣膜锚已经从近侧护套内释放之后并且在瓣膜锚和锚框架已经从递送装置释放之后,递送装置可以构造为紧凑地重新组装并撤回到导引器护套中,以便使对递送装置推进的血管的任何损害最小化。
例如,在至少一个实施例中,如图7a所示,近侧外壳210可包括近侧部分250,以有助于近侧护套构件204的远端部208与近侧外壳210的重新对准(例如,径向重新对准)。
如图7a所示,近侧部分250可以耦联到芯部件220。此外,近侧部分250可以可选地在近侧方向上是圆锥形或锥形的和/或具有圆周凸部252和/或圆周腔254,这可以有助于近侧护套构件204相对于近侧外壳210沿着递送装置200的纵轴线的重新对准。近侧部分250的逐渐变细可以使得近侧护套构件204的远端部208向远侧平稳地前进到近侧部分250上方,以及当远端部208接近近侧邻接表面214时,圆周凸部252可以接触近侧护套构件204的远端部208的内表面。
例如,如图7a所示,圆周凸部252可以在近侧方向上从近侧邻接表面214逐渐变细。利用这样的构造,当近侧护套构件204朝向近侧外壳210向远侧滑动时,圆周凸部252可以有利地朝向近侧外壳210的近侧邻接表面214向远侧引导近侧护套构件204的远端部208,使得近侧护套构件204的外表面与近侧外壳210的外表面对准。因此,近侧外壳210的外表面和近侧护套构件204的外表面可为递送装置200提供平滑的外部轮廓,这使得当递送装置200在体管腔内组织内移动时,可以有利地降低递送装置200捕获或以其他方式损坏体管腔内组织的可能性。
可选地,近侧部分250可包括三个圆周凸部252和三个圆周腔254。圆周凸部252可从近侧邻接表面214向近侧延伸。三个圆周腔254可对应于在近侧护套构件204和近侧外壳210的近侧部分250之间的瓣膜锚的u形构件(其容纳在近侧护套构件204内)的数量。
一些实施例的该有利特征可以使得远侧外壳212沿着递送装置200适当地定位,以便确保远侧外壳212在取出递送装置200期间不会阻碍在或卡在任何结构上。
还如图6-7b所示,近侧和远侧外壳210、212可共同容纳支撑框架102。第一和第二芯部件220、222可被致动以使近侧和远侧外壳210、212分离,从而允许支撑框架102在瓣膜锚104内就位时自展开。
例如,通过沿着递送装置200的纵轴线相对于彼此推动或拉动第一芯部件220、第二芯部件222和/或近侧护套构件204,临床医生可以控制纵向移动这些部件中的每一个以允许瓣膜假体100的支撑框架102和瓣膜锚104的释放。
此外,在一些实施例中,为了有助于将递送装置200递送到目标位置,如图7a-7d所示,第二芯部件222可包括管腔218以允许递送装置200沿着导丝移动,导丝可以延伸穿过第二芯部件222的管腔218。
图7a-7d进一步示出了在支撑框架102的释放期间近侧和远侧外壳210、212的位置。在将近侧和远侧外壳210、212从图7a中所示的位置分离到图7b中所示的位置之后,支撑框架102的第一端部110可以开始从压缩构造展开到展开构造。在一些实施例中,支撑框架102可在其第一端部110处具有一个或多个锚109(也参见图2),当与自体瓣膜结构接合时,可补充向外的扩展力(由于支撑框架102自展开)及其所产生的摩擦接合,以减轻支撑框架102相对于自体瓣膜结构的下游迁移。因此,通过首先打开第一端部110(在第二端部112之前,并且经由近侧和远侧外壳210、212的相对移动),第一端部110可以“开出花”以有助于释放支撑框架和/或与自体解剖结构(例如瓣膜结构本身)接合,以确保支撑框架102相对于自体瓣膜结构的纵向位置。此后,可以控制和释放支撑框架102的第二端部112以从近侧外壳210脱离并释放。
在一些实施例中,第一端部110和第二端部112可以以相同或不同的速率同时打开。例如,在一些实施例中,第一端部110和第二端部112可以同时打开,但是第一端部110以比第二端部112更快的速率打开。
有利地,近侧外壳210和远侧外壳212的使用使得更大的控制和增强支撑框架102的操作。例如,通过控制近侧外壳210和远侧外壳212的分离位置和速率,可以控制第一端部110和第二端部112处的支撑框架102的打开。此外,通过控制远侧外壳212的移动,可以相对于第二端部112的打开的定时和速率(其可以通过近侧外壳210的移动来控制)来控制第一端部110的打开的定时和速率。
另外且有利地,通过具有分离的近侧和远侧外壳210、212,递送装置200可以经历减小的摩擦力并且使外壳210、212相对于支撑框架102的行进最小化。
具体地,根据一些实施例,远侧载体组件206可包括柱塞机构260,柱塞机构260可有助于支撑框架102的展开。柱塞机构260可从压缩状态(图7a中所示)扩展到展开状态(如图7b所示)。柱塞机构260可由弹簧或其他装置偏压,以便自动地从压缩状态移动到展开状态。然而,在一些实施例中,柱塞机构260也可由临床医生手动致动。
如所示的,柱塞机构260可包括柱塞头262和偏压装置264。此外,柱塞机构260可容纳在远侧外壳212的管状部272的远侧管腔270内。例如,偏压装置264可为弹簧。偏压装置264可以置于远侧管腔270的内部结构或壁274与柱塞头262的远侧面表面或结构276之间。柱塞头262可以在远侧管腔270内向近侧移动,以便继续在支撑框架102的第一端部110上施加向近侧取向的力,直到支撑框架102离开远侧管腔270。此后,根据一些实施例,当支撑框架102继续展开时,支撑框架102可以自展开,直到第二端部112被拉出近侧外壳210的管状部282的近侧管腔280。支撑框架102的展开状态在图7c和7d中示出。
一些实施例还可以提供自对准特征以使得递送组件的构件从释放状态(其中瓣膜假体的构件从与递送组件的接合释放)移动到嵌套或收起状态,其中递送组件具有对准的外表面或在接缝外部轮廓处邻接的外表面,这使得当从患者的脉管系统取回递送组件时,倾向于减少阻碍在脉管系统上的可能性。例如,可选地,在支撑框架102已经从远侧载体组件206展开和释放之后,柱塞头262可以有利地有助于远侧载体组件206的近侧和远侧外壳210、212的重新定位和重新对准,以准备从患者移除递送装置200。
例如,柱塞头262可包括圆锥形或锥形近侧部286。圆锥形近侧部286可构造成在递送期间不仅接触支撑框架102的第一端部,但也可帮助相对于递送装置200的纵轴线集中近侧外壳210的管状部282的远端部290并且帮助将远端部290与远侧外壳212的管状部272的近端部292对准。
此外,在一些实施例中,柱塞头262可以至少部分地从远侧外壳212的管状部272向近侧延伸出来或从远侧外壳212的管状部272向外延伸。例如,柱塞头262可包括外周表面294,外周表面294不仅可以接触管状部272的内表面296,而且当管状部282向远侧前进到柱塞头262的圆锥形近侧部分286上方时,也可以接触管状部282的内表面298。同样地,如图7d所示,近侧外壳210的远端部290可以与远侧外壳212的近端部292定位在邻接接触位置299中。因此,柱塞机构260不仅可以有助于支撑框架102的展开,而且还可以有助于近侧和远侧外壳210、212的自对准和重新定位,以便确保近侧外壳210和远侧外壳210在取出递送装置200期间均不会阻碍在或卡在任何结构上。
根据本文公开的至少一个实施例,递送装置可任选地包括柱塞机构,该柱塞机构具有可径向展开超过远侧外壳212的管状部272的外径的特征。此外,柱塞机构还可以以接合远侧外壳212的管状部272的近端的方式构造。因此,代替图7a-7d所示实施例中所示的柱塞机构260,递送装置可以可选地包括鼻锥保护器,这可以有助于支撑框架的展开并且有利地提供在远侧方向上从第一直径到第二更大直径逐渐锥形化的接触表面或斜坡,以避免或减少当递送装置200向近侧撤回时递送装置200的任何捕获或接合。此外,鼻锥保护器可增加鼻锥或远侧载体组件206的柱强度。以这种方式,当临床医生向递送组件200施加近侧缩回力以将递送装置200缩回到递送导管中时,鼻锥保护器可帮助避免鼻锥或远侧载体组件206的破裂或脱位。
例如,图8a-8f示出了可以有助于支撑框架102的展开的鼻锥保护器260a,类似于图7a-7d中所示的柱塞机构260。鼻锥保护器260a可从压缩状态(图8b中所示)纵向移动到展开状态(图8c中所示)。鼻锥保护器260a可由弹簧或其他装置偏压,以便自动地从压缩状态移动到展开状态。然而,在一些实施例中,鼻锥保护器260a也可由临床医生手动致动。
如图8a所示,鼻锥保护器260a可包括具有瓣状物263的柱塞头部262a,瓣状物263各自从鼻锥保护器260a径向延伸并包括倾斜表面263a。倾斜表面263a可构造成接合支撑框架102的远端并且将支撑框架102推出远侧外壳212,类似于上述的柱塞机构260,这可有助于支撑框架102的展开。在一些实施例中,鼻锥保护器260a可包括聚醚醚酮(peek)或其他热塑性塑料。
在至少一个实施例中,如下所述的,瓣状物263可构造成当鼻锥保护器260a定位在远侧外壳212的管腔内时径向向内偏转,但是当瓣状物263的至少一部分离开远侧外壳212时,瓣状物263径向向外展开。因此,瓣状物263可以朝向径向展开位置弹性偏压。
另外,鼻锥保护器260a可包括中央管腔261a,递送装置200的芯部件220可通过中央管腔261a延伸。在这方面,可以允许鼻锥保护器260a沿着递送装置的芯部件滑动。
此外,鼻锥保护器260a可与远侧载体组件206一起使用,以确保在取回递送装置200期间近侧外壳210和远侧外壳212均不会阻碍在或卡在递送导管或任何解剖结构上。在至少一个实施例中,鼻锥保护器260a的倾斜表面263a还可以有助于近侧和远侧外壳210、212的自对准和重新定位,类似于由柱塞机构260提供的。
在使用中,因为鼻锥保护器260a提供平滑的倾斜表面,使得递送装置200可以接触抵靠解剖结构或递送导管的任何突起,因此,鼻锥保护器260a可以有利地使在将递送装置200缩回到递送导管期间临床医生需要的牵引力或缩回力最小化。当然,鼻锥保护器260a的另一个有益效果是防止或减少对血管的任何创伤。
如所示的,鼻锥保护器260a可被偏压成径向向外弹开,以在其展开状态下抵靠远侧外壳212的近端接合。在展开状态下,瓣状物263可以在分离部267a处分开。此外,瓣状物263每个可包括接合齿266a,接合齿266a具有从其相应的瓣状物263的外表面径向偏移的外表面,从而允许瓣状物263径向展开超过远侧外壳212的内径。齿266a可具有从瓣状物263的外表面径向偏移的接触表面。此外,当齿266与远侧外壳212的近端接合时,瓣状物263的外表面可径向延伸超过远侧外壳212的外表面。
在一些实施例中,每个瓣状物263的远侧接合表面265a可与远侧外壳212的近端邻接。如所示的,在预期将递送装置200向近侧撤回到递送导管530中的情况下,鼻锥保护器260a的倾斜表面263a可使近侧和远侧外壳210、212相对于彼此对准并有助于近侧和远侧外壳210、212相对于彼此重新定位。另外,鼻锥保护器260a的倾斜表面263a可提供有角度的表面,该有角度的表面不会阻碍或接合递送导管530的远端531(参见图8f)。
如图8b所示,鼻锥保护器260a可容纳在远侧外壳212的管状部272的远侧管腔270内。鼻锥保护器260a可经由偏压装置264耦联到远侧外壳212并经由偏压装置264向近侧推出远侧外壳212。如关于柱塞机构260所述的,偏压装置264可为弹簧。瓣状物263可被径向压缩以容纳在远侧管腔270内。偏压装置264可置于远侧管腔270的内部结构或壁274与柱塞头262a的远侧表面或结构276之间。柱塞头262a可以在远侧管腔270内向近侧移动,以便继续在支撑框架102的第一端部110上施加向近侧取向的力,直到支撑框架102离开远侧管腔270。此后,根据一些实施例,当支撑框架102继续展开时,支撑框架102可以自展开,直到第二端部112被拉出近侧外壳210的管状部282的近侧管腔280。支撑框架102的展开状态在图8c-8f中示出。
如图8c和8d所示,当鼻锥保护器260a前进时(图8c示出了处于半展开状态的鼻锥保护器260a)并且远侧接合表面265a延伸超过远侧管腔270的近端(图8d示出了处于完全展开状态的鼻锥保护器260a)时,瓣状物263可径向展开以接合抵靠远侧管腔270。可选地,鼻锥保护器260a的近端可由与中央管腔261a接合的颈部轴向保持,以使远侧接合表面265a与远侧外壳212的近端保持轴向邻接。
如图8e所示,除了在递送期间接触支撑框架102的第一端部之外,倾斜表面263a还可帮助相对于递送装置200的纵轴线集中近侧外壳210的管状部282的远端部290并且帮助将远端部290与远侧外壳212的管状部272的近端部292对准。
此外,如图8f所示,在一些实施例中,倾斜表面263a使得近侧护套构件204与远侧外壳212同心对准,使将近侧和远侧外壳210、212缩回到近侧护套构件中所需的缩回力最小化。在一些实施例中,倾斜表面263a可具有约45度的坡度角,或范围可在约10度到约80度之间,约20度到约70度之间,约30度到约60度之间,或约40度到约50度之间。
图9a-9c示出了根据至少一个实施例的递送装置的可选方面。这些图未示出可以结合到实施例中的递送装置的所有构件。然而,这些图中所示的特征可以结合到递送装置的实施例中,以有助于与瓣膜锚的接合和/或有助于在瓣膜锚在目标位置处的移植和释放期间瓣膜锚的递送和控制。
根据本文公开的至少一个实施例,认识到当递送装置移动通过血管时,在递送装置在通过血管的曲折部时,递送装置可以弯曲(bent)或弯曲(curved)。当发生这种情况时,抓紧件可能倾向于在近侧护套构件内径向移动,这可能导致抓紧件的远端或接合端相对于彼此纵向移位或未对准。这可能导致在递送期间瓣膜锚的弯曲或未对准,而这可能使放置更具挑战性。
更具体地,在至少一个实施例中,抓紧件机构(多个)可以从共平面(其可相对于递送装置的纵轴线大致垂直地取向)从手柄致动器延伸(参见例如,上文提到的2018年12月18日提交的美国专利申请no.62/781,537的图13a-13h)并且具有大致相等的纵向长度。另外,每个抓紧件机构可以源自近侧护套构件内的给定径向或圆周位置、扇区或象限。如果递送装置沿直线路径延伸,则抓紧件的远端或接合端也将在共平面(其相对于递送装置的纵轴线大致垂直取向)中对准,从而与瓣膜锚的区域接合,如上文提到的2018年12月18日提交的美国专利申请no.62/781,537的图5所示。
然而,在使用中,如果近侧护套构件例如,由于血管的曲折而弯曲(如图9a所示),则每个抓紧件机构可以从近侧护套构件内其原始的圆周或径向位置、扇区或象限移出。发生这种情况是因为每个单独的抓紧件机构将倾向于在近侧护套构件内的直的线性路径中延伸,并且仅在抓紧件机构撞击近侧护套构件的内壁时才弯曲。结果,抓紧件机构可以会聚抵靠在近侧护套构件中的弯曲的外壁上,这可以改变抓紧件的远端或接合端的相对定位。因此,代替在相对于近侧护套构件的纵轴线大致垂直取向的共平面内对准或定位,抓紧件的远端或接合端可以定位在平面外或简单地在相对于近侧护套构件的纵轴线垂直延伸的共平面之外。这种未对准可产生瓣膜锚的应力、未对准、非预期脱离或弯曲,瓣膜锚的接合区域最优选地在递送期间保持在共平面(其相对于近侧护套构件的纵轴线大致垂直地取向)内。
因此,至少一个实施例可以构造为包括对准毂,该对准毂可以沿着抓紧件机构的远侧部保持或固定抓紧件机构的至少一部分的纵向位置。以这种方式,尽管抓紧件机构的中间部可以径向未对准或偏离其在近侧护套构件内的原始径向或圆周位置、扇区或象限,但是对准毂可以有利地用于重置或重新对准抓紧件的位置,使得纵向位置可以位于基本上相同或共平面(该共平面相对于近侧护套构件的纵轴线垂直定位)内。
例如,图9a-9c示出了可任选地用在递送装置的至少一个实施例中的远侧毂或抓紧件对准毂230。如所示的,抓紧件对准毂230可用于将抓紧件226a的远端固定或保持在期望的共平面中,以使得抓紧件226a与瓣膜锚104的期望和/或可预测的接合和脱离。具体地,即使近侧护套构件204530的弯曲是通过或经过血管的弯曲度,例如在弯曲处操纵,抓紧件对准毂230也可以使得抓紧件226a的远端保持在共平面中。
如图9a和9b所示,抓紧件对准毂230可以相对于递送装置的远侧部分附近的抓紧件226a的管状外壳228a结合或固定,或直接地结合或固定到递送装置的远侧部分附近的抓紧件226a的管状外壳228a。在一些实施例中,抓紧件对准毂230可以距离递送装置的远端至少约1英寸、2英寸、3英寸、3.5英寸或4英寸固定到管状外壳228a。
参照图9b,抓紧件226a和相应的管状外壳228a延伸穿过抓紧件对准毂230(在第一或近端236与第二或远端238之间),穿过通过抓紧件对准毂230中形成的管状外壳通道232。管状外壳228a可以结合或机械耦联到管状外壳通道232,以便相对于抓紧件对准毂230接合或固定管状外壳228a。即使管状外壳228a可以受到沿递送装置的远侧部分相对于抓紧件对准毂230的纵向移动的约束,在一些实施例中,仍然可以允许抓紧件226a在管状外壳228a内移动,以有助于与瓣膜锚的接合和/或脱离。然而,因为管状外壳228a受到滑动限制,所以当近侧护套构件204移动通过或移动成曲线或曲折时,也可以限制抓紧件226a的远端相对于彼此纵向移位。与一个实施例相比,倾向于相对于彼此纵向移位更少
如所示的,芯部件220可穿过第一或近端236到达第二或远端238,穿过通过抓紧件对准毂230形成的芯部件通道234。芯部件220可可移动地通过芯部件通道234。例如,在一些实施例中,抓紧件对准毂230可相对于芯部件220移动,而管状外壳228a固定到抓紧件对准毂230。
参考图9c,抓紧件对准毂230的外表面239可具有大致圆筒形形状。在一些实施例中,外表面239的圆筒形形状可使得抓紧件对准毂230在导管530内自由移动。如所示的,管状外壳通道232和芯部件通道234可布置成当导管530在引入和递送期间被操纵时在管状外壳228a和芯部件220之间保持期望的对准。此外,在至少一个实施例中,管状外壳通道232和芯部件220在抓紧件对准毂230处的横截面布置可大致类似于它们在手柄致动器处的横截面布置。
另外,根据至少一个实施例,管状外壳通道232和芯部件通道234以及抓紧件对准毂230的布置可以进一步减少或避免管状外壳228a和芯部件220相对于导管530的管腔的纵轴线的扭曲或未对准。
如所示的,在至少一个实施例中,管状外壳通道232可以沿着与抓紧件对准毂230的周边接界的弧线彼此相邻地设置,偏移抓紧件对准毂230的中心轴线。芯部件通道234的横截面直径可以大于管状外壳通道232的相应横截面直径。芯部件通道234可以从抓紧件对准毂230的中心轴线偏移并与管状外壳通道232间隔开。这样的构造可以使得抓紧件对准毂232具有最小的横截面直径,同时允许每个管状外壳通道232和芯部件通道234被限制在其中。
然而,在至少一个实施例中,管状外壳通道232可以围绕芯部件通道234圆周地设置。可选地,管状外壳通道232可以等距地设置。
参考图7e、10a和10b,近侧外壳210的近侧部分250可包括有助于使近侧部分250与瓣膜锚接合和对准的特征。如图7e和10a所示,近侧外壳210的近侧部分250具有圆周凸部252和圆周腔254。每个圆周腔254可以由两个圆周凸部252之间的空间限定。如图10b所示,瓣膜锚104的相应u形构件可以被接收在圆周空腔254中,位于圆周凸部252之间。
例如,当装载瓣膜锚104并且近侧护套构件204覆盖瓣膜锚104时,瓣膜锚104的每个u形构件可定位在相应的圆周腔254中,在近侧部分250与近侧护套构件204之间。图7e中所示的近侧外壳210的近侧部分250的横截面(沿着图7d的线7e-7e截取)还示出了每个圆周腔254可以由两个圆周凸部252之间的空间限定,使得瓣膜锚104可以被接收或定位在圆周腔254中。
圆周凸部252和圆周腔254可有助于近侧护套构件204相对于近侧外壳210沿递送装置200的纵轴线重新对准。近侧部分250可在近侧方向上呈圆锥形或锥形,从而有助于近侧护套构件204相对于近侧外壳210沿递送装置200的纵轴线对准。在图7e、10a和10b所示的示例中,近侧部分250具有三个圆周凸部252和三个圆周腔254。然而,在另一个示例中,可以实现不同数量的圆周凸部252和/或不同数量的圆周腔254。
如上所述,递送装置200提供若干益处,例如使得递送装置200容易通过脉管系统的紧凑的通过轮廓,可靠的瓣膜锚的控制和定位,而在自体瓣环和窦内,经由耦联机构160可预测的支撑框架102和瓣膜锚104的相对定位,以及递送装置200的无阻碍取回。
- 还没有人留言评论。精彩留言会获得点赞!