用于肌营养不良的外显子跳跃寡聚物缀合物的制作方法
用于肌营养不良的外显子跳跃寡聚物缀合物
[0001]
相关申请
[0002]
本申请要求2018年5月30日提交的美国申请号15/993,287、2018年5月30日提交的美国申请号15/993,267和2018年5月29日提交的美国临时申请号62/677,484的优先权。上述申请的全部教导以全文引用的方式并入。
[0003]
通过efs-web以电子方式提交的序列表的引用
[0004]
与此同时提交的电子提交序列表的内容(名称:8163.52.wo00_sequence_listing.txt;大小:3kb;创建日期:2019年5月16日)以全文引用的方式并入本文中。
技术领域
[0005]
本公开涉及适用于人肌营养不良蛋白基因中外显子52跳跃的新型反义寡聚物缀合物及其药物组合物。本公开还提供了使用新型反义寡聚物和反义寡聚物缀合物诱导外显子52跳跃的方法,在具有适合外显子52跳跃的肌营养不良蛋白基因突变的受试者中产生肌营养不良蛋白的方法,以及治疗具有适合外显子52跳跃的肌营养不良蛋白基因突变的受试者的方法。
背景技术:
[0006]
正在使用一系列化学试剂开发反义技术来影响各种不同水平(转录、剪接、稳定性、翻译)的基因表达。这些研究大多集中在使用反义化合物来纠正或补偿各种适应症中的异常或疾病相关基因。反义分子能够特异性地抑制基因表达,正因为如此,许多有关寡聚物作为基因表达调控剂的研究工作都集中在抑制靶基因的表达或顺式作用元件的功能上。反义寡聚物通常针对rna,或者是有义链(例如mrna),或者是负链(在某些病毒rna靶标的情况下)。为了达到特定基因下调的所需效果,寡聚物通常促进靶标mrna的衰变、阻断mrna的翻译或阻断顺式作用rna元件的功能,从而有效地阻止靶蛋白的新生合成或病毒rna的复制。
[0007]
然而,在目的是上调天然蛋白的产生或补偿诱导翻译过早终止的突变,如无义或移码突变的情况下,这类技术没有用。在这些情况下,不应对有缺陷的基因转录物进行靶向降解或空间抑制,因此反义寡聚物化学物质不应促进靶标mrna的衰变或阻断翻译。
[0008]
在各种遗传疾病中,基因突变对基因最终表达的影响可以通过剪接过程中的靶向外显子跳跃过程来调节。剪接过程由复杂的多组分机制引导,使前体mrna中相邻的外显子-内含子连接紧密接近,并对内含子末端的磷酸二酯键进行裂解,随后在要拼接在一起的外显子之间进行重整。这个复杂而高度精确的过程是由前体mrna中的序列基序介导的,这些序列基序是相对短的、半保守的rna片段,然后参与剪接反应的各种核剪接因子与之结合。通过改变剪接机制读取或识别参与前体mrna加工的基序的方式,有可能产生差异剪接的mrna分子。目前已经认识到,在正常的基因表达过程中,大多数人类基因都是选择性剪接的,尽管还没有确定所涉及的机制。bennett等人(美国专利号6,210,892)描述了使用反义寡聚物类似物对野生型细胞mrna加工的反义调节,所述反义寡聚物类似物不诱导rnase h介导的靶rna的裂解。这在能够产生缺乏特定外显子的选择性剪接的mrna中发现了效用(参
见例如sazani,kole等人2007年描述的缺乏编码跨膜域外显子的可溶性tnf超家族受体的产生)。
[0009]
在正常功能蛋白因其中的突变而过早终止的情况下,通过反义技术恢复一些功能蛋白产生的手段已经被证明是可以通过在剪接过程中进行干预的,如果可以从一些基因中特异性地删除与致病突变相关的外显子,有时可以产生缩短的蛋白产物,该产物具有与天然蛋白相似的生物学特性,或者具有足够的生物学活性,以改善与外显子相关的突变所引起的疾病(参见例如sierakowska,sambade等人1996;wilton,lloyd等人1999;van deutekom,bremmer-bout等人2001;lu,mann等人2003;aartsma-rus,janson等人2004)。kole等人(美国专利号:5,627,274;5,916,808;5,976,879;和5,665,593)公开了使用不促进靶标前体mrna衰变的修饰的反义寡聚物类似物对抗异常剪接的方法。bennett等人(美国专利号6,210,892)描述了亦使用反义寡聚物类似物对野生型细胞mrna加工的反义调节,所述反义寡聚物类似物不诱导rnase h介导的靶rna的裂解。
[0010]
靶向外显子跳跃的过程可能在长基因中特别有用,其中有许多外显子和内含子,外显子的遗传构成有冗余,或者蛋白质能够在没有一个或多个特定外显子的情况下发挥作用。重定向基因处理以治疗与各种基因突变引起的截短相关的遗传疾病的努力集中在使用反义寡聚物上,所述反义寡聚物:(1)与参与剪接过程的元件完全或部分重叠;或(2)在足够接近元件的位置与前体mrna结合,以破坏剪接因子的结合和功能,而这些因子通常会介导在该元件上发生的特定剪接反应。
[0011]
杜氏肌营养不良(dmd)是由蛋白质肌营养不良蛋白的表达缺陷引起的。编码该蛋白的基因含有79个外显子,分布在200多万个dna核苷酸上。任何改变外显子阅读框,或引入终止密码子,或特征在于去除整个框外一个或多个外显子,或一个或多个外显子重复的外显子突变,都可能破坏功能性肌营养不良蛋白的产生,导致dmd。
[0012]
已发现一种不太严重的肌营养不良形式,即贝克尔肌营养不良(bmd),其中突变,通常是一个或多个外显子的缺失,导致沿整个肌营养不良蛋白转录物的正确阅读框,从而使mrna翻译成蛋白质的过程不会过早终止。如果在处理突变的肌营养不良蛋白前体mrna时,上游和下游外显子的连接保持了基因的正确阅读框,其结果是编码蛋白质的mrna具有短的内部缺失,但保留了一些活性,从而产生了贝克尔表型。
[0013]
多年来,已知不改变肌营养不良蛋白阅读框的一个或多个外显子的缺失会引起bmd表型,而引起移码的外显子缺失会引起dmd(monaco,bertelson等人1988)。一般来说,肌营养不良蛋白突变包括点突变和外显子缺失,这些突变改变了阅读框,从而中断了正确的蛋白质翻译,导致dmd。还应注意的是,一些bmd和dmd患者的外显子缺失覆盖多个外显子。
[0014]
据报道,用反义寡核糖核苷酸对突变的肌营养不良蛋白前体mrna剪接进行体外和体内调节(参见例如matsuo,masumura等人1991;takeshima,nishio等人1995;pramono,takeshima等人1996;dunckley,eperon等人1997;dunckley,manoharan等人1998;wilton,lloyd等人1999;mann,honeyman等人2002;errington,mann等人2003)。
[0015]
反义寡聚物已被专门设计成靶向前体mrna的特定区域,通常是外显子,以诱导跳过dmd基因的突变,从而将这些框外突变恢复到框内,以便能够产生内部缩短但具有功能的肌营养不良蛋白。已知这种反义寡聚物完全靶向外显子内(所谓的外显子内部序列)或靶向从外显子跨入内含子一部分的剪接供体或剪接受体连接处。
[0016]
发现和开发这种用于dmd的反义寡聚物是先前研究的一个领域。这些开发包括来自:(1)西澳大利亚大学和sarepta therapeutics(本申请的受让人):wo 2006/000057;wo 2010/048586;wo 2011/057350;wo 2014/100714;wo 2014/153240;wo 2014/153220;(2)academisch ziekenhuis leiden/prosensa technologies(现在的biomarin pharmaceutical):wo 02/24906;wo 2004/083432;wo 2004/083446;wo 2006/112705;wo 2007/133105;wo 2009/139630;wo 2009/054725;wo 2010/050801;wo 2010/050802;wo 2010/123369;wo 2013/112053;wo 2014/007620;(3)卡罗莱纳医学中心:wo 2012/109296;(4)royal holloway:要求受益于且包括美国序列号61/096,073及61/164,978的专利和申请;如us 8,084,601及us2017-0204413(4)jcr pharmaceuticals and matsuo:us 6,653,466;要求受益于且包括jp 2000-125448的专利和申请,如us 6,653,467;要求受益于且包括jp 2000-256547的专利和申请,如us 6,727,355;wo 2004/048570;(5)nippon shinyaku:wo 2012/029986;wo 2013/100190;wo 2015/137409;wo 2015/194520;和(6)association institut de myologie/universite pierre et marie bern/centre national de la recherche scientifique/synthena ag:wo 2010/115993;wo 2013/053928。
[0017]
发现和开发与细胞穿透肽缀合的反义寡聚物用于dmd也是一个研究领域(参见pct公开号wo 2010/048586;wu,b.等人,《美国病理学杂志(theamerican journal ofpathology)》,第181(2)卷:392-400,2012;wu,r.等人,《核酸研究(nucleicacids research)》,第35(15)卷:5182-5191,2007;mulders,s.等人,19届世界肌肉协会国际大会,柏林海报展示,2014年10月;bestas,b.等人,《临床研究杂志(thejournal of clinical investigation)》,doi:10.1172/jci76175,2014;jearawiriyapaisarn,n.等人,《分子疗法(molecular therapy)》,第16(9)卷:1624-1629,2008;jearawiriyapaisarn,n.等人,《心血管研究(cardiovascular research)》,第85卷:444-453,2010;moulton,h.m.等人,《生化学会会刊(biochemicalsociety transactions)》,第35(4)卷:826-828,2007;yin,h.等人,《分子疗法》,第19(7)卷:1295-1303,2011;abes,r.等人,《肽科学杂志(j.pept.sci.)》,第14卷:455-460,2008;lebleu,b.等人,《先进药物递送评论(advanced drug delivery reviews)》,第60卷:517-529,2008;mcclorey,g.等人,《基因疗法(gene therapy)》,第13卷:1373-1381,2006;alter,j.等人,《自然
·
医学(nature medicine)》,第12(2)卷:175-177,2006;和youngblood,d.等人,美国化学学会,《生物缀合化学(bioconjugate chem.)》,2007,18(1),第50-60页)。
[0018]
细胞穿透肽(cpp),例如富含精氨酸的肽转运部分,可以有效地增强例如与cpp缀合的反义寡聚物向细胞内的穿透力。
[0019]
尽管作出了这些努力,但仍然需要改进的靶向外显子52的反义寡聚物和相应的药物组合物,这些药物组合物对产生肌营养不良蛋白和治疗dmd的治疗方法可能有用。
技术实现要素:
[0020]
本文提供的反义寡聚物缀合物包括与cpp缀合的反义寡聚物部分。在一个方面,本公开提供了反义寡聚物缀合物,其包含:
[0021]
长度为25个亚基的反义寡聚物,能够结合选定的靶标以诱导人肌营养不良蛋白基
因中的外显子跳跃,其中所述反义寡聚物包含与指定为退火位点的肌营养不良蛋白前体mrna的外显子52靶区互补的碱基序列;以及
[0022]
通过接头部分与所述反义寡聚物缀合的细胞穿透肽(cpp)。
[0023]
在一些实施例中,退火位点是h52a(-01+24)。
[0024]
在一些实施例中,反义寡聚物的碱基与吗啉代环结构相连,其中吗啉代环结构通过含磷的亚基间键连接,所述亚基间键将一个环结构的吗啉代氮与相邻环结构的5'外环碳连接。在某些实施例中,细胞穿透肽是六个精氨酸单位(“r
6”),而接头部分是甘氨酸。在一些实施例中,反义寡聚物包含指定为seq id no:1的碱基序列。
[0025]
在另一方面,本公开提供了长度为25个亚基的反义寡聚物,其能够结合选定的靶标以诱导人肌营养不良蛋白基因中的外显子跳跃,其中所述反义寡聚物包含与指定为退火位点的肌营养不良蛋白前体mrna的外显子52靶区互补的碱基序列。
[0026]
在一些实施例中,退火位点是h52a(-01+24)。
[0027]
在一些实施例中,反义寡聚物的碱基与吗啉代环结构相连,其中吗啉代环结构通过含磷的亚基间键连接,所述亚基间键将一个环结构的吗啉代氮与相邻环结构的5'外环碳连接。在一些实施例中,反义寡聚物包含指定为seq id no:1的碱基序列。
[0028]
在各个方面,本公开提供了可根据式(i)的反义寡聚物缀合物:
[0029][0030]
或其药学上可接受的盐,其中:
[0031]
每个nu是核碱基,其一起形成靶向序列;以及
[0032]
t是选自以下的部分:
[0033][0034]
r1是c
1-c6烷基;
[0035]
其中所述靶向序列与指定为h52a(-01+24)的肌营养不良蛋白前体mrna中的外显子52退火位点互补。
[0036]
在另一方面,本公开提供了式(v)的反义寡聚物缀合物:
[0037][0038]
或其药学上可接受的盐,其中:
[0039]
每个nu是核碱基,其一起形成靶向序列;
[0040]
t是选自以下的部分:
[0041][0042]
r1是c
1-c6烷基;以及
[0043]
r2选自h或乙酰基,其中所述靶向序列与指定为h52a(-01+24)的肌营养不良蛋白前体mrna中的外显子52退火位点互补。
[0044]
在另一方面,本公开提供了式(iva)的反义寡聚物缀合物:
[0045]
在另一方面,本公开提供了药物组合物,其包括本公开的反义寡聚物或反义寡聚物缀合物以及药学上可接受的载体。在一些实施例中,药学上可接受的载体是盐水溶液,其包括磷酸盐缓冲液。
[0046]
在另一方面,本公开提供了一种用于治疗有需要的受试者的杜氏肌营养不良(dmd)的方法,其中所述受试者具有适合于外显子52跳跃的肌营养不良蛋白基因的突变,所述方法包含向所述受试者施用本公开的反义寡聚物或反义寡聚物缀合物。本公开还解决了本公开的反义寡聚物或反义寡聚物缀合物用于制造供治疗有需要的受试者的杜氏肌营养不良(dmd)用的药物的用途,其中所述受试者具有适合于外显子52跳跃的肌营养不良蛋白基因的突变。
[0047]
在另一方面,本公开提供了一种在具有适合于外显子52跳跃的肌营养不良蛋白基因突变的受试者中恢复mrna阅读框以诱导肌营养不良蛋白产生的方法,所述方法包含向所述受试者施用本公开的反义寡聚物或反义寡聚物缀合物。在另一方面,本公开提供了一种在具有适合于外显子52跳跃的肌营养不良蛋白基因突变的受试者中在mrna加工期间从肌营养不良蛋白前体mrna中排除外显子52的方法,所述方法包含向所述受试者施用本公开的反义寡聚物或反义寡聚物缀合物。在另一方面,本公开提供了一种在具有适合于外显子52跳跃的肌营养不良蛋白基因突变的受试者中结合肌营养不良蛋白前体mrna的外显子52的方法,所述方法包含向所述受试者施用本公开的反义寡聚物或反义寡聚物缀合物。
[0048]
在另一方面,本公开提供了用于疗法的本文公开内容的反义寡聚物或反义寡聚物缀合物。在某些实施例中,本公开提供了用于治疗杜氏肌营养不良的本公开的反义寡聚物或反义寡聚物缀合物。在某些实施例中,本公开提供了用于制造用于疗法的药物的本公开的反义寡聚物或反义寡聚物缀合物。在某些实施例中,本公开提供了用于制造用于治疗杜氏肌营养不良的药物的本公开的反义寡聚物或反义寡聚物缀合物。
[0049]
在另一方面,本公开还提供了用于治疗有需要的受试者的杜氏肌营养不良(dmd)的试剂盒,其中所述受试者具有适合于外显子52跳跃的肌营养不良蛋白基因的突变,所述
试剂盒包含至少包装在合适的容器中的本公开的反义寡聚物或反义寡聚物缀合物及其使用说明书。
[0050]
当结合附图阅读以下对本公开的详细描述时,这些和其它目标和特征将被更充分地理解。
附图说明
[0051]
图1描绘了一段正常的肌营养不良蛋白前体mrna及成熟mrna。
[0052]
图2描绘了一段异常的肌营养不良蛋白前体mrna(dmd的实例)和由此产生的非功能性、不稳定的肌营养不良蛋白。
[0053]
图3描绘了依特立生,其被设计成跳跃外显子51,修复前体mrna的“框内”阅读。
[0054]
图4提供了在处理后96小时,通过rt-pcr测量的不同浓度的pmo#1和ppmo#1在健康人成肌细胞中跳跃外显子52的百分比的柱状图。误差条代表平均值
±
sd。
[0055]
图5a-5d提供了测量用pmo(pmo4225)或ppmo(ppmo4225)处理不同时间点[7天(5a)、30天(5b)、60天(5c)和90天(5d)]的mdx小鼠的四头肌中肌营养不良蛋白的蛋白质印迹分析的代表性图像。
[0056]
图6a提供了描绘通过蛋白质印迹分析确定的由pmo(pmo4225)或ppmo(ppmo4225)在注射后90天内诱导的mdx小鼠的四头肌中野生型肌营养不良蛋白的百分比的线图。
[0057]
图6b提供了描绘通过rt-pcr确定的由pmo(pmo4225)或ppmo(ppmo4225)在注射后90天内诱导的mdx小鼠的四头肌中外显子23跳跃的百分比的线图。
[0058]
图7a-7d提供了测量用pmo(pmo4225)或ppmo(ppmo4225)处理不同时间点[7天(7a)、30天(7b)、60天(7c)和90天(7d)]的mdx小鼠的膈膜中肌营养不良蛋白的蛋白质印迹分析的代表性图像。
[0059]
图8a提供了描绘通过蛋白质印迹分析确定的由pmo(pmo4225)或ppmo(ppmo4225)在注射后90天内诱导的mdx小鼠的膈膜中野生型肌营养不良蛋白的百分比的线图。
[0060]
图8b提供了描绘通过rt-pcr确定的由pmo(pmo4225)或ppmo(ppmo4225)在注射后90天内诱导的mdx小鼠的膈膜中外显子23跳跃的百分比的线图。
[0061]
图9a-9d提供了测量用pmo(pmo4225)或ppmo(ppmo4225)处理不同时间点[7天(9a)、30天(9b)、60天(9c)和90天(9d)]的mdx小鼠的心脏中肌营养不良蛋白的蛋白质印迹分析的代表性图像。
[0062]
图10a提供了描绘通过蛋白质印迹分析确定的由pmo(pmo4225)或ppmo(ppmo4225)在注射后90天内诱导的mdx小鼠的心脏中野生型肌营养不良蛋白的百分比的线图。
[0063]
图10b提供了描绘通过rt-pcr确定的由pmo(pmo4225)或ppmo(ppmo4225)在注射后90天内诱导的mdx小鼠的心脏中外显子23跳跃的百分比的线图。
[0064]
图11提供了免疫组织化学分析,显示由pmo(pmo4225)或ppmo(ppmo4225)诱导的mdx小鼠左四头肌中的肌营养不良蛋白。
[0065]
图12a-b提供了测量用不同剂量的pmo(pmo4225)或ppmo(ppmo4225)处理的mdx小鼠的心脏中肌营养不良蛋白的蛋白质印迹分析的代表性图像:40mg/kg、80mg/kg和120mg/kg。
[0066]
图13提供了描绘在注射后30天通过蛋白质印迹分析确定的由不同剂量的pmo
(pmo4225)或ppmo(ppmo4225)诱导的mdx小鼠的心脏中野生型肌营养不良蛋白的百分比的柱状图:40mg/kg、80mg/kg和120mg/kg。
[0067]
图14a-b提供了测量用不同剂量的pmo(pmo4225)或ppmo(ppmo4225)处理的mdx小鼠的膈膜中肌营养不良蛋白的蛋白质印迹分析的代表性图像:40mg/kg、80mg/kg和120mg/kg。
[0068]
图15提供了描绘在注射后30天通过蛋白质印迹分析确定的由不同剂量的pmo(pmo4225)或ppmo(ppmo4225)诱导的mdx小鼠的膈膜中野生型肌营养不良蛋白的百分比的柱状图:40mg/kg、80mg/kg和120mg/kg。
[0069]
图16a-b提供了测量用不同剂量的pmo(pmo4225)或ppmo(ppmo4225)处理的mdx小鼠的四头肌中肌营养不良蛋白的蛋白质印迹分析的代表性图像:40mg/kg、80mg/kg和120mg/kg。
[0070]
图17提供了描绘在注射后30天通过蛋白质印迹分析确定的由不同剂量的pmo(pmo4225)或ppmo(ppmo4225)诱导的mdx小鼠的四头肌中野生型肌营养不良蛋白的百分比的柱状图:40mg/kg、80mg/kg和120mg/kg。
[0071]
图18显示了通过pmo合成方法b执行的偶合循环。
[0072]
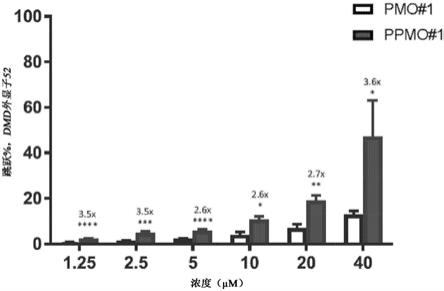
图19提供了免疫组织化学分析,显示与在mdx小鼠和野生型小鼠中的盐水相比,由ppmo(ppmo4225)诱导的mdx小鼠膈膜和心脏中的肌营养不良蛋白和层粘连蛋白。
[0073]
图20提供了在处理后96小时,通过rt-pcr测量的不同浓度的pmo#1和ppmo#1在健康人肌管中跳跃外显子52的百分比的柱状图。误差条代表平均值
±
sd。
具体实施方式
[0074]
本公开的实施例大体上涉及改进的反义寡聚物和反义寡聚物缀合物及其使用方法,其专门设计用于诱导人肌营养不良蛋白基因的外显子跳跃。肌营养不良蛋白在肌肉功能中起着至关重要的作用,并且各种与肌肉相关的疾病以该基因的突变形式为特征。因此,在某些实施例中,本文所述的改进的反义寡聚物和反义寡聚物缀合物诱导人肌营养不良蛋白基因的突变形式(例如在杜氏肌营养不良(dmd)和贝克尔肌营养不良(bmd)中发现的突变的肌营养不良蛋白基因)中的外显子跳跃。
[0075]
由于突变引起的异常mrna剪接事件,这些突变的人肌营养不良蛋白基因表达有缺陷的肌营养不良蛋白或根本不表达可测量的肌营养不良蛋白,这种情况导致各种形式的肌营养不良。为了补救这种情况,本公开的反义寡聚物和反义寡聚物缀合物与突变的人肌营养不良基因的预处理mrna的选定区域杂交,诱导该原本异常剪接的肌营养不良蛋白mrna中的外显子跳跃和差异剪接,从而使肌肉细胞产生编码功能性肌营养不良蛋白的mrna转录物。在某些实施例中,所产生的肌营养不良蛋白不一定是肌营养不良蛋白的“野生型”形式,而是肌营养不良蛋白的一种截短但具有功能的形式。
[0076]
通过增加肌肉细胞中功能性肌营养不良蛋白的水平,这些和相关的实施例可用于预防和治疗肌营养不良,特别是那些以由于异常的mrna剪接而表达缺陷的肌营养蛋白为特征的形式的肌营养不良,如dmd和bmd。本文所述的特定反义寡聚物和反义寡聚物缀合物与其它寡聚物相比,进一步提供了改进的肌营养不良蛋白-外显子特异性靶向,因此与治疗相关形式的肌营养不良的替代方法相比,具有明显且实用的优势。
[0077]
因此,本公开涉及反义寡聚物缀合物,其包含:
[0078]
长度为25个亚基的反义寡聚物,能够结合选定的靶标以诱导人肌营养不良蛋白基因中的外显子跳跃,其中所述反义寡聚物包含与指定为退火位点的肌营养不良蛋白前体mrna的外显子52靶区互补的碱基序列;以及
[0079]
通过接头部分与所述反义寡聚物缀合的细胞穿透肽(cpp)。
[0080]
本公开还涉及长度为25个亚基的反义寡聚物,其能够结合选定的靶标以诱导人肌营养不良蛋白基因中的外显子跳跃,其中所述反义寡聚物包含与指定为退火位点的肌营养不良蛋白前体mrna的外显子52靶区互补的碱基序列。
[0081]
在本公开的反义寡聚物和反义寡聚物缀合物的一些实施例中,退火位点是h52a(-01+24)。
[0082]
在一些实施例中,反义寡聚物的碱基与吗啉代环结构相连,其中吗啉代环结构通过含磷的亚基间键连接,所述亚基间键将一个环结构的吗啉代氮与相邻环结构的5'外环碳连接。在某些实施例中,细胞穿透肽是r6,而接头部分是甘氨酸。在一些实施例中,反义寡聚物包含指定为seq id no:1的碱基序列,其中每个胸腺嘧啶碱基(t)任选地是尿嘧啶碱基(u)。
[0083]
除非另有定义,否则本文所用的所有技术和科学术语具有与本公开所属领域的普通技术人员通常所理解相同的含义。尽管在本公开的实践或测试中可以使用与本文描述的方法和材料相似或等同的任何方法和材料,但描述了优选的方法和材料。为了本公开的目的,以下术语定义如下。
[0084]
i.定义
[0085]“约”是指与参考数量、水平、值、数目、频率、百分比、尺寸、大小、量、重量或长度相差多达30、25、20、15、10、9、8、7、6、5、4、3、2或1%的数量、水平、值、数目、频率、百分比、尺寸、大小、量、重量或长度。
[0086]
除非另有说明,否则本文所用的术语“烷基”是指饱和的直链或支链烃。在某些实施例中,烷基是伯、仲或叔烃。在某些实施例中,烷基包括一至十个碳原子,即c1至c
10
烷基。在某些实施例中,烷基包括一到六个碳原子,即c1至c6烷基。在某些实施例中,烷基选自由甲基、cf3、ccl3、cfcl2、cf2cl、乙基、ch2cf3、cf2cf3、丙基、异丙基、丁基、异丁基、第二丁基、叔丁基、戊基、异戊基、新戊基、己基、异己基、3-甲基戊基、2,2-二甲基丁基和2,3-二甲基丁基组成的组。该术语包括取代和未取代的烷基,包括卤代烷基。在某些实施例中,烷基是氟化烷基。可以对烷基进行取代的部分的非限制性实例选自卤素(氟、氯、溴或碘)、羟基、氨基、烷基氨基、芳基氨基、烷氧基、芳氧基、硝基、氰基、磺酸、硫酸酯基、膦酸、磷酸酯基或膦酸酯基组成的组,这些部分未受保护或必要时受保护,如本领域技术人员所熟知的,例如,如greene等人,《有机合成中的保护基团(protective groups in organic synthesis)》,john wiley and sons,第二版,1991中所教示,特此以引用的方式并入。
[0087]
如本文关于受试者或患者所用的“适于外显子52跳跃”旨在包括在肌营养不良蛋白基因中具有一个或多个突变的受试者和患者,所述突变不存在肌营养不良蛋白前体mrna的外显子52的跳跃,引起阅读框移码,从而破坏了前体mrna的翻译,导致受试者或患者无法产生功能性或半功能性肌营养不良蛋白。肌营养不良蛋白基因中适合于外显子52跳跃的突变的实例包括例如缺失:外显子2至51、外显子8至51、外显子20至51、外显子22至51、外显子
51、外显子53、外显子53至55、外显子53至57、外显子53至59、外显子53至60、外显子53至67、外显子53至69、外显子53至75和外显子53至78。确定患者是否在肌营养不良蛋白基因中具有适合于外显子跳跃的突变完全在本领域技术人员的能力范围内(参见例如aartsma-rus等人(2009)《人类突变(hum mutat.)》30:293-299;gurvich等人,《人类突变》2009;30(4)633-640;和fletcher等人(2010)《分子疗法(molecular therapy)》18(6)1218-1223)。
[0088]
如本文所用,术语“寡聚物”是指通过亚基间键连接的亚基序列。在某些情况下,术语“寡聚物”用于指“反义寡聚物”。对于“反义寡聚物”,每个亚基由以下组成:(i)核糖或其衍生物;和(ii)与之结合的核碱基,使碱基配对部分的顺序通过watson-crick碱基配对形成与核酸(通常是rna)中的靶序列互补的碱基序列,以在靶序列内形成核酸:寡聚物异源双链体,条件是亚基、亚基间键或两者都不是天然存在的。在某些实施例中,反义寡聚物是pmo。在其它实施例中,反义寡聚物是2'-o-甲基硫代磷酸酯。在其它实施例中,本公开的反义寡聚物是肽核酸(pna)、锁核酸(lna)或桥接核酸(bna),如2'-o,4'-c-乙烯桥接核酸(ena)。本文中描述了另外的示例性实施例。
[0089]
术语“互补”和“互补性”是指通过watson-crick碱基配对规则彼此相关的两个或更多个寡聚物(即,每个包含核碱基序列)。例如,核碱基序列“t-g-a(5'
→
3')”与核碱基序列“a-c-t(3'
→
5')”互补。互补性可以是“部分的”,其中根据碱基配对规则,给定核碱基序列的不到全部核碱基与另一核碱基序列匹配。例如,在一些实施例中,给定核碱基序列与另一核碱基序列之间的互补性可以是约70%、约75%、约80%、约85%、约90%或约95%。或者,给定核碱基序列和另一核碱基序列之间可能存在“完全”或“完美”(100%)互补性,以继续实例。核碱基序列之间的互补程度对序列之间杂交的效率和强度有显著影响。
[0090]
术语“有效量”和“治疗有效量”在本文中可互换使用,并指作为单剂量或作为一系列剂量的一部分施用于哺乳动物受试者的治疗化合物如反义寡聚物的量,其可有效地产生期望的治疗效果。对于反义寡聚物,这种效果通常是通过抑制所选靶序列的翻译或天然剪接加工,或产生临床上有意义量的肌营养不良蛋白(统计显著性)而带来的。
[0091]
在一些实施例中,有效量是至少10mg/kg或至少20mg/kg的包括反义寡聚物的组合物,以治疗受试者一段时间。在一些实施例中,有效量是至少20mg/kg的包括反义寡聚物的组合物,以将受试者中的肌营养不良蛋白阳性纤维的数量增加到正常的至少20%。在某些实施例中,有效量是10mg/kg或至少至少20mg/kg的包括反义寡聚物的组合物,以稳定、维持或改善患者相对于健康同伴的步行距离,例如在6mwt中的20%缺陷。在各种实施例中,有效量是至少10mg/kg至约30mg/kg,至少20mg/kg至约30mg/kg,约25mg/kg至约30mg/kg,或约30mg/kg至约50mg/kg。在一些实施例中,有效量是约10mg/kg、约20mg/kg、约30mg/kg或约50mg/kg。在另一方面,有效量是至少约10mg/kg、约20mg/kg、约25mg/kg、约30mg/kg或约30mg/kg至约50mg/kg,持续至少24周、至少36周或至少48周,从而将受试者中的肌营养不良蛋白阳性纤维的数量增加到正常的至少20%、约30%、约40%、约50%、约60%、约70%、约80%、约90%、约95%,并稳定或改善患者相对于健康同伴的步行距离,例如在6mwt中的20%缺陷。在一些实施例中,治疗将患者中的肌营养不良蛋白阳性纤维的数量增加到正常的20-60%或30-50%。
[0092]“增强(enhance/enhancing)”或“增加(increase/increasing)”或“刺激(stimulate/stimulating)”一般是指一种或多种反义寡聚物或反义寡聚物缀合物或上述
任何一种的药物组合物在细胞或受试者中产生或引起更大的生理反应(即下游效应)的能力,与没有反义寡聚物、没有反义寡聚物缀合物或对照化合物引起的反应相比。更大的生理反应可包括增加肌营养不良蛋白的功能形式的表达,或增加肌肉组织中肌营养不良蛋白相关的生物活性,以及根据本领域的理解和本文的描述显而易见的其它反应。还可以测量肌肉功能的增加,包括肌肉功能增加或改善约1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或100%。也可以测量表达功能性肌营养不良蛋白的肌肉纤维的百分比,包括在约1%、2%、5%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或100%的肌肉纤维中增加肌营养不良蛋白的表达。例如,已经表明,如果25-30%的纤维表达肌营养不良蛋白,则大约40%的肌肉功能改善可以发生(参见例如dellorusso等人,《美国国家科学院院刊(proc natl acad sci usa)》99:12979-12984,2002)。“增加”或“增强”的量通常是“统计学上显著”的量,可以包括增加1.1、1.2、2、3、4、5、6、7、8、9、10、15、20、30、40、50或更多倍(例如,500、1000倍,包括介于1和大于1的所有整数和小数点),例如,1.5、1.6、1.7、1.8等)由不存在药剂(无反义寡聚物或反义寡聚物缀合物)或对照化合物产生的量。
[0093]
如本文所用,术语“功能”和“功能性”等是指生物、酶或治疗功能。
[0094]“功能性”肌营养不良蛋白一般是指具有足够生物活性的肌营养不良蛋白,以减少肌肉组织的进行性降解,这原本是肌营养不良的特征,通常与存在于某些dmd或bmd受试者中的改变的或“缺陷”形式的肌营养不良蛋白相比。在某些实施例中,功能性肌营养不良蛋白可以具有野生型肌营养不良蛋白的体外或体内生物活性的约10%、20%、30%、40%、50%、60%、70%、80%、90%或100%(包括介于两者之间的所有整数),根据本领域中的常规技术测量。作为一个实例,体外肌肉培养物中的肌营养不良蛋白相关活性可以根据肌管大小、肌原纤维组织(或无组织)、收缩活性和乙酰胆碱受体的自发聚集来测量(参见例如棕色等人,《细胞科学杂志(journal of cell science.)》112:209-216,1999)。动物模型也是研究疾病发病机理的宝贵资源,并提供了测试肌营养不良蛋白相关活性的手段。两个最广泛使用的dmd研究动物模型是mdx小鼠和金毛猎犬肌营养不良(grmd)狗,它们都是肌营养不良蛋白阴性的(参见例如collins和morgan,《国际实验病理学杂志(int j exp pathol)》84:165-172,2003)。这些和其它动物模型可用于测量各种肌营养不良蛋白的功能活性。包括肌营养不良蛋白的截短形式,例如在施用本公开的某些外显子跳跃反义寡聚物或反义寡聚物缀合物之后产生的那些形式。
[0095]
术语“错配”或“不匹配”是指寡聚物核碱基序列中的一个或多个核碱基(无论是连续的还是分开的)根据碱基配对规则与靶前体mrna不匹配。虽然通常需要完美的互补性,但一些实施例可以包括一个或多个但优选6、5、4、3、2或1个相对于靶前体mrna的错配。在寡聚物内任何位置的变异都包括在内。在某些实施例中,本公开的反义寡聚物和反义寡聚物缀合物包括内部末端变化附近的核碱基序列的变化,并且如果存在,通常在5'和/或3'末端的约6、5、4、3、2或1个亚基内。
[0096]
术语“吗啉代”、“吗啉代寡聚物”和“pmo”是指具有以下通用结构的磷酰二胺吗啉代寡聚物:
[0097][0098]
并且如summerton,j.等人,《反义与核酸药物开发(antisense&nucleic acid drug development)》,7:187-195(1997)的图2中所述。本文所述的吗啉代包括前述通用结构的所有立体异构体和互变异构体。吗啉代寡聚物的合成、结构和结合特征详述于美国专利号:5,698,685;5,217,866;5,142,047;5,034,506;5,166,315;5,521,063;5,506,337;8,076,476;和8,299,206;所有这些专利都以引用的方式并入本文中。
[0099]
在某些实施例中,吗啉代在寡聚物的5'或3'端与“尾部”部分缀合以增加其稳定性和/或溶解性。示例性尾部包括:
[0100][0101]
在上文示例性尾部部分中,“teg”或“eg3”是指以下尾部部分:
[0102][0103]
在上文示例性尾部部分中,“gt”是指以下尾部部分:
[0104][0105]
如本文所用,术语
“-
g-r
6”和
“-
g-r
6-ac”可互换使用,并且指与本公开的反义寡聚物缀合的肽部分。在各种实施例中,“g”代表通过酰胺键与“r
6”缀合的甘氨酸残基,并且每个“r”代表通过酰胺键缀合在一起的精氨酸残基,使得“r
6”表示通过酰胺键缀合在一起的六(6)个精氨酸残基。精氨酸残基可以具有任何立体构型,例如,精氨酸残基可以是l-精氨酸残基、d-精氨酸残基或d-和l-精氨酸残基的混合物。在某些实施例中,
“-
g-r
6”或
“-
g-r
6-ac”与本公开的pmo反义寡聚物的3'最末端吗啉代亚基的吗啉环氮缀合。在一些实施例中,
“-
g-r
6”或
“-
g-r
6-ac”与本公开的反义寡聚物的3'端缀合,并且具有下式:
[0106][0107]
术语“核碱基”(nu)、“碱基配对部分”或“碱基”可互换使用,指天然存在的或“天然”dna或rna(例如尿嘧啶、胸腺嘧啶、腺嘌呤、胞嘧啶和鸟嘌呤)中发现的嘌呤或嘧啶碱基,以及这些天然存在的嘌呤和嘧啶的类似物。这些类似物可赋予寡聚物改进的特性,例如结合亲和力。示例性的类似物包括次黄嘌呤(肌苷的基础成分);2,6-二氨基嘌呤;5-甲基胞嘧啶;c5-丙炔基修饰的嘧啶;10-(9-(氨基乙氧基)苯噁嗪基)(g-钳)等。
[0108]
碱基配对部分的其它实例包括但不限于尿嘧啶、胸腺嘧啶、腺嘌呤、胞嘧啶、鸟嘌呤和次黄嘌呤(肌苷),它们各自的氨基基团由酰基保护基团保护,2-氟尿嘧啶、2-氟胞嘧
啶、5-溴尿嘧啶、5-碘尿嘧啶、2,6-二氨基嘌呤、氮杂胞嘧啶、嘧啶类似物如假异胞嘧啶和假尿嘧啶以及其它修饰的核碱基,如8-取代的嘌呤、黄嘌呤或次黄嘌呤(后两者为天然降解产物)。还考虑了以下所公开的修饰的核碱基:chiu和rana,《rna》,2003,9,1034-1048;limbach等人《核酸研究》,1994,22,2183-2196;以及revankar和rao,《综合天然产物化学(comprehensive natural products chemistry)》,第7卷,313,其内容以引用的方式并入本文中。
[0109]
碱基配对部分的其它实例包括但不限于其中已添加一个或多个苯环的大小扩大的核碱基。核酸碱基替代物描述于:glen research目录(www.glenresearch.com);kruegerat等人,《化学研究述评(acc.chem.res.)》,2007,40,141-150;kool,et,《化学研究述评》,2002,35,936-943;benner s.a.等人,《自然综述遗传学(nat.rev.genet.)》,2005,6,553-543;romesberg,f.e.等人,《化学生物学新见(curr.opin.chem.biol.)》,2003,7,723-733;和hirao,i.,《化学生物学新见》2006,10,622-627;其内容以引用的方式并入本文中,预期可用于本文所述的反义寡聚物和反义寡聚物缀合物。大小扩大的核碱基的实例包括以下所示的核碱基及其互变异构形式。
[0110][0111]
本文所用的短语“肠胃外施用(parenteral administration/administered parenterally)”是指除肠内和局部施用以外的施用方式,通常通过注射,并且包括但不限于静脉内、肌肉内、动脉内、鞘内、囊内、眶内、心内、皮内、腹膜内、经气管、皮下、表皮下、关
节内、囊下、蛛网膜下、脊柱内和胸骨内注射和输注。
[0112]
为了清楚起见,包括例如式(iv)在内的本公开的结构从5'到3'是连续的,并且为了方便以紧凑的形式描绘整个结构,已经包括标有“断点a”、“断点b”和“断点c”的各种说明断点。如熟练的技术人员所理解的那样,例如,“断点a”的每个指示显示了在这些点处的结构的图示的接续。熟练的技术人员理解,对于上述结构中的“断点b”和“断点c”的每个实例也是如此。然而,这些图示断点均无意于表明,熟练的技术人员也不会将其理解为意味着上述结构的实际中断。
[0113]
如本文所用,在结构式中使用的一组括号表示括号之间的结构特征是重复的。在一些实施例中,使用的括号可以是“[”和“]”,在某些实施例中,用于表示重复的结构特征的括号可以是“(”和“)”。在一些实施例中,括号之间的结构特征的重复迭代次数为括号外指示的次数,如2、3、4、5、6、7等。在各种实施例中,括号之间的结构特征的重复迭代次数由括号外指示的变量如“z”指示。
[0114]
如本文所用,在结构式内绘制到手性碳或磷原子的直键或波状键表示手性碳或磷的立体化学是未定义的,旨在包括手性中心的所有形式和/或其混合物。下面描绘了这类图示的实例。
[0115][0116]
短语“药学上可接受的”是指物质或组合物必须在化学和/或毒理学上与构成制剂的其它成分和/或用其治疗的受试者相容。
[0117]
本文所用的短语“药学上可接受的载体”是指无毒的、惰性的固体、半固体或液体填充剂、稀释剂、囊封材料或任何类型的配制助剂。可以充当药学上可接受的载体的材料的一些实例是糖类,如乳糖、葡萄糖和蔗糖;淀粉,如玉米淀粉和马铃薯淀粉;纤维素及其衍生物,如羧甲基纤维素钠、乙基纤维素和乙酸纤维素;粉状黄蓍;麦芽;明胶;滑石;赋形剂,如可可脂和栓剂蜡;油,如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;二醇,如丙二醇;酯,如油酸乙酯和月桂酸乙酯;琼脂;缓冲剂,如氢氧化镁和氢氧化铝;海藻酸;无热原质水;等渗盐水;林格氏溶液;乙醇;磷酸盐缓冲溶液;无毒相容润滑剂,如月桂基硫酸钠和硬脂酸镁;着色剂;脱模剂;涂布剂;甜味剂;调味剂;芳香剂;防腐剂和抗氧化剂;根据配方师的判断。
[0118]
关于肌营养不良蛋白合成或生产的术语“恢复”一般是指用本文所述的反义寡聚物或反义寡聚物缀合物治疗后,肌营养不良的患者产生肌营养不良蛋白,包括截短形式的肌营养不良蛋白。在一些实施例中,治疗导致患者中新型肌营养不良蛋白的产生增加1%、5%、10%、20%、30%、40%、50%、60%、70%、80%、90%或100%(包括两者之间的所有整数)。在一些实施例中,治疗将受试者中肌营养不良蛋白阳性纤维的数量增加到正常的至少
约20%、约30%、约40%、约50%、约60%、约70%、约80%、约90%或约95%至100%。在其它实施例中,治疗将受试者中肌营养不良蛋白阳性纤维的数量增加到正常的约20%至约60%或约30%至约50%。治疗后患者中肌营养不良蛋白阳性纤维的百分比可通过肌肉活检使用已知技术确定。例如,可从合适的肌肉,如患者的肱二头肌中取肌肉活检。
[0119]
阳性肌营养不良蛋白纤维的百分比分析可在治疗前和/或治疗后或在整个治疗过程中的时间点进行。在一些实施例中,治疗后活检取自治疗前活检的对侧肌肉。治疗前和治疗后的肌营养不良蛋白表达分析可以使用任何合适的肌营养不良蛋白检测法进行。在一些实施例中,使用作为肌营养不良蛋白的标志物的抗体,例如单克隆或多克隆抗体,对来自肌肉活检的组织切片进行免疫组织化学检测。例如,可以使用mandys106抗体,其是肌营养不良蛋白的高度敏感标志物。可以使用任何合适的二抗。
[0120]
在一些实施例中,肌营养不良蛋白阳性纤维的百分比通过将阳性纤维的数量除以计数的总纤维来计算。正常的肌肉样品具有100%的肌营养不良蛋白阳性纤维。因此,肌营养不良蛋白阳性纤维的百分比可以表示为正常的百分比。为了控制治疗前肌肉以及回复性纤维中痕量肌营养不良蛋白的存在,在计数治疗后肌肉中的肌营养不良蛋白阳性纤维时,可以使用患者治疗前肌肉的切片设置基线。这可以用作计数该患者治疗后肌肉的切片中的肌营养不良蛋白阳性纤维的阈值。在其它实施例中,抗体染色的组织切片也可以用于使用bioquant图像分析软件(bioquant image analysis corporation,nashville,tn)进行肌营养不良蛋白定量。总肌营养不良蛋白荧光信号强度可报告为正常的百分比。此外,使用单克隆或多克隆抗肌营养不良蛋白抗体的蛋白质印迹分析可用于确定肌营养不良蛋白阳性纤维的百分比。例如,可以使用来自leica biosystems的抗肌营养不良蛋白抗体ncl-dys1。还可以通过确定肌聚糖复合物(β,γ)和/或神经元nos的组分的表达来分析肌营养不良蛋白阳性纤维的百分比。
[0121]
在一些实施例中,用本公开的反义寡聚物或反义寡聚物缀合物进行的治疗减缓或减少了dmd患者的进行性呼吸肌功能障碍和/或衰竭,这在没有治疗的情况下是可以预期的。在一些实施例中,用本公开的反义寡聚物或反义寡聚物缀合物进行的治疗可以减少或消除对通气辅助的需要,而这种需要在没有治疗的情况下是可以预期的。在一些实施例中,用于跟踪疾病过程的呼吸功能测量以及潜在治疗干预的评估包括最大吸气压力(mip)、最大呼气压力(mep)和用力肺活量(fvc)。mip和mep分别测量一个人在吸气和呼气期间可能产生的压力水平,并且是呼吸肌力量的敏感测量。mip是对膈膜肌无力的量度。
[0122]
在一些实施例中,mep可能在其它肺功能测试(包括mip和fvc)变化之前下降。在某些实施例中,mep可以是呼吸功能障碍的早期指标。在某些实施例中,fvc可用于测量最大吸气后强制呼气期间排出的空气总量。在dmd患者中,fvc与身体生长同时增加,直到十几岁初期。然而,随着生长减缓或因疾病进展而受阻,以及肌肉无力的进展,肺活量进入下降阶段,并在10至12岁后以平均每年约8至8.5%的速度下降。在某些实施例中,mip百分比预测(mip根据体重调整)、mep百分比预测(mep根据年龄调整)和fvc百分比预测(fvc根据年龄和身高调整)是支持性分析。
[0123]
如本文所用,术语“受试者”和“患者”包括表现出症状或有表现出症状风险的任何动物,所述症状可以用本公开的反义寡聚物或反义寡聚物缀合物进行治疗,例如患有或有风险患有dmd或bmd或与这些病况相关的任何症状(例如肌纤维丧失)的受试者(或患者)。合
适的受试者(或患者)包括实验室动物(如小鼠、大鼠、兔子或豚鼠)、农场动物和家畜或宠物(如猫或狗)。包括非人类的灵长类动物和优选人类患者(或受试者)。还包括在具有适合于外显子51跳跃的肌营养不良蛋白基因突变的受试者(或患者)中产生肌营养不良蛋白的方法。
[0124]
本文所用的短语“全身施用(systemic administration/administered systemically)”和“外周施用(peripheral administration/administered peripherally)”是指除直接进入中枢神经系统以外的化合物、药物或其它材料的施用,使其进入患者的系统,从而经历代谢和其他类似过程,例如皮下施用。
[0125]
短语“靶向序列”是指与靶前体mrna中的核苷酸序列互补的寡聚物的核碱基序列。在本公开的一些实施例中,靶前体mrna中的核苷酸序列是指定为h52a(-01+24)的肌营养不良蛋白前体mrna中的外显子52退火位点。
[0126]
对受试者(例如哺乳动物,如人类)或细胞的“治疗”是试图改变受试者或细胞的自然进程而使用的任何类型的干预。治疗包括但不限于施用寡聚物或其药物组合物,并且可以预防性地或在病理事件开始后或与病原体接触后进行。治疗包括对与肌营养不良蛋白相关的疾病或病况的症状或病理的任何理想效果,如在某些形式的肌营养不良中,并且可以包括例如在所治疗的疾病或病况的一个或多个可测量的标志物中的最小变化或改善。还包括“预防性”治疗,其可以针对降低正在治疗的疾病或病况的进展速率,延迟该疾病或病况的发作,或降低其发作的严重性。“治疗”或“预防”不一定表示完全根除、治愈或预防疾病或病况或其相关症状。
[0127]
在一些实施例中,用本公开的反义寡聚物或反义寡聚物缀合物进行治疗增加新型肌营养不良蛋白的产生,延缓疾病进展,减缓或减少行走能力的丧失,减少肌肉炎症,减少肌肉损伤,改善肌肉功能,减少肺功能的丧失,和/或增强肌肉再生,这在没有治疗的情况下是可以预期的。在一些实施例中,治疗维持、延缓或减缓疾病进展。在一些实施例中,治疗维持行走能力或减少行走能力的丧失。在一些实施例中,治疗维持肺功能或减少肺功能的丧失。在一些实施例中,治疗维持或增加患者的稳定步行距离,如通过6分钟步行测试(6mwt)测量。在一些实施例中,治疗维持或减少步行/跑步10米的时间(即,10米步行/跑步测试)。在一些实施例中,治疗维持或减少从仰卧位站立的时间(即,站立时间测试)。在一些实施例中,治疗维持或减少爬四层标准楼梯的时间(即,四层楼梯爬升测试)。在一些实施例中,治疗维持或减少患者的肌肉炎症,如通过例如mri(例如,腿部肌肉的mri)测量。在一些实施例中,mri测量t2和/或脂肪分数以识别肌肉退化。mri可以识别由炎症、水肿、肌肉损伤和脂肪浸润引起的肌肉结构和组成的变化。
[0128]
在一些实施例中,用本公开的反义寡聚物或反义寡聚物缀合物进行治疗增加新型肌营养不良蛋白的产生,并减缓或减少在没有治疗的情况下预期的行走能力的丧失。例如,治疗可以稳定、维持、改善或增加受试者的行走能力(例如,步行的稳定)。在一些实施例中,治疗维持或增加患者的稳定步行距离,如通过mcdonald等人描述的6分钟步行测试(6mwt)测量(《肌肉神经(muscle nerve)》,2010;42:966-74,以引用的方式并入本文中)。6分钟步行距离(6mwd)的变化可以表示为绝对值、百分比变化或%预测值的变化。在一些实施例中,治疗维持或改善受试者相对于健康同伴的20%缺陷的6mwt中的稳定步行距离。可以通过计算%预测值来确定6mwt中相对于健康同伴的典型表现的dmd患者的表现。例如,对于男
性,%预测的6mwd可以使用以下公式计算:196.72+(39.81
×
年龄)-(1.36
×
年龄2)+(132.28
×
身高(米))。对于女性,%预测的6mwd可以使用以下公式计算:188.61+(51.50
×
年龄)-(1.86
×
年龄2)+(86.10
×
身高(米))(henricson等人《公共科学图书馆潮流(plos curr.)》,2012,第2版,以引用的方式并入本文中)。在一些实施例中,用反义寡聚物进行治疗使患者的稳定步行距离从基线增加到大于3、5、6、7、8、9、10、15、20、25、30或50米(包括两者之间的所有整数)。
[0129]
dmd患者的肌肉功能丧失可能发生在儿童期正常生长发育的背景下。事实上,尽管进行性肌肉损伤,但患有dmd的较年幼的儿童在大约1年的过程中可能会在6mwt期间显示出步行距离的增加。在一些实施例中,将来自dmd患者的6mwd与典型发育的对照受试者和来自年龄和性别匹配的受试者的现有正常数据进行比较。在一些实施例中,可以使用基于年龄和身高的方程拟合到正常数据中来说明正常的生长和发育。这样的方程可用于将6mwd转换为dmd受试者的百分比预测值(%预测值)。在某些实施例中,对%预测的6mwd数据的分析代表了一种解释正常生长和发育的方法,并且可以显示在早期年龄(例如,小于或等于7岁)的功能获得代表dmd患者的稳定而不是改善能力(henricson等人《公共科学图书馆潮流》,2012,第2版,以引用的方式并入本文中)。
[0130]
提出并公开了一种反义分子命名系统,以区分不同的反义分子(参见mann等人,(2002)《基因医学杂志(j gen med)》4,644-654)。当测试几种稍有不同的反义分子时,这种命名法变得特别贴切,这些反义分子都针对同一靶区,如下所示:
[0131]
h#a/d(x:y)。
[0132]
第一个字母表示物种(例如h:人类,m:鼠类,c:犬类)。“#”表示目标肌营养不良蛋白外显子编号。“a/d”分别表示外显子起始和末端的受体或供体剪接位点。(x y)表示退火坐标,其中
“-”
或“+”分别表示内含子或外显子的序列。例如,a(-6+18)将表示目标外显子之前的内含子的最后6个碱基和目标外显子的前18个碱基。最近的剪接位点将是受体,所以这些坐标将以“a”开头。描述供体剪接位点的退火坐标可以是d(+2-18),其中最后2个外显子碱基和前18个内显子碱基对应于反义分子的退火位点。完全外显子的退火坐标将用a(+65+85)表示,即从该外显子开始的第65和85个核苷酸之间的位点。
[0133]
ii.反义寡聚物
[0134]
a.设计用于诱导外显子52跳跃的反义寡聚物和反义寡聚物缀合物
[0135]
在某些实施例中,本公开的反义寡聚物和反义寡聚物缀合物与肌营养不良蛋白基因的外显子52靶区互补,并诱导外显子52跳跃。特别是,本公开涉及与指定为退火位点的肌营养不良蛋白前体mrna的外显子52靶区互补的反义寡聚物和反义寡聚物缀合物。在一些实施例中,退火位点是h52a(-01+24)。
[0136]
本公开的反义寡聚物和反义寡聚物缀合物靶向肌营养不良蛋白前体mrna并诱导外显子52的跳跃,因此其从成熟的剪接的mrna转录物中被排除或跳过。通过跳跃外显子52,将被破坏的阅读框恢复为框内突变。虽然dmd由各种遗传亚型构成,但本公开的反义寡聚物和反义寡聚物缀合物被特别设计为跳跃肌营养不良蛋白前体mrna的外显子52。适合于跳跃外显子52的dmd突变包含dmd患者的一个亚组(8%)。
[0137]
诱导外显子52跳跃的反义寡聚物或反义寡聚物缀合物的核碱基序列被设计为与肌营养不良蛋白前体mrna的外显子52内的特定靶序列互补。在一些实施例中,反义寡聚物
或反义寡聚物缀合物的反义寡聚物是pmo,其中pmo的每个吗啉代环与核碱基相连,包括例如dna中发现的核碱基(腺嘌呤、胞嘧啶、鸟嘌呤和胸腺嘧啶)。
[0138]
b.寡聚物化学特征
[0139]
本公开的反义寡聚物和反义寡聚物缀合物可以采用多种反义寡聚物化学物质。寡聚物化学物质的实例包括但不限于吗啉代寡聚物、硫代磷酸酯修饰的寡聚物、2'o-甲基修饰的寡聚物、肽核酸(pna)、锁核酸(lna)、硫代磷酸酯寡聚物、2'o-moe修饰的寡聚物、2'-氟修饰的寡聚物、2'o,4'c-乙烯桥接核酸(ena)、三环dna、三环dna硫代磷酸酯亚基、2'-o-[2-(n-甲基氨甲酰基)乙基]修饰的寡聚物,包括上述任何一种的组合。硫代磷酸酯和2'-o-me修饰的化学物质可以组合生成2'o-me-硫代磷酸酯主链。参见例如pct公开号wo/2013/112053和wo/2009/008725,其均以全文引用的方式并入本文中。下文进一步描述了本公开的寡聚物化学物质的示例性实施例。
[0140]
1.肽核酸(pna)
[0141]
肽核酸(pna)是dna的类似物,其主链在结构上与脱氧核糖主链同形,由n-(2-氨基乙基)甘氨酸单元组成,嘧啶或嘌呤碱基与之相连。含有天然嘧啶和嘌呤碱基的pna与遵循watson-crick碱基配对规则的互补寡聚物杂交,并在碱基对识别方面模拟dna(egholm,buchardt等人1993)。pna的主链是由肽键而不是磷酸二酯键形成的,这使得它们非常适合于反义应用(参见下面的结构)。主链不带电,导致pna/dna或pna/rna双螺旋体表现出大于正常的热稳定性。pna不被核酸酶或蛋白酶识别。下面描绘了pna的非限制性实例。
[0142][0143]
尽管天然结构发生了根本的结构变化,但pna能够以螺旋形式与dna或rna进行序列特异性结合。pna的特征包括对互补dna或rna的高结合亲和力,由单碱基错配引起的去稳定化作用,对核酸酶和蛋白酶的抗性,与dna或rna的杂交不依赖于盐浓度,以及与同型嘌呤dna形成三螺旋体。panagene
tm
已开发出其专有的bts pna单体(bts;苯并噻唑-2-磺酰基)和专有的寡聚化工艺。使用bts pna单体进行的pna寡聚化是由脱保护、偶合和封端的重复循环构成。pna可以使用本领域已知的任何技术合成生产。参见例如美国专利号:6,969,766;
7,211,668;7,022,851;7,125,994;7,145,006;和7,179,896。另见美国专利号:5,539,082;5,714,331;和5,719,262,用于制备pna。pna化合物的进一步教导可见于nielsen等人,《科学(science)》,254:1497-1500,1991。以上各项以全文引用的方式并入。
[0144]
2.锁核酸(lna)
[0145]
反义寡聚物和反义寡聚物缀合物也可以含有“锁核酸”亚基(lna)。“lna”是一类称为桥接核酸(bna)的修饰的成员。bna的特征在于将核糖环的构象锁定在c30-内(北)糖褶中的共价键。对于lna来说,桥是由2'-o和4'-c位置之间的亚甲基构成。lna增强了主链预组织和碱基堆积,以提高杂交和热稳定性。
[0146]
lna的结构可见于例如wengel等人,《化学通讯(chemical communications)》(1998)455;koshkin等人,《四面体(tetrahedron)》(1998)54:3607;jesper wengel,《化学研究述评》(1999)32:301;obika等人,《四面体快报(tetrahedron letters)》(1997)38:8735;obika等人,《四面体快报》(1998)39:5401;和obika等人,《生物有机医药化学(bioorganic medicinal chemistry)》(2008)16:9230,其以全文引用的方式并入本文中。下面描绘了lna的非限制性实例。
[0147][0148]
本公开的反义寡聚物和反义寡聚物缀合物可以掺入一个或多个lna;在某些情况下,反义寡聚物和反义寡聚物缀合物可以完全由lna构成。合成个别lna核苷亚基并将其掺入寡聚物中的方法描述于例如美国专利号:7,572,582;7,569,575;7,084,125;7,060,809;7,053,207;7,034,133;6,794,499;和6,670,461中;其中每一个均以全文引用的方式并入。典型的亚基间连接基团包括磷酸二酯和硫代磷酸酯部分;或者,可以采用不含磷的连接基团。其它实施例包括含有lna的反义寡聚物或反义寡聚物缀合物,其中每个lna亚基被dna亚基分开。某些反义寡聚物和反义寡聚物缀合物由交替的lna和dna亚基构成,其中亚基间连接基团是硫代磷酸酯。
[0149]
2'o,4'c-乙烯桥接核酸(ena)是bna类的另一成员。下面描绘非限制性实例。
[0150][0151]
ena寡聚物及其制备描述于obika等人,《四面体快报》(1997)38(50):8735中,其以全文引用的方式并入本文中。本公开的反义寡聚物和反义寡聚物缀合物可以掺入一个或多个ena亚基。
[0152]
3.解锁核酸(una)
[0153]
反义寡聚物和反义寡聚物缀合物也可以含有解锁核酸(una)亚基。una和una寡聚物是rna的类似物,其中亚基的c2'-c3'键已被裂解。虽然lna是构象受限的(相对于dna和rna),但una是非常灵活的。例如,wo 2016/070166中公开了una。下面描绘了una的非限制性实例。
[0154][0155]
典型的亚基间连接基团包括磷酸二酯和硫代磷酸酯部分;或者,可以采用不含磷的连接基团。
[0156]
4.硫代磷酸酯
[0157]“硫代磷酸酯”(或s-寡核苷酸)是正常dna的变体,其中一个非桥接氧被硫取代。下面描绘了硫代磷酸酯的非限制性实例。
[0158][0159]
核苷酸间键的硫化减少了核酸内切酶和核酸外切酶的作用,包括5'至3'和3'至5'dna pol 1核酸外切酶、核酸酶s1和p1、rna酶、血清核酸酶和蛇毒磷酸二酯酶。硫代磷酸酯通过两种主要途径制备:通过元素硫在二硫化碳中的溶液对膦酸氢盐的作用,或通过用二硫化四乙基秋兰姆(tetd)或3h-1,2-苯并二硫醇-3-酮1,1-二氧化物(bdtd)使亚磷酸三酯硫化的方法(参见例如iyer等人,《有机化学杂志(j.org.chem.)》55,4693-4699,1990,其以全文引用的方式并入本文中)。后一种方法避免了元素硫在大多数有机溶剂中的不溶性和二硫化碳的毒性问题。tetd法和bdtd法也能产生纯度较高的硫代磷酸酯。
[0160]
5.三环dna和三环硫代磷酸酯亚基
[0161]
三环dna(tc-dna)是一类受约束的dna类似物,其中每个核苷酸通过引入环丙烷环进行修饰,以限制主链的构象灵活性,并优化扭转角γ的主链几何结构。含同型碱基腺嘌呤和胸腺嘧啶的tc-dna与互补rna形成异常稳定的a-t碱基对。三环dna及其合成描述于国际专利申请公开号wo 2010/115993中,其以全文引用的方式并入本文中。本公开的反义寡聚物和反义寡聚物缀合物可以掺入一个或多个三环dna亚基;在某些情况下,反义寡聚物和反义寡聚物缀合物可以完全由三环dna亚基构成。
[0162]
三环硫代磷酸酯亚基是具有硫代磷酸酯亚基间键的三环dna亚基。三环硫代磷酸酯亚基及其合成描述于国际专利申请公开号wo 2013/053928中,其以全文引用的方式并入本文中。本公开的反义寡聚物和反义寡聚物缀合物可以掺入一个或多个三环dna亚基;在某些情况下,反义寡聚物和反义寡聚物缀合物可以完全由三环dna亚基构成。下面描绘了三环dna/三环硫代磷酸酯亚基的非限制性实例。
[0163][0164]
6.2'o-甲基、2'o-moe和2'-f寡聚物
[0165]“2'-o-me寡聚物”分子在核糖分子的2'-oh残基处携带甲基。2'-o-me-rna表现出
与dna相同(或相似)的行为,但防止核酸酶降解。2'-o-me-rna也可以与硫代磷酸酯寡聚物(pto)组合以进一步稳定。2'o-me寡聚物(磷酸二酯或硫代磷酸酯)可以根据本领域的常规技术合成(参见例如yoo等人,《核酸研究》32:2008-16,2004,其以全文引用的方式并入本文中)。下面描绘了2'o-me寡聚物的非限制性实例。
[0166][0167]
2'o-甲氧基乙基寡聚物(2'-o moe)在核糖分子之2'-oh残基处携带甲氧基乙基,且论述于martin等人,《瑞士化学学报(helv.chim.acta)》,78,486-504,1995中,其以全文引用的方式并入本文中。下面描绘了2'o moe亚基的非限制性实例。
[0168][0169]
2'-氟(2'-f)寡聚物在2'位置处具有氟基代替2'oh。下面描绘了2'-f寡聚物的非限制性实例。
[0170][0171]
2'-氟寡聚物进一步描述于wo 2004/043977中,其以全文引用的方式并入本文中。
[0172]
2'o-甲基、2'o-moe和2'-f寡聚物还可包含一个或多个硫代磷酸酯(ps)键,如下所示。
[0173][0174]
此外,2'o-甲基、2'o-moe和2'-f寡聚物可以在整个寡聚物中包含ps亚基间键,例如,如下面描绘的2'o-甲基ps寡聚物敦沙普森(drisapersen)。
[0175][0176]
或者,2'o-甲基、2'o-moe和/或2'-f寡聚物可以在寡聚物的末端包含ps键,如下所示。
[0177][0178]
其中:
[0179]
r是ch2ch2och3(甲氧基乙基或moe);以及
[0180]
x、y和z分别表示在指定的5'-侧翼、中央间隙和3'-侧翼区域中的每个区域内包含的核苷酸数目。
[0181]
本公开的反义寡聚物和反义寡聚物缀合物可以掺入一个或多个2'o-甲基、2'o-moe和2'-f亚基,并且可以利用本文所述的任何亚基间键。在某些情况下,本公开的反义寡聚物或和反义寡聚物缀合物可以完全由2'o-甲基、2'o-moe或2'-f亚基构成。本公开的反义寡聚物或反义寡聚物缀合物的一个实施例完全由2'o-甲基亚基构成。
[0182]
7.2'-o-[2-(n-甲基氨甲酰基)乙基]寡聚物(mce)
[0183]
mce是可用于本公开的反义寡聚物和反义寡聚物缀合物的2'o修饰的核糖核苷的另一个实例。此处,2'oh被衍生为2-(n-甲基氨甲酰基)乙基部分,以增加核酸酶抗性。下面描绘了mce寡聚物的非限制性实例。
[0184][0185]
mce及其合成描述于yamada等人,《有机化学杂志》(2011)76(9):3042-53中,其以全文引用的方式并入本文中。本公开的反义寡聚物和反义寡聚物缀合物可以掺入一个或多个mce亚基。
[0186]
9.2'-o-nma寡聚物
[0187][0188]
9.立体特异性寡聚物
[0189]
立体特异性寡聚物是指通过合成方法固定每个含磷键的立体化学从而产生基本上立体纯的寡聚物的那些寡聚物。下面描绘了立体特异性寡聚物的非限制性实例。
[0190][0191]
在以上实例中,寡聚物的每个磷具有相同的立体构型。另外的实例包括上述的寡聚物。例如,lna、ena、三环dna、mce、2'o-甲基、2'o-moe、2'-f和吗啉代基寡聚物可以用立体特异性的含磷核苷间键,例如硫代磷酸酯、磷酸二酯、氨基磷酸酯、二氨基磷酸酯或其它含磷核苷间键来制备。立体特异性寡聚物、用于制备这类寡聚物的制备方法、手性控制合成、手性设计和手性助剂详述于例如wo2017192664、wo2017192679、wo2017062862、wo2017015575、wo2017015555、wo2015107425、wo2015108048、wo2015108046、wo2015108047、wo2012039448、wo2010064146、wo2011034072、wo2014010250、wo2014012081、wo20130127858和wo2011005761中,其中每一个都以全文引用的方式并入本文中。
[0192]
立体特异性寡聚物可以具有r
p
或s
p
构型的含磷核苷间键。键的立体构形受控的手性含磷键被称为“立体纯”,而键的立体构形不受控制的手性含磷键被称为“立体无规”。在某些实施例中,本公开的寡聚物包含多个立体纯和立体无规键,使得所得寡聚物在寡聚物的预指定位置具有立体纯亚基。在国际专利申请公开号wo 2017/062862 a2的图7a和7b中提供了立体纯亚基的位置的实例。在一个实施例中,寡聚物中的所有手性含磷键都是立体无规的。在一个实施例中,寡聚物中的所有手性含磷键都是立体纯的。
[0193]
在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物中的所有n个手性含磷键都是立体无规的。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物中的所有n个手性含磷键都是立体纯的。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物中的n个含磷键中的至少10%(至最接近的整数)是立体纯的。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物中的n个含磷键中的至少20%(至最接近的整数)是立体纯的。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物中的n个含磷键中的至少30%(至最接近的整数)是立体纯的。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物中的n个含磷键中的至少40%(至最接近的整数)是立体纯的。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物中的n个含磷键中的至少50%(至最接近的整数)是立体纯的。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物中的n个含磷键中的至
少60%(至最接近的整数)是立体纯的。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物中的n个含磷键中的至少70%(至最接近的整数)是立体纯的。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物中的n个含磷键中的至少80%(至最接近的整数)是立体纯的。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物中的n个含磷键中的至少90%(至最接近的整数)是立体纯的。
[0194]
在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少2个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少3个相同立体取向(即s
p or r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少4个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少5个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少6个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少7个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少8个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少9个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少10个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少11个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少12个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少13个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少14个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少15个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少16个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少17个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少18个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少19个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。在具有n个手性含磷键(其中n是1或更大的整数)的寡聚物的一个实施例中,寡聚物含有至少20个相同立体取向(即s
p
或r
p
)的连续的立体纯含磷键。
[0195]
10.吗啉代寡聚物
[0196]
本公开的示例性实施例涉及具有以下通用结构的二氨基磷酸酯吗啉代寡聚物:
[0197][0198]
并且如summerton,j.等人,《反义与核酸药物开发》,7:187-195(1997)的图2中所述。本文所述的吗啉代旨在涵盖前述通用结构的所有立体异构体和互变异构体。吗啉代寡聚物的合成、结构和结合特征详述于美国专利号:5,698,685;5,217,866;5,142,047;5,034,506;5,166,315;5,521,063;5,506,337;8,076,476;和8,299,206,所有这些专利都以引用的方式并入本文中。
[0199]
在某些实施例中,吗啉代在寡聚物的5'或3'端与“尾部”部分缀合以增加其稳定性和/或溶解性。示例性尾部包括:
[0200]
[0201][0202]
在各种实施例中,本公开的反义寡聚物缀合物是根据式(i):
[0203][0204]
或其药学上可接受的盐,其中:
[0205]
每个nu是核碱基,其一起形成靶向序列;
[0206]
t是选自以下的部分:
[0207][0208]
r1是c
1-c6烷基;
[0209]
其中所述靶向序列与指定为h52a(-01+24)的肌营养不良蛋白前体mrna中的外显子52退火位点互补。
[0210]
在各种实施例中,t是
[0211]
在各种实施例中,r1是甲基、cf3、ccl3、cfcl2、cf2cl、乙基、ch2cf3、cf2cf3、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基、异戊基、新戊基、己基、异己基、3-甲基戊基、2,2-二甲基丁基或2,3-二甲基丁基。
[0212]
在一些实施例中,式(i)的反义寡聚物缀合物是其hcl(盐酸)盐。在某些实施例中,hcl盐是6hcl盐。
[0213]
在一些实施例中,每个nu独立地选自胞嘧啶(c)、鸟嘌呤(g)、胸腺嘧啶(t)、腺嘌呤(a)、5-甲基胞嘧啶(5mc)、尿嘧啶(u)和次黄嘌呤(i)。
[0214]
在一些实施例中,靶向序列是seq id no:1(5'-ctgttccaaatcctgcattgttgcc-3'),其中每个胸腺嘧啶(t)任选地是尿嘧啶(u)。
[0215]
在各种实施例中,t是并且靶向序列是seq id no:1(5'-ctgttccaaatcctgcattgttgcc-3'),其中每个胸腺嘧啶(t)任选地是尿嘧啶(u)。
[0216]
在各种实施例中,t是并且靶向序列是seq id no:1(5'-ctgttccaaatcctgcattgttgcc-3')。
[0217]
在一些实施例中,包括例如式(i)的一些实施例,本公开的反义寡聚物缀合物是根据式(ii):
[0218][0219]
或其药学上可接受的盐,其中:
[0220]
每个nu是核碱基,其一起形成与指定为h52a(-01+24)的肌营养不良蛋白前体mrna中的外显子52退火位点互补的靶向序列。
[0221]
在一些实施例中,每个nu独立地选自胞嘧啶(c)、鸟嘌呤(g)、胸腺嘧啶(t)、腺嘌呤(a)、5-甲基胞嘧啶(5mc)、尿嘧啶(u)和次黄嘌呤(i)。
[0222]
在各种实施例中,每个nu从1至25并且5'至3'是(seq id no:1):
[0223][0224]
其中a是c是g是并且x是在某些实施例中,每个x独立地是
[0225]
在一些实施例中,式(ii)的反义寡聚物缀合物是其hcl(盐酸)盐。在某些实施例中,hcl盐是6hcl盐。
[0226]
在一些实施例中,包括例如式(ii)的一些实施例,本公开的反义寡聚物缀合物是根据式(iia):
[0227][0228]
其中每个nu是核碱基,其一起形成与指定为h52a(-01+24)的肌营养不良蛋白前体mrna中的外显子52退火位点互补的靶向序列。
[0229]
在一些实施例中,每个nu独立地选自胞嘧啶(c)、鸟嘌呤(g)、胸腺嘧啶(t)、腺嘌呤(a)、5-甲基胞嘧啶(5mc)、尿嘧啶(u)和次黄嘌呤(i)。
[0230]
在各种实施例中,每个nu从1至25并且5'至3'是(seq id no:1):
[0231][0232]
[0233]
其中a是c是g是并且x是在某些实施例中,每个x是
[0234]
在一些实施例中,包括例如式(ii)和式(iia)的反义寡聚物缀合物的实施例,靶向序列是seq id no:1(5'-ctgttccaaatcctgcattgttgcc-3'),其中每个胸腺嘧啶(t)任选地是尿嘧啶(u)。在各种实施例中,包括例如式(ii)和式(iia)的反义寡聚物缀合物的实施例,靶向序列是seq id no:1(5'-ctgttccaaatcctgcattgttgcc-3')。
[0235]
在一些实施例中,包括例如式(i)的反义寡聚物缀合物的实施例,本公开的反义寡聚物缀合物是根据式(iii):
[0236][0237]
或其药学上可接受的盐。
[0238]
在一些实施例中,式(iii)的反义寡聚物缀合物是其hcl(盐酸)盐。在某些实施例中,hcl盐是6hcl盐。
[0239]
在一些实施例中,包括例如式(iii)的反义寡聚物缀合物的实施例,本公开的反义寡聚物缀合物是根据式(iiia):
[0240][0241]
在本公开的一些实施例中,包括一些式(i)的反义寡聚物缀合物的实施例和式(iii)的反义寡聚物缀合物的实施例,反义寡聚物缀合物是根据式(iv):
[0242][0243]
或其药学上可接受的盐。
[0244]
在一些实施例中,式(iv)的反义寡聚物缀合物是其hcl(盐酸)盐。在某些实施例中,hcl盐是6hcl盐。
[0245]
在一些实施例中,包括例如式(iv)的反义寡聚物缀合物的实施例,本公开的反义寡聚物缀合物是根据式(iva):
[0246][0247]
在各种实施例中,本公开的反义寡聚物是根据式(v):
[0248][0249]
或其药学上可接受的盐,其中:
[0250]
每个nu是核碱基,其一起形成靶向序列;
[0251]
t是选自以下的部分:
[0252][0253]
r1是c
1-c6烷基;以及
[0254]
r2选自h或乙酰基,
[0255]
其中所述靶向序列与指定为h52a(-01+24)的肌营养不良蛋白前体mrna中的外显子52退火位点互补。
[0256]
在各种实施例中,t是
[0257]
在各种实施例中,r1是甲基、cf3、ccl3、cfcl2、cf2cl、乙基、ch2cf3、cf2cf3、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基、异戊基、新戊基、己基、异己基、3-甲基戊基、2,2-二甲基丁基或2,3-二甲基丁基。
[0258]
在一些实施例中,每个nu独立地选自胞嘧啶(c)、鸟嘌呤(g)、胸腺嘧啶(t)、腺嘌呤(a)、5-甲基胞嘧啶(5mc)、尿嘧啶(u)和次黄嘌呤(i)。
[0259]
在一些实施例中,靶向序列是seq id no:1(5'-ctgttccaaatcctgcattgttgcc-3'),其中每个胸腺嘧啶(t)任选地是尿嘧啶(u)。
[0260]
在各种实施例中,t是并且靶向序列是seq id no:1(5'-ctgttccaaatcctgcattgttgcc-3'),其中每个胸腺嘧啶(t)任选地是尿嘧啶(u)。
[0261]
在各种实施例中,t是并且靶向序列是seq id no:1(5'-ctgttccaaatcctgcattgttgcc-3')。
[0262]
在一些实施例中,包括例如式(iv)的一些实施例,本公开的反义寡聚物是根据式(v):
[0263][0264]
或其药学上可接受的盐,其中:
[0265]
r选自h或乙酰基;并且
[0266]
每个nu是核碱基,其一起形成与指定为h52a(-01+24)的肌营养不良蛋白前体mrna中的外显子53退火位点互补的靶向序列。
[0267]
在一些实施例中,r是h。在各种实施例中,r是乙酰基。
[0268]
在一些实施例中,每个nu独立地选自胞嘧啶(c)、鸟嘌呤(g)、胸腺嘧啶(t)、腺嘌呤(a)、5-甲基胞嘧啶(5mc)、尿嘧啶(u)和次黄嘌呤(i)。
[0269]
在各种实施例中,每个nu从1至25并且5'至3'是(seq id no:1):
[0270][0271]
其中a是c是g是并且x是在某些实施例中,每个x独立地是
[0272]
在各种实施例中,r是h并且每个nu从1至25并且5'至3'是(seq id no:1):
[0273][0274]
其中a是c是g是并且x是在某些实施例中,每个x独立地是
[0275]
在本公开的一些实施例中,包括一些式(v)的反义寡聚物的实施例和式(vi)的反义寡聚物的实施例,反义寡聚物是根据式(vii):
[0276][0277]
或其药学上可接受的盐。
[0278]
在另一方面,本公开提供了式(viia)的反义寡聚物缀合物:
[0279][0280]
或其药学上可接受的盐。
[0281]
10.核碱基修饰和取代
[0282]
在某些实施例中,本公开的反义寡聚物和反义寡聚物缀合物由rna核碱基和dna核碱基(在本领域中通常简称为“碱基”)构成。rna碱基通常称为腺嘌呤(a)、尿嘧啶(u)、胞嘧
卤尿嘧啶、5-丙炔基尿嘧啶、5-丙炔基胞嘧啶、5-氨基甲基尿嘧啶、5-羟甲基尿嘧啶、5-氨基甲基胞嘧啶、5-羟甲基胞嘧啶、super t)、7-脱氮鸟嘌呤、7-脱氮腺嘌呤、7-氮杂-2,6-二氨基嘌呤、8-氮杂-7-脱氮鸟嘌呤、8-氮杂-7-脱氮腺嘌呤、8-氮杂-7-脱氮-2,6-二氨基嘌呤、super g、super a和n4-乙基胞嘧啶或其衍生物;n
2-环戊基鸟嘌呤(cpent-g)、n
2-环戊基-2-氨基嘌呤(cpent-ap)和n
2-丙基-2-氨基嘌呤(pr-ap)、假尿嘧啶或其衍生物;以及简并或通用碱基,如2,6-二氟甲苯,或不存在碱基,如无碱基位点(例如1-脱氧核糖、1,2-二脱氧核糖、l-脱氧-2-o-甲基核糖;或吡咯烷衍生物,其中环氧已被氮置换(氮杂核糖))。super a、super g和super t的衍生物的实例可见于美国专利6,683,173(epoch biosciences),其以引用的方式全部并入本文中。cpent-g、cpent-ap和pr-ap被证明在掺入sirna中时降低免疫刺激作用(peacock h.等人《美国化学学会杂志(j.am.chem.soc.)》2011,133,9200)。假尿嘧啶是尿嘧啶的天然存在的异构化形式,具有c-糖苷而不是尿苷中的常规n-糖苷。与含尿苷的mpvna相比,含假尿苷的合成mrna可能具有改进的安全概况(wo 2009127230,以引用的方式全部并入本文中)。
[0292]
某些核碱基对于增加本公开的反义寡聚物和反义寡聚物缀合物的结合亲和力特别有用。这些包括5-取代的嘧啶、6-氮杂嘧啶和n-2、n-6和o-6取代的嘌呤,包括2-氨基丙基腺嘌呤、5-丙炔基尿嘧啶和5-丙炔基胞嘧啶。5-甲基胞嘧啶取代已被证明可使核酸双螺旋体稳定性提高0.6-1.2℃,并且是目前优选的碱基取代,尤其是与2'-o-甲氧基乙基糖修饰组合时,更是如此。另外的示例性修饰核碱基包括其中核碱基的至少一个氢原子被氟取代的那些。
[0293]
11.反义寡聚物和反义寡聚物缀合物的药学上可接受的盐
[0294]
本文所述的反义寡聚物和反义寡聚物缀合物的某些实施例可以含有碱性官能团,如氨基或烷基氨基,因此,能够与药学上可接受的酸形成药学上可接受的盐。在这方面,术语“药学上可接受的盐”是指本公开的反义寡聚物或反义寡聚物缀合物的相对无毒的无机和有机酸加成盐。这些盐可以在施用媒介物或剂型制造过程中原位制备,或通过将本公开的纯化的反义寡聚物或反义寡聚物缀合物以其游离碱形式与合适的有机或无机酸分别反应,并在随后的纯化过程中分离出这样形成的盐。代表性盐包括氢溴酸盐、盐酸盐、硫酸盐、硫酸氢盐、磷酸盐、硝酸盐、乙酸盐、戊酸盐、油酸盐、棕榈酸盐、硬脂酸盐、月桂酸盐、苯甲酸盐、乳酸盐、甲苯磺酸酯、柠檬酸盐、马来酸盐、富马酸盐、琥珀酸盐、酒石酸盐、萘二甲酸盐、甲磺酸盐、葡萄糖庚酸盐、乳糖醛酸盐和月桂基磺酸盐等。(参见例如berge等人(1977)“药物盐(pharmaceutical salts)”,《药物科学杂志(j.pharm.sci.)》66:1-19)。
[0295]
主题反义寡聚物或反义寡聚物缀合物的药学上可接受的盐包括反义寡聚物或反义寡聚物缀合物的常规无毒盐或季铵盐,例如来自无毒有机或无机酸的盐。例如,这种常规的无毒盐包括衍生自无机酸如盐酸、氢溴酸、硫酸、氨基磺酸、磷酸、硝酸等的盐;以及由有机酸如乙酸、丙酸、琥珀酸、乙醇酸、硬脂酸、乳酸、苹果酸、酒石酸、柠檬酸、抗坏血酸、棕榈酸、马来酸、羟基马来酸、苯乙酸、谷氨酸、苯甲酸、水杨酸、对氨基苯磺酸、2-乙酰氧基苯甲酸、富马酸、甲苯磺酸、甲磺酸、乙烷二磺酸、草酸、羟乙磺酸等制备的盐。
[0296]
在某些实施例中,本公开的反义寡聚物和反义寡聚物缀合物可以含有一个或多个酸性官能团,因此能够与药学上可接受的碱形成药学上可接受的盐。在这些情况下,术语“药学上可接受的盐”是指本公开的反义寡聚物或反义寡聚物缀合物的相对无毒的无机和
有机碱加成盐。这些盐同样可以在施用媒介物或剂型制造过程中原位制备,或通过将纯化的反义寡聚物或反义寡聚物缀合物以其游离酸形式与合适的碱,如药学上可接受的金属阳离子的氢氧化物、碳酸盐或碳酸氢盐,与氨,或与药学上可接受的有机伯、仲或叔胺分别反应。代表性的碱金属或碱土金属盐包括锂盐、钠盐、钾盐、钙盐、镁盐和铝盐等。可用于形成碱加成盐的代表性有机胺包括乙胺、二乙胺、乙二胺、乙醇胺、二乙醇胺、哌嗪等。(参见例如berge等人,见上文)。
[0297]
iii.制剂和施用模式
[0298]
在某些实施例中,本公开提供了适合于本文所述的反义寡聚物和反义寡聚物缀合物的治疗性递送的制剂或药物组合物。因此,在某些实施例中,本公开提供了药学上可接受的组合物,其包含与一种或多种药学上可接受的载体(添加剂)和/或稀释剂一起配制的治疗有效量的一种或多种本文所述的反义寡聚物或一种或多种反义寡聚物缀合物。虽然本公开的反义寡聚物或和反义寡聚物缀合物有可能单独施用,但优选以药物制剂(组合物)施用反义寡聚物或反义寡聚物缀合物。在一个实施例中,制剂的反义寡聚物或反义寡聚物缀合物分别根据式(iii)或式(vii)。
[0299]
可以适用于本公开的反义寡聚物或反义寡聚物缀合物的核酸分子的递送方法描述于例如:akhtar等人,1992,《细胞生物学趋势(trends cell bio.)》,2:139;反义寡核苷酸治疗剂的递送策略(delivery strategies for antisense oligonucleotide therapeutics),akhtar编,1995,crc press和sullivan等人,pct wo 94/02595。这些和其它方案可用于几乎任何核酸分子的递送,包括本公开的反义寡聚物和反义寡聚物缀合物。
[0300]
本公开的药物组合物可专门配制成以固体或液体形式施用,包括适应于下列情况的药物组合物:(1)口服施用,例如顿服药(水溶液或非水溶液或悬浮剂)、片剂(针对颊内、舌下或全身吸收)、大丸剂、散剂、颗粒剂、糊剂,施用于舌头;(2)肠胃外施用,例如,通过皮下、肌肉内、静脉内或硬膜外注射,例如,作为无菌溶液或悬浮液,或持续释放制剂;(3)局部施用,例如,作为乳膏、软膏或控释贴剂或喷雾剂施用于皮肤;(4)阴道内或直肠内,例如,作为子宫托、乳膏或泡沫;(5)舌下;(6)经眼;(7)透皮;或(8)经鼻。
[0301]
可以充当药学上可接受的载体的材料的一些实例包括但不限于:(1)糖类,如乳糖、葡萄糖和蔗糖;(2)淀粉,如玉米淀粉和马铃薯淀粉;(3)纤维素及其衍生物,如羧甲基纤维素钠、乙基纤维素和乙酸纤维素;(4)粉状黄蓍;(5)麦芽;(6)明胶;(7)滑石;(8)赋形剂,如可可脂和栓剂蜡;(9)油,如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;(10)二醇,如丙二醇;(11)多元醇,如甘油、山梨糖醇、甘露糖醇和聚乙二醇;(12)酯,如油酸乙酯和月桂酸乙酯;(13)琼脂;(14)缓冲剂,如氢氧化镁和氢氧化铝;(15)海藻酸;(16)无热原质水;(17)等渗盐水;(18)林格氏溶液;(19)乙醇;(20)ph缓冲溶液;(21)聚酯、聚碳酸酯和/或聚酸酐;以及(22)药物制剂中采用的其它无毒相容物质。
[0302]
适合与本公开的反义寡聚物或反义寡聚物缀合物一起配制的药剂的其它非限制性实例包括:peg缀合的核酸;磷脂缀合的核酸;含有亲脂性部分的核酸;硫代磷酸酯;p-糖蛋白抑制剂(如pluronic p85),其可增强药物进入各种组织;可生物降解的聚合物,如聚(d,l-丙交酯-共乙交酯)微球,用于植入后的持续释放递送(emerich,d f等人,1999,《细胞移植(cell transplant)》,8,47-58)alkermes,inc.cambridge,mass.;以及负载的纳米颗粒,例如由聚氰基丙烯酸丁酯制成的纳米颗粒,它可以通过血脑屏障递送药物,并且可以改
变神经元的摄取机制(《神经精神药理学和生物精神病学进展(prog neuropsychopharmacol biol psychiatry)》,23,941-949,1999)。
[0303]
本公开的特征还在于使用包括含聚(乙二醇)(“peg”)脂质的表面改性脂质体的组合物(peg改性的、支链和非支链的或其组合,或长循环脂质体或隐形脂质体)。本公开的反义寡聚物或反义寡聚物缀合物也可以包含各种分子量的共价连接的peg分子。这些制剂提供了一种增加药物在靶组织中积累的方法。这类药物载体能抵抗单核吞噬系统(mps或res)的调理作用和消除作用,从而使囊封的药物有更长的血液循环时间和增强的组织暴露(lasic等人《化学评论(chem.rev.)》1995,95,2601-2627;ishiwata等人,《化学与药物通报(chem.pharm.bull.)》1995,43,1005-1011)。这样的脂质体已被证明在肿瘤中选择性地积累,推测是通过在新生血管化的靶组织中的外渗和捕获(lasic等人,《科学》1995,267,1275-1276;oku等人,1995,《生物化学与生物物理学报(biochim.biophys.acta)》,1238,86-90)。长循环脂质体增强了dna和rna的药代动力学和药效学,特别是与已知在mps的组织中积累的传统阳离子脂质体相比(liu等人,《生物化学杂志(j.biol.chem.)》1995,42,24864-24870;choi等人,国际pct公开号wo 96/10391;ansell等人,国际pct公开号wo 96/10390;holland等人,国际pct公开号wo 96/10392)。与阳离子脂质体相比,长循环脂质体也可能在更大程度上保护药物不被核酸酶降解,这是基于它们能够避免在肝脏和脾脏等代谢侵袭性mps组织中的积累。
[0304]
在另一个实施例中,本公开包括如美国专利号:6,692,911;7,163,695;和7,070,807中所述的制备用于递送的反义寡聚物医药组合物和反义寡聚物缀合物医药组合物。在这方面,在一个实施例中,本公开提供了在包含赖氨酸和组氨酸(hk)的共聚物的组合物中的本公开的反义寡聚物或反义寡聚物缀合物(如美国专利号:7,163,695;7,070,807;和6,692,911中所述),其可以单独或与peg(例如,支链或非支链peg或两者的混合物)组合,与peg和靶向基团组合,或与交联剂组合的上述任何一种。在某些实施例中,本公开提供了包含葡糖酸修饰的聚组氨酸或葡糖酸化聚组氨酸/转铁蛋白-聚赖氨酸的药物组合物中的反义寡聚物或反义寡聚物缀合物。本领域技术人员还将认识到,在组合物内可以取代具有与his和lys相似性质的氨基酸。
[0305]
润湿剂、乳化剂和润滑剂(如月桂基硫酸钠和硬脂酸镁)、着色剂、脱模剂、包衣剂、甜味剂、调味剂、芳香剂、防腐剂和抗氧化剂也可以存在于组合物中。
[0306]
药学上可接受的抗氧化剂的实例包括:(1)水溶性抗氧化剂,如抗坏血酸、半胱氨酸盐酸盐、硫酸氢钠、偏亚硫酸氢钠、亚硫酸钠等;(2)油溶性抗氧化剂,如抗坏血酸棕榈酸酯、丁基化羟基苯甲醚(bha)、丁基化羟基甲苯(bht)、卵磷脂、没食子酸丙酯、α-生育酚等;以及(3)金属螯合剂,如柠檬酸、乙二胺四乙酸(edta)、山梨糖醇、酒石酸、磷酸等。
[0307]
本公开的制剂包括适合于口服、鼻腔、局部(包括颊内和舌下)、直肠、阴道和/或肠胃外施用的制剂。制剂可以方便地以单位剂型存在,并且可以通过药学领域中众所周知的任何方法制备。可与载体材料组合以产生单一剂型的活性成分的量将根据所治疗的受试者和特定的施用方式而变化。可与载体材料组合以产生单一剂型的活性成分的量一般将是产生治疗效果的活性成分的量。一般该量将在活性成分的约0.1%至约99%的范围内,优选约5%至约70%,最优选约10%至约30%。
[0308]
在某些实施例中,本公开的制剂包含选自环糊精、纤维素、脂质体、胶束形成剂(例
如胆汁酸)和聚合物载体(例如聚酯和聚酸酐)的赋形剂;以及本公开的反义寡聚物或反义寡聚物缀合物。在一个实施例中,制剂的反义寡聚物缀合物是根据式(iii)。在一个实施例中,制剂的反义寡聚物是根据式(vii)。在某些实施例中,前述制剂使本公开的反义寡聚物缀合物口服生物可利用。
[0309]
制备这些制剂或药物组合物的方法包括使本公开的反义寡聚物缀合物与载体和任选的一种或多种辅助成分结合的步骤。通常,通过将本公开的反义寡聚物缀合物与液体载体或细粉状固体载体或两者均匀且紧密地结合,然后,如果需要,将产物成型来制备制剂。
[0310]
适于口服施用的本公开的制剂可以呈胶囊、扁囊剂、丸剂、片剂、含片(使用调味基础、通常是蔗糖和阿拉伯胶或黄蓍)、粉末、颗粒形式,或作为水性或非水性液体中的溶液或悬浮液,或作为水包油或油包水液体乳液,或作为酏剂或糖浆,或作为锭剂(使用惰性基质,如明胶和甘油,或蔗糖和阿拉伯胶)和/或作为漱口剂等,每个含有预定量的本公开的反义寡聚物缀合物作为活性成分。本公开的反义寡聚物缀合物也可作为大丸剂、舐剂或糊剂施用。
[0311]
在口服施用的本公开的固体剂型(胶囊、片剂、丸剂、糖衣药丸、散剂、颗粒剂、小丸剂等)中,活性成分可以与一种或多种药学上可接受的载体,如柠檬酸钠或磷酸二钙,和/或以下任何一种混合:(1)填充剂或增量剂,如淀粉、乳糖、蔗糖、葡萄糖、甘露糖醇和/或硅酸;(2)粘合剂,如例如羧甲基纤维素、海藻酸盐、明胶、聚乙烯吡咯烷酮、蔗糖和/或阿拉伯胶;(3)保湿剂,如甘油;(4)崩解剂,如琼脂、碳酸钙、马铃薯或木薯淀粉、海藻酸、某些硅酸盐和碳酸钠;(5)溶液缓释剂,如石蜡;(6)吸收促进剂,如季铵化合物和表面活性剂,如泊洛沙姆和月桂醇硫酸钠;(7)润湿剂,如例如鲸蜡醇、单硬脂酸甘油酯和非离子表面活性剂;(8)吸收剂,如高岭土和膨润土;(9)润滑剂,如滑石、硬脂酸钙、硬脂酸镁、固体聚乙二醇、月桂醇硫酸钠、硬脂酸锌、硬脂酸钠、硬脂酸及其混合物;(10)着色剂;和(11)控释剂,如交联聚维酮或乙基纤维素。在胶囊、片剂和丸剂的情况下,药物组合物还可包含缓冲剂。类似类型的固体药物组合物也可使用乳糖或奶糖等赋形剂以及高分子量聚乙二醇等作为软壳和硬壳明胶胶囊的填充剂。
[0312]
片剂可以通过压缩或模制来制备,任选地含有一种或多种辅助成分。压缩片剂可以使用粘合剂(例如,明胶或羟丙基甲基纤维素)、润滑剂、惰性稀释剂、防腐剂、崩解剂(例如,羟基乙酸淀粉钠或交联羧甲基纤维素钠)、表面活性剂或分散剂来制备。模制片剂可以通过在合适的机器中模制用惰性液体稀释剂润湿的粉状化合物的混合物来制备。
[0313]
本公开的药物组合物的片剂和其它固体剂型,如糖衣药丸、胶囊、丸剂和颗粒剂,可以任选地用包衣和外壳,如肠溶包衣和其它药物配制领域中众所周知的包衣刻痕或制备。它们也可以使用例如不同比例的羟丙基甲基纤维素以提供所需的释放曲线、其它聚合物基质、脂质体和/或微球配制成使其中的活性成分缓慢或受控释放。它们可以配制用于快速释放,例如冻干。它们可以通过例如通过细菌截留过滤器过滤,或通过掺入无菌固体药物组合物形式的灭菌剂来灭菌,所述灭菌剂可以在使用前立即溶解在无菌水或一些其它无菌可注射介质中。这些药物组合物还可以任选地含有遮光剂,并且其成分可以是它们仅或优选地在胃肠道的某一部分释放活性成分,任选地,以延迟的方式释放。可以使用的包埋组合物的实例包括聚合物质和蜡。如果合适,活性成分也可以与一种或多种上述赋形剂一起呈
微囊封形式。
[0314]
用于口服施用本公开的反义寡聚物缀合物的液体剂型包括药学上可接受的乳剂、微乳剂、溶液、悬浮剂、糖浆和酏剂。除活性成分外,液体剂型可含有本领域常用的惰性稀释剂,例如水或其它溶剂、增溶剂和乳化剂,例如乙醇、异丙醇、碳酸乙酯、乙酸乙酯、苯甲醇、苯甲酸苯甲酯、丙二醇、1,3-丁二醇、油(特别是棉籽油、花生油、玉米油、胚芽油、橄榄油、蓖麻油和芝麻油)、甘油、四氢呋喃醇、聚乙二醇和脱水山梨糖醇脂肪酸酯及其混合物。
[0315]
除惰性稀释剂外,口服药物组合物还可以包括佐剂,例如润湿剂、乳化剂和悬浮剂、甜味剂、调味剂、着色剂、芳香剂和防腐剂。
[0316]
除活性化合物外,悬浮液可以含有悬浮剂,例如乙氧基化异硬脂醇、聚氧化乙烯山梨糖醇和脱水山梨糖醇酯、微晶纤维素、偏氢氧化铝、膨润土、琼脂和黄蓍及其混合物。
[0317]
用于直肠或阴道施用的制剂可以作为栓剂提供,其可以通过将一种或多种本公开的化合物与一种或多种合适的无刺激性赋形剂或载体混合来制备,所述赋形剂或载体包含例如可可脂、聚乙二醇、栓剂蜡或水杨酸酯,它在室温下是固体,但在体温下是液体,因此会在直肠或阴道腔内融化并释放出活性化合物。
[0318]
本文提供的用于局部或透皮施用的寡聚物的制剂或剂型包括散剂、喷雾剂、软膏剂、糊剂、霜剂、乳液、凝胶、溶液、贴片和吸入剂。活性寡聚物缀合物可以在无菌条件下与药学上可接受的载体混合,并与可能需要的任何防腐剂、缓冲剂或推进剂混合。除本公开的活性化合物外,软膏剂、糊剂、霜剂和凝胶可以含有赋形剂,如动物和植物脂肪、油、蜡、石蜡、淀粉、黄蓍、纤维素衍生物、聚乙二醇、硅氧烷、膨润土、硅酸、滑石和氧化锌,或其混合物。
[0319]
除本公开的反义寡聚物缀合物外,散剂和喷雾剂可以含有赋形剂,如乳糖、滑石、硅酸、氢氧化铝、硅酸钙和聚酰胺粉末,或这些物质的混合物。喷雾剂可另外含有常规推进剂,例如氯氟烃和挥发性未取代的烃,例如丁烷和丙烷。
[0320]
透皮贴剂具有额外的优点,即提供本公开的反义寡聚物缀合物向身体的受控递送。这种剂型可以通过将寡聚物溶解或分散在适当的介质中来制备。吸收增强剂也可用于增加药剂穿过皮肤的通量。这种通量的速率可以通过提供速率控制膜或将药剂分散在聚合物基质或凝胶中,以及本领域已知的其它方法来控制。
[0321]
适用于肠胃外施用的药物组合物可以包含一种或多种本公开的寡聚物缀合物与一种或多种药学上可接受的无菌等渗的水性或非水性溶液、分散液、悬浮液或乳剂,或可在临使用之前重构成无菌可注射溶液或分散液的无菌粉末的组合,其可以含有糖、醇、抗氧化剂、缓冲剂、抑菌剂、使制剂与预期接受者的血液等渗的溶质或悬浮剂或增稠剂。可以在本公开的药物组合物中采用的合适的水性和非水性载体的实例包括水、乙醇、多元醇(如甘油、丙二醇、聚乙二醇等)及其合适的混合物、植物油如橄榄油和可注射的有机酯,如油酸乙酯。例如,通过使用包衣材料如卵磷脂,通过在分散体的情况下保持所需的粒度,以及通过使用表面活性剂,可以保持适当的流动性。在一个实施例中,药物组合物的反义寡聚物或反义寡聚物缀合物分别根据式(iii)或式(vii)。
[0322]
这些药物组合物还可以含有佐剂,如防腐剂、润湿剂、乳化剂和分散剂。通过包含各种抗细菌剂和抗真菌剂,例如对羟基苯甲酸酯、氯丁醇、苯酚山梨酸等,可以确保防止微生物对主题寡聚物缀合物的作用。还可能需要在组合物中包含等渗剂,例如糖、氯化钠等。此外,可以通过包含延迟吸收的试剂如单硬脂酸铝和明胶来延长可注射药物形式的吸收。
[0323]
在某些情况下,为了延长药物的作用,希望减慢皮下或肌肉内注射药物的吸收。这可以通过使用具有较差水溶性的结晶或无定形材料的液体悬浮液以及本领域已知的其它方法来实现。然后,药物的吸收率取决于其溶解率,而溶解率又取决于晶体大小和晶形。或者,通过将药物溶解或悬浮在油性媒剂中来实现胃肠外施用的药物形式的延迟吸收。
[0324]
可注射储库形式可通过在可生物降解的聚合物如聚丙交酯-聚乙交酯中形成主题寡聚物缀合物的微胶囊矩阵而制成。根据寡聚物与聚合物的比例,以及所采用的特定聚合物的性质,可以控制寡聚物的释放速率。其它可生物降解聚合物的实例包括聚(原酸酯)和聚(酸酐)。还可以通过将药物夹带在与身体组织相容的脂质体或微乳剂中来制备可注射储库制剂。
[0325]
当本公开的反义寡聚物缀合物作为药物给人类和动物施用时,它们可以单独给药,也可以作为药物组合物给药,例如含有0.1至99%(更优选10~30%)的反义寡聚物缀合物与药学上可接受的载体组合。
[0326]
本公开的配制品或制剂可以口服、胃肠外、局部或直肠给药。它们通常以适合每种施用途径的形式给药。例如,它们以片剂或胶囊形式施用,通过注射、吸入、眼药水、软膏、栓剂或输液施用;通过乳液或软膏局部施用;或通过栓剂直肠施用。
[0327]
无论选择何种施用途径,本公开的反义寡聚物缀合物(可以合适的水合形式使用)和/或本公开的药物组合物可以通过本领域技术人员已知的常规方法配制成药学上可接受的剂型。本公开的药物组合物中活性成分的实际剂量水平可以改变,以获得有效地实现特定患者、组合物和施用方式所需的治疗反应的活性成分的量,而不会对患者产生不可接受的毒性。
[0328]
所选择的剂量水平将取决于多种因素,包括所采用的本公开的特定反义寡聚物缀合物或其酯、盐或酰胺的活性,施用途径,施用时间,所采用的特定寡聚物的排泄或代谢率,吸收的速率和程度,治疗的持续时间,与所采用的特定寡聚物组合使用的其它药物、化合物和/或材料,所治疗的患者的年龄、性别、体重、状况、一般健康状况和先前的病史,以及医学技术中众所周知的类似因素。
[0329]
本领域中具有普通技术的医师或兽医可以易于确定并开处所需药物组合物的有效量。举例来说,医师或兽医可以低于为达成所需治疗作用所需水平的药物组合物中采用的本公开的反义寡聚物缀合物的剂量开始,并且逐渐增加剂量直至达成所需作用。一般来说,本公开的反义寡聚物缀合物的合适的日剂量将是有效产生治疗效果的最低剂量的反义寡聚物缀合物的量。此类有效剂量将一般取决于本文所述的因素。一般来说,本公开的反义寡聚物缀合物对患者的口服、静脉内、脑室内和皮下剂量,当用于指示的效果时,其范围为每天每公斤体重约0.0001至约100mg。
[0330]
在一些实施例中,本公开的反义寡聚物缀合物一般以约10-160mg/kg或20-160mg/kg的剂量施用。在某些情况下,可能需要大于160mg/kg的剂量。在一些实施例中,静脉内施用剂量为约0.5mg至160mg/kg。在一些实施例中,反义寡聚物缀合物以约0.5mg/kg、1mg/kg、2mg/kg、3mg/kg、4mg/kg、5mg/kg、6mg/kg、7mg/kg、8mg/kg、9mg/kg或10mg/kg的剂量施用。在一些实施例中,反义寡聚物缀合物以约10mg/kg、11mg/kg、12mg/kg、15mg/kg、18mg/kg、20mg/kg、21mg/kg、25mg/kg、26mg/kg、27mg/kg、28mg/kg、29mg/kg、30mg/kg、31mg/kg、32mg/kg、33mg/kg、34mg/kg、35mg/kg、36mg/kg、37mg/kg、38mg/kg、39mg/kg、40mg/kg、41mg/kg、
42mg/kg、43mg/kg、44mg/kg、45mg/kg、46mg/kg、47mg/kg、48mg/kg、49mg/kg 50mg/kg、51mg/kg、52mg/kg、53mg/kg、54mg/kg、55mg/kg、56mg/kg、57mg/kg、58mg/kg、59mg/kg、60mg/kg、65mg/kg、70mg/kg、75mg/kg、80mg/kg、85mg/kg、90mg/kg、95mg/kg、100mg/kg、105mg/kg、110mg/kg、115mg/kg、120mg/kg、125mg/kg、130mg/kg、135mg/kg、140mg/kg、145mg/kg、150mg/kg、155mg/kg、160mg/kg的剂量施用,包括两者之间的所有整数。在一些实施例中,寡聚物以10mg/kg施用。在一些实施例中,寡聚物以20mg/kg施用。在一些实施例中,寡聚物以30mg/kg施用。在一些实施例中,寡聚物以40mg/kg施用。在一些实施例中,寡聚物以60mg/kg施用。在一些实施例中,寡聚物以80mg/kg施用。在一些实施例中,寡聚物以160mg/kg施用。在一些实施例中,寡聚物以50mg/kg施用。
[0331]
在一些实施例中,本公开的反义寡聚物一般以约10-160mg/kg或20-160mg/kg的剂量施用。在某些情况下,可能需要大于160mg/kg的剂量。在一些实施例中,静脉内施用剂量为约0.5mg至160mg/kg。在一些实施例中,反义寡聚物以约0.5mg/kg、1mg/kg、2mg/kg、3mg/kg、4mg/kg、5mg/kg、6mg/kg、7mg/kg、8mg/kg、9mg/kg或10mg/kg的剂量施用。在一些实施例中,反义寡聚物以约10mg/kg、11mg/kg、12mg/kg、15mg/kg、18mg/kg、20mg/kg、21mg/kg、25mg/kg、26mg/kg、27mg/kg、28mg/kg、29mg/kg、30mg/kg、31mg/kg、32mg/kg、33mg/kg、34mg/kg、35mg/kg、36mg/kg、37mg/kg、38mg/kg、39mg/kg、40mg/kg、41mg/kg、42mg/kg、43mg/kg、44mg/kg、45mg/kg、46mg/kg、47mg/kg、48mg/kg、49mg/kg 50mg/kg、51mg/kg、52mg/kg、53mg/kg、54mg/kg、55mg/kg、56mg/kg、57mg/kg、58mg/kg、59mg/kg、60mg/kg、65mg/kg、70mg/kg、75mg/kg、80mg/kg、85mg/kg、90mg/kg、95mg/kg、100mg/kg、105mg/kg、110mg/kg、115mg/kg、120mg/kg、125mg/kg、130mg/kg、135mg/kg、140mg/kg、145mg/kg、150mg/kg、155mg/kg、160mg/kg的剂量施用,包括两者之间的所有整数。在一些实施例中,反义寡聚物以10mg/kg施用。在一些实施例中,反义寡聚物以20mg/kg施用。在一些实施例中,反义寡聚物以30mg/kg施用。在一些实施例中,反义寡聚物以40mg/kg施用。在一些实施例中,反义寡聚物以60mg/kg施用。在一些实施例中,反义寡聚物以80mg/kg施用。在一些实施例中,反义寡聚物以160mg/kg施用。在一些实施例中,反义寡聚物以50mg/kg施用。
[0332]
在一些实施例中,式(iii)的反义寡聚物缀合物一般以约10-160mg/kg或20-160mg/kg的剂量施用。在一些实施例中,式(iii)的反义寡聚物缀合物的静脉内施用剂量为约0.5mg至160mg/kg。在一些实施例中,式(iii)的反义寡聚物缀合物以约0.5mg/kg、1mg/kg、2mg/kg、3mg/kg、4mg/kg、5mg/kg、6mg/kg、7mg/kg、8mg/kg、9mg/kg或10mg/kg的剂量施用。在一些实施例中,式(iii)的反义寡聚物缀合物以约10mg/kg、11mg/kg、12mg/kg、15mg/kg、18mg/kg、20mg/kg、21mg/kg、25mg/kg、26mg/kg、27mg/kg、28mg/kg、29mg/kg、30mg/kg、31mg/kg、32mg/kg、33mg/kg、34mg/kg、35mg/kg、36mg/kg、37mg/kg、38mg/kg、39mg/kg、40mg/kg、41mg/kg、42mg/kg、43mg/kg、44mg/kg、45mg/kg、46mg/kg、47mg/kg、48mg/kg、49mg/kg 50mg/kg、51mg/kg、52mg/kg、53mg/kg、54mg/kg、55mg/kg、56mg/kg、57mg/kg、58mg/kg、59mg/kg、60mg/kg、65mg/kg、70mg/kg、75mg/kg、80mg/kg、85mg/kg、90mg/kg、95mg/kg、100mg/kg、105mg/kg、110mg/kg、115mg/kg、120mg/kg、125mg/kg、130mg/kg、135mg/kg、140mg/kg、145mg/kg、150mg/kg、155mg/kg、160mg/kg的剂量施用,包括两者之间的所有整数。在一些实施例中,式(iii)的反义寡聚物缀合物以10mg/kg施用。在一些实施例中,式(iii)的反义寡聚物缀合物以20mg/kg施用。在一些实施例中,式(iii)的反义寡聚物缀合物以30mg/kg施
用。在一些实施例中,式(iii)的反义寡聚物缀合物以40mg/kg施用。在一些实施例中,式(iii)的反义寡聚物缀合物以60mg/kg施用。在一些实施例中,式(iii)的反义寡聚物缀合物以80mg/kg施用。在一些实施例中,式(iii)的反义寡聚物缀合物以160mg/kg施用。在一些实施例中,式(iii)的反义寡聚物缀合物以50mg/kg施用。
[0333]
在一些实施例中,式(iv)的反义寡聚物一般以约10-160mg/kg或20-160mg/kg的剂量施用。在一些实施例中,式(iv)的反义寡聚物的静脉内施用剂量为约0.5mg至160mg/kg。在一些实施例中,式(iv)的反义寡聚物以约0.5mg/kg、1mg/kg、2mg/kg、3mg/kg、4mg/kg、5mg/kg、6mg/kg、7mg/kg、8mg/kg、9mg/kg或10mg/kg的剂量施用。在一些实施例中,式(iv)的反义寡聚物以约10mg/kg、11mg/kg、12mg/kg、15mg/kg、18mg/kg、20mg/kg、21mg/kg、25mg/kg、26mg/kg、27mg/kg、28mg/kg、29mg/kg、30mg/kg、31mg/kg、32mg/kg、33mg/kg、34mg/kg、35mg/kg、36mg/kg、37mg/kg、38mg/kg、39mg/kg、40mg/kg、41mg/kg、42mg/kg、43mg/kg、44mg/kg、45mg/kg、46mg/kg、47mg/kg、48mg/kg、49mg/kg 50mg/kg、51mg/kg、52mg/kg、53mg/kg、54mg/kg、55mg/kg、56mg/kg、57mg/kg、58mg/kg、59mg/kg、60mg/kg、65mg/kg、70mg/kg、75mg/kg、80mg/kg、85mg/kg、90mg/kg、95mg/kg、100mg/kg、105mg/kg、110mg/kg、115mg/kg、120mg/kg、125mg/kg、130mg/kg、135mg/kg、140mg/kg、145mg/kg、150mg/kg、155mg/kg、160mg/kg的剂量施用,包括两者之间的所有整数。在一些实施例中,式(iv)的反义寡聚物以10mg/kg施用。在一些实施例中,式(iv)的反义寡聚物以20mg/kg施用。在一些实施例中,式(iv)的反义寡聚物以30mg/kg施用。在一些实施例中,式(iv)的反义寡聚物以40mg/kg施用。在一些实施例中,式(iv)的反义寡聚物以60mg/kg施用。在一些实施例中,式(iv)的反义寡聚物以80mg/kg施用。在一些实施例中,式(iv)的反义寡聚物以160mg/kg施用。在一些实施例中,式(iv)的反义寡聚物以50mg/kg施用。
[0334]
如果需要,活性化合物的有效日剂量可作为二个、三个、四个、五个、六个或更多个子剂量在全天以适当的时间间隔分别施用,任选地,以单位剂型施用。在某些情形下,给药是每天施用一次。在某些实施例中,根据需要,给药是每2、3、4、5、6、7、8、9、10、11、12、13、14天,或每1、2、3、4、5、6、7、8、9、10、11、12周,或每1、2、3、4、5、6、7、8、9、10、11、12个月一次或多次施用,以维持功能性肌营养不良蛋白的所需表达。在某些实施例中,给药是每两周一次或多次施用。在一些实施例中,给药是每两周一次施用。在各种实施例中,给药是每月一次或多次施用。在某些实施例中,给药是每月一次施用。
[0335]
在各种实施例中,反义寡聚物缀合物以10mg/kg每周施用。在各种实施例中,反义寡聚物缀合物以20mg/kg每周施用。在各种实施例中,反义寡聚物缀合物以30mg/kg每周施用。在各种实施例中,反义寡聚物缀合物以40mg/kg每周施用。在一些实施例中,反义寡聚物缀合物以60mg/kg每周施用。在一些实施例中,反义寡聚物缀合物以80mg/kg每周施用。在一些实施例中,反义寡聚物缀合物以100mg/kg每周施用。在一些实施例中,反义寡聚物缀合物以160mg/kg每周施用。如本文所用,每周理解为具有每周的领域认可的含义。
[0336]
在各种实施例中,反义寡聚物以10mg/kg每周施用。在各种实施例中,反义寡聚物以20mg/kg每周施用。在各种实施例中,反义寡聚物以30mg/kg每周施用。在各种实施例中,反义寡聚物以40mg/kg每周施用。在一些实施例中,反义寡聚物以60mg/kg每周施用。在一些实施例中,反义寡聚物以80mg/kg每周施用。在一些实施例中,反义寡聚物以100mg/kg每周施用。在一些实施例中,反义寡聚物以160mg/kg每周施用。如本文所用,每周理解为具有每
周的领域认可的含义。
[0337]
在各种实施例中,反义寡聚物缀合物以10mg/kg每两周施用。在各种实施例中,反义寡聚物缀合物以20mg/kg每两周施用。在各种实施例中,反义寡聚物缀合物以30mg/kg每两周施用。在各种实施例中,反义寡聚物缀合物以40mg/kg每两周施用。在一些实施例中,反义寡聚物缀合物以60mg/kg每两周施用。在一些实施例中,反义寡聚物缀合物以80mg/kg每两周施用。在一些实施例中,反义寡聚物缀合物以100mg/kg每两周施用。在一些实施例中,反义寡聚物缀合物以160mg/kg每两周施用。如本文所用,每两周理解为具有每两周的领域认可的含义。
[0338]
在各种实施例中,反义寡聚物以10mg/kg每两周施用。在各种实施例中,反义寡聚物以20mg/kg每两周施用。在各种实施例中,反义寡聚物以30mg/kg每两周施用。在各种实施例中,反义寡聚物以40mg/kg每两周施用。在一些实施例中,反义寡聚物以60mg/kg每两周施用。在一些实施例中,反义寡聚物以80mg/kg每两周施用。在一些实施例中,反义寡聚物以100mg/kg每两周施用。在一些实施例中,反义寡聚物以160mg/kg每两周施用。如本文所用,每两周理解为具有每两周的领域认可的含义。
[0339]
在各种实施例中,反义寡聚物缀合物以10mg/kg每三周施用。在各种实施例中,反义寡聚物缀合物以20mg/kg每三周施用。在各种实施例中,反义寡聚物缀合物以30mg/kg每三周施用。在各种实施例中,反义寡聚物缀合物以40mg/kg每三周施用。在一些实施例中,反义寡聚物缀合物以60mg/kg每三周施用。在一些实施例中,反义寡聚物缀合物以80mg/kg每三周施用。在一些实施例中,反义寡聚物缀合物以100mg/kg每三周施用。在一些实施例中,反义寡聚物缀合物以160mg/kg每三周施用。如本文所用,每三周理解为具有每三周一次的领域认可的含义。
[0340]
在各种实施例中,反义寡聚物以10mg/kg每三周施用。在各种实施例中,反义寡聚物以20mg/kg每三周施用。在各种实施例中,反义寡聚物以30mg/kg每三周施用。在各种实施例中,反义寡聚物以40mg/kg每三周施用。在一些实施例中,反义寡聚物以60mg/kg每三周施用。在一些实施例中,反义寡聚物以80mg/kg每三周施用。在一些实施例中,反义寡聚物以100mg/kg每三周施用。在一些实施例中,反义寡聚物以160mg/kg每三周施用。如本文所用,每三周理解为具有每三周一次的领域认可的含义。
[0341]
在各种实施例中,反义寡聚物缀合物以10mg/kg每月施用。在各种实施例中,反义寡聚物缀合物以20mg/kg每月施用。在各种实施例中,反义寡聚物缀合物以30mg/kg每月施用。在各种实施例中,反义寡聚物缀合物以40mg/kg每月施用。在一些实施例中,反义寡聚物缀合物以60mg/kg每月施用。在一些实施例中,反义寡聚物缀合物以80mg/kg每月施用。在一些实施例中,反义寡聚物缀合物以100mg/kg每月施用。在一些实施例中,反义寡聚物缀合物以160mg/kg每月施用。如本文所用,每月理解为具有每月的领域认可的含义。
[0342]
在各种实施例中,反义寡聚物以10mg/kg每月施用。在各种实施例中,反义寡聚物以20mg/kg每月施用。在各种实施例中,反义寡聚物以30mg/kg每月施用。在各种实施例中,反义寡聚物以40mg/kg每月施用。在一些实施例中,反义寡聚物以60mg/kg每月施用。在一些实施例中,反义寡聚物以80mg/kg每月施用。在一些实施例中,反义寡聚物以100mg/kg每月施用。在一些实施例中,反义寡聚物以160mg/kg每月施用。如本文所用,每月理解为具有每月的领域认可的含义。
[0343]
如本领域中将理解的,每周、每两周、每三周或每月施用可在本文所讨论的一次或多次施用或子剂量中。
[0344]
本文所述的核酸分子、反义寡聚物和反义寡聚物缀合物可以通过本领域技术人员已知的各种方法施用于细胞,包括但不限于如本文所述和本领域中已知的囊封在脂质体中、通过离子电渗疗法或通过掺入其它媒介物中,如水凝胶、环糊精、可生物降解的纳米胶囊和生物粘附微球。在某些实施例中,可利用微乳化技术来提高亲脂性(水不溶性)药剂的生物利用率。实例包括曲美汀(trimetrine)(dordunoo,s.k.等人,《药物开发与工业制药学(drug development and industrial pharmacy)》,17(12),1685-1713,1991)和rev 5901(sheen,p.c.等人,《药学杂志(j pharm sci)》80(7),712-714,1991)。除其它好处外,微乳化通过优先引导吸收到淋巴系统而不是循环系统,从而绕过肝脏,并防止化合物在肝胆循环中被破坏,从而提高了生物利用率。
[0345]
在本公开的一个方面,制剂含有由本文提供的寡聚物和至少一种两亲载体形成的胶束,其中胶束的平均直径小于约100nm。更优选的实施例提供了平均直径小于约50nm的胶束,甚至更优选的实施例提供了平均直径小于约30nm或甚至小于约20nm的胶束。
[0346]
虽然所有合适的两亲载体都可以考虑,但目前优选的载体一般是那些具有一般公认安全(gras)状态的载体,并且当溶液与复杂的水相(如在人类胃肠道中发现的水相)接触时,既能溶解本公开的反义寡聚物缀合物,又能在后期使其微乳化。通常,满足这些要求的两亲成分的hlb(亲水与亲脂平衡)值为2-20,并且其结构含有c-6至c-20范围内的直链脂肪族基团。实例是聚乙二醇化的脂肪甘油酯和聚乙二醇。
[0347]
两亲载体的实例包括饱和与单不饱和的聚乙二醇脂肪酸甘油酯,如从完全或部分氢化的各种植物油中得到的那些。这类油可有利地由三脂肪酸、二脂肪酸和单脂肪酸甘油酯以及相应脂肪酸的二聚和单聚(乙二醇)酯组成,特别优选的脂肪酸组成包括癸酸4-10%,癸酸3-9%,月桂酸40-50%,肉豆蔻酸14-24%,棕榈酸4-14%和硬脂酸5-15%。另一类有用的两亲载体包括部分酯化的脱水山梨糖醇和/或山梨糖醇,以及饱和或单不饱和脂肪酸(span系列)或相应的乙氧基化类似物(tween系列)。
[0348]
市售的两亲载体可能特别有用,包括gelucire系列、labrafil、labrasol或lauroglycol(均由gattefosse corporation,saintpriest,france生产和分销)、peg-单油酸酯、peg-二油酸酯、peg-单月桂酸酯和二月桂酸酯、卵磷脂、聚山梨醇酯80等(由美国及全球多家公司生产和分销)。
[0349]
在某些实施例中,可以通过使用脂质体、纳米胶囊、微颗粒、微球、脂质颗粒、囊泡等进行递送,以将本公开的药物组合物引入合适的宿主细胞中。特别是,本公开的药物组合物可以配制成囊封在脂质颗粒、脂质体、囊泡、纳米球、纳米颗粒等中递送。这种递送载体的配制和使用可以使用已知的和常规的技术来进行。
[0350]
适合在本公开中使用的亲水聚合物是那些容易溶于水,可以共价连接到形成囊泡的脂质上,并且在体内可以耐受而没有毒性作用(即,是生物相容性的)的聚合物。合适的聚合物包括聚(乙二醇)(peg)、聚乳酸(也称为聚丙交酯)、聚乙二醇酸(也称为聚乙交酯)、聚乳酸-聚乙醇酸共聚物和聚乙烯醇。在某些实施例中,聚合物的重均分子量为约100或120道尔顿至约5,000或10,000道尔顿,或约300道尔顿至约5,000道尔顿。在其它实施例中,聚合物是重均分子量为约100至约5,000道尔顿,或重均分子量为约300至约5,000道尔顿的聚
(乙二醇)。在某些实施例中,聚合物是重均分子量为约750道尔顿的聚(乙二醇),例如peg(750)。聚合物也可以由其中的单体数目来定义;本公开的一个优选实施例利用至少约三个单体的聚合物,这种由三个单体组成的peg聚合物的分子量为约132道尔顿。
[0351]
可能适合在本公开中使用的其它亲水聚合物包括聚乙烯吡咯烷酮、聚甲基噁唑啉、聚乙基噁唑啉、聚羟丙基甲基丙烯酰胺、聚甲基丙烯酰胺、聚二甲基丙烯酰胺和衍生化纤维素,如羟甲基纤维素或羟乙基纤维素。
[0352]
在某些实施例中,本公开的配方包含选自以下组成的组的生物相容性聚合物:聚酰胺、聚碳酸酯、聚亚烷基、丙烯酸酯和甲基丙烯酸酯的聚合物、聚乙烯聚合物、聚乙交酯、聚硅氧烷、聚氨基甲酸酯及其共聚物、纤维素、聚丙烯、聚乙烯、聚苯乙烯、乳酸和乙醇酸的聚合物、聚酸酐、聚(正)酯、聚(丁酸)、聚(戊酸)、聚(丙交酯-共-己内酯)、多糖、蛋白质、聚透明质酸、聚氰基丙烯酸酯及其掺合物、混合物或共聚物。
[0353]
环糊精是环状寡糖,由6、7或8个葡萄糖单元组成,分别用希腊字母α、β或γ表示。葡萄糖单元通过α-1,4-糖苷键连接。由于糖单元的椅子构型,所有的仲羟基(在c-2,c-3处)都位于环的一侧,而c-6处的所有伯羟基都位于另一侧。因此,外表面是亲水的,使环糊精具有水溶性。相反,环糊精的空腔是疏水的,因为它们是由原子c-3和c-5的氢和醚类氧所衬的。这些基质允许与各种相对疏水的化合物进行络合,包括例如类固醇化合物,如17α-雌二醇(参见例如van uden等人《植物细胞组织和器官培养(plant cell tiss.org.cult.)》38:1-3-113(1994))。络合是通过范德华相互作用和氢键形成而发生。关于环糊精化学的一般综述,参见wenz,《应用化学杂志英文国际版(agnew.chem.int.ed.engl.)》,33:803-822(1994)。
[0354]
环糊精衍生物的物理化学特性在很大程度上取决于取代的种类和程度。例如,它们在水中的溶解度从不溶(例如三乙酰-β-环糊精)到147%可溶(w/v)(g-2-β-环糊精)。另外,它们可溶于许多有机溶剂。环糊精的特性使得能够通过增加或减少其溶解度来控制各种制剂组分的溶解度。
[0355]
已经描述了许多环糊精及其制备方法。例如,parmeter(i)等人(美国专利号3,453,259)和gramera等人(美国专利号3,459,731)描述了电中性环糊精。其它衍生物包括具有阳离子特性的环糊精[parmeter(ii),美国专利号3,453,257]、不溶性交联环糊精(solms,美国专利号3,420,788)和具有阴离子特性的环糊精[parmeter(iii),美国专利号3,426,011]。在具有阴离子特性的环糊精衍生物中,羧酸、亚磷酸、次膦酸、膦酸、磷酸、硫代膦酸、硫代亚磺酸和磺酸已被附接到母体环糊精[参见parmeter(iii),见上文]。此外,磺基烷基醚环糊精衍生物已由stella等人描述(美国专利号5,134,127)。
[0356]
脂质体由至少一个脂质双层膜组成,该脂质双层膜包围水性内部隔室。脂质体可按膜的类型和大小来表征。小单层囊泡(suv)具有单层膜,通常直径在0.02和0.05μm之间;大单层囊泡(luvs)通常大于0.05μm。寡层大囊泡和多层囊泡具有多个通常同心的膜层,通常大于0.1μm。具有多个非同心膜的脂质体,即在一个较大囊泡内含有几个较小囊泡,称为多囊囊泡。
[0357]
本公开的一个方面涉及包括含本公开的反义寡聚物或反义寡聚物缀合物的脂质体的制剂,其中脂质体膜被配制为提供具有增加的载量的脂质体。或者或另外,本公开的反义寡聚物或反义寡聚物缀合物可以包含在脂质体的脂质体双层内,或吸附到脂质体的脂质
体双层上。本公开的反义寡聚物或反义寡聚物缀合物可以与脂质表面活性剂聚集,并携带在脂质体的内部空间内;在这些情况下,脂质体膜被配制成抵抗活性剂-表面活性剂聚集的破坏作用。
[0358]
根据本公开的一个实施例,脂质体的脂质双层含有用聚(乙二醇)(peg)衍生的脂质,使得peg链从脂质双层的内表面延伸到由脂质体囊封的内部空间,并从脂质双层的外部延伸到周围环境中。
[0359]
本公开的脂质体中包含的活性剂为溶解形式。根据本公开的脂质体的内部空间内可夹带表面活性剂和活性剂(如含有感兴趣的活性剂的乳液或胶束)的聚集物。表面活性剂的作用是分散和溶解活性剂,并且可以选自任何合适的脂肪族、环脂肪族或芳香族表面活性剂,包括但不限于不同链长(例如,约c14至约c20)的生物相容性溶血磷脂酰胆碱(lpg)。聚合物衍生的脂质如peg-脂质也可用于胶束的形成,因为它们将起到抑制胶束/膜融合的作用,并且由于将聚合物加入到表面活性剂分子中可降低表面活性剂的cmc并有助于胶束的形成。优选的是cmo在微摩尔范围内的表面活性剂;可以利用更高的cmc表面活性剂来制备夹带在本公开的脂质体内的胶束。
[0360]
根据本公开的脂质体可以通过本领域已知的各种技术中的任何一种来制备。参见例如美国专利号4,235,871;公开的pct申请wo 96/14057;新rrc,《脂质体:一种实用的方法(liposomes:apractical approach)》,irlpress,oxford(1990),第33-104页;和lasic dd,《从物理学到应用的脂质体(liposomes from physics to applications)》,elsevier science publishers bv,amsterdam,1993。例如,本公开的脂质体可以通过将用亲水聚合物衍生的脂质扩散到预成型的脂质体中来制备,例如将预成型的脂质体暴露在由脂质接枝聚合物构成的胶束中,脂质浓度对应于脂质体中所需要的衍生脂质的最终摩尔百分比。含有亲水聚合物的脂质体也可以通过均质化、脂质场水合或挤出技术形成,如本领域中已知的。
[0361]
在另一个示例性配制程序中,活性剂首先通过超声分散在易于溶解疏水分子的溶血磷脂酰胆碱或其它低cmc表面活性剂(包括聚合物接枝脂质)中。然后将所得的活性剂胶束悬浮液用于再水化干燥的脂质样品,该样品含有合适摩尔百分比的聚合物接枝脂质或胆固醇。然后使用本领域已知的挤出技术将脂质和活性剂悬浮液形成脂质体,并通过标准柱分离将所得脂质体与未囊封的溶液分离。
[0362]
在本公开的一个方面,脂质体被制备成在选定的尺寸范围内具有基本均匀的尺寸。一种有效的施胶方法涉及将脂质体的水性悬浮液挤出通过一系列具有选定的均匀孔径的聚碳酸酯膜;膜的孔径将与通过该膜挤出产生的脂质体的最大尺寸大致对应。参见例如美国专利号4,737,323(1988年4月12日)。在某些实施例中,可以利用如和等试剂将多核苷酸或蛋白质引入细胞中。
[0363]
本公开的制剂的释放特征取决于囊封材料、囊封药物的浓度和释放调节剂的存在。例如,释放可以被操纵为依赖于ph值,例如,使用ph敏感涂层,该涂层仅在低ph值下释放,如在胃中,或在较高ph值下释放,如在肠道中。可以使用肠溶包衣来防止释放发生,直到通过胃之后。囊封在不同材料中的氰胺的多种包衣或混合物可用于在胃中获得初始释放,随后在肠道中释放。还可以通过包含盐类或成孔剂来操纵释放,这些盐类或成孔剂可以增
加水的吸收或药物从胶囊中扩散释放。改变药物溶解度的赋形剂也可用于控制释放速率。也可以掺入增强基质降解或从基质释放的药剂。它们可以加入到药物中,作为单独的相(即作为颗粒)加入,或者可以根据化合物共溶于聚合物相中。在大多数情况下,量应在0.1%与30%(w/w聚合物)之间。降解促进剂的类型包括无机盐,如硫酸铵和氯化铵;有机酸,如柠檬酸、苯甲酸和抗坏血酸;无机碱,如碳酸钠、碳酸钾、碳酸钙、碳酸锌和氢氧化锌;有机碱,如硫酸鱼精蛋白、精胺、胆碱、乙醇胺、二乙醇胺和三乙醇胺;以及表面活性剂,如和能增加基质微观结构的成孔剂(即水溶性化合物,如无机盐和糖)作为颗粒加入。其范围通常在1%与30%(w/w聚合物)之间。
[0364]
还可以通过改变颗粒在肠道内的停留时间来操纵吸收。这可以通过例如用粘膜粘合剂聚合物包覆颗粒,或选择粘膜粘合剂聚合物作为囊封材料来实现。实例包括大多数具有游离羧基的聚合物,如壳聚糖、纤维素,特别是聚丙烯酸酯(如本文所用,聚丙烯酸酯是指包括丙烯酸酯基和修饰的丙烯酸酯基如氰基丙烯酸酯和甲基丙烯酸酯的聚合物)。
[0365]
反义寡聚物或反义寡聚物缀合物可配制成包含在外科或医疗装置或植入物内,或适应于由外科或医疗装置或植入物释放。在某些方面,可以用反义寡聚物缀合物包覆或以其它方式处理植入物。例如,水凝胶或其它聚合物,如生物相容性和/或可生物降解的聚合物,可用于包覆具有本公开的药物组合物的植入物(即,该组合物可通过使用水凝胶或其它聚合物适应于医疗装置使用)。用于包覆具有药剂的医疗装置的聚合物和共聚物是本领域中众所周知的。植入物的实例包括但不限于支架、药物洗脱支架、缝合线、假体、血管导管、透析导管、血管移植物、假体心脏瓣膜、心脏起搏器、植入式心脏复律除颤器、静脉注射针、用于骨固定和形成的装置,如针、螺钉、板和其它装置,以及用于伤口愈合的人工组织基质。
[0366]
除了本文提供的方法外,根据本公开使用的反义寡聚物或反义寡聚物缀合物可以与其它药物类似地配制成以任何方便的方式用于人或兽药的施用。反义寡聚物和反义寡聚物缀合物及其相应的制剂可单独或与其它治疗策略组合施用,用于治疗肌营养不良,如成肌细胞移植、干细胞疗法、氨基糖苷类抗生素的施用、蛋白酶体抑制剂和上调疗法(例如上调肌营养相关蛋白,肌营养不良蛋白的一种常染色体旁系同源物)。
[0367]
在一些实施例中,额外的治疗剂可以在施用本公开的反义寡聚物缀合物之前、同时或之后施用。例如,反义寡聚物缀合物可与类固醇和/或抗生素组合施用。在某些实施例中,将反义寡聚物缀合物施用给正在接受背景类固醇理论(例如,间歇或慢性/连续背景类固醇疗法)的患者。例如,在一些实施例中,在施用反义寡聚物之前,患者已经用皮质类固醇治疗,并继续接受类固醇治疗。在一些实施例中,类固醇是糖皮质激素或泼尼松。
[0368]
所描述的施用途径仅旨在作为一种指导,因为熟练的从业人员将能够很容易地确定最佳的施用途径和任何特定动物和病况的剂量。已经尝试了多种在体外和体内将功能性新遗传物质引入细胞的方法(friedmann(1989)《科学》,244:1275-1280)。这些方法包括将待表达的基因整合到修饰的逆转录病毒中(friedmann(1989)见上文;rosenberg(1991)《癌症研究(cancer research)》51(18),增刊:5074s-5079s);整合到非逆转录病毒载体中(例如腺相关病毒载体)(rosenfeld等人,(1992)《细胞(cell)》,68:143-155;rosenfeld等人,(1991)《科学》,252:431-434);或通过脂质体递送与异源启动子-增强子元件相连的转基因(friedmann(1989),见上文;brigham等人,(1989)《美国医学科学杂志(am.j.med.sci.)》,298:278-281;nabel等人,(1990)《科学》,249:1285-1288;hazinski等人,et al.(1991)《美
国呼吸细胞和分子生物学杂志(am.j.resp.cell molec.biol.)》,4:206-209;以及wang和huang(1987)《美国国家科学院院刊》,84:7851-7855);与配体特异性、基于阳离子的转运系统偶合(wu和wu(1988)《生物化学杂志(j.biol.chem.)》,263:14621-14624)或使用裸dna、表达载体(nabel等人(1990),见上文;wolff等人(1990)《科学》,247:1465-1468)。将转基因直接注射到组织中仅产生局部表达(rosenfeld(1992)见上文;rosenfeld等人(1991)见上文;brigham等人(1989)见上文;nabel(1990)见上文;和hazinski等人(1991)见上文)。brigham等人的小组(《美国医学科学杂志》(1989)298:278-281和《临床研究(clinical research)》(1991)39(摘要))报道了在静脉内或气管内施用dna脂质体复合物后,仅对小鼠的肺进行体内转染。人类基因疗法程序的评论文章的一个实例是:anderson,《科学》(1992)256:808-813。
[0369]
在另一个实施例中,本公开的药物组合物可以另外包含如han等人,《自然通讯(nat.comms.)》7,10981(2016)中提供的碳水化合物,其全部内容以引用的方式并入本文中。在一些实施例中,本公开的药物组合物可包含5%的己糖碳水化合物。例如,本公开的药物组合物可包含5%的葡萄糖、5%的果糖或5%的甘露糖。在某些实施例中,本公开的药物组合物可包含2.5%的葡萄糖和2.5%的果糖。在一些实施例中,本公开的药物组合物可以包含选自以下的碳水化合物:以5体积%的量存在的阿拉伯糖、以5体积%的量存在的葡萄糖、以5体积%的量存在的山梨糖醇、以5体积%的量存在的半乳糖、以5体积%的量存在的果糖、以5体积%的量存在的木糖醇、以5体积%的量存在的甘露糖、各自以2.5体积%的量存在的葡萄糖和果糖的组合,以及以5.7体积%的量存在的葡萄糖、以2.86体积%的量存在的果糖和以1.4体积%的量存在的木糖醇的组合。
[0370]
iv.使用方法
[0371]
使用外显子跳跃来恢复肌营养不良蛋白阅读框
[0372]
治疗由肌营养不良蛋白基因的框外突变引起的dmd的潜在治疗方法是由称为bmd的肌营养不良蛋白的较轻形式提出的,这种较轻形式是由框内突变引起的。将框外突变转化为框内突变的能力将假设保留mrna阅读框,并产生内部缩短但有功能的肌营养不良蛋白。本公开的反义寡聚物和反义寡聚物缀合物被设计来实现这一目的。
[0373]
pmo与靶向的前体mrna序列的杂交干扰前体mrna剪接复合物的形成,并从成熟mrna中删除外显子52。本公开的反义寡聚物和反义寡聚物缀合物的结构和构象允许与互补序列进行序列特异性碱基配对。通过类似的机制,例如依特立生,它是一种被设计为跳跃肌营养不良蛋白前体mrna的外显子51的pmo,允许与肌营养不良蛋白前体mrna的外显子51中包含的互补序列进行序列特异性碱基配对。
[0374]
含有全部79个外显子的正常肌营养不良蛋白mrna将产生正常的肌营养不良蛋白。图1中的图形描绘了肌营养不良蛋白前体mrna和成熟mrna的一小段,从外显子47到外显子52。每个外显子的形状描绘了外显子之间的密码子是如何分割的;值得注意的是,一个密码子由三个核苷酸组成。矩形的外显子以完整的密码子开始和结束。箭头形的外显子以完整的密码子开始,但以分裂的密码子结束,仅包含密码子的核苷酸第1号。这个密码子的第2号和第3号核苷酸被包含在随后的外显子中,该外显子将以人字形开始。
[0375]
肌营养不良蛋白基因的整个外显子缺失的肌营养不良蛋白mrna通常会导致dmd。图2中的图形说明了一种已知会导致dmd的基因突变(外显子50的缺失)。由于外显子49以完
整的密码子结束并且外显子51以密码子的第二个核苷酸开始,因此外显子49之后的阅读框发生了移位,导致mrna阅读框出框,并在突变下游掺入了不正确的氨基酸。随后缺乏功能性的c端肌营养不良蛋白聚糖结合域,导致产生不稳定的肌营养不良蛋白。
[0376]
依特立生跳越外显子51来恢复mrna阅读框。由于外显子49以完整的密码子结束并且外显子52以密码子的第一个核苷酸开始,因此外显子51的缺失可以恢复阅读框,从而产生内部缩短的具有完整的肌营养不良蛋白聚糖结合位点的肌营养不良蛋白,类似于“框内”bmd突变(图3)。
[0377]
非临床研究支持使用外显子跳跃恢复肌营养不良蛋白mrna开放阅读框来改善dmd表型的可行性。在dmd的营养不良动物模型中进行的大量研究表明,通过外显子跳跃恢复肌营养不良蛋白会导致肌肉力量和功能的可靠改善(sharp 2011;yokota 2009;wu 2008;wu 2011;barton-davis 1999;goyenvalle 2004;gregorevic 2006;yue 2006;welch 2007;kawano 2008;reay 2008;van putten 2012)。一个令人信服的实例来自一项研究,其中外显子跳跃(使用pmo)疗法后的肌营养不良蛋白水平与同一组织的肌肉功能进行了比较。在营养不良的mdx小鼠中,用小鼠特异性pmo处理的胫前肌(ta)肌肉在压力诱导收缩后维持约75%的最大力容量,而未处理的对侧ta肌肉仅维持约25%的最大力容量(p<0.05)(sharp 2011)。在另一项研究中,3只营养不良的cxmd犬在2-5个月大时,接受了针对其基因突变的pmo特异性的外显子跳跃疗法,每周一次,持续5至7周或每隔一周一次,持续22周。在外显子跳跃疗法后,所有3只狗都表现出骨骼肌中广泛的、全身性的肌营养不良蛋白表达,以及相对于基线保持或改善了行走能力(15米跑步测试)。相比之下,未经治疗的年龄匹配的cxmd犬在研究过程中表现出行走能力明显下降(yokota 2009)。
[0378]
在等摩尔浓度下,pmo在mdx小鼠和表达整个人类dmd转录物的人源化dmd(hdmd)小鼠模型中都显示出比硫代磷酸酯具有更多的外显子跳跃活性(heemskirk 2009)。使用逆转录聚合酶链反应(rt-pcr)和蛋白质印迹(wb)在正常人骨骼肌细胞或具有适合于外显子51跳跃的不同突变的dmd患者肌肉细胞中进行体外实验,确定依特立生(pmo)是外显子51跳跃的有效诱导剂。依特立生诱导的外显子51跳跃已在hdmd小鼠模型体内得到证实(arechavala-gomeza 2007)。
[0379]
分析与人肌营养不良蛋白前体mrna外显子52的靶区互补并诱导外显子52跳跃的反义寡聚物或反义寡聚物缀合物的效果的临床结果包括肌营养不良蛋白阳性纤维百分比(pdpf)、六分钟步行测试(6mwt)、丧失行走能力(loa)、北极星移动评价(nsaa)、肺功能测试(pft)、无外力支持下起立(从仰卧位)的能力、新生肌营养素的产生和其它功能测量。
[0380]
在一些实施例中,本公开提供了在具有适合于外显子52跳跃的肌营养不良蛋白基因突变的受试者中产生肌营养不良蛋白的方法,所述方法包含向所述受试者施用如本文所述的反义寡聚物缀合物或其药学上可接受的盐。在一些实施例中,本公开提供了在具有适合于外显子52跳跃的肌营养不良蛋白基因突变的受试者中产生肌营养不良蛋白的方法,所述方法包含向所述受试者施用如本文所述的反义寡聚物或其药学上可接受的盐。在某些实施例中,本公开提供了在患有杜氏肌营养不良(dmd)的受试者中恢复mrna阅读框以诱导肌营养不良蛋白产生的方法,所述受试者具有适合于外显子52跳跃的肌营养不良蛋白基因突变。蛋白质的产生可以通过逆转录聚合酶链反应(rt-pcr)、蛋白质印迹分析或免疫组织化学(ihc)来测量。
[0381]
在一些实施例中,本公开提供了治疗有需要的受试者的dmd的方法,其中所述受试者具有适合于外显子52跳跃的肌营养不良蛋白基因突变,所述方法包含向所述受试者施用如本文所述的反义寡聚物缀合物或其药学上可接受的盐。在一些实施例中,本公开提供了治疗有需要的受试者的dmd的方法,其中所述受试者具有适合于外显子52跳跃的肌营养不良蛋白基因突变,所述方法包含向所述受试者施用如本文所述的反义寡聚物或其药学上可接受的盐。在各种实施例中,对受试者的治疗是通过延迟疾病进展来测量的。在一些实施例中,对受试者的治疗是通过维持受试者的行走能力或减少受试者的行走能力丧失来测量的。在一些实施例中,使用6分钟步行测试(6mwt)来测量行走能力。在某些实施例中,使用北极星移动评价(nsaa)来测量行走能力。
[0382]
在各种实施例中,本公开提供了用于维持患有dmd的受试者的肺功能或减少肺功能丧失的方法,其中所述受试者具有适合于外显子52跳跃的dmd基因突变,所述方法包含向所述受试者施用如本文所述的反义寡聚物缀合物或其药学上可接受的盐。在各种实施例中,本公开提供了用于维持患有dmd的受试者的肺功能或减少肺功能丧失的方法,其中所述受试者具有适合于外显子52跳跃的dmd基因突变,所述方法包含向所述受试者施用如本文所述的反义寡聚物或其药学上可接受的盐。在一些实施例中,肺功能以最大呼气压力(mep)测量。在某些实施例中,肺功能以最大吸气压力(mip)测量。在一些实施例中,肺功能以用力肺活量(fvc)测量。
[0383]
在另一个实施例中,本公开的药物组合物可以在本公开的方法中与碳水化合物以同一制剂或单独的制剂共同施用,如han等人,《自然通讯》7,10981(2016)中所提供,其全部内容以引用的方式并入本文中。在一些实施例中,本公开的药物组合物可以与5%的己糖碳水化合物共同施用。例如,本公开的药物组合物可以与5%的葡萄糖、5%的果糖或5%的甘露糖共同施用。在某些实施例中,本公开的药物组合物可以与2.5%的葡萄糖和2.5%的果糖共同施用。在一些实施例中,本公开的药物组合物可以与选自以下的碳水化合物共同施用:以5体积%的量存在的阿拉伯糖、以5体积%的量存在的葡萄糖、以5体积%的量存在的山梨糖醇、以5体积%的量存在的半乳糖、以5体积%的量存在的果糖、以5体积%的量存在的木糖醇、以5体积%的量存在的甘露糖、各自以2.5体积%的量存在的葡萄糖和果糖的组合,以及以5.7体积%的量存在的葡萄糖、以2.86体积%的量存在的果糖和以1.4体积%的量存在的木糖醇的组合。
[0384]
在各种实施例中,本公开的反义寡聚物或反义寡聚物缀合物与治疗有效量的非类固醇消炎化合物共同施用。在一些实施例中,非类固醇消炎化合物是nf-kb抑制剂。例如,在一些实施例中,nf-kb抑制剂可以是cat-1004或其药学上可接受的盐。在各种实施例中,nf-kb抑制剂可以是水杨酸盐和dha的缀合物。在一些实施例中,nf-kb抑制剂是cat-1041或其药学上可接受的盐。在某些实施例中,nf-kb抑制剂是水杨酸盐和epa的缀合物。在各种实施例中,nf-kb抑制剂是或其药学上可接受的盐。
[0385]
在一些实施例中,非类固醇消炎化合物是tgf-b抑制剂。例如,在某些实施例中,tgf-b抑制剂是ht-100。
[0386]
在某些实施例中,描述了如本文所述的反义寡聚物和反义寡聚物缀合物,其用于疗法。在某些实施例中,描述了如本文所述的反义寡聚物和反义寡聚物缀合物,其用于治疗杜氏肌营养不良。在某些实施例中,描述了如本文所述的反义寡聚物和反义寡聚物缀合物,其用于制造用于疗法的药物。在某些实施例中,描述了如本文所述的反义寡聚物和反义寡聚物缀合物,其用于制造用于治疗杜氏肌营养不良的药物。
[0387]
v.试剂盒
[0388]
本公开还提供了用于治疗遗传病患者的试剂盒,其包含至少一种反义分子(例如,包含seq id no:1中列出的碱基序列的反义寡聚物或含有包含seq id no:1中列出的碱基序列的反义寡聚物的反义寡聚物缀合物),包装在合适的容器中,并附有使用说明。试剂盒还可以含有外围试剂,如缓冲剂、稳定剂等。本领域的普通技术人员应理解,上述方法的应用在鉴定适用于治疗许多其它疾病的反义分子方面具有广泛的应用。在一个实施例中,试剂盒包含根据式(iii)的反义寡聚物缀合物或根据式(iv)的反义寡聚物。
[0389]
实例
[0390]
尽管出于清楚理解的目的已经通过图示和实例的方式对前述公开进行了一些详细的描述,但是根据本公开的教导,对于本领域的普通技术人员将显而易见的是,可以进行某些改变和修改。以下实例仅作为说明而非限制的方式提供。本领域的技术人员将容易识别出多种可以被改变或修改以产生基本类似结果的非关键参数。
[0391]
材料和方法
[0392]
细胞和组织培养处理条件
[0393]
分化的人肌细胞(zenbio,inc.)被用来测量外显子跳跃。具体而言,成肌细胞(zenbio,inc.,skb-f)在37℃和5%co2下在生长培养基(skb-m;zenbio,inc.)中生长至80-90%汇合。通过用分化培养基(skm-d;zenbio,inc.)替换生长培养基来启动分化。为了检测外显子52的跳跃,将1x104个分化细胞铺在24孔板中,并将1ml含有各种浓度pmo或ppmo的分化培养基(skm-d;zenbio,inc.)添加到每个孔中并温育96小时。
[0394]
蛋白质印迹分析
[0395]
对于蛋白质印迹分析,将组织用均质化缓冲液(4%sds,4m尿素,125mm tris-hcl(ph 6.8))以大约5mm直径9至18x20-μm组织切片的比例在133μl缓冲液中均质化。收集相应的裂解液,并使用rc dc蛋白质测定试剂盒按照制造商的说明(biorad目录500-0122)进行蛋白质定量。使用均质化缓冲液将组织提取物样品1:10稀释,以落在bsa标准曲线的范围内。使用25μl蛋白质裂解液、7μl nupage lds样品缓冲液(life technologies目录np0008,carlsbad,california,usa)和3μl nupage还原剂(10x)(life technologies目录np0004)制备样品,使35μl样品中含有所需的蛋白质量。在95℃下加热蛋白质样品5分钟后,将样品离心,上清液上样至nupage novex 10孔,1mm,微型3-8%聚丙烯酰胺三乙酸酯凝胶(life technologies目录ea0375),每条泳道最大总蛋白质负载量为50μg。凝胶在室温下以150伏运行,直到染料前沿已流出凝胶。在室温下,使用nupage转移缓冲液(life technologies np006-1)、10%甲醇和0.1%nupage抗氧化剂(life technologies np0005)以30伏将所得蛋白质凝胶转移到pvdf膜(life technologies目录lc2007)达75分钟。
[0396]
蛋白质转移后,将pvdf膜浸入ttbs缓冲液(1x tbs(amresco目录j640-4l),0.1%(v/v)tween-20)中。将膜转移到阻断缓冲液(含5%(w/v)脱脂奶粉(lab scientific目录m0841)的ttbs)中,并在4℃下轻轻摇动浸泡过夜。阻断后,将膜在室温下在使用阻断缓冲液1:20稀释的dys1(leica目录ncl-dys1)中温育60分钟,或在室温下在用阻断缓冲液1:100,000稀释的抗-辅肌动蛋白抗体(sigma-aldrich目录na931v)中温育20分钟,然后进行六次洗涤(每次用ttbs洗涤五分钟)。抗小鼠igg与辣根过氧化物酶(ge healthcare目录na931v)缀合,用阻断缓冲液1:40,000稀释,并加入到膜上45分钟(dys1)或15分钟(-辅肌动蛋白),随后再次进行六次洗涤。使用eclprime western检测试剂盒(ge healthcare目录rpn2232),将膜暴露在凝胶上并进行相应的显影。显影后的膜用imagequant tl plus软件(8.1版)进行扫描和分析,并使用graphpad软件进行线性回归分析。
[0397]
每个蛋白质印迹凝胶包括使用从正常组织(小鼠四头肌、膈膜或心脏)中提取的总蛋白稀释到例如64%、16%、4%、1%和0.25%(参见例如图5a和5b)并掺入到dmd组织(例如,mdx小鼠四头肌、膈膜或心脏,或nhp四头肌、膈膜或平滑肌(gi))提取物中制备的4或5点肌营养不良蛋白标准曲线。如上所述处理标准曲线样品。通过将肌营养不良蛋白条带强度与凝胶标准曲线进行比较,以野生型肌营养不良蛋白水平的百分比(%wt)形式确定肌营养不良蛋白水平。
[0398]
rt-pcr分析
[0399]
对于rt-pcr分析,使用illustra ge旋转试剂盒按照制造商的方案从细胞中分离rna。外显子52跳跃是通过rt-pcr用结合外显子50的正向引物seq id no:5(5'-ctctgagtggaaggcggtaa-3')和结合外显子53的反向引物seq id no:6(5'-acctgctcagcttcttcctt-3')来测量的。小鼠外显子23跳跃是通过rt-pcr用正向引物-seq id no:7(5'-cacatctttgatggtgtgagg-3')和反向引物seq id no:8(5'-caacttcagccatccatttctg-3')来测量的。
[0400]
rna进行rt-pcr后,使用caliper机对样品进行分析,该机使用凝胶毛细管电泳。外显子跳跃百分比用以下公式计算:(跳越条带的曲线下面积)/(跳越和未跳越条带的曲线下面积之和)x100。
[0401]
免疫组织化学:肌营养不良蛋白染色:
[0402]
小鼠四头肌的10微米冷冻组织切片用于通过含肌营养不良蛋白一抗(稀释度1:250,兔,abcam,目录号ab15277)的10%山羊血清+含1%bsa的pbs和含二抗alexa-fluoro 488山羊抗兔(稀释度1:1000)的10%山羊血清+1%bsa来检测肌营养不良蛋白。
[0403]
吗啉代亚基的制备
[0404][0405]
方案1:pmo亚基的一般合成路线
[0406]
参照方案1,其中b代表碱基配对部分,可以如图所示由相应的核糖核苷(1)制备吗啉代亚基。吗啉代亚基(2)可以任选地通过与合适的保护基前体(例如三苯甲基氯)反应而受到保护。3'保护基通常在固态寡聚物合成过程中被去除,如下文更详细地描述。碱基配对部分可以适当地保护用于固相寡聚物合成。合适的保护基包括用于腺嘌呤和胞嘧啶的苯甲酰基,用于鸟嘌呤的苯乙酰基,以及用于次黄嘌呤(i)的新戊酰氧基甲基。新戊酰氧基甲基可以引入到次黄嘌呤杂环碱基的n1位上。虽然可以采用未保护的次黄嘌呤亚基,但当碱基被保护时,活化反应的产率要高得多。其它合适的保护基包括美国专利号8,076,476中公开的那些,该专利以全文引用的方式并入本文中。
[0407]
3与活化的磷化合物4的反应产生具有所需连接部分5的吗啉代亚基。
[0408]
结构4的化合物可以使用本领域技术人员已知的许多方法来制备。然后如上所述与吗啉代部分偶合。
[0409]
结构5的化合物可用于固相寡聚物合成中,以制备包含亚基间键的寡聚物。这样的方法在本领域中是众所周知的。简而言之,结构5的化合物可以在5'端进行修饰以含有连接至固体支撑物的连接基团。一旦被支撑,就去除5的保护基(例如,在3'-端的三苯甲基),并使游离胺与结构5的第二化合物的活化的磷部分反应。重复此顺序,直到获得所需长度的寡聚物。如果需要进行3'修饰,末端3'端的保护基可以被去除或留在上面。可以使用许多方法将寡聚物从固体支撑物上去除,或者例如用碱处理以裂解与固体支撑物的连接。
[0410]
在实例中更详细地描述了本公开的一般吗啉代寡聚物和特定吗啉代寡聚物的制备。
[0411]
吗啉代寡聚物的制备
[0412]
根据方案2,使用以下方案进行本公开的化合物的制备。
[0413][0414][0415]
方案2:活性尾酸的制备
[0416]
氨基甲酸三苯甲基哌嗪苯基酯35的制备:向冷却的化合物11在二氯甲烷(6ml/g 11)中的悬浮液中添加碳酸钾(3.2eq)在水(4ml/g碳酸钾)中的溶液。向该两相混合物中缓慢添加氯甲酸苯酯(1.03eq)在二氯甲烷(2g/g氯甲酸苯酯)中的溶液。将反应混合物升温至20℃。在反应完成(1-2小时)后,分离各层。将有机层用水洗涤,并且经无水碳酸钾干燥。通过从乙腈中结晶分离出产物35。
[0417]
氨基甲酸酯醇36的制备:将氢化钠(1.2eq)悬浮于1-甲基-2-吡咯烷酮(32ml/g氢化钠)中。向该悬浮液中添加三乙二醇(10.0eq)和化合物35(1.0eq)。将所得浆液加热至95
℃。在反应完成(1-2小时)后,将混合物冷却至20℃。向该混合物中添加30%二氯甲烷/甲基叔丁基醚(v:v)和水。将含有产物的有机层依次用naoh水溶液、琥珀酸水溶液和饱和氯化钠水溶液洗涤。通过从二氯甲烷/甲基叔丁基醚/庚烷中结晶分离出产物36。
[0418]
尾酸37的制备:向化合物36在四氢呋喃(7ml/g 36)中的溶液中添加琥珀酸酐(2.0eq)和dmap(0.5eq)。将混合物加热至50℃。在反应完成(5小时)后,将混合物冷却至20℃,并用nahco3水溶液调节至ph 8.5。添加甲基叔丁醚,并将产物萃取到水层中。添加二氯甲烷,并将混合物用柠檬酸水溶液调节至ph 3。将含有产物的有机层用ph=3的柠檬酸盐缓冲液和饱和氯化钠水溶液的混合物洗涤。这种37的二氯甲烷溶液无需分离即可用于制备化合物38。
[0419]
38的制备:向化合物37的溶液中添加n-羟基-5-降冰片烯-2,3-二羧酸酰亚胺(honb)(1.02eq)、4-二甲基氨基吡啶(dmap)(0.34eq),然后添加1-(3-二甲基氨基丙基)-n'-乙基碳化二亚胺盐酸盐(edc)(1.1eq)。将混合物加热至55℃。在反应完成(4-5小时)后,将混合物冷却至20℃,并依次用1:10.2m柠檬酸/盐水和盐水洗涤。将二氯甲烷溶液进行溶剂交换成丙酮,然后交换成n,n-二甲基甲酰胺,并通过从丙酮/n,n-二甲基甲酰胺中沉淀到饱和氯化钠水溶液中来分离产物。将粗产物在水中重新浆化数次以去除残留的n,n-二甲基甲酰胺和盐类。
[0420]
pmo合成方法a:使用二硫化物锚固剂
[0421]
通过在固相合成过程中掺入亚基的程序,在二甲基咪唑啉酮(dmi)中将活化的“尾部”引入到锚固负载的树脂上。
[0422][0423]
方案3:用于合成吗啉代寡聚物的固体支撑物的制备
[0424]
该程序是在带有粗孔(40-60μm)的玻璃料、顶置式搅拌器和三通特氟龙旋塞的硅烷化、带夹套的肽容器(chemglass,nj,usa)中进行的,以使n2冒泡向上通过玻璃料或抽真空。
[0425]
以下程序中的树脂处理/洗涤步骤由两个基本操作组成:树脂流化或搅拌床反应器和溶剂/溶液萃取。对于树脂流化,将旋塞定位成允许n2向上流经玻璃料,并将指定的树脂处理/洗涤液添加到反应器中,使其渗透并完全润湿树脂。然后开始混合,并且将树脂浆料混合指定的时间。对于溶剂/溶液萃取,停止混合和n2流,并启动真空泵,然后将旋塞定位
成允许排空树脂处理/洗涤液至废料。除非另有说明,否则所有树脂处理/洗涤液体积均为15ml/g。
[0426]
在硅烷化的带夹套的肽容器中,向氨基甲基聚苯乙烯树脂(100-200目;基于氮取代的~1.0mmol/g负载;75g,1eq,polymer labs,uk,部件号1464-x799)中添加1-甲基-2-吡咯烷酮(nmp;20ml/g树脂)并在混合下使树脂溶胀1-2小时。排空溶胀溶剂后,用二氯甲烷(2x1-2min)、含5%二异丙基乙胺的25%异丙醇/二氯甲烷(2x3-4min)和二氯甲烷(2x1-2min)洗涤树脂。在排空最后的洗涤液后,用二硫化物锚固剂34在1-甲基-2-吡咯烷酮中的溶液(0.17m;15ml/g树脂,~2.5eq)处理树脂,并将树脂/试剂混合物在45℃下加热60小时。反应完成后,停止加热,抽空锚固剂溶液,并用1-甲基-2-吡咯烷酮(4x3-4min)和二氯甲烷(6x1-2min)洗涤树脂。将树脂用10%(v/v)二碳酸二乙酯在二氯甲烷中的溶液(16ml/g;2x5-6min)处理,然后用二氯甲烷(6x1-2min)洗涤。将树脂39在n2流下干燥1-3小时,然后在真空下干燥至恒重(
±
2%)。产率:原始树脂重量的110-150%。
[0427]
氨基甲基聚苯乙烯-二硫化物树脂的负载量的测定:树脂的负载量(潜在可用反应位点的数量)是通过光谱法测定每克树脂中三苯甲基(triphenylmethyl/trityl)的数量来确定。
[0428]
将已知重量的干燥树脂(25
±
3mg)转移到硅烷化的25ml容量瓶中,并添加~5ml的2%(v/v)三氟乙酸的二氯甲烷溶液。通过轻轻旋转将内容物混合,然后使其静置30分钟。用额外的2%(v/v)三氟乙酸的二氯甲烷溶液使体积达到25ml,并将内容物彻底混合。使用容积式移液管将等分的含三苯甲基的溶液(500μl)转移到10ml容量瓶中,并用甲磺酸使体积达到10ml。
[0429]
通过431.7nm处的uv吸光度测量最终溶液中的三苯甲基阳离子含量,并使用适当的体积、稀释度、消光系数(ε:41μmol-1cm-1)和树脂重量以每克树脂中的三苯甲基(μmol/g)计算树脂负载量。一式三份进行测定,并计算平均负载量。
[0430]
该实例中的树脂负载程序将为树脂提供约500μmol/g的负载量。如果在室温下进行二硫化物锚固剂掺入步骤24小时,则可获得300-400μmol/g的负载量。
[0431]
尾部负载:使用与制备氨基甲基聚苯乙烯-二硫化物树脂相同的设置和体积,可将尾部引入固体支撑物中。首先将负载有锚固剂的树脂在酸性条件下脱保护,并在偶合之前中和所得材料。对于偶合步骤,使用38(0.2m)在含有4-乙基吗啉(nem,0.4m)的dmi中的溶液代替二硫化物锚固剂溶液。在45℃下2小时后,将树脂39用含5%二异丙基乙胺的25%异丙醇/二氯甲烷洗涤两次,并用dcm洗涤一次。向树脂中添加苯甲酸酐(0.4m)和nem(0.4m)的溶液。25分钟后,将反应器夹套冷却至室温,将树脂用含5%二异丙基乙胺的25%异丙醇/二氯甲烷洗涤两次,并用dcm洗涤八次。过滤树脂40并在高真空下干燥。树脂40的负载量定义为在尾部负载中使用的原始氨基甲基聚苯乙烯-二硫化物树脂39的负载量。
[0432]
固相合成:在gilson ams-422自动多肽合成仪上,在2ml gilson聚丙烯反应柱(部件号3980270)中制备吗啉代寡聚物。当柱子停在合成仪上时,将带有水流通道的铝块放在柱子周围。ams-422将交替地添加试剂/洗涤液,保持指定的时间,并使用真空抽空柱子。
[0433]
对于长度至多约25个亚基的寡聚物,优选负载量接近500μmol/g的树脂的氨基甲基聚苯乙烯-二硫化物树脂。对于较大的寡聚物,优选负载量为300-400μmol/g的树脂的氨基甲基聚苯乙烯-二硫化物树脂。如果需要具有5'-尾部的分子,则以相同的负载准则选择
已负载尾部的树脂。
[0434]
制备以下试剂溶液:
[0435]
去三苯甲基化溶液:含10%氰基乙酸(w/v)的4:1二氯甲烷/乙腈;
[0436]
中和溶液:含5%二异丙基乙胺的3:1二氯甲烷/异丙醇;以及
[0437]
偶合溶液:含0.18m(或对于生长长度超过20个亚基的寡聚物为0.24m)具有所需碱基和连接类型的活化的吗啉代亚基和0.4m n乙基吗啉的1,3-二甲基咪唑啉酮。
[0438]
二氯甲烷(dcm)用作过渡洗涤液,分离不同的试剂溶液洗涤液。
[0439]
在合成仪上,在块设置为42℃的情况下,向每个含有30mg氨基甲基聚苯乙烯-二硫化物树脂(或尾部树脂)的柱子中添加2ml 1-甲基-2-吡咯烷酮,并使其在室温下静置30分钟。用2ml二氯甲烷洗涤2次后,采用以下合成循环:
[0440][0441]
将各个寡聚物的序列编程到合成仪中,使每个柱子以适当的顺序接收适当的偶合溶液(a、c、g、t、i)。当柱子中的寡聚物完成了其最后亚基的结合时,将柱子从块中移出,用由含有0.89m 4-乙基吗啉的4-甲氧基三苯基甲基氯(0.32m在dmi中)构成的偶合溶液手动进行最终循环。
[0442]
从树脂上裂解并去除碱基和主链保护基:甲氧基三苯甲基化后,将树脂用2ml 1-甲基-2-吡咯烷酮洗涤8次。添加1ml由0.1m 1,4-二硫苏糖醇(dtt)和0.73m三乙胺在1-甲基-2-吡咯烷酮中组成的裂解溶液,将柱子封盖,并使其在室温下静置30分钟。之后,将溶液排入12ml惠顿小瓶中。将极大收缩的树脂用300μl裂解溶液洗涤两次。向溶液中添加4.0ml浓氨水(储存在-20℃下),将小瓶盖紧(用特氟龙内衬的螺旋盖),旋转混合物以混合溶液。将小瓶置于45℃烘箱中16-24小时,以实现碱基和主链保护基的裂解。
[0443]
粗产物纯化:从烘箱中取出小瓶中的氨水溶液,并使其冷却至室温。将溶液用20ml的0.28%氨水稀释,并通过含有macroprep hq树脂(biorad)的2.5x10 cm色谱柱。用盐梯度(a:0.28%氨水与b:1m氯化钠在0.28%氨水中;60分钟内0-100%b)洗脱含甲氧基三苯甲基的峰。将合并的洗脱分汇集,并根据所需产物进一步处理。
[0444]
吗啉代寡聚物的脱甲氧基三苯甲基化:将macroprep纯化得到的汇集洗脱分用1m h3po4处理,以将ph降至2.5。初步混合后,样品在室温下静置4分钟,此时用2.8%氨水/水将其中和至ph 10-11。产物通过固相萃取(spe)纯化。
[0445]
spe柱填充和调节:将amberchrome cg-300m(rohm and haas;philadelphia,pa)(3ml)填充至20ml烧结柱(biorad econo-pac色谱柱(732-1011))中,并用3ml以下试剂冲洗树脂:0.28%nh4oh/80%乙腈;0.5m naoh/20%乙醇;水;50mm h3po4/80%乙腈;水;0.5naoh/20%乙醇;水;0.28%nh4oh。
[0446]
spe纯化:将来自脱甲氧基三苯甲基化的溶液装载到色谱柱上,并用3-6ml 0.28%氨水冲洗树脂三次。将惠顿小瓶(12ml)置于色谱柱下,用2ml含45%乙腈的0.28%氨水洗涤两次,洗脱出产物。
[0447]
产物分离:将溶液在干冰中冷冻,并将小瓶置于冷冻干燥器中,以产生蓬松的白色粉末。将样品溶解在水中,使用注射器通过0.22微米过滤器(pall life sciences,acrodisc 25mm注射器过滤器,带有0.2微米的ht tuffryn膜)过滤,并在uv分光光度计上测量光密度(od),以确定存在的寡聚物的od单位,以及分配样品进行分析。然后将溶液放回惠顿小瓶中进行冻干。
[0448]
通过maldi分析吗啉代寡聚物:maldi-tof质谱法用于确定纯化中洗脱分的组成,并为寡聚物的身份(分子量)提供证据。在用3,5-二甲氧基-4-羟基肉桂酸(芥子酸)、3,4,5-三羟基苯乙酮(thap)或α-氰基-4-羟基肉桂酸(hcca)的溶液作为基质进行稀释后运行样品。
[0449]
pmo合成方法b:使用ncp2锚固剂
[0450]
ncp2锚固剂合成:
[0451]
1.4-氟-3-硝基苯甲酸甲酯(1)的制备
[0452][0453]
向100l烧瓶中装入12.7kg 4-氟-3-硝基苯甲酸,添加40kg甲醇和2.82kg浓硫酸。将混合物在回流(65℃)下搅拌36小时。将反应混合物冷却至0℃。在38℃下形成晶体。混合物在0℃下保持4小时,然后在氮气下过滤。洗涤100l烧瓶,并用已冷却至0℃的10kg甲醇洗涤滤饼。将固体滤饼在漏斗上干燥1小时,转移到托盘,并在室温下的真空烘箱中干燥至恒重13.695kg的4-氟-3-硝基苯甲酸甲酯(100%产率;hplc 99%)。
[0454]
2.3-硝基-4-(2-氧代丙基)苯甲酸的制备
[0455]
a.(z)-4-(3-羟基-1-甲氧基-1-氧代丁-2-烯-2-基)-3-硝基苯甲酸甲酯(2)
[0456][0457]
向100l烧瓶中装入来自先前步骤的3.98kg 4-氟-3-硝基苯甲酸甲酯(1)、9.8kg dmf、2.81kg乙酰乙酸甲酯。将混合物搅拌并冷却至0℃。历时约4小时向其中添加3.66kg dbu,同时将温度维持在5℃或以下。将混合物再搅拌1小时。向反应烧瓶中添加8.15kg柠檬酸在37.5kg纯水中的溶液,同时将反应温度维持在15℃或以下。添加后,将反应混合物再搅拌30分钟,然后在氮气下过滤。将湿滤饼连同14.8kg纯水一起返回到100l烧瓶中。将浆液搅拌10分钟,然后过滤。将湿滤饼再次返回到100l烧瓶中,用14.8kg纯水制浆10分钟,然后过滤得到粗制的(z)-4-(3-羟基-1-甲氧基-1-氧代丁-2-烯-2-基)-3-硝基苯甲酸甲酯。
[0458]
b.3-硝基-4-(2-氧代丙基)苯甲酸
[0459][0460]
将粗制的(z)-4-(3-羟基-1-甲氧基-1-氧代丁-2-烯-2-基)-3-硝基苯甲酸甲酯在氮气下装入100l反应烧瓶中。向其中添加14.2kg 1,4-二噁烷并搅拌。历时2小时向混合物中添加16.655kg浓hcl和13.33kg纯水的溶液(6m hcl),同时将反应混合物的温度维持在15℃以下。当添加完成后,将反应混合物在回流(80℃)下加热24小时,冷却至室温,并在氮气下过滤。将固体滤饼用14.8kg纯水湿磨,过滤,再用14.8kg纯水湿磨并过滤。将固体与39.9kg dcm一起返回到100l烧瓶中,并在搅拌下回流1小时。添加1.5kg纯水以溶解剩余的固体。将底部有机层分到预热的72l烧瓶中,然后返回到清洁干燥的100l烧瓶中。将溶液冷却至0℃,保持1小时,然后过滤。固体滤饼用9.8kg dcm和5kg庚烷的溶液各洗涤两次,然后在漏斗上干燥。将固体转移到托盘并干燥至恒重1.855kg的3-硝基-4-(2-氧代丙基)苯甲酸。化合物1的总产率为42%。hplc 99.45%。
[0461]
3.n-三苯甲基哌嗪琥珀酸盐(ntp)的制备
[0462][0463]
在氮气下,向72l带夹套的烧瓶中装入1.805kg三苯甲基氯和8.3kg甲苯(tpc溶液)。搅拌混合物,直到固体溶解。在氮气下,向100l带夹套的反应烧瓶中添加5.61kg哌嗪、19.9kg甲苯和3.72kg甲醇。将混合物搅拌并冷却至0℃。历时4小时向其中缓慢逐份添加tpc溶液,同时将反应温度维持在10℃或以下。将混合物在10℃下搅拌1.5小时,然后使其升温至14℃。将32.6kg的纯水装入72l烧瓶中,然后转移到100l烧瓶中,同时将内部批料温度维持在20+/-5℃。使各层分开,并将底部水层分离并储存。将有机层每次用32kg纯水萃取三次,将水层分离并与储存的水溶液合并。
[0464]
将剩余的有机层冷却至18℃,并将847g琥珀酸在10.87kg纯水中的溶液逐份缓慢地添加到有机层中。将混合物在20+/-5℃下搅拌1.75小时。将混合物过滤,并将固体用2kg tbme和2kg丙酮洗涤,然后在漏斗上干燥。每次用5.7kg丙酮将滤饼湿磨两次,并在两次研磨之间进行过滤并用1kg丙酮洗涤。将固体在漏斗上干燥,然后转移到托盘上,并在室温下在真空烘箱中干燥至恒重2.32kg的ntp。产率80%。
[0465]
4.(4-(2-羟丙基)-3-硝基苯基)(4-三苯甲基哌嗪-1-基)甲酮的制备
[0466]
a.1-(2-硝基-4(4-三苯甲基哌嗪-1-羰基)苯基)丙-2-酮的制备
[0467][0468]
在氮气下,向100l带夹套的烧瓶中装入2kg 3-硝基-4-(2-氧代丙基)苯甲酸(3)、18.3kg dcm和1.845kg n-(3-二甲基氨基丙基)-n'-乙基碳化二亚胺盐酸盐(edc.hcl)。搅拌溶液直至形成均匀的混合物。在室温下历时30分钟添加3.048kg ntp,并搅拌8小时。将5.44kg的纯净水添加到反应混合物中并搅拌30分钟。使各层分离,并将含有产物的底部有机层沥干并储存。水层用5.65kg的dcm萃取两次。合并的有机层用1.08kg氯化钠在4.08kg纯水中的溶液洗涤。有机层经1.068kg的硫酸钠干燥并过滤。用1.3kg的dcm洗涤硫酸钠。将合并的有机层用252g硅胶制成浆液,并通过含有252g硅胶床的过滤漏斗过滤。用2kg的dcm洗涤硅胶床。将合并的有机层在旋转蒸发器上蒸发。向残余物中添加4.8kg的thf,然后在旋转蒸发器上蒸发,直到在thf中达到2.5体积的粗制1-(2-硝基-4(4-三苯甲基哌嗪-1-羰基)苯基)丙-2-酮。
[0469]
b.(4-(2-羟丙基)-3-硝基苯基)(4-三苯甲基哌嗪-1-基)甲酮(5)的制备
[0470][0471]
在氮气下,向100l带夹套的烧瓶中装入3600g来自先前步骤的4和9800g thf。将搅拌后的溶液冷却至≤5℃。溶液用11525g乙醇稀释,并在≤5℃下历时约2小时添加194g硼氢化钠。将反应混合物在≤5℃下再搅拌2小时。通过缓慢添加约1.1kg氯化铵在约3kg水中的溶液淬灭反应,以保持温度≤10℃。将反应混合物再搅拌30分钟,过滤以去除无机物,重新装入100l带夹套的烧瓶中,并用23kg dcm萃取。分离有机层,将水层每次用4.7kg dcm再萃取两次。合并的有机层用约800g氯化钠在约3kg水中的溶液洗涤,然后经2.7kg硫酸钠干燥。过滤悬浮液,并用2kg dcm洗涤滤饼。将合并的滤液浓缩至2.0体积,用约360g乙酸乙酯稀释,并蒸发。将粗产物装载到在氮气下用dcm填充的4kg二氧化硅的硅胶柱上,并用含2.3kg乙酸乙酯的7.2kg dcm洗脱。蒸发合并的洗脱分,并将残余物溶解在11.7kg甲苯中。过滤甲苯溶液,并将滤饼每次用2kg甲苯洗涤两次。将滤饼干燥至恒重2.275kg的化合物5(从化合物3得到的产率为46%),hplc为96.99%。
[0472]
5.(1-(2-硝基-4-(4-三苯甲基哌嗪-1羰基)苯基)丙-2-基)碳酸2,5-二氧代吡咯烷-1-基酯(ncp2锚固剂)的制备
[0473][0474]
在氮气下,向100l带夹套的烧瓶中装入4.3kg化合物5(通过h
1 nmr基于残余甲苯调节重量;在此之后将所有试剂相应地按比例调整)和12.7kg吡啶。向其中装入3.160kg dsc(78.91重量%,根据h
1 nmr),同时将内部温度维持在≤35℃。将反应混合物在环境中老化约22小时,然后过滤。用200g吡啶洗涤滤饼。分两批,每批包含1/2的滤液体积,将滤液洗涤液缓慢装入100l带夹套的烧瓶中,该烧瓶中含有约11kg柠檬酸在约50kg水中的溶液,并搅拌30分钟以使固体沉淀。用过滤漏斗收集固体,每次洗涤用4.3kg水洗涤两次,并在真空下在过滤漏斗上干燥。
[0475]
将合并的固体装入100l带夹套的烧瓶中,并溶解在28kg dcm中,用900g碳酸钾在
4.3kg水中的溶液洗涤。在1小时之后,使各层分离并去除水层。将有机层用10kg水洗涤,分离并经3.5kg硫酸钠干燥。过滤dcm,蒸发,并在真空下干燥,得到6.16kg ncp2锚固剂(114%产率)。
[0476]
负载ncp2锚固剂的树脂的合成
[0477]
向具有特氟龙旋塞的75l固相合成反应器中装入约52l nmp和2300g氨基甲基聚苯乙烯树脂。将树脂在nmp中搅拌以溶胀约2小时,然后沥干。将树脂每次洗涤用约4l dcm洗涤两次,然后每次洗涤用39l中和溶液洗涤两次,然后每次洗涤用39ldcm洗涤两次。将ncp2锚固剂溶液缓慢添加到搅拌的树脂溶液中,在室温下搅拌24小时,并沥干。将树脂每次洗涤用39l nmp洗涤四次,并且每次洗涤用39l dcm洗涤六次。将树脂用1/2dedc封端溶液处理并搅拌30分钟,沥干,再用第2个1/2dedc封端溶液处理并搅拌30分钟,沥干。将树脂每次洗涤用39l dcm洗涤六次,然后在烘箱中干燥至恒重3573.71g的负载锚固剂的树脂。
[0478]
使用ncp2锚固剂制备吗啉代寡聚物
[0479]
pmo,格罗狄森(pmo-g;seq id no:9)原料药物质的50l固相合成的代表性实例
[0480]
1.材料
[0481]
表2:起始材料
[0482][0483][0484]
起始材料的化学结构:
[0485]
a.活化的eg3尾部
[0486][0487]
b.活化的c亚基(关于制备,参见美国专利号8,067,571)
[0488][0489]
c.活化的a亚基(关于制备,参见美国专利号8,067,571)
[0490][0491]
d.活化的dpg亚基(关于制备,参见wo 2009/064471)
[0492][0493]
e.活化的t亚基(关于制备,参见wo 2013/082551)
[0494][0495]
f.负载锚固剂的树脂
[0496][0497]
其中r1是支撑介质。
[0498]
表3:用于格罗狄森原料药物质的固相寡聚物合成的溶液的描述
[0499][0500]
2.格罗狄森原料药物质的合成
[0501]
a.树脂溶胀
[0502]
将750g负载锚固剂的树脂和10.5l nmp装入50l硅烷化反应器中并搅拌3小时。排干nmp,并将负载锚固剂的树脂每次用5.5l dcm洗涤两次,每次用5.5l 30%tfe/dcm洗涤两次。
[0503]
b.循环0:eg3尾部偶合
[0504]
将负载锚固剂的树脂每次用5.5l 30%tfe/dcm洗涤三次并沥干,用5.5l cyfta溶液洗涤15分钟并沥干,再用5.5l cytfa溶液洗涤15分钟不沥干,向其中装入122ml 1:1nem/dcm,将悬浮液搅拌2分钟并沥干。将树脂用5.5l中和溶液洗涤两次,持续5分钟并沥干,然后每次用5.5l dcm洗涤两次并沥干。将706.2g活化的eg3尾部(mw 765.85)和234ml nem在3l dmi中的溶液装入树脂,在室温下搅拌3小时并沥干。将树脂每次用5.5l中和溶液洗涤两次,每次洗涤5分钟,用5.5l dcm洗涤一次并沥干。装入374.8g苯甲酸酐和195ml nem在2680ml nmp中的溶液,搅拌15分钟并沥干。将树脂与5.5l中和溶液一起搅拌5分钟,然后用5.5l dcm洗涤一次并每次用5.5l 30%tfe/dcm洗涤两次。将树脂悬浮在5.5l 30%tfe/dcm中并保持14小时。
[0505]
c.亚基偶合循环1-30
[0506]
i.偶合前处理
[0507]
在图18所述的每个偶合循环之前,将树脂:1)用30%tfe/dcm洗涤;2)a)用cytfa溶液处理15分钟并沥干,b)用cytfa溶液处理15分钟,向其中添加1:1nem/dcm,搅拌并沥干;3)与中和溶液一起搅拌三次;4)用dcm洗涤两次。参见图18。
[0508]
ii.偶合后处理
[0509]
在如图18所述排出每种亚基溶液后,将树脂:1)用dcm洗涤;和2)用30%tfe/dcm洗涤两次。如果在下一偶合循环之前将树脂保持一段时间,则不排出第二次tfe/dcm洗涤液,并且将树脂保留在所述tfe/dcm洗涤溶液中。参见图18。
[0510]
iii.活化的亚基偶合循环
[0511]
如图18所述进行偶联循环。
[0512]
iv.最终ipa洗涤
[0513]
如图18所述进行最后的偶合步骤后,将树脂每次用19.5l ipa洗涤8次,并在室温下真空干燥约63.5小时,干重为4857.9g。
[0514]
c.裂解
[0515]
将上述树脂结合的格罗狄森原料药物质分为两批,每批按以下方式处理。一批1619.3g的树脂:1)与10l nmp一起搅拌2小时,然后将nmp排出;2)每次用10l 30%tfe/dcm洗涤三次;3)用10l cytfa溶液处理15分钟;4)用10l cytfa溶液处理15分钟,然后向其中添加130ml 1:1 nem/dcm,搅拌2分钟并排出。将树脂每次用10l中和溶液处理三次,用10l dcm洗涤六次,每次用10l nmp洗涤八次。将树脂用1530.4g dtt和2980dbu在6.96l nmp中的裂解溶液处理
[0516]
2小时,以使依特立生原料药物质从树脂上脱离。将裂解溶液排出并保留在另一个容器中。反应器和树脂用4.97l nmp洗涤,将nmp与裂解溶液合并。
[0517]
d.脱保护
[0518]
将合并的裂解溶液和nmp洗涤液转移到压力容器中,向其中添加39.8l已在冰箱中
冷却至-10℃至-25℃的nh4oh(nh3·
h2o)。将压力容器密封并加热到45℃持续16小时,然后冷却到25℃。将该含有格罗狄森原料药物质的脱保护溶液用纯水以3:1稀释,并用2m磷酸将ph调节至3.0,然后用nh4oh调节至ph 8.03。hplc:c18 77.552%和scx-10 73.768%。
[0519]
格罗狄森(pmo-g)原料药物质的纯化
[0520]
将上述d部分的含有格罗狄森原料药物质的脱保护溶液上样到toyopearl super-q 650s阴离子交换树脂(tosoh bioscience)的色谱柱上,并以0-35%b的梯度在17柱体积上洗脱(缓冲液a:10mm氢氧化钠;缓冲液b:1m氯化钠在10mm氢氧化钠中),并将可接受纯度的洗脱分(c18和scx hplc)汇集到纯化的药物产品溶液中。hplc:93.571%(c18)88.270%(scx)。
[0521]
将纯化后的药物物质溶液脱盐并冻干,得到1450.72g纯化的格罗狄森药物物质。产率54.56%;hplc:93.531%(c18)88.354%(scx)。
[0522]
表5.缩写
[0523][0524][0525]
cpp缀合物的代表性实例
[0526][0527]
分析程序:使用芥子酸(sa)基质在bruker autoflextm speed上记录基质辅助的激光解吸电离飞行时间质谱(maldi-tof-ms)。在配备3000二极管阵列检测器和propactm scx-20色谱柱(250x4mm)的thermo dionex ultimate 3000系统上进行scx-hplc,流速为
1.0ml/min(ph=2;30℃柱温)。流动相为a(25%乙腈在含有24mm h3po4的水中)和b(25%乙腈在含有1m kcl和24mm h3po4的水中)。采用梯度洗脱:0min,35%b;2min,35%b;22min,80%b;25min,80%b;25.1min,35%b;30min,35%b。
[0528]
向pmo4658(1.82g,0.177mmol,通过冻干新鲜干燥两天;seq id no:10)、ac-l-arg-l-arg-l-arg-l-arg-l-arg-l-arg-gly-oh六氟乙酸盐(614.7mg,0.354mmol)和1-[双(二甲基氨基)亚甲基]-1h-1,2,3-三唑并[4,5-b]吡啶鎓3-氧化物六氟磷酸盐(hatu,134.4mg,0.354mmol)的混合物中添加二甲亚砜(dmso,20ml)。将混合物在室温下搅拌3分钟,然后添加n,n-二异丙基乙胺(dipea,68.5mg,0.530mmol)。5分钟后,浑浊的混合物变成澄清溶液。通过scx-hplc监测反应。2小时后,添加20ml的10%氢氧化铵溶液(2.8%nh3)。将混合物在室温下再搅拌2小时。通过添加400ml水来终止反应。将三氟乙醇(2.0ml)添加到溶液中。
[0529]
将溶液分为两部分,每部分用wcx柱(每柱10g树脂)纯化。首先用20%乙腈水溶液(v/v)洗涤每个wcx柱,以去除pmo4658起始材料。当maldi-tof质谱分析显示不存在pmo4658信号时,停止洗涤(每柱225ml)。然后用水洗涤每一柱(每柱100ml)。所需产物ppmo4658用2.0m胍hcl洗脱(每柱140ml)。将纯化的ppmo4658溶液汇集在一起,然后分成两部分,每部分用spe柱(每柱10克树脂)脱盐。
[0530]
首先用1.0m nacl水溶液(每柱100ml)洗涤spe柱,以生成ppmo46581的六盐酸盐。然后将每个spe柱用水洗涤(每柱200ml)。最终脱盐的ppmo-g用50%乙腈水溶液洗脱(v/v,每柱150ml)。减压抽空去除乙腈。将所得水溶液冻干,以获得所需的缀合物ppmo4658六盐酸盐(1.93g,94.5%产率)。
[0531]
实例1:pmo#1
[0532]
使用上文针对pmo-g所述的pmo合成方法b方案,合成了pmo#1:
[0533][0534]
其中每个nu从1至25并且5'至3'是:
[0535]
[0536]
其中a是c是g是并且t是
[0537]
hplc:93.33%;
[0538]
实例2:ppmo#1
[0539]
使用上文针对ppmo4658的制备所述的方案,由pmo#1合成了ppmo#1:
[0540][0541]
其中每个nu从1至25并且5'至3'是:
[0542][0543]
其中a是c是g是并且t是
[0544]
hplc:89.45%。
[0545]
实例3:体外(成肌细胞)外显子52跳跃
[0546]
针对在健康人成肌细胞中的dmd外显子52跳跃评估了如下表所述的两种靶向人肌营养不良蛋白(dmd)外显子52的化合物pmo#1和ppmo#1,其都含有相同的序列。
[0547]
人类dmd外显子52的pmo#1和ppmo#1的序列。
[0548]
名称靶向序列(ts)ts seq id no.5'3'pmo#1ctgttccaaatcctgcattgttgcc1eg3hppmo#1ctgttccaaatcctgcattgttgcc1eg3-g-r6[0549]
具体来说,健康的人成肌细胞(第5-6代,购自zen-bio,inc.的skb-f-sl)在以各种浓度(即40μm、20μm、10μm、5μm、2.5μm和1.25μm)的pmo#1或ppmo#1处理时,以~40%汇合率铺在skm-m培养基(zen-bio,inc.)中。温育九十六小时后,将成肌细胞用pbs洗涤,并用
illustra ge rnaspin 96试剂盒(目录号25-055-75,ge healthcare bio-sciences)中的ra1裂解缓冲液裂解。除了使用40μl不含rnase的水洗脱rna之外,按照制造商的建议分离总rna。
[0550]
为了确定两种化合物的外显子52跳跃,进行了两步终点rt-pcr。具体来说,首先用superscript iv第一链合成试剂盒(目录号18091200,invitrogen)按照制造商的说明使用无规六聚体将11微升总rna逆转录为cdna。通过将9μl cdna添加到platinum taq dna聚合酶pcr supermix high fidelity(目录号12532024,invitrogen)中,以靶向人dmd外显子50的正向引物(正向引物:(seq id no:5):ctctgagtggaaggcggtaa);和靶向外显子53的反向引物:(seq id no:6):acctgctcagcttcttcctt)进行pcr。使用表2中所示的程序,使用biorad cfx96实时热循环仪进行pcr扩增。通过使用dna高灵敏度试剂盒(cls760672,perkin elmer)将32μl pcr产物装载到labchip gx系统上,评估跳越或未跳越的pcr产物的表达。dmd外显子52跳跃的百分比是以跳越外显子52的条带(364bp)的摩尔浓度(nmol/)与跳越(364bp)和未跳越(482bp)条带的总摩尔浓度相比的百分比来计算的。
[0551]
使用双尾、无配对的学生t检验(同方差)来评估2组在各剂量下的平均值是否有统计学差异。p值<0.05被认为具有统计学意义。
[0552]
用于扩增具有或不具有外显子52跳跃的dmd扩增子的热循环仪程序。
[0553][0554][0555]
结果显示在下表和图4中。在图4中,误差条呈现平均值
±
sd,条柱上方的“[数值]x”表示各浓度下ppmo#1与pmo#1相比的外显子跳跃百分比的相对倍数变化,“*”表示pmo#1与ppmo#1之间的显著差异,p值<0.05。
[0556]
人成肌细胞中pmo#1和ppmo#1的dmd外显子52跳跃的百分比。
[0557][0558]
上表和图4中的数据出人意料地显示,与所有浓度的pmo#1相比,当细胞用ppmo#1处理时,成肌细胞中的外显子52跳跃结果显著更高,其程度出乎意料。这种显著的改善很可能在体内比较试验中进一步证明,如实例5的非人类灵长类动物(nhp)研究,其中用ppmo#1或pmo#1处理nhp,并在各种相关的肌肉组织中测量外显子52跳跃(参见实例5了解详情)。
[0559]
实例4:mdx小鼠研究
[0560]
mdx小鼠是一种公认的、充分表征的杜氏肌营养不良(dmd)动物模型,它含有肌营养不良基因的外显子23中的突变。已知m23d反义序列(seq id no:2)诱导外显子23跳跃并
恢复功能性肌营养不良基因的表达。将6-7周龄的mdx小鼠以40mg/kg的剂量在尾静脉中单次注射下表中的ppmo4225或pmo4225,或用生理盐水注射。
[0561]
名称靶向序列(ts)tsseq id no.5'3'pmo4225ggccaaacctcggcttacctgaaat2eg3hppmo4225ggccaaacctcggcttacctgaaat2eg3-g-r6[0562]
pmo4225和ppmo4225分别通过上述pmo方法a和cpp缀合方法制备。
[0563]
在单剂量注射后7、30、60和90天处死经过处理的小鼠(每组n=6)。如上所述,对膈膜、心脏和右四头肌进行蛋白质印迹分析以测量肌营养不良蛋白的产生,并进行rt-pcr分析以测量外显子跳跃的百分比,对左四头肌进行免疫组织化学和h/e染色。
[0564]
分别如上所述,通过蛋白质印迹定量肌营养不良蛋白的恢复,并通过rt-pcr测量外显子23跳跃的百分比。
[0565]
rt-pcr和蛋白质印迹结果显示在图5a-10b和下面的表格中。令人惊讶的是,与pmo4225相比,ppmo4225诱导的肌营养不良蛋白恢复和外显子23跳跃的水平显著较高且持续,最高水平发生在注射后30天。更令人惊讶的是,ppmo4225增加了心脏中的肌营养不良蛋白水平,而pmo4225没有;在使用pmo4225的所有时间点,心脏中都没有观察到肌营养不良蛋白和外显子跳跃。
[0566][0567][0568]
免疫组织化学结果显示于图11中。此处,ppmo4225恢复了整个四头肌的肌营养不良蛋白,而4225则产生了“斑块状”的表达模式。用ppmo4225处理的肌营养不良蛋白的均匀分布表明,骨骼肌的广泛靶向性是可以实现的。ppmo4225比pmo4225在体内的递送有显著改善。
[0569]
实例5:nhp中的外显子52跳跃
[0570]
为了进一步证明ppmo反义寡聚物外显子跳跃的功效,利用了非人类灵长类动物。具体地说,根据下表中的给药时间表,向具有完整肌肉组织的食蟹猕猴静脉内注射ppmo#1、pmo#1(来自实例3)或生理盐水:
[0571]
食蟹猕猴给药时间表
[0572][0573]
在整个研究过程中,将对动物进行观察,包括临床观察(例如,评估皮肤和毛皮、呼吸作用)和体重测量。至少在测试开始前,以及在第一次剂量和最后一次剂量(如适用)后24小时,采集血液和尿液样本。
[0574]
在每次计划的尸检,或在极端情况下安乐死,收集膈膜、十二指肠、食道和主动脉的平滑肌、四头肌、三角肌、二头肌和心脏的切片并速冻。如上所述,使用rt-pcr确定外显子52跳跃的百分比。
[0575]
实例6:mdx小鼠剂量响应研究
[0576]
以40mg/kg、80mg/kg或120mg/kg的剂量向6-7周龄的mdx小鼠的尾静脉中单次注射上述ppmo4225或pmo4225(每组n=6)。
[0577]
注射后30天处死经过处理的小鼠。基于上述蛋白质印迹方案(例如,在实例4中使用),对膈膜、四头肌和心脏进行了蛋白质印迹分析,以测量肌营养不良蛋白的产生,并进行了以下修改:
[0578]
参数实例4的蛋白质印迹方案蛋白质印迹方案修改蛋白质定量rcdc蛋白质分析试剂盒bca方法阻断步骤在4℃下过夜在rt下1小时一抗温育在rt下1小时在4℃下过夜一抗浓度1:201:500
[0579]
下表和图12-15中以%野生型形式显示了肌营养不良蛋白的恢复。
[0580][0581]
令人惊讶的是,数据显示,单剂量的ppmo4225以剂量依赖性的方式增加mdx小鼠的肌营养不良蛋白水平,其程度远远大于pmo4225。
[0582]
实例7:膈膜和心脏的mdx小鼠ihc研究
[0583]
给予6-7周龄的mdx小鼠尾静脉单次注射80mg/kg剂量的ppmo4225或生理盐水,给予6-7周龄的野生型小鼠单次注射生理盐水。在单剂量注射后30天处死经过处理的mdx小鼠、生理盐水mdx小鼠和野生型小鼠(每组n=4)。免疫组织化学结果显示于图19中。此处,结果显示,用ppmo4225处理的mdx小鼠中与dmd发病率和死亡率相关的组织中的肌营养不良蛋白均匀增加。
[0584]
*********************
[0585]
本说明书中引用的所有公开和专利申请以引用的方式并入本文,就如同各个别公开或专利申请被具体地并且单独地指示以引用的方式并入本文中一般。
[0586]
参考文献
[0587]
aartsma-rus,a.,a.a.janson等人,(2004).“反义诱导的多外显子跳跃用于杜氏肌营养不良更有意义.”《美国人类遗传学杂志(am j hum genet)》74(1):83-92.
[0588]
abes,r.等人,(2008).“富含精氨酸的细胞穿透肽:设计、结构-活性和应用,通过立体阻断寡核苷酸改变前体mrna剪接.”《肽科学杂志》14:455-460。
[0589]
alter,j.等人,(2006).“全身递送吗啉代寡核苷酸恢复体内肌营养不良蛋白的表达并改善营养不良性病理.”《自然
·
医学(nat.med.)》12(2):175-177。
[0590]
bestas,b.等人,(2014).“剪接纠正的寡核苷酸恢复x连锁无丙种球蛋白血症模型的btk功能.”《临床研究杂志》
[0591]
cirak,s.,v.arechavala-gomeza等人,(2011).“杜氏肌营养不良患者在全身性二氨基磷酸吗啉代寡聚物治疗后的外显子跳跃和肌营养不良蛋白恢复:一项开放标签、2期、剂量递增研究.”《柳叶刀(lancet)》378(9791):595-605。
[0592]
dunckley,m.g.,i.c.eperon等人,(1997).“通过反义寡核糖核苷酸调节dmd基因中的剪接.”《核苷和核苷酸(nucleosides&nucleotides)》16(7-9):1665-1668。
[0593]
dunckley,m.g.,m.manoharan等人,(1998).“通过反义寡核糖核苷酸改变培养的mdx肌肉细胞中肌营养不良蛋白基因的剪接.”《人类分子遗传学(hum mol genet)》7(7):1083-90。
[0594]
errington,s.j.,c.j.mann等人,(2003).“肌营养不良蛋白基因中反义寡核苷酸诱导的外显子跳跃的靶点选择.”《基因医学杂志(j gene med)》5(6):518-27.
[0595]
goemans,n.m.,m.tulinius等人,(2011).“pro051在杜氏肌营养不良中的全身施用.”《新英格兰医学杂志(n engl j med)》。
[0596]
jearawiriyapaisarn,n.,h.m.moulton等人,(2008).“肽缀合的吗啉代寡聚物在
mdx小鼠肌肉中诱导的肌营养不良蛋白持续表达.”《分子治疗学(mol ther)》。
[0597]
jearawiriyapaisarn,n.等人,(2010).“肽缀合的吗啉代寡聚物疗法后mdx心肌病的长期改善.”《心血管研究(cardiovascular research)》85:444-453。
[0598]
kinali,m.,v.arechavala-gomeza等人,(2009).“在杜氏肌营养不良中用吗啉代寡聚物avi-4658局部修复肌营养不良蛋白的表达:一些单盲,安慰剂对照,剂量递增,概念验证的研究.”《柳叶刀神经病学(lancet neurol)》8(10):918-28。
[0599]
leblue,b.等人,(2008).“空间封闭寡核苷酸的细胞穿透肽缀合物.”《先进药物递送评论(adv.drugdeliv.rev.)》60:517-529。
[0600]
lu,q.l.,c.j.mann等人,(2003).“跳跃mdx营养不良小鼠的突变外显子所产生的肌营养不良蛋白的功能量.”《自然
·
医学》9(8):1009-14.
[0601]
mann,c.j.,k.honeyman等人,(2002).“改良的反义寡核苷酸诱导的肌营养不良的mdx小鼠模型中的外显子跳跃.”《基因医学杂志》4(6):644-54。
[0602]
marshall,n.b.,s.k.oda等人,(2007).“富含精氨酸的细胞穿透肽有助于反义寡聚物向小鼠白细胞中的递送并改变前体mrna的剪接.”《免疫学方法杂志(journal of immunological methods)》325(1-2):114-126。
[0603]
matsuo,m.,t.masumura等人,(1991).“由于杜氏肌营养不良kobe的肌营养不良蛋白基因中的外显子缺失导致肌营养不良蛋白mrna前体剪接过程中的外显子跳跃.”《临床研究杂志》87(6):2127-31。
[0604]
mcclory,g.等人,(2006).“反义寡核苷酸诱导的外显子跳跃恢复dmd犬模型中肌营养不良蛋白的体外表达.”《基因疗法》13:1373-1381。
[0605]
monaco,a.p.,c.j.bertelson等人,(1988).“dmd基因座部分缺失的患者之间的表型差异的解释.”《基因体学(genomics)》2(1):90-5。
[0606]
moulton,h.m.,(2007).“细胞穿透肽-吗啉代缀合物改变dmd(杜氏肌营养不良)的前体mrna剪接并抑制鼠冠状病毒在体内复制.”《生物化学学会学报(biochem.society trans)》35(4):826-828。
[0607]
pramono,z.a.,y.takeshima等人,(1996).“通过转染与外显子识别序列互补的反义寡脱氧核苷酸诱导淋巴母细胞中肌营养不良蛋白转录物的外显子跳跃.”《生物化学与生物物理研究通讯(biochem biophys res commun)226(2):445-9。
[0608]
sazani,p.,r.kole等人,(2007).tnf超家族受体的剪接转换寡聚物及其在疾病治疗中的应用.pct wo2007058894,北卡罗莱纳大学
[0609]
sierakowska,h.,m.j.sambade等人,(1996).“用反义寡核苷酸修复哺乳动物细胞中地中海贫血人β-球蛋白mrna.”《美国国家科学院院刊》93(23):12840-4。
[0610]
summerton,j.和d.weller(1997).“吗啉代反义寡聚物:设计、制备和特性.”《反义核酸药物开发(antisense nucleic acid drug dev)》7(3):187-95。
[0611]
takeshima,y.,h.nishio等人,(1995).“通过修饰从肌营养不良蛋白kobe的肌营养不良蛋白基因中缺失的外显子内序列来调节上游内含子的体外剪接.”临床研究杂志95(2):515-20。
[0612]
van deutekom,j.c.,m.bremmer-bout等人,(2001).“反义诱导的外显子跳跃恢复dmd患者来源的肌肉细胞中肌营养不良蛋白的表达.”《人类分子遗传学》10(15):1547-54。
[0613]
van deutekom,j.c.,a.a.janson等人,(2007).“用反义寡核苷酸pro051进行的局部肌营养不良蛋白恢复.”《新英格兰医学杂志》357(26):2677-86。
[0614]
wilton,s.d.,a.m.fall等人,(2007).“反义寡核苷酸诱导的人肌营养不良蛋白基因转录物中的外显子跳跃.”《分子治疗学》15(7):1288-96。
[0615]
wilton,s.d.,f.lloyd等人,(1999).“使用反义寡核苷酸特异性去除mdx肌营养不良蛋白mrna的无义突变.”《神经肌肉病症(neuromuscul disord)》9(5):330-8。
[0616]
wu,b.,h.m.moulton等人,(2008).“通过修饰的吗啉代低聚物有效拯救肌营养不良蛋白可改善肌营养不良蛋白缺陷小鼠的心脏功能.”《美国国家科学院院刊》105(39):14814-9。
[0617]
wu,b.等人,(2012).“肽缀合吗啉代对营养不良性mdx小鼠肌营养不良蛋白表达的长期拯救及肌肉病理学和功能的改善.”《美国病理学杂志(theam.j.pathol.)》181(2):392-400。
[0618]
wu,p.等人,(2007)“细胞穿透肽作为吗啉代寡聚物的转运蛋白:氨基酸组成对细胞内递送和细胞毒性的影响.”《核酸研究》35(15):5182-5191。
[0619]
yin,h.,h.m.moulton等人,(2008).“细胞穿透肽缀合的反义寡核苷酸可恢复全身肌肉和心脏肌营养不良蛋白的表达和功能.”《人类分子遗传学》17(24):3909-18。
[0620]
yin,h.等人,(2011).“pip5转导肽指导mdx小鼠心脏中高效寡核苷酸介导的肌营养不良蛋白外显子跳跃和表型校正.”《分子治疗学》19(7):1295-1303。
[0621]
youngblood,d.等人,(2006).“细胞穿透肽-吗啉代寡聚物缀合物在人血清和细胞中的稳定性.”《美国化学学会杂志(am.chem.soc.)》
[0622]
序列表
[0623]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1