具有集成预调节和通过测量皮肤表面温度自动触发光热靶向治疗的光热靶向治疗系统以及相关方法与流程
[0001]
本发明涉及光热靶向治疗,并且更具体地,涉及用于光诱导热治疗嵌入媒质中的靶向特定生色团或含有特定生色团的靶标的系统和方法。
背景技术:
[0002]
嵌入在媒质中的诸如生色团和含有生色团的物体之类的靶标可以通过用光源(例如激光)加热靶标进行热破坏。例如,可以通过用激光加热皮脂直到皮脂本身或含有皮脂的皮脂腺被破坏来热破坏含有嵌入在真皮中的皮脂的皮脂腺。然而,施加足够的热能以破坏靶标也可能破坏周围的真皮和上覆的表皮,从而导致表皮和真皮的破坏以及患者的痛苦。
[0003]
先前预防表皮和真皮破坏的方案以及患者痛苦包括:
[0004]
1.预冷却表皮,然后施加光热治疗;和
[0005]
2.预冷却表皮,并在预热方案中对表皮和真皮进行预调节(即预热),然后以不同的治疗方案施加光热治疗。在某些情况下,尽管两个方案涉及不同的激光器设置和施加方案,但预热方案和治疗方案是由同一台激光器执行的,因此导致治疗方案和设备的进一步复杂性。
技术实现要素:
[0006]
根据本文所述的实施例,用于破坏嵌入在媒质中的靶标的光热靶向治疗系统包括控制器和包含光源的光热治疗单元。控制器被配置用于给与(administer)治疗方案,并且使用光源以预设的功率设置和预设的脉冲定时设置来给与治疗方案。
[0007]
在另一个实施方案中,治疗方案包括用于预热媒质和靶标的预调节过程和光热治疗过程。预调节过程和光热治疗过程均使用光源给与,而无需在预调节过程和光热治疗过程之间更改预设功率设置和预设脉冲定时设置。在另一实施例中,预调节过程比光热过程花费更长的持续时间。
[0008]
在又一个实施例中,系统包括冷却单元,并且治疗方案还包括在治疗方案之前和期间的冷却过程。在又一个实施例中,对于预调节过程和光热治疗过程两者,光源被设置为以预设的功率水平、预设的脉冲长度和预设的脉冲间隔发射一系列光脉冲。
[0009]
在又一个实施例中,预调节过程和光热治疗过程包括在预设区域上以扫描方式施加光脉冲。在示例性实施例中,预设区域是5毫米乘5毫米治疗块的2x2矩阵。
[0010]
在另一个实施例中,在预调节过程和光热治疗过程期间,媒质中的温度小于媒质变性和破坏的阈值,并且将靶标加热到大于靶标的破坏阈值的温度。在一个示例性实施例中,媒质(例如表皮)的温度小于55℃,并且将靶标加热至大于55℃的温度。在另一个实施例中,根据在患者身上治疗区域的位置来调节媒质的温度。
[0011]
在另一个实施例中,公开了一种使用用于破坏嵌入在媒质中的靶标的光热靶向治疗系统的方法。该系统包括光源。该方法包括为由光源产生的一系列光脉冲定义一组参数,
该组参数包括预设功率水平、预设脉冲长度、预设脉冲间隔和光脉冲的数量。该方法还包括根据所定义的该组参数生成该系列光脉冲,以及将该系列光脉冲给与媒质。
[0012]
在又一个实施方案中,该方法还包括在给与治疗方案的同时冷却媒质。此外,在另一个实施例中,施加该系列光脉冲包括将预设区域定义为2乘1或更大的治疗块的矩阵。在示例性实施例中,施加该系列光脉冲包括将预设区域定义为5毫米乘5毫米治疗块的2
×
2矩阵。
[0013]
在另一个实施例中,给与该系列光脉冲包括施加该系列光脉冲,使得媒质的温度小于媒质变性和破坏的阈值,并且将靶标加热至高于靶标的破坏阈值的温度。在一个示例性实施例中,给与该系列光脉冲包括提高媒质(例如表皮)的温度到小于55℃,同时将靶标加热至高于55℃的温度。
[0014]
根据本文所述的实施例,描述了一种使用光热靶向治疗系统自动启动治疗方案的方法。该方法包括在治疗位置处给与冷却机制,在治疗位置处监视皮肤表面温度,以及当皮肤表面温度达到预设阈值时,自动启动治疗方案。
[0015]
在另一个实施例中,无需通过用户的任何手动输入即可启动治疗方案。
[0016]
根据另一个实施例,描述了一种使用光热靶向治疗系统自动终止治疗方案的方法。该方法包括在在治疗区域处给与治疗方案期间,监视在治疗位置处的皮肤表面温度,并且当皮肤表面温度达到预设阈值时,自动终止治疗方案。
[0017]
根据另一实施例,无需通过用户的任何手动输入就终止治疗方案。
[0018]
在下文中描述了对预期实施例的附加修改和变化。
附图说明
[0019]
图1示出了根据实施例的示例性光热靶向治疗系统。
[0020]
图2示出了根据实施例的与光热靶向治疗系统一起使用的示例性扫描器布置。
[0021]
图3示出了根据实施例的示例性治疗矩阵布置。
[0022]
图4示出了根据实施例的适于与治疗方案或集成的预调节/光治疗方案一起使用的一组示例性光脉冲的示意图。
[0023]
图5示出了根据实施例的随着治疗光脉冲被施加,靶标皮脂腺处的随时间变化的估计温度。
[0024]
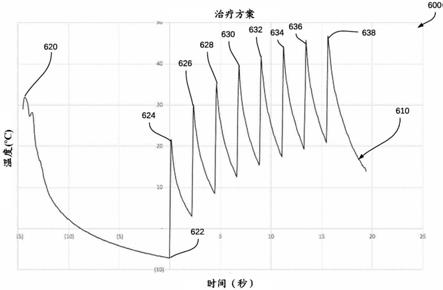
图6示出了根据实施例的在治疗方案期间在皮肤表面处随时间的变化的测量温度。
[0025]
图7示出了流程图,该流程图示出了用于在治疗方案的冷却部分期间分析所测量的皮肤表面温度,然后相应地启动治疗方案的示例性过程。
[0026]
图8示出了流程图,该流程图示出了用于在治疗方案期间继续分析所测量的皮肤表面温度,然后相应地终止治疗方案的示例性过程。
具体实施方式
[0027]
以下,参照其中示出了本发明的实施例的附图,更全面地说明本发明的实施例。然而,本发明可以以许多不同的形式来实施,并且不应被解释为限于在此阐述的实施例。而是,提供这些实施例以使得本公开将是透彻和完整的,并将向本领域技术人员充分传达本
发明的范围。在附图中,为了清楚起见,可能夸大了层和区域的尺寸和相对尺寸。贯穿全文,相同的数字表示相同的元件。
[0028]
将理解,尽管术语第一,第二,第三等在本文中可用于描述各种元件,组件,区域,层和/或部分,但是这些元件,组件,区域,层和/或部分不应受这些术语的限制。这些术语仅用于区分一个元件,组件,区域,层或部分与另一区域,层或部分。因此,在不脱离本发明的教导的情况下,下面讨论的第一元件,组件,区域,层或部分可以被称为第二元件,组件,区域,层或部分。
[0029]
为了便于描述,在本文中可以使用空间相对术语,例如“在...下方”,“在...下面”,“下方”,“在...之下”,“在...之上”,“上方”等,以便描述如图中所示的一个元件或特征与其他元件或特征的关系。将理解的是,除了图中所描绘的方位之外,空间相对术语还意图涵盖设备在使用或操作中的不同方位。例如,如果图中的装置被翻转,则被描述为在其他元件或特征“下面”,“下方”或“之下”的元件将被定向为在其他元件或特征“之上”。因此,示例性术语“下面”和“下方”可以包括在上方和在下方两个方位。可以以其他方式定向设备(旋转90度或在其他方位),并据此解释此处使用的空间相对描述语。另外,还将理解的是,当层被称为在两层“之间”时,它可以是两层之间的唯一层,或者也可以存在一个或多个中间层。
[0030]
在此使用的术语仅出于描述特定实施例的目的,并不旨在限制本发明。如本文所使用的,单数形式“一”,“一个”和“该”也意图包括复数形式,除非上下文另外明确指出。将进一步理解的是,当在本说明书中使用术语“包括”和/或“其包括”时,其规定了所述特征,整数,步骤,操作,元件和/或组件的存在,但并不排除一个或多个其他特征,整数,步骤,操作,元素,组件和/或其组的存在或添加。如本文所使用的,术语“和/或”包括一个或多个相关联的所列项目的任一个和所有组合,并且可以缩写为“/”。
[0031]
应该理解,当一个元件或层被称为在另一个元件或层“上”、“连接到”、“耦接到”或“邻近于”另一个元件或层时,它可以直接在其他元件或层上、连接到、耦接到或邻近于其他元件或层,或可以存在中间元件或层。相反,当元件被称为“直接在”另一元件或层“上”、“直接连接到”、“直接耦接到”或“紧邻于”另一元件或层时,则不存在中间元件或层。同样地,当“从”一个元件接收或提供光时,可以直接从该元件或从中间元件接收或提供光。另一方面,当“直接从”一个元件接收或提供光时,则不存在中间元件。
[0032]
在此参照截面图描述本发明的实施例,这些截面图是本发明的理想实施例(和中间结构)的示意图。这样,例如由于制造技术和/或公差导致的图示形状的变化是可以预期的。因此,本发明的实施例不应被解释为限于这里示出的区域的特定形状,而应包括例如由制造引起的形状偏差。因此,图中示出的区域本质上是示意性的,并且它们的形状不旨在示出设备的区域的实际形状,也不旨在限制本发明的范围。
[0033]
除非另有定义,否则本文中使用的所有术语(包括技术术语和科学术语)具有与本发明所属领域的普通技术人员通常所理解的相同含义。还将理解的是,诸如在常用词典中定义的那些术语应被解释为具有与它们在相关领域和/或本说明书的上下文中它们的含义一致的含义,并且将不被以理想化或过于形式化的意义解释,除非在此明确定义。
[0034]
图1示出了示例性的光热靶向治疗系统,其用于破坏嵌入媒质中的诸如特定发色团或含有发色团的物体的靶标,并将靶标加热至足够高的温度,从而在不破坏周围媒质的
情况下破坏靶标。该系统例如可以用于以靶向方式对含有作为生色团的皮脂的皮脂腺进行光热消融,同时保留了靶标皮脂腺周围的表皮和真皮。
[0035]
仍然参考图1,光热靶向治疗系统100包括冷却单元110和光治疗单元120。冷却单元110,例如通过接触或通过直接空气冷却向治疗区域,即覆盖靶标皮脂腺的皮肤外层区域,提供冷却效果的冷却机制。冷却单元110与光治疗单元120内的控制器122连接。要注意的是,虽然在图1中控制器122被示出为包含在光治疗单元120内,但是控制器可以位于冷却单元110和光治疗单元122两者之外,或者甚至位于冷却单元110内。
[0036]
控制器122还控制光治疗单元120内的其他组件,例如激光器124,显示器126,温度监视单元128,脚踏开关130,门联锁132和紧急通/断开关。激光器124为光治疗方案提供激光器功率,并且控制器122调节激光器的特定设置,例如输出功率和脉冲时间设置。激光器124可以是单个激光器或两个或更多个激光器的组合。如果使用的激光器多于一个,则将激光输出进行光学组合,以充当一个更强大的激光器。显示器126可以包括诸如冷却单元110、激光器124的运行状况和其他系统状态之类的信息。温度监测单元128例如用于监测治疗区域中的皮肤表面的温度,并且由控制器122使用测量的在治疗区域处的皮肤表面温度以调节光治疗方案。控制器122还与脚踏开关130接口,以远程接通或断开激光器124和/或冷却单元110。此外,门联锁132可用作附加的安全措施,以便当通往治疗室的门微开时,门联锁装置132检测到该状况并指示控制器122不允许光治疗单元120或至少激光器124运行。此外,可以设置紧急通/断开关134以在紧急情况下快速关闭光热靶向治疗系统100。在另一种修改中,可以添加附加的光电二极管或其他传感器以监测从激光器124发出的能量的功率水平。
[0037]
继续参考图1,光热靶向治疗系统100还包括手持式扫描器160,其是在将治疗方案施加于患者时由用户的手握住的设备的一部分。扫描器160可以被形成为例如枪状或棒状的形状,以便于用户操作。扫描器160通过冷却连接162与冷却单元110连接,以便可以使用扫描器160施加冷却方案。此外,激光器124的输出通过光纤输送164与扫描器160连接,从而可以使用扫描仪160施加治疗方案。可选地,扫描器160通过温度连接166连接到温度监测单元128,以便将在治疗区域处的皮肤温度反馈到例如控制器122。
[0038]
在图1所示的示例性实施例中,光热靶向治疗系统100的光治疗单元120以既用于治疗区域的预调节,又用于靶标皮脂腺的光治疗的单一设置提供光能量。也就是说,不是顺序地提供针对预调节而优化的光能量的施加,接着是针对光治疗而优化的不同光的施加,而是光治疗单元120以单个连续施加方案提供用于预调节和光治疗两者的光能量,而无需更改光能量设置。该集成方案节省了施加光治疗的时间和复杂性。
[0039]
图2示出了根据一个实施例的扫描器160的更多细节。冷却连接162与冷却输送单元202连接,该冷却输送单元202被配置成将冷却机制(例如,冷空气流)输送到治疗区域。来自激光器124的光纤输送164与激光能量输送单元204连接,该激光能量输送单元204包括用于将用于光热治疗方案的光能量输送到治疗区域的光学组件。最后,温度连接166与温度传感器206连接,温度传感器206测量在治疗区域处的温度以反馈给控制器122。此外,扫描器160包括通/断开关210(例如用于接通/断开激光的触发开关124)和可选的状态指示器212,其指示扫描器160的操作状态,例如是否正在操作激光器。尽管在图1中将扫描器160示意性地示出为方框,但是,实际形状被配置为易于使用。例如,扫描器160可被成形为具有手柄的
喷嘴、手枪形状或另一种合适的形状,以便于用户瞄准和控制。
[0040]
在根据一个实施例的示例性方法中,将冷却方案施加于整个治疗区域。冷却方案可包括例如在整个治疗区域上施加冷气流达规定的时间段,例如10秒。冷却之后,冷却机制(例如,冷气流)保持激活,并且将光治疗方案施加于治疗区域。在一个实施例中,方形“平顶”光束的脉冲与扫描器设备结合使用,以将激光脉冲顺序地施加到治疗区域内的各段。根据一个实施例,光治疗方案包括将设定数量的光脉冲施加到治疗区域中的每个段上,并且将激光脉冲顺序地施加到不同段上。在另一个实施例中,将激光脉冲以随机顺序施加到各段上。
[0041]
在示例性使用场景中,覆盖要治疗的皮脂腺的整个治疗区域被冷却。如图3所示,虚拟网格配置被覆盖在治疗区域上。示例性的网格配置300包括以3
×
4矩阵布置的十二个块。许多其他网格配置,例如1x1、2x1、2x2等也是可能的。在所示的示例中,治疗区域被定义为包括块310、312、324和326(分别编号为5、6、8和9)的2乘2块。
[0042]
在根据一个实施例的示例性方法中,冷却方案被施加于网格配置300中的整个治疗区域(即,块310、312、324和326)。冷却方案可以包括例如在整个治疗区域上施加冷气流达预定的时间段,例如10秒。冷却后,冷却机制(例如冷气流)保持活动状态,并且将预调节和光治疗方案被施加于治疗区域。在一个实施例中,将方形“平顶”光束的脉冲与扫描器设备结合使用,以将激光脉冲顺序地施加到块310、312、324和326。根据一个实施例,集成的预调节/光治疗方案包括将设定数量的光脉冲施加到治疗区域中的每个块上,这些块被按顺序施加脉冲。在另一个实施例中,这些块被以随机顺序施加脉冲。
[0043]
图4中示出了根据一个实施例的适合于治疗方案或集成的预调节/光治疗方案的一组脉冲的示例。序列400包括施加在治疗区域内的块之一处的光脉冲422、424、426、428、430、432和434。在一个实施例中,全部七个光脉冲具有相等的功率,并且被均匀的脉冲间隔(由双箭头442表示)分开,并且具有相同的脉冲持续时间(由间隙444表示)。在示例中,脉冲持续时间444为150毫秒,并且脉冲间隔为2秒。2秒的脉冲间隔旨在使块中的表皮和真皮冷却,以防止对其破坏。在脉冲间隔时间段内,可以将激光扫描到治疗区域内的不同块上,以提高激光的使用效率。要注意的是,图4未按比例绘制。激光脉冲的其他配置也是可能的,例如在多个脉冲上逐渐增加功率,或在多个脉冲上改变激光脉冲参数(例如,脉冲持续时间、脉冲间隔和/或峰值功率)。已认识到,还有许多其他的脉冲序列会达到在皮肤组织中沉积的相同平均能量,同时仍然保持短脉冲持续时间。
[0044]
图5示出了根据一个实施例的随着光脉冲(例如图4中所示的那些)被施加上,在治疗区域处的皮肤表面处的估计温度。在图5所示的例子中,已经通过直接空气冷却将治疗区域冷却了7秒,然后施加来自22瓦功率、持续时间为150毫秒的1726nm波长的激光器的光脉冲,持续2秒的时段,同时冷却保持开通。在此特定示例中,用于冷却以及在治疗方案期间使用的直接空气冷却提供了冷却到-22℃的高速空气柱,从而导致皮肤和空气之间的传热系数大约为350w/m^2k。
[0045]
在一个实施例中,光束尺寸为4.9mm见方。可以使用例如准直光学装置来调整确切的光束大小,这取决于治疗区域的大小、激光的功率分布,身体治疗区域的位置以及其他因素。此外,单位面积的平均激光功率应与由冷却系统达到的热量提取(heat extraction)平衡。在曲线图500中示出了所测得的皮肤表面温度的最终变化,其中峰522对应于如图4所示
的施加光脉冲422,峰424、426、428和430类似。
[0046]
脉冲持续时间应足够短,以使靶标(例如皮脂腺)处的温度迅速升高,因为长的脉冲持续时间会允许扩散而软化温度峰值。已认识到,还有许多其他的脉冲序列将达到在皮肤组织中沉积的相同平均能量,同时仍保持短的脉冲持续时间。在图5所示的示例中,每光斑平均功率为22w*0.15s/2s=1.65w。例如,可以通过以33瓦、2s的脉冲间隔施加脉冲持续100毫秒,或以25.1w、1.9s的脉冲间隔施加脉冲125ms来获得相同的每光斑平均功率。此外,单位面积的平均激光功率应与由冷却系统达到的热量提取平衡。
[0047]
继续参考图4和5,可以看到光脉冲422,424、426和428实质上导致了预调节效应,因为靶标处的温度从在峰值522处的大约40℃升高到在峰值528处的接近57℃。因此,脉冲434在约61℃的温度下产生峰534,该峰在含有发色团的靶(即,含有皮脂的皮脂腺)的破坏阈值之上。这样,简单地通过重复施加具有相同特性的光脉冲,就可以有效地整合预调节和光治疗方案,从而消除对与光治疗系统和方案不同的单独的预调节系统和方案的需求。
[0048]
还应注意,为进行预调节目的而施加的光脉冲的数量略大于影响光治疗的光脉冲的数量。该特征与现有的光热靶向治疗系统相反,因为现有的系统由于难以平衡用于治疗期间疼痛管理的冷却和预调节效果而试图最小化预调节所花的时间量。本文所述的系统和方法消除了将预调节时间最小化的担忧,因为用于预调节的相同光脉冲设置被用于光治疗。
[0049]
对特定靶标进行成功的光热治疗并减少患者不适可能包括:1)保留表皮,即表皮处的峰值温度值小于55℃;2)保留真皮,即通过平衡治疗脉冲的平均功率与冷却系统的热量提取来避免真皮过热;和3)选择性加热靶标,例如皮脂腺治疗的峰值温度高于55℃。另外,在冷却阶段期间,应避免对治疗区域进行过度冷却,以防止对表皮的冷伤害(例如冻伤)。
[0050]
应注意,在光热治疗方案期间施加的脉冲数量可以在2个脉冲直到大约100个脉冲之间的范围内,取决于诸如冷却效果、激光功率、脉冲宽度和脉冲频率这样的变量。
[0051]
可替代地,可以使用光栅扫描过程来扫描整个治疗区域上的连续波激光束,而不是将激光脉冲施加到特定的块,然后将激光移动到施加另一个激光脉冲的另一个块。在这种情况下,通过光栅扫描,可以将靶标(例如皮脂腺)中的温度升高计算为皮脂腺大小和光束速度的卷积。
[0052]
在文献中已知,组织参数,例如表皮和真皮的厚度,根据诸如年龄,性别,种族,ph,油含量和水合作用以及不同皮肤位置之间的因素而在个体之间变化。例如,即使对于同一个个体,前额也具有与背部不同的组织特性,因此对于不同的治疗位置需要不同的治疗参数设置。尽管现有的治疗方案已基于一种“适合所有患者的一种治疗”类型的方案,但在确定特定治疗方案时组织性质的这种变化会显著影响基于激光治疗痤疮的有效性。另外,由于制造的可变性和操作条件,例如,在特定的激光系统之间,确切的激光功率、光斑尺寸和冷却能力可能会有变化。减轻可能因特定机器的激光功率输出变化以及治疗条件(例如环境湿度和温度)变化而引起的治疗变化,有助于获得更均匀的治疗结果。换句话说,减少在光热治疗期间的可变性增强了安全性并提高了功效。
[0053]
一方面,在光热治疗方案开始时,皮肤表面温度的任何变化都会影响激光脉冲能量向靶标的热传递。例如,在图6中,尽管当施加第一激光脉冲时所示出的治疗方案已经将
皮肤表面冷却至大约-7℃,但是如果皮肤已经变凉或变暖,则初始峰(即峰624)将已经达到不同的温度,从而影响后续激光脉冲施加期间的总体温度上升。
[0054]
对于现有的光热治疗系统,在光热治疗方案开始时皮肤表面温度的这种变化是不可避免的,因为冷却过程包括施加冷却手段(例如冷空气或冷冻表面)达预设时间量。例如,光热治疗系统指示用户将冷空气流施加到治疗区域上达一定的秒数,然后提示用户启动光热治疗方案,包括施加激光脉冲。然而,该过程没有考虑光热治疗系统性能的潜在变化以及治疗区域中皮肤表面的热系数,因此不可避免地导致治疗功效的可变性。
[0055]
在一个实施例中,一种用于执行治疗的方法包括:在冷却期间监测皮肤表面温度,并且在达到阈值皮肤表面温度时自动触发预调节和光热治疗方案,而无需用户干预。
[0056]
可以通过结合温度测量来执行此冷却监测和自动治疗方案触发,例如使用可以内置在由医疗专业人员持有以将治疗施加于患者的扫描器中的商用、现成的低成本传感器(例如,参见图2的温度传感器206),或者通过使用单独的、商用的现成的单像素或多像素热测量设备。可以在高度本地化的级别上执行监测过程,从而即时调整治疗方案的初始化的定时。以这种方式,可以指定治疗方案以提供适当的冷却效果以使患者感到舒适,同时在冷却阶段保持在表皮和真皮破坏阈值温度以上。
[0057]
转向图7,示出了根据一个实施例的用于冷却监测和自动启动光治疗方案的示例性过程的流程图。如图7中所示,自动治疗启动过程700开始于在初始化步骤710中接通系统电源,然后在步骤712中将冷却机制施加于治疗区域。冷却机制可以是例如冷空气流。然后在步骤714中测量在治疗区域处的皮肤表面温度。温度测量可以例如使用低速红外照相机或类似设备来执行。然后,在判定716中确定所测量的皮肤表面温度是否足够冷(例如-5℃或另一预设温度设置)以开始施加治疗方案。如果对判定716的回答为“否”,则过程返回到步骤712,在该步骤继续将冷却机制施加于治疗区域。
[0058]
如果对判定716的回答为“是”,则在步骤718中,自动治疗启动过程700进行到自动启动治疗方案,而无需用户干预。在步骤720中结束自动治疗启动过程。
[0059]
可选地,出于安全原因和控制目的,可以将当前皮肤表面温度与存储的适合于不同控制参数的阈值进行比较。在整个治疗方案中以及在完成激光脉冲施加之后,可以继续监测在治疗区域处的皮肤表面温度,从而,如果继续将冷却机制施加于治疗区域,则一旦测量的表皮温度已达到例如室温或其他预设的后治疗温度设置,就可以停止冷却机制的施加。
[0060]
在图8中示出了一种可选的附加过程,其无需人工干预即可自动终止治疗方案。如图8中所示,自动治疗终止过程800从步骤810开始以启动光治疗方案。步骤810可以是例如图7的光治疗启动步骤718。替代地,自动治疗终止过程800可适用于与任何光治疗方案一起使用,而与治疗方案的启动方式无关。
[0061]
继续参考图8,自动治疗终止过程800进行到步骤812,以将一组激光脉冲给与到治疗区域。在施加该组激光脉冲期间或紧接着之后,在步骤814中测量在治疗区域处的皮肤表面温度。然后做出判定816,以确定所测量的皮肤表面温度是否高于预设阈值温度(即太热)。如果对判定816的回答为“是”,则自动治疗终止过程进行到步骤818,以自动终止光治疗方案,而无需用户的进一步参与。在步骤822中,激光器被禁用,并且该过程在步骤830中结束。如果对判定816的回答为“否”,则治疗方案继续到判定840以确定治疗方案是否已经
完成。如果对判定840的回答为“否”,则过程返回到步骤812以继续向治疗区域给与额外的激光脉冲。例如,如果治疗方案被定义为在特定治疗区域处施加八个激光脉冲,并且仅对该点施加了七个或更少的激光脉冲,则只要皮肤表面温度低于损害阈值,则触发额外的激光脉冲。如果对判定840的回答为“是”,则过程进行到步骤818、822和830,以逐渐停止治疗方案而无需进一步的用户干预。
[0062]
仍然参考图8,冷却机制可以继续可选地通过步骤812、814、816、818和/或840被施加到治疗区域,以便减轻治疗区域的潜在过热。在示例中,对于较大的治疗区域(例如5毫米乘5毫米治疗块的2x2矩阵),将设定数量的激光脉冲(例如,从1到8范围内)依次施加于每个治疗块。例如,在一个实施例中,给与激光脉冲的步骤812包括在第一治疗块处施加一个激光脉冲。在步骤814中测量皮肤表面温度,并且,如果所测量的皮肤表面温度低于预设阈值,并且光治疗方案包括施加额外脉冲,则过程返回到步骤812以将额外激光脉冲施加至治疗区。然后,在示例中,将第二激光脉冲施加到第一治疗块,或者将激光的瞄准移动到第二治疗块以向其施加激光脉冲。可以在每个激光脉冲之后移动激光的瞄准,或者可以在将激光瞄准第二个治疗块之前将连续的激光脉冲施加到单个治疗块。例如,如果在激光脉冲施加之间存在最多两秒钟的时间延迟,则可以在该时间延迟期间对治疗区域进行温度读取,并做出关于是否施加额外激光脉冲的判定。在一个实施例中,诸如激光功率、激光束大小、治疗区域尺寸以及每个治疗块要施加的激光脉冲的数量之类的治疗参数由用户预先定义,而即使没有用户干预,自动治疗终止过程也允许治疗方案的实时和特别调整,以减少对治疗区域的潜在破坏的机会。
[0063]
前述内容是对本发明的说明,并且不应解释为对本发明的限制。尽管已经描述了本发明的几个示例性实施例,但是本领域技术人员将容易理解,在实质上不脱离本发明的新颖教导和优点的情况下,在示例性实施例中的许多修改是可能的。例如,可以使用具有诸如1210nm左右的其他波长的激光器。本文描述的实施例的重要方面是通过使治疗方案的启动和/或终止自动进行,从而减少了由于操作者错误引起的潜在组织破坏,为患者增加了安全性。
[0064]
因此,许多不同的实施例源于以上描述和附图。会被理解,逐字地描述和说明这些实施例的每个组合和子组合将是过度重复和模糊的。这样,本说明书,包括附图,应被解释为构成本文所述实施例的所有组合和子组合以及制造和使用它们的方式和过程的完整书面描述,并且应支持对任何此类组合或子组合的权利要求。
[0065]
本公开包括以下条款,其是本公开的一部分。
[0066]
条款1.一种用于破坏嵌入媒质中的靶标的光热靶向治疗系统,该系统包括控制器和包含光源的光热治疗单元,其中所述控制器被配置用于给与治疗方案,并且其中使用所述光源以预设的功率设置和预设的脉冲定时设置给与所述治疗方案。
[0067]
条款2.根据条款1所述的系统,其中治疗方案包括用于预加热媒质的预调节过程和光热治疗过程,其中预调节过程和光热治疗过程都是使用光源进行给与,而无需在预调节过程和光热治疗过程之间更改预设功率设置和预设脉冲定时设置,并且其中预调节过程比光热治疗花费更长的持续时间。
[0068]
条款3.根据条款2所述的系统,还包括冷却单元,其中,治疗方案还包括用于在给与治疗方案的同时冷却媒质的冷却过程。
[0069]
条款4.根据条款3所述的系统,其中,对于预调节过程和光热治疗过程两者,光源均设置为以预设功率水平、预设脉冲长度和预设脉冲间隔发射一系列光脉冲。
[0070]
条款5.根据条款4所述的系统,其中,所述预设功率水平是在每个脉冲10瓦至50瓦的范围内。
[0071]
条款6.根据条款4所述的系统,其中,预设脉冲长度是在每个脉冲25毫秒到200毫秒的范围内。
[0072]
条款7.根据条款4所述的系统,其中,预设脉冲间隔是在0.5秒至2.5秒的范围内。
[0073]
条款8.根据条款4所述的系统,其中,所述预调节过程和所述光热治疗过程包括以扫描方式在预定区域上施加光脉冲。
[0074]
条款9.根据条款8所述的系统,其中预设区域是2乘1或更大的治疗块的矩阵。
[0075]
条款10.根据条款8所述的系统,其中,预设区域是5毫米乘5毫米治疗块的2x2矩阵。
[0076]
条款11.根据条款4所述的系统,其中,在预调节过程和光热治疗过程期间,媒质的温度小于媒质的破坏阈值,并且将靶标加热到比靶标的破坏阈值更高的温度。
[0077]
条款12.根据条款11所述的系统,其中,在预调节过程和光热治疗过程期间,媒质的温度小于55℃,并且将靶标加热到大于55℃的温度。
[0078]
条款13.根据条款11所述的系统,还包括温度监测器,用于随着将系列光脉冲施加到媒质测量媒质的温度。
[0079]
条款14.一种使用用于破坏嵌入媒质中的靶标的光热靶向治疗系统的方法,该系统包括光源,该方法包括:1)为要由光源产生的一系列光脉冲定义一组参数,该组参数包括预设功率水平、预设脉冲长度、预设脉冲间隔、以及光脉冲的数量;2)根据所定义的该组参数,产生该系列光脉冲;3)将该系列光脉冲给与媒质。
[0080]
条款15.根据条款14所述的方法,进一步包括,在将该系列光脉冲给与媒质之前,冷却用于在给与该系列光脉冲之前和同时冷却媒质的媒质。
[0081]
条款16.根据条款15所述的方法,其中施加所述系列光脉冲包括将所述预设区域定义为2乘1或更大的治疗块的矩阵。
[0082]
条款17.根据条款16所述的方法,其中施加所述系列光脉冲包括将所述预设区域定义为5毫米乘5毫米治疗块的2x2矩阵。
[0083]
条款18.根据条款14的述的方法,其中,给与所述系列光脉冲包括:施加所述系列光脉冲,以使媒质的温度小于媒质的破坏阈值,并将靶标加热到高于靶标的破坏阈值的温度。
[0084]
条款19.根据条款14所述的方法,其中,给与所述系列光脉冲包括将所述媒质的温度升高至小于55℃,同时将所述靶加热至大于55℃的温度。
[0085]
条款20.根据条款14所述的方法,还包括随着将所述系列光脉冲给与所述媒质,监测所述媒质的温度。
[0086]
条款21.一种使用光热靶向治疗系统自动启动治疗方案的方法,该方法包括在治疗位置处给与冷却机制;监测在治疗部位处的皮肤表面温度;以及当皮肤表面温度达到预设阈值时,自动启动治疗方案。
[0087]
条款22.根据条款21所述的方法,其中无需由用户任何手动输入即可执行自动启
动治疗方案。
[0088]
条款23.一种使用光热靶向治疗系统自动终止治疗方案的方法,该方法包括在在治疗区域处给与治疗方案期间,监测在治疗位置处的皮肤表面温度,以及当皮肤表面温度达到预设阈值时,自动终止治疗方案。
[0089]
条款24.根据条款23所述的方法,其中,无需由用户任何手动输入,即可执行自动终止治疗方案。
[0090]
在本说明书中,已经公开了本发明的实施例,并且尽管采用了特定术语,但是它们仅在一般和描述性意义上使用,而不是出于限制的目的。尽管已经描述了本发明的一些示例性实施例,但是本领域技术人员将容易理解,在实质上不脱离本发明的新颖教导和优点的情况下,在示例性实施例中的许多修改是可能的。因此,所有这样的修改旨在被包括在权利要求书所限定的本发明的范围内。因此,应理解,前述内容是本发明的实施例的举例说明,并且不应解释为限于所公开的具体实施例,并且对所公开的实施例以及其他实施例的修改意在被包括在所附权利要求的范围内。本发明仅由所附权利要求及其等同内容的全部范围限定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1