阿帕替尼及联合CCI-779在制备肺癌药物中的应用的制作方法
本发明涉及制药技术领域,具体涉及阿帕替尼及联合cci-779在制备肺癌药物中的应用。
背景技术:
肺癌是最常见的癌症以及癌症相关死亡的主要原因,可分为非小细胞肺癌(non-smallcelllungcancer,nsclc)和小细胞肺癌(smallcelllungcancer,sclc)。其中sclc约占所有肺癌的10%-15%,是一种高侵袭、高致死率、易广泛转移的肺癌类型,早期即可出现血行转移,约60%患者确诊时已有远处转移,5年生存率仅为7%,具有生长迅速,高度血管化的特点。血管生成是恶性肿瘤进展过程中最关键的过程之一,其为肿瘤的生长提供营养物质,促进肿瘤的生长,与肿瘤的发生、增殖和转移密切相关。血管内皮生长因子(vascularendothelialgrowthfactor,vegf)是血管生成的重要调控分子,能够和血管内皮生长因子受体2(vascularendothelialgrowthfactorreceptor,vegfr2)结合形成正反馈,调控血管内皮细胞的增殖、分化和迁移,促进新生血管形成。阻断vegfr2可抑制肿瘤诱导的血管生成。此外,几乎所有sclc患者都存在tp53和rb基因失活或突变。tp53和rb基因是重要的抑癌基因,其突变会导致细胞周期调控异常,细胞持续增殖,促进肿瘤的发生及发展。
阿帕替尼(apatinib)是一种小分子酪氨酸激酶抑制剂,能够选择性抑制vegfr2的活性,从而抑制vegf介导的细胞增殖、肿瘤微血管密度。apatinib已被证实在多种类型肿瘤中发挥作用,如胃癌、肝癌、乳腺癌、结直肠癌以及非小细胞肺癌,但是apatinib对小细胞肺癌细胞的作用尚需探索。
cci-779是一种mtor抑制剂,能够抑制肿瘤细胞的增殖和vegf产生,诱导细胞周期停滞在g1期,由于小细胞肺癌存在细胞增殖异常及vefg调控异常,故cci-779有望抑制其增殖。
但是,如何增加sclc对apatinib的敏感性,进而控制sclc患者的病情值得深入研究。
因此,如何用药,能显著控制sclc是本领域技术人员亟需解决的问题。
技术实现要素:
有鉴于此,本发明提供了阿帕替尼及联合cci-779在制备肺癌药物中的应用,尤其针对小细胞肺癌。
为了实现上述目的,本发明采用如下技术方案:
阿帕替尼在制备预防和治疗肺癌药物中的应用,肺癌为小细胞肺癌。
本发明还提供了阿帕替尼联合cci-779在制备预防和治疗小细胞肺癌药物中的应用。
优选的:阿帕替尼与cci-779的摩尔比不低于2:1。
本发明还提供了一种预防和治疗小细胞肺癌的药物组合物,包括阿帕替尼和cci-779,所述阿帕替尼与cci-779的摩尔比不低于2:1。
本发明还提供了阿帕替尼联合cci-779在制备小细胞肺癌细胞株抑制剂中的应用。
经由上述的技术方案可知,与现有技术相比,本发明公开提供了阿帕替尼及联合cci-779在制备肺癌药物中的应用,取得的技术效果为通过体外试验证实,阿帕替尼对小细胞肺癌细胞株(nci-h446)的作用具有浓度依赖性特征,高浓度阿帕替尼能够抑制小细胞肺癌细胞株的细胞增殖和迁移,诱导细胞凋亡,且与mtor抑制剂cci-779联用能够提高小细胞肺癌细胞对阿帕替尼的敏感性,在较低浓度时便能抑制小细胞肺癌细胞增殖和迁移,导致细胞周期阻滞,并诱导细胞凋亡。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据提供的附图获得其他的附图。
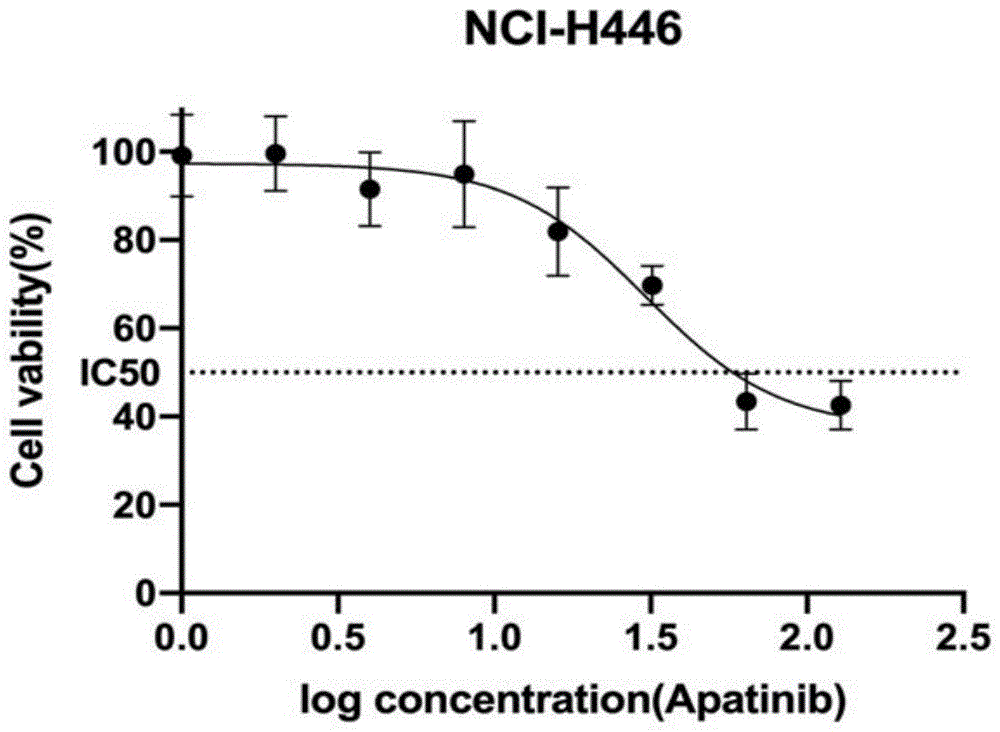
图1附图为本发明提供的apatinib抑制nci-h446细胞增殖示意图。其中apatinib的浓度范围为0~128μmol/l,处理时间为24h。
图2附图为本发明提供的cci-779抑制nci-h446活性示意图。其中cci-779的浓度范围为0~128μmol/l,处理时间为24h。
图3附图为本发明提供的cci-779处理组、低浓度apatinib联合cci-779处理组和高浓度apatinib联合cci-779处理组抑制细胞周期实验结果示意图。其中cci-779浓度为6μmol/l,apatinib的浓度分别为12μmol/l、16μmol/l、28μmol/l、32μmol/l,control为阴性对照组,处理时间为24h。
图4附图为本发明提供的对照组、cci-779处理组、低浓度和高浓度apatinib联合cci-779处理组诱导nci-h446细胞凋亡结果示意图。其中cci-779浓度为6μmol/l,apatinib的浓度分别为12μmol/l、16μmol/l、28μmol/l、32μmol/l,control为阴性对照组,处理时间为24h。
图5附图为本发明提供的对照组和apatinib诱导nci-h446细胞凋亡结果示意图。其中apatinib的浓度分别为12μmol/l、16μmol/l、28μmol/l、32μmol/l,control为阴性对照组,处理时间为24h。
图6附图为本发明提供的transwell迁移实验,对照组和apatinib处理组结果示意图。其中apatinib的浓度分别为12μmol/l、16μmol/l、28μmol/l、32μmol/l,control为阴性对照组,处理时间为24h。
图7附图为本发明提供的transwell迁移实验,对照组、cci-779处理组、低浓度apatinib联合cci-779处理组和高浓度apatinib联合cci-779处理组结果示意图。其中cci-779浓度为6μmol/l,apatinib的浓度分别为12μmol/l、16μmol/l、28μmol/l、32μmol/l,control为阴性对照组,处理时间为24h。
图8附图为本发明提供的蛋白免疫印迹实验示意图。apatinib的浓度分别为12μmol/l、16μmol/l、28μmol/l、32μmol/l,单独或联合6μmol/lcci-779处理24h后,蛋白质免疫印迹检测vegfr2、cdk6、cdk4蛋白的表达水平,gapdh为内参蛋白。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
本发明实施例公开了阿帕替尼及联合cci-779在制备肺癌药物中的应用。
所涉及的单一药品组分均为市售渠道采购,对其品牌不做限定,例如:人小细胞肺癌细胞nci-h446(tp53突变、rb突变)购自中国科学院细胞库(中国上海),阿帕替尼(apatinibmesylate,s2221)、cci-779(nsc683864,s1044)均购自selleck公司。抗体:vegfr2抗体购自abcam公司,cdk4、cdk6、gapdh抗体均购自cellsignalingtechnology公司。rpmimedium1640培养基、胎牛血清(fetalbovineserum)、胰蛋白酶均购自gibco公司。cck-8细胞增殖试剂盒、二甲基亚砜(dimethylsulfoxide,dmso)均购自bioind公司。pi/rnase染色液、细胞凋亡试剂盒均购自bd公司。transwell购自美国corning公司。
未提及的方法为常规实验方法,例如,统计学方法应用graphpadprism8.0软件对数据进行统计学分析并作图,组间数据比较采用独立样本t检验,p值取双侧检验,p<0.05为统计学有差异。未提及的试验设备为常规实验设备,在此不再一一赘述。
实施例1
细胞培养方法:
将细胞从-80℃冰箱中取出,在37℃水浴锅中快速复温,1000r/min离心3min,弃掉上清液,用新鲜培养基重悬细胞沉淀,培养于含10%胎牛血清的rpmimedium1640培养基,置于37℃、5%co2饱和湿度的培养箱中。待细胞生长至90%左右融合度时,弃掉培养基,用pbs清洗1-2遍,0.25%胰酶-edta消化传代。所有实验均采用对数生长期细胞。
cck8法测定细胞活力:
收集呈对数期稳定生长的nci-h446细胞,细胞计数板计数,调整细胞悬液浓度至2.5×104/ml,向96孔板中每孔加入200μl悬液,37℃、5%co2培养过夜,待细胞贴壁后,设置apatinib浓度梯度为0μmol/l、1μmol/l、2μmol/l、4μmol/l、8μmol/l、16μmol/l、32μmol/l、64μmol/l、128μmol/l,每个浓度设4个复孔,每个复孔加入200μl不同浓度的apatinib。37℃、5%co2孵育24h后,弃掉培养基,每孔加入100μl含10%cck-8的完全培养基,避光,37℃培养箱中孵育1h,用酶标仪测定在450nm处的吸光度,药物抑制率计算公式:(对照组od值-实验组od值)/对照组od值×100%,计算出药物的ic50。以同样的方法测定cci-779对nci-h446细胞的抑制率及ic50。
梯度处理nci-h446细胞24h后,cck8法计算出其ic50为30.44μmol/l。当药物浓度<10μmol/l时,apatinib对nci-h446细胞活力几乎没有影响;当药物浓度>10μmol/l时,apatinib开始逐渐抑制nci-h446细胞增殖,药物浓度>30.44μmol/l后才能将nci-h446细胞活力抑制在50%以下,提示apatinib对nci-h446的作用具有浓度依赖性,高浓度apatinib才能明显抑制nci-h446细胞增殖(参见图1)。
cci-779按照0μmol/l、1μmol/l、2μmol/l、4μmol/l、8μmol/l、16μmol/l、32μmol/l、64μmol/l、128μmol/l的浓度梯度处理nci-h446细胞24h后,cck8法计算出其ic50为13.59μmol/l,提示cci-779能抑制nci-h446活性(参见图2)。
实施例2
细胞周期实验。
将nci-h446细胞接种至6孔板中,加入完全培养基,待细胞汇合率达到70%-80%时,吸去孔内培养基,将各孔分为对照组、cci-779处理组、低浓度apatinib处理组(12μmol/l、16μmol/l)、高浓度apatinib处理组(28μmol/l、32μmol/l)、低浓度apatinib(12μmol/l、16μmol/l)联合cci-779处理组、高浓度apatinib(28μmol/l、32μmol/l)联合cci-779处理组,各组分别加入不同浓度药物2ml,37℃、5%co2孵育24h。收集1×106细胞于流式管中,用预冷的pbs清洗细胞,1000r/min离心3min,弃上清,逐滴加入1-2ml预冷的75%的乙醇,涡旋混匀细胞,4℃避光过夜,2000r/min离心细胞10min,弃上清,pbs清洗细胞2次以去除乙醇,将细胞重悬于0.5mlpi/rnase染色液,室温避光孵育15min,1小时之内上流式细胞仪检测。
结果表明:与对照组相比,cci-779处理组、低浓度apatinib联合cci-779处理组、高浓度apatinib联合cci-779处理组均出现明显的g1期阻滞(p<0.05)(参见图3)。
实施例3
细胞凋亡实验
将nci-h446细胞接种至6孔板中,加入完全培养基,待细胞汇合率达到70%-80%时,吸去孔内培养基,将各孔分为对照组、cci-779处理组、低浓度apatinib处理组(12μmol/l、16μmol/l)、高浓度apatinib处理组(28μmol/l、32μmol/l)、低浓度apatinib(12μmol/l、16μmol/l)联合cci-779处理组、高浓度apatinib(28μmol/l、32μmol/l)联合cci-779处理组,各组分别加入不同浓度药物2ml,37℃、5%co2孵育24h。收集5×105细胞于流式管中,用预冷的pbs清洗细胞,1000r/min离心3min,弃上清,加入100μl1×bindingbuffer重悬细胞,加入5μlannexinv-fitc,37℃培养箱中孵育10min;加入5μlpistainingsolution,轻轻混匀,避光、室温反应10min;加入400μl1×bindingbuffer,混匀,样品在1小时内用流式细胞仪检测。
结果表明:对照组凋亡细胞占总细胞的比例为(5.20±0.65)%,cci-779处理组为(4.26±0.08)%,低浓度apatinib联合cci-779处理组分别为(8.41±0.43)%、(13.76±0.26)%,高浓度apatinib联合cci-779处理组分别为(29.96±0.56)%、(38.34±0.31)%。与对照组相比,cci-779处理组nci-h446细胞凋亡无显著变化(p>0.5),低浓度和高浓度apatinib联合cci-779处理组nci-h446细胞凋亡明显增加(p<0.0001),高浓度apatinib诱导nci-h446细胞凋亡(参见图4)。
将处于对数生长期的nci-h446细胞以1×105/ml的浓度接种于6孔细胞培养板中,待细胞贴壁后,分别加入12μmol/l、16μmol/l、28μmol/l、32μmol/l低浓度的apatinib,并设置空白对照组,加药后24h后用0.25%的胰蛋白酶消化细胞,用预冷的pbs清洗细胞,1000r/min离心3min,弃上清,加入100μl1×bindingbuffer重悬细胞,加入5μlannexinv-fitc,37℃培养箱中孵育10min;加入5μlpistainingsolution,轻轻混匀,避光、室温反应10min;加入400μl1×bindingbuffer,混匀,样品在1小时内用流式细胞仪检测。
结果表明:对照组凋亡细胞占总细胞的比例为(4.18±0.30)%,低浓度apatinib处理组分别为(4.29±0.25)%、(4.88±0.17)%,高浓度apatinib处理组分别为(10.09±0.37)%、(11.22±0.81)%。与对照组相比,低浓度apatinib处理组nci-h446细胞凋亡没有显著变化(p>0.5),高浓度apatinib处理组nci-h446细胞凋亡明显增加(p<0.0001),提示高浓度apatinib能诱导nci-h446细胞凋亡(参见图5)。
实施例4
transwell迁移实验
将nci-h446细胞接种至6孔板中,加入完全培养基,待细胞汇合率达到70%-80%时,吸去孔内培养基,将各孔分为对照组、cci-779处理组、低浓度apatinib处理组、高浓度apatinib处理组、低浓度apatinib联合cci-779处理组、高浓度apatinib联合cci-779处理组,各组分别加入不同浓度药物2ml,37℃、5%co2孵育24h。使用无血清rpmimedium1640培养基调整各组细胞浓度为1×105/ml,分别取200μl加入上室,于下室加入600μl含10%胎牛血清的rpmimedium1640培养基,置于37℃、5%co2培养箱,培养24h。取出小室后,用棉签轻柔拭去上室细胞,4%多聚甲醛固定15min,结晶紫室温染色25min,并用pbs将多余染色液洗净,显微镜下观察穿过的细胞,每个样本随机选取5个视野进行拍照计数,计算平均值。
结果表明:对照组细胞迁移个数为(271.60±9.60),低浓度apatinib处理组分别为(285.60±7.61)、(255.80±3.60),高浓度apatinib处理组分别为(78.20±10.30)、(11.80±2.60)。与对照组相比,低浓度apatinib处理组nci-h446细胞迁移无显著变化(p>0.5),高浓度apatinib处理组显著抑制nci-h446细胞迁移(p<0.0001),提示高浓度apatinib显著抑制nci-h446细胞迁移(参见图6)。
将处于对数生长期的nci-h446细胞以1×105/ml的浓度接种于6孔细胞培养板中,待细胞贴壁后,分别加入12μmol/l、16μmol/l、28μmol/l、32μmol/l低浓度的apatinib,并设置空白对照组,加药后24h后用0.25%的胰蛋白酶消化细胞,使用无血清rpmimedium1640培养基调整各组细胞浓度为1×105/ml,分别取200μl加入上室,于下室加入600μl含10%胎牛血清的rpmimedium1640培养基,置于37℃、5%co2培养箱,培养24h。取出小室后,用棉签轻柔拭去上室细胞,4%多聚甲醛固定15min,结晶紫室温染色25min,并用pbs将多余染色液洗净,显微镜下观察穿过的细胞,每个样本随机选取5个视野进行拍照计数,计算平均值。
结果表明(参见图7):对照组细胞迁移个数为(275.60±9.72),cci-779处理组为(108.40±7.83),低浓度apatinib联合cci-779处理组分别为(71.30±5.33)、0,高浓度apatinib联合cci-779处理组几乎没有细胞迁移到下室。与对照组相比,cci-779处理组、低浓度apatinib联合cci-779处理组和高浓度apatinib联合cci-779处理组显著抑制nci-h446细胞迁移(p<0.0001)。
实施例5
选取药物浓度为6μmol/l(1/2ic50)的cci-779与apatinib联用。在apatinib0μmol/l、4μmol/l、8μmol/l、12μmol/l、16μmol/l、20μmol/l、24μmol/l、28μmol/l、32μmol/l浓度梯度下,应用蛋白免疫印迹实验,观察单药和联合用药时细胞周期蛋白的变化。
结果表明:单用apatinib处理nci-h446细胞时,apatinib浓度>24μmol/l,细胞周期蛋白cdk4、cdk6蛋白表达才出现明显降低,vegfr2才被明显抑制,进一步提示apatinib的作用具有浓度依赖性,较高浓度才能抑制vegfr2的表达;apatinib联合cci-779处理nci-h446细胞时,apatinib在较低浓度就能降低cdk4、cdk6蛋白表达,明显抑制vegfr2,提示cci-779联合apatinib能够降低细胞周期蛋白的表达,增加apatinib对vegfr2的抑制作用(参见图8)。
上述实施例1~5表明,高浓度的apatinib可抑制nci-h446细胞的增殖和迁移,导致细胞周期阻滞,并诱导细胞凋亡;
apatinib联合cci-779能够增加nci-h446细胞对apatinib的敏感性,抑制nci-h446细胞的增殖和迁移,导致细胞周期阻滞,并诱导细胞凋亡。
本说明书中各个实施例采用递进的方式描述,每个实施例重点说明的都是与其他实施例的不同之处,各个实施例之间相同相似部分互相参见即可。
对所公开的实施例的上述说明,使本领域专业技术人员能够实现或使用本发明。对这些实施例的多种修改对本领域的专业技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其它实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。
- 还没有人留言评论。精彩留言会获得点赞!