一种靶向肿瘤相关巨噬细胞的免疫调节微球制剂及其制备方法与应用与流程
本发明属于生物医药技术领域,具体涉及一种靶向肿瘤相关巨噬细胞的免疫调节微球制剂及其制备方法与在制备抗肿瘤产品中的应用。
背景技术:
肿瘤是目前全球性公共健康的难题,是威胁人类健康的重大问题,其发病率和死亡率逐年增高,减缓或抑制肿瘤的发病进展成为当下肿瘤治疗的主要目标。现有研究已明确肿瘤的形成发展与其所处的肿瘤微环境(tumormicroenvironment,tme)密切相关。tme不但为肿瘤生长提供必要的营养物质、生长条件和物理基质,而且通过改造和驯化浸润其中的免疫细胞如淋巴细胞、巨噬细胞等,使之发生表型、功能转变或效应细胞耗竭,以形成有利于肿瘤免疫逃逸和促进其生长的局部小环境(niche)。基于此,目前以解除免疫抑制为目的肿瘤免疫疗法如pd-1免疫检查点抑制剂和car-t等受到广泛关注,其被认为是继手术、化疗和放疗等传统肿瘤治疗方法之外,具有重要应用前景和巨大潜力的新的肿瘤治疗技术。尽管如此,现有肿瘤免疫治疗方法多集中于t细胞,而t细胞的活化和功能发挥受抗原提呈细胞如树突状细胞(dcs)和巨噬细胞
肿瘤相关巨噬细胞(tumor-associatedmacrophages,tams)是肿瘤微环境的主要组成部分,其在肿瘤组织中比例甚至可达到50%以上。大量临床证据表明,tams的数量与肿瘤发生、发展、转移和侵袭等具有密切关系,与肿瘤治疗效果和病人预后呈负相关,且与目前肿瘤免疫治疗方法如pd-1抑制剂的疗效具有反比关系。我们和其他研究者的研究结果显示,tams在肿瘤作用下,分化为具有特定表型和功能的细胞亚型,表现为细胞增殖、存活和自我复制能力显著增强,分泌免疫抑制和促癌细胞因子水平显著上升,具有直接或者间接促进肿瘤的形成发展的作用,是极具吸引力的肿瘤免疫治疗靶标。目前,针对tams的肿瘤免疫治疗策略方面,包括清除tams、干扰tams功能、重编程tams表型等,虽已取得一定的进展,但仍然存在不少问题需要解决。如不少基于tams清除目的的治疗方法缺乏肿瘤靶向性,对肿瘤微环境的渗透性较低而导致疗效不佳。而更为重要的是,因为巨噬细胞本是机体固有免疫的核心组成部分,具有抗感染、免疫调节、组织修复和维持机体平衡等重要作用,非特异性清除或普遍性重编巨噬细胞表型功能无疑对于保证抗肿瘤安全性和有效性来说是不利的,寻求机制清楚、作用靶标特异、去免疫抑制效果tams。
b细胞淋巴瘤6因子(bcelllymphoma6,bcl6)是一具有多种调节活性的转录因子。其结构包含n端btb/poz区域和c末端的6个kruppel样锌指结构。bcl6通过与靶基因启动子区域特定dna序列结合儿调控其转录和表达。bcl6靶基因涉及细胞活化、分化、发育、凋亡、增生和细胞能量代谢等众多关键分子,参与免疫、炎症、肿瘤、发育等多种生理病理过程。本研究前期显示,bcl6诱导性高表达于tams,并导致tams逆分化成为具有干细胞样、具有促肿瘤记忆的巨噬细胞表型。研究显示,bcl6通过基因转录调控作用,促进巨噬细胞增殖、抗凋亡、自我复制和分泌免疫抑制细胞因子能力增加,是肿瘤微环境中tams长期存活、数量增加和肿瘤清除能力受制的重要原因。干扰bcl6表达已显示显著的抗肿瘤体内效应,因此,bcl6有望成为以肿瘤相关巨噬细胞靶向的,以逆转免疫抑制为目标的抗肿瘤免疫治疗的潜在分子靶标。
技术实现要素:
发明目的:本发明所要解决的技术问题是针对现有技术中抗肿瘤免疫疗法中以肿瘤相关巨噬细胞为靶向、以特异性逆转免疫抑制为目的的有效靶标、技术思路和方法手段的不足,提供一种靶向肿瘤相关巨噬细胞的免疫调节微球制剂,其具有细胞和分子双靶向的、可定向转移至肿瘤微环境、有效提高抗肿瘤免疫效应。
本发明还要解决的技术问题是提供上述靶向肿瘤相关巨噬细胞的免疫调节微球制剂的制备方法。
本发明最后要解决的技术问题是提供上述靶向肿瘤相关巨噬细胞的免疫调节微球制剂在制备抗肿瘤产品中的应用。
为了解决上述技术问题,本发明公开了一种靶向肿瘤相关巨噬细胞的免疫调节微球制剂,其是以纳米微球为载体,结合巨噬细胞靶向肽(mp)和b细胞淋巴瘤6因子(bcl6)抑制肽的双靶向免疫纳米微球制剂,其通过肿瘤微环境的高效靶向,逆转肿瘤相关巨噬细胞(tams)的免疫抑制作用,有效遏制肿瘤进展,具有显著的抗肿瘤效应。
其中,所述的巨噬细胞靶向肽(mp)的氨基酸序列为yeqdpwgvkwwy;所述的b细胞淋巴瘤6因子(bcl6)抑制肽的氨基酸序列为gegiehisr。
上述靶向肿瘤相关巨噬细胞的免疫调节微球制剂的制备方法也在本发明的保护范围之内。
其中,所述的制备方法为将bcl6抑制肽(bi)负载于脂质体表面,得到bi-脂质体溶液;再将bi-脂质体溶液与mp结合,两者在ph2-4的酸性条件下混合,即得。
其中,所述的bi-脂质体溶液的制备方法为将b细胞淋巴瘤6因子抑制肽溶解于pbs缓冲液中,加入磷脂薄膜,室温震荡水化,匀化粒径,透析,去除游离态,即得。
其中,所述的磷脂薄膜的制备方法为将磷脂与胆固醇溶于三氯甲烷中,除干溶剂,即得;其中,磷脂、胆固醇和三氯甲烷的用量比为60mg:10mg:4ml。
其中,b细胞淋巴瘤6因子抑制肽与pbs缓冲液的用量比为1-4mg/ml,优选2.5mg/ml;控制磷脂薄膜的用量使磷脂与b细胞淋巴瘤6因子抑制肽的摩尔比为40:1-8:5,优选8:1。
其中,所述的震荡水化的时间为30min。
其中,所述的匀化粒径为采用探头进行超声,优选200w×10次。
其中,所述的将b细胞淋巴瘤6因子抑制肽-脂质体溶液与巨噬细胞靶向肽结合包括如下步骤:
(1)将巨噬细胞靶向肽溶于pbs缓冲液中,用hcl调节溶液的ph为2-4,优选3.5;
(2)将步骤(1)得到的溶液与b细胞淋巴瘤6因子抑制肽-脂质体溶液混合,hcl调节使其ph保持在3.5酸性条件,室温震荡30min,即得。
步骤(1)中,巨噬细胞靶向肽与pbs缓冲液的用量比为1-4mg/ml,优选3.3mg/ml。
步骤(2)中,控制步骤(1)得到溶液与b细胞淋巴瘤6因子抑制肽-脂质体溶液的用量,使巨噬细胞靶向肽与磷脂的摩尔比为1:50-1:200,优选1:50。
上述靶向肿瘤相关巨噬细胞的免疫调节微球制剂在制备抗肿瘤产品中的应用也在本发明的保护范围之内;优选地,所述的肿瘤为肺癌。
其中,所述的抗肿瘤是通过免疫调节微球制剂特异性剔除肿瘤相关巨噬细胞,抑制肿瘤相关巨噬细胞的干性转化和增殖能力,改善免疫抑制肿瘤微环境的作用,其可显著抑制体内肿瘤生长和进展,在肺癌等肿瘤防治中具有潜在应用价值。
有益效果:与现有技术相比,本发明具有如下优势:
(1)本发明首次将巨噬细胞的靶向肽与胞内信号分子抑制剂结合在一起,荷载于纳米微球,制备成定向转移至肿瘤微环境的免疫制剂。
(2)实验结果显示制剂能够显著抑制肺癌肿瘤的大小和重量,具有明显抗肿瘤作用。
(3)本发明首次发现该制剂能够显著降低肺癌肿瘤中巨噬细胞的比例和数量,逆转其干细胞样表型,为基于肿瘤巨相关噬细胞的免疫疗法提供了一种策略。
(4)本发明提供的小分子制剂一方面可以特异性靶向肿瘤巨噬细胞,另一方面因巨噬细胞本身具有的吞噬外源性颗粒的特性,而促进其被肿瘤巨噬细胞吞噬进入胞内。故相较于单一的靶分子抑制肽或小分子干扰rna,该微球颗粒细胞定位更明确,穿透性更好,在提高局部疗效和减轻全身影响方面具有其他非靶向免疫制剂和治疗方法所不具备的优势。
附图说明
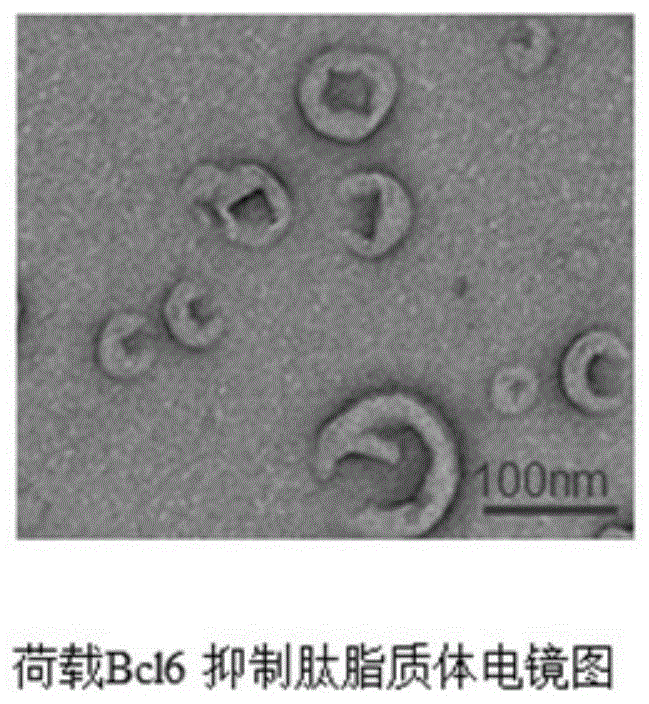
图1为荷载bcl6抑制肽脂质体电镜图。
图2为tam-bi的制备与表征。
图3为微球颗粒进入巨噬细胞的表征。
图4为bcl6在tams的表达情况及其对tams干性的影响。图5为tam-bi对小鼠肿瘤大小和重量的影响,其中***p<0.001。
图6为tam-bi对肿瘤相关巨噬细胞数量和比例的影响,其中***p<0.01。
图7为tam-bi对肿瘤相关巨噬细胞成球能力的影响,其中***p<0.01。
图8为tam-bi对肿瘤相关巨噬细胞表达干性因子的影响。
具体实施方式
根据下述实施例,可以更好地理解本发明。然而,本领域的技术人员容易理解,实施例所描述的内容仅用于说明本发明,而不应当也不会限制权利要求书中所详细描述的本发明。
实施例1
1.实验材料
1.1实验用药物及试剂:大豆磷脂与胆固醇(上海麦克林生化科);bcl6抑制肽gegiehisr与巨噬细胞靶向肽yeqdpwgvkwwy(上海吉尔生化有限公司);反转录试剂盒(thermofisherscientific);sybrgreen染料(thermofisherscientific);流式抗体(ebioscience);bcl6抗体(cellsignalingtechnology);bcl6小干扰rna(上海吉玛生物制药技术有限公司)。
1.2实验用动物及饲养:c57/bl6小鼠,6-9周龄,由南京大学模式动物所提供;全价营养颗粒饲料:由江苏省协同医药生物技术有限公司提供;饲养条件:室温20±2℃,湿度55-65%,明暗交替,光度适度,通风洁净良好。
2.实验方法
2.1巨噬细胞靶向微球制剂的构建与表征。
以bcl6抑制肽、胆固醇、磷脂按摩尔比1:1.3:8的比例,称取磷脂60mg、胆固醇10mg和bcl6抑制肽10mg。将磷脂与胆固醇溶于4ml三氯甲烷,室温旋转蒸发除干溶剂,获得磷脂薄膜。bcl6抑制肽溶解于4mlpbs缓冲液,加入磷脂薄膜中,室温震荡30min,使水化完全,探头超声200w×10次,匀化粒径。采用马尔文粒度分析仪检测其大小及电位,透射电镜检测大小及形态,并检测包封率。取适量bcl6抑制肽-脂质体于3000d透析袋,以pbs为透析介质透析5h除去游离肽,得到bcl6抑制肽-脂质体溶液。
按照巨噬细胞靶向肽、磷脂摩尔比1:50比例,称取巨噬细胞靶向肽3.3mg,溶于1mlpbs缓冲液溶液中,hcl调节溶液ph至3.5,即为巨噬细胞靶向对照制剂(tam-con)。
将此溶液与上述已制备的bcl6抑制肽-脂质体溶液混合,hcl调节使其ph保持在3.5酸性条件,室温震荡30min,即得巨噬细胞靶向免疫调节制剂(tam-bi)。
分别称取上述制备的0.5ml的tam-con或tam-bi溶于2ml的pbs缓冲溶液中,各取2份,每份0.5ml置于4ml离心管,其中一份加2ml纯水稀释作为对照组,另一份加2ml0.2mol/l碘化钠溶液,混合震摇5min。以280nm为激发波长,分别测定不同组别中色氨酸的发射波谱强度,以碘离子荧光猝灭法检验靶向肽与bcl6抑制肽的结合情况。
2.2小鼠肺癌模型的构建。
取20只c57/bl6小鼠(6-8周龄),随机分为对照组和治疗组2组,每组10只。将1×106lewis肺癌细胞分别与500μg不荷载bcl6抑制肽(tam-con,对照组)和荷载bcl6抑制肽(tam-bi,治疗组)的巨噬细胞靶向微球制剂充分混合,皮下注射于每只小鼠右侧后背部。并在造模后第3-19天,每隔一天,分别尾静脉注射上述脂质体微球。4周后处死小鼠,用于后续功能分析。
2.3巨噬细胞靶向免疫制剂对肺癌肿瘤的影响。
将上述已建立的荷瘤小鼠,取每组5只处死,剥离右侧腰背部的肿瘤,称取每只肿瘤的重量,肿瘤体积则通过测量长度(l)和宽度(w)并计算体积(v=l/2×w2)来确定。
2.4微球颗粒进入巨噬细胞的表征。
按照罗丹明与磷脂1:6的摩尔比称取罗丹明6.5mg,磷脂60mg,胆固醇10mg。将磷脂与胆固醇溶于4ml三氯甲烷,室温旋转蒸发除干溶剂,将罗丹明和10mgbcl6抑制肽溶解于4mlpbs缓冲液。将此pbs缓冲液加入磷脂薄膜中震荡30min,使水化完全,探头超声200w×10次,匀化粒径。取适量罗丹明-脂质体于3000d透析袋,以pbs为透析介质透析5h除去游离肽,即得到罗丹明-bcl6抑制肽-脂质体溶液。
将此溶液与上述已制备的罗丹明-bcl6抑制肽-脂质体溶液混合,hcl调节使其ph保持在3.5酸性条件,室温震荡30min,即得负载罗丹明的巨噬细胞靶向免疫调节制剂。
将上述已建立的荷瘤小鼠,在造模后第14天开始,连续3天每天尾静脉注射上述负载罗丹明的巨噬细胞靶向免疫调节制剂,1天后每组取3只处死,剥离右侧腰背部的肿瘤,剪碎,在每只小鼠剪碎的肿瘤组织中加入2倍体积的胶原酶a(1mg/ml),酶量为0.223u/mg,酶活定义为在37℃,ph7.5条件下作用于天然胶原蛋白,以每小时从胶原蛋白中释放的多肽相当于茚三酮显色1微摩尔亮氨酸量为一个活性单位(u)。将上述溶液混匀,置37℃,转速为180转/分的摇床中消化1小时,95%以上的组织都转变为细胞悬液,将细胞悬液过滤去除杂质,混匀,计数。取1×106个细胞,加入流式抗体抗小鼠f4/80和cd11b,避光孵育1小时,流式细胞术检测单细胞悬液中f4/80+cd11b+细胞即巨噬细胞中罗丹明阳性的细胞比例。
2.5bcl6在tams的表达情况及其对tams干性的影响。
取4只c57/bl6小鼠(6-8周龄)构建如上的肺癌模型,4周后全部处死,剥离右侧腰背部的肿瘤,剪碎,在每只小鼠剪碎的肿瘤组织中加入2倍体积的胶原酶a(1mg/ml),酶量为0.223u/mg,酶活定义为在37℃,ph7.5条件下作用于天然胶原蛋白,以每小时从胶原蛋白中释放的多肽相当于茚三酮显色1微摩尔亮氨酸量为一个活性单位(u)。将上述溶液混匀,置37℃,转速为180转/分的摇床中消化1小时,95%以上的组织都转变为细胞悬液,将细胞悬液过滤去除杂质,混匀,即为肿瘤组织细胞悬液。将每只小鼠获取的细胞接种于10cm的培养皿中,放入37℃静置40min,去除培养上清,留下的贴壁细胞即为tams。采用westernblot检测tams中bcl6的表达情况。取1×106个raw264.7巨噬细胞,将bcl6的小干扰rna(实验组)和空载体(对照组)转染至细胞中,用肺癌细胞培养上清刺激此细胞24h,收集细胞,提rna,采用qpcr法检测干性相关因子的表达情况。
2.6巨噬细胞靶向免疫制剂对巨噬细胞数量和比例的影响。
将上述已建立的荷瘤小鼠,取每组5只处死,剥离右侧腰背部的肿瘤,剪碎,在每只小鼠剪碎的肿瘤组织中加入2倍体积的胶原酶a(1mg/ml),酶量为0.223u/mg,酶活定义为在37℃,ph7.5条件下作用于天然胶原蛋白,以每小时从胶原蛋白中释放的多肽相当于茚三酮显色1微摩尔亮氨酸量为一个活性单位(u)。将上述溶液混匀,置37℃,转速为180转/分的摇床中消化1小时,95%以上的组织都转变为细胞悬液,将细胞悬液过滤去除杂质,混匀,计数。取1×106个细胞,加入流式抗体抗小鼠f4/80和cd11b,避光孵育1小时,流式细胞术检测单细胞悬液中f4/80+cd11b+细胞比例,即为肿瘤相关巨噬细胞的比例。所得比例乘以每只小鼠肿瘤总细胞数即为巨噬细胞绝对数量。
2.7巨噬细胞靶向免疫制剂对肿瘤相关巨噬细胞成球能力的影响。
将上述已建立的荷瘤小鼠,取每组5只,处死,剥离右侧腰背部的肿瘤,剪碎,在每只小鼠剪碎的肿瘤组织中加入2倍体积的胶原酶a(1mg/ml),酶量为0.223u/mg,酶活定义为在37℃,ph7.5条件下作用于天然胶原蛋白,以每小时从胶原蛋白中释放的多肽相当于茚三酮显色1微摩尔亮氨酸量为一个活性单位(u)。将上述溶液混匀,置37℃,转速为180转/分的摇床中消化1小时,95%以上的组织都转变为细胞悬液,将细胞悬液过滤去除杂质,混匀,计数。用流式细胞仪分选获得f4/80+cd11b+细胞。将巨噬细胞以1000/孔接种于24孔板中,每孔加入1ml干细胞培养基和100ng的m-csf,置37℃培养7天,用倒置荧光显微镜测定直径≥70μm的细胞球数,计算细胞成球率。
2.8巨噬细胞靶向免疫制剂对肿瘤相关巨噬细胞干性因子表达的影响。
同2.7制备获得f4/80+cd11b+细胞。取1×106细胞,提取rna,qpcr法检测干性相关因子的表达情况。
3.实验结果
3.1tam-bi制剂的制备与表征。
检测结果(图1和图2)发现包被了mp和bi双肽的脂质体(tam-bi)粒径为108.30±3.61nm,pdi为0.277,电位为-14.80±2.42mv。等量包被了mp和bi的脂质体透析前峰面积为6324276,透析后透析袋中溶液未增加,透析后测得峰面积5164960。测得包封率为81.67%。检测ph为3.5,空白脂质体的电位为-8.76±1.54mv;将巨噬细胞靶向肽(mp)与脂质体溶液混合制备tam-con,测得电位为-5.74±0.85mv。根据上述结果,脂质体表面电位增加3mv左右,说明mp负载在脂质体表面。因为mp中的色氨酸(w)具有荧光特性,碘离子能够使其荧光发生猝灭。而tam-bi由于加入的碘离子使其难以通过磷脂双分子层,因而嵌入双分子层的色氨酸与碘离子接触机会大大降低,不易发生猝灭。从结果分析,巨噬细胞靶向肽已成功嵌入包被了bcl6抑制肽的脂质体,即构建成功了双靶向tam-bi。
3.2微球颗粒进入巨噬细胞的表征。
以空白脂质体(对照组)和负载罗丹明的巨噬细胞靶向免疫调节制剂(实验组)分别作用于小鼠肺癌细胞模型。研究显示(图3),实验组小鼠tam中表达罗丹明的细胞比例高达78.3%。表明负载靶分子抑制肽的微球颗粒能够有效地被巨噬细胞特异性摄取。
3.3bcl6在tams的表达情况及其对tams干性的影响。
采用westernblot检测肺癌小鼠tams中是否表达转录因子bcl6,结果显示(图4),在tams中高表达bcl6,进一步采用bcl6的小分子rna干扰bcl6的表达,显示实验组表达干性因子如klf2,klf4,myc,nanog,oct4,sox2等的水平都显著低于对照组。表明在tams中高表达的bcl6能够促使tams分化为具有干细胞样特性的分型。
3.4tam-bi对肺癌小鼠肿瘤的影响。
以tam-con(对照组)和靶向抑制剂脂质体tam-bi(治疗组)分别作用于小鼠肺癌细胞模型。研究显示(图5),对照组小鼠生成的肿瘤体积、重量均大于治疗组,有统计学意义。表明巨噬细胞靶向免疫制剂tam-bi的确可以显著抑制肿瘤的发生发展。
3.5tam-bi对巨噬细胞数量和比例的影响。
采用流式检测对照组和治疗组肿瘤巨噬细胞的数量,结果显示(图6),tam-con处理的对照组小鼠肿瘤中,cd11b+f4/80+巨噬细胞的比例和数量均显著高于tam-bi治疗组,表明tam-bi可以显著降低肿瘤中巨噬细胞的数量,提示巨噬细胞靶向免疫制剂可以通过抑制促癌巨噬细胞而影响肿瘤发生发展。
3.6tam-bi对巨噬细胞自我更新和干性转化的影响。
具有自我更新能力(self-renewing)的巨噬细胞在体内留存时间长,增殖快,具有显著促癌作用,以细胞成球实验(spheroid-formingtest)来检测tam-bi对巨噬细胞自我更新能力的影响。结果显示(图7),tam-bi处理组的小鼠的肿瘤巨噬细胞形成干细胞样细胞球的数量、大小远低于tam-con处理组。由于细胞自我更新能力是细胞发生干性转化的重要功能性指标,进一步检测巨噬细胞表达干细胞标志分子的水平。结果显示(图8),tam-bi处理组tams表达干性因子如klf2,klf4,myc,nanog,oct4,sox2等水平显著低于对照组细胞。
综上,本发明提供了一种基于巨噬细胞和转录调控分子bcl6双靶向的的免疫微球制剂、制备方法、及在抗肿瘤治疗中的引用。以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围;且基于此发明的应用不限于肿瘤,本实施例中未明确的各组成部分均可用现有技术加以实现,并拓展至其他异常病理或疾病防治。
- 还没有人留言评论。精彩留言会获得点赞!