一种伏立康唑片及其制备方法与流程
:
1.本发明涉及医药技术领域,具体涉及一种伏立康唑片及其制备方法。
背景技术:
2.伏立康唑(voriconazole)为白色结晶性粉末,无臭,无味,几乎不溶于水,易溶于氯仿,在乙醇中溶解。其化学名为:(2r,3s)-2-(2,4-二氟苯基)-3-(5-氟基-4-嘧啶)-1-(1h-1,2,4-三唑-1-基)-2-丁醇,分子式为:c
16h14
f3n5o,分子量:349.3,分子结构式如下:
[0003][0004]
伏立康唑是第二代合成的三唑类抗真菌药,是在氟康唑结构的丙基骨架上加入了一个甲基,此外它用一个氟代嘧啶环取代了氟康唑的三唑环。其抗真菌活性较氟康唑强10-500倍,具有抗菌谱广,抗菌效力强的优点。伏立康唑的作用机制是通过竞争性抑制真菌细胞中由细胞色素p450介导的14α-甾醇去甲基化,进而抑制麦角甾醇的生物合成。麦角甾醇是真菌细胞膜的重要组成部分,它对于维持细胞膜的流动性,生物调节等起重要作用,当其生物合成受阻时,就会导致真菌的各种生命活动受到影响,降低其活性。在伏立康唑结构中,甲基的引入使其对目标酶的亲和力显著增强,嘧啶环的存在大大提高了其抗真菌活性,而在嘧啶环的5-位上再加入一个氟原子则可提高其体内抗真菌活性。体外试验表明伏立康唑具有广谱抗真菌作用,对念球菌属(包括耐氟康唑的克柔念珠菌,光滑念珠菌和白念珠菌耐药株)具有抗菌作用,对所有检测的曲菌属真菌有杀菌作用。此外,伏立康唑在体外对其他致病性真菌也有杀菌作用,包括对现有抗真菌药敏感性较低的菌属。
[0005]
伏立康唑目前主要用于侵袭性曲霉素、对氟康唑耐药的念珠菌感染、镰刀霉属及赛多孢菌属真菌所致的严重感染,尤其是治疗免疫缺陷患者所面临的进行性的、可能威胁生命的感染,也常用于中性粒细胞减少患者发热时的经验性治疗。目前已成为临床上治疗真菌感染的一线药物。
[0006]
伏立康唑在水中的溶解度极低(0.098mg/ml),其化学性质在溶液状态下不稳定,易水解成它的对应异构体(2s,3r)构型。目前伏立康唑上市剂型有:冻干粉剂、片剂、干混悬剂等。片剂具有剂量准确,含量差异较小,质量稳定,携带、运输、服用方便等优点。但现有的伏立康唑片剂溶出速度慢,在高温高湿环境中不稳定,且杂质较多,最终影响疗效。
技术实现要素:
[0007]
本发明的目的在于提供一种伏立康唑片及其制备方法,该伏立康唑片的溶出速度快,稳定性好,杂质较少,制备方法简单易操作。
[0008]
本发明一方面提供了一种伏立康唑片,包括由以下重量百分比的原料制成的片芯:伏立康唑30%-44%、微晶纤维素20%-45%、乳糖12%-30%、交联羧甲纤维素钠2.3%-5%、聚维酮k
30 2%-4%、硬脂酸镁1.2%-3%和月桂醇硫酸镁0.5%-1%;
[0009]
所述的片芯外包裹了一层包衣;
[0010]
所述的包衣包含以下重量百分比的原料:羟丙基甲基纤维素18%-24%、滑石粉0.8%-1.2%、二氧化钛1.5%-2.5%和50%乙醇溶液72.3%-79.7%。
[0011]
优选地,所述的伏立康唑片包括由以下重量百分比的原料制成的片芯:伏立康唑33%-44%、微晶纤维素20%-40%、乳糖16%-30%、交联羧甲纤维素钠2.3%-4.5%、聚维酮k
30 2%-3.5%、硬脂酸镁1.2%-2.2%和月桂醇硫酸镁0.5%-0.8%;
[0012]
所述的片芯外包裹了一层包衣;
[0013]
所述的包衣包含以下重量百分比的原料:羟丙基甲基纤维素18%-22%、滑石粉0.8%-1.0%、二氧化钛1.5%-2.1%和50%乙醇溶液74.9%-79.7%。
[0014]
优选地,所述的微晶纤维素和月桂醇硫酸镁的重量比为30-60:1;进一步优选地,所述的微晶纤维素和月桂醇硫酸镁的重量比为50:1
[0015]
优选地,所述的羟丙基甲基纤维素和滑石粉的重量比为20-25:1;进一步优选地,所述的羟丙基甲基纤维素和滑石粉的重量比约为22:1。
[0016]
更优选地,所述的伏立康唑片包括由以下重量百分比的原料制成的片芯:伏立康唑36%、微晶纤维素30%、乳糖24.8%、交联羧甲纤维素钠3.8%、聚维酮k
30 3%、硬脂酸镁1.8%和月桂醇硫酸镁0.6%;
[0017]
所述的片芯外包裹了一层包衣;
[0018]
所述的包衣包含以下重量百分比的原料:羟丙基甲基纤维素20%、滑石粉0.9%、二氧化钛1.8%和50%乙醇溶液77.3%。
[0019]
本发明另一方面提供了一种上述的伏立康唑片的制备方法,所述的制备方法包括以下步骤:
[0020]
(1)按重量百分比取聚维酮k
30
,加入纯化水,配制成浓度为5%的聚维酮水溶液;
[0021]
(2)按重量百分比取伏立康唑、微晶纤维素、乳糖、交联羧甲纤维素钠、硬脂酸镁1.8%和月桂醇硫酸镁,混合,再加入步骤(1)配制好的聚维酮水溶液,搅拌混匀,制成软材;
[0022]
(3)将步骤(2)得到的软材在40-50℃下烘干,过20目筛整粒,压片机上压制成片,得到片芯;
[0023]
(4)按重量百分比取羟丙基甲基纤维素、滑石粉和二氧化钛,边加50%乙醇溶液边搅拌,混合均匀,80目筛网,得到包衣液;
[0024]
(5)在40-50℃的条件下对片芯进行包衣,包衣增重控制为3-5%,烘干,得到伏立康唑片。
[0025]
优选地,步骤(5)中所述的烘干的条件是50-60℃烘干5-10分钟。
[0026]
与现有技术相比,本发明的有益效果为:
[0027]
本发明提供了一种伏立康唑片及其制备方法。该伏立康唑片的溶出速度更快,稳
定性更高,药物杂质较少。本发明还发现微晶纤维素和月桂醇硫酸镁具有协同作用,通过对微晶纤维素和月桂醇硫酸镁配比的调整,溶出速度明显加快,药物总杂质减少;通过调整包衣中羟丙基甲基纤维素和滑石粉的比例,药物稳定性明显提高。另外,本发明提供的伏立康唑片的制备方法工艺简单,容易操作,适合工业化大批量生产。
具体实施方式
[0028]
为了使本发明实现的技术手段、创作特征、达成目的与功效易于明白了解,下面结合具体实施例进一步阐明本发明,但下述实施例仅为本发明的优选实施例,并非全部。基于实施方式中的实施例,本领域技术人员在没有做出创造性劳动的前提下所获得其它实施例,都属于本发明的保护范围。
[0029]
下述实施例中的实验方法,如无特殊说明,均为常规方法,下述实施例中所用的药品、材料、试剂等,如无特殊说明,均可从商业途径得到。
[0030]
实施例1
[0031]
一种伏立康唑片,包括由以下重量百分比的原料制成的片芯:伏立康唑30%、微晶纤维素45%、乳糖12%、交联羧甲纤维素钠5%、聚维酮k
30 4%、硬脂酸镁3%和月桂醇硫酸镁1%;
[0032]
所述的片芯外包裹了一层包衣;
[0033]
所述的包衣包含以下重量百分比的原料:羟丙基甲基纤维素18%、滑石粉0.8%、二氧化钛1.5%和50%乙醇溶液79.7%。
[0034]
上述的伏立康唑片的制备方法,所述的制备方法包括以下步骤:
[0035]
(1)按重量百分比取聚维酮k
30
,加入纯化水,配制成浓度为5%的聚维酮水溶液;
[0036]
(2)按重量百分比取伏立康唑、微晶纤维素、乳糖、交联羧甲纤维素钠、硬脂酸镁1.8%和月桂醇硫酸镁,混合,再加入步骤(1)配制好的聚维酮水溶液,搅拌混匀,制成软材;
[0037]
(3)将步骤(2)得到的软材在40℃下烘干,过20目筛整粒,压片机上压制成片,得到片芯;
[0038]
(4)按重量百分比取羟丙基甲基纤维素、滑石粉和二氧化钛,边加50%乙醇溶液边搅拌,混合均匀,80目筛网,得到包衣液;
[0039]
(5)在40℃的条件下对片芯进行包衣,包衣增重控制为5%,50℃烘干10分钟,得到伏立康唑片。
[0040]
实施例2
[0041]
一种伏立康唑片,包括由以下重量百分比的原料制成的片芯:伏立康唑44%、微晶纤维素20%、乳糖30%、交联羧甲纤维素钠2.3%、聚维酮k
30 2%、硬脂酸镁1.2%和月桂醇硫酸镁0.5%;
[0042]
所述的片芯外包裹了一层包衣;
[0043]
所述的包衣包含以下重量百分比的原料:羟丙基甲基纤维素24%、滑石粉1.2%、二氧化钛2.5%和50%乙醇溶液72.3%%。
[0044]
上述的伏立康唑片的制备方法,所述的制备方法包括以下步骤:
[0045]
(1)按重量百分比取聚维酮k
30
,加入纯化水,配制成浓度为5%的聚维酮水溶液;
[0046]
(2)按重量百分比取伏立康唑、微晶纤维素、乳糖、交联羧甲纤维素钠、硬脂酸镁
1.8%和月桂醇硫酸镁,混合,再加入步骤(1)配制好的聚维酮水溶液,搅拌混匀,制成软材;
[0047]
(3)将步骤(2)得到的软材在50℃下烘干,过20目筛整粒,压片机上压制成片,得到片芯;
[0048]
(4)按重量百分比取羟丙基甲基纤维素、滑石粉和二氧化钛,边加50%乙醇溶液边搅拌,混合均匀,80目筛网,得到包衣液;
[0049]
(5)在50℃的条件下对片芯进行包衣,包衣增重控制为3%,60℃烘干5分钟,得到伏立康唑片。
[0050]
实施例3
[0051]
一种伏立康唑片,包括由以下重量百分比的原料制成的片芯:伏立康唑33%、微晶纤维素40%、乳糖16%、交联羧甲纤维素钠4.5%、聚维酮k
30 3.5%、硬脂酸镁2.2%和月桂醇硫酸镁0.8%;
[0052]
所述的片芯外包裹了一层包衣;
[0053]
所述的包衣包含以下重量百分比的原料:羟丙基甲基纤维素22%、滑石粉1.0%、二氧化钛2.1%和50%乙醇溶液74.9%。
[0054]
上述的伏立康唑片的制备方法,所述的制备方法包括以下步骤:
[0055]
(1)按重量百分比取聚维酮k
30
,加入纯化水,配制成浓度为5%的聚维酮水溶液;
[0056]
(2)按重量百分比取伏立康唑、微晶纤维素、乳糖、交联羧甲纤维素钠、硬脂酸镁1.8%和月桂醇硫酸镁,混合,再加入步骤(1)配制好的聚维酮水溶液,搅拌混匀,制成软材;
[0057]
(3)将步骤(2)得到的软材在45℃下烘干,过20目筛整粒,压片机上压制成片,得到片芯;
[0058]
(4)按重量百分比取羟丙基甲基纤维素、滑石粉和二氧化钛,边加50%乙醇溶液边搅拌,混合均匀,80目筛网,得到包衣液;
[0059]
(5)在45℃的条件下对片芯进行包衣,包衣增重控制为4%,55℃烘干8钟,得到伏立康唑片。
[0060]
实施例4
[0061]
一种伏立康唑片,包括由含以下重量份的原料制成的片芯:伏立康唑36%、微晶纤维素30%、乳糖24.8%、交联羧甲纤维素钠3.8%、聚维酮k
30 3%、硬脂酸镁1.8%和月桂醇硫酸镁0.6%;即,所述的微晶纤维素和月桂醇硫酸镁的重量比为50:1。
[0062]
所述的片芯外包裹了一层包衣;
[0063]
所述的包衣包含以下重量百分比的原料:羟丙基甲基纤维素20%、滑石粉0.9%、二氧化钛1.8%和50%乙醇溶液77.3%;即,所述的羟丙基甲基纤维素和滑石粉的重量比约为22:1。
[0064]
上述的伏立康唑片的制备方法,所述的制备方法包括以下步骤:
[0065]
(1)按重量百分比取聚维酮k
30
,加入纯化水,配制成浓度为5%的聚维酮水溶液;
[0066]
(2)按重量百分比取伏立康唑、微晶纤维素、乳糖、交联羧甲纤维素钠、硬脂酸镁1.8%和月桂醇硫酸镁,混合,再加入步骤(1)配制好的聚维酮水溶液,搅拌混匀,制成软材;
[0067]
(3)将步骤(2)得到的软材在48℃下烘干,过20目筛整粒,压片机上压制成片,得到片芯;
[0068]
(4)按重量百分比取羟丙基甲基纤维素、滑石粉和二氧化钛,边加50%乙醇溶液边
搅拌,混合均匀,80目筛网,得到包衣液;
[0069]
(5)在48℃的条件下对片芯进行包衣,包衣增重控制为4%,55℃烘干8钟,得到伏立康唑片。
[0070]
实施例5
[0071]
一种伏立康唑片,与实施例4的区别仅在于,微晶纤维素21%,月桂醇硫酸镁0.7%,即,所述的微晶纤维素和月桂醇硫酸镁的重量比为30:1。
[0072]
所述的制备方法与实施例4相同。
[0073]
实施例6
[0074]
一种伏立康唑片,与实施例4的区别仅在于,微晶纤维素36%,月桂醇硫酸镁0.6%,即,所述的微晶纤维素和月桂醇硫酸镁的重量比为60:1。
[0075]
所述的制备方法与实施例4相同。
[0076]
实施例7
[0077]
一种伏立康唑片,与实施例4的区别仅在于,羟丙基甲基纤维素18%,滑石粉0.9%,即,所述的羟丙基甲基纤维素和滑石粉的重量比为20:1。
[0078]
所述的制备方法与实施例4相同。
[0079]
实施例8
[0080]
一种伏立康唑片,与实施例4的区别仅在于,羟丙基甲基纤维素20%,滑石粉0.8%,即,所述的羟丙基甲基纤维素和滑石粉的重量比为25:1。
[0081]
所述的制备方法与实施例4相同。
[0082]
对比例1
[0083]
一种伏立康唑片,与实施例4的区别仅在于,不加微晶纤维素。
[0084]
所述的制备方法与实施例4相同。
[0085]
对比例2
[0086]
一种伏立康唑片,与实施例4的区别仅在于,不加月桂醇硫酸镁。
[0087]
所述的制备方法与实施例4相同。
[0088]
对比例3
[0089]
一种伏立康唑片,与实施例4的区别仅在于,不加滑石粉。
[0090]
所述的制备方法与实施例4相同。
[0091]
对比例4
[0092]
中国专利cn102133202b中公开了一种含有伏立康唑的片剂,以该发明专利的实施例2所述的处方6作为本对比例。
[0093]
实验例1
[0094]
溶出度效果检测:
[0095]
检测方法按照溶出度测定法(中国药典2010年版二部附录xc第二法),以0.1m hcl溶液900ml为溶出介质,转速为50rpm,分别在5、10、20、30和45min检测溶出度。样品为本发明实施例1-8和对比例1-4所述的伏立康唑片,相同条件重复检测50次,并计算平均值,结果如表1所示。
[0096]
表1:不同样品溶出度(%)
[0097]
组别5min10min20min30min45min
实施例167.891.996.799.399.8实施例269.392.697.199.499.9实施例371.593.297.699.5100实施例479.397.799.6100100实施例574.694.898.499.6100实施例677.496.999.399.7100实施例778.197.199.599.8100实施例876.796.799.299.7100对比例138.377.586.295.697.4对比例242.679.490.497.198.2对比例351.785.393.897.898.8对比例453.290.698.799.199.6
[0098]
由表1可知,本发明提供的伏立康唑片能够快速溶出。根据实施例4、实施例5、实施例6和对比例1和2的结果对比,发现微晶纤维素和月桂醇硫酸镁具有协同作用,可通过对微晶纤维素和月桂醇硫酸镁配比的调整,提高溶出速度。
[0099]
实验例2
[0100]
稳定性试验:
[0101]
参照《中国药典》2010年版附录中药物稳定性考察指导原则要求,将本发明实施例1-8和对比例1-4所述的伏立康唑片,分别在高温(60℃)和高湿(rh92.5%)条件下放置15天后进行检测;另外,进行加速试验检测,条件为50℃,rh92.5%放置6个月。对药物中活性成分、总杂质和溶出度等指标进行考察,结果见表2-4。
[0102]
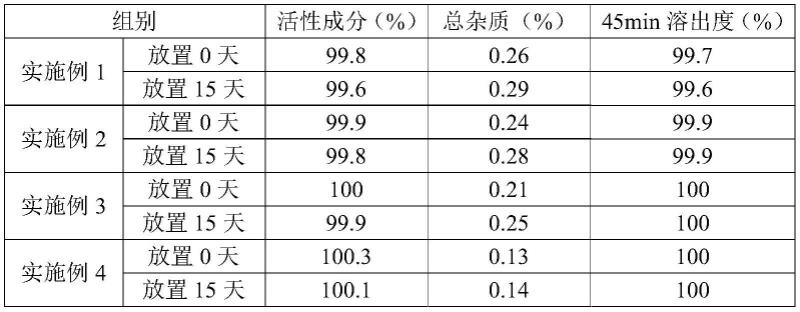
表2:高温条件下的检测结果
[0103]
[0104][0105]
表3:高湿条件下的检测结果
[0106]
[0107]
表4:加速试验检测的检测结果
[0108][0109]
由表2-4可知,本发明实施例1-8所述的伏立康唑片,在高温、高湿和加速条件下,其活性成分含量、药物总杂质含量和溶出度的变化并不明显,说明本发明提供的伏立康唑片稳定性好,药物总杂质较少。根据实施例4、实施例5、实施例6和对比例1和2第0天的结果对比,发现微晶纤维素和月桂醇硫酸镁具有协同作用,可通过对微晶纤维素和月桂醇硫酸镁配比的调整,减少药物总杂质含量;根据实施例4、7、8和对比例3的结果比较,发现加入一定比例的滑石粉,能够有效提高伏立康唑片的稳定性。
[0110]
以上所述,仅是本发明的较佳实施例而已,并非对本发明做任何形式上的限制,故凡未脱离本发明技术方案的内容,依据本发明的技术实质对以上实施例所做的任何简单修改、等同变化均视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1