一种阿戈美拉汀微乳、微乳凝胶及其制备方法与流程
1.本发明涉及一种阿戈美拉汀微乳、微乳凝胶及其制备方法,属于药物制剂学领域。
背景技术:
2.抑郁症是一种以情绪低落、兴趣减退、思维迟缓、认知功能损害为主要特征的情感障碍性疾病,具有患病率高、致残率高、复发率高和自杀率高等特点,近年来,随着社会压力增加,抑郁障碍的患病率逐年增加,成为危害人类健康的常见严重慢性疾病之一,据中国疾病预防控制中心估计,2020年我国抑郁症患病率将增至7.3%。基于抗抑郁药药理机制研究的发现,提出了抑郁症的单胺递质系统功能异常病理机制假说,现有的抗抑郁药物的主要作用机制是调节单胺递质系统。尽管新型抗抑郁药物在安全性和耐受性方面已经有很大的改进,但仍然存在着起效慢、部分患者疗效差、长期治疗中可能出现不良反应等,在治疗方面存在着很大的改进空间。
3.阿戈美拉汀是一种新型的抗抑郁药,是全球首个褪黑素类抗抑郁药,为褪黑激素受体激动剂和五羟色胺2c(5-ht2c)受体拮抗剂,其药理作用是能将褪黑激素受体激动剂活性与5-ht2c受体拮抗剂的性能结合起来,从而可有效地治疗抑郁症,改善睡眠参数和保持性功能,阿戈美拉汀对所有类型的抑郁症均有效。阿戈美拉汀是一种褪黑激素的萘类衍生物,其以萘核取代了吲哚环,使其较褪黑素更具代谢稳定性。它是一个下丘脑褪黑素受体的选择性及特异性激动剂,同时又兼有弱的5-ht受体竞争性拮抗活性,显现出一种褪黑素受体激动剂和选择性5-ht拮抗剂双重作用的新型药理学特性。它可模拟褪黑素的作用,又具有独特的作用方式,是治疗生理节律紊乱性疾病(如睡眠障碍/抑郁症)的极具前途的候选药物。阿戈美拉汀(agomelatine)为白色或类白色结晶性粉末,化学名称n-[2-(7-甲氧基萘-1-基)乙基]乙酰胺,分子式是c
15h17
no2,分子量243.3,化学结构式为:
[0004][0005]
阿戈美拉汀现有的上市剂型只有口服片剂,由法国施维雅公司开发,2009年2月24日在欧盟获得批准上市,2011年通过cfda批准在国内上市,商品名维度新。阿戈美拉汀片规格为25mg,每天睡前口服给药一次,阿戈美拉汀片虽吸收迅速,吸收率较高,但该药肝首过效应大,生物利用度低,仅有3%~4%;并且在个体间和个体内的生物差异相当大,具有高度的变异性。因此有必要对口服片剂进行改良,制备出肝毒性小、生物利用度高的给药剂型。
[0006]
透皮给药系统(tdds,transdermal drug delivery systems)是指将透皮给药的制剂施用于皮肤,药物透过皮肤,由毛细血管吸收进入全身血液循环达到有效血药浓度并转移至各组织或病变部位,起治疗或预防疾病作用。透皮给药的方式可避免口服给药可能
发生的肝首过效应及胃肠灭活;维持恒定的最佳血药浓度或生理效应,减少胃肠给药的副作用;延长有效作用时间,减少用药次数;通过改变给药面积调节给药剂量,减少个体差异,且患者可以自主用药,也可以随时停止用药。
[0007]
微乳(microemulsion,me)微乳是均一透明且热力学、动力学稳定的多相体系,由油、水、乳化剂和助乳化剂组成,粒径在10-100nm之间。微乳在透皮给药系统(transdermal drug delivery systems,tdds)中具有诸多优势,如:能显著增加药物的溶解度,维持较高的药物浓度,提高微乳与皮肤间的药物浓度梯度,增加透皮速率,增加角质层脂质双层的流动性,提高药物的透皮能力,提高生物利用度。
[0008]
微乳凝胶(microemulsion-based gels,mbgs)是将微乳加入至由天然高分子聚合物、纤维素衍生物、嵌段聚合物等高分子材料组成的凝胶基质中,形成透明、均质、稳定的凝胶网状结构,网络结构中含有微乳液滴;微乳凝胶作为一种新型经皮给药载体,具有微乳与凝胶的双重优点。微乳凝胶通过微乳提高药物的溶解度,降低皮肤的扩散屏障,增加药物的透皮能力,提高透皮速率;又能通过凝胶提高微乳的黏度,改善微乳与皮肤的黏附性和涂展性,降低药物的刺激性,达到透皮,提高生物利用度的作用。微乳凝胶作为经皮给药载体,可以避免肝脏的首过清除效应,减小药物对胃肠道的刺激,降低毒副作用,且易于涂布患者用药方便,且稳定性好。
技术实现要素:
[0009]
本发明针对上述现有剂型的不足,提供一种稳定性好、且具有渗透促进作用的阿戈美拉微乳及微乳凝胶。
[0010]
本发明解决上述问题的技术方案如下:一种阿戈美拉汀微乳,包含药物活性成分和药物载体,所述药物活性成分为阿戈美拉汀,所述药物载体包括乳化剂、助乳化剂、油相和水相。
[0011]
在本发明优选的方案中,阿戈美拉汀微乳是为水包油型微乳。
[0012]
在本发明优选的方案中,油相选自脂肪酸甘油酯、聚乙二醇甘油酯、羧酸酯和丙二醇酯中的一种或多种;优选的,脂肪酸甘油酯选自中链甘油三酯、油酸乙酯、亚油酸乙酯、单亚油酸甘油酯、三乙酸甘油酯、辛酸癸酸三甘油酯、单硬脂酸甘油酯、单油酸甘油酯中的一种或多种,聚乙二醇甘油酯选自油酸聚乙二醇甘油酯、聚乙二醇月桂醇甘油酯、辛酸癸酸聚乙二醇甘油酯、月桂酸聚乙二醇甘油酯、聚乙二醇癸酸甘油酯、聚乙二醇硬脂酸甘油酯和聚乙二醇异硬脂酸甘油酯中的一种或多种,羧酸酯选自棕榈酸异丙酯、乳酸月桂基酯、肉豆蔻酸异丙酯、己二酸二异丙酯、己二酸二正丁酯和癸二酸二乙酯中的一种或多种,丙二醇酯选自丙二醇单辛酸酯、丙二醇单月桂酸酯、丙二醇油酸酯、丙二醇豆蔻酸酯和丙二醇二辛酸二癸酸酯中的一种或多种;更优选丙二醇单辛酸酯和丙二醇单月桂酸酯中的至少一种。
[0013]
在本发明优选的方案中,乳化剂选自聚山梨醇酯、聚氧乙烯油及其衍生物、聚乙二醇甘油酯中的一种或多种;优选的,聚山梨醇酯选自吐温20、吐温40、吐温60、吐温80和吐温85中的一种或多种;聚氧乙烯油及其衍生物选自聚氧乙烯蓖麻油、聚氧乙烯三酰甘油和聚氧乙烯氢化蓖麻油中的一种或多种;聚乙二醇甘油酯选自酸癸酸聚乙二醇甘油酯、聚乙二醇月桂酸甘油酯、聚乙二醇月桂醇甘油酯、聚乙二醇癸酸甘油酯、聚乙二醇硬脂酸甘油酯和聚乙二醇异硬脂酸甘油酯中的一种或多种;更优选辛酸癸酸聚乙二醇甘油酯和聚氧乙烯氢
化蓖麻油中的至少一种。
[0014]
聚氧乙烯氢化蓖麻油包括聚氧乙烯30氢化蓖麻油、聚氧乙烯35氢化蓖麻油、聚氧乙烯40氢化蓖麻油和聚氧乙烯60氢化蓖麻油中的一种或多种;优选聚氧乙烯40氢化蓖麻油。
[0015]
在本发明优选的方案中,助乳化剂选自醇、聚乙二醇和醚中的一种或几种;优选的,醇选自无水乙醇、乙二醇、丙二醇、正丙醇、异丙醇、丙三醇、正丁醇和正辛醇中的一种的或多种,聚乙二醇选自聚乙二醇200、聚乙二醇400、聚乙二醇600和聚乙二醇800中的一种或多种,醚选自二乙二醇单乙醚、鲸蜡硬脂醇聚醚、硬脂醇聚醚、鲸蜡醇聚氧乙烯醚和月桂基聚氧乙烯醚中的一种或多种;更优选二乙二醇单乙醚和无水乙醇中的至少一种。
[0016]
在本发明优选的方案中,水相选自去离子水、蒸馏水、注射用水、高纯水或超纯水。
[0017]
在本发明优选的方案中,阿戈美拉汀微乳还包括药学上可接受的辅料,所述辅料包括保湿剂、渗透压调节剂、芳香剂、防腐剂、抗氧化剂和促渗剂中的一种或多种。
[0018]
保湿剂包括甘油、石蜡油、山梨醇、丙二醇、异丙醇、乙醇、丁二醇和透明质酸中的一种或多种。
[0019]
渗透压调节剂包括甘油、硼砂、葡萄糖、甘露糖醇、丙二醇、山梨醇和氯化钠中的一种或多种。
[0020]
芳香剂包括薰衣草精油、橘子香精、草莓香精、巧克力香精、薄荷香精和牛奶香精中的一种或多种;优选薰衣草精油;更优选的,在本发明中,以处方总重量计,芳香剂的重量百分比为0~2%;优选0~1%;更优选0.01~0.5%;进一步优选0.01~0.35%。
[0021]
防腐剂包括尼泊金甲酯、尼泊金乙酯、尼泊金丙酯、尼泊金甲酯钠、尼泊金乙酯钠、尼泊金丙酯钠、山梨酸、山梨酸钾、苯甲酸钠、三氯叔丁醇和苯扎溴铵中的一种或多种。
[0022]
抗氧化剂包括bha(丁基羟基茴香醚)、bht(二丁基羟基甲苯)、tbhq(特丁基对苯二酚)、pg(没食子酸丙酯)、ap(l-抗坏血酸棕榈酸酯)、eq(乙氧基喹啉)、焦亚硫酸钠、dltp(硫代二丙酸双月桂酯)等合成抗氧化剂以及茶多酚、生育酚、葡萄籽提取物等天然抗氧化剂。
[0023]
促渗剂包括油酸、硬脂酸、异硬脂酸、乳酸、月桂酸、聚乙二醇、肉豆蔻酸异丙酯、棕榈酸异丙酯、二甲基乙酰胺、甘油三酸酯、薄荷醇、薄荷脑、丙二醇、冰片、蛇床子油、氮酮、十四烷基硫酸钠、香叶醇、茴香脑和癸基甲基亚砜中的一种或多种。
[0024]
在本发明优选的方案中,以处方总重量计,阿戈美拉汀的重量百分比为0.1~20%;优选0.1~15%;更优选0.5~10%;进一步优选1~5%;更进一步优选1~3%;例如1~2.5%、1.5~2.5%、2%、1%等。
[0025]
在本发明优选的方案中,以处方总重量计,油相的重量百分比为1~35%;优选1~25%;更优选1~15%;进一步优选3~10%,例如5%、9.5%;更进一步优选4~8%。
[0026]
在本发明优选的方案中,以处方总重量计,乳化剂的重量百分比为1~50%;优选1~35%;更优选5~25%;进一步优选5~15%;更进一步优选6~12%;例如10~12%、10.8%等。
[0027]
在本发明优选的方案中,以处方总重量计,助乳化剂的重量百分比为1~30%;优选1~25%;更优选5~25%;进一步优选5~20%;更进一步优选5~15%,例如5~8%、7.4%等;或者,优选10~25%;更优选15~22%。
[0028]
在本发明优选的方案中,以处方总重量计,水相的重量百分比为10~90%;优选40~85%;更优选50~80%;进一步优选55~75%,例如62%、64%、70.3%;更进一步优选60~70%或62~72%。
[0029]
在本发明优选的方案中,以处方总重量计,乳化剂和助乳化剂的重量和占处方总重量比例优选在30%以下,更优选在20%以下;
[0030]
在本发明优选的方案中,以处方总重量计,各组分的重量百分比如下:
[0031]
组分百分比阿戈美拉汀0.1~20%油相1~40%乳化剂1~60%助乳化剂1~30%水相5~90%
[0032]
;
[0033]
或者,
[0034]
组分百分比阿戈美拉汀0.1~15%油相1~35%乳化剂1~50%助乳化剂1~30%芳香剂0~2%水相10~90%
[0035]
;
[0036]
或者,
[0037]
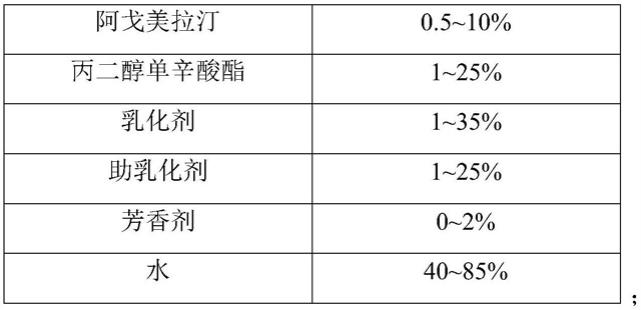
组分百分比阿戈美拉汀0.5~10%油相1~25%乳化剂1~35%助乳化剂1~25%芳香剂0~2%水相40~85%
[0038]
;
[0039]
或者,
[0040]
组分百分比阿戈美拉汀1~5%油相1~15%乳化剂5~25%助乳化剂5~25%芳香剂0~1%水相50~80%
[0041]
;
[0042]
或者,
[0043]
组分百分比阿戈美拉汀1~5%油相3~15%乳化剂5~15%助乳化剂5~25%芳香剂0~0.5%水相55~75%
[0044]
;
[0045]
或者,
[0046]
组分百分比阿戈美拉汀1~5%油相3~15%乳化剂5~15%助乳化剂5~15%芳香剂0~0.5%水相55~75%
[0047]
。
[0048]
在本发明优选的方案中,油相为丙二醇单辛酸酯时,以处方总重量计,各组分的重量百分比如下:
[0049][0050][0051]
或者,
[0052]
组分百分比阿戈美拉汀1~5%丙二醇单辛酸酯3~15%乳化剂5~15%助乳化剂5~25%芳香剂0~0.5%水55~75%
[0053]
;
[0054]
或者,
[0055]
组分百分比阿戈美拉汀1~5%丙二醇单辛酸酯3~15%乳化剂5~15%助乳化剂5~25%芳香剂0~0.5%水55~75%
[0056]
;
[0057]
或者,
[0058][0059][0060]
或者,
[0061]
组分百分比阿戈美拉汀1~5%丙二醇单辛酸酯3~15%聚氧乙烯蓖麻油5~15%二乙二醇单乙基醚5~25%芳香剂0~0.5%水55~75%
[0062]
;
[0063]
或者,
[0064]
组分百分比阿戈美拉汀1~5%丙二醇单辛酸酯3~10%聚氧乙烯蓖麻油5~15%二乙二醇单乙基醚10~25%薰衣草精油0~0.5%水55~75%
[0065]
;
[0066]
或者,
[0067][0068][0069]
或者,
[0070]
组分百分比阿戈美拉汀1~5%丙二醇单辛酸酯3~15%聚氧乙烯氢化蓖麻油5~15%二乙二醇单乙基醚5~25%水55~75%
[0071]
或者,
[0072]
组分百分比阿戈美拉汀1~2.5%丙二醇单辛酸酯5~10%聚氧乙烯氢化蓖麻油10~12%二乙二醇单乙基醚5~20%水62~75%
[0073]
或者,
[0074]
组分百分比阿戈美拉汀2%丙二醇单辛酸酯9.5%聚氧乙烯氢化蓖麻油10.8%二乙二醇单乙基醚7.4%水70.3%
[0075]
或者,
[0076][0077][0078]
在本发明优选的方案中,油相为丙二醇单月桂酸酯,以处方总重量计,各组分的重量百分比如下:
[0079]
组分百分比阿戈美拉汀0.5~10%丙二醇单月桂酸酯1~25%乳化剂1~35%助乳化剂1~25%芳香剂0~2%水40~85%
[0080]
;
[0081]
或者,
[0082]
组分百分比阿戈美拉汀1~5%丙二醇单月桂酸酯3~15%乳化剂5~15%助乳化剂5~25%芳香剂0~0.5%水55~75%
[0083]
;
[0084]
或者,
[0085]
[0086][0087]
或者,
[0088]
组分百分比阿戈美拉汀1~5%丙二醇单月桂酸酯3~15%聚氧乙烯蓖麻油5~15%二乙二醇单乙基醚5~25%芳香剂0~0.5%水55~75%
[0089]
;
[0090]
或者,
[0091]
组分百分比阿戈美拉汀1~5%丙二醇单月桂酸酯3~10%聚氧乙烯蓖麻油5~15%二乙二醇单乙基醚10~25%薰衣草精油0~0.5%水55~75%
[0092]
;
[0093]
或者,
[0094]
组分百分比阿戈美拉汀1~5%丙二醇单月桂酸酯3~15%聚氧乙烯蓖麻油5~15%二乙二醇单乙基醚5~25%薰衣草精油0~0.5%水55~75%
[0095]
。
[0096]
或者,
[0097]
组分百分比阿戈美拉汀1~5%丙二醇单月桂酸酯3~15%聚氧乙烯氢化蓖麻油5~15%二乙二醇单乙基醚5~25%水55~75%
[0098]
或者,
[0099]
组分百分比阿戈美拉汀1.5~2.5%丙二醇单月桂酸酯8~10%聚氧乙烯氢化蓖麻油10~12%二乙二醇单乙基醚5~8%水62~75%
[0100]
或者,
[0101]
组分百分比阿戈美拉汀2%丙二醇单月桂酸酯9.5%聚氧乙烯氢化蓖麻油10.8%二乙二醇单乙基醚7.4%水70.3%
[0102]
在本发明优选的方案中,所述阿戈美拉汀微乳的粒径为10-100nm;优选的,粒径可以为10~90nm,或者30~100nm,或者40~80nm;或者50~80nm;或者50~65nm。
[0103]
在本发明优选的方案中,本发明上述阿戈美拉汀微乳的应用,可以直接涂抹于患处,也可制备成其他药物剂型,如喷雾剂、膜剂、软膏、乳膏、凝胶、贴剂、巴布剂等,优选所述药物剂型为凝胶或贴剂。
[0104]
本发明所述的阿戈美拉汀微乳的制备方法,包括以下步骤:
[0105]
1)称取所述重量配比的阿戈美拉汀、油相、乳化剂、助乳化剂,磁力搅拌下混合均匀;或者,称取所述重量配比的乳化剂、助乳化剂与油相,磁力搅拌下混合均匀,再将阿戈美拉汀溶解在混合物中;
[0106]
2)将水相加入步骤1)得到的混合溶液中,磁力搅拌下混合均匀,即得阿戈美拉汀微乳。
[0107]
本发明还提供一种阿戈美拉汀微乳凝胶,包括阿戈美拉汀微乳和凝胶基质。
[0108]
在本发明优选的方案中,凝胶基质包括卡波姆、羟丙甲基纤维素、羧甲基纤维素钠、黄原胶、阿拉伯胶、海藻酸钠和泊洛沙姆中的一种或多种;优选卡波姆。
[0109]
可用于本发明的卡波姆包括卡波姆980、卡波姆934、卡波姆940、卡波姆941、卡波姆971、卡波姆974、卡波姆981、卡波姆etd 2020、卡波姆ultrez 21。
[0110]
在本发明优选的方案中,凝胶基质的加入量为阿戈美拉汀微乳总重量的0.1%~3%;优选0.1%~1.5%;更优选0.3%~1.0%;进一步优选0.5%~0.7%。
[0111]
在本发明优选的方案中,微乳凝胶还包括ph调节剂,优选所述ph调节剂调节ph至3.0~10.0;优选4.0~8.0;更优选5.0~6.5;ph调节剂包括盐酸、氢氧化钠、磷酸盐、硼酸、硼酸盐、三羟甲基氨基甲烷、枸橼酸、枸橼酸盐、和三乙醇胺中的一种或多种;优选三乙醇胺。
[0112]
本发明所述的阿戈美拉汀微乳凝胶的制备方法,包括向阿戈美拉汀微乳中加入凝胶基质经溶胀、搅拌均匀后,加入ph调节剂调节ph值,制得的均一透明半固体制剂,即为阿戈美拉汀微乳凝胶。
[0113]
在本发明所述的阿戈美拉汀微乳和阿戈美拉汀微乳凝胶在用于制备治疗精神类
疾病药物中的应用,优选的,所述精神类疾病是指抑郁症,更优选的,所述精神类疾病是指重症抑郁症。
[0114]
本发明制备微乳的油相、乳化剂和助乳化剂,有时也起着药物促渗剂的作用。可见,微乳液作为药物载体可能促进药物的经皮吸收。以微乳为药物活性成分阿戈美拉汀的载体,制备微乳的关键在于组分的选择与各组分比例的设计。
[0115]
本发明向微乳液中加入高分子凝胶材料,可以形成透明、稳定的网状结构,在网络中含有微乳液液滴,称为微乳液凝胶,凝胶稳定的三维网状结构可防止药物沉淀的析出,这一点对于具有多晶现象的阿戈美拉汀的给药来讲是十分有意义的。考察不同凝胶基质及同一基质不同浓度对微乳凝胶形成的影响,从而得到高渗透性的阿戈美拉汀微乳凝胶制剂。本发明凝胶具有很好的相容性,对皮肤的刺激性小。
[0116]
药物微乳凝胶经皮给药的限速步骤主要有两个,一是药物从基质中释放的过程,二是药物经皮肤的渗透过程。微乳液组成的设计可影响以上两个步骤。为通过调整微乳的组成配方来控制药物的经皮吸收提供了可能。
[0117]
本发明将阿戈美拉汀、透皮给药系统、微乳和微乳凝胶联合应用,制成毒副作用小、稳定性好、疗效高的抗抑郁类药物。目前尚无阿戈美拉汀微乳和微乳凝胶透皮制剂的公开报道,本发明采用微乳和微乳凝胶可明显提高载药能力,所需乳化剂、助乳化剂量少,且可显著增强阿戈美拉汀透过皮肤的能力,且起效时间快,增加单位面积累积渗透量,进而提高生物利用度,给药方便。另外,本发明的制备工艺简单易行,可工业化生产,制得的产品质量稳定,便于储存运输。
具体实施方式
[0118]
以下对本发明的原理和特征进行描述,所举实例只用于解释本发明,并非用于限定本发明的范围。
[0119]
实施例1总重量为100g的阿戈美拉汀微乳的制备
[0120]
实施例1.1
[0121]
组分物料名称处方量(g)活性成分阿戈美拉汀0.5油相单亚油酸甘油酯3.0乳化剂吐温8013.4助乳化剂无水乙醇5.3水相水77.8
[0122]
将上述重量的油相、乳化剂、助乳化剂、阿戈美拉汀充分混合均匀,在室温、磁力搅拌条件下滴加上述重量的水,继续搅拌30分钟,即得阿戈美拉汀微乳。
[0123]
实施例1.2
[0124]
组分物料名称处方量(g)活性成分阿戈美拉汀0.5油相丙二醇单辛酸酯3.0乳化剂聚氧乙烯蓖麻油7.2助乳化剂丙二醇9.5
水相水79.8
[0125]
制备方法同实施例1.1。
[0126]
实施例1.3
[0127][0128][0129]
制备方法同实施例1.1。
[0130]
实施例1.4
[0131]
组分物料名称处方量(g)活性成分阿戈美拉汀5.0油相油酸乙酯13.8乳化剂聚氧乙烯氢化蓖麻油25.5助乳化剂二乙二醇单乙基醚10.8水相水44.9
[0132]
制备方法同实施例1.1。
[0133]
实施例1.5
[0134]
组分物料名称处方量(g)活性成分阿戈美拉汀3.0油相单亚油酸甘油酯9.8乳化剂聚氧乙烯氢化蓖麻油30.6助乳化剂聚乙二醇4003.5水相水53.1
[0135]
制备方法同实施例1.1。
[0136]
实施例1.6
[0137]
组分物料名称处方量(g)活性成分阿戈美拉汀2.0油相丙二醇单月桂酸酯8乳化剂辛酸癸酸聚乙二醇甘油酯18.5助乳化剂丙三醇3.0水相水68.5
[0138]
制备方法同实施例1.1。
[0139]
实施例1.7
[0140][0141][0142]
制备方法同实施例1.1。
[0143]
实施例1.8
[0144]
组分物料名称处方量(g)活性成分阿戈美拉汀3.0油相丙二醇单月桂酸酯9.8乳化剂聚氧乙烯蓖麻油18.6助乳化剂二乙二醇单乙基醚10.2助乳化剂无水乙醇4.2水相水54.2
[0145]
制备方法同实施例1.1。
[0146]
实施例1.9
[0147]
组分物料名称处方量(g)活性成分阿戈美拉汀2.0油相丙二醇单辛酸酯9.5乳化剂聚氧乙烯氢化蓖麻油10.8助乳化剂二乙二醇单乙基醚7.4水相水70.3
[0148]
制备方法同实施例1.1。
[0149]
实施例1.10
[0150]
组分物料名称处方量(g)活性成分阿戈美拉汀2.0油相单亚油酸甘油酯9.5乳化剂聚氧乙烯氢化蓖麻油10.8助乳化剂二乙二醇单乙基醚7.4水相水70.3
[0151]
制备方法同实施例1.1。
[0152]
实施例1.11
[0153]
[0154][0155]
制备方法同实施例1.1。
[0156]
实施例1.12
[0157]
组分物料名称处方量(g)活性成分阿戈美拉汀2.0油相丙二醇单辛酸酯6.0乳化剂聚氧乙烯氢化蓖麻油9.0助乳化剂二乙二醇单乙基醚17.9芳香剂薰衣草精油0.1水相水65.0
[0158]
将上述重量的油相、乳化剂、助乳化剂、芳香剂、阿戈美拉汀充分混合均匀,在室温、磁力搅拌条件下滴加上述重量的水,继续搅拌30分钟,即得阿戈美拉汀微乳。
[0159]
实施例1.13
[0160]
组分物料名称处方量(g)活性成分阿戈美拉汀2.0油相丙二醇单辛酸酯6.0乳化剂聚氧乙烯氢化蓖麻油9.0助乳化剂二乙二醇单乙基醚17.9防腐剂尼泊金甲酯0.1水相水65.0
[0161]
将上述重量的油相、乳化剂、助乳化剂、防腐剂、阿戈美拉汀充分混合均匀,在室温、磁力搅拌条件下滴加上述重量的水,继续搅拌30分钟,即得阿戈美拉汀微乳。
[0162]
实施例1.14
[0163][0164][0165]
将上述重量的油相、乳化剂、助乳化剂、芳香剂、防腐剂、阿戈美拉汀充分混合均
匀,在室温、磁力搅拌条件下滴加上述重量的水,继续搅拌30分钟,即得阿戈美拉汀微乳。
[0166]
实施例1.15
[0167]
组分物料名称处方量(g)活性成分阿戈美拉汀1.0油相丙二醇单辛酸酯4.95乳化剂聚氧乙烯氢化蓖麻油14.85助乳化剂二乙二醇单乙基醚29.7水相水49.5
[0168]
将上述重量的乳化剂、助乳化剂与油相混合均匀,再将阿戈美拉汀溶解在混合物中,在室温、磁力搅拌条件下,滴加上述重量的水,继续搅拌30分钟,即得阿戈美拉汀微乳。
[0169]
实施例1.16
[0170]
组分物料名称处方量(g)活性成分阿戈美拉汀1.0油相丙二醇单辛酸酯5.0乳化剂聚氧乙烯氢化蓖麻油10.0助乳化剂二乙二醇单乙基醚20.0水相水64
[0171]
制备方法同实施例1.1。
[0172]
实施例1.17
[0173]
组分物料名称处方量(g)活性成分阿戈美拉汀2.0油相丙二醇单月桂酸酯9.5乳化剂聚氧乙烯氢化蓖麻油10.8助乳化剂二乙二醇单乙基醚7.4水相水70.3
[0174]
制备方法同实施例1.1。
[0175]
对照例1.1
[0176]
组分物料名称处方量(g)活性成分阿戈美拉汀2.0溶剂二乙二醇单乙基醚46.8促渗剂丙二醇5.2水相水46.0
[0177]
将上述重量的溶剂、促渗剂、阿戈美拉汀充分混合均匀,在室温、磁力搅拌条件下滴加上述重量的水,继续搅拌30分钟,即得阿戈美拉汀溶液。
[0178]
对照例1.2
[0179]
组分物料名称处方量(g)活性成分阿戈美拉汀5.0溶剂二乙二醇单乙基醚46.8
促渗剂丙二醇5.2水相水43.0
[0180]
制备方法同对照例1.1
[0181]
将上述实施例1.1-1.17制备的阿戈美拉汀微乳,以及对照例1.1、1.2进行检测,测定方法及结果如下:
[0182]
1、阿戈美拉汀微乳粒径检测
[0183]
仪器:zetasizer电位-粒度分析仪(英国马尔文)温度为25℃。粒度测量结果见表1。
[0184]
2、阿戈美拉汀微乳体外渗透试验检测
[0185]
用剃须刀小心剔除大鼠腹部毛发,剥离腹部皮肤,仔细除去皮下组织及粘连物,用生理盐水清洗干净,滤纸吸干水分。组装franz扩散池(有效面积1.76cm2),将鼠皮置于供给室与接收室之间,角质层朝向供给室,真皮层朝向接收室,固定。将franz扩散池置于32℃
±
0.5℃恒温加热磁力搅拌器上,转速350rpm。在供给室中加入阿戈美拉汀微乳(相当阿戈美拉汀10mg),以30%乙醇-生理盐水作为接收介质,分别于0.5、1、2、3、4、6小时取样3ml,每次补充同体积空白接收介质并排除气泡,所取液体经0.45μm微孔滤膜滤过后,采用hplc法检测样品中阿戈美拉汀的含量,计算相应点的累积透过量(μg/cm2)。结果见表1。
[0186]
表1.阿戈美拉汀微乳粒度和体外渗透试验检测表
[0187][0188][0189]
实施例2.阿戈美拉汀微乳凝胶的制备
[0190]
实施例2.1
[0191]
将实施例1.7制备的100g阿戈美拉汀微乳与重量为0.5g的卡波姆混合,充分溶胀,加入三乙醇胺溶液,调节ph至5.0~6.5,即得到阿戈美拉汀微乳凝胶。其中充分溶胀指在室温下溶胀过夜或在40℃条件下溶胀2小时以上即可。上述微乳凝胶溶胀过程包括但不限于所列的温度、时间,最终是以达到溶胀目的为准。
[0192]
上述阿戈美拉汀微乳或阿戈美拉汀微乳凝胶中还可加入防腐剂、抗氧剂、保水剂等成分。
[0193]
实施例2.2
[0194]
将实施例1.8制备的100g阿戈美拉汀微乳与重量为0.5g的卡波姆混合,充分溶胀,加入三乙醇胺溶液,调节ph至5.0~6.5,得到阿戈美拉汀微乳凝胶。
[0195]
实施例2.3
[0196]
将实施例1.9制备的100g阿戈美拉汀微乳与重量为0.5g的卡波姆混合,充分溶胀,加入三乙醇胺溶液,调节ph至5.0~6.5,得到阿戈美拉汀微乳凝胶。
[0197]
实施例2.4
[0198]
将实施例1.10制备的100g阿戈美拉汀微乳与重量为0.3g的卡波姆混合,充分溶胀,加入三乙醇胺溶液,调节ph至5.0~6.5,得到阿戈美拉汀微乳凝胶。
[0199]
实施例2.5
[0200]
将实施例1.10制备的100g阿戈美拉汀微乳与重量为0.5g的卡波姆混合,充分溶胀,加入三乙醇胺溶液,调节ph至5.0~6.5,得到阿戈美拉汀微乳凝胶。
[0201]
实施例2.6
[0202]
将实施例1.10制备的100g阿戈美拉汀微乳与重量为0.8g的卡波姆混合,充分溶胀,加入三乙醇胺溶液,调节ph至5.0~6.5,得到阿戈美拉汀微乳凝胶。
[0203]
实施例2.7
[0204]
将实施例1.10制备的100g阿戈美拉汀微乳与重量为1.0g的卡波姆混合,充分溶胀,加入三乙醇胺溶液,调节ph至5.0~6.5,得到阿戈美拉汀微乳凝胶。
[0205]
对照例2.1
[0206]
将对照例1.1制备的100g阿戈美拉汀溶液与重量为0.4g的卡波姆混合,充分溶胀,加入三乙醇胺溶液,调节ph至5.0~6.5,得到阿戈美拉汀凝胶。
[0207]
对照例2.2
[0208]
将对照例1.2制备的100g阿戈美拉汀溶液与重量为0.4g的卡波姆混合,充分溶胀,加入三乙醇胺溶液,调节ph至5.0~6.5,得到阿戈美拉汀凝胶。
[0209]
将上述实施例2.1-2.7制备的阿戈美拉汀微乳凝胶进行检测,测定方法及结果如下:
[0210]
1、阿戈美拉汀微乳凝胶粘度的测定
[0211]
用粘度计检测微乳凝胶的粘度,温度为25℃。粘度测量结果见表2。
[0212]
2、阿戈美拉汀微乳凝胶的体外经皮渗透试验
[0213]
皮肤的获取方法、franz扩散池的组装及测定方法同“阿戈美拉汀微乳的体外经皮渗透试验”。在供给池中加入实施例2.1-2.7阿戈美拉汀微乳凝胶300mg。体外经皮渗透试验测量结果见表2。
[0214]
表2.阿戈美拉汀微乳凝胶粘度和体外经皮渗透试验检测表
[0215] 粘度(mpa.s)q6(μg/cm2)实施例2.128380
±
32245.17
±
8.23实施例2.225847
±
54573.38
±
2.72实施例2.329053
±
42185.85
±
7.52
实施例2.426634
±
53853.42
±
6.88实施例2.531208
±
36548.42
±
6.88实施例2.648425
±
34743.58
±
3.11对照例2.128431
±
38618.58
±
3.22对照例2.227652
±
42733.36
±
2.56
[0216]
3、皮肤刺激性研究
[0217]
使用白色雄性兔子(n=3)作为测试动物。用电动剃须刀将背侧的兔毛剃去,然后将大约50mg的实施例2.2和对照例2.2样品分别涂在每只兔的两个部位(对应位置),涂抹面积大约10cm2。将兔子放回笼子里。在给药24小时后,用自来水擦拭测试部位除去残留的凝胶。通过肉眼观察兔子皮肤红斑/水肿的情况,连续观察3天,按照表3和表4标准进行评分和评价。
[0218]
表3.皮肤刺激反应评分
[0219]
红斑评分无红斑0勉强可见1明显红斑2中等~严重红斑3紫红色红斑并有焦痂形成4水肿/无水肿0勉强可见1皮肤隆起轮廓清楚2水肿隆起约1mm3水肿隆起超过1mm,范围扩大4总分8
[0220]
表4.皮肤刺激强度评价
[0221]
强度分值无刺激性0~0.4轻刺激性0.5~2.9中等刺激性3.0~5.9强刺激性6.0~8.0
[0222]
结果两组均没有观察到红斑/水肿,得分为0。因此,阿戈美拉汀微乳凝胶对皮肤无刺激性。
[0223]
4、稳定性实验
[0224]
将实施例2.3-2.4制备的阿戈美拉汀微乳凝胶置于30℃
±
2℃;rh65%
±
5%条件下。分别于0,1,2,3,6个月末取样观察凝胶的的情况,测式结果见表5。结果显示阿戈美拉汀微乳凝胶稳定性良好。
[0225]
表5.阿戈美拉汀微乳凝胶稳定性测式结果
[0226][0227]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1