含有可活化抗体的组合物的制作方法
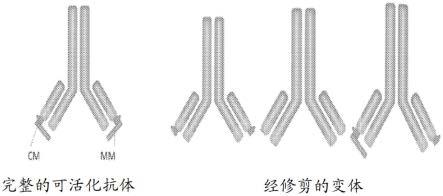
含有可活化抗体的组合物
1.相关申请的交叉引用
2.本技术要求2020年4月9日提交的美国临时申请第63/007,776号的优先权权益,所述申请的整个内容通过引用方式并入本文。
3.对序列表的引用
4.本技术包括以电子格式提交的序列表。该序列表的名称为“cytx-056-pct_st25.txt”,创建于2021年3月31日,并且大小为88,000字节。电子格式的序列表中的信息是本技术的一部分,并通过引用方式以其整体并入本文。
技术领域
5.本公开涉及与完整的可活化抗体及其经修剪的变体有关的组合物和方法,包括组合物和用于制备、纯化、测量、监测和使用所述组合物的方法。
背景技术:
6.单克隆抗体是一类不断增长的治疗性化合物,每一类都被设计为结合至多种临床适应症中的任何一种涉及的靶抗原。迄今为止,存在大量处于研究阶段或批准作为新药的单克隆抗体产品。虽然该产品类别的迅速增长导致用于制造它们的工艺取得了重大进展,但产品聚集仍然是每个新单克隆抗体药物的制造工艺开发过程中必须解决的重要问题。varsha,等人biopharm international第26卷,第3期。产品聚集是不想要的,因为它导致药物产品的产量降低,并且如果不从药物产物组合物中去除的话会导致潜在的安全问题。同上。例如,聚集可能会导致亚可见颗粒形成,这些颗粒可能会暴露正常情况下未暴露的表位,如果施用于患者可能会导致免疫原性增加。同上。
7.聚集体通常是在细胞培养中的产品表达过程中、下游处理中的产品纯化过程中或储存过程中不可逆地形成的大的、缠结的变性抗体分子簇。同上。多种因素可能有助于聚集体的形成。已经寻求基于抗体的疗法的安全性和/或功效的改进,并且在某些情况下,通过修饰分子的结构实现了基于抗体的疗法的安全性和/或功效的改进。然而,在某些情况下,这些结构变化给纯化的基于抗体的疗法的制造引入了另外的挑战。
8.因此,非常需要用于制造基于抗体的治疗性化合物的新工艺。
技术实现要素:
9.在一个方面,本公开包括组合物,其包含完整的可活化抗体及其经修剪的变体,其中所述经修剪的变体以减少的量存在。在一些方面,其经修剪的变体包含抗原结合结构域(ab)和可切割部分(cm)的至少一部分。在一些方面,经修剪的变体缺少来自至少一个前结构域的掩蔽部分(mm)。
10.在一些方面,所述组合物包含如通过还原性sds-cge所测量的至少约90%的完整的可活化抗体、如通过还原性sds-cge所确定的小于约10%的经修剪的变体、如通过se-hplc所确定的小于约5%的高分子量物质(hmws)以及如通过相应的hcp elisa所确定的小
于约150ppm的宿主细胞蛋白(hcp)。在一些方面,所述组合物包含大于95%的完整可活化抗体和0.05%至5%的经修剪的变体。在一些方面,所述组合物包含大于90%的完整可活化抗体、0.05%至5%的经修剪的变体、小于150ppm的宿主细胞蛋白(hcp)和/或小于5%的hmws。在一些方面,所述组合物包含大于96%的完整可活化抗体、0.05%至4%的经修剪的变体、小于150ppm的hcp和/或小于5%的hmws。在一些方面,所述组合物包含大于97%的完整可活化抗体、0.05%至3%的经修剪的变体、小于150ppm的宿主细胞蛋白(hcp)和/或小于5%的hmws。在一些方面,所述组合物包含大于98%的完整可活化抗体、0.05%至2%的经修剪的变体、小于150ppm的宿主细胞蛋白(hcp)和/或小于5%的hmws。在一些方面,所述组合物包含大于99%的完整可活化抗体、0.05%至1%的经修剪的变体、小于150ppm的宿主细胞蛋白(hcp)和/或小于5%的hmws。在一些方面,本公开包括装有所述组合物的容器、小瓶、注射器或注射器装置。
11.在一个方面,本公开包括用于生产组合物的工艺,所述组合物包含:(a)大于95%的完整可活化抗体,其包含mm、cm和ab;(b)0.05%至5%的其经修剪的变体,所述方法包括将包含水、(a)、(b)和第一盐的水性原料加载到色谱柱上,其中所述色谱柱包括固定相,所述固定相包括支持基质和与其结合的疏水性配体,并用包含水和第二盐的洗脱液洗脱色谱柱以获得组合物。在一个方面,所述工艺包括将工艺流中的经修剪的变体的量减少75%至90%。在一个方面,所述工艺包括将工艺流中的hcp的量减少75%至90%。在一个方面,所述工艺包括将工艺流中的hmws的量减少75%至90%。在一个方面,所述工艺包括将工艺流中的经修剪的变体、hcp和hmws的量减少70%至95%。
12.在一个方面,本公开包括将完整的可活化抗体与其经修剪的变体分离的方法,所述其经修剪的变体与完整的可活化抗体的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一的氨基酸序列,所述方法(i)将包含水、完整的可活化抗体、其经修剪的变体和第一盐的水性原料加载到色谱柱,其中所述色谱柱包括固定相,所述固定相包含支持基质和与其结合的疏水性配体,和(ii)用包含水和第二盐的洗脱液洗脱色谱柱以获得组合物,其中所述工艺流中所述经修剪的变体的量减少至少70%。在一些实施方案中,所述工艺流中所述经修剪的变体的量减少至少75%、80%、85%或90%。
13.在一个方面,本公开包括组合物和用于制备组合物的工艺,所述组合物具有至少90重量%、91重量%、92重量%、93重量%、94重量%、95重量%、96重量%、97重量%、98重量%或99重量%的完整的可活化抗体形式的组合物中总蛋白,并且0.1重量%至10重量%的其聚集的和经修剪的变体形式的总蛋白。
14.在一个方面,本公开包括用于生产药物组合物的方法,所述药物组合物包含完整的可活化抗体和小于5%的其经修剪的变体、小于5%的其聚集体、小于150ppm的hcp或它们的组合,所述方法包括将包含水、(a)、(b)和第一盐的水性原料加载到色谱柱上,其中所述色谱柱包括固定相,所述固定相包含支持基质和与其结合的疏水性配体,并用包含水和第二盐的洗脱液洗脱色谱柱以获得所述组合物。
15.在一些方面,本公开包括将本文公开的组合物施用于有需要的受试者,例如,患有癌症、炎性疾病、自身免疫性疾病或其组合的患者。在一些方面,本公开包括施用含亚毒性剂量的可活化抗体的经修剪的变体和一定剂量的在疾病微环境中被活化的可活化抗体的本文公开的组合物。在一些方面,本公开包括通过施用本公开的组合物来扩大治疗受试者
的治疗窗。
16.在一个方面,本发明提供用于生产完整的可活化抗体的纯化组合物的工艺,所述工艺包括:
17.(a)将包含水、完整的可活化抗体、经修剪的杂质和第一盐的水性原料加载到色谱柱上,
18.其中所述色谱柱包括固定相,所述固定相包含支持基质和与其结合的配体,
19.其中所述配体包含疏水取代基,并且
20.其中所述完整的可活化抗体包含(i)对第一生物靶标具有特异性结合亲和力的至少第一抗原结合结构域(ab),和(ii)第一前结构域,
21.其中所述至少第一ab包含第一抗体轻链可变结构域(vl)和第一抗体重链可变结构域(vh),
22.其中所述第一前结构域包含第一掩蔽部分(mm)和第一可切割部分(cm),并且
23.其中所述第一ab与所述第一前结构域偶联;和
24.(b)用包含水和第二盐的洗脱液洗脱所述色谱柱以产生包含纯化组合物的洗脱物,所述纯化组合物包含完整的可活化抗体,
25.其中所述洗脱物基本上不含所述经修剪的杂质。
26.在另一个方面,所述水性原料还包含其他杂质,诸如,例如宿主细胞蛋白(hcp)和/或高分子量物质(hmws),其中这些杂质的量在洗脱物中显著减少。
27.在其他方面,本发明提供不含或含有极低残留量的经修剪的杂质的纯化的完整的可活化抗体组合物。
28.在又其他方面,本发明提供不含或含有极低残留量的经修剪的杂质、宿主细胞蛋白(hcp)和高分子量物质(hmws)的纯化的完整的可活化抗体组合物。
29.在另一个方面,本公开包括用于通过以下在组合物生产过程中确定或监测可活化抗体及其经修剪的变体的相对量的方法:对包含可活化抗体群体和其经修剪的变体群体的样品组合物进行凝胶毛细管电泳程序;在凝胶毛细管电泳程序中将可活化抗体群体与其经修剪的变体群体分离;以及通过确定对应于完整的编码前结构域的多肽的峰面积和对应于一种或多种其经修剪的编码前结构域的多肽的峰面积来量化可活化抗体群体及其经修剪的变体群体的相对量。
附图说明
30.图1a描绘从可活化抗pdl1抗体的生物收获物获得的样品的质量分光光度法分析结果。结果显示对应于相应的单臂经修剪的杂质的预期分子量的单峰。在完全经修剪的杂质的预期分子量处没有观察到峰。
31.图1b描绘从可活化抗pd1抗体的生物收获物获得的样品的质量分光光度法分析结果。结果显示对应于相应的单臂经修剪的杂质的预期分子量的单峰。在完全经修剪的杂质的预期分子量处没有观察到峰。
32.图1c描绘从可活化抗cd166抗体的生物收获物获得的样品的质量分光光度法分析结果。结果显示对应于相应的单臂经修剪的杂质的预期分子量的单峰。在完全经修剪的杂质的预期分子量处没有观察到峰。
33.图2a示意性地描绘完整的可活化抗体及其经修剪的变体的结构。
34.图2b示意性地描绘用本公开的方法处理之前可能存在于组合物中的完整的可活化抗体及其经修剪的变体的混合物。
35.图3a示意性地描绘:(1)将图2b的混合物施用于受试者的细胞;(2)施用后完整的可活化抗体及其经修剪的变体与所述受试者的细胞的结合;(3)来自所述组合物的经修剪的变体与健康组织的结合;(4)完整的可活化抗体在患病(例如,肿瘤)组织的环境中的活化以及活化的抗体与其的结合。
36.图3b示意性地描绘:(1)当施用于受试者时用本公开的方法处理后存在于组合物中的完整的可活化抗体的结合;(2)施用的完整的可活化抗体缺乏与健康组织的结合;和(3)完整的可活化抗体在仅患病(例如,肿瘤)组织的环境中的活化以及活化的抗体与其结合。
37.图4a描绘在通过蛋白a色谱纯化后对包含抗cd-166可活化抗体的样品进行的还原性十二烷基硫酸钠(sds)毛细管凝胶电泳(sds-cge)的结果。
38.图4b描绘对包含抗cd-166可活化抗体的样品进行阴离子离子交换色谱(阴离子iex)之后对洗脱物样品进行的还原性sds-cge的结果。阴离子iex步骤的水性原料包括蛋白a色谱步骤的洗脱物,其分析描绘于图4a中。
39.图4c描绘通过疏水相互作用色谱(hic)纯化后对包含抗cd-166可活化抗体的样品进行的还原性sds毛细管凝胶电泳(sds-cge)的结果。hic步骤的水性原料包括阴离子iex步骤的洗脱物,其分析描绘于图4b中。
40.图5描绘如实施例2中所述用于纯化包含完整可活化抗cd166抗体和相应的经修剪的杂质的水性原料的阳离子交换色谱的评估。通过将第一缓冲液(25mm naoac,500mm nacl,ph 5.0(80cv梯度))混合到第二缓冲液(25mm naoac,25mm nacl,ph 5.0)中用nacl梯度洗脱该柱。线“a”代表在280nm处的吸光度,线“b”代表在254nm处的吸光度,线“c”代表以ms/cm为单位的电导率,以及线“d”代表混合到第二缓冲液中的第一缓冲液的百分比。左侧y轴表示吸光度(mau),右侧y轴表示电导率(ms/cm),并且x轴表示流分(ml)。
具体实施方式
41.由于广泛的靶点表达引起的毒性限制了单克隆抗体疗法的治疗效果。为了解决这个问题,已经生产了重组产生的可活化抗体,其包含抗原结合结构域(ab)、可切割部分(cm)和能够抑制所述ab与其靶标特异性结合的掩蔽部分(mm)。此类可活化抗体仅在通过暴露于某些蛋白酶,特别是在局限性疾病环境(例如,肿瘤微环境)中被上调的蛋白酶而活化后,才在与生物靶标的结合特异性方面表现与抗体类似。
42.本发明人现已发现,由于在制造工艺过程中存在于宿主细胞中的蛋白酶以及蛋白酶底物的相对不稳定性,通常发现含有可活化抗体的组合物含有显著比例的缺乏mm的经修剪的变体,并且因此是游离的,可无差别结合至健康细胞上的靶标,从而可能导致与单克隆抗体相关的剂量依赖性毒性和副作用。治疗剂量中经修剪的变体的存在可能因经修剪的变体被扣押于正常组织中而具有降低体循环中可用于抵达靶组织(例如,癌性组织)的完整的可活化抗体的剂量的作用。除了存在经修剪的变体之外,本发明人还观察到某些含有可活化抗体的组合物由于聚集还含有显著比例的高分子量物质,这可能会降低功效并增加免疫
原性。特别地,本发明人现已发现,除了由切割引起的截短之外,经修剪的变体与可活化抗体亲本在大小上相似且氨基酸序列是同一的。由于经修剪的变体和完整的可活化抗体在大小和结构以及物理化学性质方面的相似性,因此以高收率将经修剪的变体与完整的可活化抗体亲本分离以获得具有高纯度(例如,高百分比的完整、非聚集的可活化抗体)的组合物具有挑战性。如下所述,本发明人已发现用于纯化可活化抗体组合物以选择性地去除经修剪的变体的方法,产生包含高水平的完整的可活化抗体而经修剪的变体水平低或不可检测的组合物。
43.定义
44.术语“可活化抗体”、“蛋白酶可活化抗体”和“完整的可活化抗体”在本文中可互换用于指代重组产生的“经掩蔽的”结合化合物,其被设计为仅在其通过暴露于某些蛋白酶而被活化后才在与生物靶标的结合特异性方面表现与抗体类似。在结构上,可活化抗体包含:(1)抗原结合结构域(ab),其在未被掩蔽时可特异性地结合生物靶标;和(2)与ab偶联的前结构域(通过肽键合),其包含掩蔽部分(mm)和可切割部分(cm)或由mm和cm组成。
45.术语“氨基酸阴离子”在本文中是指氨基酸的阴离子形式。阴离子部分可以例如是去质子化的α-羧基或r-基团羧基(例如,天冬氨酸、谷氨酸等中的r-基团羧基部分)等。
46.术语“氨基酸阳离子”在本文中是指氨基酸的阳离子形式。阳离子部分可以例如是质子化的α-胺或r-基团胺(例如,精氨酸(即,胍基部分)、色氨酸、天冬酰胺、谷氨酰胺、赖氨酸、组氨酸等中的r基团胺部分)等。
47.术语“氨基酸盐”在本文中是指氨基酸的盐。说明性的氨基酸盐包括,例如,精氨酸盐酸盐、赖氨酸盐酸盐等。
48.术语“抗原结合结构域”和“ab”在本文中可互换用于指代对生物靶标具有特异性结合亲和力的结合结构域,其由一种或多种编码抗体轻链可变结构域(vl)和抗体重链可变结构域(vh)的多肽形成。
49.如本文所用,术语“生物靶标”是指哺乳动物物种天然的蛋白质。
50.如本文所用,术语“前结构域”在本文是指具有至少编码掩蔽部分(mm)和可切割部分(cm)的氨基酸序列的肽。前结构域可以包含其他序列元件,诸如,例如间隔区、一个或多个接头(例如,位于mm和cm之间和/或mm和vl之间和/或mm和vh之间和/或cm和vl之间和/或cm和vh之间等)等。
51.如本文所用,术语“掩蔽部分”和“mm”在本文中可互换用于指代当位于ab的近端时干扰ab与生物靶标结合的肽。
52.术语“可切割部分”和“cm”在本文中可互换用于指代包含至少一种蛋白酶的底物的肽。
53.术语“经修剪的杂质”和“经修剪的变体”在本文中可互换用于指代在蛋白酶介导的完整的可活化抗体切割后产生的分子。经修剪的杂质包含相应的可活化抗体的ab,但缺少mm的全部或一部分(因此缺少前结构域的全部或一部分,例如缺少至少一个cm的全部或一部分并且缺少对应mm的全部)。术语“经修剪的杂质”和“经修剪的变体”可以包括“单臂经修剪的”和“完全经修剪的”物质。
54.如本文所用,术语“特异性结合亲和力”是指ab与特定生物靶标的优先结合。
55.术语“单臂经修剪的杂质”或“单臂经修剪的物质”在本文中可互换用于指代其中
相应完整的可活化抗体的仅一个前结构域的全部或一部分缺失的经修剪的杂质。术语“单臂经修剪的”与可活化抗体的变体结合使用,其中所述完整的可活化抗体包含两个或更多个抗原结合结构域(ab)和两个或更多个前结构域。
56.术语“单臂经修剪的杂质”或“单臂经修剪的物质”在本文中可互换用于指代其中相应完整可活化抗体的每个前结构域的全部或一部分缺失的经修剪的杂质。
57.术语“肽”、“多肽”和“蛋白质”在本文中可互换用于指代包含天然存在的或非天然存在的氨基酸残基或氨基酸类似物的聚合物或低聚物。
58.术语“经修剪的杂质百分比”、“经修剪的杂质百分比”、“经修剪的编码前结构域的多肽百分比”和“经修剪的编码前结构域的多肽%”在本文中可互换用于指代存在于组合物中的经修剪的编码前结构域的多肽的相对量,以经修剪的和完整的编码前结构域的多肽的总量的百分比计,其中数量是通过还原性sds-毛细管凝胶电泳(“还原性sds-cge”)来确定的。还原性sds-cge测定在实施例1中进行了说明。经修剪的杂质百分比是基于经修剪的编码前结构域的多肽和完整的编码前结构域的多肽的峰面积相对百分比计算如下:
[0059][0060]
其中:
[0061][0062][0063]
对应于检测到的所有物质的总峰面积是指sds-cge色谱仪中所有峰面积的总和。
[0064]
术语“完整的可活化抗体百分比”、“完整的可活化抗体%”、“完整的编码前结构域的多肽百分比”和“完整的编码前结构域的多肽%”在本文中可互换用于指代存在于组合物中的完整的编码前结构域的多肽的相对量,以经修剪的和完整的编码前结构域的多肽的总量的百分比计,其中数量是通过还原性sds-cge来确定的,诸如,例如实施例1中说明的还原性sds-cge。完整的可活化抗体百分比是基于经修剪的编码前结构域的多肽和完整的编码前结构域的多肽的峰面积相对百分比计算如下:
[0065][0066]
其中:
[0067][0068][0069]
术语“编码前结构域的多肽”是指可活化抗体中的多肽,其包含编码前结构域的氨基酸序列。编码前结构域的多肽可以包含一种或多种编码除前结构域之外的可活化抗体的其他元件的氨基酸序列。例如,如果前结构域位于编码抗体轻链的多肽内,则编码前结构域的多肽也至少编码vl。同样,在其他实施方案中,如果前结构域位于编码抗体重链的多肽
内,则编码前结构域的多肽也至少编码vh。类似地,如果前结构域位于编码scfv链的多肽内,则编码前结构域的多肽还进一步至少编码vl和vh。
[0070]
术语“经修剪的编码前结构域的多肽”在本文中是指在修剪所述前结构域后产生的截短的编码前结构域的多肽。
[0071]
术语“完整的编码前结构域的多肽”在本文中是指未被修剪并且其含有完整的前结构域的编码前结构域的多肽。
[0072]
术语“基本上耗尽”在本文中用于指代不存在可检测的经修剪的杂质或如与存在于水性原料中的经修剪的杂质水平相比经修剪的杂质的相对水平已减少至少20%的洗脱物组合物,其中减少百分比计算如下:
[0073][0074]
其中“经修剪的杂质%”与上面定义的相同。
[0075]
术语“基本上不含”在本文中与经修剪的变体和经修剪的杂质一起用于指代不存在可检测的经修剪的杂质或存在经修剪的杂质的组合物,其中所述经修剪的杂质百分比如通过sds-cge所确定小于5%,例如,4%、3%、2%、1%、0.5%、0.1%、0.05%或介于0和5%之间的任何数值或范围。
[0076]
术语“结合的相应的经修剪的杂质”和“结合的经修剪的杂质”在本文中可互换用于指代保留在色谱柱中的经修剪的杂质。
[0077]
术语“间隔区”在本文中是指在前结构域的游离末端整合的氨基酸残基或肽。在一些方面,间隔区(或“首部(header)”)可以包含谷氨酰胺(q)残基。在一些方面,间隔区中的残基使氨肽酶和/或外肽酶作用最小化以防止n末端氨基酸的切割。
[0078]
术语“接头”在本文中是指氨基酸残基或肽,其作用是提供可活化抗体的mm、cm和/或ab元件之间的其他的物理分离。
[0079]
如本文所用,术语“高分子量物质”和“hmws”在本文中可互换用于指代有效分子量大于单体的完整的可活化抗体分子量的组合物杂质(例如,聚集体),如通过尺寸排阻高效液相色谱法(se-hplc,诸如实施例1中描述的测定)所确定。
[0080]
术语“有效分子量”是指通过se-hplc测定(诸如实施例1中描述的测定)确定的分子量。
[0081]
如本文所用,术语“等度(的)”是指在洗脱步骤期间使用具有基本上恒定或固定组成的洗脱液。
[0082]
如本文所用,术语“疏水相互作用色谱固定相”或“hic固定相”可互换地指代一类具有被设计为通过专门的疏水相互作用与化合物相互作用的配体的固定相。
[0083]
术语“多模式色谱固定相”或“mmc固定相”在本文中可互换地指代一种固定相,其具有通过疏水相互作用与化合物相互作用的配体,以及一种或多种不是疏水相互作用的额外类型的相互作用(例如,静电(通过带电的配体取代基)、氢键、亲硫性等)。
[0084]
如本文所用,术语“宿主细胞蛋白”和“hcp”在本文中可互换用于指代由其表达完整的可活化抗体的宿主细胞天然的蛋白。
[0085]
如本文所用,术语“总蛋白产率”是指基于水性原料中的总蛋白质在色谱洗脱物中回收的总蛋白质的百分比,并且如uv光谱测定中通过280nm波长处的吸光度测量。
[0086]
如本文所用,术语“介入单元操作”是指发生在细胞培养工艺步骤和疏水色谱工艺步骤之间的工艺步骤。
[0087]
术语“散装中间产物组合物”是指介入单元操作的产品的组合物。
[0088]
如本文所用,术语“生物收获组合物”是指源自产生包含所关注的可活化抗体的组合物的细胞培养步骤的组合物。
[0089]
术语“连续(的)”当结合描述单元操作之间的关系使用时,在本文中用于指代两个或更多个在时间和顺序方面,或者分批、半连续或连续,第一、然后第二,依此类推按顺序执行的单元操作。
[0090]
如本文所用,术语“缀合试剂”是指缀合部分的反应形式,其包含与反应性接头共价结合的缀合部分。
[0091]
如本文所用,术语“基本上对应”当结合两个氨基酸序列使用时,是指当最佳比对时至少约90%的同一性水平。
[0092]
当两个多肽序列是使用定义的参数(即定义的氨基酸取代矩阵、空位存在罚分(也称为空位开放罚分)和空位延伸罚分)进行比对以达到那对序列可能的最高相似性分数时,它们被“最佳比对”。blosum62矩阵(henikoff和henikoff(1992)proc.natl.acad.sci.usa 89(22):10915-10919)通常用作多肽序列比对算法(诸如blastp)中的默认评分取代矩阵。对所比对序列之一中单个氨基酸空位的引入施加空位存在罚分,并对空位中的每个残基位置施加空位延伸罚分。除非另有说明,否则本文采用的比对参数为:blossum62评分矩阵、空位存在罚分-11和空位延伸罚分-1。比对分数由比对开始和结束处每个序列的氨基酸位置(例如,比对窗口)定义,并且任选地通过在一个或两个序列中插入一个或多个空位以达到可能的最高相似度分数。
[0093]
关于本文提供的任何和所有数值范围,所述范围旨在包括限定该范围的数值界限。
[0094]
本发明的方法和组合物
[0095]
本发明涉及基本上不含经修剪的杂质的完整蛋白酶可活化抗体的纯化组合物的生产以及生产此类组合物的工艺。制备纯化组合物的工艺在去除其他杂质方面也是有效的。在结构上,可活化抗体包含:(1)抗原结合结构域(ab),其在未被掩蔽时可特异性地结合生物靶标;和(2)与ab偶联的前结构域,其包含掩蔽部分(mm)和可切割部分(cm)。cm相对于mm和ab组分定位,使得cm的切割导致mm从其邻近ab的位置释放。因此,切割通常导致产生能够特异性地结合生物靶标的经活化的抗体。通常,可活化抗体是同二聚体,所述同二聚体包含两个相同的ab、两个相同的cm和两个相同的mm。在此类情况下,可活化抗体的经修剪的变体可以是单臂经修剪的变体,其中两个cm中只有一个被切割,因此经修剪的变体包含一个完整的cm和一个完整的mm,但缺少一个cm的一部分和一个mm的全部。
[0096]
可活化抗体可被设计成通过在cm中掺入而在患病组织中选择性活化,cm是在患病组织中更普遍地发现处于活性状态的蛋白酶的底物。因此,可活化抗体有可能减轻当单克隆抗体结合广泛分布在疾病部位之外的生物靶标时可能引起的靶标介导的毒性。参见desnoyers等人,science translational medicine(16october 2013)5(207):207ra144。可活化抗体描述于多个公布中,包括例如wo 2009/025846、wo 2010/096838、wo 2010/081173、wo 2013/163631、wo 2013/192546、wo 2013/192550、wo 2014/026136、wo 2014/
052462、wo 2014/107599、wo 2014/197612、wo 2015/013671、wo 2015/048329、wo 2015/066279、wo 2015/116933、wo 2016/014974、wo 2016/118629、wo 2016/149201、wo 2016/179285、wo 2016/179257、wo 2016/179335、wo 2017/011580、pct/us2017/059740、美国临时申请序列号62/469,429、62/572,467和62/613,358、wo 2012/025525、wo 2017/025698、wo 2016/046778、wo 2016/179003、wo 2016/182064、wo 2017/156178、wo 2017/143094、wo 2017/162587、wo 2013/128194,这些中的每一个均通过引用方式以其整体并入本文。适用于本发明的工艺和组合物的可活化抗体的进一步说明性实例在下文更详细地描述。
[0097]
尽管是非常需要的产品,但可活化抗体的纯化组合物的制造因其可活化的性质而变得更具挑战性。对可活化抗体生物收获物的分析揭示了经修剪的杂质(仅与可活化抗体相关的化合物)的存在。由于脱靶毒性和降低的功效的潜在影响,因此不希望在组合物或药物产品中具有大量的经修剪的杂质,即可以自由结合其生物靶标的“经活化的”可活化抗体。由于可能影响产品的安全性,因此不希望药物产品中存在经修剪的变体。
[0098]
由于所需产物和经修剪的杂质之间在诸如分子大小、结构、氨基酸组成等性质方面的差异相对较小,而且它们的氨基酸序列在其大多数的各自结构中是100%同一的,因此使得从完整的可活化抗体组合物中去除经修剪的杂质具有挑战性。在结构上,完整的可活化抗体和相应的经修剪的杂质之间的区别在于经修剪的杂质中至少一种前结构域的全部或一部分不存在。在一些实施方案中,掩蔽部分是相对短的肽序列,例如长度少于50个氨基酸,少于40、30、20、15、14、13、12、11或10个氨基酸,并且经修剪的物质和完整的可活化抗体可能相差大约掩蔽部分中的氨基酸数量。此外,发明人已经发现单臂经修剪的变体是主要的经修剪的变体,使得完整的可活化抗体和经修剪的变体之间的全部差异是不存在单个前结构域的一部分,例如经修剪的变体与完整的可活化抗体不同之处仅在于缺少mm和cm的一部分。因此,完整的可活化抗体及其经修剪的变体的大小和理化性质是相似的,使得分子的分离变得困难。
[0099]
包含具有两条轻链(各编码前结构域)和两条重链的可活化抗体的生物收获物组合物的表征揭示了所有或几乎所有的经修剪的杂质似乎是单臂经修剪的杂质(即,未完全修剪的杂质),如图1a至图1c中三种不同的可活化抗体组合物的质谱图所示。因此,当可活化抗体具有多于一个编码前结构域的多肽时,完整的可活化抗体和经修剪的杂质的分离会由于主要的经修剪的物质、单臂修剪的杂质在结构上与相应的完整抗体的结构非常相似的事实而加剧。在一些方面,经修剪的杂质的分子量是完整的可活化抗体的分子量的约93%、94%、95%、96%、97%、98%或99%。在一些方面,经修剪的编码前结构域的多肽的分子量为完整的编码前结构域的多肽分子量的约93%、94%、95%、96%、97%、98%或99%。在一些方面,经修剪的杂质与完整的可活化抗体的氨基酸序列是约93%、94%、95%、96%、97%、98%或99%同一的。
[0100]
在一些方面,经修剪的变体可以包括前结构域的1、2、3、4或更多个氨基酸残基。在一些方面,经修剪的变体可以包括cm的1、2、3、4或更多个氨基酸残基。在一些方面,经修剪的变体可以包括接头的1、2、3、4或更多个氨基酸残基。在一些方面,经修剪的变体可以包括接头和cm的1、2、3、4或更多个氨基酸残基。
[0101]
尽管存在这一挑战,但还是发现了一种工艺,其在以相对较高的收率将完整的可活化抗体与相应的经修剪的杂质分离时是非常有效的。生产完整的可活化抗体的纯化组合
物的工艺包括:
[0102]
(a)将包含水、完整的可活化抗体、经修剪的杂质和第一盐的水性原料加载到色谱柱上,
[0103]
其中所述色谱柱包括固定相,所述固定相包含支持基质和与其结合的配体,
[0104]
其中所述配体包含疏水取代基,并且
[0105]
其中所述完整的可活化抗体包含(i)对第一生物靶标具有特异性结合亲和力的至少第一抗原结合结构域(ab),和(ii)第一前结构域,
[0106]
其中所述至少第一ab包含第一抗体轻链可变结构域(vl)和第一抗体重链可变结构域(vh),
[0107]
其中所述第一前结构域包含第一掩蔽部分(mm)和第一可切割部分(cm),并且
[0108]
其中所述第一ab与所述第一前结构域偶联;和
[0109]
(b)用包含水和第二盐的洗脱液洗脱所述色谱柱以产生包含纯化组合物的洗脱物,所述纯化组合物包含完整的可活化抗体,
[0110]
其中所述洗脱物基本上不含所述经修剪的杂质。
[0111]
步骤(a)和(b)在本文中统称为“疏水色谱工艺”。洗脱物以及因此纯化的组合物都基本上耗尽了经修剪的杂质。在来自色谱柱的洗脱产物中观察到完整的可活化抗体和相应的经修剪的杂质的不同且分离的峰。尽管完整杂质和经修剪的杂质的结构相似,但这些化合物很容易在至少部分依赖疏水相互作用的色谱柱上分离。产生的富含完整的可活化抗体的洗脱物基本上耗尽了相应的经修剪的杂质。该工艺是一种易于扩展和高生产性的工艺,用于以高总蛋白产量生成高纯度的完整的可活化抗体的组合物。
[0112]
已发现完整的可活化抗体在相应的经修剪的杂质之前以单独的峰洗脱,并且也在其他杂质诸如例如高分子量物质(“hmws”)和宿主细胞蛋白(hcp)之前洗脱。如实施例中所证明的,在包含完整的可活化抗体和具有不同氨基酸序列和对不同生物靶标具有特异性的相应经修剪的杂质的多种水性原料组成中观察到这种现象。鉴于达到的分离度和峰分布,在一些实施方案中,洗脱步骤(b)是在等度条件下进行的。
[0113]
在许多实施方案中,在进行步骤(b)之后,所述工艺还包括柱清洗步骤,其包括用清洗剂清洗柱。通常在这些实施方案中,本发明的工艺不包括在柱清洗步骤之前用第二洗脱液从色谱柱洗脱结合的相应经修剪的杂质和/或其他杂质(如果存在于水性原料中的话)(诸如,例如hmws、hcp等)的步骤。由于在洗脱完整的可活化抗体后杂质基本上保留在柱上,因此可能需要在不单独洗脱杂质的情况下进行清洁步骤,从而进一步提高本发明工艺的高生产性质。合适的清洁剂包括本领域已知的多种清洁剂中的任一种,包括例如酸水溶液;碱水溶液、有机溶剂、混合有机溶剂(例如,包括两种或更多种不同的有机溶剂)、一种或多种有机溶剂的水性混合物、前述任一种的混合物等。说明性清洁剂包括氢氧化钠水溶液、乙醇、异丙醇、乙二醇、盐酸胍溶液、酸性胃蛋白酶溶液、月桂酰肌氨酸钠溶液等,以及它们中的两种或更多种的任何组合。
[0114]
关于本发明工艺中使用的固定相,可以使用多种已知的支持基质材料中的任何一种。合适的说明性支持基质材料包括亲水性聚合物,诸如,例如碳水化合物(诸如,例如琼脂糖(例如,sepharose品牌(ge healthcare lifesciences)、capto
tm impres(ge healthcare lifesciences)、交联纤维素(例如,cellufine
tm hic介质(amsbio)等)、基于聚甲基丙烯酸
酯的树脂(例如,macro-hic树脂(bio-rad,inc.)等)、基于聚苯乙烯的树脂(例如,bio-beads
tm sm-2树脂(bio-rad,inc.)等)、二氧化硅、合成共聚物,以及任何其他本领域已知的色谱支持基质材料。支持基质可以是多种形式中的任一种,包括,例如颗粒形式、珠形式、膜形式等。
[0115]
在本发明的工艺中可以使用具有疏水取代基的多种已知配体物质中的任何一种。示例性的疏水性取代基包括,例如,直链烷基取代基(包括,例如,甲基、乙基、正丙基、正丁基、正戊基、正己基、正庚基、正辛基等)、支化的烷基取代基(诸如,例如异丙基、叔丁基等)、芳基取代基(诸如,例如苯基、烷基取代的苯基等)等,以及两种或更多种类型的疏水性取代基的任何组合。在一些实施方案中,所述疏水性取代基包括c4至c
10
烷基取代基(即,c4、c5、c6、c7、c8、c9或c
10
取代基)和/或苯基取代基。通常,c4至c
10
烷基取代基选自由丁基取代基(即,c4)或辛基取代基(即,c8)组成的组。所述疏水性取代基可以通过多种键联(包括,例如o-醚、s-醚等)中的任何一种与支持基质偶联。适用于本发明实践的示例性配体(包括-o-接头)包括-o-ph、-s-(ch2)
3-ch3(-s-丁基)、-o-(ch2)
3-ch3(o-丁基)、-o-(ch2)
7-ch3(o-辛基)、-o-ch
2-choh-ch
2-oh、-o-ch-(ch3)2等。在某些实施方案中,如下文更详细所描述,所述配体可以还包含另外的取代基,其通过疏水性以外的相互作用(诸如,例如静电、氢键合、亲硫性等)促进分离。
[0116]
在一些实施方案中,所述固定相是疏水相互作用色谱(hic)固定相,其仅通过疏水相互作用促进分离。示例性的hic固定相配体可包含上文所述的任何疏水性取代基。在某些实施方案中,所述配体包含选自由苯基、丁基、辛基和异丙基组成的组的取代基。hic固定相很容易商购获得。在具体实施方案中,所述固定相包含选自由-o-苯基、-s-(ch2)
3-ch3(即,-s-丁基)、-o-(ch2)
3-ch3(即,-o-丁基)、-o-(ch2)
7-ch3(即,-o-辛基)、-o-ch
2-choh-ch
2-oh、-o-ch-(ch3)2等,以及两种或更多种不同配体的任何组合。
[0117]
在其他实施方案中,所述固定相是多模式色谱(mmc)固定相。在这些实施方案中,所述配体包含一个或多个疏水性取代基,以及至少一个其他的取代基,其基于疏水性以外的相互作用(诸如,例如静电、氢键合、亲硫性等)促进分离。适用于本发明实践的说明性mmc固定相包含具有例如疏水性取代基和一个或多个选自由硫化物取代基、羧基取代基和胺取代基组成的组的取代基的配体。通常,羧基取代基和/或胺取代基是在所采用的工艺条件下带电的。适用于本发明实践的mmc固定相包括具有选自由n-苄基甲基乙醇胺、n-苄基甲基乙醇胺、n-苯甲酰基-高半胱氨酸、n-苯甲酰基-高半胱氨酸、辛胺等组成的组的配体的固定相。
[0118]
固定配体中疏水性取代基的存在似乎对促进完整的可活化抗体与经修剪的杂质的分离具有显著影响。使用如实施例3(使用hic固定相)、实施例4(使用hic固定相)和实施例5(使用mmc固定相)中所示的疏水色谱工艺,可实现完整的可活化抗体与经修剪的杂质的分离至较高程度。相比之下,如实施例2中所述,使用阳离子交换色谱法无法实现完整的可活化抗体与经修剪的杂质的分离。同样,阴离子色谱法的使用似乎对将完整的可活化抗体与经修剪的杂质分离没有影响,如实施例3至实施例5中所述。
[0119]
所述疏水色谱工艺是通过将包含水、完整的可活化抗体、经修剪的杂质和第一盐的水性原料加载到色谱柱上来启动。在一些实施方案中,所述水性原料可以包含另外的组分,包括另外的杂质,诸如,例如细胞培养工艺步骤的一种或多种产物(例如,宿主细胞蛋
白、dna等)、一种或多种来自上游纯化单元操作的残留化合物(例如,蛋白a、蛋白g等)、hmws(例如,存在于水性原料中的单体可活化抗体物质的聚集体等)、低分子量物质(lmws)等。
[0120]
适合用作水性原料中的第一盐的盐可以是任何促进完整的可活化抗体和经修剪的杂质与柱的固定相结合的盐。水性原料的合适的第一盐和第一盐浓度以及洗脱液的第二盐和第二盐浓度可以通过使用盐浓度梯度进行一系列测试运行并确定影响完整的可活化抗体与固定相结合同时允许杂质洗涤通过固定相或保持与固定相结合的盐和盐浓度,并确定影响所需的完整的可活化抗体从固定相上选择性洗脱的第二盐和盐浓度。在一些实施方案中,所述第一盐和所述第二盐是相同的盐。在其他实施方案中,所述第一盐和所述第二盐是不同的盐。所述第一盐和/或第二盐也可以各自独立地包含盐物质的混合物。
[0121]
说明性的第一盐和第二盐各自独立地包含选自由po
43-、so
42-、oh-、hpo
42-、ch3coo-(乙酸根离子)、柠檬酸根离子、f-、cl-、br-、h2po
4-、i-、no
3-、clo
4-、scn-、氨基酸阴离子等组成的组的阴离子。在一些实施方案中,第一盐和第二盐可以各自独立地包含选自由n(ch3)
4+
、nh
4+
、cs
+
、rb
+
、k
+
、na
+
、h
+
、ca
+
、mg
2+
、al
3+
、氨基酸阳离子等组成的组的阳离子。所述第一盐可以恰好在疏水色谱工艺步骤之前被引入到包含完整的可活化抗体和相应的经修剪的杂质的水性组合物中,或者它可以结合疏水色谱工艺步骤上游的工艺步骤(例如,在如下所述的干预单元操作中)被引入。在该后一种情况下,可以任选地向组合物中添加另外的第一盐和/或可以将组合物稀释以适应柱的期望负载条件。
[0122]
当色谱柱包括hic固定相时,所述第一盐通常表现出亲液(盐析)行为。此类盐可以容易地例如从hofmeister系列离子中确定。参见,例如,tadeo等人,biophysical journal(2009)97:2595和hyde等人,org.process res.dev.(2017)21:1355,两者均通过引用方式以其整体并入本文。在一些实施方案中,所述第一盐和所述第二盐各自独立地包含比离液更强的亲液性的阴离子和/或阳离子。在这些实施方案的某些实施方案中,所述第一盐和所述第二盐各自独立地包含选自由po
43-、so
42-、oh-、hpo
42-、f-、ch3coo-(乙酸根离子)、柠檬酸根离子、氨基酸阴离子和cl-组成的组的阴离子。在其他实施方案中,所述第一盐和所述第二盐各自独立地包含选自由po
43-、so
42-和hpo
42-组成的组的阴离子。
[0123]
在一些实施方案中,所述第一盐和所述第二盐可以各自独立地包含选自由n(ch3)
4+
、nh
4+
、cs
+
、rb
+
、k
+
、na
+
、h
+
、ca
+
、mg
2+
、al
3+
、氨基酸阳离子组成的组的阳离子。在一些实施方案中,所述第一盐和所述第二盐各自独立地包含选自由nh
4+
、k
+
、na
+
、li
+
和mg
2+
组成的组的阳离子。在某些实施方案中,所述第一盐和所述第二盐各自独立地包含选自由nh
4+
、k
+
和na
+
组成的组的阳离子。在一些实施方案中,所述第一盐和所述第二盐各自独立地包含选自由nh
4+
、k
+
和na
+
组成的组的阳离子以及选自由po
43-、so
42-、oh-、hpo
42-、ch3coo-(乙酸根离子)、柠檬酸根离子、f-、cl-、br-、h2po
4-、i-、no
3-、clo
4-和scn-组成的组的阴离子。
[0124]
在一些实施方案中,所述第一盐和所述第二盐各自独立地选自由(nh4)2so4、na2so4、na3po4、k3po4、nacl、kcl和ch3coonh4组成的组。在某些实施方案中,所述第一盐和所述第二盐各自独立地选自由(nh4)2so4、na2so4、na3po4和k3po4组成的组。在其他实施方案中,所述第一盐和所述第二盐各自独立地选自由(nh4)2so4和na2so4组成的组。在某些实施方案中,所述第一盐和所述第二盐中的至少一者包含(nh4)2so4。在这些实施方案的一些实施方案中,所述第一盐和所述第二盐二者都包含(nh4)2so4。在其他实施方案中,所述第一盐和所述第二盐中的至少一者包含na2so4。在这些实施方案的一些实施方案中,所述第一盐和所述
第二盐二者都包含na2so4。
[0125]
当所述色谱柱包括hic固定相时,所述洗脱液的极性通常低于所述水性原料。在一些实施方案中,所述第一盐浓度(即,在水性原料中)大于所述第二盐浓度(即,在洗脱液中)。例如,所述第一盐浓度可以比所述第二盐浓度高约1.5倍、约2倍、约3倍、约4倍、约5倍、约6倍、约7倍、约8倍、约9倍或约10倍。例如,所述第一盐可以包括约1.5m的硫酸铵,并且所述第二盐可以包括约0.25m的硫酸铵(所述第一盐的浓度比所述第二盐的浓度高约6倍)。当希望使用不同于第一盐的第二盐时,所述第二盐如与所述第一盐相比通常具有较低的亲液强度。根据hofmeister离子强度系列,可以容易地确定具有更大或更小亲液强度的阳离子和阴离子。参见,例如,tadeo等人,biophysical journal(2009)97:2595和hyde等人,org.process res.dev.(2017)21:1355,两者均通过引用方式以其整体并入本文。在一些实施方案中,洗脱液还包含水混溶性有机溶剂,诸如,例如醇、二醇、多元醇等。
[0126]
当色谱柱包括mmc固定相时,所述第一盐通常表现出离液(盐溶)行为。如同与hic固定相结合使用的盐一样,适合与基于mmc的工艺结合使用的盐也可以容易地从hofmeister系列离子中确定。在一些实施方案中,所述第一盐和第二盐各自独立地包含比亲液更强的离液性的阴离子和/或阳离子。参见,例如,tadeo等人,biophysical journal(2009)97:2595和hyde等人,org.process res.dev.(2017)21:1355,两者均通过引用方式以其整体并入本文。在这些实施方案的某些实施方案中,所述第一盐和第二盐各自独立地包含选自由cl-、br-、h2po
4-、i-、no
3-、clo
4-、氨基酸阴离子和scn-组成的组的阴离子。在这些实施方案的一些实施方案中,所述第一盐和第二盐各自独立地包含选自由cl-、br-、h2po
4-、i-、no
3-、氨基酸阴离子和clo
4-以及scn-组成的组的阴离子。
[0127]
在一些实施方案中,所述第一盐和第二盐可以各自独立地包含选自由n(ch3)
4+
、nh
4+
、ba
+
、ca
2+
、mg
2+
、cs
+
、rb
+
、k
+
、na
+
和氨基酸阳离子组成的组的阳离子。在一些实施方案中,阳离子选自n(ch3)
4+
、nh
4+
、ca
2+
、mg
2+
、k
+
、na
+
和氨基酸阳离子。当使用氨基酸阳离子时,它通常是精氨酸阳离子(例如,具有带正电荷的胍基部分)。
[0128]
说明性的第一盐包括,例如,精氨酸氯化物或精氨酸盐酸盐、nacl等。当色谱柱包括mmc固定相时,所述第一盐和所述第二盐通常是相同的盐。在这些实施方案中,所述洗脱液通常包含的盐浓度大于水性原料中盐的浓度。例如,所述洗脱液(第二盐)盐浓度可以比原料(第一盐)盐浓度高约1.5倍、约2倍、约3倍、约4倍、约5倍、约6倍、约7倍、约8倍、约9倍或约10倍。当所述第一盐和第二盐不同时,通常选择如与第一盐相比离液强度更高的第二盐。根据hofmeister离子强度系列,可以容易地确定具有更大或更小离液强度的阳离子和阴离子。参见,例如,tadeo等人,biophysical journal(2009)97:2595和hyde等人,org.process res.dev.(2017)21:1355,两者均通过引用方式以其整体并入本文。在第一盐和第二盐不同的某些实施方案中,洗脱液包含第一盐和第二盐二者。在一些方面,所述第一盐可以包括约30mm的氯化钠作为唯一的盐,并且第二盐可以包括约30mm的氯化钠和约90mm的精氨酸盐酸盐。
[0129]
水性原料和洗脱液也可以各自独立地包含一种或多种缓冲剂。合适的缓冲剂包括一种或多种盐,诸如,例如上文作为合适的第一盐列出的那些盐中的任何一种;酸,诸如,例如2-(n-吗啉代)乙磺酸(mes)、(3-(n-吗啉代)丙磺酸)(mops)、(4-(2-羟乙基)-1-哌嗪乙磺酸)(hepes)、氯化氢等;和/或碱,诸如,例如氢氧化钠、氢氧化钾等。
[0130]
在某些实施方案中,经修剪的杂质由单臂经修剪的杂质组成。在一些其中完整的可活化抗体包含多个ab和相应地多个前结构域的实施方案中,所述经修剪的杂质可以包含经修剪的杂质物质的混合物。在这些实施方案的一些实施方案中,经修剪的杂质种类的混合物包括单臂经修剪的杂质和完全经修剪的杂质。在完整的可活化抗体包含多个ab和相应地多个前结构域的其他实施方案中,所述经修剪的杂质基本上由单臂经修剪的杂质组成。在这些实施方案的一些实施方案中,所述经修剪的物质由单臂经修剪的杂质组成。单臂经修剪的杂质和完全经修剪的杂质可以容易地通过质谱法确定。
[0131]
在一些实施方案中,水性原料包括处于约5.0至约8.0、或约5.0至约7.5、或约5.0至约7.0、或约5.5至约6.5、或约5.7至6.3、或约5.8至6.2、或约5.6至约6.0的范围内的ph。进行加载和洗脱步骤的温度可以相同或不同。在一些实施方案中,加载和洗脱步骤各自独立地在约10℃至约30℃的范围内、或约15℃至约30℃的范围内、或约15℃至约29℃的范围内、或约15℃至约28℃的范围内、或约15℃至约27℃的范围内、或约15℃至约26℃的范围内、或约15℃至约25℃的范围内、或约16℃至约25℃的范围内、或约17℃至约25℃的范围内、或约18℃至约25℃的范围内的温度下进行。通常,加载和洗脱步骤是在相同温度范围内的温度下进行。通常加载和洗脱步骤的目标温度大致相同。在一些实施方案中,可能希望在与进行加载步骤的温度不同的温度下进行洗脱步骤。在某些实施方案中,可能希望在高于或低于上述范围的端点的温度下进行工艺步骤。例如,当使用hic固定相时,加载步骤中使用的较高温度可能会增加与柱的疏水相互作用,并且洗脱步骤中的较低温度可能会通过减少与柱的疏水相互作用而促进组分从柱上释放。
[0132]
色谱柱可以预先调节以具有与水性原料大致相同的ph、第一盐浓度和温度。这可以通过将足够量(例如,一个或多个柱体积)的具有与水性原料相同的ph、第一盐浓度和/或温度的缓冲液加载到色谱柱中直到在柱中达到目标条件来实现。
[0133]
在加载步骤之后,可以在洗脱步骤之前用洗涤缓冲液洗涤该柱以从柱中去除非结合组分。在一些实施方案中,所述洗涤缓冲液包含与水性原料中第一盐的浓度大致相同浓度或浓度高于水性原料中第一盐浓度的盐,并且通常具有与水性原料大约相同的ph。
[0134]
已经发现,包含完整的可活化抗体和杂质的水性原料可以使用本文所述的工艺以高总蛋白质产率纯化。在一些实施方案中,如通过280nm波长处的吸光度所确定,所述洗脱物中总蛋白的产率为至少约60%、至少约65%、至少约70%、或至少约71%、或至少约72%、或至少约73%、或至少约74%、或至少约75%、或至少约76%、或至少约77%、或至少约78%、或至少约79%、或至少约80%、或至少约81%、或至少约82%、或至少约83%、或至少约84%、或至少约85%、或至少约86%、或至少约87%、或至少约88%、或至少约89%、或至少约90%、或至少约91%、或至少约92%、或至少约93%、或至少约94%、或至少约95%。用于确定总蛋白的说明性吸光度测定描述于下文实施例1中。
[0135]
疏水色谱工艺在从工艺流(即,统称为进入疏水工艺的水性原料流和流出疏水工艺的洗脱液流)中去除经修剪的杂质方面高度有效。在一些实施方案中,如通过还原性sds-毛细管凝胶电泳(sds-cge)所测量,所述水性原料中经修剪的杂质的相对量与所述洗脱物中经修剪的杂质的相对量相比的减少水平为至少约2倍、至少约3倍、至少约4倍、至少约5倍、至少约6倍、至少约7倍、或至少约8倍、或至少约9倍、或至少10倍、或至少约15倍、或至少约20倍。在一些实施方案中,在洗脱物中未检测到经修剪的杂质。术语“经修剪的杂质的相
对量”在本文中是指如下文所定义的“经修剪的杂质%”。
[0136]
如本文所用,短语“减少水平”或“减少”(及其语法变体)当与杂质(诸如经修剪的杂质、hcp、hwms等)结合使用时,是指如通过将水性原料中杂质的量与洗脱物中杂质的量比较所确定的杂质量减少的程度。杂质减少的水平可以用比率(或等效地,作为减少倍数)或以减少百分比来表示。
[0137]
当洗脱物中存在经修剪的杂质时,经修剪的杂质水平的减少倍数由以下公式确定:
[0138][0139]
其中,水性进料和洗脱物每一者中的“经修剪的杂质%”是根据以下公式确定:
[0140][0141]
其中:
[0142]
和
[0143][0144]
和,
[0145][0146]
其中:
[0147]
和
[0148][0149]
在上述公式中,经修剪的杂质是根据受修剪影响的多肽(即,编码前结构域的多肽)来定量。编码前结构域的多肽可以是抗体轻链、抗体重链、scfv等,取决于那些多肽是否也编码前结构域。例如,在前结构域与抗体轻链偶联的情况下,经修剪的杂质的相对量(即,经修剪的杂质%)是通过将洗脱物中轻链经修剪的杂质峰面积%除以以下各项之和来计算:a)洗脱物中轻链经修剪的杂质峰面积%和b)洗脱物中完整的轻链的峰面积%。经修剪的编码前结构域的多肽和完整的编码前结构域的多肽的峰面积很容易通过还原性sds-cge测定法确定,诸如实施例1中描述的测定法。
[0150]
因此,在这些实施方案中,如通过还原性sds-毛细管凝胶电泳(sds-cge)测定法(诸如实施例1中描述的测定法)所确定,所述水性原料中%经修剪的杂质与洗脱物中%经修剪的杂质的比率相应地为至少约2、或至少约3、或至少约4、或至少约5、或至少约6、或至少约7、或至少约8、或至少约9、或至少约10、或至少约15、或至少约20。
[0151]
在一些实施方案中,如通过还原性sds-cge(诸如实施例1中描述的测定法)所确定,所述水性原料中经修剪的杂质的相对量与洗脱物中经修剪的杂质的相对量相比对应于减少水平为至少约50%、或至少约55%、或至少约60%、或至少约65%、或至少约70%、或至少约75%、或至少约76%、或至少约77%、或至少约78%、或至少约79%、或至少约80%、或至少约81%、或至少约82%、或至少约83%、或至少约84%、或至少约85%、或至少约86%、或至少约87%、或至少约88%、或至少约89%、或至少约90%、或至少约91%、或至少约92%、或至少约93%、或至少约94%、或至少约95%、或至少约96%、或至少约97%、或至少约98%、或至少约99%。经修剪的杂质的减少百分比(%)由以下公式确定:
[0152][0153]
其中水性原料和洗脱物每一者的经修剪的杂质%如上所定义。
[0154]
在一些实施方案中,所述洗脱物包含相对量为水性原料中存在的经修剪的杂质的小于约50%、或小于约45%、或小于约40%、或小于约35%、或小于约30%、或小于约25%、或小于约24%、或小于约23%、或小于约22%、或小于约21%、或小于约20%、或小于约19%、或小于约18%、或小于约17%、或小于约16%、或小于约15%、或小于约14%、或小于约13%、或小于约12%、或小于约11%、或小于约10%的经修剪的杂质。作为水性原料中经修剪的杂质的百分比,所述洗脱物中经修剪的杂质的相对量确定如下:
[0155][0156]
其中水性原料和洗脱物每一者的经修剪的杂质%如上所定义。
[0157]
在一些实施方案中,如通过还原性sds-cge所测量,所述洗脱物包含相对量为水性原料中存在的经修剪的杂质的小于约15%、或小于约14%、或小于约13%、或小于约12%、或小于约11%、或小于约10%、或小于约10%、或小于约9%、或小于约8%、或小于约7%、或小于约6%的量的经修剪的杂质。在一些实施方案中,如通过还原性sds-cge所测量,所述洗脱物包含相对量为水性原料中存在的经修剪的杂质的约2%至15%、或约3%至约15%、或约4%至约15%、或约5%至约15%、或约2%至约10%、或约3%至约10%范围的经修剪的杂质。
[0158]
因此,所述疏水工艺在产生具有相对低水平的经修剪的杂质的洗脱物(和完整的可活化抗体的相应纯化组合物)方面是有效的。在某些实施方案中,如通过还原性sds-cge所确定,所述洗脱物(和完整的可活化抗体的相应纯化组合物)包含经修剪的杂质的相对量在约0.1%至约15%的经修剪的杂质、或约0.1%至约10%的经修剪的杂质、或约0.1%至约10%的经修剪的杂质、或约0.1%至约5%的经修剪的杂质、或约0.1%至约4%的经修剪的杂质、或约0.1%至约3%的经修剪的杂质、或约0.1%至约2%的经修剪的杂质、或约0.1%
至约1%的经修剪的杂质的范围内。经修剪的杂质百分比是如上定义计算的。经修剪的杂质百分比可以在分离程序完成后立即从洗脱物中取出的样品中测量,并且可以立即通过sds-cge分析或冷冻直到通过sds-cge分析。
[0159]
在一些实施方案中,如通过还原性sds-cge所测量,所述洗脱物(和完整的可活化抗体的相应纯化组合物)包含小于约5%、或小于约4%、或小于约3%、或小于约2%、或小于约1%、或小于约0.9%、或小于约0.8%、或小于约0.7%、或小于约0.6%、或小于约0.5%的经修剪的杂质。在其他实施方案中,如通过还原性sds-cge所测量,所述洗脱物包含小于约2%、或小于约1%、或小于约0.9%、或小于约0.8%、或小于约0.7%、或小于约0.6%、或小于约0.5%的经修剪的杂质。在某些实施方案中,所述洗脱物(和完整的可活化抗体的相应纯化组合物)不包含可检测的经修剪的杂质。
[0160]
在一些实施方案中,所述水性原料包含一种或多种选自由宿主细胞蛋白(hcp)、高分子量物质(hmws)及其组合组成的组的其他的杂质。本发明的方法在显著减少这些杂质的量方面也是有效的。在洗脱步骤中,hcp和hmws似乎大部分都与经修剪的杂质一起保留在柱中。
[0161]
在某些实施方案中,其他的杂质是hcp。在这些实施方案中,该工艺在从工艺流中去除hcp方面非常有效。在一些实施方案中,如通过相应的hcp elisa测定法所确定,按百万分率(ppm)计,由疏水色谱工艺实现的降低水平为至少约3倍、或至少约4倍、或至少约5倍、或至少约6倍、或至少约7倍、或至少约8倍、或至少约9倍、或至少约10倍。如通过相应的hcp elisa测定法所确定,hcp的减少倍数是通过将水性进料中hcp的量除以洗脱物中hcp的量(以ppm计)确定的,即,
[0162][0163]
hcp的量可以很容易地使用用于多种不同宿主细胞(包括,例如,哺乳动物、酵母、细菌和转基因宿主物种)的可从市场上商购的宿主细胞蛋白elisa试剂盒确定。术语“相应的hcp elisa测定法”在本文中用于指代宿主细胞蛋白elisa测定法,其使用与用于产生可活化抗体的宿主细胞相关的蛋白质的抗体。相应地,在一些实施方案中,如通过相应的hcp elisa测定法所确定,按百万分率(ppm)计,所述水性原料中hcp的量与所述洗脱物中hcp的量的比率为至少约4、或至少约5、或至少约6、或至少约7、或至少约8、或至少约9、或至少约10。
[0164]
就hcp的降低百分比(%)而言,在某些实施方案中,如通过相应的hcp elisa测定法所确定,按ppm计,所述降低水平为至少约50%、或至少约55%、或至少约60%、或至少约65%、或至少约70%、或至少约75%、或至少约76%、或至少约77%、或至少约78%、或至少约79%、或至少约80%、或至少约81%、或至少约82%、或至少约83%、或至少约84%、或至少约85%、或至少约86%、或至少约87%、或至少约88%、或至少约89%、或至少约90%。hcp减少百分比由以下公式确定:
[0165][0166]
相应地,在一些实施方案中,所述洗脱物包含的hcp为水性原料中存在hcp的小于
约50%、或小于约45%、或小于约40%、或小于约35%、或小于约25%、或小于约24%、或小于约23%、或小于约22%、或小于约21%、或小于约20%、或小于约19%、或小于约18%、或小于约17%、或小于约16%、或小于约15%、或小于约14%、或小于约13%、或小于约12%、或小于约11%、或小于约10%。作为水性原料中存在的hcp的百分比,所述洗脱物中hcp的相对量由以下公式确定:
[0167][0168]
在一些实施方案中,如通过相应的hcp elisa所测量,所述洗脱物(和完整的可活化抗体的相应纯化组合物)包含小于约150ppm、或小于约140ppm、或小于约130ppm、或小于约120ppm、或小于约110ppm、或小于约100ppm、或小于约90ppm、或小于约80ppm、或小于约70ppm、或小于约60ppm、或小于约50ppm、或小于约45ppm、或小于约40ppm、或小于约35ppm、或小于约30ppm、或小于约25ppm、或小于约20ppm、或小于约15ppm、或小于约10ppm的hcp。在某些实施方案中,所述洗脱物(和完整的可活化抗体的相应纯化组合物)不包含可检测的hcp。
[0169]
在其他实施方案中,所述洗脱物(和纯化的可活化抗体的相应组合物)包含hcp的量在约0.5ppm hcp至约150ppm hcp、或约0.5ppm hcp至约140ppm hcp、或0.5ppm hcp至约130ppm hcp、或约0.5ppm hcp至约120ppm、或约0.5ppm hcp至约110ppm、或约0.5ppm hcp至约100ppm hcp、或约0.5ppm hcp至约90ppm hcp、或约0.5ppm hcp至约90ppm hcp、或约0.5ppm hcp至约80ppm hcp、或约0.5ppm hcp至约70ppm hcp、或约0.5ppm hcp至约60ppm hcp、或约0.5ppm至约50ppm hcp、或约0.5ppm hcp至约45ppm hcp、或约0.5ppm hcp至约40ppm hcp、或约0.5ppm hcp至约40ppm hcp、或约0.5ppm hcp至约35ppm hcp、或约0.5ppm hcp至约30ppm hcp、或约1ppm hcp至约25ppm hcp、或约1ppm hcp至约20ppm hcp、或约0.5ppm hcp至约15ppm hcp、或约0.5ppm hcp至约10ppm hcp的范围内。
[0170]
在某些实施方案中,所述洗脱物(和可活化抗体的相应纯化组合物)包含hcp的量在约1ppm hcp至约150ppm hcp、或约1ppm hcp至约140ppm hcp、或1ppm hcp至约130ppm hcp、或约1ppm hcp至约120ppm、或约1ppm hcp至约110ppm、或约1ppm hcp至约100ppm hcp、或约1ppm hcp至约90ppm hcp、或约1ppm hcp至约90ppm hcp、或约1ppm hcp至约80ppm hcp、或约1ppm hcp至约70ppm hcp、或约1ppm hcp至约60ppm hcp、或约1ppm至约50ppm hcp、或约1ppm hcp至约45ppm hcp、或约1ppm hcp至约40ppm hcp、或约1ppm hcp至约40ppm hcp、或约1ppm hcp至约35ppm hcp、或约1ppm hcp至约30ppm hcp、或约1ppm hcp至约25ppm hcp、或约1ppm hcp至约20ppm hcp、或约1ppm hcp至约15ppm hcp、或约1ppm hcp至约10ppm hcp的范围内。
[0171]
在其他实施方案中,所述其他的杂质是单独的或与hcp组合的hmws。hmws可以通过尺寸排阻(se)-hplc检测和量化。说明性se-hplc测定法描述于实施例1中。在色谱图主峰的左侧检测到高分子量物质(hmws)。在这些实施方案中,所述疏水色谱工艺在从工艺流中去除hmws方面非常有效。在一些实施方案中,由疏水色谱工艺实现的hmws量的减少水平是至少约2倍、或至少约3倍、或至少约4倍、或至少约5倍,其中hmws是通过尺寸排阻(se)-hplc量化的。示例性se-hplc测定法描述于实施例1中。hmws的减少倍数以及相应地水性原料中hmws的量与洗脱物中hmws的量的比率均由下式确定:
[0172][0173]
其中:
[0174]
(hmws峰面积%)
水性原料
是通过se-hplc测定法确定的对应于水性原料中hmws的所有峰的总和除以所有峰面积的总和(即,总峰面积);和
[0175]
(hmws峰面积%)
洗脱物
是如se-hplc确定的洗脱物中对应于hmws的所有峰的总和除以所有峰面积的总和(总峰面积)。
[0176]
因此,在这些实施方案中,水性原料中hmws的量与洗脱物中hmws的量的比率相应地为至少约2、或至少约3、或至少约4、或至少约5,其中hmws的量由se-hplc确定。
[0177]
在一些实施方案中,如通过se-hplc所确定,通过疏水色谱工艺实现的hmws减少水平从hmws减少百分比(%)来看为至少约50%、或至少约55%、或至少约60%、或至少约65%、或至少约70%、或至少约75%、或至少约76%、或至少约77%、或至少约78%、或至少约79%、或至少约80%、或至少约81%、或至少约82%、或至少约83%、或至少约84%、或至少约85%、或至少约86%、或至少约87%、或至少约88%、或至少约89%、或至少约90%、或至少约91%、或至少约92%、或至少约93%、或至少约94%、或至少约95%、或至少约96%、或至少约98%、或为至少约99%。hmws的减少百分比根据以下公式确定:
[0178][0179]
其中水性原料和洗脱物的hmws峰面积%如上文所定义。
[0180]
在一些实施方案中,如通过se-hplc所确定,所述洗脱物中hmws的相对量以水性原料中存在的hmws的百分比计为水性原料中存在的hmws的小于约50%、或小于约45%、或小于约40%、或小于约35%、或小于约25%、或小于约30%、或小于约25%、或小于约20%、或小于约15%、或小于约15%。洗脱物中hmws的相对量占水性原料中存在的hmws的百分比计算如下:
[0181][0182]
其中水性原料和洗脱物的hmws峰面积%如上文所定义。
[0183]
在一些实施方案中,如通过se-hplc所确定,所述洗脱物(和完整的可活化抗体的相应纯化组合物)包含小于约5%、或小于约4%、或小于约3%、或小于约2%、或小于约1%的hmws,其中hmws%对应于(hmws峰面积%)
洗脱物
,并如上所述所确定。
[0184]
在其他实施方案中,所述洗脱物(和完整的可活化抗体的相应纯化组合物)包含小于约3%、或小于约2%、或小于约1%的hmws。在一些实施方案中,所述洗脱物包含小于约2%、或小于约1%的hmws。
[0185]
在一些实施方案中,如通过se-hplc所确定,所述洗脱物(和完整的可活化抗体的相应纯化组合物)包含hmws的量在约0.1%、0.2%或0.3% hmws至约5% hmws、或约0.2% hmws至约4% hmws、或约0.2%hmws至约3% hmws、或约0.2% hmws至约2% hmws、或约0.2% hmws至约1% hmws的范围内,其中%基于总峰面积来确定。在某些实施方案中,所述洗脱物(和完整的可活化抗体的相应纯化组合物)不包含可检测的hmws。
[0186]
在本文所述工艺的一些实施方案中,如通过还原性sds-cge所测量,所述水性原料包含大于约0.5%经修剪的杂质,或大于约0.6%、或大于约0.7%、或大于约0.8%、或大于约0.9%、或大于约1%、或大于约1.5%、或大于约2%、或大于约2.5%、或大于约3%、或大于约3.5%、或大于约4%、或大于约4.5%、或大于约5%、或大于约5.5%、或大于约6%、或大于约6.5%、或大于约7%、或大于约7.5%、或大于约8%、或大于约8.5%、或大于约9%、或大于约9.5%、或大于约10%、或大于约10.5%、或大于约11%、或更大超过约11.5%、或大于约12%、或大于约12.5%、或大于约13%、或大于约13.5%经修剪的杂质。经修剪的杂质百分比在上文中定义。
[0187]
本发明的工艺产生的洗脱物是完整的可活化抗体的高纯度组合物。如通过还原性sds-cge所测量,得到的洗脱物(和完整的可活化抗体的相应纯化组合物)通常包含至少约90%、或至少约91%、或至少约92%、或至少约93%、或至少约94%、或至少约95%、或至少约96%、或至少约97%、或至少约98%、或至少约98.5%、或至少约99%的完整的可活化抗体。说明性的sds-cge测定法描述于实施例1中。完整的杂质百分比如上文所述计算(即,(完整的可活化抗体百分比)
洗脱物
)。
[0188]
在一个方面,本公开包括用于生产组合物的工艺,所述组合物包含:(a)大于95%的完整的可活化抗体,其包含mm、cm和ab;和(b)0.05%至5%的其经修剪的变体,所述工艺包括将包含水、(a)、(b)和第一盐的水性原料加载到色谱柱上,其中所述色谱柱包括固定相,所述固定相包括支持基质和与其结合的疏水性配体,并用包含水和第二盐的洗脱液洗脱色谱柱以获得组合物。在一个方面,所述工艺包括将工艺流中的经修剪的变体的量减少75%至90%。在一个方面,所述工艺包括将工艺流中的hcp的量减少75%至90%。在一个方面,所述工艺包括将工艺流中的hmws的量减少75%至90%。在一个方面,所述工艺包括将工艺流中的经修剪的变体、hcp和hmws的量减少70%至95%。
[0189]
可活化抗体通常通过培养经工程改造以表达所需完整的可活化抗体的细胞以生物学方式产生。例如,细胞可以是哺乳动物宿主细胞。在一些方面,细胞可以是人胚肾(hek)细胞,例如,hek293细胞,或中国仓鼠卵巢(cho)细胞。在这些工艺中,可活化抗体是作为细胞培养上清液、细胞裂解物或其他源自包含可活化抗体的细胞培养物的类似组合物从细胞培养物中收获的。生物收获物组合物是通过使用例如离心、过滤或其他固液分离工艺从上清液或裂解物中分离细胞和细胞碎片来获得的。
[0190]
疏水色谱工艺通常部署在细胞培养步骤的下游,通过任选地一个或多个干预单元操作用于去除生物收获物组合物和如果适用的话任何散装中间产物组合物中可能存在的至少一部分的非免疫球蛋白、宿主细胞蛋白和其他杂质。
[0191]
每个细胞培养步骤、任选的一个或多个介入单元操作和疏水色谱工艺可以作为分批工艺进行,或任选地,前述单元操作中的任何两个或更多个可以作为连续或半连续工艺在任选集成系统中进行。在一些实施方案中,细胞培养步骤是作为分批补料操作进行的。在一些实施方案中,细胞培养步骤是作为连续进料或灌注操作进行的。
[0192]
在一些实施方案中,生物收获物组合物和/或一种或多种散装中间产物组合物是在进料到下一个单元操作之前经一段时间来分级的。散装中间产物组合物可以任选地通过添加一种或多种调理剂来调节以使其适合作为下一个后续单元操作的进料。示例性调理剂包括例如缓冲剂(即,一种或多种缓冲剂)、盐(例如,第一盐)、碱、酸等。
[0193]
因此,在本发明的实践中使用的水性原料可以包括生物收获物组合物或散装中间产物组合物。在一些实施方案中,在步骤(a)之前,该工艺包括:
[0194]
(a0)使包含完整的可活化抗体和相应的经修剪的杂质的生物收获物组合物经受一个或多个选自由离心步骤、过滤步骤、亲和色谱步骤、病毒灭活步骤、尺寸排阻色谱步骤、病毒过滤步骤和离子交换(iex)色谱步骤组成的组的干预单元操作以产生一种或多种散装中间产物组合物,其中所述水性原料包含至少一种散装中间产物组合物。在一些实施方案中,所述工艺包括至少两个或更多个干预单元操作的组合。
[0195]
在一些实施方案中,所述生物收获物组合物经受至少两个或更多个,或在某些实施方案中,经受至少三个或更多个选自由离心步骤、过滤步骤、亲和色谱步骤、病毒灭活步骤、尺寸排阻色谱步骤、病毒过滤步骤和离子交换色谱步骤的组的连续干预单元操作。在一些实施方案中,使生物收获物组合物经受亲和色谱步骤,并且通常另外经受病毒灭活步骤和任选的离子交换色谱步骤。例如,可以使用亲和色谱,通过使用固定化配体诸如例如蛋白a(即,“蛋白a色谱”步骤)、蛋白g(即,“蛋白g色谱”步骤)等将含免疫球蛋白(ig)的组分与生物收获物组合物中的其他组分分离。在某些实施方案中,步骤(a0)的一个或多个干预单元操作包括亲和色谱步骤和离子交换色谱步骤。在一些实施方案中,步骤(a0)的一个或多个干预单元操作包括亲和色谱步骤、病毒灭活步骤、过滤步骤(例如,切向流过滤步骤、超滤步骤、渗滤步骤等)以及离子交换色谱步骤。在某些实施方案中,所述离子交换色谱步骤是阴离子交换色谱步骤。在一些方面,本公开的方法包括排除本公开中描述的操作的任何一种操作或其组合的方法。例如,本公开的方法可以排除阴离子交换步骤。作为另一个实例,本公开的方法可以排除阴离子交换步骤。作为另一个实例,本公开的方法可以排除尺寸排阻色谱步骤。
[0196]
当所述工艺采用一种或多种干预单元操作时,由紧邻疏水色谱工艺上游的干预单元操作产生的散装中间产物组合物在本文中称为“预进料”。在一些实施方案中,所述预进料可直接用作水性原料。在某些实施方案中,所述预进料可以通过添加一种或多种组分,诸如,例如第一盐、一种或多种缓冲剂(诸如,例如盐、酸和/或碱)等来调节。
[0197]
相对于经修剪的杂质富含完整的可活化抗体的洗脱物(和完整的可活化抗体的相应纯化组合物),可以任选地经受一个或多个下游单元操作以产生下游产物组合物。说明性下游单元操作包括,例如,(其他的)纯化过程、化学合成工艺、稀释工艺、溶剂交换工艺、配制工艺、冻干工艺或其两个或更多个的任何组合。例如,在一个实施方案中,所述工艺还包括使洗脱物经受一个或多个选自由离心步骤、过滤步骤(例如,切向流过滤、超滤、渗滤等)、亲和色谱步骤、病毒灭活步骤、尺寸排阻色谱步骤、病毒过滤步骤、离子交换色谱步骤以及其两个或更多个的任何组合组成的组的下游单元操作。洗脱物和下游产物组合物通常没有可检测的量或具有含有非常少量的经修剪的杂质和/或hcp和/或hmws。洗脱物和下游产物组合物可以基本上不含经修剪的杂质。
[0198]
在一些实施方案中,通过使洗脱物或下游产物组合物与结合剂在足以生成缀合的可活化抗体的条件下接触,使通过本发明的工艺产生的纯化的完整的可活化抗体组合物(例如,洗脱物或下游产物组合物)经受化学缀合反应。缀合部分用于赋予可活化抗体另外的特性,诸如,例如延长的半衰期(例如,其中所述缀合部分是半衰期延长剂,诸如,例如聚乙二醇(peg)部分、人血清白蛋白(hsa部分)等);细胞毒性(其中缀合部分是毒素的全部或
一部分,诸如,例如多拉司汀(dolastin)或其衍生物(例如,澳瑞斯汀e、afp、mmaf、mmae、mmad、dmaf、dmae等以及它们的衍生物)、类美登素(maytansinoid)或其衍生物、dm1、dm4、多霉素或其衍生物、加利车霉素或其衍生物、吡咯并苯并二氮或其衍生物或二聚体、重金属(例如,钡、金、铂等)、假单胞菌毒素a变体(例如,pe38、zz-pe38等)、zj-101、osw-1、o6-苄基鸟嘌呤的4-硝基苄氧基羰基衍生物、拓扑异构酶抑制剂、哈米特林(hemiasterlin)、三尖杉碱、高三尖杉酯碱(homoharringonine)、吡咯并苯二氮二聚体、吡咯并苯并二氮杂(pyrrolobenzodiazepene)、官能化的吡咯并苯并二氮杂、官能化的吡咯并苯并二氮杂二聚体、加利车霉素、鬼臼毒素、紫杉烷、长春花生物碱等,以及多种其他已知细胞毒剂中的任一种);抗病毒活性(例如,其中所述缀合部分是阿昔洛韦、vira a、symetrel、涡轮他汀(turbostatin)、芬他汀(phenstatin)、羟基芬他汀(hydroxyphenstatin)、海绵抑素(spongistatin)5、海绵抑素7、哈利他汀(halistatin)1、哈利他汀2、哈利他汀3、修饰的苔藓抑素的全部或一部分、卤代坎普他汀(halocomstatin)、吡咯并苯并咪唑(pyrrolobenzimadazole)、西溴抑素(cibrostatin)6、doxaliform、蒽环类抗生素、西马多丁类似物(例如,cemch2-sh)等);抗真菌活性(例如,其中所述缀合部分是制霉菌素的全部或一部分等);抗肿瘤活性(例如,其中所述缀合部分是亚德里亚霉素、柔红霉素、博来霉素、爱克兰(alkeran)、长春碱(velban)、安可平(oncovin)、氟尿嘧啶、甲氨蝶呤、噻替派、比生群、诺凡酮、硫鸟嘌呤、丙卡比嗪、阿糖胞苷等的全部或一部分);抗菌活性(例如,其中所述缀合部分是氨基糖苷、链霉素、新霉素、卡那霉素、阿米卡星、庆大霉素、妥布霉素、链霉素b、壮观霉素、氨苄青霉素、磺胺、多粘菌素、氯霉素等的全部或一部分);抗支原体活性(例如,其中所述缀合部分是泰乐菌素、壮观霉素等的全部或一部分);以及各种其他理想的另外特性中的任何一种。
[0199]
赋予此类所需特性和功能的缀合部分可使用本领域已知的方法和反应性接头容易地缀合至可活化抗体。在一些实施方案中,由如本文所述的纯化的可活化抗体组合物制备的缀合的可活化抗体的组合物也基本上不含经修剪的杂质和/或hcp和/或hmws。关于经修剪的杂质、hcp和hmws,这些缀合的可活化抗体组合物通常具有与本文所述的洗脱物和纯化的完整的可活化抗体组合物相同的纯度和杂质谱。
[0200]
在另一个实施方案中,本发明提供了可以通过本发明的方法生产的纯化的完整的可活化抗体组合物。在一些实施方案中,所述纯化的完整的可活化抗体组合物包含如通过还原性sds-cge所测量的至少约90%的完整的可活化抗体,其中完整的可活化抗体%如上文定义;如通过还原性sds-cge所测量的小于约15%的经修剪的杂质,其中经修剪的杂质%如上文定义;如通过se-hplc所测量的小于约5%的hmws,其中hmws%如上文定义;以及如通过相应的hcp elisa测定法所测量的小于约150ppm的hcp。在这些实施方案的某些实施方案中,纯化的完整的可活化抗体组合物包含至少约91%、或至少约92%、或至少约93%、或至少约94%、或至少约95%、或至少约96%、或至少约97%、或至少约98%、或至少约99%完整的可活化抗体。
[0201]
在这些纯化的完整的可活化抗体组合物中的一些组合物中,如通过sds-cge所测量,组合物包含小于约14%、或小于约13%、或小于约12%、或小于约11%、或小于约10%、或小于约9%、或小于约8%、或小于约7%、或小于约6%经修剪的杂质。在某些实施方案中,如通过还原性sds-cge所测量,洗脱物(和完整的可活化抗体的相应纯化组合物)包含小于
hcp至约20ppm hcp,或约1ppm hcp至约15ppm hcp,或约1ppm hcp至约10ppm hcp的范围内。
[0206]
在一些实施方案中,如通过se-hplc所确定,纯化的完整的可活化抗体组合物包含小于约4%、或小于约3%、或小于约2%、或小于约1%的hmws,其中hmws%如上所定义。
[0207]
在某些实施方案中,如通过se-hplc所确定,纯化的完整的可活化抗体组合物包含hmws的量在约0.2% hmws至约5% hmws,或约0.2% hmws至约4% hmws,或约0.2% hmws至约3% hmws,或约0.2% hmws至约2% hmws,或约0.2% hmws至约1% hmws的范围内。在一些实施方案中,纯化的完整的可活化抗体组合物不包含可检测的hmws。
[0208]
在一些方面,如通过sds-cge所测量,所述纯化的完整的可活化抗体组合物包含大于90%的完整的可活化抗体和0.05%至5%的经修剪的变体。在一些方面,所述组合物包含大于90%的完整的可活化抗体和0.05%至5%的经修剪的变体(如通过sds-cge所确定)、小于150ppm的宿主细胞蛋白(hcp)(如通过宿主细胞elisa所确定)和小于5%的高分子量物质(hmws)(由se-hplc所确定)。在一些方面,所述组合物包含大于96%的完整的可活化抗体、0.05%至4%的经修剪的变体、小于150ppm的宿主细胞蛋白(hcp)和小于5%的hmws。在一些方面,所述组合物包含大于97%的完整的可活化抗体、0.05%至3%的经修剪的变体、小于150ppm的宿主细胞蛋白(hcp)和小于5%的hmws。在一些方面,所述组合物包含大于98%的完整的可活化抗体、0.05%至2%的经修剪的变体、小于150ppm的宿主细胞蛋白(hcp)和小于5%的hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至5%的经修剪的变体、小于100ppm的宿主细胞蛋白(hcp)和小于3%的hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至3%的经修剪的变体、小于100ppm的宿主细胞蛋白(hcp)和小于3%的hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至2%的经修剪的变体、小于100ppm的宿主细胞蛋白(hcp)和小于3%的hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至5%的经修剪的变体、小于100ppm的宿主细胞蛋白(hcp)和小于2%的hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至5%的经修剪的变体、小于100ppm的宿主细胞蛋白(hcp)和小于1.5%的hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至3%的经修剪的变体、小于100ppm的宿主细胞蛋白(hcp)和小于1.5%的hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至2%的经修剪的变体、小于100ppm的宿主细胞蛋白(hcp)和小于1.5%的hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至5%的经修剪的变体、小于25ppm的宿主细胞蛋白(hcp)和小于1.5%的hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至3%的经修剪的变体、小于25ppm的宿主细胞蛋白(hcp)和小于1.5%的hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至2%的经修剪的变体、小于25ppm的宿主细胞蛋白(hcp)和小于1.5%的hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至2%的经修剪的变体、小于10ppm的宿主细胞蛋白(hcp)和小于1.5%的hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至5%的经修剪的变体、小于25ppm的宿主细胞蛋白(hcp)和小于1.0%的hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至3%的经修剪的变体、小于25ppm的宿主细胞蛋白(hcp)和小于1.0%的hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至2%的经修剪的变体、小于25ppm的宿主细胞蛋白(hcp)和小于1.0%的
hmws。在一些方面,所述组合物包含大于95%的完整的可活化抗体、0.05%至2%的经修剪的变体、小于10ppm的宿主细胞蛋白(hcp)和小于1.0%的hmws。在一些方面,所述经修剪的变体是单臂经修剪的物质。
[0209]
本发明还提供药物组合物,其包含本发明的完整的可活化抗体的纯化组合物和一种或多种药学上可接受的组分。在一些实施方案中,药学上可接受的组分是药学上可接受的赋形剂。此类组合物可以通过将药学上可接受的赋形剂添加到由本发明的工艺生产的纯化组合物(诸如,例如,本发明的完整的可活化抗体的纯化组合物,或由其衍生的其他的组合物)中来制备。适用于本发明的组合物的药学上可接受的赋形剂是本领域众所周知的,并且包括例如无菌水、表面活性剂(例如,非离子表面活性剂、阳离子表面活性剂和/或阴离子表面活性剂)、缓冲剂(酸、碱和/或盐)、醇、二醇、多元醇、糖(例如,单糖、二糖和/或多糖)、亲水性聚合物(例如,聚乙二醇(peg)、聚乙烯醇、增溶剂(例如,环糊精等)等。所述组合物可以是液体形式或者它可以是固体形式,例如,颗粒形式。例如,所述固体形式可以通过将相应的液体组合物冻干以形成冻干的药物组合物来制备。
[0210]
当药物组合物为液体形式时,它通常还包含水(例如,无菌水)。在一些实施方案中,所述组合物还包含水和一种或多种选自由表面活性剂、缓冲剂、糖及其两种或更多种的任何组合的组成的组的组分。当药物组合物为固体(例如,冻干)形式时,它通常包含一种或多种选自由糖和缓冲剂组成的组的组分。在一些实施方案中,所述组合物包含糖。
[0211]
本发明的工艺和组合物可以使用多种可活化抗体中的任何一种。如下文的实例中所示,所述工艺显示能够产生完整的可活化抗体的纯化组合物,其中经修剪的杂质以及hcp和hmws显著减少。在每个使用本发明的工艺纯化包含这些可活化抗体的水性原料的情况下,富含完整的可活化抗体并且基本上去除了包括经修剪的杂质、hmws的洗脱物首先洗脱。这一观察结果在多种可活化抗体氨基酸序列中是一致的。因此,相信本发明的方法适用于多种粗制可活化抗体组合物中的任何一种,而不管可活化抗体的特定氨基酸序列如何(例如,mm、cm、ab)。因此,可以使用本发明的工艺纯化的组合物可以包含具有ab组分的可活化抗体,所述ab组分能够通过例如掺入来自已知结合至所需生物靶标的抗体的vl和vh cdr氨基酸序列而特异性地结合至本领域已知的多种生物靶标中的任何一种(当未被掩蔽时),或替代地,或通过使用本领域已知的多种已知抗体发现筛选平台中的任何一种来鉴定。
[0212]
生物靶标的说明性类别包括细胞表面受体和分泌的结合蛋白(例如,生长因子等)、可溶性酶、结构蛋白(例如,胶原蛋白、纤连蛋白等)等。合适的生物靶标包括,例如,1-02-lfa-3、α4-整联蛋白、α-v-整联蛋白、α4β1-整联蛋白、agr2、抗lewis y、apelin j受体、april、b7-h4、baff、btla、c5补体、c-242、ca9、ca19-9(lewis a)、碳酸酐酶9、cd2、cd3、cd6、cd9、cd11a、cd19、cd20、cd22、cd25、cd28、cd30、cd33、cd40、cd40l、cd41、cd44、cd44v6、cd47、cd51、cd52、cd56、cd64、cd70、cd71、cd74、cd80、cd81、cd86、cd95、cd117、cd125、cd132(il-2rg)、cd133、cd137、cd137、cd138、cd166、cd172a、cd248、cdh6、ceacam5(cea)、ceacam6(nca-90)、claudin-3、claudin-4、cmet、胶原蛋白、cripto、csfr、csfr-1、ctla-4、ctgf、cxcl10、cxcl13、cxcr1、cxcr2、cxcr4、cyr61、dl44、dlk1、dll4、dpp-4、dsg1、egfr、egfrviii、内皮素b受体(etbr)、enpp3、epcam、epha2、erbb3、rsv的f蛋白、fap、fgf-2、fgf-8、fgfr1、fgfr2、fgfr3、fgfr4、叶酸受体、gal3st1、g-csf、g-csfr、gd2、gitr、glut1、glut4、gm-csf、gm-csfr、gp iib/iiia受体、gp130、gpiib/iiia、gpnmb、grp78、her2/neu、hvem、透
明质酸酶、icos、ifnα、ifnβhgf、hgh、透明质酸酶、icos、ifnα、ifnβ、ifnγ、ige、ige受体(fceri)、igf、igf1r、il1b、il1r、il2、il11、il12p40、il-12r、il-12rβ1、il13、il13r、il15、il17、il18、il21、il23、il23r、il27/il27r(wsx1)、il29、il-31r、il31/il31r、il-2r、il4、il4-r、il6、il-6r、胰岛素受体、jagged配体、jagged 1、jagged 2、lag-3、lif-r、lewis x、light、lrp4、lrrc26、mcsp、间皮素、mrp4、muc1、粘蛋白-16(muc16、ca-125)、na/katp酶、中心粒细胞弹性蛋白酶、ngf、nicastrin、notch受体、notch 1、notch 2、notch 3、notch 4、nov、osm-r、ox-40、par2、pdgf-aa、pdgf-bb、pdgfrα、pdgfrβ、pd-1、pd-l1、pd-l2、磷脂酰丝氨酸、p1gf、psca、psma、raag12、rage、slc44a4、磷酸鞘氨醇1、steap1、steap2、tag-72、tapa1、tgfβ、tigit、tim-3、tlr2、tlr6、tlr7、tlr8、tlr9、tmem31、tnfα、tnfr、tnfrs12a、trail-r1、trail-r2、转铁蛋白、转铁蛋白受体、trk-a、trk-b、upar、vap1、vcam-1、vegf、vegf-a、vegf-b、vegf-c、vegf-d、vegfr1、vegfr2、vegfr3、vista、wisp-1、wisp-2、wisp-3等。
[0213]
ab由vl和vh形成(并且因此可活化抗体包含vl和vh),所述vl和vh直接或间接地例如通过共价键或非共价键连接在一起。在一些实施方案中,所述vl和vh是通过一个或多个二硫键(例如,通过一个或多个cys-cys二硫键)、通过肽接头、通过合成接头、通过天然存在的接头等连接在一起。在结构上,每个ab可以独立地为多种形式中的任何一种,诸如,例如fab、f(ab')2、单特异性fab2、双特异性fab2、三特异性fab3、scfv、双特异性双抗体、三特异性三抗体、scfv-fc、微型抗体、双特异性t细胞衔接器(例如,bite
tm
)、双亲和再靶向抗体(dart抗体)等。合适的双特异性形式包括本领域已知的多种双特异性抗体形式中的任何一种,包括描述于kontermann等人,"bispecific antibodies",drug discovery today(2015)20(7):838-847中的双特异性抗体,其通过引用方式以其整体并入本文。
[0214]
在一些实施方案中,所述可活化抗体包含具有一组第一vl cdr(即,第一vl cdr1、第一vl cdr2和第一vl cdr3)的第一vl和具有一组第一vh cdr(即,第一vh cdr1、第一vh cdr2和第一vh cdr3)的第一vh,其中所述vl和vh一起形成对应的ab。在一些实施方案中,所述可活化抗体还具有对第二生物靶标具有特异性结合亲和力的第二ab,其中所述第二ab包含第二vl、第二vh和第二前结构域,所述第二前结构域包含第二mm和第二cm,其中所述第二ab与第二前结构域偶联。在这些实施方案中,所述第二vl包含一组第二vl cdr(即,第二vl cdr1、第二vl cdr2和第二vl cdr3)和具有一组第二vh cdr(即,第二vh cdr1、第二vh cdr2和第二vh cdr3)的第二vh,其中所述vl和vh一起形成对应的第二ab。具有另外的ab(来自第三vl和第三vh氨基酸序列等)的可活化抗体的纯化组合物可使用本发明的工艺来制备,其中每个另外的ab具有相应的mm和与其偶联的cm。对应于ab的每组vl和vh可以由单个多肽(诸如,例如,scfv等)或两个多肽(诸如抗体轻链和抗体重链)编码。对多种生物靶标具有结合特异性的vh和vl cdr序列是本领域已知的,并且可以掺入本发明的工艺和组合物中使用的可活化抗体中。
[0215]
在一些实施方案中,当可活化抗体包含第二vl和第二vh时,第一vl cdr组中每个cdr的氨基酸序列是与第二vl cdr组中相应cdr的氨基酸序列同一的。在某些实施方案中,第一vh cdr组中每个cdr的氨基酸序列是与第二vh cdr组中相应cdr的氨基酸序列同一的。在这些实施方案中,第一ab和第二ab(即,当未被掩蔽时)通常对相同的生物靶标物质具有结合特异性。
igg1;n325s/l328f igg1等。在一些实施方案中,经工程改造的fc结构域包含一个或多个选自由n297a igg1、n297q igg1和s228p igg4组成的组的取代。氨基酸残基编号基于欧盟编号系统。
[0221]
在本发明的实践中采用的可活化抗体可以多种结构构型存在。下文提供了可活化抗体的说明性结构式。应注意,尽管在下式中mm和cm被指示为不同的组分,但是在本文所公开的所有示例性实施方案(包括式)中,可以设想mm和cm的氨基酸序列可重叠,例如,使得cm完全或部分地包含在mm内。
[0222]
在可活化抗体内,所述cm可以直接或间接地通过一个或多个接头定位在mm和ab之间。通常,所述可活化抗体的mm、cm和ab组分中的每一者都以选自由以下(从n末端至c末端)组成的组的结构排列:
[0223]
(mm)-(cm)-(ab);或
[0224]
(ab)-(cm)-(mm)
[0225]
其中mm、cm和ab如先前所定义,并且其中每个
“‑”
独立地指代直接或间接的(即,通过如下文所述的接头)键联。
[0226]
在许多实施方案中,所述可活化抗体可能包含一个或多个接头以便在所述mm-cm接点、所述cm-ab接点或两者中的一者或多者处赋予柔性。例如,在某些实施方案中,所述可活化抗体可包含以选自由以下(从n末端至c末端或从c末端至n末端)的结构排列的mm、cm和ab组分:
[0227]
(mm)-l1-(cm)-(ab);
[0228]
(mm)-(cm)-l2-(ab);或
[0229]
(mm)-l1-(cm)-l2-(ab)
[0230]
其中mm、cm和ab如上文所定义;其中每个接头l1和l2可相同或不同,并且各自独立地可任选地存在或不存在。
[0231]
在一些实施方案中,所述完整的可活化抗体包含第一ab,其中所述第一vl由第一轻链编码,并且其中所述第一vh由第一重链编码,并且其中所述第一轻链进一步编码一种或多种选自由前结构域、接头、轻链恒定结构域及其任何两个或更多个的组合组成的组的组分,并且其中所述第一重链进一步编码一种或多种选自由前结构域、接头、一个或多个重链恒定结构域、铰链区及其任何两个或多个的组合组成的组,条件是所述轻链和所述重链中仅一者编码所述前结构域。在某些实施方案中,如上文更详细描述的,所述完整的可活化抗体还包含fc结构域。在这些实施方案的一些实施方案中,所述可活化抗体包含第一ab(包含第一vl和第一vh)和第二ab(包含第二vl和第二vh)。在一个具体实施方案中,所述第一vl和所述第二vh通过接头连接在一起,并且所述第二vl和所述第一vh通过接头连接在一起。在其他的具体实施方案中,所述可活化抗体包含第一单链抗体和第二单链抗体,所述第一单链抗体包含所述第一vl、第一接头和所述第一vh,所述第二单链抗体包含所述第二vl、第二接头和所述第二vh,其中所述第一单链抗体和所述第二单链抗体通过第三接头连接在一起。
[0232]
本发明的组合物和工艺中使用的可活化抗体可以包含多种具有作为蛋白酶底物起作用的氨基酸序列的cm中的任何一种。合适的底物氨基酸序列可使用多种已知技术中的任一种容易地鉴别,所述技术包括美国专利第7,666,817号、美国专利第8,563,269号、pct
公布第wo 2014/026136号以及boulware等人“evolutionary optimization of peptide substrates for proteases that exhibit rapid hydrolysis kinetics,”biotechnol bioeng.106.3(2010):339-46中描述的那些。
[0233]
在一些实施方案中,所述cm包含用于在疾病状况或患病组织中具有活性(例如,上调或在其他方面不调节)的蛋白酶的底物,使得当所述可活化抗体暴露于蛋白酶时所述蛋白酶切割可活化抗体中的cm。示例性的疾病状况包括,例如,癌症(例如,在患病组织是肿瘤组织的情况下)和炎症或自身免疫状况(例如,在患病组织是发炎组织的情况下)。在一些实施方案中,所述cm包含用于半胱氨酸蛋白酶的底物。如图3a和3b所示,本公开的完整的可活化抗体的cm可以在患病组织的微环境中被切割,其中切割所述cm的蛋白酶相对于健康组织被过表达。因此,本公开的纯化的可活化抗体组合物能够将目标治疗剂量的完整的可活化抗体递送至相关病变组织,同时最小化将亚治疗剂量递送至患病组织的可能性,并且另外地,避免递送经修剪的由此活性的抗体至受试者的健康组织。
[0234]
可以使用多种已知技术中的任何一种容易地鉴定合适的底物,所述技术包括美国专利号7,666,817、美国专利号8,563,269、pct公开号wo 2014/026136,boulware等人,“evolutionary optimization of peptide substrates for proteases that exhibit rapid hydrolysis kinetics,”biotechnolo.bioeng.(2010)106.3:339-46中描述的那些技术,上述参考文献中的每一个特此通过引用整体并入。示例性底物包括用于以下蛋白酶的一种或多种的底物的那些底物:adam、adam样或adamts(例如adam8、adam9、adam10、adam12、adam15、adam17/tace、adamdec1、adamts1、adamts4、adamts5);天冬氨酸蛋白酶(例如,bace、肾素等);天冬氨酸组织蛋白酶(例如,组织蛋白酶d、组织蛋白酶e等);半胱天冬酶(例如,半胱天冬酶1、半胱天冬酶2、半胱天冬酶3、半胱天冬酶4、半胱天冬酶5、半胱天冬酶6、半胱天冬酶7、半胱天冬酶7、半胱天冬酶8、半胱天冬酶9、半胱天冬酶10、半胱天冬酶14等);半胱氨酸蛋白酶(例如克鲁兹蛋白酶(crupzipain)、豆荚蛋白酶(legumain)、otubain-2等);激肽释放酶相关肽酶(klk)(例如,klk4、klk5、klk6、klk7、klk8、klk10、klk11、klk13、klk14等);金属蛋白酶(例如,穿膜肽酶(meprin)、中性内肽酶(neprilysin)、前列腺特异性膜抗原(psma)、骨形态发生蛋白1(bmp-1)等);基质金属蛋白酶(mmp)(例如,mmp1、mmp2、mmp3、mmp7、mmp8、mmp9、mmp10、mmp11、mmp12、mmp13、mmp14、mmp15、mmp16、mmp17、mmp19、mmp20、mmp23、mmp24、mmp26、mmp27等);丝氨酸蛋白酶(例如,活化蛋白c、组织蛋白酶a、组织蛋白酶g、糜蛋白酶、凝血因子蛋白酶(例如,fviia、fixa、fxa、fxia、fxiia等));弹性蛋白酶、颗粒酶b、胍基苯甲酰酶(guanidinobenzoatase)、htra1、人中性粒细胞弹性蛋白酶、乳铁蛋白、marapsin、ns3/4a、pace4、纤溶酶、前列腺特异性抗原(psa)、组织纤溶酶原活化物(tpa)、凝血酶、类胰蛋白酶、尿激酶(upa)、ii型跨膜丝氨酸蛋白酶(ttsp)(例如,desc1、dpp-4、fap、hepsin、蛋白裂解酶-2、mt-sp1/蛋白裂解酶、tmprss2、tmprss3、tmprss4等)等。特定的可活化抗体cm描述于例如wo 2010/081173、wo 2015/048329、wo 2015/116933和wo 2016/118629中,上述专利中的每一个均通过引用方式以其整体并入本文。
[0235]
在一些实施方案中,存在于完整的可活化抗体中的至少一种或多种cm(例如,第一和第二cm(如果存在)中的一者或两者)包含用于至少一种mmp的底物。在这些实施方案的某些实施方案中,所述mmp选自由mmp9、mmp14、mmp1、mmp3、mmp13、mmp17、mmp11和mmp19组成的组。在具体的实施方案中,存在于所述完整的可活化抗体中的至少一种或多种cm(例如,第
一和第二cm(如果存在)中的一者或两者)包含用于mmp14的底物。在某些实施方案中,所述cm是用于至少一种选自由以下组成的组的蛋白酶的底物:基质金属蛋白酶(mmp)、凝血酶、中性粒细胞弹性蛋白酶、半胱氨酸蛋白酶、豆荚蛋白酶和诸如蛋白裂解酶(mt-sp1)和尿激酶(upa)的丝氨酸蛋白酶。不受理论束缚,据信这些蛋白酶在癌症、炎症或自身免疫中的至少一者中被上调或以其他方式不调节。
[0236]
在一些实施方案中,存在于所述完整的可活化抗体中的至少一种或多种cm(例如,第一和第二cm(如果存在)中的一者或两者)包含氨基酸序列,所述氨基酸序列包含用于至少两种不同蛋白酶(即,至少第一蛋白酶和至少第二蛋白酶)的底物。在这些实施方案中,所述切割位点对于至少两种不同的蛋白酶可以相同或不同。合适的第一和第二蛋白酶包括上文所述蛋白酶中的任何一种。在这些实施方案的某些实施方案中,所述第一蛋白酶选自由mmp、凝血酶、中性粒细胞弹性蛋白酶、半胱氨酸蛋白酶、upa、豆荚蛋白酶和蛋白裂解酶组成的组,并且所述第二蛋白酶选自由上述蛋白酶中任何一种组成的组。在一些实施方案中,所述第一蛋白酶是基质金属蛋白酶(mmp),并且所述第二蛋白酶是丝氨酸蛋白酶(sp)。
[0237]
所述cm可以设计成包含两种或更多种用于至少两种或更多种不同蛋白酶的已知底物,其中所述两种或更多种底物直接或直接地彼此共价串联连接,并且其中所述cm与所述ab偶联。例如,cm可以包含直接或间接共价连接到第二底物的第一底物,其中所述第一底物是用于第一蛋白酶的底物,并且所述第二底物是用于第二蛋白酶的底物,其中所述第一和第二蛋白酶是不同的蛋白酶,并且其中所述cm与所述ab偶联。在一些实施方案中,所述第一底物和所述第二底物各自是长度不超过约25个氨基酸残基、或长度不超过约24个、或不超过约23个、或不超过约22个、或不超过约21个、或不超过约20个、或不超过约19个、或不超过约18个、或不超过约17个、或不超过约15个氨基酸残基的肽。
[0238]
在一些实施方案中,所述完整的可活化抗体包含至少一种用于选自由mmp、凝血酶、中性粒细胞弹性蛋白酶、半胱氨酸蛋白酶、upa、豆荚蛋白酶和蛋白裂解酶组成的组的蛋白酶的底物。在一些实施方案中,所述可活化抗体包含两个前结构域,并且因此包含第一cm和第二cm。在这些实施方案中的某些实施方案中,所述第一cm和所述第二cm包含用于相同蛋白酶的底物。在这些实施方案的一些实施方案中,所述第一cm包含第一底物,并且所述第二cm包含第二底物,其中所述第一底物和所述第二底物是用于两种不同蛋白酶的底物。
[0239]
在某些实施方案中,所述可活化抗体中的至少一个cm(例如,如果第二前结构域存在于所述可活化抗体中,则第一cm和第二cm中的至少一者)包含选自seq id no:1-67组成的组的氨基酸序列。在一些实施方案中,存在于可活化抗体中的每个cm(例如,如果第二前结构域存在于所述可活化抗体中,则第一cm和第二cm两者)独立地包含选自由seq id no:1-67组成的组的氨基酸序列。在这些实施方案的某些实施方案中,存在于所述可活化抗体中的每个cm包含相同的氨基酸序列(例如,如果第二前结构域存在于所述可活化抗体中,则所述第一cm和所述第二cm包含相同的氨基酸序列)。
[0240]
本发明的组合物和工艺中使用的所述可活化抗体的mm组分可以具有多种长度中的任何一种。在一些实施方案中,存在于所述可活化抗体中的每个mm(例如,第一mm;第一mm和第二mm;等)各自是长度不超过约30个氨基酸残基、或长度不超过约29个、或不超过约28个、或不超过约27个、或不超过约26个、或不超过约25个、或不超过约24个、或不超过约23个、或不超过约22个、或不超过约21个、或不超过约20个氨基酸残基的肽。存在的每个mm降
低相应的ab特异性地结合至其各自的生物靶标的能力。
[0241]
所述mm可以以多种方式抑制所述可活化抗体与生物靶标的结合。例如,所述mm可以结合至所述ab,从而抑制所述可活化抗体与所述生物靶标的结合。所述mm可以变构或空间抑制所述可活化抗体与生物靶标的结合。在一些实施方案中,所述mm特异性地结合至所述ab。合适的mm可以使用多种已知技术中的任何一种来鉴定,所述已知技术包括美国专利申请公布第2009/0062142号和第2012/0244154号以及pct公开第wo 2014/026136号中描述的技术,上述公开中的每一个特此通过引用方式以其整体并入。
[0242]
通常,所述可活化抗体针对生物靶标的解离常数(kd)大于相应ab(不存在所述mm)针对所述生物靶标的kd。
[0243]
在一些实施方案中,所述mm减少ab与其生物靶标的结合至少约50%、或至少约60%、或至少约65%、或至少约70%、或至少约75%、或至少约80%、或至少约85%、或至少约90%、或至少约91%、或至少约92%、或至少约93%、或至少约94%、或至少约95%、或至少约96%、或至少约97%、或至少约98%、或至少约99%以及甚至100%,持续至少约2小时、或至少约4小时、或至少约6小时、或至少约8小时、或至少约12小时、或至少约24小时、或至少约28小时、或至少约30小时、或至少约36小时、或至少约48小时、或至少约60小时、或至少约72小时、或至少约84小时、或至少约96小时、或至少约5天、或至少约10天、或至少约15天、或至少约30天、或至少约45天、或至少约60天、或至少约90天、或至少约120天、或至少约150天、或至少约180天、或至少约1个月、或至少约2个月、或至少约3个月、或至少约4个月、或至少约5个月、或至少约6个月、或至少约7个月、或至少约8个月、或至少约9个月、或至少约10个月、或至少约11个月、或至少约12个月或更长时间。说明性的mm包括描述于例如wo 2009/025846、wo 2010/096838、wo 2010/081173、wo 2013/163631、wo 2013/192546、wo 2013/192550、wo 2014/026136、wo 2014/052462、wo 2014/107599、wo 2014/197612、wo 2015/013671、wo 2015/048329、wo 2015/066279、wo 2015/116933、wo 2016/014974、wo 2016/118629、wo 2016/149201、wo 2016/179285、wo 2016/179257、wo 2016/179335、wo 2017/011580、pct/us2017/059740和美国临时申请序列号62/469,429、62/572,467中的那些mm,所述专利中的每一个均通过引用方式以其整体并入本文。
[0244]
本发明的实践中使用的可活化抗体可以含有一种或多种另外的结构元件,诸如,例如一种或多种接头,或可以赋予结构益处的其他氨基酸残基或肽,诸如n末端间隔区氨基酸残基或氨基酸序列等。
[0245]
适合用于本发明的组合物和工艺的可活化抗体中的接头可为多种长度中的任何一种。合适的接头包括具有在以下范围内的长度的那些接头:约1个至约20个氨基酸残基,或约1个至约19个氨基酸残基,或约1个至约18个氨基酸残基,或约1个至约17个氨基酸残基,或约1个至约16个氨基酸残基,或约1个至约15个氨基酸残基,或约2个至约15个氨基酸残基,或约3个至约15个氨基酸残基,或约3个至约14个氨基酸残基,或约3个至约13个氨基酸残基,或约3个至约12个氨基酸残基。在一些实施方案中,所述可活化抗体包含一个或多个接头,所述接头各自独立地包含1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20个氨基酸残基。
[0246]
通常,所述接头是包含一个或多个选自由gly、ser、ala和thr组成的组的氨基酸残基的柔性接头,并且通常,所述接头包含一个或多个选自由gly和ser组成的组的氨基酸残
no:122组成的组的氨基酸序列。
[0249]
另一组的说明性cdr包括一起形成对人pd1具有结合特异性的ab的vl和vh中的那些cdr,其中所述vl包含具有seq id no:123或seq id no:129的氨基酸序列的vl cdr1、具有seq id no:124的氨基酸序列的vl cdr2以及具有seq id no:125的氨基酸序列的vl cdr3,并且所述vh包含具有seq id no:126的氨基酸序列的vh cdr1、具有seq id no:127的氨基酸序列的vh cdr2以及具有seq id no:128的氨基酸序列的vh cdr3。在这些可活化抗体中,所述mm可以包含选自由seq id no:130-280组成的组的氨基酸序列。包含这些cdr的特异性抗pd1可活化抗体包含同一的第一轻链和第二轻链以及同一的第一重链和第二重链,其中所述第一和第二轻链中的每一者都包含同一的第一和第二vl氨基酸序列、同一的第一和第二mm、同一的第一和第二cm以及同一的第一和第二轻链恒定结构域,其中所述第一和第二轻链中的每一者都包含seq id no:281的氨基酸序列,并且其中所述第一和第二重链中的每一者都包含同一的第一和第二vh氨基酸序列以及同一的第一和第二重链恒定结构域,并且其中所述第一和第二重链中的每一者都包含seq id no:282的氨基酸序列。
[0250]
另一组的说明性cdr包括一起形成对人pdl1具有结合特异性的ab的vl和vh中的那些cdr,其中所述vl包含具有seq id no:283的氨基酸序列的vl cdr1、具有seq id no:284的氨基酸序列的vl cdr2以及具有seq id no:285的氨基酸序列的vl cdr3,并且所述vh包含具有seq id no:286的氨基酸序列的vh cdr1、具有seq id no:287的氨基酸序列的vh cdr2以及具有seq id no:288的氨基酸序列的vh cdr3。在这些可活化抗体中,所述mm可以包含选自由seq id no:289-313组成的组的氨基酸序列。包含这些cdr的特异性抗pdl1可活化抗体包含同一的第一轻链和第二轻链以及同一的第一重链和第二重链,其中所述第一和第二轻链中的每一者都包含同一的第一和第二vl氨基酸序列、同一的第一和第二mm、同一的第一和第二cm以及同一的第一和第二轻链恒定结构域,其中所述第一和第二轻链中的每一者都包含seq id no:314的氨基酸序列,并且其中所述第一和第二重链中的每一者都包含同一的第一和第二vh氨基酸序列以及同一的第一和第二重链恒定结构域,并且其中所述第一和第二重链中的每一者都包含seq id no:315的氨基酸序列。
[0251]
在另一个方面,本公开包括用于在组合物生产工艺中通过对包含可活化抗体群体和其经修剪的变体群体的样品组合物进行凝胶毛细管电泳程序,确定或监测可活化抗体及其经修剪的变体的相对量的方法。凝胶毛细管电泳程序可以是还原性sds-cge或非还原性sds-cge。在一个方面,所述方法涉及使用还原性sds-cge程序将完整的编码前结构域的多肽群体与其经修剪的变体群体分离,并通过确定对应于完整的编码前结构域的多肽的峰面积和对应于一种或多种其经修剪的编码前结构域的多肽的峰面积来量化可活化抗体的群体和其经修剪的变体的群体的相对量。在另一个方面,所述方法涉及使用非还原性sds-cge程序将可活化抗体群体与其经修剪的变体群体分离,并通过确定对应于完整的可活化抗体的峰面积及其经修剪的变体的峰面积来量化可活化抗体群体和其经修剪的变体群体的相对量。
[0252]
在一些方面,本文所述的凝胶毛细管电泳方法可以鉴定通过其他色谱法诸如尺寸排阻色谱法(例如,se-hplc)、阴离子交换色谱法或阳离子交换色谱法未观察到的经修剪的变体的存在。
[0253]
因此,在一些方面,本文所述的定量凝胶毛细管电泳方法可用于评估可活化抗体
的产品和工艺质量,例如,用于药物生产工艺中的质量控制监测。在一些方面,所述方法可用于确定包含可活化抗体的纯化组合物是否适合用于制备药物组合物。在一些方面,本公开包括用于制备包含可活化抗体的药物组合物的方法,其包括a)提供包含完整的可活化抗体及其经修剪的变体的纯化组合物,b)通过对样品进行还原性或非还原性sds-cge程序而将完整的可活化抗体物质与其经修剪的变体分离,c)通过确定对应于完整的可活化抗体或完整的编码前结构域的多肽的峰面积和对应于经修剪的抗体或一种或多种其经修剪的含有前结构域的多肽的峰面积,和d)当样品中经修剪的变体的相对量小于阈值时选择经纯化的组合物用于制备药物组合物。在一些方面,所述阈值是3%经修剪的变体。在一些方面,所述阈值为2.5%、2%、1.9%、1.8%、1.7%、1.6%、1.5%、1.4%、1.3%、1.2%、1.1%、1.0%、0.9%、0.8%、0.7%、0.6%、0.5%、0.4%、0.3%或0.2%。
[0254]
在一些方面,本公开提供用于在组合物生产工艺中确定或监测可活化抗体及其经修剪的变体的相对百分比的方法,所述方法包括:
[0255]
a)使包含可活化抗体群体和其经修剪的变体群体的样品组合物经受凝胶毛细管电泳程序;
[0256]
b)在所述凝胶毛细管电泳程序中将可活化抗体群体与其经修剪的变体群体分离;以及
[0257]
c)通过确定对应于完整的含有前结构域的多肽的峰面积和对应于一种或多种其经修剪的含有前结构域的多肽的峰面积来量化可活化抗体群体和其经修剪的变体群体的相对量。
[0258]
在一些方面,样品组合物是表达所述可活化抗体的细胞的细胞收获物组合物。在一些方面,所述样品组合物已经过蛋白亲和色谱。在一些方面,所述样品组合物已经过离子交换色谱。在一些方面,所述样品组合物已经过阴离子交换色谱。在一些方面,所述样品组合物已经过阳离子交换色谱。在一些方面,所述样品组合物已经过疏水作用色谱。在一些方面,所述样品组合物已经过多模式色谱。在一些方面,所述相对百分比是在细胞收获、蛋白亲和色谱、离子交换色谱、疏水作用色谱和多模式色谱中的两个或更多个的每一个后,通过量化可活化抗体群体和其经修剪的变体群体的相对百分比来监测的。在一些方面,步骤a)包括使样品组合物中的可活化抗体及其经修剪的变体与还原剂接触。在一些方面,所述还原剂是二硫赤藓糖醇(dte)、二硫苏糖醇(dtt)、β-巯基乙醇或其组合。在一些方面,步骤a)包括使样品组合物中的可活化抗体及其经修剪的变体与变性剂接触。在一些方面,所述变性剂是十二烷基硫酸钠(sds)。在一些方面,所述方法还包括使用sds蛋白质分子量标准进行凝胶毛细管电泳程序和产生分子量标准校准曲线。在一些方面,步骤c)包括获得含有对应于经受凝胶毛细管电泳程序的可活化抗体及其经修剪的变体各自的峰的电泳图。在一些方面,所述方法还包括对对应于所述可活化抗体及其经修剪的变体各自的每个峰进行峰积分以获得经修剪的编码前结构域的多肽的峰面积和完整的编码前结构域的多肽的峰面积。
[0259]
以下实施例还说明了本发明的实践,但不应解释为以任何方式限制其范围。
[0260]
实施例
[0261]
实施例1
[0262]
分析方法
[0263]
a.总蛋白浓度
[0264]
水性原料和纯化产物的总蛋白浓度是通过uv光谱法确定的。在分离步骤之后立即取出每个洗脱物的样品并冷冻直至用于本文所述的测定,例如总蛋白、sds-cge、se-hplc和hcp elisa测定。将样品在超纯水中连续稀释,并使用uv分光光度计(cary 60uv-可见分光光度计,agilent technologies,inc.)在280nm波长处测量蛋白质吸光度。蛋白质浓度是根据beer-lambert定律在280nm波长下使用基于氨基酸序列计算的摩尔消光系数确定的。参见,例如,pace等人,protein science(1995)4:2411。
[0265]
总蛋白产率计算如下:
[0266][0267]
b.通过十二烷基硫酸钠-还原性凝胶毛细管电泳(sds-cge)进行可活化抗体的定量
[0268]
可活化抗体组合物的纯度(完整的可活化抗体%)使用十二烷基硫酸钠-毛细管凝胶电泳(sds-cge)方法和紫外光电二极管阵列(pda)检测(pa 800plus pharmaceutical analysis system,beckman coulter,inc.,brea,ca)来确定。使用0.5m 1,4-二硫赤藓糖醇(sigma aldrich,目录号d8255-5g)还原含有可活化抗体的样品,然后在十二烷基硫酸钠(sds)存在下进行热变性。变性后,所述样品都是通过含有sds聚合物基质的毛细管中按大小分离,其为电泳分离提供筛分选择性。
[0269]
igg纯度和异质性的测定是如制造商说明手册中所述,按照制造商的说明使用包括sds蛋白质分级标准品、缓冲剂和来自sciex的igg纯度和异质性测定试剂盒中提供的部分的试剂运行。
[0270]
分子量标准校准曲线是根据制造商的说明生成。进行峰积分并检查电泳图以鉴定多肽峰。对应于经修剪的编码前结构域的多肽的峰出现在预期的完整的编码前结构域的多肽峰之前。
[0271]
完整的可活化抗体百分比(即,完整的可活化抗体%或“纯度”)和经修剪的杂质百分比确定如下:
[0272][0273][0274]
其中:
[0275][0276][0277]
c.通过尺寸排阻高效液相色谱法(se-hplc)进行hmws的量化
[0278]
尺寸排阻高效液相色谱法(se-hplc)用于定量本文所述组合物中hmws的量。
[0279]
在超纯水中制备含有200mm k2po4和150mm kcl的流动相(ph 6.8
±
0.1)。在配有自
动进样器(dionex u3000 hplc,ultimate
tm wps-3000tbrs恒温生物相容性自动进样器,thermofisher scientific)及柱的hplc系统上进行分析:分析柱(tskgel g3000swxl,目录号08541,tosoh bioscience llc)、保护柱(tskgel guard swxl,6mm
×
40mm,目录号08543,tosoh bioscience llc)和烧结预柱(0.5μm预柱釉料,upchurch scientific,目录号a-318)。在样品分析之前,用流速为0.5ml/min的流动相平衡柱。用去离子水或更高级别的水将用于分析的样品根据需要稀释至1mg/ml的目标浓度。参考材料是相应的单体可活化抗体(即,非聚集的活化抗体)。如有必要,用磷酸盐缓冲盐水(pbs)将参考材料稀释至1mg/ml的目标浓度。
[0280]
对于uv检测,样品分析是在220nm(4nm带宽)和280nm(4nm带宽)的波长下进行;柱温箱环境温度;自动进样器中样品温度5℃
±
3℃;流速为0.5ml/min;以及运行时间30min/样品。在进样参考材料之前,在每个系列的样品开始时进行配制缓冲空白进样。进样20μg参考材料,然后进样40μg测试样品。在每个系列的测试样品的每个进样系列后进样20μg参考材料。
[0281]
使用chromeleon 7cds(thermo scientific)中的smart cobra wizard整合测试样品的色谱图。在主(参考材料)峰的右侧检测到低分子量物质(lmws)。在主峰的左侧检测到一个或多个对应于高分子量物质(hmws)的峰。基于色谱图中所有峰的所有峰面积之和(总峰面积)计算相对峰面积百分比。将观察到的每个hmws峰的峰面积相加,并将该总和除以总峰面积并乘以100以生成对应于hmws的峰面积百分比(即,hmws%)。
[0282]
d.宿主细胞蛋白(hcp)
[0283]
根据制造商的说明(cho hcp elisa试剂盒,(f550),cygnus technologies,inc.),使用市场上可商购的hcp elisa试剂盒确定hcp的定量(以ppm(ng/ml产物)为单位)。
[0284]
实施例2
[0285]
比较例:阳离子交换色谱法
[0286]
作为纯化包含完整的可活化抗-cd166抗体和相应的经修剪的杂质的水性原料的方法,对阳离子交换色谱法进行评估。所述水性原料的经修剪的杂质百分比大于7.5%。所述水性原料包含》98%的单体。抗cd166可活化抗体具有两条轻链和两条重链。每条轻链编码mm、cm、vl和恒定区,并且各具有seq id no:120的氨基酸序列。每条重链编码vh和恒定区,并且各具有seq id no:121的氨基酸序列。每对重链和轻链的vh和vl在未被掩蔽时一起形成能够结合人cd166的fab。如实施例1a中所述,通过在280nm的波长处的吸光度所确定,所述水性原料具有10mg/ml的总蛋白质负载。通过用平衡缓冲液进行1:10稀释,将所述水性原料调节至ph 5.0,并加载到阳离子交换树脂(capto s impact,ge lifesciences)。通过将第一缓冲液(25mm naoac,500mm nacl,ph 5.0(80cv梯度))混合到第二缓冲液(25mm naoac,25mm nacl,ph 5.0)中,用ph 5的nacl梯度洗脱柱。收集1ml级分。在色谱图中观察到单峰,从中收集1ml级分并通过还原性sds-cge进行分析。图5显示了得到的色谱图(线“a”代表280nm处的吸光度)。结果表明,完整的可活化抗体和经修剪的杂质都存在,但没有实现(峰)分离。因此,阳离子交换色谱法不会导致完整的可活化抗体与经修剪的变体的有效分离。
[0287]
实施例3
[0288]
可活化抗体的纯化组合物的制备
[0289]
使用本发明的疏水色谱工艺处理包含与实施例2中所述相同的抗cd166可活化抗体的水性原料。
[0290]
对包含完整的可活化抗体和经修剪的杂质的生物反应器收获物上清液进行蛋白a亲和色谱步骤,然后进行病毒灭活步骤和阴离子交换色谱(阴离子iex)步骤。这些工艺没有导致完整的可活化抗体与经修剪的变体的有效分离。图4a描绘了来自蛋白a亲和色谱步骤的洗脱物样品的sds-cge分析结果。观察到包含经修剪的变体的显著峰(峰1,“经修剪的lc”)。图4b描绘了来自阴离子iex步骤的洗脱物样品的sds-cge分析结果。观察到包含经修剪的变体的显著峰(峰1,“经修剪的lc”),并且经修剪的变体的峰面积与来自早期蛋白a色谱步骤的洗脱物相比没有减少。收集来自阴离子iex步骤的产物用于在疏水色谱工艺中进一步处理,所述工艺使用加载有疏水作用色谱固定相的色谱柱(即,疏水作用色谱(hic)柱)。
[0291]
hic柱是使用capto
tm phenyl impres(ge healthcare)作为树脂(即,固定相)以结合-洗脱模式进行。该树脂是基于琼脂糖的具有含苯基的配体的树脂。水性原料是通过使用含有20mm 2-(n-吗啉代)乙磺酸(mes)和1.5m硫酸铵(nh4)2so4(ph 6)的缓冲液处理从阴离子iex步骤收集的产物来制备。将水性原料分成两个等分试样“等分试样1”和“等分试样2”,分别在两个循环“循环1”和“循环2”中通过疏水作用色谱柱进行处理。将包括柱和缓冲液在内的色谱设备放置在保持在22℃
±
1℃的温度柜中。
[0292]
在两个循环中将两个等分试样加载到柱上。将循环1的上样密度设置为最大值20mg/ml(树脂),将循环2设置为16mg/ml(树脂)。使用含有20mm mes和0.26m硫酸铵的缓冲液(ph 6.0)洗脱柱。削峰标准(2mm路径长度的uv池)设置为50mau向上拐点和600mau向下拐点。收集洗脱物并用1m naoh溶液清洗柱。总蛋白浓度是如实施例1中所述通过uv吸光度来确定,并且总蛋白产率是基于水性原料和洗脱物的体积和蛋白质浓度来计算。疏水色谱工艺步骤的总蛋白质产率在下表1中提供。
[0293]
表1.疏水色谱工艺(hic)
[0294][0295]
如实施例1中所述,通过还原sds-cge测定法确定完整可活化抗体和截短杂质的相对量。完整可活化抗体%和截短杂质%的计算基于轻链进行编码前结构域的多肽。
[0296]
下面的表2中提供了疏水色谱工艺步骤的工艺性能指标的总结。
[0297]
表2.疏水色谱步骤-工艺性能
[0298][0299]
阴离子iex步骤(紧邻疏水色谱步骤的上游)似乎对减少中间组合物中经修剪的杂质量没有可测量的影响。参见图4a和图4b。相比之下,疏水色谱工艺步骤(使用hic柱)对去除经修剪的杂质具有显著影响。参见图4c,其描绘了来自疏水色谱步骤的洗脱物样品的sds-cge分析结果。在图4c中没有观察到对应于经修剪的变体的峰。如与水性原料中经修剪的物质量相比,洗脱物中经修剪的物质量表明疏水色谱工艺可有效地将工艺流中经修剪的杂质量减少约8至9.6倍。对于两个循环,每个洗脱物中经修剪的杂质的残留水平显著低于水性原料中存在的水平。如通过还原性sds-cge所测量,两个循环的洗脱物中的纯度水平(完整的可活化抗体%)保持高水平,所述洗脱物中残留的经修剪的杂质水平低于1%经修剪的杂质。
[0300]
所述水性原料和洗脱物组合物中的宿主细胞蛋白水平是使用实施例1中描述的hcp elisa分析方法表征的。结果显示在下表3中。hcp的量以ppm报告(即,以ng/ml表示的hcp(如通过相应的hcp elisa所确定)除以以mg/ml表示的产物浓度(如通过实施例1a中所述280nm波长处的吸光度所确定))。
[0301]
表3.宿主细胞蛋白的定量
[0302][0303]
使用hic固定相的疏水色谱工艺步骤可有效地将工艺流中的hcp水平减少约7倍或更多。洗脱物中的hcp残留水平小于原料水平的约15%。
[0304]
原料和洗脱物中的hmws水平也是使用实施例1中描述的se-hplc测定法评估的。结果显示在下表4中。
[0305]
表4.hmws的定量
[0306][0307]
结果表明,该工艺可有效地从工艺流中去除85%或更多的hmws。所得洗脱物组合物含有的hmws小于水性原料中存在的hmws的约15%(循环1)和10%(循环2)。
[0308]
洗脱物(纯化)组合物中完整的可活化抗体、经修剪的杂质、hcp和hmws的相对量的总结在下表5中提供。
[0309]
表5.纯化的组合物
[0310][0311]
*基于对应于总轻链(完整的和经修剪的)的峰面积%,如实施例1中所述通过sds-cge所确定。
[0312]
**如实施例1中所述通过se-hplc所确定。
[0313]
实现了经修剪的杂质和完整的可活化抗体之间的峰分离,并导致这些具有非常相似的分子量和氨基酸序列的物质成功分离。结果表明,疏水色谱工艺步骤在生成相对于完整的可活化抗体而言为高纯度且经修剪的杂质、hcp和hmws残留水平低的组合物方面非常有效。
[0314]
实施例4
[0315]
可活化抗pd1抗体的纯化组合物的制备
[0316]
将包含由从两次生物反应器运行(50l规模(“运行1”)和1,000l规模(“运行2”))生产抗pd1可活化抗体的培养产物纯化以去除包括经修剪的杂质在内的各种杂质。抗pd1可活化抗体具有两条轻链和两条重链,每条轻链编码mm、cm、vl和恒定区并且各具有seq id no:281的氨基酸序列,每条重链编码vh和恒定区并且各具有seq id no:282的氨基酸序列。每个vh和vl一起形成当未被掩蔽时能够结合靶标人pd1的fab。
[0317]
每个生物反应器运行的下游纯化工艺是相似的。对包含所述可活化抗pd1抗体产物的生物反应器收获物上清液进行基于蛋白a的亲和色谱步骤,然后进行病毒灭活步骤和阴离子交换色谱(阴离子iex)步骤。这些工艺没有导致完整的可活化抗体与经修剪的变体
的有效分离。收集产物用于在hic柱中进一步处理。使用20mm mes和1.8m硫酸铵(ph 6.0),将运行1的阴离子iex步骤的产物电导率调整至127.0
±
13ms/cm,运行2的产物电导率则调整至126ms/cm
±
13。将产物分成等分试样,根据hic柱的负载能力对其分级。随后将每个等分试样(水性原料)加载到在22
±
1℃的温度下以结合/洗脱(b/e)模式操作的hic柱(capto
tm phenyl impres,ge healthcare)上。用20mm mes、0.4m硫酸铵(ph 6.0)的水溶液洗脱柱。收集洗脱物并用0.01m naoh溶液汽提柱。
[0318]
总蛋白浓度是如实施例1中所述通过uv吸光度来确定,并且总蛋白产率是基于水性原料和洗脱物的体积和蛋白质浓度来计算。应用于hic柱的每个等分试样的总蛋白产率列于下表6中。
[0319]
表6.疏水色谱工艺(hic),总蛋白产率
[0320][0321]
结果表明,两次运行的总蛋白产率都相对较高。
[0322]
完整的可活化抗体和经修剪的杂质的相对量是如实施例1中所述通过还原性sds-cge测定法确定的。完整的可活化抗体%和经修剪的杂质%的计算是基于轻链进行的,所述轻链是编码前结构域的多肽。
[0323]
运行1和运行2的疏水色谱工艺步骤的工艺性能指标的总结分别提供在下表7a和7b中。
[0324]
表7a.疏水色谱步骤-工艺性能,运行1
[0325][0326][0327]
表7b.疏水色谱步骤-工艺性能,运行2
[0328][0329]
如在实施例3中描述的工艺方案中,疏水色谱步骤上游的阴离子iex步骤似乎对减少中间组合物的经修剪的杂质的量没有可检测的影响。相比之下,疏水色谱工艺步骤在减少工艺流中经修剪的杂质的数量方面非常有效。还使用实施例1中描述的hcp elisa测定法分析中间组合物的hcp存在。结果显示在表8a(运行1)和表8b(运行2)中。
[0330]
表8a.宿主细胞蛋白的定量(运行1)
[0331][0332][0333]
表8b.宿主细胞蛋白的定量(运行2)
[0334][0335]
结果表明疏水色谱工艺步骤在将工艺流中的hcp量减少至少4倍方面是有效的。
[0336]
还使用实施例1中描述的se-hplc测定法评估了水性原料和洗脱物样品中的hmws水平。hmws定量结果提供在表9a(运行1)和9b(运行2)中。
[0337]
表9a.hmws的定量(运行1)
[0338][0339]
表9b.hmws的定量(运行2)
[0340][0341][0342]
结果表明疏水色谱工艺在降低工艺流中的hmws水平方面非常有效。
[0343]
下表10a(运行1)和表10b(运行2)中提供了通过本发明的疏水色谱工艺产生的纯化组合物中完整的可活化抗体、经修剪的杂质、hcp和hmws的相对量的总结。
[0344]
表10a.纯化的组合物,运行1(50l)
[0345][0346]
*基于对应于总轻链(完整的和经修剪的)的峰面积%,如实施例1中所述通过sds-cge所确定。
[0347]
**如实施例1中所述通过se-hplc所确定。
[0348]
表10b.纯化的组合物,运行2(1000l)
[0349][0350]
*基于对应于总轻链(完整的和经修剪的)的峰面积%,如实施例1中所述通过sds-cge所确定。
[0351]
**如实施例1中所述通过se-hplc所确定。
[0352]
结果表明,本发明的疏水色谱方法,在这种情况下使用hic柱成功地从工艺流中去除经修剪的物质、hcp和hmws,从而产生完整的可活化抗体的高纯度组合物。
[0353]
实施例5
[0354]
抗pdl1可活化抗体的纯化组合物的制备
[0355]
使用本发明的疏水色谱方法处理包含抗pdl1可活化抗体的培养产物以去除各种杂质。抗pdl1可活化抗体具有两条轻链和两条重链,每条轻链编码mm、cm、vl和恒定区并且各具有seq id no:314的氨基酸序列,每条重链编码vh和恒定区并且各具有seq id no:315的氨基酸序列。每个vh和vl一起形成当未被掩蔽时能够结合靶标人pdl1的fab。
[0356]
对包含完整的可活化抗体和经修剪的杂质的生物反应器收获物上清液进行蛋白a亲和色谱步骤,然后进行病毒灭活步骤和阴离子iex步骤。这些工艺没有导致完整的可活化抗体与经修剪的变体的有效分离。收集来自阴离子iex步骤的产物,用于在疏水色谱工艺中进一步处理,所述工艺使用加载有多模式色谱固定相的色谱柱(即,多模式色谱(mmc)柱)。
[0357]
mmc柱是使用capto
tm mmc impres(ge healthcare)作为树脂(即,具有n-苯甲酰基-高半胱氨酸配体的固定相)在22
±
4℃的温度下以结合-洗脱模式进行。
[0358]
中间产物组合物(ph 5.9)用25mm mes、30mm nacl调节,然后分成两等份(水性原料)并在两个循环中处理。每次运行的上样密度为30mg/ml
树脂
。洗涤柱,然后用ph 5.9的25mm mes、30mm nacl、90mm盐酸精氨酸洗脱。收集洗脱物并用1m naoh溶液清洗柱。
[0359]
总蛋白浓度是如实施例1中所述通过uv吸光度来确定,并且总蛋白产率是基于水性原料和洗脱物的体积和蛋白质浓度来计算。疏水色谱工艺步骤的总蛋白质产率在下表11中提供。
[0360]
表11.疏水色谱工艺(mmc)
[0361][0362]
结果表明,该工艺获得了相对较高的总蛋白产率。
[0363]
完整的可活化抗体和经修剪的杂质的相对量是如实施例1所述通过还原性sds-cge确定的。结果总结在表12中。
[0364]
表12.使用mmc的疏水色谱步骤
–
工艺性能
[0365][0366]
结果表明,疏水色谱工艺的实施,在这种情况下,使用mmc柱有效地从工艺流中去除了大于85%的经修剪的杂质,导致该杂质减少了大于8倍。在两个洗脱物样品中,完整的可活化抗体的水平(纯度)高,均大于98%。相比之下,阴离子iex步骤在降低工艺流中截断的杂质水平方面似乎没有效果。
[0367]
还分析了mmc原料和洗脱物组合物中是否存在hcp。结果示于表13中。
[0368]
表13.宿主细胞蛋白的定量
[0369][0370]
结果表明,使用mmc色谱柱的疏水色谱步骤可有效地减少mmc原料组成中的hcp量,对于等分试样1减少了大于6倍(大于84%),对于等分试样2减少了大于11倍(大于90%)。对于等分试样1和2,洗脱物中hcp的残留量分别小于原料水平的16%和约9%。
[0371]
还使用实施例1中描述的se-hplc测定法评估原料和洗脱物样品中的hmws量。hmws定量结果提供在下表14中。
[0372]
表14.hmws的定量
[0373][0374]
结果表明,疏水色谱工艺步骤,在这种情况下使用mmc柱在从工艺流中去除大部分hmws方面非常有效。
[0375]
下表15中提供了通过本发明的疏水色谱工艺产生的纯化组合物中完整的可活化
抗体、经修剪的杂质、hcp和hmws的相对量的总结。
[0376]
表15.纯化组合物
[0377][0378]
*基于对应于总轻链(完整的和经修剪的)的峰面积%,如实施例1中所述通过sds-cge所确定。
[0379]
**如实施例1中所述通过se-hplc所确定。
[0380]
结果表明,疏水色谱工艺步骤在生成相对于完整的可活化抗体而言相对较纯且经修剪的杂质、hcp和hmws(如果全部存在)残留水平低的组合物方面非常有效。
[0381]
实施例6
[0382]
从具有高水平经修剪的杂质的水性原料制备可活化抗pdl1抗体的纯化组合物
[0383]
a.水性原料:3.1%经修剪的杂质
[0384]
将包含实施例5中描述的抗pdl1抗体的水性原料加载到mmc柱上。水性原料的组成包括3.1%的经修剪的杂质和大于98%的单体形式的可活化抗体(即,小于2%的hmws)。
[0385]
mmc柱是使用capto
tm mmc impres(ge healthcare)作为树脂(即,具有n-苯甲酰基-高半胱氨酸配体的固定相)在22
±
4℃的温度下以结合-洗脱模式进行。水性原料用25mm mes、30mm nacl(ph 6)调节。用ph 6的25mm mes、30mm nacl、20mm盐酸精氨酸洗涤柱,然后用ph 6的25mm mes、30mm nacl、90mm盐酸精氨酸洗脱。用1m naoh溶液清洗柱。
[0386]
总蛋白浓度是如实施例1中所述通过uv吸光度来确定,并且总蛋白产率是基于水性原料和洗脱物的体积和蛋白质浓度来计算。所得洗脱物中经修剪的杂质的水平降低了大于7.5倍,使得水性原料中少于约13%的经修剪的杂质保留在洗脱物中。单体可活化抗体的量保持在大于98%。总蛋白产率大于65%。
[0387]
b.水性原料:13.5%经修剪的杂质
[0388]
将包含实施例5中描述的抗pdl1抗体的水性原料加载到mmc柱上(加载有capto
tm impres树脂(ge healthcare),并如上文a部分所述进行处理。水性原料的组成包括13.5%经修剪的杂质和大于96.8%单体形式的可活化抗体(即,大于3% hmws)。所得洗脱物中经修剪的杂质水平降低了大于7倍(小于水性原料中经修剪的杂质的14%),并且单体可活化抗体的量大于98%(即,小于2% hmws)。总蛋白产率大于65%。
[0389]
这些实验的结果表明,疏水色谱工艺可以用于纯化具有相对高的经修剪的杂质负载的水性原料。疏水色谱工艺导致组合物基本上不含经修剪的杂质。
[0390]
序列表示于下表16中。
[0391]
表16.氨基酸序列
[0392][0393]
[0394]
[0395]
[0396]
[0397]
[0398]
[0399]
[0400]
[0401][0402]
[0403]
本发明的方面
[0404]
以下是本文描述的本发明的非限制性方面:
[0405]
1.一种用于生产完整的可活化抗体的纯化组合物的工艺,所述工艺包括:
[0406]
(a)将包含水、完整的可活化抗体、经修剪的杂质和第一盐的水性原料加载到色谱柱上,
[0407]
其中所述色谱柱包括固定相,所述固定相包含支持基质和与其结合的配体,
[0408]
其中所述配体包含疏水取代基,并且
[0409]
其中所述完整的可活化抗体包含(i)对第一生物靶标具有特异性结合亲和力的至少第一抗原结合结构域(ab),和(ii)第一前结构域,
[0410]
其中所述至少第一ab包含第一抗体轻链可变结构域(vl)和第一抗体重链可变结构域(vh),
[0411]
其中所述第一前结构域包含第一掩蔽部分(mm)和第一可切割部分(cm),并且
[0412]
其中所述第一ab与所述第一前结构域偶联;和
[0413]
(b)用包含水和第二盐的洗脱液洗脱所述色谱柱以产生包含纯化组合物的洗脱物,所述纯化组合物包含完整的可活化抗体,
[0414]
其中所述洗脱物基本上不含所述经修剪的杂质。
[0415]
2.如方面1所述的工艺,其中所述洗脱步骤(b)是在等度条件下进行。
[0416]
3.如方面1-2中任一项所述的工艺,其中在步骤(b)之后,所述工艺还包括柱清洗步骤,所述柱清洗步骤包括用清洗剂清洗所述色谱柱,并且其中所述工艺不包括所述清洗步骤之前洗脱结合的经修剪的杂质的步骤。
[0417]
4.如方面1-3中任一项所述的工艺,其中所述第一盐和所述第二盐各自独立地包含选自由po
43-、so
42-、oh-、hpo
42-、ch3coo-、柠檬酸根离子、氨基酸阴离子、f-、cl-、br-、h2po
4-、i-、no
3-、clo
4-和scn-组成的组的阴离子。
[0418]
5.如方面1-4中任一项所述的工艺,其中所述第一盐和所述第二盐各自独立地包含选自由n(ch3)
4+
、nh
4+
、cs
+
、rb
+
、k
+
、na
+
、h
+
、ca
+
、mg
2+
、al
3+
和氨基酸阳离子组成的组的阳离子。
[0419]
6.如方面1-5中任一项所述的工艺,其中所述配体包含一个或多个选自由直链烷基取代基、支化烷基取代基和芳基取代基组成的组的疏水取代基。
[0420]
7.如方面1-6中任一项所述的工艺,其中所述配体包含c4至c
10
烷基取代基。
[0421]
8.如方面1-7中任一项所述的工艺,其中所述配体包含支化烷基取代基。
[0422]
9.如方面1-8中任一项所述的工艺,其中所述配体包含芳基取代基。
[0423]
10.如方面9所述的工艺,其中所述芳基取代基是苯基。
[0424]
11.如方面1-10中任一项所述的工艺,其中所述固定相是疏水作用色谱(hic)固定相。
[0425]
12.如方面11所述的工艺,其中所述第一盐和所述第二盐各自独立地包含选自由po
43-、so
42-、oh-、hpo
42-、f-、ch3coo-、柠檬酸根离子、氨基酸阴离子和cl-组成的组的阴离子。
[0426]
13.如方面11-12中任一项所述的工艺,其中所述第一盐和第二盐各自独立地包含选自由po
43-、so
42-和hpo
42-组成的组的阴离子。
[0427]
14.如方面11-13中任一项所述的工艺,其中所述第一盐和第二盐各自独立地包含
选自由n(ch3)
4+
、nh
4+
、cs
+
、rb
+
、k
+
、na
+
、h
+
、ca
+
、mg
2+
、al
3+
和氨基酸阳离子组成的组的阳离子。
[0428]
15.如方面11-14中任一项所述的工艺,其中所述第一盐和第二盐各自独立地包含选自由nh
4+
、k
+
、na
+
、li
+
和mg
2+
组成的组的阳离子。
[0429]
16.如方面11-15中任一项所述的工艺,其中所述第一盐和第二盐各自独立地包含选自由nh
4+
、k
+
和na
+
组成的组的阳离子。
[0430]
17.如方面11-16中任一项所述的工艺,其中所述第一盐和第二盐各自独立地包含选自由nh
4+
、k
+
和na
+
组成的组的阳离子和选自由po
43-、so
42-、oh-、hpo
42-、ch3coo-、柠檬酸根离子、f-、cl-、br-、h2po
4-、i-、no
3-、clo
4-和scn-组成的组的阴离子。
[0431]
18.如方面11-17中任一项所述的工艺,其中所述第一盐和第二盐各自独立地选自由(nh4)2so4、na2so4、na3po4、k3po4、nacl、kcl和ch3coonh4组成的组。
[0432]
19.如方面11-18中任一项所述的工艺,其中所述第一盐和第二盐各自独立地选自由(nh4)2so4、na2so4、na3po4和k3po4组成的组。
[0433]
20.如方面11-19中任一项所述的工艺,其中所述第一盐和第二盐各自独立地选自由(nh4)2so4和na2so4组成的组。
[0434]
21.如方面11-20中任一项所述的工艺,其中所述第一盐和所述第二盐是相同的盐。
[0435]
22.如方面11-20中任一项所述的工艺,其中所述第一盐和所述第二盐是不同的盐。
[0436]
23.如方面11-22中任一项所述的工艺,其中所述水性原料和洗脱液分别包含第一盐浓度和第二盐浓度,并且其中所述第一盐浓度大于所述第二盐浓度。
[0437]
24.如方面1-10中任一项所述的工艺,其中所述固定相是多模式色谱(mmc)固定相,其中所述配体还包含至少一个其他的取代基,所述其他的取代基基于除疏水性之外的相互作用促进分离。
[0438]
25.如方面24所述的工艺,其中所述至少一个其他的取代基基于选自由静电、氢键合和亲硫性组成的组的相互作用促进分离。
[0439]
26.如方面24-25中任一项所述的工艺,其中所述至少一个其他的取代基是选自由硫化物取代基、羧基取代基和胺取代基组成的组。
[0440]
27.如方面24-26中任一项所述的工艺,其中所述至少一个其他的取代基包括羧基取代基。
[0441]
28.如方面24-27中任一项所述的工艺,其中所述至少一个其他的取代基包括胺取代基。
[0442]
29.如方面24-28中任一项所述的工艺,其中所述至少一个其他的取代基包括硫化物取代基。
[0443]
30.如方面24-29中任一项所述的工艺,其中所述第一盐和所述第二盐各自独立地包含选自由cl-、br-、h2po
4-、i-、no
3-、氨基酸阴离子、clo
4-和scn-组成的组的阴离子。
[0444]
31.如方面24-30中任一项所述的工艺,其中所述第一盐和第二盐各自独立地包含选自由n(ch3)
4+
、nh
4+
、ba
+
、ca
2+
、mg
2+
、cs
+
、rb
+
、k
+
、na
+
和氨基酸阳离子组成的组的阳离子。
[0445]
32.如方面24-31中任一项所述的工艺,其中所述第一盐和第二盐中的至少一个是氨基酸阳离子。
[0446]
33.如方面32所述的工艺,其中所述氨基酸阳离子是精氨酸阳离子。
[0447]
34.如方面24-33中任一项所述的工艺,其中所述第一盐和所述第二盐是相同的。
[0448]
35.如方面24-33中任一项所述的工艺,其中所述第一盐和所述第二盐是不同的。
[0449]
36.如方面24-31中任一项所述的工艺,其中所述第一盐是na+阳离子,并且所述第二盐包含na+阳离子和精氨酸阳离子。
[0450]
37.如方面24-36中任一项所述的工艺,其中所述水性原料和洗脱物分别包含第一盐浓度和第二盐浓度,并且其中所述第二盐浓度大于所述第一盐浓度。
[0451]
38.如方面37所述的工艺,其中所述第二盐浓度大于所述第一盐浓度至少2倍。
[0452]
39.如方面37所述的工艺,其中所述第二盐浓度大于所述第一盐浓度至少3倍。
[0453]
40.如方面36或37所述的工艺,其中所述第二盐中na+阳离子的浓度与所述第一盐中na+阳离子的浓度相同,并且其中所述第二盐还包含所述第一盐中不存在的精氨酸阳离子。
[0454]
41.如方面11-20中任一项所述的工艺,其中所述第一盐和第二盐是相同的,并且选自由(nh4)2so4和na2so4组成的组。
[0455]
42.如方面23或41所述的工艺,其中所述第一盐浓度大于所述第二盐浓度至少2倍。
[0456]
43.如方面23或41所述的工艺,其中所述第一盐浓度大于所述第二盐浓度至少3倍。
[0457]
44.如方面1-43中任一项所述的工艺,其中所述水性原料包括在约5.0至约8.0、或约5.0至约7.5、或约5.0至约7.0、或约5.5至约6.5的范围内的ph值。
[0458]
45.如方面1-44中任一项所述的工艺,其中所述水性原料的ph大于所述洗脱液的ph。
[0459]
46.如方面1-44中任一项所述的工艺,其中所述水性原料的ph小于所述洗脱液的ph。
[0460]
47.如方面1-44中任一项所述的工艺,其中所述水性原料的ph与所述洗脱液的ph大致相同。
[0461]
48.如方面47所述的工艺,其中所述水性原料的ph和所述洗脱液的ph为约5.5至约6.5。
[0462]
49.如方面47所述的工艺,其中所述水性原料的ph和所述洗脱液的ph为约5.8至约6.2。
[0463]
50.如方面11所述的工艺,其中所述第一盐和第二盐单独地选自由(nh4)2so4和na2so4组成的组,并且其中所述水性原料的ph和所述洗脱液的ph为约5.5至约6.5。
[0464]
51.如方面50所述的工艺,其中所述第一盐浓度为约1.0至2.0m,并且其中所述第二盐浓度为约0.2至约0.6m。
[0465]
52.如方面50所述的工艺,其中所述第一盐浓度大于所述第二盐浓度至少两倍、至少三倍、至少四倍或至少五倍。
[0466]
53.如方面24所述的工艺,其中所述第一盐是nacl,并且所述第二盐是nacl和盐酸精氨酸,并且其中所述水性原料的ph和所述洗脱液的ph为约5.5至约6.5。
[0467]
54.如方面53所述的工艺,其中所述第一盐浓度为约30mm nacl,并且所述第二盐
浓度为约30mm nacl和约90mm盐酸精氨酸。
[0468]
55.如方面53所述的工艺,其中所述第二盐浓度大于所述第一盐浓度至少两倍、至少三倍、至少四倍或至少五倍。
[0469]
56.如方面1-55中任一项所述的工艺,其中步骤(a)和(b)是在约3℃至约40℃的范围内、或在约10℃至约30℃的范围内、或在约15℃至约30℃的范围内、或在约22℃
±
4℃的范围内的温度下进行。
[0470]
57.如方面56所述的工艺,其中步骤(a)和(b)是在22℃
±
4℃的温度下进行。
[0471]
58.如方面1-57中任一项所述的工艺,其中如通过280nm波长处的吸光度所确定,所述工艺得到至少约70%、或至少约71%、或至少约72%、或至少约73%、或至少约74%、或至少约75%、或至少约76%、或至少约77%、或至少约78%、或至少约79%、或至少约80%、或至少约81%、或至少约82%、或至少约83%、或至少约84%、或至少约85%、或至少约86%、或至少约87%、或至少约88%、或至少约89%、或至少约90%、或至少约91%、或至少约92%、或至少约93%、或至少约94%、或至少约95%的总蛋白产率。
[0472]
59.如方面1-58中任一项所述的工艺,其中如通过还原性sds-cge所确定,基于经修剪的杂质百分比,所述水性原料中经修剪的杂质量与所述洗脱物中经修剪的杂质量的比率为至少约2、或至少约3、或至少约4、或至少约5、或至少约6、或至少约7、或至少约8、或至少约9、或至少约10、或至少约15、或至少约20。
[0473]
60.如方面1-59中任一项所述的工艺,其中如通过还原性sds-cge所确定,所述洗脱物包含经修剪的杂质相对量为所述水性原料中存在的经修剪的杂质的小于约小于约15%、或小于约14%、或小于约13%、或小于约12%、或小于约11%、或小于约10%、或小于约10%、或小于约9%、或小于约8%、或小于约7%、或小于约6%。
[0474]
61.如方面60所述的工艺,其中如通过还原性sds-cge所确定,所述洗脱物包含小于约5%、或小于约4%、或小于约3%、或小于约2%、或小于约1%、或小于约0.9%、或小于约0.8%、或小于约0.7%、或小于约0.6%、或小于约0.5%的经修剪的杂质。
[0475]
62.如方面61所述的工艺,其中如通过还原性sds-cge所确定,所述洗脱物包含小于约2%、或小于约1%、或小于约0.9%、或小于约0.8%、或小于约0.7%、或小于约0.6%、或小于约0.5%的经修剪的杂质。
[0476]
63.如方面1-62中任一项所述的工艺,其中如通过还原性sds-cge所确定,所述洗脱物包含经修剪的杂质的相对量在约0.1%至约15%经修剪的杂质,或约0.1%至约10%经修剪的杂质,或约0.1%至约10%经修剪的杂质,或约0.1%至约5%经修剪的杂质,或约0.1%至约4%经修剪的杂质,或约0.1%至约3%经修剪的杂质,或约0.1%至约2%经修剪的杂质,或约0.1%至约1%经修剪的杂质的范围内。
[0477]
64.如方面1-62中任一项所述的工艺,其中如通过还原性sds-cge所确定,所述洗脱物不包含可检测的经修剪的杂质。
[0478]
65.如方面1-64中任一项所述的工艺,其中所述水性原料和所述洗脱物各自独立地包含选自由mes、mops或hepes组成的组的缓冲剂。
[0479]
66.如方面59-64中任一项所述的工艺,其中所述第一ab包含抗体轻链和抗体重链,并且其中第一前结构域通过肽键与所述第一ab的抗体轻链偶联,并且其中如通过还原性sds-cge所确定,所述经修剪的杂质的相对量是基于所述轻链经修剪的变体和所述完整
的可活化抗体的轻链来确定。
[0480]
67.如方面1-64中任一项所述的工艺,其中所述第一前结构域通过肽键与所述第一ab偶联。
[0481]
68.如方面1-67中任一项所述的工艺,其中所述水性原料还包含选自由宿主细胞蛋白(hcp)和高分子量物质(hmws)组成的组的杂质。
[0482]
69.如方面68所述的工艺,其中所述水性原料还包含hcp。
[0483]
70.如方面69所述的工艺,其中如通过相应的hcp elisa测定法所确定,以ppm计所述水性原料中hcp的量与所述洗脱物中hcp的量的比率为至少约2、或至少约3、或至少约4、或至少约5、或至少约6、或至少约7、或至少约8、或至少约9、或至少约10。
[0484]
71.如方面69-70中任一项所述的工艺,其中如通过相应的hcp elisa所测量,所述洗脱物包含小于约150ppm、或小于约140ppm、或小于约130ppm、或小于约120ppm、或小于约110ppm、或小于约100ppm、或小于约90ppm、或小于约80ppm、或小于约70ppm、或小于约60ppm、或小于约50ppm、或小于约45ppm、或小于约40ppm、或小于约35ppm、或小于约30ppm、或小于约25ppm、或小于约20ppm、或小于约15ppm、或小于约10ppm hcp,或小于约5ppm hcp,或小于约1ppm hcp。
[0485]
72.如方面69-70中任一项所述的工艺,其中所述洗脱物包含hcp的量在约0.5ppm hcp至约150ppm hcp,或约0.5ppm hcp至约140ppm hcp,或0.5ppm hcp至约130ppm hcp,或约0.5ppm hcp至约120ppm,或约0.5ppm hcp至约110ppm,或约0.5ppm hcp至约100ppm hcp,或约0.5ppm hcp至约90ppm hcp,或约0.5ppm hcp至约90ppm hcp,或约0.5ppm hcp至约80ppm hcp,或约0.5ppm hcp至约70ppm hcp,或约0.5ppm hcp至约60ppm hcp,或约0.5ppm至约50ppm hcp,或约0.5ppm hcp至约45ppm hcp,或约0.5ppm hcp至约40ppm hcp,或约0.5ppm hcp至约40ppm hcp,或约0.5ppm hcp至约35ppm hcp,或约0.5ppm hcp至约30ppm hcp,或约1ppm hcp至约25ppm hcp,或约1ppm hcp至约20ppm hcp,或约0.5ppm hcp至约15ppm hcp,或约0.5ppm hcp至约10ppm hcp的范围内。
[0486]
73.如方面69-70中任一项所述的工艺,其中如通过相应的hcp elisa测定法所测量,所述洗脱物不包含可检测的hcp。
[0487]
74.如方面1-73中任一项所述的工艺,其中所述水性原料还包含hmws。
[0488]
75.如方面74所述的工艺,其中如通过尺寸排阻(se)-hplc所测量,以峰面积百分比计所述水性原料中hmws的量与所述洗脱物中hmws的量的比率为至少约2、或至少约3、或至少约4、或至少约5。
[0489]
76.如方面74-75中任一项所述的工艺,其中如通过se-hplc所测量,所述洗脱物包含小于约5% hmws,或小于约4% hmws,或小于约3% hmws,或小于约2% hmws,或小于约1% hmws。
[0490]
77.如方面74-75中任一项所述的工艺,其中如通过se-hplc所确定,所述洗脱物包含hmws的量在约0.2% hmws至约5% hmws,或约0.2% hmws至约4% hmws,或约0.2% hmws至约3% hmws,或约0.2%hmws至约2% hmws,或约0.2% hmws至约1% hmws的范围内。
[0491]
78.如方面74-75中任一项所述的工艺,其中如通过se-hplc所测量,所述洗脱物不包含可检测的hmws。
[0492]
79.如方面1-78中任一项所述的工艺,其中如通过还原性sds-cge所确定,所述洗脱物包含至少约90%的完整的可活化抗体,或至少约91%、或至少约92%、或至少约93%、或至少约94%、或至少约95%的完整的可活化抗体。
[0493]
80.如方面79所述的工艺,其中所述第一ab包含抗体轻链和抗体重链,并且其中第一前结构域通过肽键与所述第一ab的抗体轻链偶联,并且其中如通过还原性sds-cge所确定,所述完整的可活化抗体百分比是基于所述完整的可活化抗体的轻链和轻链经修剪的变体来确定。
[0494]
81.如方面1-80中任一项所述的工艺,其中在步骤(a)之前,所述工艺还包括:
[0495]
(a0)使包含所述完整的可活化抗体和所述经修剪的杂质的生物收获物组合物经受一个或多个选自由离心步骤、过滤步骤、亲和色谱步骤、病毒灭活步骤、尺寸排阻色谱步骤、病毒过滤步骤、离子交换色谱步骤和其任何两个或更多个的组合组成的组的干预性单元操作以产生一种或多种散装中间产物组合物,其中所述水性原料包含至少一种散装中间产物组合物。
[0496]
82.如方面1-81中任一项所述的工艺,其中所述洗脱物经受一个或多个下游单元操作以产生下游产物组合物。
[0497]
83.如方面82所述的工艺,其中所述一个或多个下游单元操作选自由其他的纯化工艺、化学合成工艺、稀释工艺、溶剂交换工艺、配制工艺、冻干工艺和其两种或多种的任何组合组成的组。
[0498]
84.如方面82或83所述的工艺,其中所述一个或多个下游单元操作包括选自由离心步骤、过滤步骤、亲和色谱步骤、病毒灭活步骤、尺寸排阻色谱步骤、病毒过滤步骤、离子交换色谱步骤以及其两种或更多种的任何组合组成的组的其他的纯化工艺。
[0499]
85.如方面82-84中任一项所述的工艺,其中所述一个或多个下游单元操作包括冻干工艺。
[0500]
86.如方面82-85中任一项所述的工艺,其中所述一个或多个下游单元操作是化学合成工艺。
[0501]
87.如方面86所述的工艺,其中所述化学合成工艺是化学缀合反应。
[0502]
88.如方面1-87中任一项所述的工艺,其中如通过还原性sds-cge所确定,所述水性原料包含大于约0.5%经修剪的杂质,或大于约0.6%、或大于约0.7%、或大于约0.8%、或大于约0.9%、或大于约1%、或大于约1.5%、或大于约2%、或大于约2.5%、或大于约3%、或大于约3.5%、或大于约4%、或大于约4.5%经修剪的杂质。
[0503]
89.如方面1-88中任一项所述的工艺,其中所述完整的可活化抗体包含第二ab和第二前结构域,并且其中如通过质谱法所确定,所述经修剪的杂质包括单臂经修剪的杂质。
[0504]
90.如方面89所述的工艺,其中所述第二ab与所述第一ab相同,并且其中所述第二前结构域与所述第一前结构域相同。
[0505]
91.如方面89或90所述的工艺,其中如通过质谱法所确定,所述经修剪的杂质基本上由单臂经修剪的杂质组成。
[0506]
92.如方面89或90所述的工艺,其中如通过质谱法所确定,所述经修剪的杂质由单臂经修剪的杂质组成。
[0507]
93.一种通过方面1-92中任一项所述的工艺生产的纯化的完整的可活化抗体组合
物。
[0508]
94.一种纯化的产物组合物,其包含方面82-87中任一项所述的下游产物组合物。
[0509]
95.如方面1-92中任一项所述的工艺,其中所述洗脱物包含如通过还原性sds-cge所确定的至少约90%完整的可活化抗体、如通过还原性sds-cge所确定的小于约15%经修剪的杂质、如通过se-hplc所确定的小于约5% hmws以及如通过相应的hcp elisa所确定的小于约150ppm hcp。
[0510]
96.如方面95所述的工艺,其中如通过还原性sds-cge所确定,所述洗脱物包含小于约5%经修剪的杂质。
[0511]
97.如方面96所述的工艺,其中如通过还原性sds-cge所确定,所述洗脱物包含小于约3%经修剪的杂质。
[0512]
98.一种纯化的完整的可活化抗体组合物,其包含通过方面1-97中任一项所述的工艺生产的洗脱物。
[0513]
99.一种纯化的完整的可活化抗体组合物,其包含如通过还原性sds-cge所确定的至少约90%完整的可活化抗体、如通过还原性sds-cge所确定的小于约15%经修剪的杂质、如通过se-hplc所确定的小于约5% hmws以及如通过相应的hcp elisa所确定的小于约150ppm hcp。
[0514]
100.如方面98或99所述的纯化的完整的可活化抗体组合物,其中如通过还原性sds-cge所确定,所述组合物包含小于约14%经修剪的杂质,或小于约13%经修剪的杂质,或小于约12%经修剪的杂质,或小于约12%经修剪的杂质,或小于约11%经修剪的杂质,或小于约10%经修剪的杂质,或小于约9%经修剪的杂质,或小于约8%经修剪的杂质,或小于约7%经修剪的杂质,或小于6%经修剪的杂质。
[0515]
101.如方面98-100中任一项所述的纯化的完整的可活化抗体组合物,其中如通过还原性sds-cge所确定,所述组合物包含小于约5%经修剪的杂质,或小于约4%经修剪的杂质,或小于约3%经修剪的杂质,或小于约2%经修剪的杂质。
[0516]
102.如方面98-101中任一项所述的纯化的完整的可活化抗体组合物,其中如通过还原性sds-cge所确定,所述组合物包含小于约1%经修剪的杂质,或小于约0.9%经修剪的杂质,或小于约0.8%经修剪的杂质,或小于约0.7%经修剪的杂质,或小于约0.6%经修剪的杂质,或小于约0.5%经修剪的杂质。
[0517]
103.如方面98或99所述的纯化的完整的可活化抗体组合物,其中如通过还原性sds-cge所确定,所述组合物包含经修剪的杂质的相对量在约0.1%至约15%经修剪的杂质,或约0.1%至约10%经修剪的杂质,或约0.1%至约10%经修剪的杂质,或约0.1%至约5%经修剪的杂质,或约0.1%至约4%经修剪的杂质,或约0.1%至约3%经修剪的杂质,或约0.1%至约2%经修剪的杂质,或约0.1%至约1%经修剪的杂质的范围内。
[0518]
104.如方面98或99所述的纯化的完整的可活化抗体组合物,其中如通过还原性sds-cge所确定,所述组合物不包含可检测的经修剪的杂质。
[0519]
105.如方面98-104中任一项所述的纯化的完整的可活化抗体组合物,其中如通过相应的hcp elisa测定法所确定,所述组合物包含小于约140ppm hcp,或小于约130ppm hcp,或小于约120ppm hcp,或小于约110ppm hcp,或小于约100ppm hcp,或小于约90ppm hcp,或小于约80ppm hcp,或小于约70ppm hcp,或小于约60ppm hcp,或小于约50ppm hcp,
或小于约45ppm hcp,或小于约40ppm hcp,或小于约35ppm hcp,或小于约30ppm hcp,或小于约25ppm hcp,或小于约20ppm hcp,或小于约15ppm hcp,或小于约10ppm hcp。
[0520]
106.如方面98-105中任一项所述的纯化的完整的可活化抗体组合物,其中所述组合物包含hcp的量在约1ppm hcp至约150ppm hcp,或约1ppm hcp至约140ppm hcp,或1ppm hcp至约130ppm hcp,或约1ppm hcp至约120ppm,或约1ppm hcp至约110ppm,或约1ppm hcp至约100ppm hcp,或约1ppm hcp至约90ppm hcp,或约1ppm hcp至约90ppm hcp,或约1ppm hcp至约80ppm hcp,或约1ppm hcp至约70ppm hcp,或约1ppm hcp至约60ppm hcp,或约1ppm至约50ppm hcp,或约1ppm hcp至约45ppm hcp,或约1ppm hcp至约40ppm hcp,或约1ppm hcp至约40ppm hcp,或约1ppm hcp至约35ppm hcp,或约1ppm hcp至约30ppm hcp,或约1ppm hcp至约25ppm hcp,或约1ppm hcp至约t 20ppm hcp,或约1ppm hcp至约15ppm hcp,或约1ppm hcp至约10ppm hcp的范围内。
[0521]
107.如方面98-106中任一项所述的纯化的完整可活化抗体组合物,其中如通过se-hplc所确定,所述组合物包含小于约4% hmws,或小于约3% hmws,或小于约2% hmws,或小于约1% hmws。
[0522]
108.如方面98或99所述的纯化的完整的可活化抗体组合物,其中如通过se-hplc所确定,所述组合物包含hmws的量在约0.2%hmws至约5% hmws,或约0.2% hmws至约4% hmws,或约0.2% hmws至约3% hmws,或约0.2% hmws至约2% hmws,或约0.2% hmws至约1%hmws的范围内。
[0523]
109.如方面98-108中任一项所述的纯化的完整的可活化抗体组合物,其中如通过还原性sds-cge所确定,所述组合物包含至少约91%、或至少约92%、或至少约93%、或至少约94%、或至少约95%完整的可活化抗体。
[0524]
110.如方面98-109中任一项所述的纯化的完整的可活化抗体组合物,其中所述组合物是冻干的。
[0525]
111.一种药学上可接受的组合物,其包含如方面98-110中任一项所述的组合物和药学上可接受的赋形剂。
[0526]
112.如方面1-92或95-97中任一项所述的工艺,如方面93或98-110中任一项所述的纯化的完整的可活化抗体组合物,如方面94所述的纯化产物组合物或如方面111所述的药学上可接受的组合物,其中所述完整的可活化抗体中的第一cm包含蛋白酶的底物,所述蛋白酶相对于健康组织在患病组织中过度表达。
[0527]
113.如方面1-92、95-97或112中任一项所述的工艺,如方面93、98-110中任一项所述的纯化的完整的可活化抗体组合物,如方面94或112中任一项所述的纯化产物组合物,或如方面110或111中任一项所述的药学上可接受的组合物,其中所述完整的可活化抗体还包含(i i i)对第二生物靶标具有特异性结合亲和力的第二ab,和(iv)第二前结构域,
[0528]
其中所述第二ab包含第二vl和第二vh,
[0529]
其中所述第二前结构域包含第二mm和第二cm,并且
[0530]
其中所述第二ab与所述第二前结构域偶联。
[0531]
114.如方面113所述的工艺、纯化的完整的可活化抗体组合物、纯化的产物组合物或药学上可接受的组合物,其中所述第二cm包含用于蛋白酶的底物,所述蛋白酶相对于健康组织在患病组织中过度表达。
[0532]
115.如方面113-114中任一项所述的工艺、纯化的完整的可活化抗体组合物、纯化产物组合物或药学上可接受的组合物,其中所述第一cm和所述第二cm包含同一的氨基酸序列。
[0533]
116.如方面113-115中任一项所述的工艺、纯化的完整的可活化抗体组合物、纯化产物组合物或药学上可接受的组合物,其中所述第一cm和所述第二cm包含不同的氨基酸序列。
[0534]
117.如方面113-116中任一项所述的工艺、纯化的完整的可活化抗体组合物、纯化产物组合物或药学上可接受的组合物,其中所述第一生物靶标和所述第二生物靶标是不同的。
[0535]
118.如方面113-117中任一项所述的工艺、纯化的完整的可活化抗体组合物、纯化产物组合物或药学上可接受的组合物,其中所述第一生物靶标和所述第二生物靶标中的至少一者是t细胞共受体。
[0536]
119.如方面118所述的工艺、纯化的完整的可活化抗体组合物、纯化产物组合物或药学上可接受的组合物,其中所述t细胞共受体是分化簇3(cd3)t细胞共受体。
[0537]
120.如方面113-115中任一项所述的工艺、纯化的完整的可活化抗体组合物、纯化产物组合物或药学上可接受的组合物,其中所述第二ab与所述第一ab是同一的,并且其中所述第二前结构域与所述第一前结构域是同一的。
[0538]
121.如方面120所述的工艺、纯化的完整的可活化抗体组合物、纯化产物组合物或药学上可接受的组合物,其中所述第一生物靶标和所述第二生物靶标是cd166。
[0539]
122.如方面120所述的工艺、纯化的完整的可活化抗体组合物、纯化产物组合物或药学上可接受的组合物,其中所述第一生物靶标和所述第二生物靶标是pd-1。
[0540]
123.如方面120所述的工艺、纯化的完整的可活化抗体组合物、纯化产物组合物或药学上可接受的组合物,其中所述第一生物靶标和所述第二生物靶标是pdl-1。
[0541]
虽然出于清楚和理解的目的已经相当详细地描述了前述发明,但是本领域技术人员通过阅读本公开将清楚,可以在不背离本发明的真实范围的前提下,在形式和细节上做出各种变化。应理解,本文所述的材料、实例和实施方案仅为了说明的目的,而非旨在限制,并且本领域技术人员将想到根据本发明的各种修改或变化,这些修改或变化均包括在所附权利要求书的精神和范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- OTUD5的单克隆抗体制备及其在癌症治疗中的用途的制造方法与工艺
- 氧化白藜芦醇或氧化白藜芦醇联合抗生素在制备抗真菌感染产品中的应用的制造方法与工艺
- 一种3D打印技术制备治疗高磷血症的口腔速崩片的方法与流程
- 特异性人EWS‑FLI1融合蛋白抗体的制备方法及在制备尤文肉瘤诊断抗体试剂的应用与制造工艺
- 抗下垂基板及其制备和使用的方法与制造工艺
- 用于修饰抗体以制备免疫缀合物的特定位点的制造方法与工艺
- 汉坦病毒S基因克隆、表达、单克隆抗体的制备方法及其应用与制造工艺
- 一种膜蛋白CD14的抗体的制备方法及应用与制造工艺
- 用于治疗癌症的抗CCR4抗体和4‑1BB激动剂的组合的制造方法与工艺
- 一种识别磷铝酸盐矿物浸蚀剂的制备及使用方法与制造工艺