抗HBV抗体及其使用方法与流程
抗hbv抗体及其使用方法
技术领域
1.本发明涉及针对抗乙型肝炎病毒(hbv)的抗体及其使用方法。
背景技术:
2.尽管有有效的疫苗可供使用,但慢性乙型肝炎病毒(hbv)感染是影响全球超过2.5亿人的主要医疗保健问题(who,2017)。由于hbv相关的肝硬化、肝功能衰竭和肝细胞癌,感染导致每年大约100万人死亡(who,2017)。hbv是一种dna病毒,属于嗜肝dna病毒科(hepadnaviridae)家族,它以传染性病毒粒子或dane颗粒的形式产生,但也以非传染性亚病毒颗粒的形式产生(seeger等人,2013)。病毒粒子和亚病毒颗粒在其表面展示三种形式的hbv包膜糖蛋白或hbv表面抗原(hbsag):l-hbs(大)、m-hbs(中)和s-hbs(小)。因此,比传染性hbv病毒粒子数量多的缺陷颗粒充当免疫诱饵(seeger等人,2013)。目前治疗慢性hbv的疗法很少能实现由hbsag消失和抗hbs抗体血清转换所定义的功能性治愈。然而,在超过90%的成年感染患者和约1%的自发清除感染的慢性感染患者(称为hbv血清转换者或自然控制者)中,自然免疫应答可以成功控制hbv感染(bauer等人,2011;chu和liaw,2016;mcmahon,2009;rehermann和nascimbeni,2005)。强大且多特异性的hbv特异性cd4
+
和cd8
+
t细胞应答是在控制感染中的关键免疫效应物(bauer等人,2011)。然而,b细胞和抗体也有助于在功能性治愈后长期清除和防止病毒反弹(bertoletti和ferrari,2016;corti等人,2018;rehermann和nascimbeni,2005)。例如,尽管患者中的hbsag-/抗hbs
+
抗体血清转换与无法检测到的hbv dna水平相关(mcmahon,2009),但正在接受b细胞耗竭疗法以治疗非霍奇金淋巴瘤的功能性治愈的个体hbv再激活的风险较高,这会迅速导致严重的肝功能障碍(kusumoto等人,2019;perrillo等人,2015)。因此,控制和最终消除hbv感染的关键免疫成分可能包括广泛而强大的抗原特异性t细胞应答,以及介导hbsag清除和终身保护性免疫的中和抗hbs抗体的开发(bertoletti和ferrari,2016;corti等人,2018)。
3.为应答hbv感染而产生的中和抗体靶向所有3种hbsag形式。它们识别s-hbs抗原环并干扰与肝细胞上的硫酸乙酰肝素蛋白多糖(hs)的预附着,或识别l-hbs的pres1结构域并阻断与宿主细胞受体牛磺胆酸钠共转运多肽(ntcp)的结合(corti等人,2018)。由hbv疫苗接种(基于重组s-hbs免疫原)诱导的针对s-hbs环的“决定因素”部分的igg抗体,或施用于存在暴露于多克隆hbv免疫球蛋白输注风险个体的igg抗体可对hbv感染提供保护(samuel等人,1993;west和calandra,1996)。已从免疫小鼠和少数人类免疫供体中分离出几种中和抗pres和抗s-hbs抗体(corti等人,2018)。s-hbs中和抗体可能有助于hbv血清转换者的病毒清除和长期抑制,就像它们保护疫苗接种者免受感染一样。然而,尚未通过克隆和表征人hbsag特异性抗体来研究功能性治愈的hbv感染个体对hbv的记忆b细胞应答。
技术实现要素:
4.本发明提供抗s-hbs抗体及其使用方法。
附图说明
5.图1.从hbv疫苗接种者和控制者中克隆的s-hbs记忆抗体
6.(a)来自hbv疫苗接种者(hbvv,n=6,底部曲线)和控制者(hbvc,n=8,顶部曲线)的血清igg的平均s-hbsag反应性。阴影区域表示值范围。代表性的流式细胞术图显示了hbv疫苗接种者和控制者中的s-hbs结合igg
+
记忆b细胞(显示了bv4和bc3)。ns-hbsag和rs-hbsag分别是人源性天然s-hbs抗原和重组s-hbs抗原。
7.(b)s-hbsag捕获的igg
+
记忆b细胞抗体的s-hbsag-elisa反应性(左)和从hbvv和hbvc中分离出来的s-hbs特异性单克隆抗体的百分比(%s-hbsag
+
)(右)。显示了根据hbvc中s-hbs抗体滴度(《150iu/ml和》900iu/ml)的%s-hbsag
+
。capt-rhbags、rhbags捕获elisa。
8.(c)气泡图显示了根据s-hbs特异性igg抗体的igh和igl链可变结构域中体细胞突变百分比的克隆扩增水平。每个供体的扩展大小如下面的条形图所示。
9.(d)火山图分析比较了来自hbv免疫供体的s-hbsag特异性b细胞和来自健康个体的igg记忆b细胞的免疫球蛋白(ig)基因谱(上)。虚线上方的点表示两种ig基因谱之间的统计学显著差异。显示了vh(dh)jh重排频率的比较(下)。pv,p值;fc,倍数变化。
10.(e)s-hbs记忆igg中构象依赖性与非构象抗体的分布。测试抗体的总数显示在饼图的中心。红外免疫印迹显示抗s-hbs igg记忆b细胞抗体对变性s-hbs蛋白有反应(右上)。显示了肽反应性s-hbs抗体的elisa结合曲线(右下,四次重复的平均值
±
sd)。
11.图2.人s-hbs记忆抗体的中和活性
12.(a)s-hbs igg抗体对基因型d hbv体外感染heparg细胞的中和活性。显示了每种抗体(n=72)的50%抑制浓度(ic
50
)值(左上),以及中和抗体与非活性抗体的分布(左下)。(b)显示了根据结合的s-hbs抗原(右上)和体细胞超突变百分比(%shm)(右下)的中和能力。
13.(c)通过northern印迹法在heparg细胞中使用hdv rna定量,所选s-hbs igg抗体抗hdv的体外中和活性。ge,基因组等价物。
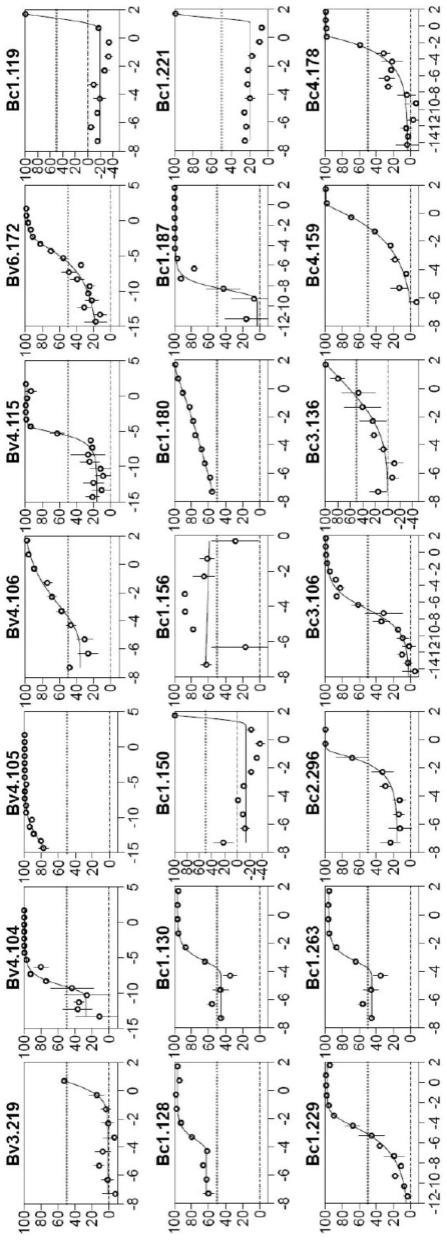
14.(d)人s-hbs抗体在aav-hbv转导小鼠中的体内中和活性。在用0.5mg抗s-hbs抗体pibv4.104(n=9)、bc1.187(n=9)、bc1.263(n=6)、bc4.204(n=4)或mgo53同种型对照(n=5)静脉注射治疗一次的aav-hbv转导小鼠中监测循环血液s-hbs水平。粗线代表平均值。
15.(e)显示了在每只小鼠施用0.25mg(白色)和0.5mg(黑色)抗体后s-hbs滴度在最低点(注射后第2天,dpi2)的log
10
变化。用线表示平均值。
16.(f)在静脉注射一次1mg抗s-hbs抗体bc1.187的aav-hbv转导小鼠(n=6)中监测循环血液s-hbs和hbv dna水平。s-hbs和hbv dna水平随时间变化的平均log
10
显示在右侧。
17.图3.人hbv中和抗体的交叉反应性
18.(a)热图比较了hbv中和抗体对adw和ayw基因型d s-hbs蛋白的elisa反应性(测量为图14中的auc值)。右侧的代表性elisa图显示了所选抗体对重组hbv疫苗engerix-b(ayw)和genhevac(adw)的反应性。误差条表示测定重复的sd。
19.(b)热图比较了hbv中和抗体对来自系统发育树(左上)中描述的基因型的s-hbs抗原的反应性,以流式细胞术确定的结合s-hbs表达细胞的百分比表示。数据代表两个独立实验之一。hb1和mgo53分别是阳性和阴性对照。左下角的细胞图显示了hb1抗体的代表性反应
性谱。右侧的elisa图显示了所选抗体对除g之外的所有基因型的重组s-hbs抗原的反应性。误差条表示测定重复的sd。
20.(c)与(b)相同,但左上图描绘的s-hbs突变蛋白不同。
21.(d)图表比较了bc1.187对从a到d基因型的hbv病毒感染原代人肝细胞的中和活性。误差条表示测定一式三份的sem。
22.(e)图表显示了通过heparg中和测定确定的pibv4.104和bc1.187对来自基因型a、c和d的hbv病毒的中和曲线。误差条表示测定一式三份的sem。
23.图4.人hbv中和抗体的结合特征
24.(a)热图显示所选hbv中和抗体与重组hbsag突变蛋白的elisa结合。颜色值与反应水平成正比。
25.(b)热图显示s-hbs与hbv中和抗体结合的竞争。较浅的颜色表示较强的抑制作用;黑色表示没有竞争。
26.(c)图表比较了通过流式细胞术(上)和elisa(下)测量的所选hbv中和抗体及其种系对应物与s-hbs结合。
27.(d)通过heparg中和测定确定的bc1.187、bc4.204和pibv4.104的种系版本对基因型d hbv病毒的中和活性。误差条表示测定一式三份的sd。
28.(e)所选s-hbs人抗体在人蛋白质微阵列上的反应性谱。每个点对应于参考(ref:mgo53,y轴)和测试抗体(x轴)在单个蛋白质上给出的z分数。标签表示免疫反应蛋白(z》5)。
29.图5.使用有效的hbv交叉中和抗体bc1.187进行体内治疗。
30.(a)每2天用0.5mg抗s-hbs bc1.187或同种型对照mgo53嵌合抗体静脉注射治疗16天的aav-hbv转导小鼠(n=7每组)中hbv感染随时间的演变。示出了循环血液hbsag、hbeag和hbv dna水平。粗线表示平均值。
31.(b)每周接受腹腔内注射人抗s-hbs抗体bc1.187(20mg/kg~0.4mg,n=7,直线;50mg/kg~1mg,n=5,虚线)持续3周的huhep小鼠中hbv感染随时间的演变。显示了与基线(右)相比的循环血液hbsag、hbeag和hbv dna水平(左)和δlog
10
值。粗线表示平均值。
32.图6.表格示出了hbv免疫供体的临床和免疫病毒学特征。
33.图7a和图7b.表格示出了人抗s-hbs抗体的免疫球蛋白基因谱和中和活性。
34.图8.纯化的血清iggs和血液igg+记忆b细胞与s-hbs抗原的结合。
35.(a)代表性elisa图示出了来自hbv疫苗接种者(hbvv)和控制者(hbvc)的纯化血清igg抗体对重组(rs-hbs)和人源性天然(ns-hbs)s-hbs颗粒的反应性。误差条表示重复值的sem。(b)流式细胞图示出了用于单细胞分选igg+记忆b细胞与用作诱饵的荧光标记的rs-hbs和ns-hbs蛋白结合的门控策略。示出了所有供体的s-hbs反应性igg+记忆b细胞群。
36.图9.s-hbs捕获的igg+记忆b细胞抗体的s-hbs反应性。
37.(a)热图示出了从hbv疫苗接种者和血清转换者克隆的s-hbs结合记忆抗体对ns-hbs和rs-hbs(固定和捕获)的elisa反应性。示出了三次重复的光密度值的平均值。(b)小提琴图示出了(a)中所示结合的累积elisa光密度(cod)值。示出了每个供体从s-hbs捕获的igg+记忆b细胞克隆的s-hbs特异性抗体的比例(右)。
38.图10.s-hbs特异性igg+记忆b细胞的免疫球蛋白基因谱。
39.(a)饼图比较了来自健康个体(igg.mb)的血液s-hbs特异性igg+记忆b细胞和igg+
记忆b细胞的vh/jh基因使用分布(prigent等人,2016)。分析的抗体序列数量显示在每个饼图的中心。(b)条形图比较了由s-hbs特异性和对照igg+记忆b细胞表达的单一免疫球蛋白vh基因的分布。(c)表达vh1-69的s-hbs抗体的cdrh2区域(由kabat定义)的氨基酸比对。灰色残基表示与种系vh基因(顶部)相比的取代。(d)与(b)相同,但igg亚型(左)和κ-vsλ-ig链使用(右)不同。(e)与(b)相同,但cdrh3长度和正电荷数不同。cdrh3长度的平均值显示在每个直方图下方。(f)与(a)相同,但vκ/jκ和vλ/jλ基因使用不同。(g)小提琴图比较了s-hbs特异性和对照igg+记忆b细胞中vh、vκ和vλ基因的突变数量。平均突变数量(mut.)显示在每个点图下方。使用未配对的学生t检验和welch校正比较抗体组之间的突变数量。(h)图表示出了基于抗s-hbs igh和igl序列的抗原驱动选择的贝叶斯估计。使用2
×
2和2
×
5fisher精确检验对组进行比较(在a、b、d、e和f中)。
40.图11.人抗s-hbs抗体对变性的s-hbsag和s-hbsag肽的反应性。
41.(a)抗s-hbs抗体对跨膜结构域缺失的s-hbsag蛋白(δtm-rs-hbsag)的elisa反应性。hb1和mgo53分别是阳性和阴性对照。虚线表示正反应性的临界od
405nm
。(b)与(a)相同,但对应于推定的s-hbsag环122-137和139-148的环肽不同。(c)抗s-hbs抗体对s-hbsag重叠线性肽的热图反应性。显示了s-hbsag肽的氨基酸序列(右)和总平均亲水性值(gravy)(下)。
42.图12a和b.人s-hbs抗体对体外hbv的中和作用。
43.图表显示了在体外heparg测定中测量的所选人s-hbs抗体对基因型d hbv病毒的中和曲线。水平虚线表示50%中和,从中可以得出ic50值来自x轴上的抗体浓度。
44.图13.在hbv-aav小鼠中被动施用人s-hbs抗体。
45.(a)人s-hbs抗体在aav-hbv转导小鼠中的体内中和活性。在用0.25mg抗s-hbs抗体bv4.104(n=6)、bc1.187(n=6)、bc1.263(n=6)、bc4.204(n=6)或mgo53同种型对照(n=5)静脉注射治疗一次的aav-hbv转导小鼠中监测循环血液hbsag水平。粗线表示平均值。显示每只小鼠静脉注射施用0.25mg抗体后,hbsag滴度随时间改变的log10(δlog10 s-hbs)。(b)图表显示了用0.25mg(左)和0.5mg(右)s-hbs抗体处理一次的小鼠中人igg滴度随时间的演变。粗线表示平均值。
46.图14.hbv中和抗体与重组血清型特异性s-hbs蛋白的结合。
47.代表性elisa图显示了所选hbv中和抗体与纯化的重组adw(直线)和ayw(虚线)s-hbs蛋白的结合。hb1和mgo53分别是阳性和阴性对照。显示了来自两个独立实验之一的测定重复的平均值
±
sem。
48.图15.hbv中和抗体对基因型特异性s-hbs蛋白的交叉反应性。
49.(a)(b)中使用的来自不同hbv基因型的共有s-hbs蛋白序列的氨基酸比对。残留变化以灰色突出显示。(b)细胞图比较了所选hbv中和抗体对基因型特异性s-hbs抗原的反应性谱。数据代表两个独立实验之一。hb1和mgo53分别是阳性和阴性对照。ctr,未转染的细胞对照(从底部开始);fi,荧光强度。
50.图16.hbv中和抗体对s-hbs突变蛋白的反应性。(a)细胞图比较了所选hbv中和抗体对显示自然发生的逃逸突变(t126a、m133t、y134v或g145r)或s-hbs n-糖基化位点中的突变(n126s)的基因型d s-hbs突变蛋白的反应性。数据代表两个独立实验之一。hb1和mgo53分别是阳性和阴性对照。ctr,未转染的细胞对照(从底部开始);fi,荧光强度。
51.图17.强效hbv中和抗体的多反应性和自身反应性。(a)所选人s-hbs抗体(n=8)人
蛋白质微阵列的反应性谱。对于每个蛋白质点,由参考(ref:mgo53)和测试给出的平均荧光强度(mfi)分别描绘在y和x轴上。每个点代表重复阵列蛋白的平均值。对角线表示参考抗体和测试抗体的结合相等。标记的点表示z分数》5的免疫反应蛋白。(b)频率直方图显示了与非反应性抗体mgo53相比,s-hbs抗体的mfi信号的log10蛋白质位移(σ)。多反应性指数(pi)对应于所有阵列蛋白质位移的高斯平均值。(c)通过ifa和elisa测定所选s-hbs抗体与表达hep2的自身抗原的结合。ctr+,试剂盒的阳性对照。mgo53和ed38分别是阴性和阳性对照抗体。比例尺代表40μm。右下角的条形图显示了通过elisa测量的hep-2反应性。显示了来自一式两份进行的两个独立实验的值的平均值
±
sd。
52.图18.在慢性hbv感染的小鼠中被动施用中和抗体。
53.(a)每3-4天腹腔内注射0.5mg的人抗s-hbs抗体bc1.187或mgo53同种型对照治疗17天的aav-hbv转导小鼠(n=7)中随时间变化的循环血液hbsag水平。示出了平均δlog10 hbsag值(右)。阴影区域表示抗体治疗期。(b)通过elisa测量的(a)中所示的治疗小鼠中的鼠抗人igg抗体水平。(c)b6小鼠(n=4)中被动施用的嵌合bc1.187抗体(0.5mg静脉注射)的igg浓度。mubc1.187抗体以天为单位的半衰期(t1/2)显示在右上角。(d)每周接受静脉注射(0.5mg)的嵌合抗s-hbs抗体bc1.187和mgo53同种型对照的c57bl/6j小鼠随时间变化的δlog10 s-hbs水平。粗线表示平均值。(e)每2天用0.5mg的嵌合抗s-hbs抗体bc1.187或mgo53同种型对照静脉注射治疗16天的aav-hbv转导小鼠(n=7)中随时间变化的δlog10 hbsag和hbv dna水平。粗线表示平均值。阴影区域表示抗体治疗期。
54.图19.bc1.187抗体治疗hbv感染的huhep小鼠。
55.(a)感染基因型d hbv并用抗hbs bc1.187以20mg/kg或50mg/kg人抗体腹腔内注射治疗3周的每只huhep小鼠的随时间变化的血液hbsag、hbeag和hbv dna水平。(b)每3-4天接受非hbv同种型对照mgo53(20mg/kg腹腔内注射)或恩替卡韦(etv)治疗3周的huhep小鼠中hbv感染随时间的演变。示出了hbsag、hbeag和hbv dna的血液水平。(c)图表示出了受感染的huhep小鼠和用20mg/kg(直线)和50mg/kg(虚线)的bc1.187腹腔内注射治疗17天(阴影区域)的小鼠中随时间变化的人血清白蛋白水平。
具体实施方式
56.i.定义
57.出于本文目的的“受体人框架”是这样的框架,其包含来源于如下所定义的人免疫球蛋白框架或人共有框架的轻链可变结构域(vl)框架或重链可变结构域(vh)框架的氨基酸序列。“来源于”人免疫球蛋白框架或人共有框架的受体人框架可包含与该人免疫球蛋白框架或人共有框架相同的氨基酸序列,或者其可以包含氨基酸序列变化。在一些方面,氨基酸变化的数量为10个或更少、9个或更少、8个或更少、7个或更少、6个或更少、5个或更少、4个或更少、3个或更少或2个或更少。在一些方面,vl受体人框架在序列上与vl人免疫球蛋白框架序列或人共有框架序列相同。
[0058]“亲和力”是指分子(例如,抗体)的单个结合位点与其结合配偶体(例如,抗原)之间的非共价相互作用的总和的强度。除非另有说明,否则如本文所用,“结合亲和力”是指内在结合亲和力,其反映了结合对的成员(例如,抗体和抗原)之间的1:1相互作用。分子x对其配偶体y的亲和力一般可由解离常数(kd)表示。亲和力可以通过本领域已知的常规方法测
hbs抗体竞争结合。例如,与参考s-hbs抗体“与相同表位结合的抗体”是指在竞争测定中阻断参考抗s-hbs抗体与其抗原的结合达50%或更高的抗体,反之,参考抗体在竞争测定中阻断该抗体与其抗原的结合达50%或更高。同样例如,为了确定抗体是否与参考抗s-hbs抗体结合相同表位,使参考抗体在饱和条件下与s-hbs结合。在去除过量的参考抗s-hbs抗体后,评定所讨论的抗s-hbs抗体与s-hbs结合的能力。如果在参考抗s-hbs抗体饱和结合后抗s-hbs抗体能够与s-hbs结合,则可以得出结论,所讨论的抗s-hbs抗体与和参考抗s-hbs抗体不同的表位结合。但是,如果所讨论的抗s-hbs抗体在参考抗s-hbs抗体饱和结合后不能与s-hbs结合,则所讨论的抗s-hbs抗体可能与和参考抗s-hbs抗体所结合的表位相同的表位结合。为了确认所讨论的抗体是结合于同一表位还是由于空间原因而使其受阻,可以使用常规实验(例如,使用elisa、ria、表面等离子体共振、流式细胞术或任何其他本领域可获得的定量或定性的抗体结合测定法进行的肽突变和结合分析)。该测定应以两种设置进行,即,两种抗体均为饱和抗体。如果在这两种设置中,只有第一(饱和)抗体能够与s-hbs结合,则可以得出结论,所讨论的抗s-hbs抗体和参考抗s-hbs抗体竞争结合s-hbs。
[0067]
在一些方面,如在竞争性结合测定中测量的,如果一种抗体1、5、10、20或100倍过量抑制另一种抗体的结合至少50%、至少75%、至少90%或甚至99%或更高,则认为两种抗体结合相同或重叠的表位(参见例如junghans等人,cancer res.50(1990)1495-1502)。
[0068]
在一些方面,如果抗原中减少或消除一种抗体的结合的基本上所有氨基酸突变也减少或消除另一种抗体的结合,则认为两种抗体结合相同的表位。如果只有一种减少或消除一种抗体结合的氨基酸突变的子集减少或消除另一种抗体的结合,则两种抗体被认为具有“重叠表位”。
[0069]
术语“嵌合”抗体是指这样的抗体,在该抗体中重链和/或轻链的一部分来源于特定来源或物种,而重链和/或轻链的其余部分来源于不同的来源或物种。
[0070]
抗体的“类别”是指抗体的重链所具有的恒定结构域或恒定区的类型。存在五大类抗体:iga、igd、ige、igg和igm,并且这些抗体中的一些可以进一步分为亚类(同种型),例如igg1、igg2、igg3、igg4、iga1和iga2。在某些方面,抗体是igg1同种型。在某些方面,抗体是具有p329g、l234a和l235a突变以降低fc区效应子功能的igg1同种型。在其他方面,抗体是igg2同种型。在某些方面,抗体是在铰链区具有s228p突变的igg4同种型,以改善igg4抗体的稳定性。对应于不同类别的免疫球蛋白的重链恒定结构域分别称为α、δ、ε、γ和μ。抗体的轻链基于其恒定结构域的氨基酸序列,可以归属于两种类型中的一种,这两种类型称为卡帕(κ)和兰姆达(λ)。
[0071]
如本技术中所用的术语“衍生自人源的恒定区”或“人恒定区”表示亚类igg1、igg2、igg3或igg4的人抗体的恒定重链区和/或恒定轻链κ或λ区。此类恒定区在现有技术中是众所周知的并且例如,通过以下描述的:kabat,e.a.,等人,sequences of proteins of immunological interest,第5版,public health service,national institutes of health,bethesda,md(1991)(还参见,例如johnson,g.,和wu,t.t.,nucleic acids res.28(2000)214-218;kabat,e.a.,等人,proc.natl.acad.sci.usa 72(1975)2785-2788)。除非本文另外规定,否则恒定区中氨基酸残基的编号是根据eu编号系统,eu编号系统也称为kabat的eu索引,如在kabat,e.a.等人,sequences of proteins of immunological interest,第5版,public health service,national institutes of health,bethesda,
md(1991),nih publication 91-3242中所述。
[0072]“效应子功能”是指可归因于抗体的fc区、随着抗体同种型的变化而变化的那些生物学活性。抗体效应子功能的实例包括:c1q结合和补体依赖性细胞毒性(cdc);fc受体结合;抗体依赖性细胞介导的细胞毒性(adcc);吞噬作用;细胞表面受体(例如,b细胞受体)的下调;以及b细胞活化。
[0073]
药剂(例如,药物组合物)的“有效量”是指在必要的剂量下和必要的时段内,有效实现期望的治疗或预防结果的量。
[0074]
本文的术语“fc区”用于定义免疫球蛋白重链的c末端区,该c末端区包含恒定区的至少一部分。该术语包括天然序列fc区和变体fc区。在一个方面,人igg重链fc区从cys226或从pro230延伸至重链的羧基末端。然而,由宿主细胞产生的抗体可以经历对来自重链c端的一个或更多个(特别是一个或两个)氨基酸的翻译后切割。因此,由宿主细胞通过表达编码全长重链的特定核酸分子产生的抗体可以包括全长重链,或者该抗体可以包括全长重链的切割变体。这可能是重链的最后两个c末端氨基酸为甘氨酸(g446)和赖氨酸(k447,eu编号)的情况。因此,fc区的c末端赖氨酸(lys447)或c末端甘氨酸(gly446)和赖氨酸(lys447)可以存在或可以不存在。如果没有另外指明,则包含fc区的重链的氨基酸序列在本文中被表示为具有c末端甘氨酸-赖氨酸二肽。在一个方面,包括如本文所指定的fc区的重链包含在根据本发明的抗体中,该重链缺乏c末端甘氨酸-赖氨酸二肽(g446和k447,eu编号系统)。在一个方面,包括如本文所指定的fc区的重链包含在根据本发明的抗体中,该重链缺乏c末端甘氨酸残基(k447,根据eu索引编号)。除非本文另外规定,否则fc区或恒定区中氨基酸残基的编号是根据eu编号系统,eu编号系统也称为eu索引,如在kabat等人,sequences of proteins of immunological interest,第5版,public health service,national institutes of health,bethesda,md,1991中所述。
[0075]“框架”或“fr”是指除互补决定区(cdr)之外的可变结构域残基。可变结构域的fr通常由以下四个fr结构域组成:fr1、fr2、fr3和fr4。因此,cdr和fr序列通常在vh(或vl)中以如下序列出现:fr1-cdr-h1(cdr-l1)-fr2-cdr-h2(cdr-l2)-fr3-cdr-h3(cdr-l3)-fr4。
[0076]
术语“全长抗体”、“完整抗体”及“全抗体”在本文中可互换地用于指代具有基本上类似于天然抗体结构的结构或具有含有如本文所定义的fc区的重链的抗体。
[0077]
术语“宿主细胞”、“宿主细胞系”和“宿主细胞培养物”可互换使用,并且是指外源核酸已被引入其中的细胞,包括此类细胞的子代。宿主细胞包括“转化体”和“转化细胞”,其包括原代转化细胞和来源于该原代转化细胞的子代,不考虑传代次数。子代可能不与亲本细胞的核酸内容物完全一致,而是可能含有突变。本文包括如在原始转化细胞中筛选或选择的具有相同功能或生物活性的突变子代。
[0078]“人抗体”是这样的抗体,其具有的氨基酸序列与由人或人细胞产生的或来源于利用人抗体谱或其他人抗体编码序列的非人来源的抗体的氨基酸序列相对应。人抗体的该定义特别地排除了包含非人抗原结合残基的人源化抗体。
[0079]“人共有框架”是这样的框架,其表示在人免疫球蛋白vl或vh框架序列的选择中最常存在的氨基酸残基。一般而言,人免疫球蛋白vl或vh序列的选择来自于可变结构域序列的亚组。一般而言,序列的亚组是如kabat等人,sequences of proteins of immunological interest,第5版,nih publication 91-3242,bethesda md(1991),第1-3
卷中所述的亚组。在一个方面,对于vl,该亚组是如kabat等人,出处同上中的亚组κi。在一个方面,对于vh,该亚组是如kabat等人,出处同上中的亚组iii。
[0080]“人源化”抗体是指这样的嵌合抗体,其包含来自非人cdr的氨基酸残基和来自人fr的氨基酸残基。在某些方面,人源化抗体将基本上包含所有的至少一个、通常两个可变结构域,其中所有或基本上所有cdr对应于非人抗体的cdr,并且所有或基本上所有的fr对应于人抗体的fr。人源化抗体任选地可以包含来源于人抗体的抗体恒定区的至少一部分。“人源化形式”的抗体,例如,非人抗体,是指已经进行过人源化的抗体。
[0081]
如本文所用,术语“高变区”或“hvr”是指抗体可变结构域的在序列上高变并确定抗原结合特异性的各个区域,例如“互补决定区”(“cdr”)。
[0082]
通常,抗体包含六个cdr;三个在vh中(cdr-h1、cdr-h2、cdr-h3),并且三个在vl中的(cdr-l1、cdr-l2、cdr-l3)。本文中的示例性cdr包括:
[0083]
(a)出现在以下氨基酸残基处的高可变环:26至32(l1)、50至52(l2)、91至96(l3)、26至32(h1)、53至55(h2)和96至101(h3)(chothia和lesk,j.mol.biol.196:901-917(1987));
[0084]
(b)存在于氨基酸残基24-34(l1)、50-56(l2)、89-97(l3)、31-35b(h1)、50-65(h2)和95-102(h3)处的cdr(kabat等人,sequences of proteins of immunological interest,第5版,public health service,national institutes of health,bethesda,md(1991));以及
[0085]
(c)出现在以下氨基酸残基处的抗原接触点:27c至36(l1)、46至55(l2)、89至96(l3)、30至35b(h1)、47至58(h2),以及93至101(h3)(maccallum等人,j.mol.biol.262:732-745(1996))。
[0086]
除非另外指明,否则cdr根据出处同上的kabat等人所述的方法确定。本领域的技术人员将理解,cdr名称也可以根据出处同上的chothia所述的方法、出处同上的mccallum所述的方法或者任何其他在科学上接受的命名系统来确定。
[0087]“免疫缀合物”是与一种或多种异源分子,包括但不限于细胞毒性剂缀合的抗体。
[0088]“个体”或“受试者”是哺乳动物。哺乳动物包括但不限于驯养的动物(例如牛、绵羊、猫、犬和马)、灵长类动物(例如人和非人灵长类动物,诸如猴)、兔以及啮齿类动物(例如小鼠和大鼠)。在某些方面,个体或受试者是人。
[0089]“分离的”抗体为已从其自然环境的组分中分离的抗体。在一些方面,通过例如电泳(例如,sds-page、等电聚焦(ief)、毛细管电泳)或色谱(例如,离子交换或反相hplc)方法测定,将抗体纯化至大于95%或99%的纯度。关于评定抗体纯度的方法的综述,请参见例如flatman等人,j.chromatogr.b 848:79-87(2007)。本文所述的任何抗体都可以是分离的抗体。
[0090]
术语“核酸分子”或“多核苷酸”包括包含核苷酸聚合物的任何化合物和/或物质。每个核苷酸由碱基组成,特别是嘌呤或嘧啶碱基(即胞嘧啶(c)、鸟嘌呤(g)、腺嘌呤(a)、胸腺嘧啶(t)或尿嘧啶(u))、糖(即脱氧核糖或核糖)和磷酸酯基团。通常,核酸分子通过碱基序列进行描述,其中所述碱基代表核酸分子的一级结构(线性结构)。碱基序列通常表示为从5'至3'。在本文中,术语核酸分子涵盖脱氧核糖核酸(dna)(包括例如互补dna(cdna)和基因组dna)、核糖核酸(rna)(特别是信使rna(mrna))、dna或rna的合成形式,以及包含这些分
子中的两种或更多种的混合聚合物。核酸分子可以是线性的或环状的。此外,术语核酸分子包括有义链和反义链,以及单链和双链形式。此外,本文所描述的核酸分子可含有天然存在的或非天然存在的核苷酸。非天然存在的核苷酸的示例包括具有衍生化的糖或磷酸主链键或经化学修饰的残基的经修饰的核苷酸碱基。核酸分子还涵盖适合作为用于本发明的抗体的体外和/或体内(例如,在宿主或患者体内)直接表达的载体的dna和rna分子。此类dna(例如cdna)或rna(例如mrna)载体可以是未修饰的或经修饰的。例如,可以对mrna进行化学修饰以增强rna载体的稳定性和/或编码分子的表达,使得可以将mrna注射到受试者体内以产生体内抗体(参见例如stadler等人,nature medicine 2017,在线发表于2017年6月12日,doi:10.1038/nm.4356或ep 2 101 823 b1)。
[0091]“分离的”核酸是指已自其自然环境的组分中分离的核酸分子。分离的核酸包括这样的核酸分子,其包含在通常含有核酸分子的细胞中,但该核酸分子存在于染色体外或与其天然染色体位置不同的染色体位置处。
[0092]“编码抗s-hbs抗体的分离的核酸”是指编码抗s-hbs抗体重链和轻链(或其片段)的一个或多个核酸分子,包括在单一载体或单独的载体中的此类核酸分子,以及存在于宿主细胞中一个或多个位置的此类核酸分子。
[0093]
如本文所用的术语“单克隆抗体”是指从基本上同质的抗体群体获得的抗体,即,除了可能的变异抗体(例如含有天然存在的突变或在单克隆抗体制剂的生产过程中产生,此类变体通常以少量存在)之外,包含该群体的各个抗体是相同的和/或结合相同的表位。与通常包括针对不同决定簇(表位)的不同抗体的多克隆抗体制剂相反,单克隆抗体制剂中的每种单克隆抗体针对抗原上的单一决定簇。因此,修饰语“单克隆”表示抗体的特征是从基本上同质的抗体群体获得的,并且不应解释为需要通过任何特定方法产生抗体。例如,根据本发明的单克隆抗体可以通过多种技术制备,包括但不限于杂交瘤方法、重组dna方法、噬菌体展示方法,以及利用含有全部或部分人免疫球蛋白基因座的转基因动物的方法,在本文中描述了用于制备单克隆抗体的此类方法和其他示例性方法。
[0094]“裸抗体”是指不缀合至异源部分(例如,细胞毒性部分)或放射性标记的抗体。裸抗体可存在于药物组合物中。
[0095]“天然抗体”是指具有不同结构的天然免疫球蛋白分子。例如,天然igg抗体是约150,000道尔顿的异四聚体糖蛋白,由经二硫键合的两条相同轻链和两条相同重链构成。从n端至c端,每条重链均具有可变结构域(vh),亦称为可变重链结构域或重链可变区,随后为三个恒定重链结构域(ch1、ch2和ch3)。类似地,从n端至c端,每条轻链均具有可变结构域(vl),亦称为可变轻链结构域或轻链可变区,随后为恒定轻链(cl)结构域。
[0096]
术语“包装插页”用于指治疗产品的商业包装中通常包括的说明书,其含有涉及此类治疗产品的使用的有关适应症、用法、剂量、施用、联合疗法、禁忌症和/或警告的信息。
[0097]
相对于参照多肽序列的“氨基酸序列同一性百分比(%)”被定义为在比对候选序列与参考多肽序列并引入空位(如果必要的话)以实现最大的序列同一性百分比之后,并且在出于比对的目的而不考虑将任何保守性取代作为序列同一性的组成部分的情况下,候选序列中的氨基酸残基与参考多肽序列中的氨基酸残基相同的百分比。用于确定氨基酸序列同一性百分比的比对可以通过本领域技术范围内的各种方式实现,例如使用公众可获得的计算机软件,诸如blast、blast-2、clustal w、megalign(dnastar)软件或fasta程序包。本
hbsag(abbott)或monolisa s-hbsag ultra(bio-rad,法国)elisa。
[0104]
术语“可变区”或“可变结构域”是指抗体重链或轻链的参与抗体与抗原结合的结构域。天然抗体的重链和轻链的可变结构域(分别为vh和vl)通常具有相似的结构,其中每个结构域包含四个保守框架区(fr)和三个互补决定区(cdr)。(参见,例如,kindt等人,kuby immunology,第6版,w.h.freeman and co.,第91页(2007)。)单个vh或vl结构域可足以赋予抗原结合特异性。此外,结合特定抗原的抗体可分别使用来自结合该抗原的抗体的vh或vl结构域来进行分离,以筛选互补vl或vh结构域的文库。参见,例如,portolano等人,j.immunol.150:880-887(1993);clarkson等人,nature 352:624-628(1991)。
[0105]
如本文所用的术语“载体”是指能够载运与其相连的另一核酸的核酸分子。该术语包括作为自我复制核酸结构的载体,以及并入其已被引入的宿主细胞的基因组中的载体。某些载体能够指导与其可操作地连接的核酸的表达。此类载体在本文中称为“表达载体”。
[0106]
ii.组合物和方法
[0107]
一方面,本发明部分基于发明人对来自能够自然清除慢性乙型肝炎病毒(hbv)感染并获得防止再感染的个体(“控制者”)和接种抗hbv疫苗的个体(“疫苗接种者”)的抗体的鉴定。本发明人已确定此类抗体可能具有有利的特性,诸如对s-hbs抗原的高亲和力或结合活性、有效的中和活性和/或跨基因型反应性。在某些方面,提供了与s-hbs结合的抗体。本发明的抗体可用于例如诊断或治疗乙型肝炎。
[0108]
a.示例性抗s-hbs抗体
[0109]
在一个方面,本发明提供了与s-hbs结合的抗体。在一个方面,提供了与s-hbs结合的分离的抗体。在一个方面,本发明提供了与s-hbs特异性结合的抗体。在某些方面,抗s-hbs抗体具有以下一个或多个特性:
[0110]
·
与s-hbs(例如,seq id no:253的s-hbs)结合;和/或
[0111]
·
与一种或多种具有seq id no:254至262的s-hbs蛋白(例如,至少seq id no:257)结合,任选地与两种或更多种所述蛋白(例如,至少seq id no:257和258)结合,任选地与三种、四种、五种、六种、七种、八种或更多种所述蛋白结合,任选地与所有所述蛋白结合;和/或
[0112]
·
与亚型adw和/或ayw的s-hbs结合,例如基因型d的,优选地为adw和ayw亚型的s-hbs;
[0113]
·
避免了对自身抗原诸如半乳糖凝集素(galectin)-3/-8和e3泛素-蛋白连接酶ubr2的显著的交叉反应性;和/或
[0114]
·
具有针对hbv基因型d的中和活性(例如,如在体外或体内测量的);
[0115]
·
对hbv基因型a至d中的每一种具有中和活性(例如,如在体外或体内测量的);和/或
[0116]
·
可在体内抑制病毒血症。
[0117]
例如,在一些实施例中,抗体可具有在体外测量的≤1ng/ml的针对hbv基因组d的中和ic50值。
[0118]
在其他示例性实施例中,抗体可具有以下特性:
[0119]
·
与seq id no:254至262的蛋白质中的每一种交叉反应;和
[0120]
·
对hbv基因型d具有中和活性(例如,如在体外或体内测量的)。
[0121]
所述示例性抗体还可以优选地避免针对自身抗原诸如半乳糖凝集素-3/-8和e3泛素-蛋白连接酶ubr2的显著的交叉反应性。
[0122]
抗体可以以如本文所述的kd,例如,≤1μm、≤100nm、≤10nm、≤1nm、≤0.1nm、≤0.01nm,或≤0.001nm与s-hbs结合和/或与具有seq id no:254至262的一种或多种s-hbs蛋白结合。在一些实施例中,抗体可以以比针对相同抗原的参考抗体的kd高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于该参考抗体的kd的kd值与s-hbs结合和/或与具有seq id no:254至262的一种或多种s-hbs蛋白结合,其中参考抗体选自由以下项组成的组:bc1.187、bv4.115、bc8.159、bv6.172、bc1.229、bc8.111、bc1.128、bc3.106、bc1.180、bv4.104、bc8.104、bc4.204、bc1.263和bv4.105。
[0123]
替代性地,抗体可以显示出针对s-hbs和/或具有seq id no:254至262的一种或多种s-hbs蛋白的结合活性,该结合活性至少是参考抗体针对相同抗原的结合活性的25%、50%、60%、70%、75%、80%、85%、90%、95%或100%,其中参考抗体选自由以下项组成的组:bc1.187、bv4.115、bc8.159、bv6.172、bc1.229、bc8.111、bc1.128、bc3.106、bc1.180、bv4.104、bc8.104、bc4.204、bc1.263和bv4.105(在同一测定中评估时,例如,elisa测定或流式细胞术测定)。在一些实施例中,优选活性可以为参考抗体活性的至少50%。任选地,参考抗体可以是bc1.187,即当在同一测定中评估时,抗体可以显示出至少25%、50%、60%、70%、75%、80%、85%、90%、95%或100%的bc1.187与参考抗原的结合活性。
[0124]
在其他方面,抗体可以以比参考抗体的ec50高不超过50、10、9、8、7、6,5、4、3或2倍,或小于或等于的ec50与s-hbs结合/或与具有seq id no:254至262的一种或多种s-hbs蛋白结合,其中ec50通过elisa或流式细胞术测量,并且其中参考抗体选自由以下项组成的组:bc1.187、bv4.115、bc8.159、bv6.172、bc1.229、bc8.111、bc1.128、bc3.106、bc1.180、bv4.104、bc8.104、bc4.204、bc1.263和bv4.105。
[0125]“避免显著的交叉反应性”是指抗体不显示与参考蛋白的显著结合,例如具有大于1μm的kd,或例如在本文所述的测定中没有可检测的结合。
[0126]
在一些实施例中,中和针对hbv基因型例如基因型d的根据本发明的抗体可以例如具有≤50ng/ml或≤10ng/ml的体外病毒感染性ic50值。优选抗体可以具有≤1ng/ml、≤500pg/ml或在一些实施例中≤100pg/ml、≤50pg/ml或≤10pg/ml的ic50。在一些实施例中,中和抗体可以具有≤1pg/ml,任选地≤0.1pg/ml的ic50值。任选地,ic50值可以大于0.01pg/ml或0.005pg/ml。在另一个实施例中,中和针对特定hbv基因型例如基因型d的抗体可以具有比参考抗体针对相同基因型的ic50值高不超过50、10、9、8、7、6、5、4、3或2倍或小于或等于其的ic50值,其中参考抗体选自由以下项组成的组:bc1.187、bv4.115、bc8.159、bv6.172、bc1.229、bc8.111、bc1.128、bc3.106、bc1.180、bv4.104、bc8.104、bc4.204、bc1.263和bv4.105(当在同一测定中评估时)。
[0127]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,中和特定hbv基因型的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体对相同基因型的体内中和活性或病毒血症抑制活性,例如,参考抗体选自由以下项组成的组:bc1.187、bv4.115、bc8.159、bv6.172、bc1.229、bc8.111、bc1.128、bc3.106、bc1.180、bv4.104、bc8.104、bc4.204、bc1.263和bv4.105。
[0128]
在一些实施例中,抗体可以与seq id no:254至262的蛋白质中的每一种交叉反应
(例如,如上所述,对每种蛋白质具有结合活性)并且体外中和hbv-基因型d的ic50≤100pg/ml。任选地,ic
50
值可以是≤50pg/ml或≤10pg/ml。在一些实施例中,ic50值可以是≤1pg/ml,任选地≤0.1pg/ml。
[0129]
根据本发明的特定抗体的各种实施例在下面的a-n部分中列出。
[0130]a[0131]
在一个方面,本发明提供了包含vh结构域的抗体,该vh结构域包含选自以下各项的至少一个、至少两个或所有三个vh cdr序列:(a)包含seq id no:1的氨基酸序列的cdr-h1、(b)包含seq id no:2的氨基酸序列的cdr-h2、(c)包含seq id no:3的氨基酸序列的cdr-h3。在另一方面,抗体包含vh结构域,该vh结构域包含以下cdr:(a)包含seq id no:1的氨基酸序列的cdr-h1;(b)包含seq id no:2的氨基酸序列的cdr-h2;和(c)包含seq id no:3的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0132]
在一个方面,vh结构域可以进一步包含一个或多个重链框架序列,该序列选自以下各项:(a)seq id no:7的重链框架区1(hc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:8的重链框架区2(hc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:9的重链框架区3(hc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:10的重链框架区4(hc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vh结构域包含如(a)至(d)中定义的每个重链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0133]
在另一方面,抗s-hbs抗体包含与seq id no:16的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变结构域(vh)序列。一方面,抗s-hbs抗体包含与seq id no:16的氨基酸序列具有至少95%序列同一性的重链可变结构域(vh)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vh序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:16中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:16中的vh序列,包括该序列的翻译后修饰。在一个具体方面,vh包含一、二或三个选自以下各项的cdr:(a)包含seq id no:1的氨基酸序列的cdr-h1,(b)包含seq id no:2的氨基酸序列的cdr-h2和(c)包含seq id no:3的氨基酸序列的cdr-h3。
[0134]
在另一方面,抗s-hbs抗体包含seq id no:16的vh的一个或多个重链cdr序列。在一个方面,抗s-hbs抗体包含seq id no:16的vh结构域的一个或多个(优选所有三个)重链cdr氨基酸序列和与seq id no:16的vh结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0135]
在另一方面,本发明提供了包含vl结构域的抗体,该vl结构域包含选自以下各项的至少一个、至少两个或所有三个vl cdr序列:(a)包含seq id no:4的氨基酸序列的cdr-l1、(b)包含seq id no:5的氨基酸序列的cdr-l2、(c)包含seq id no:6的氨基酸序列的cdr-l3。在另一方面,抗体包含vl结构域,该vh结构域包含以下cdr:(a)包含seq id no:4的氨基酸序列的cdr-l1;(b)包含seq id no:5的氨基酸序列的cdr-l2;和(c)包含seq id no:6的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0136]
在一个方面,抗s-hbs抗体vl结构域可以进一步包含一个或多个轻链框架序列,该序列选自以下各项:(a)seq id no:11的轻链框架区1(lc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:12的轻链框架区2(lc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:13的轻链框架区3(lc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:14的轻链框架区4(lc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vl结构域包含如(a)至(d)中定义的每个轻链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0137]
在另一方面,提供了抗s-hbs抗体,其中该抗体包含与seq id no:15的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变结构域(vl)序列。一方面,抗s-hbs抗体包含与seq id no:15的氨基酸序列具有至少95%序列同一性的轻链可变结构域(vl)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vl序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:15中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:15中的vl序列,包括该序列的翻译后修饰。在一个具体方面,vl包含一、二或三个选自以下各项的cdr:(a)包含seq id no:4的氨基酸序列的cdr-l1,(b)包含seq id no:5的氨基酸序列的cdr-l2和(c)包含seq id no:6的氨基酸序列的cdr-l3。
[0138]
在另一个实施例中,抗s-hbs抗体包含seq id no:15的vl的一个或多个cdr序列。在一个方面,抗s-hbs抗体包含seq id no:15的vl结构域的一个或多个(优选所有三个)轻链cdr氨基酸序列和与seq id no:15的vl结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0139]
在另一方面,提供一种抗s-hbs抗体,其中该抗体包含如在上文提供的任一方面中的vh序列以及如在上文提供的任一方面中的vl序列。
[0140]
例如,在一个示例性实施例中,抗体包含:包含seq id no:3的cdr-h3的vh结构域;和包含seq id no:6的cdr-l3的vl结构域。任选地,vh结构域进一步包含seq id no:2的cdr-h2。
[0141]
在另一示例性实施例中,抗体包含:
[0142]
i)包含以下cdr的vh结构域:(a)包含seq id no:1的氨基酸序列的cdr-h1;(b)包含seq id no:2的氨基酸序列的cdr-h2;和(c)包含seq id no:3的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代;和
[0143]
ii)vl结构域,该vl结构域包含以下cdr:(a)包含seq id no:4的氨基酸序列的cdr-l1;(b)包含seq id no:5的氨基酸序列的cdr-l2;和(c)包含seq id no:6的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0144]
在另一示例性实施例中,抗体包含:
[0145]
i)重链可变结构域(vh)序列,其与seq id no:16的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;以及
[0146]
ii)轻链可变结构域(vl)序列,其与seq id no:15的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。
[0147]
在另一个示例性实施例中,抗s-hbs抗体包含:(a)包含seq id no:1的氨基酸序列的cdr-h1;(b)包含seq id no:2的氨基酸序列的cdr-h2;(c)包含seq id no:3的氨基酸序列的cdr-h3;(d)包含seq id no:4的氨基酸序列的cdr-l1;(e)包含seq id no:5的氨基酸序列的cdr-l2;和(f)包含seq id no:6的氨基酸序列的cdr-l3,和vh结构域,其与seq id no:16的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;和vl结构域,其与seq id no:15的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。在一个方面,vh结构域与seq id no:16的氨基酸序列具有至少95%序列同一性。在一个方面,vl结构域与seq id no:15的氨基酸序列具有至少95%序列同一性。在一个实施例中,抗体与s-hbs特异性结合。在另一个实施例中,抗体与s-hbs结合,其解离常数(kd)与包含seq id no:16的vh序列和seq id no:15的vl序列的抗体的解离常数(kd)相比降低多达10倍或提高多达10倍。
[0148]
一方面,抗体分别包含seq id no:16和seq id no:15中的vh序列和vl序列,包括那些序列的翻译后修饰。
[0149]
在另一方面,抗体可以包含seq id no:17的全长轻链和/或seq id no:18或263的全长重链。
[0150]
在进一步方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体所结合的相同表位结合。例如,在某些方面中,提供了与抗s-hbs抗体所结合的相同表位结合的抗体,该抗体包含seq id no:16的vh序列以及seq id no:15的vl序列。在某些方面,提供了与seq id no:253的s-hbs的以下残基中的一个或多个结合的抗体:c137和任选地c138、k141、g145和/或c149。在一些实施例中,抗体可以进一步与i152、n146、c147和/或t148;和任选地w156中的一个或多个结合。抗体可以包含如上定义的任何序列。
[0151]
在另一方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体竞争结合s-hbs。
[0152]
在一些实施例中,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或
100%的参考抗体bc1.187与s-hbs(例如,seq id no:253的s-hbs)的结合活性。另外地或可替代地,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.187与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254至262的蛋白质中的每一种的结合活性。
[0153]
参考抗体bc1.187是一种抗s-hbs抗体,其包含seq id no:16的vh序列和seq id no:15的vl序列。它具有seq id no:18或263的全长重链和seq id no:17的全长轻链。seq id no:263包含由载体lt615368.1表达的igg1恒定区,如实例中所用。
[0154]
在一些实施例中,当在同一测定中评估时,本节中所述的抗体可以以比参考抗体bc1.187对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与s-hbs(例如seq id no:253的s-hbs)结合。
[0155]
另外地或可替代地,当在同一测定中评估时,如本节中所述的抗体可以以比参考抗体bc1.187对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254-262的蛋白质中的每一种结合。
[0156]
在一些实施例中,如本节中所述的抗体可以以比参考抗体bc1.187的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与s-hbs(例如,seq id no:253的s-hbs)结合,如通过elisa或流式细胞术测量的。可替代地或另外地,抗体可以以比参考抗体bc1.187的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254至262的蛋白质中的每一种结合,如通过elisa或通过流式细胞术测量的。
[0157]
在一些实施例中,如本节中所述的抗体可以具有或保留针对hbv基因型a、b、c和/或d,任选地所有a、b、c和d的体外中和活性。例如,如本节中所述的抗体可以具有或保留针对hbv基因型d的体外中和活性,ic50值≤1pg/ml,任选地≤0.1pg/ml。
[0158]
在另一个实施例中,当使用同一测定(例如,如本文所述的体外中和测定)评估时,抗体可以具有用于中和hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的ic50值,其比参考抗体bc1.187对相同基因型的ic50值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于参考抗体bc1.187对相同基因型的ic50值。
[0159]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.187对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内中和活性。
[0160]
任选地,抗体可以例如在感染hbv基因型a、b、c或d,任选地d的个体中体内抑制病毒血症。任选地,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.187对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内病毒血症抑制活性。
[0161]b[0162]
在一个方面,本发明提供了包含vh结构域的抗体,该vh结构域包含选自以下各项的至少一个、至少两个或所有三个vh cdr序列:(a)包含seq id no:19的氨基酸序列的cdr-h1、(b)包含seq id no:20的氨基酸序列的cdr-h2、(c)包含seq id no:21的氨基酸序列的
cdr-h3。在另一方面,抗体包含vh结构域,该vh结构域包含以下cdr:(a)包含seq id no:19的氨基酸序列的cdr-h1;(b)包含seq id no:20的氨基酸序列的cdr-h2;和(c)包含seq id no:21的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0163]
在一个方面,vh结构域可以进一步包含一个或多个重链框架序列,该序列选自以下各项:(a)seq id no:25的重链框架区1(hc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:26的重链框架区2(hc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:27的重链框架区3(hc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:28的重链框架区4(hc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vh结构域包含如(a)至(d)中定义的每个重链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0164]
在另一方面,抗s-hbs抗体包含与seq id no:34的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变结构域(vh)序列。一方面,抗s-hbs抗体包含与seq id no:34的氨基酸序列具有至少95%序列同一性的重链可变结构域(vh)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vh序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:34中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:34中的vh序列,包括该序列的翻译后修饰。在一个具体方面,vh包含一、二或三个选自以下各项的cdr:(a)包含seq id no:19的氨基酸序列的cdr-h1,(b)包含seq id no:20的氨基酸序列的cdr-h2和(c)包含seq id no:21的氨基酸序列的cdr-h3。
[0165]
在另一方面,抗s-hbs抗体包含seq id no:34的vh的一个或多个重链cdr序列。在一个方面,抗s-hbs抗体包含seq id no:34的vh结构域的一个或多个(优选所有三个)重链cdr氨基酸序列和与seq id no:34的vh结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0166]
在另一方面,本发明提供了包含vl结构域的抗体,该vl结构域包含选自以下各项的至少一个、至少两个或所有三个vl cdr序列:(a)包含seq id no:22的氨基酸序列的cdr-l1、(b)包含seq id no:23的氨基酸序列的cdr-l2、(c)包含seq id no:24的氨基酸序列的cdr-l3。在另一方面,抗体包含vl结构域,该vh结构域包含以下cdr:(a)包含seq id no:22的氨基酸序列的cdr-l1;(b)包含seq id no:23的氨基酸序列的cdr-l2;和(c)包含seq id no:24的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0167]
在一个方面,抗s-hbs抗体vl结构域可以进一步包含一个或多个轻链框架序列,该
序列选自以下各项:(a)seq id no:29的轻链框架区1(lc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:30的轻链框架区2(lc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:31的轻链框架区3(lc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:32的轻链框架区4(lc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vl结构域包含如(a)至(d)中定义的每个轻链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0168]
在另一方面,提供了抗s-hbs抗体,其中该抗体包含与seq id no:33的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变结构域(vl)序列。一方面,抗s-hbs抗体包含与seq id no:33的氨基酸序列具有至少95%序列同一性的轻链可变结构域(vl)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vl序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:33中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:33中的vl序列,包括该序列的翻译后修饰。在一个具体方面,vl包含一、二或三个选自以下各项的cdr:(a)包含seq id no:22的氨基酸序列的cdr-l1,(b)包含seq id no:23的氨基酸序列的cdr-l2和(c)包含seq id no:24的氨基酸序列的cdr-l3。
[0169]
在另一个实施例中,抗s-hbs抗体包含seq id no:33的vl的一个或多个cdr序列。在一个方面,抗s-hbs抗体包含seq id no:33的vl结构域的一个或多个(优选所有三个)轻链cdr氨基酸序列和与seq id no:33的vl结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0170]
在另一方面,提供一种抗s-hbs抗体,其中该抗体包含如在上文提供的任一方面中的vh序列以及如在上文提供的任一方面中的vl序列。
[0171]
例如,在一个示例性实施例中,抗体包含:包含seq id no:21的cdr-h3的vh结构域;和包含seq id no:24的cdr-l3的vl结构域。任选地,vh结构域进一步包含seq id no:20的cdr-h2。
[0172]
在另一示例性实施例中,抗体包含:
[0173]
i)包含以下cdr的vh结构域:(a)包含seq id no:19的氨基酸序列的cdr-h1;(b)包含seq id no:20的氨基酸序列的cdr-h2;和(c)包含seq id no:21的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代;和
[0174]
ii)vl结构域,该vl结构域包含以下cdr:(a)包含seq id no:22的氨基酸序列的cdr-l1;(b)包含seq id no:23的氨基酸序列的cdr-l2;和(c)包含seq id no:24的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或
三个氨基酸被另一种氨基酸取代。
[0175]
在另一示例性实施例中,抗体包含:
[0176]
i)重链可变结构域(vh)序列,其与seq id no:34的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;以及
[0177]
ii)轻链可变结构域(vl)序列,其与seq id no:33的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。
[0178]
在另一个示例性实施例中,抗s-hbs抗体包含:(a)包含seq id no:19的氨基酸序列的cdr-h1;(b)包含seq id no:20的氨基酸序列的cdr-h2;(c)包含seq id no:21的氨基酸序列的cdr-h3;(d)包含seq id no:22的氨基酸序列的cdr-l1;(e)包含seq id no:23的氨基酸序列的cdr-l2;和(f)包含seq id no:24的氨基酸序列的cdr-l3,和vh结构域,其与seq id no:34的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;和vl结构域,其与seq id no:33的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。在一个方面,vh结构域与seq id no:34的氨基酸序列具有至少95%序列同一性。在一个方面,vl结构域与seq id no:33的氨基酸序列具有至少95%序列同一性。在一个实施例中,抗体与s-hbs特异性结合。在另一个实施例中,抗体与s-hbs结合,其解离常数(kd)与包含seq id no:34的vh序列和seq id no:33的vl序列的抗体的解离常数(kd)相比降低多达10倍或提高多达10倍。
[0179]
一方面,抗体分别包含seq id no:34和seq id no:33中的vh序列和vl序列,包括那些序列的翻译后修饰。
[0180]
在另一方面,抗体可以包含seq id no:35的全长轻链和/或seq id no:36或264的全长重链。
[0181]
在进一步方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体所结合的相同表位结合。例如,在某些方面中,提供了与抗s-hbs抗体所结合的相同表位结合的抗体,该抗体包含seq id no:34的vh序列以及seq id no:33的vl序列。在某些方面,提供了与seq id no:253的s-hbs的以下残基中的一个或多个结合的抗体:c138、c139和/或c149,以及任选地r169。任选地,抗体可以进一步与l109、r122、c147、t148、i152、w156、f161和/或w165中的一个或多个结合。抗体可以包含如上定义的任何序列。
[0182]
在另一方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体竞争结合s-hbs。
[0183]
在一些实施例中,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.180与s-hbs(例如,seq id no:253的s-hbs)的结合活性。
[0184]
另外地或可替代地,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.180与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254至262的蛋白质中的每一种的结合活性。
[0185]
参考抗体bc1.180具有seq id no:34的vh序列和seq id no:33的vl序列。它具有seq id no:36或264的全长重链和seq id no:35的全长轻链。seq id no:264包含由载体lt615368.1表达的igg1恒定区,如实例中所用。
[0186]
在一些实施例中,当在同一测定中评估时,本节中所述的抗体可以以比参考抗体bc1.180对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与s-hbs(例如seq id no:253的s-hbs)结合。
[0187]
另外地或可替代地,当在同一测定中评估时,如本节中所述的抗体可以以比参考抗体bc1.180对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254-262的蛋白质中的每一种结合。
[0188]
在一些实施例中,如本节中所述的抗体可以以比参考抗体bc1.180的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与s-hbs(例如,seq id no:253的s-hbs)结合,如通过elisa或流式细胞术测量的。可替代地或另外地,抗体可以以比参考抗体bc1.180的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254至262的蛋白质中的每一种结合,如通过elisa或通过流式细胞术测量的。在一些实施例中,如本节中所述的抗体可以具有或保留针对hbv基因型a、b、c和/或d,任选地所有a、b、c和d的体外中和活性。例如,如本节中所述的抗体可以具有或保留针对hbv基因型d的体外中和活性,例如ic50值≤1pg/ml,任选地≤0.1pg/ml。
[0189]
在另一个实施例中,当使用同一测定(例如,如本文所述的中和测定)进行评估时,抗体可以具有用于中和hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的ic
50
值,其比参考抗体bc1.180对相同基因型的ic50值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于参考抗体bc1.180对相同基因型的ic50值。
[0190]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.180对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内中和活性。
[0191]
任选地,抗体可以例如在感染hbv基因型a、b、c或d,任选地d的个体中体内抑制病毒血症。任选地,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.180对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内病毒血症抑制活性。
[0192]
c.
[0193]
在一个方面,本发明提供了包含vh结构域的抗体,该vh结构域包含选自以下各项的至少一个、至少两个或所有三个vh cdr序列:(a)包含seq id no:37的氨基酸序列的cdr-h1、(b)包含seq id no:38的氨基酸序列的cdr-h2、(c)包含seq id no:39的氨基酸序列的cdr-h3。在另一方面,抗体包含vh结构域,该vh结构域包含以下cdr:(a)包含seq id no:37的氨基酸序列的cdr-h1;(b)包含seq id no:38的氨基酸序列的cdr-h2;和(c)包含seq id no:39的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0194]
在一个方面,vh结构域可以进一步包含一个或多个重链框架序列,该序列选自以下各项:(a)seq id no:43的重链框架区1(hc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:44的重链框架区2(hc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、
91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:45的重链框架区3(hc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:46的重链框架区4(hc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vh结构域包含如(a)至(d)中定义的每个重链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0195]
在另一方面,抗s-hbs抗体包含与seq id no:52的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变结构域(vh)序列。一方面,抗s-hbs抗体包含与seq id no:52的氨基酸序列具有至少95%序列同一性的重链可变结构域(vh)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vh序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:52中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:52中的vh序列,包括该序列的翻译后修饰。在一个具体方面,vh包含一、二或三个选自以下各项的cdr:(a)包含seq id no:37所示的氨基酸序列的cdr-h1,(b)包含seq id no:38所示的氨基酸序列的cdr-h2,以及(c)包含seq id no:39所示的氨基酸序列的cdr-h3。
[0196]
在另一方面,抗s-hbs抗体包含seq id no:52的vh的一个或多个重链cdr序列。在一个方面,抗s-hbs抗体包含seq id no:52的vh结构域的一个或多个(优选所有三个)重链cdr氨基酸序列和与seq id no:52的vh结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0197]
在另一方面,本发明提供了包含vl结构域的抗体,该vl结构域包含选自以下各项的至少一个、至少两个或所有三个vl cdr序列:(a)包含seq id no:40的氨基酸序列的cdr-l1、(b)包含seq id no:41的氨基酸序列的cdr-l2、(c)包含seq id no:42的氨基酸序列的cdr-l3。在另一方面,抗体包含vl结构域,该vh结构域包含以下cdr:(a)包含seq id no:40的氨基酸序列的cdr-l1;(b)包含seq id no:41的氨基酸序列的cdr-l2;和(c)包含seq id no:42的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0198]
在一个方面,抗s-hbs抗体vl结构域可以进一步包含一个或多个轻链框架序列,该序列选自以下各项:(a)seq id no:47的轻链框架区1(lc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:48的轻链框架区2(lc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:49的轻链框架区3(lc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:50的轻链框架区4(lc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vl结构域包含如(a)
至(d)中定义的每个轻链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0199]
在另一方面,提供了抗s-hbs抗体,其中该抗体包含与seq id no:51的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变结构域(vl)序列。一方面,抗s-hbs抗体包含与seq id no:51的氨基酸序列具有至少95%序列同一性的轻链可变结构域(vl)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vl序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:51中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:51中的vl序列,包括该序列的翻译后修饰。在一个具体方面,vl包含一、二或三个选自以下各项的cdr:(a)包含seq id no:40的氨基酸序列的cdr-l1,(b)包含seq id no:41的氨基酸序列的cdr-l2和(c)包含seq id no:42的氨基酸序列的cdr-l3。
[0200]
在另一个实施例中,抗s-hbs抗体包含seq id no:51的vl的一个或多个cdr序列。在一个方面,抗s-hbs抗体包含seq id no:51的vl结构域的一个或多个(优选所有三个)轻链cdr氨基酸序列和与seq id no:51的vl结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0201]
在另一方面,提供一种抗s-hbs抗体,其中该抗体包含如在上文提供的任一方面中的vh序列以及如在上文提供的任一方面中的vl序列。
[0202]
例如,在一个示例性实施例中,抗体包含:包含seq id no:39的cdr-h3的vh结构域;和包含seq id no:42的cdr-l3的vl结构域。任选地,vh结构域进一步包含seq id no:38的cdr-h2。
[0203]
在另一示例性实施例中,抗体包含:
[0204]
i)包含以下cdr的vh结构域:(a)包含seq id no:37的氨基酸序列的cdr-h1;(b)包含seq id no:38的氨基酸序列的cdr-h2;和(c)包含seq id no:39的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代;和
[0205]
ii)vl结构域,该vl结构域包含以下cdr:(a)包含seq id no:40的氨基酸序列的cdr-l1;(b)包含seq id no:41的氨基酸序列的cdr-l2;和(c)包含seq id no:42的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0206]
在另一示例性实施例中,抗体包含:
[0207]
i)重链可变结构域(vh)序列,其与seq id no:52的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;以及
[0208]
ii)轻链可变结构域(vl)序列,其与seq id no:51的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。
[0209]
在另一个示例性实施例中,抗s-hbs抗体包含:(a)包含seq id no:37的氨基酸序列的cdr-h1;(b)包含seq id no:38的氨基酸序列的cdr-h2;(c)包含seq id no:39的氨基
hbs)结合,如通过elisa或流式细胞术测量的。可替代地或另外地,抗体可以以比参考抗体bc3.106的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254至262的蛋白质中的每一种结合,如通过elisa或通过流式细胞术测量的。
[0220]
在一些实施例中,如本节中所述的抗体可以具有或保留针对hbv基因型a、b、c和/或d,任选地所有a、b、c和d的体外中和活性。例如,如本节中所述的抗体可以具有或保留针对hbv基因型d的体外中和活性,例如ic50值≤10pg/ml,任选地≤1pg/ml。
[0221]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有用于中和hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的ic
50
值,其比参考抗体bc3.106对相同基因型的ic
50
值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于参考抗体bc3.106对相同基因型的ic50值。
[0222]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc3.106对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内中和活性。
[0223]
任选地,抗体可以例如在感染hbv基因型a、b、c或d,任选地d的个体中体内抑制病毒血症。任选地,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc3.106对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内病毒血症抑制活性。
[0224]
d.
[0225]
在一个方面,本发明提供了包含vh结构域的抗体,该vh结构域包含选自以下各项的至少一个、至少两个或所有三个vh cdr序列:(a)包含seq id no:55的氨基酸序列的cdr-h1、(b)包含seq id no:56的氨基酸序列的cdr-h2、(c)包含seq id no:57的氨基酸序列的cdr-h3。在另一方面,抗体包含vh结构域,该vh结构域包含以下cdr:(a)包含seq id no:55的氨基酸序列的cdr-h1;(b)包含seq id no:56的氨基酸序列的cdr-h2;和(c)包含seq id no:57的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0226]
在一个方面,vh结构域可以进一步包含一个或多个重链框架序列,该序列选自以下各项:(a)seq id no:61的重链框架区1(hc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:62的重链框架区2(hc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:63的重链框架区3(hc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:64的重链框架区4(hc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vh结构域包含如(a)至(d)中定义的每个重链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0227]
在另一方面,抗s-hbs抗体包含与seq id no:70的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变结构域
(vh)序列。一方面,抗s-hbs抗体包含与seq id no:70的氨基酸序列具有至少95%序列同一性的重链可变结构域(vh)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vh序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:70中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:70中的vh序列,包括该序列的翻译后修饰。在一个具体方面,vh包含一、二或三个选自以下各项的cdr:(a)包含seq id no:55所示的氨基酸序列的cdr-h1,(b)包含seq id no:56所示的氨基酸序列的cdr-h2,以及(c)包含seq id no:57所示的氨基酸序列的cdr-h3。
[0228]
在另一方面,抗s-hbs抗体包含seq id no:70的vh的一个或多个重链cdr序列。在一个方面,抗s-hbs抗体包含seq id no:70的vh结构域的一个或多个(优选所有三个)重链cdr氨基酸序列和与seq id no:70的vh结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0229]
在另一方面,本发明提供了包含vl结构域的抗体,该vl结构域包含选自以下各项的至少一个、至少两个或所有三个vl cdr序列:(a)包含seq id no:58的氨基酸序列的cdr-l1、(b)包含seq id no:59的氨基酸序列的cdr-l2、(c)包含seq id no:60的氨基酸序列的cdr-l3。在另一方面,抗体包含vl结构域,该vh结构域包含以下cdr:(a)包含seq id no:58的氨基酸序列的cdr-l1;(b)包含seq id no:59的氨基酸序列的cdr-l2;和(c)包含seq id no:60的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0230]
在一个方面,抗s-hbs抗体vl结构域可以进一步包含一个或多个轻链框架序列,该序列选自以下各项:(a)seq id no:65的轻链框架区1(lc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:66的轻链框架区2(lc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:67的轻链框架区3(lc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:68的轻链框架区4(lc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vl结构域包含如(a)至(d)中定义的每个轻链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0231]
在另一方面,提供了抗s-hbs抗体,其中该抗体包含与seq id no:69的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变结构域(vl)序列。一方面,抗s-hbs抗体包含与seq id no:69的氨基酸序列具有至少95%序列同一性的轻链可变结构域(vl)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vl序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:69中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方
面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:69中的vl序列,包括该序列的翻译后修饰。在一个具体方面,vl包含一、二或三个选自以下各项的cdr:(a)包含seq id no:58的氨基酸序列的cdr-l1,(b)包含seq id no:59的氨基酸序列的cdr-l2和(c)包含seq id no:60的氨基酸序列的cdr-l3。
[0232]
在另一个实施例中,抗s-hbs抗体包含seq id no:69的vl的一个或多个cdr序列。在一个方面,抗s-hbs抗体包含seq id no:69的vl结构域的一个或多个(优选所有三个)轻链cdr氨基酸序列和与seq id no:69的vl结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0233]
在另一方面,提供一种抗s-hbs抗体,其中该抗体包含如在上文提供的任一方面中的vh序列以及如在上文提供的任一方面中的vl序列。
[0234]
例如,在一个示例性实施例中,抗体包含:包含seq id no:57的cdr-h3的vh结构域;和包含seq id no:60的cdr-l3的vl结构域。任选地,vh结构域进一步包含seq id no:56的cdr-h2。
[0235]
在另一示例性实施例中,抗体包含:
[0236]
i)包含以下cdr的vh结构域:(a)包含seq id no:55的氨基酸序列的cdr-h1;(b)包含seq id no:56的氨基酸序列的cdr-h2;和(c)包含seq id no:57的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代;和
[0237]
ii)vl结构域,该vl结构域包含以下cdr:(a)包含seq id no:58的氨基酸序列的cdr-l1;(b)包含seq id no:59的氨基酸序列的cdr-l2;和(c)包含seq id no:60的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0238]
在另一示例性实施例中,抗体包含:
[0239]
i)重链可变结构域(vh)序列,其与seq id no:70的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;以及
[0240]
ii)轻链可变结构域(vl)序列,其与seq id no:69的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。
[0241]
在另一个示例性实施例中,抗s-hbs抗体包含:(a)包含seq id no:55的氨基酸序列的cdr-h1;(b)包含seq id no:56的氨基酸序列的cdr-h2;(c)包含seq id no:57的氨基酸序列的cdr-h3;(d)包含seq id no:58的氨基酸序列的cdr-l1;(e)包含seq id no:59的氨基酸序列的cdr-l2;和(f)包含seq id no:60的氨基酸序列的cdr-l3,和vh结构域,其与seq id no:70的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;和vl结构域,其与seq id no:69的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。在一个方面,vh结构域与seq id no:70的氨基酸序列具有至少95%序列同一性。在一个方面,vl结构域与seq id no:69的氨基酸序列具有至少95%序列同一性。在一个实施例中,抗体与s-hbs特异性结合。在另一个实施例中,抗体与s-hbs结合,其解离常数(kd)与包含seq id no:70的vh序列和seq id no:69的vl序列的抗体的解离常数(kd)相比降低多达10倍或提高多达10倍。
[0242]
一方面,抗体分别包含seq id no:70和seq id no:69中的vh序列和vl序列,包括那些序列的翻译后修饰。
[0243]
在另一方面,抗体可以包含seq id no:71的全长轻链和/或seq id no:72或266的全长重链。
[0244]
在进一步方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体所结合的相同表位结合。例如,在某些方面中,提供了与抗s-hbs抗体所结合的相同表位结合的抗体,该抗体包含seq id no:70的vh序列以及seq id no:69的vl序列。在某些方面,提供了与seq id no:253的s-hbs的以下残基中的一个或多个结合的抗体:c121、r122、c124、c137、c139、k141、n146、c147和/或c149。在一些实施例中,抗体还可以与i110、t118、p120、c138、p142、d144、t148和/或i152中的一个或多个结合。抗体可以包含如上定义的任何序列。
[0245]
在另一方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体竞争结合s-hbs。
[0246]
在一些实施例中,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv4.104与s-hbs(例如,seq id no:253的s-hbs)的结合活性。
[0247]
另外地或可替代地,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv4.104与seq id no:257和258中的一个或多个或seq id no:257和258的蛋白质中的每一种、任选地至少seq id no:257的蛋白质的结合活性。
[0248]
参考抗体bv4.104具有seq id no:70的vh序列和seq id no:69的vl序列。它具有seq id no:72或266的全长重链和seq d no:71的全长轻链。seq id no:266包含由载体lt615368.1表达的igg1恒定区,如实例中所用。
[0249]
在一些实施例中,当在同一测定中评估时,本节中所述的抗体可以以比参考抗体bv4.104对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与s-hbs(例如seq id no:253的s-hbs)结合。
[0250]
另外地或可替代地,当在同一测定中评估时,抗体可以以比参考抗体bv4.104对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与seq id no:257和258中的一个或多个或seq id no:257和258的蛋白质中的每一种、任选地至少seq id no:257的蛋白质结合。
[0251]
在一些实施例中,如本节中所述的抗体可以以比参考抗体bv4.104的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与s-hbs(例如,seq id no:253的s-hbs)结合,如通过elisa或流式细胞术测量的。可替代地或另外地,抗体可以以比参考抗体bv4.104的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与seq id no:257和258中的一个或多个或seq id no:257和258的蛋白质中的每一种、任选地至少seq id no:257的蛋白质结合,如通过elisa或通过流式细胞术测量的。
[0252]
在一些实施例中,如本节中所述的抗体可具有或保留针对hbv基因型d的体外中和活性,例如ic50值≤100pg/ml、任选地≤10pg/ml。
[0253]
在另一个实施例中,当使用同一测定(例如,如本文所述的体外中和测定)评估时,抗体可以具有用于中和hbv基因型d的ic
50
值,其比参考抗体bv4.104对相同基因型的ic
50
值
高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于参考抗体bv4.104对相同基因型的ic50值。
[0254]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv4.104对hbv基因型d的体内中和活性。
[0255]
任选地,抗体可以例如在感染hbv基因型d的个体中体内抑制病毒血症。任选地,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv4.104对hbv基因型d的体内病毒血症抑制活性。
[0256]
e.
[0257]
在一个方面,本发明提供了包含vh结构域的抗体,该vh结构域包含选自以下各项的至少一个、至少两个或所有三个vh cdr序列:(a)包含seq id no:73的氨基酸序列的cdr-h1、(b)包含seq id no:74的氨基酸序列的cdr-h2、(c)包含seq id no:75的氨基酸序列的cdr-h3。在另一方面,抗体包含vh结构域,该vh结构域包含以下cdr:(a)包含seq id no:73的氨基酸序列的cdr-h1;(b)包含seq id no:74的氨基酸序列的cdr-h2;和(c)包含seq id no:75的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0258]
在一个方面,vh结构域可以进一步包含一个或多个重链框架序列,该序列选自以下各项:(a)seq id no:79的重链框架区1(hc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:80的重链框架区2(hc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:81的重链框架区3(hc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:82的重链框架区4(hc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vh结构域包含如(a)至(d)中定义的每个重链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0259]
在另一方面,抗s-hbs抗体包含与seq id no:88的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变结构域(vh)序列。一方面,抗s-hbs抗体包含与seq id no:88的氨基酸序列具有至少95%序列同一性的重链可变结构域(vh)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vh序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:88中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:88中的vh序列,包括该序列的翻译后修饰。在一个具体方面,vh包含一、二或三个选自以下各项的cdr:(a)包含seq id no:73所示的氨基酸序列的cdr-h1,(b)包含seq id no:74所示的氨基酸序列的cdr-h2,以及(c)包含seq id no:75所示的氨基酸序列的cdr-h3。
[0260]
在另一方面,抗s-hbs抗体包含seq id no:88的vh的一个或多个重链cdr序列。在一个方面,抗s-hbs抗体包含seq id no:88的vh结构域的一个或多个(优选所有三个)重链cdr氨基酸序列和与seq id no:88的vh结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0261]
在另一方面,本发明提供了包含vl结构域的抗体,该vl结构域包含选自以下各项的至少一个、至少两个或所有三个vl cdr序列:(a)包含seq id no:76的氨基酸序列的cdr-l1、(b)包含seq id no:77的氨基酸序列的cdr-l2、(c)包含seq id no:78的氨基酸序列的cdr-l3。在另一方面,抗体包含vl结构域,该vh结构域包含以下cdr:(a)包含seq id no:76的氨基酸序列的cdr-l1;(b)包含seq id no:77的氨基酸序列的cdr-l2;和(c)包含seq id no:78的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0262]
在一个方面,抗s-hbs抗体vl结构域可以进一步包含一个或多个轻链框架序列,该序列选自以下各项:(a)seq id no:83的轻链框架区1(lc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:84的轻链框架区2(lc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:85的轻链框架区3(lc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:86的轻链框架区4(lc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vl结构域包含如(a)至(d)中定义的每个轻链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0263]
在另一方面,提供了抗s-hbs抗体,其中该抗体包含与seq id no:87的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变结构域(vl)序列。一方面,抗s-hbs抗体包含与seq id no:87的氨基酸序列具有至少95%序列同一性的轻链可变结构域(vl)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vl序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:87中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:87中的vl序列,包括该序列的翻译后修饰。在一个具体方面,vl包含一、二或三个选自以下各项的cdr:(a)包含seq id no:76的氨基酸序列的cdr-l1,(b)包含seq id no:77的氨基酸序列的cdr-l2和(c)包含seq id no:78的氨基酸序列的cdr-l3。
[0264]
在另一个实施例中,抗s-hbs抗体包含seq id no:87的vl的一个或多个cdr序列。在一个方面,抗s-hbs抗体包含seq id no:87的vl结构域的一个或多个(优选所有三个)轻链cdr氨基酸序列和与seq id no:87的vl结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0265]
在另一方面,提供一种抗s-hbs抗体,其中该抗体包含如在上文提供的任一方面中的vh序列以及如在上文提供的任一方面中的vl序列。
[0266]
例如,在一个示例性实施例中,抗体包含:包含seq id no:75的cdr-h3的vh结构域;和包含seq id no:78的cdr-l3的vl结构域。任选地,vh结构域进一步包含seq id no:74的cdr-h2。
[0267]
在另一示例性实施例中,抗体包含:
[0268]
i)包含以下cdr的vh结构域:(a)包含seq id no:73的氨基酸序列的cdr-h1;(b)包含seq id no:74的氨基酸序列的cdr-h2;和(c)包含seq id no:75的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代;和
[0269]
ii)vl结构域,该vl结构域包含以下cdr:(a)包含seq id no:76的氨基酸序列的cdr-l1;(b)包含seq id no:77的氨基酸序列的cdr-l2;和(c)包含seq id no:78的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0270]
在另一示例性实施例中,抗体包含:
[0271]
i)重链可变结构域(vh)序列,其与seq id no:88的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;以及
[0272]
ii)轻链可变结构域(vl)序列,其与seq id no:87的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。
[0273]
在另一个示例性实施例中,抗s-hbs抗体包含:(a)包含seq id no:73的氨基酸序列的cdr-h1;(b)包含seq id no:74的氨基酸序列的cdr-h2;(c)包含seq id no:75的氨基酸序列的cdr-h3;(d)包含seq id no:76的氨基酸序列的cdr-l1;(e)包含seq id no:77的氨基酸序列的cdr-l2;和(f)包含seq id no:78的氨基酸序列的cdr-l3,和vh结构域,其与seq id no:88的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;和vl结构域,其与seq id no:87的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。在一个方面,vh结构域与seq id no:88的氨基酸序列具有至少95%序列同一性。在一个方面,vl结构域与seq id no:87的氨基酸序列具有至少95%序列同一性。在一个实施例中,抗体与s-hbs特异性结合。在另一个实施例中,抗体与s-hbs结合,其解离常数(kd)与包含seq id no:88的vh序列和seq id no:87的vl序列的抗体的解离常数(kd)相比降低多达10倍或提高多达10倍。
[0274]
一方面,抗体分别包含seq id no:88和seq id no:87中的vh序列和vl序列,包括那些序列的翻译后修饰。
[0275]
在另一方面,抗体可以包含seq id no:89的全长轻链和/或seq id no:90或267的全长重链。
[0276]
在进一步方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体所结合的相同表位结合。例如,在某些方面中,提供了与抗s-hbs抗体所结合的相同表位结合的抗体,该抗体包含seq id no:88的vh序列以及seq id no:87的vl序列。在某些方面,提供了与seq id no:253的s-hbs的以下残基中的一个或多个结合的抗体:c121,和/或i110、p120、c124、c137、c139、c147、t148和/或c149中的一个或多个。任选地,抗体可以进一步与c138、k141、
p142、d144、g145、p150、i152和/或w156中的一个或多个结合。抗体可以包含如上定义的任何序列。
[0277]
在另一方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体竞争结合s-hbs。
[0278]
在一些实施例中,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc8.111与s-hbs(例如,seq id no:253的s-hbs)的结合活性。
[0279]
另外地或可替代地,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc8.111与seq id no:254-262的蛋白质中的一种或多种(例如,至少seq id no:257)、任选地seq id no:254至262的蛋白质中的每一种的结合活性。
[0280]
参考抗体bc8.111具有seq id no:88的vh序列和seq id no:87的vl序列。它具有seq id no:90或267的全长重链和seq id no:89的全长轻链。seq id no:267包含由载体lt615368.1表达的igg1恒定区,如实例中所用。在一些实施例中,当在同一测定中评估时,本节中所述的抗体可以以比参考抗体bc8.111对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与s-hbs(例如seq id no:253的s-hbs)结合。
[0281]
另外地或可替代地,当在同一测定中评估时,抗体可以以比参考抗体bc8.111对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254-262的蛋白质中的每一种结合。
[0282]
在一些实施例中,如本节中所述的抗体可以以比参考抗体bc8.111的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与s-hbs(例如,seq id no:253的s-hbs)结合,如通过elisa或流式细胞术测量的。可替代地或另外地,抗体可以以比参考抗体bc8.111的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与seq id no:254-262中的一个或多个或seq id no:254-262的蛋白质中的每一种、任选地至少seq id no:257的蛋白质结合,如通过elisa或通过流式细胞术测量的。
[0283]
在一些实施例中,如本节中所述的抗体可以具有或保留针对hbv基因型a、b、c和/或d,任选地所有a、b、c和d的体外中和活性。例如,如本节中所述的抗体可以具有或保留针对hbv基因型d的体外中和活性,例如ic
50
值≤100pg/ml,任选地≤10pg/ml。
[0284]
在另一个实施例中,当使用同一测定(例如,如本文所述的体外中和测定)进行评估时,抗体可以具有用于中和hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的ic
50
值,其比参考抗体bc8.111对相同基因型的ic50值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于参考抗体bc8.111对相同基因型的ic50值。
[0285]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc8.111对hbv基因型a、b、c和/或d的体内中和活性。
[0286]
任选地,抗体可以例如在感染hbv基因型a、b、c或d、任选地d的个体中体内抑制病毒血症。任选地,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc8.111对hbv基因
型a、b、c和/或d的体内病毒血症抑制活性。
[0287]
f.
[0288]
在一个方面,本发明提供了包含vh结构域的抗体,该vh结构域包含选自以下各项的至少一个、至少两个或所有三个vh cdr序列:(a)包含seq id no:91的氨基酸序列的cdr-h1、(b)包含seq id no:92的氨基酸序列的cdr-h2、(c)包含seq id no:93的氨基酸序列的cdr-h3。在另一方面,抗体包含vh结构域,该vh结构域包含以下cdr:(a)包含seq id no:91的氨基酸序列的cdr-h1;(b)包含seq id no:92的氨基酸序列的cdr-h2;和(c)包含seq id no:93的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0289]
在一个方面,vh结构域可以进一步包含一个或多个重链框架序列,该序列选自以下各项:(a)seq id no:97的重链框架区1(hc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:98的重链框架区2(hc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:99的重链框架区3(hc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:100的重链框架区4(hc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vh结构域包含如(a)至(d)中定义的每个重链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0290]
在另一方面,抗s-hbs抗体包含与seq id no:106的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变结构域(vh)序列。一方面,抗s-hbs抗体包含与seq id no:106的氨基酸序列具有至少95%序列同一性的重链可变结构域(vh)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vh序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:106中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:106中的vh序列,包括该序列的翻译后修饰。在一个具体方面,vh包含一、二或三个选自以下各项的cdr:(a)包含seq id no:91所示的氨基酸序列的cdr-h1,(b)包含seq id no:92所示的氨基酸序列的cdr-h2,以及(c)包含seq id no:93所示的氨基酸序列的cdr-h3。
[0291]
在另一方面,抗s-hbs抗体包含seq id no:106的vh的一个或多个重链cdr序列。在一个方面,抗s-hbs抗体包含seq id no:106的vh结构域的一个或多个(优选所有三个)重链cdr氨基酸序列和与seq id no:106的vh结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0292]
在另一方面,本发明提供了包含vl结构域的抗体,该vl结构域包含选自以下各项的至少一个、至少两个或所有三个vl cdr序列:(a)包含seq id no:94的氨基酸序列的cdr-l1、(b)包含seq id no:95的氨基酸序列的cdr-l2、(c)包含seq id no:96的氨基酸序列的
cdr-l3。在另一方面,抗体包含vl结构域,该vh结构域包含以下cdr:(a)包含seq id no:94的氨基酸序列的cdr-l1;(b)包含seq id no:95的氨基酸序列的cdr-l2;和(c)包含seq id no:96的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0293]
在一个方面,抗s-hbs抗体vl结构域可以进一步包含一个或多个轻链框架序列,该序列选自以下各项:(a)seq id no:101的轻链框架区1(lc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:102的轻链框架区2(lc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:103的轻链框架区3(lc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:104的轻链框架区4(lc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vl结构域包含如(a)至(d)中定义的每个轻链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0294]
在另一方面,提供了抗s-hbs抗体,其中该抗体包含与seq id no:105的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变结构域(vl)序列。一方面,抗s-hbs抗体包含与seq id no:105的氨基酸序列具有至少95%序列同一性的轻链可变结构域(vl)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vl序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:105中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:105中的vl序列,包括该序列的翻译后修饰。在一个具体方面,vl包含一、二或三个选自以下各项的cdr:(a)包含seq id no:94的氨基酸序列的cdr-l1,(b)包含seq id no:95的氨基酸序列的cdr-l2和(c)包含seq id no:96的氨基酸序列的cdr-l3。
[0295]
在另一个实施例中,抗s-hbs抗体包含seq id no:105的vl的一个或多个cdr序列。在一个方面,抗s-hbs抗体包含seq id no:105的vl结构域的一个或多个(优选所有三个)轻链cdr氨基酸序列和与seq id no:105的vl结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0296]
在另一方面,提供一种抗s-hbs抗体,其中该抗体包含如在上文提供的任一方面中的vh序列以及如在上文提供的任一方面中的vl序列。
[0297]
例如,在一个示例性实施例中,抗体包含:包含seq id no:93的cdr-h3的vh结构域;和包含seq id no:96的cdr-l3的vl结构域。任选地,vh结构域进一步包含seq id no:92的cdr-h2。
[0298]
在另一示例性实施例中,抗体包含:
[0299]
i)包含以下cdr的vh结构域:(a)包含seq id no:91的氨基酸序列的cdr-h1;(b)包含seq id no:92的氨基酸序列的cdr-h2;和(c)包含seq id no:93的氨基酸序列的cdr-h3;
或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代;和
[0300]
ii)vl结构域,该vl结构域包含以下cdr:(a)包含seq id no:94的氨基酸序列的cdr-l1;(b)包含seq id no:95的氨基酸序列的cdr-l2;和(c)包含seq id no:96的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0301]
在另一示例性实施例中,抗体包含:
[0302]
i)重链可变结构域(vh)序列,其与seq id no:106的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;以及
[0303]
ii)轻链可变结构域(vl)序列,其与seq id no:105的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。
[0304]
在另一个示例性实施例中,抗s-hbs抗体包含:(a)包含seq id no:91的氨基酸序列的cdr-h1;(b)包含seq id no:92的氨基酸序列的cdr-h2;(c)包含seq id no:93的氨基酸序列的cdr-h3;(d)包含seq id no:94的氨基酸序列的cdr-l1;(e)包含seq id no:95的氨基酸序列的cdr-l2;和(f)包含seq id no:96的氨基酸序列的cdr-l3,和vh结构域,其与seq id no:106的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;和vl结构域,其与seq id no:105的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。在一个方面,vh结构域与seq id no:106的氨基酸序列具有至少95%序列同一性。在一个方面,vl结构域与seq id no 105的氨基酸序列具有至少95%序列同一性。在一个实施例中,抗体与s-hbs特异性结合。在另一个实施例中,抗体与s-hbs结合,其解离常数(kd)与包含seq id no:106的vh序列和seq id no:105的vl序列的抗体的解离常数(kd)相比降低多达10倍或提高多达10倍。
[0305]
一方面,抗体分别包含seq id no:106和seq id no:105中的vh序列和vl序列,包括那些序列的翻译后修饰。
[0306]
在另一方面,抗体可以包含seq id no:107的全长轻链和/或seq id no:108或268的全长重链。
[0307]
在进一步方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体所结合的相同表位结合。例如,在某些方面中,提供了与抗s-hbs抗体所结合的相同表位结合的抗体,该抗体包含seq id no:106的vh序列以及seq id no:105的vl序列。在某些方面,提供了与seq id no:253的s-hbs的以下残基中的一个或多个结合的抗体:w156和/或r169。任选地,抗体可以另外与i152和/或c138中的一个或多个结合。抗体可以包含如上定义的任何序列。
[0308]
在另一方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体竞争结合s-hbs。
[0309]
在一些实施例中,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc8.104与s-hbs(例如,seq id no:253的s-hbs)的结合活性。
[0310]
另外地或可替代地,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或
100%的参考抗体bc8.104与seq id no:254-262的蛋白质中的一种或多种(例如,至少seq id no:257)、任选地seq id no:254至262的蛋白质中的每一种的结合活性。
[0311]
参考抗体bc8.104具有seq id no:106的vh序列和seq id no:105的vl序列。它具有seq id no:108或268的全长重链和seq id no:107的全长轻链。seq id no:268包含由载体lt615368.1表达的igg1恒定区,如实例中所用。
[0312]
在一些实施例中,当在同一测定中评估时,本节中所述的抗体可以以比参考抗体bc8.104对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与s-hbs(例如seq id no:253的s-hbs)结合。
[0313]
另外地或可替代地,当在同一测定中评估时,本节中所述的抗体可以以比参考抗体bc8.104对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254-262的蛋白质中的每一种结合。
[0314]
在一些实施例中,如本节中所述的抗体可以以比参考抗体bc8.104的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与s-hbs(例如,seq id no:253的s-hbs)结合,如通过elisa或流式细胞术测量的。可替代地或另外地,抗体可以以比参考抗体bc8.104的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与seq id no:254-262中的一个或多个或seq id no:254-262的蛋白质中的每一种、任选地至少seq id no:257的蛋白质结合,如通过elisa或通过流式细胞术测量的。
[0315]
在一些实施例中,如本节中所述的抗体可以具有或保留针对hbv基因型a、b、c和/或d,任选地所有a、b、c和d的体外中和活性。例如,如本节中所述的抗体可以具有或保留针对hbv基因型d的体外中和活性,例如ic50值≤100pg/ml,任选地≤10pg/ml。
[0316]
在另一个实施例中,当使用同一测定(例如,如本文所述的体外中和测定)评估时,抗体可以具有用于中和hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的ic50值,其比参考抗体bc8.104对相同基因型的ic50值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于参考抗体bc8.104对相同基因型的ic50值。
[0317]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc8.104对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的中和活性。
[0318]
任选地,抗体可以例如在感染hbv基因型a、b、c或d,任选地d的个体中体内抑制病毒血症。任选地,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc8.104对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内病毒血症抑制活性。
[0319]
g.
[0320]
在一个方面,本发明提供了包含vh结构域的抗体,该vh结构域包含选自以下各项的至少一个、至少两个或所有三个vh cdr序列:(a)包含seq id no:109的氨基酸序列的cdr-h1、(b)包含seq id no:110的氨基酸序列的cdr-h2、(c)包含seq id no:111的氨基酸序列的cdr-h3。在另一方面,抗体包含vh结构域,该vh结构域包含以下cdr:(a)包含seq id no:109的氨基酸序列的cdr-h1;(b)包含seq id no:110的氨基酸序列的cdr-h2;和(c)包含seq id no:111的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个
或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0321]
在一个方面,vh结构域可以进一步包含一个或多个重链框架序列,该序列选自以下各项:(a)seq id no:115的重链框架区1(hc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:116的重链框架区2(hc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:117的重链框架区3(hc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:118的重链框架区4(hc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vh结构域包含如(a)至(d)中定义的每个重链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0322]
在另一方面,抗s-hbs抗体包含与seq id no:124的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变结构域(vh)序列。一方面,抗s-hbs抗体包含与seq id no:124的氨基酸序列具有至少95%序列同一性的重链可变结构域(vh)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vh序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:124中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:124中的vh序列,包括该序列的翻译后修饰。在一个具体方面,vh包含一、二或三个选自以下各项的cdr:(a)包含seq id no:109所示的氨基酸序列的cdr-h1,(b)包含seq id no:110所示的氨基酸序列的cdr-h2,以及(c)包含seq id no:111所示的氨基酸序列的cdr-h3。
[0323]
在另一方面,抗s-hbs抗体包含seq id no:124的vh的一个或多个重链cdr序列。在一个方面,抗s-hbs抗体包含seq id no:124的vh结构域的一个或多个(优选所有三个)重链cdr氨基酸序列和与seq id no:124的vh结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0324]
在另一方面,本发明提供了包含vl结构域的抗体,该vl结构域包含选自以下各项的至少一个、至少两个或所有三个vl cdr序列:(a)包含seq id no:112的氨基酸序列的cdr-l1、(b)包含seq id no:113的氨基酸序列的cdr-l2、(c)包含seq id no:114的氨基酸序列的cdr-l3。在另一方面,抗体包含vl结构域,该vh结构域包含以下cdr:(a)包含seq id no:112的氨基酸序列的cdr-l1;(b)包含seq id no:113的氨基酸序列的cdr-l2;和(c)包含seq id no:114的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0325]
在一个方面,抗s-hbs抗体vl结构域可以进一步包含一个或多个轻链框架序列,该序列选自以下各项:(a)seq id no:119的轻链框架区1(lc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:120的轻链框架区2(lc-fr2)或与其具有至少85%、86%、87%、
88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:121的轻链框架区3(lc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:122的轻链框架区4(lc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vl结构域包含如(a)至(d)中定义的每个轻链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0326]
在另一方面,提供了抗s-hbs抗体,其中该抗体包含与seq id no:123的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变结构域(vl)序列。一方面,抗s-hbs抗体包含与seq id no:123的氨基酸序列具有至少95%序列同一性的轻链可变结构域(vl)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vl序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:123中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:123中的vl序列,包括该序列的翻译后修饰。在一个具体方面,vl包含一、二或三个选自以下各项的cdr:(a)包含seq id no:112的氨基酸序列的cdr-l1,(b)包含seq id no:113的氨基酸序列的cdr-l2和(c)包含seq id no:114的氨基酸序列的cdr-l3。
[0327]
在另一个实施例中,抗s-hbs抗体包含seq id no:123的vl的一个或多个cdr序列。在一个方面,抗s-hbs抗体包含seq id no:123的vl结构域的一个或多个(优选所有三个)轻链cdr氨基酸序列和与seq id no:123的vl结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0328]
在另一方面,提供一种抗s-hbs抗体,其中该抗体包含如在上文提供的任一方面中的vh序列以及如在上文提供的任一方面中的vl序列。
[0329]
例如,在一个示例性实施例中,抗体包含:包含seq id no:111的cdr-h3的vh结构域;和包含seq id no:114的cdr-l3的vl结构域。任选地,vh结构域进一步包含seq id no:110的cdr-h2。
[0330]
在另一示例性实施例中,抗体包含:
[0331]
i)包含以下cdr的vh结构域:(a)包含seq id no:109的氨基酸序列的cdr-h1;(b)包含seq id no:110的氨基酸序列的cdr-h2;和(c)包含seq id no:111的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代;和
[0332]
ii)vl结构域,该vl结构域包含以下cdr:(a)包含seq id no:112的氨基酸序列的cdr-l1;(b)包含seq id no:113的氨基酸序列的cdr-l2;和(c)包含seq id no:114的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0333]
在另一示例性实施例中,抗体包含:
[0334]
i)重链可变结构域(vh)序列,其与seq id no:124的氨基酸序列具有至少90%、
91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;以及
[0335]
ii)轻链可变结构域(vl)序列,其与seq id no:123的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。
[0336]
在另一个示例性实施例中,抗s-hbs抗体包含:(a)包含seq id no:109的氨基酸序列的cdr-h1;(b)包含seq id no:110的氨基酸序列的cdr-h2;(c)包含seq id no:111的氨基酸序列的cdr-h3;(d)包含seq id no:112的氨基酸序列的cdr-l1;(e)包含seq id no:113的氨基酸序列的cdr-l2;和(f)包含seq id no:114的氨基酸序列的cdr-l3,和vh结构域,其与seq id no:124的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;和vl结构域,其与seq id no:123的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。在一个方面,vh结构域与seq id no:124的氨基酸序列具有至少95%序列同一性。在一个方面,vl结构域与seq id no 123的氨基酸序列具有至少95%序列同一性。在一个实施例中,抗体与s-hbs特异性结合。在另一个实施例中,抗体与s-hbs结合,其解离常数(kd)与包含seq id no:124的vh序列和seq id no:123的vl序列的抗体的解离常数(kd)相比降低多达10倍或提高多达10倍。
[0337]
一方面,抗体分别包含seq id no:124和seq id no:123中的vh序列和vl序列,包括那些序列的翻译后修饰。
[0338]
在另一方面,抗体可以包含seq id no:125的全长轻链和/或seq id no:126或269的全长重链。
[0339]
在进一步方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体所结合的相同表位结合。例如,在某些方面中,提供了与抗s-hbs抗体所结合的相同表位结合的抗体,该抗体包含seq id no:124的vh序列以及seq id no:123的vl序列。在某些方面,提供了与seq id no:253的s-hbs的以下残基中的一个或多个结合的抗体:c137、c138和/或d144。任选地,抗体可以进一步与p142、n146、t148、c149、i152和/或w156中的一个或多个结合。抗体可以包含如上定义的任何序列。
[0340]
在另一方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体竞争结合s-hbs。
[0341]
在一些实施例中,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv6.172与s-hbs(例如,seq id no:253的s-hbs)的结合活性。
[0342]
另外或可替代地,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv6.172与seq id no:254-262(例如,至少seq id no:257)的蛋白质中的一种或多种、任选地seq id no:254至262的蛋白质中的每一种的结合活性。
[0343]
参考抗体bv6.172具有seq id no:124的vh序列和seq id no:123的vl序列。它具有seq id no:126或269的全长重链和seq id no:125的全长轻链。seq id no:269包含由载体lt615368.1表达的igg1恒定区,如实例中所用。
[0344]
在一些实施例中,当在同一测定中评估时,本节中所述的抗体可以以比参考抗体bv6.172对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与
s-hbs(例如seq id no:253的s-hbs)结合。
[0345]
另外地或可替代地,当在同一测定中评估时,抗体可以以比参考抗体bv6.172对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254-262的蛋白质中的每一种结合。
[0346]
在一些实施例中,如本节中所述的抗体可以以比参考抗体bv6.172的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与s-hbs(例如,seq id no:253的s-hbs)结合,如通过elisa或流式细胞术测量的。可替代地或另外地,抗体可以以比参考抗体bv6.172的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与seq id no:254-262中的一个或多个或seq id no:254-262的蛋白质中的每一种、任选地至少seq id no:257的蛋白质结合,如通过elisa或通过流式细胞术测量的。
[0347]
在一些实施例中,如本节中所述的抗体可具有或保留针对hbv基因型d的体外中和活性,例如ic
50
值≤100pg/ml、任选地≤10pg/ml。
[0348]
在另一个实施例中,当使用同一测定(例如,如本文所述的体外中和测定)评估时,抗体可以具有用于中和hbv基因型a、b、c和/或d的ic
50
值,其比参考抗体bv6.172对相同基因型的ic
50
值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于参考抗体bv6.172对相同基因型的ic50值。
[0349]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv6.172对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内中和活性。
[0350]
任选地,抗体可以例如在感染hbv基因型a、b、c或d,任选地d的个体中体内抑制病毒血症。任选地,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv6.172对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内病毒血症抑制活性。
[0351]
h.
[0352]
在一个方面,本发明提供了包含vh结构域的抗体,该vh结构域包含选自以下各项的至少一个、至少两个或所有三个vh cdr序列:(a)包含seq id no:127的氨基酸序列的cdr-h1、(b)包含seq id no:128的氨基酸序列的cdr-h2、(c)包含seq id no:129的氨基酸序列的cdr-h3。在另一方面,抗体包含vh结构域,该vh结构域包含以下cdr:(a)包含seq id no:127的氨基酸序列的cdr-h1;(b)包含seq id no:128的氨基酸序列的cdr-h2;和(c)包含seq id no:129的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0353]
在一个方面,vh结构域可以进一步包含一个或多个重链框架序列,该序列选自以下各项:(a)seq id no:133的重链框架区1(hc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:134的重链框架区2(hc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:135的重链框架区3(hc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:136的
重链框架区4(hc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vh结构域包含如(a)至(d)中定义的每个重链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0354]
在另一方面,抗s-hbs抗体包含与seq id no:142的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变结构域(vh)序列。一方面,抗s-hbs抗体包含与seq id no:142的氨基酸序列具有至少95%序列同一性的重链可变结构域(vh)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vh序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:142中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:142中的vh序列,包括该序列的翻译后修饰。在一个具体方面,vh包含一、二或三个选自以下各项的cdr:(a)包含seq id no:127所示的氨基酸序列的cdr-h1,(b)包含seq id no:128所示的氨基酸序列的cdr-h2,以及(c)包含seq id no:129所示的氨基酸序列的cdr-h3。
[0355]
在另一方面,抗s-hbs抗体包含seq id no:142的vh的一个或多个重链cdr序列。在一个方面,抗s-hbs抗体包含seq id no:142的vh结构域的一个或多个(优选所有三个)重链cdr氨基酸序列和与seq id no:142的vh结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0356]
在另一方面,本发明提供了包含vl结构域的抗体,该vl结构域包含选自以下各项的至少一个、至少两个或所有三个vl cdr序列:(a)包含seq id no:130的氨基酸序列的cdr-l1、(b)包含seq id no:131的氨基酸序列的cdr-l2、(c)包含seq id no:132的氨基酸序列的cdr-l3。在另一方面,抗体包含vl结构域,该vh结构域包含以下cdr:(a)包含seq id no:130的氨基酸序列的cdr-l1;(b)包含seq id no:131的氨基酸序列的cdr-l2;和(c)包含seq id no:132的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0357]
在一个方面,抗s-hbs抗体vl结构域可以进一步包含一个或多个轻链框架序列,该序列选自以下各项:(a)seq id no:137的轻链框架区1(lc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:138的轻链框架区2(lc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:139的轻链框架区3(lc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:140的轻链框架区4(lc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vl结构域包含如(a)至(d)中定义的每个轻链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0358]
在另一方面,提供了抗s-hbs抗体,其中该抗体包含与seq id no:141的氨基酸序
列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变结构域(vl)序列。一方面,抗s-hbs抗体包含与seq id no:141的氨基酸序列具有至少95%序列同一性的轻链可变结构域(vl)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vl序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:141中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:141中的vl序列,包括该序列的翻译后修饰。在一个具体方面,vl包含一、二或三个选自以下各项的cdr:(a)包含seq id no:130的氨基酸序列的cdr-l1,(b)包含seq id no:131的氨基酸序列的cdr-l2和(c)包含seq id no:132的氨基酸序列的cdr-l3。
[0359]
在另一个实施例中,抗s-hbs抗体包含seq id no:141的vl的一个或多个cdr序列。在一个方面,抗s-hbs抗体包含seq id no:141的vl结构域的一个或多个(优选所有三个)轻链cdr氨基酸序列和与seq id no:141的vl结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0360]
在另一方面,提供一种抗s-hbs抗体,其中该抗体包含如在上文提供的任一方面中的vh序列以及如在上文提供的任一方面中的vl序列。
[0361]
例如,在一个示例性实施例中,抗体包含:包含seq id no:129的cdr-h3的vh结构域;和包含seq id no:132的cdr-l3的vl结构域。任选地,vh结构域进一步包含seq id no:128的cdr-h2。
[0362]
在另一示例性实施例中,抗体包含:
[0363]
i)包含以下cdr的vh结构域:(a)包含seq id no:127的氨基酸序列的cdr-h1;(b)包含seq id no:128的氨基酸序列的cdr-h2;和(c)包含seq id no:129的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代;和
[0364]
ii)vl结构域,该vl结构域包含以下cdr:(a)包含seq id no:130的氨基酸序列的cdr-l1;(b)包含seq id no:131的氨基酸序列的cdr-l2;和(c)包含seq id no:132的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0365]
在另一示例性实施例中,抗体包含:
[0366]
i)重链可变结构域(vh)序列,其与seq id no:142的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;以及
[0367]
ii)轻链可变结构域(vl)序列,其与seq id no:141的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。
[0368]
在另一个示例性实施例中,抗s-hbs抗体包含:(a)包含seq id no:127的氨基酸序列的cdr-h1;(b)包含seq id no:128的氨基酸序列的cdr-h2;(c)包含seq id no:129的氨基酸序列的cdr-h3;(d)包含seq id no:130的氨基酸序列的cdr-l1;(e)包含seq id no:131的氨基酸序列的cdr-l2;和(f)包含seq id no:132的氨基酸序列的cdr-l3,和vh结构域,其与seq id no:142的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、
97%、98%、99%或100%序列同一性;和vl结构域,其与seq id no:141的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。在一个方面,vh结构域与seq id no:142的氨基酸序列具有至少95%序列同一性。在一个方面,vl结构域与seq id no 141的氨基酸序列具有至少95%序列同一性。在一个实施例中,抗体与s-hbs特异性结合。在另一个实施例中,抗体与s-hbs结合,其解离常数(kd)与包含seq id no:142的vh序列和seq id no:141的vl序列的抗体的解离常数(kd)相比降低多达10倍或提高多达10倍。
[0369]
一方面,抗体分别包含seq id no:142和seq id no:141中的vh序列和vl序列,包括那些序列的翻译后修饰。
[0370]
在另一方面,抗体可以包含seq id no:143的全长轻链和/或seq id no:144或270的全长重链。
[0371]
在进一步方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体所结合的相同表位结合。例如,在某些方面中,提供了与抗s-hbs抗体所结合的相同表位结合的抗体,该抗体包含seq id no:142的vh序列以及seq id no:141的vl序列。在某些方面,提供了与seq id no:253的s-hbs的以下残基中的一个或多个结合的抗体:c137、c138和/或c139。任选地,抗体还与c124结合,任选地进一步与w156结合,并且任选地与n146、t148和/或i152中的一个或多个结合。抗体可以包含如上定义的任何序列。
[0372]
在另一方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体竞争结合s-hbs。
[0373]
在一些实施例中,当在同一测定(例如elisa或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv4.115与s-hbs(例如,seq id no:253的s-hbs)的结合活性。
[0374]
另外或可替代地,当在同一测定(例如elisa或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv4.115与seq id no:254-262(例如,至少seq id no:257)的蛋白质中的一种或多种、任选地seq id no:254至262的蛋白质中的每一种的结合活性。
[0375]
参考抗体bv4.115具有seq id no:142的vh序列和seq id no:141的vl序列。它具有seq id no:144或270的全长重链和seq id no:143的全长轻链。seq id no:270包含由载体lt615368.1表达的igg1恒定区,如实例中所用。
[0376]
在一些实施例中,当在同一测定中评估时,本节中所述的抗体可以以比参考抗体bv4.115对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与s-hbs(例如seq id no:253的s-hbs)结合。
[0377]
另外地或可替代地,当在同一测定中评估时,抗体可以以比参考抗体bv4.115对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254-262的蛋白质中的每一种结合。
[0378]
在一些实施例中,如本节中所述的抗体可以以比参考抗体bv4.115的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与s-hbs(例如,seq id no:253的s-hbs)结合,如通过elisa或流式细胞术测量的。可替代地或另外地,抗体可以以比参考抗体
bv4.115的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与seq id no:254-262中的一个或多个或seq id no:254-262的蛋白质中的每一种、任选地至少seq id no:257的蛋白质结合,如通过elisa或通过流式细胞术测量的。
[0379]
在一些实施例中,如本节中所述的抗体可以具有或保留针对hbv基因型a、b、c和/或d,任选地所有a、b、c和d的体外中和活性。例如,如本节中所述的抗体可以具有或保留针对hbv基因型d的体外中和活性,例如ic50值≤100pg/ml,任选地≤10pg/ml。
[0380]
在另一个实施例中,当使用同一测定(例如,如本文所述的体外中和测定)评估时,抗体可以具有用于中和hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的ic50值,其比参考抗体bv4.115对相同基因型的ic50值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于参考抗体bv4.115对相同基因型的ic50值。
[0381]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv4.115对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内中和活性。
[0382]
任选地,抗体可以例如在感染hbv基因型a、b、c或d,任选地d的个体中体内抑制病毒血症。任选地,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv4.115对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内病毒血症抑制活性。
[0383]
i.
[0384]
在一个方面,本发明提供了包含vh结构域的抗体,该vh结构域包含选自以下各项的至少一个、至少两个或所有三个vh cdr序列:(a)包含seq id no:145的氨基酸序列的cdr-h1、(b)包含seq id no:146的氨基酸序列的cdr-h2、(c)包含seq id no:147的氨基酸序列的cdr-h3。在另一方面,抗体包含vh结构域,该vh结构域包含以下cdr:(a)包含seq id no:145的氨基酸序列的cdr-h1;(b)包含seq id no:146的氨基酸序列的cdr-h2;和(c)包含seq id no:147的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0385]
在一个方面,vh结构域可以进一步包含一个或多个重链框架序列,该序列选自以下各项:(a)seq id no:151的重链框架区1(hc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:152的重链框架区2(hc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:153的重链框架区3(hc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:154的重链框架区4(hc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vh结构域包含如(a)至(d)中定义的每个重链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0386]
在另一方面,抗s-hbs抗体包含与seq id no:160的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变结构域(vh)序列。一方面,抗s-hbs抗体包含与seq id no:160的氨基酸序列具有至少95%序列同
一性的重链可变结构域(vh)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vh序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:160中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:160中的vh序列,包括该序列的翻译后修饰。在一个具体方面,vh包含一、二或三个选自以下各项的cdr:(a)包含seq id no:145所示的氨基酸序列的cdr-h1,(b)包含seq id no:146所示的氨基酸序列的cdr-h2,以及(c)包含seq id no:147所示的氨基酸序列的cdr-h3。
[0387]
在另一方面,抗s-hbs抗体包含seq id no:160的vh的一个或多个重链cdr序列。在一个方面,抗s-hbs抗体包含seq id no:160的vh结构域的一个或多个(优选所有三个)重链cdr氨基酸序列和与seq id no:160的vh结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0388]
在另一方面,本发明提供了包含vl结构域的抗体,该vl结构域包含选自以下各项的至少一个、至少两个或所有三个vl cdr序列:(a)包含seq id no:148的氨基酸序列的cdr-l1、(b)包含seq id no:149的氨基酸序列的cdr-l2、(c)包含seq id no:150的氨基酸序列的cdr-l3。在另一方面,抗体包含vl结构域,该vh结构域包含以下cdr:(a)包含seq id no:148的氨基酸序列的cdr-l1;(b)包含seq id no:149的氨基酸序列的cdr-l2;和(c)包含seq id no:150的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0389]
在一个方面,抗s-hbs抗体vl结构域可以进一步包含一个或多个轻链框架序列,该序列选自以下各项:(a)seq id no:155的轻链框架区1(lc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:156的轻链框架区2(lc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:157的轻链框架区3(lc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:158的轻链框架区4(lc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vl结构域包含如(a)至(d)中定义的每个轻链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0390]
在另一方面,提供了抗s-hbs抗体,其中该抗体包含与seq id no:159的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变结构域(vl)序列。一方面,抗s-hbs抗体包含与seq id no:159的氨基酸序列具有至少95%序列同一性的轻链可变结构域(vl)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vl序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:159中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含
seq id no:159中的vl序列,包括该序列的翻译后修饰。在一个具体方面,vl包含一、二或三个选自以下各项的cdr:(a)包含seq id no:148的氨基酸序列的cdr-l1,(b)包含seq id no:149的氨基酸序列的cdr-l2和(c)包含seq id no:150的氨基酸序列的cdr-l3。
[0391]
在另一个实施例中,抗s-hbs抗体包含seq id no:159的vl的一个或多个cdr序列。在一个方面,抗s-hbs抗体包含seq id no:159的vl结构域的一个或多个(优选所有三个)轻链cdr氨基酸序列和与seq id no:159的vl结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0392]
在另一方面,提供一种抗s-hbs抗体,其中该抗体包含如在上文提供的任一方面中的vh序列以及如在上文提供的任一方面中的vl序列。
[0393]
例如,在一个示例性实施例中,抗体包含:包含seq id no:147的cdr-h3的vh结构域;和包含seq id no:150的cdr-l3的vl结构域。任选地,vh结构域进一步包含seq id no:146的cdr-h2。
[0394]
在另一示例性实施例中,抗体包含:
[0395]
i)包含以下cdr的vh结构域:(a)包含seq id no:145的氨基酸序列的cdr-h1;(b)包含seq id no:146的氨基酸序列的cdr-h2;和(c)包含seq id no:147的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代;和
[0396]
ii)vl结构域,该vl结构域包含以下cdr:(a)包含seq id no:148的氨基酸序列的cdr-l1;(b)包含seq id no:149的氨基酸序列的cdr-l2;和(c)包含seq id no:150的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0397]
在另一示例性实施例中,抗体包含:
[0398]
i)重链可变结构域(vh)序列,其与seq id no:160的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;以及
[0399]
ii)轻链可变结构域(vl)序列,其与seq id no:159的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。
[0400]
在另一个示例性实施例中,抗s-hbs抗体包含:(a)包含seq id no:145的氨基酸序列的cdr-h1;(b)包含seq id no:146的氨基酸序列的cdr-h2;(c)包含seq id no:147的氨基酸序列的cdr-h3;(d)包含seq id no:148的氨基酸序列的cdr-l1;(e)包含seq id no:149的氨基酸序列的cdr-l2;和(f)包含seq id no:150的氨基酸序列的cdr-l3,和vh结构域,其与seq id no:160的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;和vl结构域,其与seq id no:159的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。在一个方面,vh结构域与seq id no:160的氨基酸序列具有至少95%序列同一性。在一个方面,vl结构域与seq id no 159的氨基酸序列具有至少95%序列同一性。在一个实施例中,抗体与s-hbs特异性结合。在另一个实施例中,抗体与s-hbs结合,其解离常数(kd)与包含seq id no:160的vh序列和seq id no:159的vl序列的抗体的解离常数(kd)相比降低多达10倍或提高多达10倍。
[0401]
一方面,抗体分别包含seq id no:160和seq id no:159中的vh序列和vl序列,包括那些序列的翻译后修饰。
[0402]
在另一方面,抗体可以包含seq id no:161的全长轻链和/或seq id no:162或271的全长重链。
[0403]
在进一步方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体所结合的相同表位结合。例如,在某些方面中,提供了与抗s-hbs抗体所结合的相同表位结合的抗体,该抗体包含seq id no:160的vh序列以及seq id no:159的vl序列。在某些方面,提供了与seq id no:253的s-hbs的以下残基中的一个或多个结合的抗体:c121、k141、d144和/或g145。任选地,抗体可以进一步与c139、c147、c149、i152和/或w156中的一个或多个结合。抗体可以包含如上定义的任何序列。
[0404]
在另一方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体竞争结合s-hbs。
[0405]
在一些实施例中,当在同一测定(例如elisa或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.229与s-hbs(例如,seq id no:253的s-hbs)的结合活性。
[0406]
另外或可替代地,当在同一测定(例如elisa或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.229与seq id no:254-262(例如,至少seq id no:257)的蛋白质中的一种或多种、任选地seq id no:254至262的蛋白质中的每一种的结合活性。
[0407]
参考抗体bc1.229具有seq id no:160的vh序列和seq id no:159的vl序列。它具有seq id no:162或271的全长重链和seq id no:161的全长轻链。seq id no:271包含由载体lt615368.1表达的igg1恒定区,如实例中所用。
[0408]
在一些实施例中,当在同一测定中评估时,本节中所述的抗体可以以比参考抗体bc1.229对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与s-hbs(例如seq id no:253的s-hbs)结合。
[0409]
另外地或可替代地,当在同一测定中评估时,抗体可以以比参考抗体bc1.229对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254-262的蛋白质中的每一种结合。
[0410]
在一些实施例中,如本节中所述的抗体可以以比参考抗体bc1.229的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与s-hbs(例如,seq id no:253的s-hbs)结合,如通过elisa或流式细胞术测量的。可替代地或另外地,抗体可以以比参考抗体bc1.229的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与seq id no:254-262中的一个或多个或seq id no:254-262的蛋白质中的每一种、任选地至少seq id no:257的蛋白质结合,如通过elisa或通过流式细胞术测量的。
[0411]
在一些实施例中,如本节中所述的抗体可以具有或保留针对hbv基因型a、b、c和/或d,任选地所有a、b、c和d的体外中和活性。例如,如本节中所述的抗体可以具有或保留针对hbv基因型d的体外中和活性,例如ic50值≤1ng/ml,任选地≤100pg/ml。
[0412]
在另一个实施例中,当使用同一测定(例如,如本文所述的体外中和测定)评估时,
抗体可以具有用于中和hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的ic
50
值,其比参考抗体bc1.229对相同基因型的ic
50
值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于参考抗体bc1.229对相同基因型的ic50值。
[0413]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.229对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内中和活性。
[0414]
任选地,抗体可以例如在感染hbv基因型a、b、c或d,任选地d的个体中体内抑制病毒血症。任选地,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.229对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内病毒血症抑制活性。
[0415]
j.
[0416]
在一个方面,本发明提供了包含vh结构域的抗体,该vh结构域包含选自以下各项的至少一个、至少两个或所有三个vh cdr序列:(a)包含seq id no:163的氨基酸序列的cdr-h1、(b)包含seq id no:164的氨基酸序列的cdr-h2、(c)包含seq id no:165的氨基酸序列的cdr-h3。在另一方面,抗体包含vh结构域,该vh结构域包含以下cdr:(a)包含seq id no:163的氨基酸序列的cdr-h1;(b)包含seq id no:164的氨基酸序列的cdr-h2;和(c)包含seq id no:165的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0417]
在一个方面,vh结构域可以进一步包含一个或多个重链框架序列,该序列选自以下各项:(a)seq id no:169的重链框架区1(hc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:170的重链框架区2(hc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:171的重链框架区3(hc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:172的重链框架区4(hc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vh结构域包含如(a)至(d)中定义的每个重链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0418]
在另一方面,抗s-hbs抗体包含与seq id no:178的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变结构域(vh)序列。一方面,抗s-hbs抗体包含与seq id no:178的氨基酸序列具有至少95%序列同一性的重链可变结构域(vh)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vh序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:178中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:178中的vh序列,包括该序列的翻译后修饰。在一个具体方面,vh包含一、二或三个选自以下各项的cdr:(a)包含seq id no:163所示的氨基酸序列的cdr-h1,(b)包含seq id no:164所示
的氨基酸序列的cdr-h2,以及(c)包含seq id no:165所示的氨基酸序列的cdr-h3。
[0419]
在另一方面,抗s-hbs抗体包含seq id no:178的vh的一个或多个重链cdr序列。在一个方面,抗s-hbs抗体包含seq id no:178的vh结构域的一个或多个(优选所有三个)重链cdr氨基酸序列和与seq id no:178的vh结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0420]
在另一方面,本发明提供了包含vl结构域的抗体,该vl结构域包含选自以下各项的至少一个、至少两个或所有三个vl cdr序列:(a)包含seq id no:166的氨基酸序列的cdr-l1、(b)包含seq id no:167的氨基酸序列的cdr-l2、(c)包含seq id no:168的氨基酸序列的cdr-l3。在另一方面,抗体包含vl结构域,该vh结构域包含以下cdr:(a)包含seq id no:166的氨基酸序列的cdr-l1;(b)包含seq id no:167的氨基酸序列的cdr-l2;和(c)包含seq id no:168的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0421]
在一个方面,抗s-hbs抗体vl结构域可以进一步包含一个或多个轻链框架序列,该序列选自以下各项:(a)seq id no:173的轻链框架区1(lc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:174的轻链框架区2(lc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:175的轻链框架区3(lc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:176的轻链框架区4(lc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vl结构域包含如(a)至(d)中定义的每个轻链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0422]
在另一方面,提供了抗s-hbs抗体,其中该抗体包含与seq id no:177的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变结构域(vl)序列。一方面,抗s-hbs抗体包含与seq id no:177的氨基酸序列具有至少95%序列同一性的轻链可变结构域(vl)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vl序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:177中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:177中的vl序列,包括该序列的翻译后修饰。在一个具体方面,vl包含一、二或三个选自以下各项的cdr:(a)包含seq id no:166的氨基酸序列的cdr-l1,(b)包含seq id no:167的氨基酸序列的cdr-l2和(c)包含seq id no:168的氨基酸序列的cdr-l3。
[0423]
在另一个实施例中,抗s-hbs抗体包含seq id no:177的vl的一个或多个cdr序列。在一个方面,抗s-hbs抗体包含seq id no:177的vl结构域的一个或多个(优选所有三个)轻链cdr氨基酸序列和与seq id no:177的vl结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的
id no:253的s-hbs的以下残基结合的抗体:c121、c138、c139、c147和/或c149。任选地,抗体可以另外与l109、r122、t123、c124、m133、y134、s136、k141和/或i152中的一个或多个结合。抗体可以包含如上定义的任何序列。
[0436]
在另一方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体竞争结合s-hbs。
[0437]
在一些实施例中,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc8.159与s-hbs(例如,seq id no:253的s-hbs)的结合活性。
[0438]
另外或可替代地,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc8.159与seq id no:254-262(例如,至少seq id no:257)的蛋白质中的一种或多种、任选地seq id no:254至262的蛋白质中的每一种的结合活性。
[0439]
参考抗体bc8.159具有seq id no:178的vh序列和seq id no:177的vl序列。它具有seq id no:180或272的全长重链和seq id no:179的全长轻链。seq id no:272包含由载体lt615368.1表达的igg1恒定区,如实例中所用。
[0440]
在一些实施例中,当在同一测定中评估时,本节中所述的抗体可以以比参考抗体bc8.159对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与s-hbs(例如seq id no:253的s-hbs)结合。
[0441]
另外地或可替代地,当在同一测定中评估时,抗体可以以比参考抗体bc8.159对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254-262的蛋白质中的每一种结合。
[0442]
在一些实施例中,如本节中所述的抗体可以以比参考抗体bc8.159的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与s-hbs(例如,seq id no:253的s-hbs)结合,如通过elisa或流式细胞术测量的。可替代地或另外地,抗体可以以比参考抗体bc8.159的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与seq id no:254-262中的一个或多个或seq id no:254-262的蛋白质中的每一种、任选地至少seq id no:257的蛋白质结合,如通过elisa或通过流式细胞术测量的。
[0443]
在一些实施例中,如本节中所述的抗体可以具有或保留针对hbv基因型a、b、c和/或d,任选地所有a、b、c和d的体外中和活性。例如,如本节中所述的抗体可以具有或保留针对hbv基因型d的体外中和活性,例如ic50值≤1ng/ml,任选地≤100pg/ml。
[0444]
在另一个实施例中,当使用同一测定(例如,如本文所述的体外中和测定)评估时,抗体可以具有用于中和hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的ic50值,其比参考抗体bc8.159对相同基因型的ic50值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于参考抗体bc1.187对相同基因型的ic50值。
[0445]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc8.159对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内中和活性。
[0446]
任选地,抗体可以例如在感染hbv基因型a、b、c或d,任选地d的个体中体内抑制病
毒血症。任选地,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc8.159对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内病毒血症抑制活性。
[0447]
k.
[0448]
在一个方面,本发明提供了包含vh结构域的抗体,该vh结构域包含选自以下各项的至少一个、至少两个或所有三个vh cdr序列:(a)包含seq id no:181的氨基酸序列的cdr-h1、(b)包含seq id no:182的氨基酸序列的cdr-h2、(c)包含seq id no:183的氨基酸序列的cdr-h3。在另一方面,抗体包含vh结构域,该vh结构域包含以下cdr:(a)包含seq id no:181的氨基酸序列的cdr-h1;(b)包含seq id no:182的氨基酸序列的cdr-h2;和(c)包含seq id no:183的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0449]
在一个方面,vh结构域可以进一步包含一个或多个重链框架序列,该序列选自以下各项:(a)seq id no:187的重链框架区1(hc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:188的重链框架区2(hc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:189的重链框架区3(hc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:190的重链框架区4(hc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vh结构域包含如(a)至(d)中定义的每个重链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0450]
在另一方面,抗s-hbs抗体包含与seq id no:196的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变结构域(vh)序列。一方面,抗s-hbs抗体包含与seq id no:196的氨基酸序列具有至少95%序列同一性的重链可变结构域(vh)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vh序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:196中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:196中的vh序列,包括该序列的翻译后修饰。在一个具体方面,vh包含一、二或三个选自以下各项的cdr:(a)包含seq id no:181所示的氨基酸序列的cdr-h1,(b)包含seq id no:182所示的氨基酸序列的cdr-h2,以及(c)包含seq id no:183所示的氨基酸序列的cdr-h3。
[0451]
在另一方面,抗s-hbs抗体包含seq id no:196的vh的一个或多个重链cdr序列。在一个方面,抗s-hbs抗体包含seq id no:196的vh结构域的一个或多个(优选所有三个)重链cdr氨基酸序列和与seq id no:196的vh结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0452]
在另一方面,本发明提供了包含vl结构域的抗体,该vl结构域包含选自以下各项
的至少一个、至少两个或所有三个vl cdr序列:(a)包含seq id no:184的氨基酸序列的cdr-l1、(b)包含seq id no:185的氨基酸序列的cdr-l2、(c)包含seq id no:186的氨基酸序列的cdr-l3。在另一方面,抗体包含vl结构域,该vh结构域包含以下cdr:(a)包含seq id no:184的氨基酸序列的cdr-l1;(b)包含seq id no:185的氨基酸序列的cdr-l2;和(c)包含seq id no:186的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0453]
在一个方面,抗s-hbs抗体vl结构域可以进一步包含一个或多个轻链框架序列,该序列选自以下各项:(a)seq id no:191的轻链框架区1(lc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:192的轻链框架区2(lc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:193的轻链框架区3(lc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:194的轻链框架区4(lc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vl结构域包含如(a)至(d)中定义的每个轻链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0454]
在另一方面,提供了抗s-hbs抗体,其中该抗体包含与seq id no:195的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变结构域(vl)序列。一方面,抗s-hbs抗体包含与seq id no:195的氨基酸序列具有至少95%序列同一性的轻链可变结构域(vl)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vl序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:195中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:195中的vl序列,包括该序列的翻译后修饰。在一个具体方面,vl包含一、二或三个选自以下各项的cdr:(a)包含seq id no:184的氨基酸序列的cdr-l1,(b)包含seq id no:185的氨基酸序列的cdr-l2和(c)包含seq id no:186的氨基酸序列的cdr-l3。
[0455]
在另一个实施例中,抗s-hbs抗体包含seq id no:195的vl的一个或多个cdr序列。在一个方面,抗s-hbs抗体包含seq id no:195的vl结构域的一个或多个(优选所有三个)轻链cdr氨基酸序列和与seq id no:195的vl结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0456]
在另一方面,提供一种抗s-hbs抗体,其中该抗体包含如在上文提供的任一方面中的vh序列以及如在上文提供的任一方面中的vl序列。
[0457]
例如,在一个示例性实施例中,抗体包含:包含seq id no:183的cdr-h3的vh结构域;和包含seq id no:186的cdr-l3的vl结构域。任选地,vh结构域进一步包含seq id no:182的cdr-h2。
[0458]
在另一示例性实施例中,抗体包含:
[0459]
i)包含以下cdr的vh结构域:(a)包含seq id no:181的氨基酸序列的cdr-h1;(b)包含seq id no:182的氨基酸序列的cdr-h2;和(c)包含seq id no:183的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代;和
[0460]
ii)vl结构域,该vl结构域包含以下cdr:(a)包含seq id no:184的氨基酸序列的cdr-l1;(b)包含seq id no:185的氨基酸序列的cdr-l2;和(c)包含seq id no:186的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0461]
在另一示例性实施例中,抗体包含:
[0462]
i)重链可变结构域(vh)序列,其与seq id no:196的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;以及
[0463]
ii)轻链可变结构域(vl)序列,其与seq id no:195的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。
[0464]
在另一个示例性实施例中,抗s-hbs抗体包含:(a)包含seq id no:181的氨基酸序列的cdr-h1;(b)包含seq id no:182的氨基酸序列的cdr-h2;(c)包含seq id no:183的氨基酸序列的cdr-h3;(d)包含seq id no:184的氨基酸序列的cdr-l1;(e)包含seq id no:185的氨基酸序列的cdr-l2;和(f)包含seq id no:186的氨基酸序列的cdr-l3,和vh结构域,其与seq id no:196的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;和vl结构域,其与seq id no:195的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。在一个方面,vh结构域与seq id no:196的氨基酸序列具有至少95%序列同一性。在一个方面,vl结构域与seq id no 195的氨基酸序列具有至少95%序列同一性。在一个实施例中,抗体与s-hbs特异性结合。在另一个实施例中,抗体与s-hbs结合,其解离常数(kd)与包含seq id no:196的vh序列和seq id no:195的vl序列的抗体的解离常数(kd)相比降低多达10倍或提高多达10倍。
[0465]
一方面,抗体分别包含seq id no:196和seq id no:195中的vh序列和vl序列,包括那些序列的翻译后修饰。
[0466]
在另一方面,抗体可以包含seq id no:197的全长轻链和/或seq id no:198或273的全长重链。
[0467]
在进一步方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体所结合的相同表位结合。例如,在某些方面中,提供了与抗s-hbs抗体所结合的相同表位结合的抗体,该抗体包含seq id no:196的vh序列以及seq id no:195的vl序列。在某些方面,提供了与seq id no:253的s-hbs的以下残基结合的抗体:c121、c124、c137、c138、c139、c147和/或c149,也任选地i152。任选地,抗体进一步与v106、p108、w156和/或f161中的一个或多个结合。抗体可以包含如上定义的任何序列。
[0468]
在另一方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体竞争结合s-hbs。
[0469]
在一些实施例中,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或
100%的参考抗体bc1.128与s-hbs(例如,seq id no:253的s-hbs)的结合活性。
[0470]
另外地或可替代地,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.128与seq id no:254-262的蛋白质中的一种或多种(例如,至少seq id no:257)、任选地seq id no:254至262的蛋白质中的每一种的结合活性。
[0471]
参考抗体bc1.128具有seq id no:196的vh序列和seq id no:195的vl序列。它具有seq id no:198或273的全长重链和seq id no:197的全长轻链。seq id no:273包含由载体lt615368.1表达的igg1恒定区,如实例中所用。
[0472]
在一些实施例中,当在同一测定中评估时,本节中所述的抗体可以以比参考抗体bc1.128对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与s-hbs(例如seq id no:253的s-hbs)结合。
[0473]
另外地或可替代地,当在同一测定中评估时,抗体可以以比参考抗体bc1.128对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254-262的蛋白质中的每一种结合。
[0474]
在一些实施例中,如本节中所述的抗体可以以比参考抗体bc1.128的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与s-hbs(例如,seq id no:253的s-hbs)结合,如通过elisa或流式细胞术测量的。可替代地或另外地,抗体可以以比参考抗体bc1.128的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与seq id no:254-262中的一个或多个或seq id no:254-262的蛋白质中的每一种、任选地至少seq id no:257的蛋白质结合,如通过elisa或通过流式细胞术测量的。
[0475]
在一些实施例中,如本节中所述的抗体可以具有或保留针对hbv基因型a、b、c和/或d,任选地所有a、b、c和d的体外中和活性。例如,如本节中所述的抗体可以具有或保留针对hbv基因型d的体外中和活性,例如ic50值≤10ng/ml,任选地≤1ng/ml。
[0476]
在另一个实施例中,当使用同一测定(例如,如本文所述的体外中和测定)评估时,抗体可以具有用于中和hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的ic
50
值,其比参考抗体bc1.128对相同基因型的ic
50
值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于参考抗体bc1.128对相同基因型的ic50值。
[0477]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.128对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内中和活性。
[0478]
任选地,抗体可以例如在感染hbv基因型a、b、c或d,任选地d的个体中体内抑制病毒血症。任选地,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.128对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内病毒血症抑制活性。
[0479]
l.
[0480]
在一个方面,本发明提供了包含vh结构域的抗体,该vh结构域包含选自以下各项的至少一个、至少两个或所有三个vh cdr序列:(a)包含seq id no:199的氨基酸序列的cdr-h1、(b)包含seq id no:200的氨基酸序列的cdr-h2、(c)包含seq id no:201的氨基酸
序列的cdr-h3。在另一方面,抗体包含vh结构域,该vh结构域包含以下cdr:(a)包含seq id no:199的氨基酸序列的cdr-h1;(b)包含seq id no:200的氨基酸序列的cdr-h2;和(c)包含seq id no:201的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0481]
在一个方面,vh结构域可以进一步包含一个或多个重链框架序列,该序列选自以下各项:(a)seq id no:205的重链框架区1(hc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:206的重链框架区2(hc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:207的重链框架区3(hc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:208的重链框架区4(hc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vh结构域包含如(a)至(d)中定义的每个重链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0482]
在另一方面,抗s-hbs抗体包含与seq id no:214的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变结构域(vh)序列。一方面,抗s-hbs抗体包含与seq id no:214的氨基酸序列具有至少95%序列同一性的重链可变结构域(vh)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vh序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:214中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:214中的vh序列,包括该序列的翻译后修饰。在一个具体方面,vh包含一、二或三个选自以下各项的cdr:(a)包含seq id no:199所示的氨基酸序列的cdr-h1,(b)包含seq id no:200所示的氨基酸序列的cdr-h2,以及(c)包含seq id no:201所示的氨基酸序列的cdr-h3。
[0483]
在另一方面,抗s-hbs抗体包含seq id no:214的vh的一个或多个重链cdr序列。在一个方面,抗s-hbs抗体包含seq id no:214的vh结构域的一个或多个(优选所有三个)重链cdr氨基酸序列和与seq id no:214的vh结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0484]
在另一方面,本发明提供了包含vl结构域的抗体,该vl结构域包含选自以下各项的至少一个、至少两个或所有三个vl cdr序列:(a)包含seq id no:202的氨基酸序列的cdr-l1、(b)包含seq id no:203的氨基酸序列的cdr-l2、(c)包含seq id no:204的氨基酸序列的cdr-l3。在另一方面,抗体包含vl结构域,该vh结构域包含以下cdr:(a)包含seq id no:202的氨基酸序列的cdr-l1;(b)包含seq id no:203的氨基酸序列的cdr-l2;和(c)包含seq id no:204的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0485]
在一个方面,抗s-hbs抗体vl结构域可以进一步包含一个或多个轻链框架序列,该
序列选自以下各项:(a)seq id no:209的轻链框架区1(lc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:210的轻链框架区2(lc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:211的轻链框架区3(lc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:212的轻链框架区4(lc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vl结构域包含如(a)至(d)中定义的每个轻链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0486]
在另一方面,提供了抗s-hbs抗体,其中该抗体包含与seq id no:213的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变结构域(vl)序列。一方面,抗s-hbs抗体包含与seq id no:213的氨基酸序列具有至少95%序列同一性的轻链可变结构域(vl)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vl序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:213中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:213中的vl序列,包括该序列的翻译后修饰。在一个具体方面,vl包含一、二或三个选自以下各项的cdr:(a)包含seq id no:202的氨基酸序列的cdr-l1,(b)包含seq id no:203的氨基酸序列的cdr-l2和(c)包含seq id no:204的氨基酸序列的cdr-l3。
[0487]
在另一个实施例中,抗s-hbs抗体包含seq id no:213的vl的一个或多个cdr序列。在一个方面,抗s-hbs抗体包含seq id no:213的vl结构域的一个或多个(优选所有三个)轻链cdr氨基酸序列和与seq id no:213的vl结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0488]
在另一方面,提供一种抗s-hbs抗体,其中该抗体包含如在上文提供的任一方面中的vh序列以及如在上文提供的任一方面中的vl序列。
[0489]
例如,在一个示例性实施例中,抗体包含:包含seq id no:201的cdr-h3的vh结构域;和包含seq id no:204的cdr-l3的vl结构域。任选地,vh结构域进一步包含seq id no:200的cdr-h2。
[0490]
在另一示例性实施例中,抗体包含:
[0491]
i)包含以下cdr的vh结构域:(a)包含seq id no:199的氨基酸序列的cdr-h1;(b)包含seq id no:200的氨基酸序列的cdr-h2;和(c)包含seq id no:201的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代;和
[0492]
ii)vl结构域,该vl结构域包含以下cdr:(a)包含seq id no:202的氨基酸序列的cdr-l1;(b)包含seq id no:203的氨基酸序列的cdr-l2;和(c)包含seq id no:204的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个
或三个氨基酸被另一种氨基酸取代。
[0493]
在另一示例性实施例中,抗体包含:
[0494]
i)重链可变结构域(vh)序列,其与seq id no:214的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;以及
[0495]
ii)轻链可变结构域(vl)序列,其与seq id no:213的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。
[0496]
在另一个示例性实施例中,抗s-hbs抗体包含:(a)包含seq id no:199的氨基酸序列的cdr-h1;(b)包含seq id no:200的氨基酸序列的cdr-h2;(c)包含seq id no:201的氨基酸序列的cdr-h3;(d)包含seq id no:202的氨基酸序列的cdr-l1;(e)包含seq id no:203的氨基酸序列的cdr-l2;和(f)包含seq id no:204的氨基酸序列的cdr-l3,和vh结构域,其与seq id no:214的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;和vl结构域,其与seq id no:213的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。在一个方面,vh结构域与seq id no:214的氨基酸序列具有至少95%序列同一性。在一个方面,vl结构域与seq id no:213的氨基酸序列具有至少95%序列同一性。在一个实施例中,抗体与s-hbs特异性结合。在另一个实施例中,抗体与s-hbs结合,其解离常数(kd)与包含seq id no:214的vh序列和seq id no:213的vl序列的抗体的解离常数(kd)相比降低多达10倍或提高多达10倍。
[0497]
一方面,抗体分别包含seq id no:214和seq id no:213中的vh序列和vl序列,包括那些序列的翻译后修饰。
[0498]
在另一方面,抗体可以包含seq id no:215的全长轻链和/或seq id no:216或274的全长重链。
[0499]
在进一步方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体所结合的相同表位结合。例如,在某些方面中,提供了与抗s-hbs抗体所结合的相同表位结合的抗体,该抗体包含seq id no:214的vh序列以及seq id no:213的vl序列。在某些方面,提供了与seq id no:253的s-hbs的残基f179结合的抗体。抗体可以包含如上定义的任何序列。
[0500]
在另一方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体竞争结合s-hbs。
[0501]
在一些实施例中,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc4.204与s-hbs(例如,seq id no:253的s-hbs)的结合活性。另外地或可替代地,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc4.204与具有seq id no:254、255、256、257、258、260和/或262、任选地至少seq id no:257的序列的蛋白质的结合活性。
[0502]
参考抗体bc4.204具有seq id no:214的vh序列和seq id no:213的vl序列。它具有seq id no:216或274的全长重链和seq id no:215的全长轻链。seq id no:274包含由载体lt615368.1表达的igg1恒定区,如实例中所用。
[0503]
在一些实施例中,当在同一测定中评估时,本节中所述的抗体可以以比参考抗体
bc4.204对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与s-hbs(例如seq id no:253的s-hbs)结合。另外地或可替代地,当在同一测定中评估时,抗体可以以比参考抗体bc4.204对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与seq id no:254、255、256、257、258、260和/或262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254-262的蛋白质中的每一种结合。
[0504]
在一些实施例中,如本节中所述的抗体可以以比参考抗体bc4.204的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与s-hbs(例如,seq id no:253的s-hbs)结合,如通过elisa或流式细胞术测量的。可替代地或另外地,抗体可以以比参考抗体bc4.204的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与具有seq id no:254、255、256、257、258、260和/或262序列的蛋白质中的一种或多种或其中的每一种、任选地至少seq id no:257的蛋白质结合,如通过elisa或通过流式细胞术测量的。
[0505]
在一些实施例中,如本节中所述的抗体可以具有或保留针对hbv基因型a、b、c和/或d,任选地所有a、b、c和d的体外中和活性。例如,如本节中所述的抗体可以具有或保留针对hbv基因型d的体外中和活性,例如ic50值≤10ng/ml,任选地≤1ng/ml。
[0506]
在另一个实施例中,当使用同一测定(例如,如本文所述的体外中和测定)评估时,抗体可以具有用于中和hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的ic50值,其比参考抗体bc4.204对相同基因型的ic50值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于参考抗体bc1.187对相同基因型的ic50值。
[0507]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc4.204对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内中和活性。
[0508]
任选地,抗体可以例如在感染hbv基因型a、b、c或d,任选地d的个体中体内抑制病毒血症。任选地,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc4.204对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内病毒血症抑制活性。
[0509]
m.
[0510]
在一个方面,本发明提供了包含vh结构域的抗体,该vh结构域包含选自以下各项的至少一个、至少两个或所有三个vh cdr序列:(a)包含seq id no:217的氨基酸序列的cdr-h1、(b)包含seq id no:218的氨基酸序列的cdr-h2、(c)包含seq id no:219的氨基酸序列的cdr-h3。在另一方面,抗体包含vh结构域,该vh结构域包含以下cdr:(a)包含seq id no:217的氨基酸序列的cdr-h1;(b)包含seq id no:218的氨基酸序列的cdr-h2;和(c)包含seq id no:219的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0511]
在一个方面,vh结构域可以进一步包含一个或多个重链框架序列,该序列选自以下各项:(a)seq id no:223的重链框架区1(hc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:224的重链框架区2(hc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:225的重链框架区3(hc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、
92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:226的重链框架区4(hc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vh结构域包含如(a)至(d)中定义的每个重链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0512]
在另一方面,抗s-hbs抗体包含与seq id no:232的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变结构域(vh)序列。一方面,抗s-hbs抗体包含与seq id no:232的氨基酸序列具有至少95%序列同一性的重链可变结构域(vh)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vh序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:232中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:232中的vh序列,包括该序列的翻译后修饰。在一个具体方面,vh包含一、二或三个选自以下各项的cdr:(a)包含seq id no:217所示的氨基酸序列的cdr-h1,(b)包含seq id no:218所示的氨基酸序列的cdr-h2,以及(c)包含seq id no:219所示的氨基酸序列的cdr-h3。
[0513]
在另一方面,抗s-hbs抗体包含seq id no:232的vh的一个或多个重链cdr序列。在一个方面,抗s-hbs抗体包含seq id no:232的vh结构域的一个或多个(优选所有三个)重链cdr氨基酸序列和与seq id no:232的vh结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0514]
在另一方面,本发明提供了包含vl结构域的抗体,该vl结构域包含选自以下各项的至少一个、至少两个或所有三个vl cdr序列:(a)包含seq id no:220的氨基酸序列的cdr-l1、(b)包含seq id no:221的氨基酸序列的cdr-l2、(c)包含seq id no:222的氨基酸序列的cdr-l3。在另一方面,抗体包含vl结构域,该vh结构域包含以下cdr:(a)包含seq id no:220的氨基酸序列的cdr-l1;(b)包含seq id no:221的氨基酸序列的cdr-l2;和(c)包含seq id no:222的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0515]
在一个方面,抗s-hbs抗体vl结构域可以进一步包含一个或多个轻链框架序列,该序列选自以下各项:(a)seq id no:227的轻链框架区1(lc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:228的轻链框架区2(lc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:229的轻链框架区3(lc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:230的轻链框架区4(lc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vl结构域包含如(a)至(d)中定义的每个轻链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0516]
在另一方面,提供了抗s-hbs抗体,其中该抗体包含与seq id no:231的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变结构域(vl)序列。一方面,抗s-hbs抗体包含与seq id no:231的氨基酸序列具有至少95%序列同一性的轻链可变结构域(vl)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vl序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:231中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:231中的vl序列,包括该序列的翻译后修饰。在一个具体方面,vl包含一、二或三个选自以下各项的cdr:(a)包含seq id no:220的氨基酸序列的cdr-l1,(b)包含seq id no:221的氨基酸序列的cdr-l2和(c)包含seq id no:222的氨基酸序列的cdr-l3。
[0517]
在另一个实施例中,抗s-hbs抗体包含seq id no:231的vl的一个或多个cdr序列。在一个方面,抗s-hbs抗体包含seq id no:231的vl结构域的一个或多个(优选所有三个)轻链cdr氨基酸序列和与seq id no:231的vl结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0518]
在另一方面,提供一种抗s-hbs抗体,其中该抗体包含如在上文提供的任一方面中的vh序列以及如在上文提供的任一方面中的vl序列。
[0519]
例如,在一个示例性实施例中,抗体包含:包含seq id no:219的cdr-h3的vh结构域;和包含seq id no:222的cdr-l3的vl结构域。任选地,vh结构域进一步包含seq id no:218的cdr-h2。
[0520]
在另一示例性实施例中,抗体包含:
[0521]
i)包含以下cdr的vh结构域:(a)包含seq id no:217的氨基酸序列的cdr-h1;(b)包含seq id no:218的氨基酸序列的cdr-h2;和(c)包含seq id no:219的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代;和
[0522]
ii)vl结构域,该vl结构域包含以下cdr:(a)包含seq id no:220的氨基酸序列的cdr-l1;(b)包含seq id no:221的氨基酸序列的cdr-l2;和(c)包含seq id no:222的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0523]
在另一示例性实施例中,抗体包含:
[0524]
i)重链可变结构域(vh)序列,其与seq id no:232的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;以及
[0525]
ii)轻链可变结构域(vl)序列,其与seq id no:231的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。
[0526]
在另一个示例性实施例中,抗s-hbs抗体包含:(a)包含seq id no:217的氨基酸序列的cdr-h1;(b)包含seq id no:218的氨基酸序列的cdr-h2;(c)包含seq id no:219的氨基酸序列的cdr-h3;(d)包含seq id no:220的氨基酸序列的cdr-l1;(e)包含seq id no:221的氨基酸序列的cdr-l2;和(f)包含seq id no:222的氨基酸序列的cdr-l3,和vh结构
域,其与seq id no:232的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;和vl结构域,其与seq id no:231的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。在一个方面,vh结构域与seq id no:232的氨基酸序列具有至少95%序列同一性。在一个方面,vl结构域与seq id no:231的氨基酸序列具有至少95%序列同一性。在一个实施例中,抗体与s-hbs特异性结合。在另一个实施例中,抗体与s-hbs结合,其解离常数(kd)与包含seq id no:232的vh序列和seq id no:231的vl序列的抗体的解离常数(kd)相比降低多达10倍或提高多达10倍。
[0527]
一方面,抗体分别包含seq id no:232和seq id no:231中的vh序列和vl序列,包括那些序列的翻译后修饰。
[0528]
在另一方面,抗体可以包含seq id no:233的全长轻链和/或seq id no:234或275的全长重链。
[0529]
在进一步方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体所结合的相同表位结合。例如,在某些方面中,提供了与抗s-hbs抗体所结合的相同表位结合的抗体,该抗体包含seq id no:232的vh序列以及seq id no:231的vl序列。在某些方面,提供了与seq id no:253的s-hbs的以下残基结合的抗体:w165和/或r169,以及任选地m103。抗体可以包含如上定义的任何序列。
[0530]
在另一方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体竞争结合s-hbs。
[0531]
在一些实施例中,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.263与s-hbs(例如,seq id no:253的s-hbs)的结合活性。
[0532]
另外地或可替代地,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.263与seq id no:254-262的蛋白质中的一种或多种(例如,至少seq id no:257)、任选地seq id no:254至262的蛋白质中的每一种的结合活性。
[0533]
参考抗体bc1.263具有seq id no:232的vh序列和seq id no:231的vl序列。它具有seq id no:234或275的全长重链和seq id no:233的全长轻链。seq id no:275包含由载体lt615368.1表达的igg1恒定区,如实例中所用。
[0534]
在一些实施例中,当在同一测定中评估时,本节中所述的抗体可以以比参考抗体bc1.263对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与s-hbs(例如seq id no:253的s-hbs)结合。
[0535]
另外地或可替代地,当在同一测定中评估时,抗体可以以比参考抗体bc1.263对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与seq id no:254-262中的一个或多个(例如,至少seq id no:257)、任选地seq id no:254-262的蛋白质中的每一种结合。
[0536]
在一些实施例中,如本节中所述的抗体可以以比参考抗体bc1.263的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与s-hbs(例如,seq id no:253的s-hbs)结合,如通过elisa或流式细胞术测量的。可替代地或另外地,抗体可以以比参考抗体
bc1.263的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与seq id no:254-262中的一个或多个或seq id no:254-262的蛋白质中的每一种、任选地至少seq id no:257的蛋白质结合,如通过elisa或通过流式细胞术测量的。
[0537]
在一些实施例中,如本节中所述的抗体可以具有或保留针对hbv基因型a、b、c和/或d,任选地所有a、b、c和d的体外中和活性。例如,如本节中所述的抗体可以具有或保留针对hbv基因型d的体外中和活性,例如ic50值≤100pg/ml,任选地≤10pg/ml。
[0538]
在另一个实施例中,当使用同一测定(例如,如本文所述的体外中和测定)评估时,抗体可以具有用于中和hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的ic
50
值,其比参考抗体bc1.263对相同基因型的ic
50
值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于参考抗体bc1.263对相同基因型的ic50值。
[0539]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.263对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的中和活性。
[0540]
任选地,抗体可以例如在感染hbv基因型a、b、c或d,任选地d的个体中体内抑制病毒血症。任选地,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bc1.263对hbv基因型a、b、c和/或d,任选地至少d,任选地所有a、b、c和d的体内病毒血症抑制活性。
[0541]
n.
[0542]
在一个方面,本发明提供了包含vh结构域的抗体,该vh结构域包含选自以下各项的至少一个、至少两个或所有三个vh cdr序列:(a)包含seq id no:235的氨基酸序列的cdr-h1、(b)包含seq id no:236的氨基酸序列的cdr-h2、(c)包含seq id no:237的氨基酸序列的cdr-h3。在另一方面,抗体包含vh结构域,该vh结构域包含以下cdr:(a)包含seq id no:235的氨基酸序列的cdr-h1;(b)包含seq id no:236的氨基酸序列的cdr-h2;和(c)包含seq id no:237的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0543]
在一个方面,vh结构域可以进一步包含一个或多个重链框架序列,该序列选自以下各项:(a)seq id no:241的重链框架区1(hc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:242的重链框架区2(hc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:243的重链框架区3(hc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:244的重链框架区4(hc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vh结构域包含如(a)至(d)中定义的每个重链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0544]
在另一方面,抗s-hbs抗体包含与seq id no:250的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的重链可变结构域(vh)序列。一方面,抗s-hbs抗体包含与seq id no:250的氨基酸序列具有至少95%序列同
一性的重链可变结构域(vh)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vh序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:250中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含seq id no:250中的vh序列,包括该序列的翻译后修饰。在一个具体方面,vh包含一、二或三个选自以下各项的cdr:(a)包含seq id no:235所示的氨基酸序列的cdr-h1,(b)包含seq id no:236所示的氨基酸序列的cdr-h2,以及(c)包含seq id no:237所示的氨基酸序列的cdr-h3。
[0545]
在另一方面,抗s-hbs抗体包含seq id no:250的vh的一个或多个重链cdr序列。在一个方面,抗s-hbs抗体包含seq id no:250的vh结构域的一个或多个(优选所有三个)重链cdr氨基酸序列和与seq id no:250的vh结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0546]
在另一方面,本发明提供了包含vl结构域的抗体,该vl结构域包含选自以下各项的至少一个、至少两个或所有三个vl cdr序列:(a)包含seq id no:238的氨基酸序列的cdr-l1、(b)包含seq id no:239的氨基酸序列的cdr-l2、(c)包含seq id no:240的氨基酸序列的cdr-l3。在另一方面,抗体包含vl结构域,该vh结构域包含以下cdr:(a)包含seq id no:238的氨基酸序列的cdr-l1;(b)包含seq id no:239的氨基酸序列的cdr-l2;和(c)包含seq id no:240的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0547]
在一个方面,抗s-hbs抗体vl结构域可以进一步包含一个或多个轻链框架序列,该序列选自以下各项:(a)seq id no:245的轻链框架区1(lc-fr1)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体、(b)seq id no:246的轻链框架区2(lc-fr2)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体(c)seq id no:247的轻链框架区3(lc-fr3)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体和(d)seq id no:248的轻链框架区4(lc-fr4)或与其具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的变体。任选地,vl结构域包含如(a)至(d)中定义的每个轻链框架序列。任选地,百分比序列同一性是95%。任选地,百分比序列同一性是98%。
[0548]
在另一方面,提供了抗s-hbs抗体,其中该抗体包含与seq id no:249的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性的轻链可变结构域(vl)序列。一方面,抗s-hbs抗体包含与seq id no:249的氨基酸序列具有至少95%序列同一性的轻链可变结构域(vl)序列。在某些方面,具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性的vl序列相对于参考序列含有取代(例如,保守取代)、插入或缺失,但是包含该序列的抗s-hbs抗体保留了与s-hbs结合的能力。在某些方面,在seq id no:249中,总共有1至10个氨基酸已被取代、插入和/或缺失。在某些方面,取代、插入或缺失发生在cdr之外的区域(即,在fr中)。任选地,抗s-hbs抗体包含
seq id no:249中的vl序列,包括该序列的翻译后修饰。在一个具体方面,vl包含一、二或三个选自以下各项的cdr:(a)包含seq id no:238的氨基酸序列的cdr-l1,(b)包含seq id no:239的氨基酸序列的cdr-l2和(c)包含seq id no:240的氨基酸序列的cdr-l3。
[0549]
在另一个实施例中,抗s-hbs抗体包含seq id no:249的vl的一个或多个cdr序列。在一个方面,抗s-hbs抗体包含seq id no:249的vl结构域的一个或多个(优选所有三个)轻链cdr氨基酸序列和与seq id no:249的vl结构域的框架氨基酸序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%序列同一性的框架。任选地,序列同一性为95%或98%。
[0550]
在另一方面,提供一种抗s-hbs抗体,其中该抗体包含如在上文提供的任一方面中的vh序列以及如在上文提供的任一方面中的vl序列。
[0551]
例如,在一个示例性实施例中,抗体包含:包含seq id no:237的cdr-h3的vh结构域;和包含seq id no:240的cdr-l3的vl结构域。任选地,vh结构域进一步包含seq id no:236的cdr-h2。
[0552]
在另一示例性实施例中,抗体包含:
[0553]
i)包含以下cdr的vh结构域:(a)包含seq id no:235的氨基酸序列的cdr-h1;(b)包含seq id no:236的氨基酸序列的cdr-h2;和(c)包含seq id no:237的氨基酸序列的cdr-h3;或其变体,其中cdr-h1、cdr-h2或cdr-h3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代;和
[0554]
ii)vl结构域,该vl结构域包含以下cdr:(a)包含seq id no:238的氨基酸序列的cdr-l1;(b)包含seq id no:239的氨基酸序列的cdr-l2;和(c)包含seq id no:240的氨基酸序列的cdr-l3;或其变体,其中cdr-l1、cdr-l2或cdr-l3中的一个或多个中的一个、两个或三个氨基酸被另一种氨基酸取代。
[0555]
在另一示例性实施例中,抗体包含:
[0556]
i)重链可变结构域(vh)序列,其与seq id no:250的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;以及
[0557]
ii)轻链可变结构域(vl)序列,其与seq id no:249的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。
[0558]
在另一个示例性实施例中,抗s-hbs抗体包含:(a)包含seq id no:235的氨基酸序列的cdr-h1;(b)包含seq id no:236的氨基酸序列的cdr-h2;(c)包含seq id no:237的氨基酸序列的cdr-h3;(d)包含seq id no:238的氨基酸序列的cdr-l1;(e)包含seq id no:239的氨基酸序列的cdr-l2;和(f)包含seq id no:240的氨基酸序列的cdr-l3,和vh结构域,其与seq id no:250的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性;和vl结构域,其与seq id no:249的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性。在一个方面,vh结构域与seq id no:250的氨基酸序列具有至少95%序列同一性。在一个方面,vl结构域与seq id no:249的氨基酸序列具有至少95%序列同一性。在一个实施例中,抗体与s-hbs特异性结合。在另一个实施例中,抗体与s-hbs结合,其解离常数(kd)与包含seq id no:250的vh序列和seq id no:249的vl序列的抗体的解离常数(kd)相比降低多达10倍或提高多达10倍。
[0559]
一方面,抗体分别包含seq id no:250和seq id no:249中的vh序列和vl序列,包括那些序列的翻译后修饰。
[0560]
在另一方面,抗体可以包含seq id no:251的全长轻链和/或seq id no:252或276的全长重链。
[0561]
在进一步方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体所结合的相同表位结合。例如,在某些方面中,提供了与抗s-hbs抗体所结合的相同表位结合的抗体,该抗体包含seq id no:250的vh序列以及seq id no:249的vl序列。在某些方面,提供了与seq id no:253的s-hbs的以下残基结合的抗体:c124、c137、c138和/或c139;任选地r122、c149和/或i152;和任选地w156。抗体可以包含如上定义的任何序列。
[0562]
在另一方面,本发明提供一种抗体,其与本文所提供的抗s-hbs抗体竞争结合s-hbs。
[0563]
在一些实施例中,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv4.105与s-hbs(例如,seq id no:253的s-hbs)的结合活性。
[0564]
另外地或可替代地,当在同一测定(例如elisa测定或流式细胞术测定)中评估时,如本节中所述的抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv4.105与seq id no:257、258、259、260和/或261的蛋白质中的一种或多种、任选地其中的每一种、任选地至少seq id no:257的结合活性。
[0565]
参考抗体bv4.105具有seq id no:250的vh序列和seq id no:249的vl序列。它具有seq id no:252或276的全长重链和seq id no:251的全长轻链。seq id no:276包含由载体lt615368.1表达的igg1恒定区,如实例中所用。
[0566]
在一些实施例中,当在同一测定中评估时,本节中所述的抗体可以以比参考抗体bv4.105对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与s-hbs(例如seq id no:253的s-hbs)结合。
[0567]
另外地或可替代地,当在同一测定中评估时,抗体可以以比参考抗体bv4.105对相同抗原的kd值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的kd值与seq id no:257、258、259、260和/261中的一个或多个、任选地seq id no:257、258、259、260和/或261的蛋白质中的每一种、任选地至少seq id no:257结合。
[0568]
在一些实施例中,如本节中所述的抗体可以以比参考抗体bv4.105的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与s-hbs(例如,seq id no:253的s-hbs)结合,如通过elisa或流式细胞术测量的。可替代地或另外地,抗体可以以比参考抗体bv4.105的ec50高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于其的ec50与seq id no:257、258、259、260和/261的蛋白质中的一种或多种、任选地其中的每一种、任选地至少seq id no:257结合,如通过elisa或通过流式细胞术测量的。
[0569]
在一些实施例中,如本节中所述的抗体可以具有或保留针对hbv基因型d、e、f和/或h,任选地所有基因型d、e、f和h的体外中和活性。例如,如本节中所述的抗体可以具有或保留针对hbv基因型d的体外中和活性,例如ic50值≤100pg/ml,任选地≤10pg/ml。
[0570]
在另一个实施例中,当使用同一测定(例如,如本文所述的体外中和测定)评估时,抗体可以具有用于中和hbv基因型d、e、f、g和/或h,任选地至少d,任选地所有d、e、f、g和h的
ic50值,其比参考抗体bv4.105对相同基因型的ic
50
值高不超过50、10、9、8、7、6、5、4、3或2倍,或小于或等于参考抗体bv4.105对相同基因型的ic50值。
[0571]
在另一个实施例中,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv4.105对hbv基因型d、e、f、g和/或h,任选地至少d,任选地所有d、e、f、g和h的中和活性。
[0572]
任选地,抗体可以例如在感染hbv基因型d、e、f、g或h,任选地d的个体中体内抑制病毒血症。任选地,当使用同一测定(例如,如本文所述的测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体bv4.105对hbv基因型d、e、f、g和/或h,任选地至少d,任选地所有d、e、f、g和h的体内病毒血症抑制活性。
[0573]
一般而言,根据本发明任何方面(包括上述a-n中任何一个)的抗s-hbs抗体可以是单克隆抗体,包括嵌合抗体、人源化抗体或人抗体。在一个方面,抗s-hbs抗体是抗体片段,例如,fv、fab、fab'、scfv、双体抗体或f(ab')2片段。
[0574]
在另一个一般方面,抗体可以为全长抗体,例如本文所定义的完整igg1、igg2、igg3抗体或其他抗体类别或同种型。
[0575]
全长抗体的c末端赖氨酸(lys447)可以存在或不存在。在另一方面,c末端甘氨酸(gly446)和c末端赖氨酸(lys447)可以存在或不存在。
[0576]
在进一步方面,根据任一上述方面所述的抗s-hbs抗体可单独或组合地纳入如以下1-7节所述的特征。
[0577]
1.抗体亲和力
[0578]
在某些方面,本文提供的抗体针对靶蛋白的解离常数(kd)为≤1μm、≤100nm、≤10nm、≤1nm、≤0.1nm、≤0.01nm或≤0.001nm(例如,10-8
m或更小,例如10-8
m至10-13
m,例如10-9
m至10-13
m)。
[0579]
在其他方面,本文提供的抗体具有或保持比参考抗体针对靶蛋白的kd值高不超过50、10、9、8、7、6、5、4、3或2倍或小于或等于其的kd,其中参考抗体选自由以下项组成的组:bc1.187、bv4.115、bc8.159、bv6.172、bc1.229、bc8.111、bc1.128、bc3.106、bc1.180、bv4.104、bc8.104、bc4.204、bc1.263和bv4.105。
[0580]
一方面,使用表面等离子体共振测定法测量kd。例如,使用-2000或-3000(biacore,inc.,piscataway,nj)在25℃下用固定的抗原cm5芯片以~10个响应单位(ru)进行测定。在一个方面,根据供应商说明书,用n-乙基-n'-(3-二甲基氨基丙基)-碳化二亚胺盐酸盐(edc)及n-羟基琥珀酰亚胺(nhs)活化羧甲基化的葡聚糖生物感测器芯片(cm5,biacore,inc.)。将抗原用10mm醋酸钠ph 4.8稀释至5μg/ml(约0.2μm),之后以5μl/分钟的流量进行注射以获得大约10响应单位(ru)的偶联蛋白。注射抗原之后,注射1m乙醇胺以阻断未反应的基团。关于动力学测量,在25℃,以约25μl/min的流速注射在含有0.05%聚山梨酯20(tween 20
tm
)表面活性剂(pbst)的pbs中的fab的两倍连续稀释液(0.78nm至500nm)。使用简单的一对一langmuir结合模型(evaluation software 3.2版),通过同时拟合缔合与解离感测器图来计算缔合速率(k
on
)与解离速率(k
off
)。平衡解离常数(kd)计算为比率k
off
/k
on
。参加例如chen等人,j.mol.biol.293:865-881(1999)。若通过上述表面等离子体共振测定得出缔合速率超过
106m-1
s-1
,则可通过使用荧光淬灭技术测定缔合速率,即如在分光计诸如配备止流装置的分光光度计(aviv instruments)或8000系列slm-aminco
tm
分光光度计(thermospectronic)中用搅拌比色杯所测得的,在浓度渐增的抗原存在下,测量在25℃下pbs ph 7.2中的20nm抗抗原抗体(fab形式)的荧光发射强度(激发=295nm;发射=340nm,16nm带通)的增加或减少。
[0581]
在另一方面,elisa可用于计算kd值,例如,如friguet等人j immunol.methods(1985)77(2):305-19所描述的。
[0582]
2.抗体片段
[0583]
在某些方面,本文提供的抗体是抗体片段。
[0584]
一方面,抗体片段是fab’、fab
’‑
sh或f(ab’)2片段,特别是fab片段。木瓜蛋白酶消化完整抗体产生两个相同的抗原结合片段,称为“fab”片段,其各自包含重链可变结构域和轻链可变结构域(分别为vh和vl)以及轻链的恒定结构域(cl)和重链的第一恒定结构域(ch1)。因此,术语“fab片段”是指包括vl结构域和cl结构域的轻链以及包括vh结构域和ch1结构域的重链片段的抗体片段。“fab'片段”与fab片段的不同之处在于fab'片段在ch1结构域的羧基端添加残基,这些残基包括来自抗体铰链区的一个或多个半胱氨酸。fab'-sh是fab'片段,其中恒定结构域的半胱氨酸残基带有游离巯基。胃蛋白酶处理产生f(ab')2片段,该片段具有两个抗原结合位点(两个fab片段)和fc区的一部分。关于对包含补救受体结合表位残基并具有增加的体内半衰期的fab和f(ab')2片段的讨论,请参见美国专利号5,869,046。
[0585]
在另一方面,抗体片段是双体抗体、三体抗体或四体抗体。“双体抗体”是具有两个抗原结合位点的抗体片段,其可以是二价或双特异性的。参见,例如,ep 404,097;wo 1993/01161;hudson等人,nat.med.9:129-134(2003);和hollinger等人,proc.natl.acad.sci.usa 90:6444-6448(1993)。三体抗体和四体抗体也在hudson等人,nat.med.9:129-134(2003)中进行了描述。
[0586]
在另一个方面,抗体片段为单链fab片段。“单链fab片段”或“scfab”是由抗体重链可变结构域(vh)、抗体重链恒定结构域1(ch1)、抗体轻链可变结构域(vl)、抗体轻链恒定结构域(cl)和接头组成的多肽,其中抗体结构域和接头在n末端至c末端方向上具有以下顺序中的一种:a)vh-ch1-接头-vl-cl、b)vl-cl-接头-vh-ch1、c)vh-cl-接头-vl-ch1,或d)vl-ch1-接头-vh-cl。特别地,所述接头是至少30个氨基酸,优选地在32个与50个氨基酸之间的多肽。所述单链fab片段经由cl结构域与ch1结构域之间的天然二硫键而稳定化。此外,这些单链fab片段可以通过经由插入半胱氨酸残基(例如,根据kabat编号的可变重链中的44位和可变轻链中的100位)生成链间二硫键,而进一步稳定化。
[0587]
在另一方面,抗体片段是单链可变片段(scfv)。“单链可变片段”或“scfv”是抗体的重链可变结构域(vh)和轻链可变结构域(vl)的融合蛋白,是通过接头连接的。特别地,接头是10个至约25个氨基酸的短多肽,并且通常富含甘氨酸以获得柔性,以及富含丝氨酸或苏氨酸以获得溶解性,并且可以将vh的n-末端与vl的c-末端连接,或反之亦然。尽管去除了恒定区并且引入了接头,但该蛋白质仍保留了原始抗体的特异性。关于scfv片段的综述,参见例如pl
ü
ckthun,载于the pharmacology of monoclonal antibodies,第113卷,rosenburg和moore编辑(springer-verlag,new york),第269至第315页(1994);还可参见
wo 93/16185;以及美国专利号5,571,894和5,587,458。
[0588]
在另一方面,抗体片段是单结构域抗体。“单结构域抗体”是包含抗体的全部或部分重链可变结构域或者抗体的全部或部分轻链可变结构域的抗体片段。在某些方面,单结构域抗体是人单结构域抗体(domantis,inc.,waltham,ma;参见例如美国专利号6,248,516b1)。
[0589]
抗体片段可以通过各种技术制备,包括但不限于完整抗体的蛋白水解消化以及由重组宿主细胞(例如大肠杆菌)重组产生,如本文所述。
[0590]
3.嵌合抗体和人源化抗体
[0591]
在某些方面,本文提供的抗体是嵌合抗体。某些嵌合抗体描述于,例如,美国专利号4,816,567和morrison等人,proc.natl.acad.sci.usa,81:6851-6855(1984)中。在一个实例中,嵌合抗体包含非人可变区(例如,源自小鼠、大鼠、仓鼠、兔或非人灵长类动物(诸如猴)的可变区)和人恒定区。在另一个实例中,嵌合抗体为其中类别或亚类已经与亲本抗体的类别或亚类改变的“类别转换”抗体。嵌合抗体包括其抗原结合片段。
[0592]
在某些方面,嵌合抗体是人源化抗体。通常,将非人抗体人源化以减少对人的免疫原性,同时保留亲本非人抗体的特异性和亲和力。通常,人源化抗体包含一个或多个可变结构域,其中cdr(或其部分)源自非人抗体,并且fr(或其部分)源自人抗体序列。人源化抗体任选地还将包含人恒定区的至少一部分。在一些方面,人源化抗体中的一些fr残基被来自非人抗体(例如,cdr残基所来源于的抗体)的相应残基取代,例如以恢复或改善抗体特异性或亲和力。
[0593]
人源化抗体及其制备方法在例如almagro和fransson,front.biosci.13:1619-1633(2008)中综述,并且进一步描述于例如riechmann等人,nature 332:323-329(1988);queen等人,proc.nat’l acad.sci.usa 86:10029-10033(1989);美国专利号5,821,337、7,527,791、6,982,321和7,087,409;kashmiri等人,methods 36:25-34(2005)(描述了特异性决定区(sdr)移植);padlan,mol.immunol.28:489-498(1991)(描述了“表面再塑”);dall’acqua等人,methods 36:43-60(2005)(描述了“fr改组”);以及osbourn等人,methods 36:61-68(2005)和klimka等人,br.j.cancer,83:252-260(2000)(描述了用于fr改组的“指导选择”方法)中。
[0594]
可用于人源化的人框架区包括但不限于:使用“最佳拟合”方法选择的框架区(参见,例如,sims等人j.immunol.151:2296(1993));来源于轻链或重链可变区的特定亚组的人抗体的共有序列的框架区(参见,例如,carter等人proc.natl.acad.sci.usa,89:4285(1992);以及presta等人j.immunol.,151:2623(1993));人成熟(体细胞突变)框架区或人种系框架区(参见,例如,almagro和fransson,front.biosci.13:1619-1633(2008));以及来源于筛选fr文库的框架区(参见,例如,baca等人,j.biol.chem.272:10678-10684(1997)和rosok等人,j.biol.chem.271:22611-22618(1996))。
[0595]
4.人抗体
[0596]
在某些方面,本文提供的抗体是人抗体。可以使用本领域已知的各种技术来产生人抗体。人抗体一般描述于van dijk和van de winkel,curr opin pharmacol.5:368-74(2001)和lonberg,curr opin immunol.20:450-459(2008)中。
[0597]
可以通过以下方式来制备人抗体:将免疫原施用于转基因动物,该转基因动物已
被修饰以响应于抗原激发而产生具有人可变区的完整人抗体或完整抗体。此类动物通常含有全部或部分人免疫球蛋白基因座,该全部或部分人免疫球蛋白基因座替代内源性免疫球蛋白基因座,或者在动物的染色体外存在或随机整合至动物的染色体中。在此类转基因小鼠中,内源性免疫球蛋白基因座通常已被灭活。关于从转基因动物获得人抗体的方法的综述,参见lonberg,nat.biotech.23:1117-1125(2005)。还参见例如描述xenomouse
tm
技术的美国专利号6,075,181和6,150,584;描述技术的美国专利号5,770,429;描述k-m技术的美国专利号7,041,870,以及描述技术的美国专利申请公开号us2007/0061900)。可以进一步修饰来自由此类动物产生的完整抗体的人可变区,例如通过与不同的人恒定区组合。
[0598]
人抗体也可以通过基于杂交瘤的方法制备。已经描述了用于产生人单克隆抗体的人骨髓瘤和小鼠-人杂交骨髓瘤细胞系。(参见例如kozbor j.immunol.,133:3001(1984);brodeur等人,monoclonal antibody production techniques and applications,第51-63页(marcel dekker,inc.,new york,1987);以及boerner等人,j.immunol.,147:86(1991)。)经由人b细胞杂交瘤技术产生的人抗体也如li等人,proc.natl.acad.sci.usa,103:3557-3562(2006)所述。另外的方法包括例如在美国专利号7,189,826(描述了从杂交瘤细胞系产生单克隆人igm抗体)和ni,xiandai mianyixue,26(4):265-268(2006)(描述了人-人杂交瘤)中描述的那些方法。人类杂交瘤技术(trioma技术)也描述于vollmers和brandlein,histology and histopathology,20(3):927-937(2005)和vollmers和brandlein,methods and findings in experimental and clinical pharmacology,27(3):185-91(2005)中。
[0599]
人抗体还可以通过分离选自人源噬菌体展示文库的可变结构域序列产生。然后可以将此类可变结构域序列与预期的人恒定结构域结合。从抗体文库中选择人抗体的技术描述如下。
[0600]
5.源自文库的抗体
[0601]
在某些方面,本文提供的抗体衍生自文库。可以通过筛选组合文库中具有一个或多个所需活性的抗体来分离本发明的抗体。用于筛选组合文库的方法综述于例如lerner等人,nature reviews 16:498-508(2016)中。例如,本领域已知多种方法用于产生噬菌体展示文库并筛选此类文库以获得具有所需结合特征的抗体。此类方法综述于例如frenzel等人,mabs 8:1177-1194(2016);bazan等人,human vaccines and immunotherapeutics 8:1817-1828(2012)和zhao等人,critical reviews in biotechnology 36:276-289(2016)中,以及hoogenboom等人,methods in molecular biology 178:1-37(o’brien等人编辑,human press,totowa,nj,2001)中和marks和bradbury,methods in molecular biology 248:161-175(lo编辑,human press,totowa,nj,2003)中。
[0602]
在某些噬菌体展示方法中,将vh和vl基因的所有组成成分通过聚合酶链式反应(pcr)单独克隆,并在噬菌体文库中随机重组,然后可以从所述噬菌体文库中筛选抗原结合噬菌体,如在winter等人,annual review of immunology 12:433-455(1994)中所描述的。噬菌体通常将抗体片段展示为单链fv(scfv)片段或fab片段。来自经免疫的来源的文库提供针对免疫原的高亲和力抗体,而无需构建杂交瘤。可替代地,可以克隆所有天然组成成分(例如,来自人的所有天然组成成分)以提供针对广泛的非自身抗原和自身抗原的抗体的单
一来源,而无需任何免疫,如由griffiths等人在embo journal 12:725-734(1993)中所描述的。此外,还通过以下方式来合成天然文库:克隆来自干细胞的未重排的v基因区段;以及使用含有随机序列的pcr引物来编码高度可变的cdr3区并完成体外重排,如由hoogenboom和winter在journal of molecular biology 227:381-388(1992)中所描述的。描述人抗体噬菌体文库的专利出版物包括,例如:美国专利号5,750,373;7,985,840;7,785,903和8,679,490以及美国专利公开号2005/0079574、2007/0117126、2007/0237764和2007/0292936。
[0603]
本领域已知用于筛选具有一种或多种所需活性的抗体的组合文库的方法的其他实例包括核糖体和mrna展示,以及对细菌、哺乳动物细胞、昆虫细胞或酵母细胞进行抗体展示和选择的方法。用于酵母表面展示的方法综述于例如scholler等人,methods in molecular biology 503:135-56(2012)和cherf等人,methods in molecular biology 1319:155-175(2015)以及zhao等人,methods in molecular biology 889:73-84(2012)中。用于核糖体展示的方法描述于例如he等人,nucleic acids research 25:5132-5134(1997)和hanes等人,pnas 94:4937-4942(1997)中。
[0604]
在本文中从人抗体文库分离出的抗体或抗体片段被认为是人抗体或人抗体片段。
[0605]
6.多特异性抗体
[0606]
在某些方面,本文提供的抗体是多特异性抗体,特别是双特异性抗体。“多特异性抗体”是对至少两个不同位点(即,不同抗原上的不同表位或相同抗原上的不同表位)具有结合特异性的单克隆抗体。在某些方面,多特异性抗体具有三种或更多种结合特异性。在某些方面,结合特异性中的一种是针对s-hbs的,并且另一种特异性是针对任何其他抗原的。在某些方面,双特异性抗体可以与s-hbs的两个(或更多个)不同的表位结合。多特异性(例如双特异性)抗体也可用于将细胞毒剂或细胞定位于表达s-hbs的细胞。可以将多特异性抗体制备为全长抗体或抗体片段。
[0607]
用于制备多特异性抗体的技术包括但不限于具有不同特异性的两种免疫球蛋白重链-轻链对的重组共表达(参见milstein和cuello,nature 305:537(1983))及“杵臼结构”工程化(参见例如,美国专利5,731,168,以及atwell等人,j.mol.biol.270:26(1997))。多特异性抗体还可以通过以下方式来制备:工程化用于制备抗体fc-异二聚体分子的静电操纵效应(参见例如,wo 2009/089004);使两个或更多个抗体或片段交联(参见例如,美国专利号4,676,980,以及brennan等人,science,229:81(1985));使用亮氨酸拉链来产生双特异性抗体(参见例如,kostelny等人,j.immunol.,148(5):1547-1553(1992)和wo 2011/034605);使用用于避免轻链错配问题的常用轻链技术(参见例如,wo 98/50431);使用用于制备双特异性抗体片段的“双体抗体”技术(参见例如hollinger等人,proc.natl.acad.sci.usa,90:6444-6448(1993));以及使用单链fv(sfv)二聚体(参见例如gruber等人,j.immunol.,152:5368(1994));以及如tutt等人j.immunol.147:60(1991)中所述制备三特异性抗体。
[0608]
本文还包括具有三个或更多个抗原结合位点的工程化抗体,包括例如“章鱼抗体”或者dvd-ig(参见例如,wo 2001/77342和wo 2008/024715)。具有三个或更多个抗原结合位点的多特异性抗体的其他示例可以在wo 2010/115589、wo 2010/112193、wo 2010/136172、wo 2010/145792和wo 2013/026831中找到。双特异性抗体或其抗原结合片段还包括“双重
作用fab”或“daf”,其包含与s-hbs以及另一种不同抗原结合或与s-hbs的两个不同表位结合的抗原结合位点(参见例如,us 2008/0069820和wo 2015/095539)。
[0609]
多特异性抗体也可以以不对称形式提供,其中在具有相同抗原特异性的一个或多个结合臂中有结构域互换,即通过交换vh/vl结构域(参见例如,wo 2009/080252和wo 2015/150447)、ch1/cl结构域(参见例如,wo 2009/080253)或完整的fab臂(参见例如,wo 2009/080251、wo 2016/016299,还参见schaefer等人,pnas,108(2011)1187-1191,以及klein等人,mabs 8(2016)1010-20)。在一方面,多特异性抗体包含交叉fab片段。术语“交叉fab片段”或“xfab片段”或“交换型fab片段”是指这样的fab片段,其中重链和轻链的可变区或恒定区被交换。交叉fab片段包含由轻链可变区(vl)和重链恒定区1(ch1)组成的多肽链,以及由重链可变区(vh)和轻链恒定区(cl)组成的多肽链。还可以通过将荷电或非荷电的氨基酸突变引入结构域界面以指导正确的fab配对,以对不对称fab臂进行工程化。参见例如wo 2016/172485。
[0610]
多特异性抗体的各种其他分子形式是在本领域中已知的并且包括在本文中(参见例如spiess等人,mol immunol 67(2015)95-106)。
[0611]
本文还包括的一种特定类型的多特异性抗体是这样的双特异性抗体,该双特异性抗体设计用于同时结合靶细胞(例如,感染细胞)上的表面抗原和t细胞受体(tcr)复合物的活化不变组分(诸如cd3),以用于再靶向t细胞以杀伤靶细胞。因此,在某些方面中,本文提供的抗体是多特异性抗体,特别是双特异性抗体,其中结合特异性之一针对s-hbs而另一个针对cd3。
[0612]
可用于此目的双特异性抗体形式的实例包括但不限于:所谓“bite”(双特异性t细胞募召剂)分子,其中两个scfv分子通过柔性接头融合(参见例如wo 2004/106381;wo 2005/061547;wo 2007/042261;wo 2008/119567;nagorsen和exp cell res 317,1255-1260(2011));双体抗体(holliger等人,prot eng 9,299-305(1996))及其衍生物,诸如串联双体抗体(“tandab”;kipriyanov等人,j mol biol 293,41-56(1999));“dart”(双亲和性重新靶向)分子,其基于双体抗体形式,但具有c末端二硫键以实现额外的稳定化(johnson等人,j mol biol 399,436-449(2010));以及所谓的三功能抗体,其为完整的杂交小鼠/大鼠igg分子(如seimetz等人所综述:cancer treat rev 36,458-467(2010))。本文所包含的特定的t细胞双特异性抗体形式描述于以下文献中:wo 2013/026833;wo 2013/026839;wo 2016/020309;bacac等人,oncoimmunology 5(8)(2016)e1203498。
[0613]
7.抗体变体
[0614]
在某些方面中,设想了本文提供的抗体的氨基酸序列变体。例如,可能期望改变抗体的结合亲和力和/或其他生物学特性。抗体的氨基酸序列变体可以通过向编码抗体的核苷酸序列中引入适当的修饰或通过肽合成来制备。此类修饰包括例如抗体氨基酸序列内残基的缺失、和/或插入和/或取代。可以进行缺失、插入和取代的任何组合以实现最终构建体,前提条件是最终构建体具有所需特征,例如抗原结合。
[0615]
a)取代、插入和删除性变体
[0616]
在某些方面,提供了具有一个或多个氨基酸取代的抗体变体。用于取代诱变的感兴趣的位点包括cdr和fr。保守取代在表1中的“优选取代”标题下示出。更多实质性改变提
供于表1的“示例性取代”标题下,并且在下文参考氨基酸侧链类别进行了进一步描述。可以将氨基酸取代引入目标抗体中,并对产物进行所需活性(例如保留/改善的抗原结合、降低的免疫原性,或改善的adcc或cdc)筛选。
[0617]
表1
[0618][0619][0620]
可根据共同的侧链特性将氨基酸分组:
[0621]
(1)疏水性:正亮氨酸、met、ala、val、leu、ile;
[0622]
(2)中性亲水性:cys、ser、thr、asn、gln;
[0623]
(3)酸性:asp、glu;
[0624]
(4)碱性:his、lys、arg;
[0625]
(5)影响链取向的残基:gly,pro;
[0626]
(6)芳族:trp、tyr、phe。
[0627]
非保守性取代将需要用这些类别中的一个的成员交换另一类别的成员。
[0628]
一种类型的取代变体涉及取代亲本抗体(例如,人源化抗体或人抗体)的一个或多
个高可变区残基。通常,相对于亲本抗体,选为用于进一步研究的一个或多个所得变体将在某些生物学特性方面(例如,亲和力增加、免疫原性降低)有改变(例如,改善)和/或将基本上保留亲本抗体的某些生物学特性。示例性取代变体是亲和力成熟抗体,其可例如使用诸如本文所述的那些基于噬菌体展示的亲和力成熟技术方便地生成。简要地说,对一个或多个cdr残基进行突变并且将变体抗体展示在噬菌体上并针对特定生物学活性(例如结合亲和力)进行筛选。
[0629]
例如,可在cdr中作出改变(例如,取代),以改善抗体亲和力。此类改变可发生于cdr“热点”中,即由体细胞成熟过程中发生高频突变的密码子编码的残基(参见例如,chowdhury,methods mol.biol.207:179-196(2008))和/或与抗原接触的残基(检测所得变体vh或vl的结合亲和力。通过构建并自二级文库重新选择而实现的亲和力成熟已被例如hoogenboom等人在methods in molecular biology 178:1-37(o'brien等人编,human press,totowa,nj,(2001))中进行描述。在亲和力成熟的某些方面,通过多种方法(例如,易错pcr、链改组或寡核苷酸定向诱变)的任何一种将多样性引入选择用于成熟的可变基因中。然后创建一个二级文库。随后对该文库进行筛选以鉴别具有所需亲和力的任何抗体变体。引入多样性的另一种方法涉及cdr定向方法,其中将若干cdr残基(例如,每次4至6个残基)随机化。参与抗原结合的cdr残基可例如使用丙氨酸扫描突变或建模来特异性地鉴别。具体而言,常常靶向cdr-h3和cdr-l3。
[0630]
在某些方面,取代、插入或缺失可发生在一个或多个cdr内,只要此类改变基本上不降低抗原结合分子的抗原结合能力即可。例如,可在cdr中进行基本上不降低结合亲和力的保守性改变(例如,如本文提供的保守性取代)。这样的改变可以例如在cdr中的抗原接触残基的外部。在上文提供的某些变体vh和vl序列中,每个cdr要么保持不变,要么包含不超过一个、两个或三个氨基酸取代。
[0631]
可用于鉴别可被靶向诱变的抗体残基或区域的方法称作“丙氨酸扫描诱变”,如cunningham和wells(1989)science,244:1081-1085所述。在此方法中,鉴别残基或一组靶残基(例如,带电残基,诸如arg、asp、his、lys和glu)并用中性或带负电的氨基酸(例如,丙氨酸或多丙氨酸)替换以确定抗体与抗原的相互作用是否受到影响。可在对初始取代展示功能敏感性的氨基酸位置引入其他取代。可替代地或另外地,可以使用抗原-抗体复合物的晶体结构鉴别抗体与抗原之间的接触点。可靶向或消除作为取代的候选的此类接触残基和相邻残基。可筛选变体以确定它们是否具备期望的特性。
[0632]
氨基酸序列插入包括长度范围为一个残基至含有一百个或更多个残基的多肽的氨基和/或羧基末端融合,以及一个或多个氨基酸残基的序列内插入。末端插入的实例包括具有n末端甲硫氨酰残基的抗体。抗体分子的其他插入变体包括将抗体的n末端或c末端与增加抗体的血清半衰期的酶(例如,对于adept(抗体定向酶前药治疗))或多肽融合。
[0633]
b)糖基化变体
[0634]
在某些方面,改变本文提供的抗体以增加或降低抗体糖基化的程度。糖基化位点向抗体的添加或缺失可通过改变氨基酸序列以产生或去除一个或多个糖基化位点而方便地实现。
[0635]
当抗体包含fc区时,与其相连的寡糖可以被改变。由哺乳动物细胞产生的天然抗体通常包含支链的、双触角寡糖,该双触角寡糖通常通过n-键结连接至fc区的ch2结构域的
asn297。参见,例如,wright等人tibtech 15:26-32(1997)。寡糖可包括各种碳水化合物,例如,甘露糖、n-乙酰基葡糖胺(glcnac)、半乳糖和唾液酸,以及附接于双触角寡糖结构的“主干”中的glcnac的岩藻糖。在一些方面中,可对本发明的抗体中的寡糖进行修饰,以产生具有某些改善的特性的抗体变体。
[0636]
一方面,提供了具有非岩藻糖基化的寡糖的抗体变体,即缺少(直接或间接地)连接在fc区的岩藻糖的寡糖结构。这样的非岩藻糖基化的寡糖(也称为“去岩藻糖基化”的寡糖)特别是n-连接的寡糖,其缺少在双触角寡糖结构的茎中连接第一glcnac的岩藻糖残基。一方面,提供了与天然或亲本抗体相比在fc区中具有增加比例的非岩藻糖基化寡糖的抗体变体。例如,非岩藻糖基化寡糖的比例可以为至少约20%、至少约40%、至少约60%、至少约80%或甚至约100%(即不存在岩藻糖基化寡糖)。非岩藻糖基化寡糖的百分比,如例如wo 2006/082515中所述,如通过maldi-tof质谱法测量的,是缺少岩藻糖残基的寡糖的(平均)量相对于与asn 297连接的所有寡糖(例如复杂、杂合和高甘露糖结构)之和。asn297是指位于fc区中约297位的天冬酰胺残基(fc区残基的eu编号);然而,由于抗体中的微小序列变化,asn297也可以位于297位上游或下游大约
±
3个氨基酸,即在294位和300位之间。在fc区中具有非岩藻糖基化寡糖比例增加的此类抗体可具有改善的fcγriiia受体结合和/或改善的效应子功能,特别是改善的adcc功能。参见例如us 2003/0157108和us 2004/0093621。
[0637]
能够产生岩藻糖基化减少的抗体的细胞系的实例包括缺乏蛋白质岩藻糖基化的lec13 cho细胞(ripka等人.arch.biochem.biophys.249:533-545(1986);us 2003/0157108;和wo 2004/056312,尤其是在实例11中),以及敲除细胞系,例如α-1,6-岩藻糖基转移酶基因,fut8,敲除cho细胞(参见,例如,yamane-ohnuki等人.biotech.bioeng.87:614-622(2004);kanda,y.等人,biotechnol.bioeng.,94(4):680-688(2006);和wo 2003/085107),或具有降低或取消的gdp-岩藻糖合成或转运蛋白活性的细胞(参见,例如,us2004259150、us2005031613、us2004132140、us2004110282)。
[0638]
在另一方面,抗体变体提供了二等分的寡糖,例如,其中连接至抗体的fc区的双触角寡糖被glcnac二等分。如上所述,这样的抗体变体可以具有减少的岩藻糖基化和/或改善的adcc功能。此类抗体变体的实例描述于例如umana等人,nat biotechnol 17,176-180(1999);ferrara等人,biotechn bioeng 93,851-861(2006);wo 99/54342;wo 2004/065540,wo 2003/011878。
[0639]
还提供了在连接于fc区的寡糖中具有至少一个半乳糖残基的抗体变体。这样的抗体变体可以具有改善的cdc功能。此类抗体变体描述于例如wo 1997/30087、wo 1998/58964和wo 1999/22764中。
[0640]
c)fc区变体
[0641]
在某些方面,一个或多个氨基酸修饰可引入本文提供的抗体的fc区中,从而生成fc区变体。fc区变体可包含人fc区序列(例如人igg1、igg2、igg3或igg
4 fc区),其在一个或多个氨基酸位置上包含氨基酸修饰(例如取代)。
[0642]
在某些方面,本发明考虑具有一些但不是全部效应子功能的抗体变体,这使其成为其中抗体的体内半衰期很重要而某些效应子功能(例如补体依赖性细胞毒性(cdc)和抗体依赖性细胞介导的细胞毒性(adcc))不必要或有害的应用的理想候选者。可以进行体外和/或体内细胞毒性测定,以确认cdc和/或adcc活性的降低/耗尽。例如,可以进行fc受体
(fcr)结合测定以确保抗体缺乏fcγr结合(因此可能缺乏adcc活性),但是保留fcrn结合能力。介导adcc的主要细胞nk细胞仅表达fcγriii,而单核细胞表达fcγri、fcγrii和fcγriii。造血细胞上的fcr表达总结在ravetch和kinet,annu.rev.immunol.9:457-492(1991)的第464页的表3中。用于评估目标分子的adcc活性的体外测定的非限制性实例描述于美国专利号5,500,362(参见例如hellstrom,i.等人proc.nat'l acad.sci.usa 83:7059-7063(1986))和hellstrom,i等人,proc.nat'l acad.sci.usa 82:1499-1502(1985);5,821,337(参见bruggemann,m.等人,j.exp.med.166:1351-1361(1987))。可替代地,可使用非放射性测定方法(参见例如,用于流式细胞术的acti
tm
非放射性细胞毒性测定(celltechnology,inc.mountain view,ca);以及cytotox非放射性细胞毒性测定(promega,madison,wi)。用于此类测定的有用效应物细胞包括外周血单核细胞(pbmc)和自然杀伤(nk)细胞。可替代地或另外地,可例如在诸如在clynes等人,proc.nat’l acad.sci.usa 95:652-656(1998)中公开的动物模型中体内评定感兴趣的分子的adcc活性。也可以进行c1q结合测定以确认抗体不能结合c1q,因此缺乏cdc活性。参见例如wo 2006/029879和wo 2005/100402中的c1q和c3c结合elisa。为了评估补体活化,可以执行cdc测定(参见例如gazzano-santoro等人,j.immunol.methods 202:163(1996);cragg,m.s.等人,blood 101:1045-1052(2003);以及cragg,m.s.和m.j.glennie,blood 103:2738-2743(2004))。fcrn结合和体内清除率/半衰期测定也可以使用本领域已知的方法执行(参见例如petkova,s.b.等人,int’l.immunol.18(12):1759-1769(2006);wo 2013/120929 al)。
[0643]
具有降低的效应子功能的抗体包括具有fc区残基238、265、269、270、297、327和329中一个或多个的取代的那些(美国专利号6,737,056)。此类fc突变体包括在第265、269、270、297和327位氨基酸中两个或更多个处具有取代的fc突变体,包括所谓的“dana”fc突变体,其残基265和297被取代为丙氨酸(美国专利号7,332,581)。
[0644]
描述了具有改善的或降低的与fcr的结合的某些抗体变体。(参见例如美国专利号6,737,056;wo 2004/056312;以及shields等人,j.biol.chem.9(2):6591-6604(2001)。)
[0645]
在某些方面,抗体变体包含具有一个或多个改善adcc的氨基酸取代的fc区,例如,在fc区的298、333和/或334位的取代(残基的eu编号)。
[0646]
在某些方面,抗体变体包含具有一个或多个减少fcγr结合的氨基酸取代的fc区,例如fc区的234位和235位的取代(残基的eu编号)。一方面,取代是l234a和l235a(lala)。在某些方面,抗体变体进一步包含在衍生自人igg
1 fc区的fc区中的d265a和/或p329g。一方面,在衍生自人igg
1 fc区的fc区中,取代是l234a、l235a和p329g(lala-pg)。(参见例如wo 2012/130831)。在另一方面,在衍生自人igg
1 fc区的fc区中,取代是l234a、l235a和d265a(lala-da)。
[0647]
在一些方面,在fc区中进行导致改变(即,改善或减少)c1q结合和/或补体依赖性细胞毒性(cdc)的改变,例如,如美国专利号6,194,551、wo 99/51642以及idusogie等人.j.immunol.164:4178-4184(2000)中所描述。
[0648]
具有延长的半衰期和改善的新生儿fc受体(fcrn)结合、负责将母体igg转移至胎儿(guyer,r.l.等人,j.immunol.117:587(1976),以及kim,j.k.等人,j.immunol.24:249(1994))的抗体描述于us 2005/0014934(hinton等人)中。那些抗体包含这样的fc区,该fc区中具有改善fc区与fcrn的结合的一个或多个取代。此类fc变体包括在以下fc区残基中的
一处或多处具有取代的fc变体:238、252、254、256、265、272、286、303、305、307、311、312、317、340、356、360、362、376、378、380、382、413、424或434,例如对fc区残基434的取代(参见,例如美国专利号7,371,826;dall'acqua,w.f.等人.j.biol.chem.281(2006)23514-23524)。
[0649]
通过定点诱变已经鉴定了对小鼠fc-小鼠fcrn相互作用至关重要的fc区残基(参见例如dall’acqua,w.f.等人.j.immunol 169(2002)5171-5180)。相互作用涉及残基i253、h310、h433、n434和h435(残基的eu编号)(medesan,c.等人,eur.j.immunol.26(1996)2533;firan,m.等人,int.immunol.13(2001)993;kim,j.k.等人,eur.j.immunol.24(1994)542)。发现残基i253、h310和h435对于人fc与鼠fcrn的相互作用至关重要(kim,j.k.等人,eur.j.immunol.29(1999)2819)。对人fc-人fcrn复合物的研究已表明,残基i253、s254、h435和y436对于该相互作用至关重要(firan,m.等人,int.immunol.13(2001)993;shields,r.l.等人,j.biol.chem.276(2001)6591-6604)。在yeung,y.a.等人(j.immunol.182(2009)7667-7671)中已经报道并且检查了残基248至259和301至317和376至382和424至437的各种突变体。
[0650]
在某些方面,抗体变体包含具有一个或多个减少fcrn结合的氨基酸取代的fc区(在一些实施例中为igg1的fc区),例如,在fc区的253、和/或310和/或435位的取代(残基的eu编号)。在某些方面,抗体变体包含在位置253、310和435位具有氨基酸取代的fc区。一方面,在衍生自人igg1 fc区的fc区中,取代是i253a、h310a和h435a。参见,例如grevys,a.等人,j.immunol.194(2015)5497-5508。
[0651]
在某些方面,抗体变体包含具有一个或多个减少fcrn结合的氨基酸取代的fc区(在一些实施例中为igg1的fc区),例如,在fc区的310、和/或433和/或436位的取代(残基的eu编号)。在某些方面,抗体变体包含在位置310、433和436位具有氨基酸取代的fc区。一方面,在衍生自人igg1 fc区的fc区中,取代是h310a、h433a和y436a。(参见,例如,wo 2014/177460 al)。
[0652]
在某些方面,抗体变体包含具有一个或多个增加fcrn结合的氨基酸取代的fc区(在一些实施方案中为igg1的fc区),例如,在fc区的252、和/或254和/或256位的取代(残基的eu编号)。在某些方面,抗体变体包含在位置252、254和256位具有氨基酸取代的fc区。一方面,在衍生自人igg
1 fc区的fc区中,取代是m252y、s254t和t256e。有关fc区变体的其他实例,另外参见:duncan和winter,nature 322:738-40(1988);美国专利号5,648,260;美国专利号5,624,821;以及wo 94/29351。
[0653]
在某些方面,抗体变体包含具有一个或多个增加fcrn结合的氨基酸取代的fc区(在一些实施方案中为igg1的fc区),例如,在fc区的428、和/或434和/或436位的取代(残基的eu编号)。在某些方面,抗体变体包含在位置428、434和436位具有氨基酸取代的fc区。一方面,在衍生自人igg1 fc区的fc区中,取代是m428l、n434a和y436t。在另一方面,抗体变体包含在位置434例如n434a具有氨基酸取代的fc区。
[0654]
在某个进一步的方面,抗体变体包含具有一个或多个增加fcrn结合的氨基酸取代的fc区(在一些实施例中为igg1的fc区),例如,在307和/或434位的取代,例如t307h和/或n434h,例如t307h和n434h。
[0655]
在某些具体实施例中,抗体变体包含如本文所阐述的重链,其通过以下取代修饰:
i)m252y、s254t和t256e;ii)m428l、n434a和y436t;iii)n434a;或iv)t307h和n434h。
[0656]
例如,抗体可以包含通过由选自以下各项组成的组的取代修饰的seq id no:17的轻链和seq id no:18或263的重链:i)m252y、s254t和t256e;ii)m428l、n434a和y436t;iii)n434a以及iv)t307h和n434h。
[0657]
在另一个具体的实施例中,抗体可以包含seq id no:35的轻链和seq id no:36或264的重链,它们通过由选自以下各项组成的组的取代修饰:i)m252y、s254t和t256e;ii)m428l、n434a和y436t;iii)n434a以及iv)t307h和n434h。
[0658]
在另一个具体的实施例中,抗体可以包含seq id no:53的轻链和seq id no:54或265的重链,它们通过选自由以下各项组成的组的取代修饰:i)m252y、s254t和t256e;ii)m428l、n434a和y436t;iii)n434a以及iv)t307h和n434h。
[0659]
在另一个具体的实施例中,抗体可以包含seq id no:71的轻链和seq id no:72或266的重链,它们通过选自由以下各项组成的组的取代修饰:i)m252y、s254t和t256e;ii)m428l、n434a和y436t;iii)n434a以及iv)t307h和n434h。
[0660]
在另一个具体的实施例中,抗体可以包含seq id no:89的轻链和seq id no:90或267的重链,它们通过选自由以下各项组成的组的取代修饰:i)m252y、s254t和t256e;ii)m428l、n434a和y436t;iii)n434a以及iv)t307h和n434h。
[0661]
在另一个具体的实施例中,抗体可以包含seq id no:107的轻链和seq id no:108或268的重链,它们通过选自由以下各项组成的组的取代修饰:i)m252y、s254t和t256e;ii)m428l、n434a和y436t;iii)n434a以及iv)t307h和n434h。
[0662]
在另一个具体的实施例中,抗体可以包含seq id no:125的轻链和seq id no:126或269的重链,它们通过选自由以下各项组成的组的取代修饰:i)m252y、s254t和t256e;ii)m428l、n434a和y436t;iii)n434a以及iv)t307h和n434h。
[0663]
在另一个具体的实施例中,抗体可以包含seq id no:143的轻链和seq id no:144或270的重链,它们通过选自由以下各项组成的组的取代修饰:i)m252y、s254t和t256e;ii)m428l、n434a和y436t;iii)n434a以及iv)t307h和n434h。
[0664]
在另一个具体的实施例中,抗体可以包含seq id no:161的轻链和seq id no:162或271的重链,它们通过选自由以下各项组成的组的取代修饰:i)m252y、s254t和t256e;ii)m428l、n434a和y436t;iii)n434a以及iv)t307h和n434h。
[0665]
在另一个具体的实施例中,抗体可以包含seq id no:179的轻链和seq id no:180或272的重链,它们通过选自由以下各项组成的组的取代修饰:i)m252y、s254t和t256e;ii)m428l、n434a和y436t;iii)n434a以及iv)t307h和n434h。
[0666]
在另一个具体的实施例中,抗体可以包含seq id no:197的轻链和seq id no:198或273的重链,它们通过选自由以下各项组成的组的取代修饰:i)m252y、s254t和t256e;ii)m428l、n434a和y436t;iii)n434a以及iv)t307h和n434h。
[0667]
在另一个具体的实施例中,抗体可以包含seq id no:215的轻链和seq id no:216或274的重链,它们通过选自由以下各项组成的组的取代修饰:i)m252y、s254t和t256e;ii)m428l、n434a和y436t;iii)n434a以及iv)t307h和n434h。
[0668]
在另一个具体的实施例中,抗体可以包含seq id no:233的轻链和seq id no:234或275的重链,它们通过选自由以下各项组成的组的取代修饰:i)m252y、s254t和t256e;ii)
m428l、n434a和y436t;iii)n434a以及iv)t307h和n434h。
[0669]
在另一个具体的实施例中,抗体可以包含seq id no:251的轻链和seq id no:252或276的重链,它们通过选自由以下各项组成的组的取代修饰:i)m252y、s254t和t256e;ii)m428l、n434a和y436t;iii)n434a以及iv)t307h和n434h。
[0670]
如本文报道的抗体的重链的c末端可以是以氨基酸残基pgk结束的完整c末端。重链的c末端可以是缩短的c末端,在所述缩短的c末端中已经去除了一个或两个c末端氨基酸残基。在一个优选的方面,重链的c末端是以pg结束的缩短的c末端。在本文报道的所有方面中的一个方面,如本文所指定的包含包括c末端ch3结构域的重链的抗体,包含c末端甘氨酸-赖氨酸二肽(g446和k447,氨基酸位置的eu索引编号)。在本文报道的所有方面的一个方面中,如本文所指定的包含包括c末端ch3结构域的重链的抗体,包含c末端甘氨酸残基(g446,氨基酸位置的eu索引编号)。
[0671]
d)半胱氨酸工程化改造的抗体变体
[0672]
在某些方面,可能需要产生半胱氨酸工程化改造的抗体,例如thiomab
tm
抗体,其中抗体的一个或多个残基被半胱氨酸残基取代。在特定实施例中,取代的残基存在于抗体的可接近位点。如本文进一步描述的,通过用半胱氨酸取代那些残基,从而将反应性硫醇基团定位于抗体的可接近位点,并且可用于将抗体与其他部分(诸如药物部分或接头-药物部分)缀合,以产生免疫缀合物。半胱氨酸工程化改造的抗体可以如例如在美国专利号7,521,541、8,30,930、7,855,275、9,000,130或wo 2016040856中所述产生。
[0673]
e)抗体衍生物
[0674]
在某些方面,本文提供的抗体可被进一步修饰以包含本领域已知的并且容易获得的附加非蛋白质部分。适合于抗体衍生化的部分包括但不限于水溶性聚合物。水溶性聚合物的非限制性示例包括但不限于聚乙二醇(peg)、乙二醇/丙二醇的共聚物、羧甲基纤维素、葡聚糖、聚乙烯醇、聚乙烯吡咯烷酮、聚-1,3-二氧戊环、聚-1,3,6-三噁烷、乙烯/马来酸酐共聚物、聚氨基酸(均聚物或随机共聚物)和葡聚糖或聚(n-乙烯吡咯烷酮)聚乙二醇、丙二醇均聚物、聚环氧丙烷/环氧乙烷共聚物、聚氧乙烯化多元醇(例如甘油)、聚乙烯醇以及它们的混合物。由于其在水中的稳定性,聚乙二醇丙醛在制造中可具有优势。聚合物可具有任何分子量,并且可以具有支链或不具有支链。附接至抗体的聚合物的数目可变,并且如果附接了多于一个聚合物,那么它们可以为相同或不同的分子。通常,可基于以下考虑因素测定用于衍生化的聚合物的数目和/或类型,包括但不限于抗体待改善的特定特性或功能、抗体衍生物是否将用于限定条件下的疗法等。
[0675]
b.重组方法和组合物
[0676]
可以使用重组方法和组合物来产生抗体,例如,如在us 4,816,567中所述。对于这些方法,提供了编码抗体的一种或多种分离的核酸。
[0677]
在天然抗体或天然抗体片段的情况下,需要两种核酸,一种用于轻链或其片段,一种用于重链或其片段。此类核酸编码构成抗体的vl的氨基酸序列和/或构成抗体的vh的氨基酸序列(例如抗体的轻链和/或重链)。这些核酸可以在相同的表达载体上或不同的表达载体上。
[0678]
在具有异源二聚重链的某些双特异性抗体的情况下,需要四种核酸,一种用于第一轻链,一种用于包含第一异单体(heteromonomeric)fc区多肽的第一重链,一种用于第二
轻链,并且一种用于包含第二异单体fc区多肽的第二重链。四种核酸可包含在一种或多种核酸分子或表达载体中。此类核酸编码构成抗体的第一vl的氨基酸序列和/或构成抗体的包含第一异单体fc区的第一vh的氨基酸序列和/或构成抗体的第二vl的氨基酸序列和/或构成抗体的包含第二异单体fc区的第二vh的氨基酸序列(例如抗体的第一轻链和/或第二轻链和/或第一重链和/或第二重链)。这些核酸可以在相同的表达载体上或在不同的表达载体上,通常这些核酸位于两个或三个表达载体上,即一个载体可以包含这些核酸中的多于一种。这些双特异性抗体的示例是crossmab(参见例如schaefer,w.等人,pnas,108(2011)11187-1191)。例如,该异单体重链中的一条包含所谓的“杵突变(knob mutation)”(t366w,以及任选地s354c或y349c中的一者),并且该异单体重链中的另一条包含所谓的“臼突变(hole mutation)”(t366s、l368a和y407v,以及任选地y349c或s354c)(参见例如carter,p.等人,immunotechnol。2(1996)73),根据eu索引编号。
[0679]
在一个方面,提供了编码如在本文所报道的方法中使用的抗体的分离的核酸。
[0680]
在一方面,提供了一种制备抗s-hbs抗体的方法,其中该方法包括在适于表达抗体的条件下培养包括如上提供的编码抗体的核酸的宿主细胞,以及任选地从宿主细胞(或宿主细胞培养基)中回收抗体。
[0681]
对于抗s-hbs抗体重组生产,将编码抗体的核酸(例如,如上所述)分离并插入至一个或多个载体中以用于在宿主细胞中进一步克隆和/或表达。可以使用常规程序来容易地对此类核酸进行分离和测序(例如,通过使用能够与编码抗体的重链和轻链的基因特异性结合的寡核苷酸探针),或通过重组方法产生或通过化学合成获得此类核酸。
[0682]
用于克隆或表达编码抗体的载体的合适宿主细胞包括本文所述的原核或真核细胞。例如,可以在细菌中产生抗体,特别是当不需要糖基化和fc效应子功能时。关于在细菌中表达抗体片段和多肽,参见例如us 5,648,237、us 5,789,199和us 5,840,523(还参见charlton,k.a.,在:methods in molecular biology,第248卷,lo,b.k.c.主编,humana press,totowa,nj(2003),第245-254页中,描述抗体片段在大肠杆菌中的表达。)抗体可在表达后在可溶性级分中从细菌细胞糊中分离,并且可以进一步纯化。
[0683]
除了原核生物外,诸如丝状真菌或酵母等真核微生物也是用于编码抗体的载体的合适克隆或表达宿主,该真核微生物包括真菌和酵母菌株,其糖基化途径已经“人源化”,从而导致产生具有部分或完全人糖基化模式的抗体。参见gerngross,t.u.,nat.biotech.22(2004)1409-1414;以及li,h.等人,nat.biotech.24(2006)210-215。
[0684]
用于表达糖基化抗体的合适宿主细胞也来源于多细胞生物(无脊椎动物和脊椎动物)。无脊椎动物细胞的实例包括植物细胞和昆虫细胞。已经鉴定出了可以与昆虫细胞结合使用,特别是用于转染草地夜蛾(spodoptera frugiperda)细胞的许多杆状病毒株。
[0685]
植物细胞培养物也可用作宿主。参见例如us 5,959,177、us 6,040,498、us 6,420,548、us 7,125,978和us 6,417,429(描述了用于在转基因植物中产生抗体的plantibodiestm技术)。
[0686]
脊椎动物细胞也可用作宿主。例如,适于在悬浮液中生长的哺乳动物细胞系可能是有用的。有用的哺乳动物宿主细胞系的其他实例是由sv40转化的猴肾cv1系(cos-7);人胚肾细胞系(如在例如graham,f.l.等人,j.gen virol.36(1977)59-74中所述的293或293t细胞);小仓鼠肾细胞(bhk);小鼠塞尔托利氏细胞(例如在mather,j.p.,biol.reprod.23
(1980)243-252中描述的tm4细胞);猴肾细胞(cv1);非洲绿猴肾细胞(vero-76);人宫颈癌细胞(hela);犬肾细胞(mdck);布法罗大鼠肝细胞(brl 3a);人肺细胞(w138);人肝细胞(hep g2);小鼠乳腺肿瘤(mmt 060562);tri细胞(如例如在mather,j.p.等人,annals n.y.acad.sci.383(1982)44-68中所述);mrc 5细胞;以及fs4细胞。其他有用的哺乳动物宿主细胞系包括中国仓鼠卵巢(cho)细胞,包括dhfr-cho细胞(urlaub,g.等人,proc.natl.acad.sci.usa 77(1980)4216-4220);以及骨髓瘤细胞系,诸如y0、ns0和sp2/0。关于适用于抗体产生的某些哺乳动物宿主细胞系的综述,参见例如yazaki,p.和wu,a.m.,methods in molecular biology,第248卷,lo,b.k.c.(编辑),humana press,totowa,nj(2004),第255-268页。
[0687]
一方面,宿主细胞是真核细胞,例如中国仓鼠卵巢(cho)细胞或淋巴细胞(例如y0、ns0、sp20细胞)。
[0688]
c.测定
[0689]
可通过本技术领域中已知的各种测定,对本文所提供的抗s-hbs抗体的物理/化学特性和/或生物活性来进行鉴别、筛选或表征。
[0690]
1.结合测定和其他测定
[0691]
在一个方面,本发明的抗体的抗原结合活性通过例如elisa、流式细胞术、蛋白质印迹等已知方法进行测试。
[0692]
用于elisa的s-hbs抗原可以是颗粒形式。可通过在宿主细胞中重组表达抗原(例如s-hbs)并将抗原自组装成颗粒来提供用于elisa方案的颗粒。例如,抗原可以在酵母宿主细胞(诸如毕赤酵母)或哺乳动物细胞(诸如中国仓鼠卵巢(cho)细胞)中表达。
[0693]
elisa测定可以包括以下步骤:i)用s-hbs抗原包被elisa板ii)用bsa封闭板;iii)洗涤;iv)与连续稀释的igg抗体一起孵育;v)洗涤;vi)与山羊抗人igg-hrp抗体一起孵育;vii)用hrp显色底物使板显影;viii)测量405nm(od405nm)处的光密度。
[0694]
通过elisa测量的结合活性可以量化为曲线下面积(auc),如从od405nm-浓度曲线确定的。因此,该方法可以包括ix)从od405nm-浓度曲线确定auc。可以比较这些值以比较测试抗体与参考抗体的活性,以百分比表示。或者,ec50值可以从elisa测定中确定,作为获得od450nm的半最大值时的浓度。
[0695]
流式细胞术测定可以包括以下步骤:i)在人细胞系中表达s-sbs;ii)固定和透化细胞;iii)使细胞与igg抗体一起孵育;iv)洗涤;v)使细胞与af647缀合的山羊抗人igg抗体一起孵育;vi)洗涤并在pbs中重悬;和vii)通过流式细胞术确定结合的表达s-hbs的细胞的百分比或平均荧光强度(mfi)。
[0696]
抗体的连续稀释可用于确定流式细胞术测定中的ec50。可替代地,当测试抗体和参考抗体以相同的浓度,例如,10ug/ml或替代地以参考抗体的ec50(如在流式细胞术测定中确定的)使用时,可以比较结合的表达s-hbs的细胞的百分比或mfi获得的值,以将测试抗体的活性表示为参考抗体活性的百分比。
[0697]
在评估相对结合活性时,应使用相同的方法测试抗体。它们也可以以相同的形式进行评估,例如,都作为igg。在此类实施例中,参考抗体将具有本文提供的所述参考抗体的全长序列。包含如本文定义的vh和vl结构域(例如,包含作为参考抗体的vh和/或vl结构域的变体的vh和/或vl结构域)的测试抗体的结合活性可以以包含参考抗体的恒定结构域和
铰链序列的igg形式评估。
[0698]
示例性方案如下所述。
[0699]
方案1
[0700]
用经纯化的抗原(例如,pbs中125ng/孔)包被高结合96孔elisa板(costar,corning)过夜。洗涤后(例如,用0.05% tween 20-pbs(pbst)),用2% bsa、1mm edta-pbst(封闭溶液)封闭板2小时,洗涤,并与pbs中的连续稀释抗体一起孵育。洗涤后,通过添加山羊hrp缀合的抗人igg(例如,封闭溶液中最终浓度为0.8μg/ml,immunology jackson immunoreseach)和hrp显色底物(例如,abts溶液,euromedex)来使板显色。光密度测量在405nm(od405nm)进行。结合可以量化为来自od405nm-浓度曲线的曲线下面积(auc),并且可以比较两种抗体的auc,以百分比评估相对活性。可替代地,可以将抗体的ec50确定为获得od450nm的半最大值时的浓度。
[0701]
可以使用hydrospeed
tm
微孔板清洗机和sunrise
tm
微孔板吸光度读数器(tecan)进行实验。每个实验中可以包括阴性对照抗体mgo53和合适的阳性对照(诸如hb1)(kucinskaite-kodze等人,2016)。
[0702]
方案2
[0703]
在使用流式细胞术来测量结合活性的示例性方案中,用编码s-hbs的载体(每106个细胞0.65μg质粒dna),例如,使用前面描述的pei沉淀法(lorin和mouquet,2015)转染人细胞系(例如freestyle
tm 293-f)。转染后48小时,将转染和未转染的对照细胞固定和透化,例如使用cytofix/cytoperm
tm
溶液试剂盒(bd biosciences),然后在4℃使0.5x106细胞与igg抗体一起孵育45分钟(例如,在perm/wash
tm
溶液中;bd biosciences)。在一个实施例中,测试抗体和参考抗体以10ug/ml使用。在另一个实施例中,测试抗体和参考抗体可以以如在流式细胞术测定中所确定的参考抗体的ec50使用。洗涤后,使细胞与af647缀合的山羊抗人igg抗体(1:1000稀释度;thermo fisher scientific)在4℃下一起孵育20分钟,洗涤并重悬于pbs中。通过流式细胞术评估结合的表达s-hbs的细胞的百分比和/或信号的平均荧光强度(mfi),并比较两种抗体获得的值,以百分比评估相对值。可以使用cytoflex流式细胞仪(beckman coulter)获取数据,并使用flowjo软件(v10.3;flowjo llc)进行分析。
[0704]
方案3
[0705]
在使用流式细胞术评估ec50的示例性方案中,用编码ss-hbs的载体(每106个细胞0.65μg质粒dna),例如,使用前面描述的pei沉淀法(lorin和mouquet,2015)转染人细胞系(例如freestyle
tm 293-f)。转染后48小时,例如使用cytofix/cytoperm
tm
溶液试剂盒(bd biosciences)将转染和未转染的对照细胞固定和透化,然后在4℃使0.5x106细胞与pbs中的连续稀释的igg抗体一起孵育45分钟(例如在perm/wash
tm
溶液中;bd biosciences)。洗涤后,使细胞与af647缀合的山羊抗人igg抗体(1:1000稀释度;thermo fisher scientific)在4℃下一起孵育20分钟,洗涤并重悬于pbs中。通过流式细胞术评估结合的表达s-hbs的细胞的百分比或信号的平均荧光强度(mfi),并将ec50确定为获得结合细胞的半最大百分比或mfi时的浓度。
[0706]
另一方面,竞争测定可用于鉴定与选自由以下各项组成的组的用于结合s-hbs的参考抗体竞争的抗体:bc1.187、bv4.115、bc8.159、bv6.172、bc1.229、bc8.111、bc1.128、bc3.106、bc1.180、bv4.104,bc8.104、bc4.204、bc1.263和bv4.105。在某些方面,这种竞争
性抗体与选自由以下各项组成的组的参考抗体结合的相同表位(例如,线性表位或构象表位)结合:bc1.187、bv4.115、bc8.159、bv6.172、bc1.229、bc8.111、bc1.128、bc3.106、bc1.180、bv4.104、bc8.104、bc4.204、bc1.263和bv4.105。用于定位抗体与之结合的表位的详细示例性方法提供于:morris(1996),“epitope mapping protocols”,收录于methods in molecular biology第66卷(humana press,totowa,nj)。
[0707]
在示例性竞争测定中,将固定的s-hbs在包含与s-hbs结合的第一标记抗体(例如,选自由以下各项组成的组的参考抗体:bc1.187、bv4.115、bc8.159、bv6.172、bc1.229、bc8.111、bc1.128、bc3.106、bc1.180、bv4.104、bc8.104、bc4.204、bc1.263和bv4.105)和正在测试其与第一抗体竞争结合s-hbs的能力的第二未标记抗体的溶液中孵育。该第二抗体可存在于杂交瘤上清液中。作为对照,将固定化s-hbs在包含第一标记抗体而非包含第二未标记抗体的溶液中孵育。在容许第一抗体与s-hbs结合的条件下孵育之后,去除过量未结合的抗体,并且测量与固定化s-hbs缔合的标记的量。如果相对于对照样品,测试样品中与固定化的s-hbs缔合的标记的量大幅减少,则表明该第二抗体在与该第一抗体竞争以结合到s-hbs。参见harlow和lane(1988)antibodies:a laboratory manual第14章(cold spring harbor laboratory,cold spring harbor,ny)。
[0708]
另一个示例性竞争测定是竞争elisa。纯化抗体(例如,选自由以下各项组成的组的参考抗体:bc1.187、bv4.115、bc8.159、bv6.172、bc1.229、bc8.111、bc1.128、bc3.106、bc1.180、bv4.104、bc8.104、bc4.204、bc1.263和bv4.105)使用ez-link sulfo-nhs-biotin试剂盒(thermo fisher scientific)进行生物素化。将抗原或抗原颗粒(例如,rs-hbs)包被的板封闭、洗涤、与生物素化抗体(浓度为0.33nm)在1:2连续稀释的pbs中的抗体竞争剂溶液(igg浓度范围为0.83至106.7nm)中孵育2小时,并使用hrp缀合的链霉亲和素使其显色。使用hydrospeed
tm
微孔板清洗机和sunrise
tm
微孔板吸光度读数器(tecan)进行实验,在405nm(od405nm)处进行光密度测量。
[0709]
2.活性测定
[0710]
在一个方面,提供用于鉴定其具有生物活性的抗s-hbs抗体的测定。生物活性可以包括例如体外或体内的中和活性和/或减少体内病毒血症的能力。还提供了在体内和/或体外具有此类生物活性的抗体。
[0711]
体外中和活性可以是抑制hbv对原代人肝细胞或人肝细胞系的感染。这可以确定为与不存在抗体相比上清液s-hbs的减少。体内中和活性可以确定为感染hbv的循环s-hbs动物(例如小鼠或人)的减少。
[0712]
病毒性病毒血症的减少可以确定为hbv感染动物(例如小鼠或人)的血清中hbv dna的减少。
[0713]
例如,抗体可具有≤50μg/ml、≤10μg/ml、≤1μg/ml、≤500ng/ml、≤100ng/ml、≤50ng/ml、≤10ng/ml、≤1ng/ml、≤500pg/ml、≤100pg/ml、≤50pg/ml、≤10pg/ml或≤1pg/ml的用于体外抑制特定基因型(例如基因型d)的hbv感染性的ic50值。在一些实施例中,优选的抗体可以具有≤50ng/ml或≤10ng/ml的ic50。优选抗体可以具有≤1ng/ml、≤500pg/ml或在一些实施例中≤100pg/ml、≤50pg/ml或≤10pg/ml的ic50。在一些实施例中,中和抗体可以具有≤1pg/ml,任选地≤0.1pg/ml的ic50值。
[0714]
在另一个实施例中,抗体可以具有针对特定基因型例如基因型d的ic50值,其比参
考抗体针对相同基因型的ic50值高不超过50、10、9、8、7、6、5、4、3或2倍或小于或等于参考抗体针对相同基因型的ic50值,其中参考抗体选自由以下项组成的组:bc1.187、bv4.115、bc8.159、bv6.172、bc1.229、bc8.111、bc1.128、bc3.106、bc1.180、bv4.104、bc8.104、bc4.204、bc1.263和bv4.105(当在同一体外测定中评估时)。
[0715]
在另一个实施例中,当使用同一测定(例如,如本文所述的体内测定)评估时,抗体可以具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体对特定hbv基因型的中和活性。
[0716]
在一些实施例中,本发明的抗体具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体对hbv基因型a、b、c和/或d病毒的体内中和活性,其中参考抗体选自由以下项组成的组:bc1.187、bv4.115、bc8.159、bv6.172、bc1.229、bc8.111、bc1.128、bc3.106、bc1.180、bv4.104、bc8.104、bc4.204、bc1.263和bv4.105。.在一些实施例中,本发明的抗体具有或保留至少50%、60%、70%、75%、80%、85%、90%、95%或100%的参考抗体针对hbv基因型a、b、c和/或d病毒的病毒血症抑制活性,其中参考抗体选自由以下项组成的组:bc1.187、bv4.115、bc8.159、bv6.172、bc1.229、bc8.111、bc1.128、bc3.106、bc1.180、bv4.104、bc8.104、bc4.204、bc1.263和bv4.105。
[0717]
在某些方面中,测试本发明的抗体的此类生物活性。
[0718]
下面将示例性的体外中和测定描述为方案4。下面将示例性的体内中和测定描述为方案5。方案6中描述了病毒血症抑制的示例性测定。
[0719]
在评估相对活性时,应使用相同的方法测试抗体。两种抗体都可以被评估为igg:在这样的实施例中,参考抗体将具有本文提供的所述参考抗体的全长序列。包含如本文定义的vh和vl结构域(例如,包含作为参考抗体的vh和/或vl结构域的变体的vh和/或vl结构域)的测试抗体的结合活性可以以包含参考抗体的恒定结构域和铰链序列的igg形式评估。
[0720]
方案4(用于评估体外中和的ic50值)
[0721]
在示例性方案中,通过在室温下使hbv病毒粒子(moi 20-30)与连续稀释的测试抗体孵育1小时来评估hbv抗体的体外中和活性。然后将hbv抗体混合物添加到96孔板中的肝细胞中,最终浓度为4% peg 8000(sigma)。受感染的细胞在37℃下孵育20小时,然后用pbs洗涤4次以去除hbv接种物并重新填充完全培养基。感染后6天,例如,根据制造商的说明使用s-hbs clia试剂盒(autobio)量化上清液中的s-hbs抗原含量。中和活性被确定为与不存在抗体的对照相比上清液s-hbs的减少。ic50值是半数最大抑制浓度,测量感染性的抑制。
[0722]
细胞可以是原代人肝细胞或人肝细胞系。可用于方案的示例性肝细胞是可从phoenixbio(hiroshima,japan)获得的、通过胶原酶灌注法(tateno等人,2015)从具有人源化肝脏的嵌合upa/scid小鼠中分离的原代人肝细胞(phh)。其他示例性肝细胞是可从biopredic international(saint-gregoire,france)获得的heparg细胞系。
[0723]
方案5(用于评估体内中和活性)
[0724]
在用于评估体内中和活性的示例性方案中,在用0.5mg的测试抗体静脉内治疗一次的经aav-hbv转导的小鼠中监测循环血液s-hbs水平。通过elisa测量循环血液s-hbs。中和活性被确定为在最低点处循环血液s-hbs量的减少(最大减少)。
[0725]
方案6(用于评估体内病毒血症抑制)
[0726]
选择携带高水平的循环s-hbsag(》104iu/ml)的aav-hbv小鼠作为受试者。以20mg/
kg单次静脉内(i.v.)注射测试抗体。使用qiaamp blood mini试剂盒(qiagen,germany)从小鼠血清中纯化hbv dna,并如前所述通过定量pcr进行定量(cougot等人,2012)。通过评估最低点(最大减少)处的hbv dna的量来确定病毒血症抑制活性。
[0727]
d.用于诊断和检测的方法和组合物
[0728]
在某些方面,本文提供的抗s-hbs抗体中的任一种可用于检测生物样品中s-hbs的存在。如本文所用的术语“检测”涵盖定量或定性检测。在某些方面,生物样品包括血液、血浆或血清样品。
[0729]
在一个方面,提供了用于诊断或检测方法中的抗s-hbs抗体。在另一方面,提供了检测生物样品中s-hbs的存在的方法。在某些方面中,该方法包括在允许抗s-hbs抗体和s-hbs两者结合的条件下使生物样品与抗s-hbs抗体接触,以及检测是否在抗s-hbs抗体与s-hbs之间形成了复合物。此类方法可以是体外或体内方法。在一个方面中,抗s-hbs抗体用于选择能够用抗s-hbs抗体进行治疗的受试者,例如其中s-hbs是用于选择患者的生物标志物。
[0730]
可以使用本发明的抗体诊断的示例性疾患包括乙型肝炎,例如慢性乙型肝炎。
[0731]
在某些方面中,提供了标记的抗s-hbs抗体。标记包括但不限于直接检测的标记或部分(诸如荧光标记、发色标记、电子致密标记、化学发光标记,以及放射性标记),以及间接(例如通过酶促反应或分子相互作用)检测的部分(诸如酶或配体)。示例性标记包括但不限于放射性同位素
32
p、
14
c、
125
i、3h和
131
i;荧光团,诸如稀土螯合物或荧光素及其衍生物、罗丹明及其衍生物、丹酰、伞形酮;荧光素酶(luceriferase),例如萤火虫荧光素酶和细菌荧光素酶(美国专利号4,737,456);虫荧光素、2,3-二氢二氮杂萘二酮、辣根过氧化物酶(hrp)、碱性磷酸酶、β-半乳糖苷酶、葡糖淀粉酶、溶菌酶;糖氧化酶,例如葡萄糖氧化酶、半乳糖氧化酶和葡萄糖-6-磷酸脱氢酶;杂环氧化酶,诸如尿酸氧化酶和黄嘌呤氧化酶;与采用过氧化氢来氧化染料前体的酶(诸如hrp、乳过氧化物酶,或微过氧化物酶)偶联;生物素/抗生物素蛋白、纺丝标记、噬菌体标记、稳定自由基,等等。
[0732]
e.药物组合物
[0733]
在其他方面,提供了包含本文提供的任一种抗体的药物组合物,其例如用于以下任一种治疗方法中。在一个方面,药物组合物包含本文所提供的抗体中的任一者,以及药用载体。在另一方面,药物组合物包含任一种本文提供的抗体和例如如下所述的至少一种另外的治疗剂。
[0734]
本文所述的抗s-hbs抗体的药物组合物通过将此类具有所需纯度的抗体与一种或多种任选的药用载体混合(remington's pharmaceutical sciences第16版,osol,a.ed.(1980)),制成冻干组合物或水溶液的形式。药用载体在所用的剂量和浓度下对受治疗者一般无毒,并且包括但不限于:缓冲剂,诸如组氨酸、磷酸盐、柠檬酸盐、乙酸盐和其他有机酸;抗氧化剂,包括抗坏血酸和蛋氨酸;防腐剂(诸如十八烷基二甲基苄基氯化铵;氯化六甲双铵;苯扎氯铵;苄索氯铵;苯酚、丁醇或苄醇;对羟基苯甲酸烷基酯,诸如对羟基苯甲酸甲酯或对羟基苯甲酸丙酯;儿茶酚;间苯二酚;环己醇;3-戊醇;间甲酚);低分子量(少于约10个残基)多肽;蛋白质,诸如血清白蛋白、明胶或免疫球蛋白;亲水性聚合物,诸如聚乙烯吡咯烷酮;氨基酸,诸如甘氨酸、谷氨酰胺、天冬酰胺、组氨酸、精氨酸或赖氨酸;单糖、二糖和其他碳水化合物,包括葡萄糖、甘露糖或糊精;螯合剂,诸如edta;糖,诸如蔗糖、甘露醇、海藻
糖或山梨糖醇;成盐抗衡离子,诸如钠;金属络合物(例如锌蛋白络合物);和/或非离子表面活性剂,诸如聚乙二醇(peg)。本文的示例性药用载体还包括间质药物分散剂,诸如可溶中性活性透明质酸酶糖蛋白(shasegp),例如人可溶性ph-20透明质酸酶糖蛋白,诸如rhuph20(halozyme,inc.)。某些示例性shasegp和使用方法(包括rhuph20)描述于美国专利公布号2005/0260186和2006/0104968中。在一个方面中,将shasegp与一种或多种另外的糖胺聚糖酶(诸如软骨素酶)组合。
[0735]
示例性的冻干抗体组合物描述于美国专利号6,267,958中。水性抗体组合物包括在美国专利号6,171,586和wo 2006/044908中描述的那些,后者中的组合物包含组氨酸-乙酸盐缓冲剂。
[0736]
本文的药物组合物还可以含有多于一种对于所治疗的特定适应症期望的活性成分,优选地是具有不会对彼此造成不利影响的互补活性的那些活性成分。例如,可能需要进一步提供一种或多种选自以下各项的另外的治疗剂:抗病毒药物,诸如核苷酸类似物逆转录酶抑制剂或核苷类似物,例如恩替卡韦、富马酸替诺福韦二吡呋酯、替诺福韦艾拉酚胺、拉米夫定、阿德福韦或替比夫定;靶向hbv序列的sirna;旨在恢复宿主先天性和适应性免疫应答的药剂,例如,infα或聚乙二醇化的ifnα;治疗性疫苗,诸如gs-4774、abx-203、tg-1050、ino-1800;tlr激动剂,诸如抗tlr抗体、脂肽、脂多糖、poly i:c(聚肌胞苷酸)、poly iclc(poly i:c-聚-l-赖氨酸)、咪喹莫特、gsk2245035、gsk2445053、ro6864018、ro7020531、gs-9620、gs-9688、852a(合成咪唑喹啉模拟病毒ssrna)、瑞喹莫德、vtx-2337(小分子选择性tlr8激动剂模拟病毒ssrna)、bacillus calmette-gu
é
rin(bcg)、mpl(单磷酰脂质a)和/或cpg寡核苷酸;和/或检查点抑制剂,诸如抗体(例如拮抗剂或阻断抗体),例如靶向ctla4(例如伊匹木单抗、曲美木单抗)、pd-1(例如纳武单抗、匹利组单抗)、pd-l1(例如mpdl3280a、medi4736、msb0010718c)、tim-3、2b4、a2ar、b7-h3、b7-h4、btla、ido、kir、lag3、nox2、vista、siglec7或siglec9(fanning等人,2019;gehring和protzer,2019;maini和burton,2019)。此类活性成分适当地以对预期目的有效的量组合存在。
[0737]
活性成分可以包埋在例如通过凝聚技术或通过界面聚合而制备的微胶囊(例如分别为羟甲基纤维素或明胶微胶囊和聚(甲基丙烯酸甲酯)微胶囊)中;包埋在胶体药物递送系统(例如,脂质体、白蛋白微球、微乳液、纳米粒子和纳米胶囊)中;或包埋在粗乳液中。此类技术公开于remington's pharmaceutical sciences第16版,osol,a.编(1980)中。
[0738]
可以制备用于缓释的药物组合物。缓释制剂的合适实例包括含有抗体的固态疏水聚合物的半透性基质,这些基质是例如膜或微胶囊等成型制品的形式。
[0739]
用于体内施用的药物组合物通常是无菌的。例如,无菌可以通过无菌过滤膜过滤而容易地实现。
[0740]
f.治疗方法和施用途径
[0741]
本文提供的任何s-hbs抗体可用于治疗方法。
[0742]
在一个方面,提供一种用作药物的抗s-hbs抗体。在其他方面,提供了用于治疗乙型肝炎的抗s-hbs抗体,例如用于治疗慢性乙型肝炎病毒感染。在某些方面中,提供一种用于治疗方法中的抗s-hbs抗体。在某些方面,本发明提供了抗s-hbs抗体以用于治疗患有乙型肝炎例如慢性乙型肝炎病毒感染的个体的方法中,该方法包括向该个体施用有效量的抗s-hbs抗体。在一个这样的方面,例如如下所描述的,该方法进一步包括向个体施用有效量
的至少一种另外的治疗剂(例如,一种、两种、三种、四种、五种或六种另外的治疗剂)。在另一方面,本发明提供了用于降低乙型肝炎病毒载量、降低可检测的血清hbsag或提供hbv功能性治愈的抗s-hbs抗体。在某些方面,本发明提供了一种抗s-hbs抗体,用于在个体中降低乙型肝炎病毒载量、降低可检测的血清hbsag或提供hbv功能性治愈的方法,包括向个体施用有效量的抗s-hbs抗体以降低病毒载量、降低可检测的血清hbsag或提供hbv功能性治愈。hbv功能性治愈是指乙型肝炎表面抗原(hbsag)的血清清除,即血清中没有可检测到的hbsag。根据上述方面中的任一者的“个体”优选地是人。
[0743]
在另一方面,本发明提供抗s-hbs抗体在制造或制备药物中的用途。在一个方面,该药物用于治疗乙型肝炎,例如慢性乙型肝炎。在进一步的方面,该药物用于治疗乙型肝炎,例如慢性乙型肝炎的方法中,包括向患有所述病况的个体施用有效量的药物。在一个这样的方面,例如如下所描述的,该方法进一步包括向个体施用有效量的至少一种另外的治疗剂。在另一方面,该药物用于降低乙型肝炎病毒载量、降低可检测的血清hbsag或提供hbv功能性治愈。在另一方面,该药物用于在个体中降低乙型肝炎病毒载量、降低可检测的血清hbsag或提供hbv功能性治愈的方法,包括向个体施用有效量的药物以降低病毒载量、降低可检测血清hbsag或提供hbv功能性治愈。根据上述方面中的任一方面的“个体”可以是人。
[0744]
在另一方面,本发明提供了一种治疗乙型肝炎,例如慢性乙型肝炎的方法。在一个方面,该方法包括向患有乙型肝炎,例如慢性乙型肝炎的个体施用有效量的抗s-hbs抗体。在一个这样的方面,如下所描述的,该方法进一步包括向个体施用有效量的至少一种另外的治疗剂。
[0745]
根据上述方面中的任一方面的“个体”可以是人。
[0746]
在另一方面,本发明提供一种用于降低乙型肝炎病毒载量、降低可检测的血清hbsag或提供hbv功能性治愈的方法。一方面,该方法包括向个体施用有效量的抗s-hbs抗体以降低病毒载量/降低可检测的血清hbsag/提供功能性治愈。在一个方面,“个体”是人。
[0747]
在另一方面,本发明提供了包含本文提供的任一种抗s-hbs抗体的药物组合物,其例如用于上述任一种治疗方法中。在一个方面中,药物组合物包含本文提供的任一种抗s-hbs抗体以及药用载体。在另一方面,药物组合物包含本文提供的任一种抗s-hbs抗体和例如如下所述的至少一种另外的治疗剂。
[0748]
本发明的抗体可以单独施用或用于组合疗法。例如,该组合疗法包括施用本发明的抗体并且施用至少一种另外的治疗剂(例如,一种、两种、三种、四种、五种或六种另外的治疗剂)。在某些方面,联合疗法包括施用本发明的抗体和施用至少一种另外的治疗剂,诸如:抗病毒药物,诸如核苷酸类似物逆转录酶抑制剂或核苷类似物,例如,恩替卡韦、富马酸替诺福韦二吡呋酯、替诺福韦艾拉酚胺、拉米夫定、阿德福韦或替比夫定;靶向hbv序列的sirna;旨在恢复宿主先天性和适应性免疫应答的药剂,例如,infα或聚乙二醇化的ifnα;治疗性疫苗,诸如gs-4774、abx-203、tg-1050、ino-1800;tlr激动剂,诸如抗tlr抗体、脂肽、脂多糖、poly i:c(聚肌胞苷酸)、poly iclc(poly i:c-聚-l-赖氨酸)、咪喹莫特、gsk2245035、gsk2445053、ro6864018、ro7020531、gs-9620、gs-9688、852a(合成咪唑喹啉模拟病毒ssrna)、瑞喹莫德、vtx-2337(小分子选择性tlr8激动剂模拟病毒ssrna)、bacillus calmette-gu
é
rin(bcg)、mpl(单磷酰脂质a)和/或cpg寡核苷酸;和/或检查点抑制剂,诸如抗体(例如拮抗剂或阻断抗体),例如靶向ctla4(例如伊匹木单抗、曲美木单抗)、pd-1(例如
纳武单抗、匹利组单抗)、pd-l1(例如mpdl3280a、medi4736、msb0010718c)、tim-3、2b4、a2ar、b7-h3、b7-h4、btla、ido、kir、lag3、nox2、vista、siglec7或siglec9(fanning等人,2019;gehring和protzer,2019;maini和burton,2019)。
[0749]
上述此类组合疗法涵盖组合施用(其中两种或更多种治疗剂包括在相同或单独的药物组合物中)和单独施用,在单独施用的情况下,本发明的抗体的施用可以在施用另外的治疗剂或药剂之前、同时和/或之后进行。在一个方面中,抗s-hbs抗体的施用和另外的治疗剂的施用在彼此相距约一个月内,或在约一周、两周或三周内,或在约一天、二天、三天、四天、五天或六天之内进行。在一个方面,在治疗的第1天将抗体和另外的治疗剂施用于患者。
[0750]
本发明的抗体(和任何另外的治疗剂)可以通过任何合适的方式施用,包括肠胃外、肺内和鼻内,并且如果需要的话用于局部治疗、病灶内施用。肠胃外输注包括肌内、静脉内、动脉内、腹膜内或皮下施用。给药可以通过任何合适的途径进行,例如通过注射,诸如静脉内或皮下注射,部分取决于施用是短暂的还是长期的。本文考虑了各种给药时间安排,包括但不限于在各个时间点处的单次或多次施用、推注施用,以及脉冲输注。
[0751]
本发明的抗体将以符合良好医学实践的方式配制、给药和施用。在这种情况下需要考虑的因素包括所治疗的特定疾患、所治疗的特定哺乳动物、个体患者的临床病症、疾患的原因、药剂的递送部位、施用方法、施用的时间安排,以及执业医师已知的其他因素。该抗体不是必须的,而是任选地与一种或多种目前用于预防或治疗所讨论的疾患的制剂共同配制。这些其他制剂的有效量取决于药物组合物中存在的抗体的量、疾患或治疗的类型以及上面讨论的其他因素。这些通常以与本文所述相同的剂量和施用途径使用,或以本文所述剂量的约1%至99%使用,或以任何剂量且通过经验/临床上确定为合适的任何途径使用。
[0752]
为了预防或治疗疾病,本发明的抗体的适当剂量(当单独使用或与一种或多种其他另外治疗剂组合使用时)将取决于待治疗的疾病类型、抗体的类型、疾病的严重程度和病程、施用分子用于预防还是治疗目的、患者的病史和对抗体的应答以及主治医师的酌处权。抗体适当地一次或在一系列治疗中施用于患者。取决于疾病的类型和严重性,约1μg/kg至15mg/kg(例如0.1mg/kg
‑‑
10mg/kg)的抗体可以是例如通过一次或多次单独施用或通过连续输注而施用于患者的初始候选剂量。取决于上述因素,一种典型的日剂量的范围可以为约1μg/kg至100mg/kg或更多。对于数天或更长时间的重复施用,取决于病症,治疗通常会持续直至发生期望的疾病症状抑制。抗体的一种示例性剂量的范围为约0.05mg/kg至约10mg/kg。因此,可以向患者施用约0.5mg/kg、2.0mg/kg、4.0mg/kg或10mg/kg(或它们的任何组合)的一种或多种剂量。此类剂量可以间歇施用,例如每周或每三周施用(例如,使得患者接受约两次至约二十次,或例如约六次剂量的抗体)。可施用初始更高负荷剂量,然后施用一次或多次更低剂量。这种疗法的进展易于通过常规的技术和测定法来监测。
[0753]
g.制品
[0754]
在本发明的另一个方面中,提供了一种制品,其含有可用于治疗、预防和/或诊断上述病症的物质。该制品包括容器和在该容器上或与该容器相关的标签或包装说明书。合适的容器包括例如瓶子、小瓶、注射器、iv溶液袋等。该容器可以由诸如玻璃或塑料等多种材料形成。该容器容纳组合物,该组合物本身或与另一种组合物组合能够有效地治疗、预防和/或诊断病症,并且该容器可以具有无菌进入口(例如,该容器可以是静脉内溶液袋或具有可由皮下注射针刺穿的塞子的小瓶)。组合物中的至少一种活性剂是本发明的抗体。标签
或包装插页指示该组合物用于治疗所选择的病症。此外,该制品可包括(a)第一容器,该第一容器中含有包含本发明的抗体的组合物;以及(b)第二容器,该第二容器中含有包含另外的细胞毒性剂或其他治疗剂组合物。本发明该方面中的制品还可包含包装插页,该包装插页指示该组合物可用于治疗特定病症。可替代地或另外地,该制品还可包括第二(或第三)容器,该第二(或第三)容器包括药用缓冲液,诸如抑菌性注射用水(bwfi)、磷酸盐缓冲盐水、林格氏溶液和葡萄糖溶液。该制品可以还包括从商业和用户角度来看所需的其他物质,包括其他缓冲剂、稀释剂、过滤器、针头和注射器。
[0755]
序列
[0756]
下表括号中显示的氨基酸可以存在或不存在。
[0757]
[0758]
[0759]
[0760]
[0761]
[0762]
[0763]
[0764]
[0765]
[0766]
[0767]
[0768]
[0769]
[0770]
[0771]
[0772][0773]
[0774]
[0775]
[0776]
[0777]
[0778]
[0779][0780]
iv.实例
[0781]
以下是本发明的方法和组合物的实例。应当理解,在给出以上提供的一般描述的情况下,可以实践各种其他实施方案。
[0782]
材料和方法
[0783]
人体样品
[0784]
hbv疫苗接种者和hbv血清转换者的血液样品获自icareb生物库平台(巴斯德研究所)的健康供体队列,符合法国国家药品安全局(ansm)于2012年5月24日批准的cosimmgen协议,以及人身保护委员会(cpp)于2014年1月17日批准的协议。图6总结了供体的主要临床生物学特征。所有来自hbv疫苗接种者和血清转换者的样品均作为临床研究协议rapivib的一部分获得,该协议符合并在获得所有法国立法和监管机构的伦理批准后进行。rapivib协议于2015年7月30日获得巴斯德研究所的临床研究委员会的批准(#2014-058)、于2015年4月29日获得ansm的批准(#150457b-41)、于2015年6月10日获得cpp ile-de-france iii的
批准(#2015-100220-49/3267)。该协议遵循国家信息与自由委员会(cnil)的mr-001参考方法。所有供体都书面同意参与这项研究,并使用受试者编码在伪匿名条件下收集数据。使用plaque plus(ge healthcare)从供体血液中分离外周血单个核细胞(pbmc),并使用蛋白g琼脂糖凝胶4快速流动珠(ge healthcare,chicago,il)通过批次/重力流亲和层析纯化血浆或血清igg抗体。
[0785]
抗原和抗体对照
[0786]
从感染的受试者中纯化的天然s-hbsag和重组s-hbsag颗粒(ayw亚型)由roche制备和生物素化。重组hbsag颗粒(ayw)在中国仓鼠卵巢细胞中产生(aventis pasteur,val de reuil,france)(michel et al.,1984)。adw亚型hbsag颗粒(hbv基因型a)在酵母毕赤酵母表达系统中产生,并在基因工程和生物技术中心生产设施(cigb,havana,cuba;j.aguilar博士的善意馈赠)中纯化(《95%纯度)。通过使用clc main workbench 7软件(v7.5.3,qiagen aarhus a/s)对单个hbv基因型序列(a,n=205;b,n=495;c,n=1322;d,n=382;e,n=314;f,n=271;g,n=6;h,n=40;i,n=7)进行多重氨基酸比对,构建共有基因型特异性s-hbs片段。使用anza 5和11限制酶(thermo fisher scientific)将编码共有s-hbs、g3s接头、10xhis-和avi-标签的密码子优化的核苷酸片段克隆到pcdna
tm
3.1/zeo
(+)
表达载体(thermo fisher scientific)中。对于跨膜(tm)结构域缺失的s-hbs蛋白(δtm-s-hbs)的生产,生成相同的构建体,但其中s-hbs dna片段缺少tm1、tm3、tm4结构域,并且tm2被替换为(g3s)5接头。合成和脱盐了二硫键桥接s-hbs/d 122-137(rtctttaqgtsmypsc)和139-148(ctkpsdgnct)环肽和包括整个consd s-hbs区域但具有高疏水性的一个跨膜结构域2肽(iflfilllclif)除外的3个氨基酸重叠的12聚体肽(n=24)(genscript hk limited)。非hbv抗体mgo53(wardemann和nussenzweig,2007)用作同种型对照。作为阳性对照,中和鼠hb1抗体对s-hbsag的“a”决定簇的119-gpcrtct-125线性表位具有特异性(kucinskaite-kodze等人,2016),以具有人fc的嵌合重组igg1的形式使用下面描述的表达克隆系统生产。鼠抗前s2抗体1f6(kuttner等人,1999)以嵌合人fab片段的形式生产,用作下文描述的丙氨酸扫描图中的捕获分子。
[0787]
单b细胞facs分选和抗体的表达克隆
[0788]
通过cd19 macs(miltenyi biotec)从供体的pbmc中分离外周血人b细胞,并用live/dead可固定死细胞染色试剂盒(thermo fisher scientific)将其染色。然后使纯化的b细胞在4℃下与生物素化的重组或天然s-hbs抗原一起孵育30分钟,用1% fbs-pbs(facs缓冲液)洗涤,并在4℃下与小鼠抗人抗体(cd19 a700(hib19)、igg bv786(g18-145)、cd27 pe-cf594(m-t271)(bd biosciences)、iga fitc(is11-8e10,miltenyi biotec))和链霉亲和素r-pe缀合物(thermo fisher scientific)的混合物一起孵育30分钟。洗涤染色的细胞并重新悬浮在1mm edta facs缓冲液中。使用如前所述的facs aria iii分选器(becton dickinson,franklin lakes,nj)将单一s-hbs
+
cd19
+
igg
+
b细胞分选至96孔pcr板中(tiller等人,2008)。如前所述,使用superscript iv逆转录酶(thermo fisher scientific)合成单细胞cdna,然后对igh、igκ和igλ基因进行巢式pcr扩增,并对ig基因特征进行序列分析(tiller等人,2008)。对于所选抗体的种系(gl)的还原,如前所述,通过将突变的v
h-(dh)-jh和v
l-j
l
基因片段替换为gl对应物来构建序列(mouquet等人,2012)。如前所述,将纯化的消化pcr产物克隆到人igγ1-、igκ-或igλ-表达载体(基因库号分别为
lt615368.1、lt615369.1和lt615370.1)(tiller等人,2008)中。通过将编码人igγ1/igκ恒定区的dna序列替换为小鼠igγ2-和igκ(合成dna片段,geneart,thermo fisher scientific)的dna序列,从原始igg1表达载体(tiller等人,2008)生成鼠igγ2和igκ表达载体,然后用于克隆嵌合mgo53和bc1.187抗体。重组抗体是通过使用如前所述的pei沉淀法(lorin和mouquet,2015)对freestyle
tm 293-f悬浮细胞(thermo fisher scientific)进行瞬时共转染产生的。通过蛋白g亲和层析(protein g4fast flow,ge healthcare,chicago,il)纯化重组人igg抗体。针对pbs透析纯化的抗体。体内输注的制剂经过微过滤(-cl装置-0.1μm pvdf膜,merck-millipore,darmstadt,德国),并使用toxinsensor
tm
显色lal内毒素检测试剂盒(genscript)检查内毒素水平。
[0789]
elisa
[0790]
如前所述进行elisa(planchais等人,2019)。简而言之,用纯化的rs-hbs和ns-hbs(pbs中125ng/孔)包被高结合96孔elisa板(costar,corning)过夜。用0.05% tween 20-pbs(pbst)洗涤后,将板用2% bsa、1mm edta-pbst(封闭溶液)封闭2小时,洗涤,并与pbs中的连续稀释的纯化血清igg和重组单克隆抗体一起孵育。对于夹心elisa,用纯化的igg抗体(pbs中250ng/孔)包被板过夜,并在与pbs中的生物素化rs-hbs(pbs中100ng/孔)一起孵育之前如上所述进行处理。洗涤后,通过添加山羊hrp缀合的抗人igg或hrp缀合的链霉亲和素(封闭溶液中的最终浓度为0.8μg/ml,immunology jackson immunoreseach)和hrp显色底物(abts溶液,euromedex)使板显色。对于竞争elisa,使用ez-link sulfo-nhs-biotin试剂盒(thermo fisher scientific)对纯化抗体进行生物素化。将rs-hbs包被的板封闭、洗涤、与生物素化抗体(浓度为0.33nm)在1:2连续稀释的pbs中的抗体竞争剂溶液(igg浓度范围为0.83至106.7nm)中孵育2小时,并使用hrp缀合的链霉亲和素使其显色。使用hydrospeed
tm
微孔板清洗机和sunrise
tm
微孔板吸光度读数器(tecan)进行实验,在405nm(od
405nm
)处进行光密度测量。使用与先前描述的相同程序测试抗s-hbs抗体与环状和重叠线性肽的结合(mouquet等人,2006)。在至少两个独立实验中对所有抗体进行两次重复或三次重复测试,其中包括mgo53阴性和适当的阳性对照。
[0791]
丙氨酸扫描图
[0792]
如前所述(salisse和sureau,2009),使用fugene 6试剂(roche)通过huh-7细胞与psvld3和pt7hb2.7质粒的共转染产生突变型hbv包膜蛋白。用纯化的人s-hbs抗体(pbs中0.5μg/孔)包被高结合96孔elisa板(costar,corning)过夜。在pbst洗涤和2小时封闭步骤后,使板与含有hbsag野生型和突变型蛋白的培养上清液一起孵育2小时。如上所述,洗涤后,使板与纯化的带his标签的1f6 fab片段(125ng/孔)一起孵育1小时,洗涤并通过添加兔hrp缀合的抗6xhis标签抗体(在封闭溶液中以1:4,000稀释,ab1187,abcam)和hrp显色底物(abts溶液,euromedex)使其显色。根据以下公式计算结合百分比:([od]
突变型
/[od]
野生型
)x 100。
[0793]
流式细胞术结合测定
[0794]
使用如前所述的pei沉淀法(lorin和mouquet,2015),使用编码s-hbs的载体(每106个细胞0.65μg质粒dna)转染freestyle
tm 293-f。转染后48小时,使用cytofix/cytoperm
tm
溶液试剂盒(bd biosciences)将转染和未转染的对照细胞固定和透化,然后在4
℃下使0.5x106细胞与igg抗体一起孵育45分钟(10ug/ml,除非另有说明,在perm/wash
tm
溶液中;bd biosciences)。洗涤后,使细胞与af647缀合的山羊抗人igg抗体(1:1000稀释度;thermo fisher scientific)在4℃下一起孵育20分钟,洗涤并重悬于pbs中。使用cytoflex流式细胞仪(beckman coulter)获取数据,并使用flowjo软件(v10.3;flowjo llc)进行分析。
[0795]
蛋白质微阵列
[0796]
所有实验均在4℃下使用protoarray人蛋白质微阵列(thermo fisher scientific)进行。如前所述(planchais等人,2019),微阵列在封闭溶液(thermo fisher)中封闭1小时,洗涤并与2.5μg/ml的igg抗体一起孵育1小时30分钟。如前所述(planchais等人,2019),洗涤后,使阵列与af647缀合的山羊抗人igg抗体(pbs中1μg/ml;thermo fisher scientific)一起孵育1小时30分钟,并使用genepix 4000b微阵列扫描仪(molecular devices)和genepix pro 6.0软件(molecular devices)使其显色。使用软件(sicasys software gmbh,germany)对荧光强度进行量化,并使用graphpad prism软件(v8.1.2,graphpad prism inc.)将每种抗体(来自重复的蛋白质点)的平均荧光强度(mfi)信号与参考抗体mgo53(非多反应同种型对照)作图。对于每种抗体,使用prospector软件(v5.2.3,thermo fisher scientific)计算z分数,并如前所述计算对角线的偏差(σ)和多反应性指数(pi)值(planchais等人,2019)。当pi》0.21时,抗体被定义为多反应性。
[0797]
hep-2细胞结合测定
[0798]
人抗s-hbs和对照igg抗体(mgo53和ed38(meffre等人,2004;wardemann等人,2003))与表达hep-2细胞的自身抗原的结合在50μg/ml下按照制造商的说明通过elisa(ana-hep-2,aesku.diagnostics,wendelsheim,germany)和间接免疫荧光测定(ifa)(ana hep-2aesku.diagnostics)进行分析。使用荧光显微镜axio imager 2(zeiss,jena,germany)检查ifa切片,并在imagopole平台(巴斯德研究所)使用zen成像软件(zen 2.0蓝色版,zeiss)以40倍的放大倍率和5000ms采集下拍摄照片。
[0799]
hbv中和测定
[0800]
heparg和hepg2.2.15细胞系分别获自biopredic international(saint-gregoire,france)和dr.michael nassal(university hospital freiburg,germany)。heparg细胞在添加10% heparg生长补充剂(biopredic)的williams e培养基(thermo fisher scientific)中培养,并在感染前使用1.8% dmso分化至少2周。通过胶原酶灌注法(tateno等人,2015)从具有人源化肝脏的嵌合upa/scid小鼠中分离出的原代人肝细胞(phh)获自phoenixbio(hiroshima,japan)。在phoenix bio提供的培养基中,以每孔7x104细胞的浓度将phh接种在i型胶原蛋白包被的96孔板上。hbv基因型d病毒在hepg2.2.15细胞培养上清液中产生,并使用聚乙二醇沉淀法浓缩(hantz等人,2009)。通过梯度超速离心从含hbv的血清(美国红十字会)中纯化基因型a至c的hbv病毒。简而言之,将1.5ml血清应用到optiprep
tm
梯度(10-50%,sigma)上,并在4℃下以32,000rpm离心3小时。收集级分(2ml)并使用s-hbs clia试剂盒(autobio)和qpcr定量分析hbs抗原表达。通过超深度测序(ddl诊断实验室,荷兰)获得所有纯化病毒分离物的全基因组序列,并使用乙型肝
炎病毒数据库hbvdb(http://hbvdb.ibcp.fr)确定hbv基因型(hayer等人,2013)。通过在heparg或phh完全培养基中使hbv病毒粒子(moi 20-30)与连续稀释的抗体在室温下孵育1小时来评估hbv抗体的中和活性。然后将hbv抗体混合物添加到96孔板中的细胞中,最终浓度为4% peg 8000(sigma)。感染的细胞在37℃下孵育20小时,然后用pbs洗涤4次以去除hbv接种物并重新填充完全培养基。感染后6天,根据制造商的说明,使用s-hbs clia试剂盒(autobio)量化上清液中的s-hbs抗原含量。
[0801]
hdv中和测定
[0802]
使用如前所述的hdv模型(sureau,2010)进行体外中和测定,除了表达ntcp的huh-106细胞替代了heparg细胞(verrier等人,2016)。在接种后第1天,将huh-106细胞(1x105细胞/20mm直径孔)在4%聚乙二醇(peg)8000存在下暴露于5x107基因组当量(ge)的hdv病毒粒子16小时。为了测定中和作用,将接种物与500ng/ml单克隆抗体的1:2稀释液混合,并在接种前将混合物在37℃下孵育1小时。在接种后9天(dpi)收获细胞,用于测量作为感染标志物的细胞内hdv rna。使用
32
p-标记的rna探针通过northern印迹分析检测hdv rna信号,并使用磷光成像仪r(bas-1800ii;fuji)进行量化。
[0803]
慢性hbv小鼠模型
[0804]
在6-8周龄c57bl/6小鼠(janvier labs,le genest-saint-isle,france)中,通过单次静脉注射(眶后静脉窦)5x10
10
携带有复制能力的hbv-dna基因组的血清型2/8腺相关病毒的病毒基因组,建立了慢性hbv感染(dion等人,2013)。病毒原液由plateforme de th
é
rapie g
é
nique(inserm u1089,nantes,france)生产并滴定为病毒基因组当量(ge healthcare)和每毫升病灶形成单位。转导后六周,向携带hbv的小鼠静脉内施用抗体(每只小鼠每次注射0.25、0.5或1mg)。收集血液样品并储存在-20℃。分别使用monolisa s-hbsag ultra(bio-rad,france)elisa试剂盒和eti-ebk plus no140(diasorin sa,italy)确定血清s-hbsag和hbeag水平。通过参考用已知浓度的s-hbsag(architect s-hbsag calibrators,bio-rad,france)和paul-ehrlich-institut标准建立的标准曲线计算浓度,并分别以iu/ml和pei u/ml表示。使用qiaamp blood mini试剂盒(qiagen,germany)从小鼠血清中纯化hbv dna,并如前所述通过定量pcr进行定量(cougot等人,2012)。含有1.2个hbv基因组拷贝的payw1.2质粒的连续稀释液用作定量标准。结果以iu/ml表示,检测阈值为1000iu/ml。所有的实验动物方案均经过巴斯德研究所动物护理委员会的审查和批准,符合法国和欧洲的动物福利法规和公共卫生服务建议(apafis#15408-2018060517005070v1)。所有hbv感染实验均在a3动物设施中进行。
[0805]
hbv huhep小鼠模型
[0806]
为了生成huhep模型,balb/c rag2-/-il-2rγc-/-nod.sirpa upa
tg/tg
(brgs-upa)小鼠脾内注射7x105新鲜解冻的人肝细胞(bd biosciences,corning)(srick-marchand等人,2015)。用物种特异性人白蛋白(halb)elisa(bethyl laboratories)确定血浆样品的肝嵌合性,用1x107hbv基因组等价物腹膜内感染≥100microg/ml halb的huhep小鼠(dusseaux等人,2017)。具有》106hbv dna拷贝/ml的hbv感染的小鼠每3-4天以20mg/kg小鼠、或每周以1mg/小鼠腹腔注射bnab ch1-187或同种型对照(mgo53)igg,或在medidrop sucralose(clear h2o)中口服递送恩替卡韦(etv)0.3mg/kg/天(baraclude,bms)。对于反弹阶段,小鼠恢复饮水。动物被安置在无病原体条件下的隔离室中,并受到人道的照顾。实验由巴斯德
研究所(法国巴黎)的机构伦理委员会批准,并由法国教育和研究部(menesr#02162.02)验证。
[0807]
统计分析
[0808]
对于ig基因谱分析,使用双侧2
×
2和2
×
5fisher精确检验对各组进行比较。使用带有welch校正的未配对学生t检验比较抗体组之间的vh、vκ和vλ突变的数量。火山图分析是通过以下进行的:比较各组之间的206个个体抗体基因特征,并报告由双侧2
×
2fisher精确检验给出的每个参数的δ平均值(x轴)和-log
10 p值(y轴)。使用graphpad prism软件(v8.1.2,graphpad prism inc.)和用于2
×
5fisher检验的sisa在线工具(http://www.quantitativeskills.com/sisa)进行统计分析。
[0809]
实例1:来自hbv疫苗接种者和控制者的人s-hbs单克隆抗体
[0810]
为了表征记忆b细胞抗体对hbv表面糖蛋白的应答,用荧光标记的重组或天然s-hbs颗粒对来自具有高血清抗hbsag igg抗体滴度(图6)的六名疫苗接种者和八名血清转换者的外周血b细胞进行染色(图1a和图8)。从通过单细胞流式细胞仪分选捕获的3,452个s-hbs结合igg+记忆b细胞中,我们通过重组表达克隆生产了总共170个独特的人单克隆抗体(见上文)。从hbv疫苗接种者和控制者克隆的s-hbs+记忆b细胞抗体与s-hbs颗粒的elisa结合分析表明,分别只有21.1%(0-61.5%)和55.2%(33.3-90.9%)与hbsag具有高亲和力(p=0.011,图1b和图9)。在hbv控制者中,高滴度的循环hbsag抗体与hbv特异性b细胞的更大恢复相关(35.2%vs 64.7%,p=0.036)。通过elisa检测缺乏s-hbs反应性的旁观者b细胞几乎都是多反应性的(未显示),因此可能通过与病毒颗粒的非包膜成分相互作用而被捕获。hbv特异性记忆b细胞主要是克隆扩增的一部分,并表达体细胞突变的免疫球蛋白基因,显示抗原驱动的成熟标志(图1c、10f和10g)。免疫球蛋白基因特征与来自健康对照的igg+记忆b细胞的比较显示,在hbv特异性b细胞谱中vh1(即vh1-69和vh1-18,p=0.041)、jh4(p=0.0017)和重排vh1(dh)jh4(p=0.017)基因,以及igg1/igg3亚类表达(p=0.019)的使用增加(图1d、图7和图10)。在利用vh1-69基因的hbv抗体中(占总数的14%),60%在疏水crdh2尖端的第54位具有种系编码的苯丙氨酸(图8c),这被证明是许多针对流感病毒、hcv和hiv-1的人类中和抗体所必需的(chen等人,2019)。只有四种抗s-hbs igg抗体(n=72)通过免疫印迹识别变性的s-hbs抗原,没有一种与“a”决定簇肽结合,而两种与“a”区域两侧的线性表位反应(图11),表明大多数s-hbs记忆抗体靶向构象表位(图1e)。我们得出结论,大多数的人s-hbs igg记忆b细胞表达富含vh1编码免疫球蛋白的构象依赖性igg1和igg3抗体。
[0811]
实例2:人s-hbs记忆b细胞抗体的体外和体内hbv中和作用
[0812]
为了确定s-hbs记忆b细胞抗体是否中和hbv,我们在基于heparg细胞的测定中测量了它们对基因型d病毒的体外中和活性。总体而言,61%的s-hbs抗体阻断了hbv感染,50%的抑制浓度(ic50)范围为50μg/ml下降到0.05pg/ml(图2a、图7和图12)。在hbv控制者中,69%的抗体具有中和作用,包括35%的ic50值低于50ng/ml的有效中和剂(图2a和图7)。具有较高超突变负荷和对s-hbs抗原更广泛反应性的s-hbs抗体更容易抑制hbv感染(图2b)。hbv中和剂同样表达vh1-69f54和l54等位基因。丁型肝炎病毒(hdv)是一种德尔塔病毒(deltavirus)属的有缺陷的hbv卫星病毒,包被有hbv包膜蛋白(sureau和negro,2016)。因此,我们询问hbv中和抗体是否也可以在体外预防hdv感染。正如预期的那样,在huh-106细
胞测定中,选定的抗体中和hdv的效率与hbv一样(图2c)。
[0813]
为了评估中和抗s-hbs抗体的体内活性,我们基于重组hbv编码腺相关病毒(aav)的肝脏靶向转导生成了hbv持久性小鼠(dion等人,2013)。选择了四种有效的hbv中和剂并将其被动转移到携带高水平循环s-hbsag(》104iu/ml)的aav-hbv小鼠中。单次静脉内(i.v.)注射约20mg/kg的抗体导致注射后2天(dpi)的病毒血症显著下降,而用较低的抗体剂量治疗效果较温和,因为抗体的快速耗尽超过了hbv粒子(图2d、图2e和图13)。两种最有效的抗体bc1.187和bv4.104在最低点(dpi2)分别诱导1.7和2.1log10的平均下降(图2e)。下降后2天病毒反弹伴随抗体衰减,循环hbsag在dpi7时恢复到基线水平(图2d和图13b)。由于体内病毒血症的下降取决于所施用抗体的量,我们接下来考虑确定增加剂量的hbv交叉中和抗体bc1.187的影响。接受单次注射约40mg/kg的bc1.187(每只小鼠静脉注射1mg)的病毒血症aav-hbv小鼠在dpi2时病毒血症平均最大减少2.8log10(图2f),hbsag水平持续低于基线至少12天(图2f)。在接受治疗的动物中,hbv dna载量随着血清hbsag滴度的变化而下降,平均下降3.6log10,在病毒反弹前6只小鼠中有4只最后一次注射bc1.187后长达一周内达到无法检测到的水平(图2f)。
[0814]
实例3:强效人hbv中和抗体的跨基因型活性
[0815]
根据“a”决定簇中的特定氨基酸变异(adr、adw、ayr、ayw)将hbv分为四种主要血清型,并根据基于病毒基因组的系统发育(a到j)分为10种基因型(kato等人,2016)。结合分析表明,最有效的hbv中和抗体(71%)能够分别识别用于genhevac-b和engerix-b疫苗的adw和ayw hbsag颗粒(图3a)。重要的是,大约一半的中和剂与来自9种不同基因型(a到i)的共有s-hbs蛋白发生同样的交叉反应(图3b)。其他显示出更多异质的结合特征,抗体不与f和h基因型反应(19%,全部来自供体bc4),或与d-f和h结合,或仅与d和e结合(图3b)。为了验证跨基因型hbv结合反映了交叉中和潜力,我们测量了hbv交叉反应中和剂bc1.187对来自基因型a、b、c和d的hbv病毒粒子感染原代人肝细胞的体外中和活性。正如预期的那样,bc1.187中和了所有4种基因型的hbv病毒,尽管基因型a和c比b和d更有效(图3d)。在heparg细胞测定中,基因型a和c病毒粒子也对bc1.187高度敏感,而bv4.104与其反应性谱一致,仅有效中和基因型d hbv(图3e)。
[0816]
在人类中,已经描述了几种hbv逃逸突变,其中g145r是s蛋白区域中最普遍的替代(chotiyaputta和lok,2009;huang等人,2012)。因此,我们评估了其中一些突变是否会影响强效中和剂对hbv的识别(图3e和图16)。对于大约一半的抗体,仅在g145r突变蛋白中检测到s-hbs结合的显著降低或丧失,表明已知破坏“a”决定簇的抗原性的g145r突变(huang等人,2012;salisse和sureau,2009)可能不利于某些hbv抗体的中和活性。突变体结合分析还表明,没有一种中和抗体与在n146位发现的s-hbs上的独特n-聚糖相互作用(图3e和图16)。总的来说,这些数据表明,hbv控制者中的s-hbs特异性记忆b细胞可以产生有效的交叉中和抗体,能够消除循环hbsag颗粒并抑制hbv病毒血症。
[0817]
实例4:强效人hbv中和抗体的结合特征
[0818]
为了绘制强效中和hbv抗体靶向的表位,我们使用了具有覆盖hbsag的主要亲水区的取代的突变hbsag蛋白文库进行了丙氨酸扫描elisa实验。尽管所有测试的抗体都呈现出独特的识别模式,但可以根据突变敏感性识别常见的结合谱(图4a)。关键表位区域主要位于“a”决定簇内部,但也位于n末端和c末端s-hbs区域(分别为bc8.109和bc1.263)之外。其
他一些无法明确识别(bc4.204、bc4.194、bc4.178、bc3.106和bc8.104)(图4a)。“a”决定簇中的中和表位非常复杂,包括以下各项中的主要相互作用残基):(i)“迷你”和第二个环(bc8.159和bc1.130),(ii)第一个环和第二个环(bv4.105和bv4.106)、所有3个环(bv4.104、bc8.111、bc1.128和bc1.156),或主要在第二个环(bv4.115、bv6.172、bc1.187、bc1.229和bc1 180)(图4a)。接下来,我们进行了竞争性s-hbs结合elisa分析,以评估中和表位之间的重叠程度。在上述每个抗体类别中,交叉竞争分子大多以独立的串联形式被发现:bv4.104/bc8.111、bc8.128/bv4.106、bc1.180/bc1.263和bc3.106/bc6.149(图4c)。三重中和剂bc4.194/bc4.204/bc4.178识别出一个常见的非构象表位,该表位未通过图谱明确定义(图1e、图4a和图4b),但可能位于hbsag n末端或c末端的最远端部分。在这方面,所有3种抗体都不能结合f和h基因型,这主要与预测为跨膜结构域3(q178-y225)的区域中的其他基因型不同(图11)。此外,bc4.204的结合因f179a突变而降低,并且与c末端(191-200)中的线性肽的结合也较弱(图4a和图15)。较大的表位簇包含中和抗体,该中和抗体的表位更集中在第二个环(bv4.115、bv6.172、bc1.187、bc1.229),但也能够干扰其他中和剂的s-hbs结合(图4b)。
[0819]
为了检查体细胞突变是否有助于hbv中和抗体的活性,我们恢复了三种具有代表性的强效中和剂中的突变,以产生它们推定的种系前体(gl)。代表性的gl版本显示出异质的hbv识别谱:bc4.204-gl未能与s-hbs反应,而bc1.187-gl和bv4.104-gl仍然结合,但与成熟的对应物相比,相对亲和力要低得多(图4c)。与突变抗体相比,gl igg显示较弱,但对基因型d hbv特别是bc1.187-gl的体外heparg细胞感染具有显著抑制活性,ic50为0.08μg/ml(图4d)。这意味着尽管b细胞前体表达的某些种系抗体可以结合和中和高浓度的hbv,但它们的高亲和力hbsag结合和有效的hbv中和需要体细胞突变。
[0820]
人类类别转换记忆b细胞,包括针对病毒抗原的高亲和力b细胞克隆,可以与自身抗原发生交叉反应(andrews等人,2015;prigent等人,2018;prigent等人,2016;tiller等人,2007)。因此,我们使用临床自身抗体测定(hep-2细胞ifa和elisa)和微阵列免疫印迹(》9,000种人类蛋白质)评估了10种选定的有效hbv中和剂的自身反应性。除了bc1.263之外,没有一种hbv中和剂显示出多反应性,这是通过与同种型对照相比微阵列荧光信号的整体偏移来测量的(图18a)。只有bc1.263和bc4.204抗体分别显示出针对半乳糖凝集素-3/-8和e3泛素-蛋白连接酶ubr2的显著交叉反应性(z分数》5)(图4d和图18b)。没有hbv中和剂显示阳性hep-2 elisa反应性(图18c),尽管通过ifa使用高抗体浓度检测到低(bc1.187,bc1.263)至中等(bc4.194,bc4.204)的与hep-2细胞抗原的结合(图18c)。
[0821]
实例5:强效交叉中和抗体bc1.187在体内抑制hbv
[0822]
为了确定来自自然控制者的强效hbv中和剂是否能在体内稳定抑制hbv病毒血症,用bc1.187抗体(0.5mg静脉内注射,~20mg/kg,每周两次)治疗aav-hbv小鼠17天(图19a)。病毒血症小鼠在用bc1.187治疗时经历了循环hbsag水平的降低,但在用同种型对照时没有(图19a)。然而,鼠抗人igg抗体(称为ada,抗药物抗体)的发展迅速改变了治疗效果(图19b)。为了克服或限制ada的产生,我们通过将抗体的可变结构域与鼠igγ2a和igk恒定区相结合来生成bc1.187的嵌合版本。嵌合bc1.187抗体(c-bc1.187)在未转导的野生型小鼠中具有3.9天的血清半衰期(图19c),并且在aav-hbv小鼠中每周施用时导致可重现的病毒血症下降(连续3周dpi2时平均0.88
±
0.07log10)(图19d)。每2天用0.5mg的c-bc1.187而不
是对照抗体静脉内注射治疗16天导致从第4天开始所有aav-hbv小鼠的循环hbsag下降,与设定点相比平均下降2.5log10倍(图5a)。在c-bc1.187治疗期间,hbv病毒血症(以病毒dna iu/ml计)也急剧减少了平均2.5log10倍,到第21天,除一只小鼠外,其他所有小鼠均达到无法检测到的水平(图5a)。在最后一次注射抗体后,hbsag和hbv病毒血症仍被抑制两周,然后回升至基线水平(图5a)。正如该模型所预期的那样,hbe抗原(病毒复制的替代标志物)的血清水平在治疗期间保持不变(图5a)。
[0823]
我们接下来想知道bc1.187是否可以改变体内hbv感染的自然过程。稳定移植人肝细胞(huhep)的balb/c rag2-/-sirpanodalb-upatg/tg小鼠感染了基因型d hbv。一旦感染建立,小鼠接受每两周一次(每只小鼠20mg/kg)或每周一次(每只小鼠50mg/kg)bc1.187注射3周。与aav-hbv体内模型一致,对于20mg/kg和50mg/kg给药方案,用bc1.187(而非非hbv抗体和核苷逆转录酶抑制剂对照)治疗,在病毒血症huhep小鼠中诱导循环hbsag水平在dpi21下分别平均降低2.1和2log10倍(图5b和图19a)。然而,hbv病毒血症在每周接受注射50mg/kg的bc1.187的组中下降更有效(在dpi21下平均下降为1.76log10,而20mg/kg为0.64log10)(图5b)。在随访结束时,两只治疗前病毒血症低的小鼠对20mg/kg给药方案的应答显示出完全的病毒抑制(28.6%,n=7)(图5b和图19b)。在60%的小鼠(n=5)中最后一次注射50mg/kg bc1.187后,循环hbsag水平下降并在2周内无法检测到。在这些小鼠中,一只死亡,另一只经历病毒反弹,最后一只在治疗后在hbv病毒血症再次出现之前仍控制感染一个多月(图5b和图19b)。在bc1.187抗体治疗后,hbeag的循环水平也降低了,但与hbsag相比程度较低(对于20mg/kg,在dpi21下的平均倍数变化为0.26log10,对于50mg/kg的平均倍数变化为0.49log10)(图5b)。人白蛋白的血清滴度在监测期间保持不变(图19c),表明植入是稳定的并且不受治疗影响。
[0824]
发明内容
[0825]
少数个体可以自然地清除慢性乙型肝炎病毒(hbv)感染,并获得疫苗接种所赋予的免受再次感染的保护。为了检查对hbv的保护性体液应答,我们从hbv疫苗接种者和控制者的记忆b细胞中克隆了针对病毒表面糖蛋白s-shbs的人抗体。我们发现来自自然控制者的s-shbs记忆b细胞主要产生能够与几种病毒基因型交叉反应的中和抗体。人类中和hbv抗体由一组不同的免疫球蛋白基因编码,并识别s-shbs抗原上的各种构象表位。引人注目的是,在hbv小鼠模型中,使用从控制者中分离出的强效交叉中和剂bc1.187进行单一疗法可在体内抑制病毒血症,并导致治疗后控制某些动物的感染。因此,中和s-shbs抗体可能在hbv的自发控制中发挥关键作用,并代表了有望在慢性感染人类中实现hbv功能性治愈的免疫疗法。
[0826]
本文所述的某些抗体的结果总结于下表2中。这总结了图3的结果。因此,“血清型”数据报告了hbv中和抗体对adw和ayw基因型d s-hbs蛋白的elisa反应性(测量为图14中的auc值)。“跨基因型结合”报告了hbv中和抗体对来自指定基因型的s-hbs抗原的反应性,以流式细胞术确定的结合s-hbs表达细胞的百分比表示。“突变型结合”与“跨基因型结合”相同,但不同的是描述的s-hbs突变型蛋白。ic50值是针对来自基因型d的hbv病毒对原代人肝细胞感染的中和活性。表3提供了从elisa图计算的ec50值,显示所选抗体对重组hbv疫苗engerix-b(ayw)和genhevac(adw)的反应性(图3)。
[0827][0828]
表3
[0829][0830]
讨论
[0831]
在慢性hbv感染中,大多数hbsag特异性b细胞是非典型记忆淋巴细胞,表现出多种b细胞功能障碍,诸如分化为产生抗体的细胞的能力改变,从而可能产生hbv中和抗体(burton等人,2018;salimzadeh等人,2018)。相比之下,在急性期和慢性期治愈感染的个体的循环b细胞分泌可能参与血清转换的hbsag抗体(salimzadeh等人,2018;xu等人,2015)。为了表征免疫供体中针对hbv表面抗原的记忆b细胞,我们研究了从hbv控制者和疫苗接种者的血液中循环的单一s-hbs特异性igg
+
克隆的重组人抗体的分子和功能特性。我们的研究表明,尽管vh1-jh4编码克隆中度富集,但来自hbv控制者以及疫苗接种者的循环s-hbs特异性记忆b细胞,表达主要识别hbv表面糖蛋白上的构象表位的多种免疫球蛋白基因谱。从控制者克隆的大多数抗s-hbs igg可以在体外中和hbv,其中一些在非常低的浓度下具有活性,包括针对抗hdv感染。在体内评估的强效中和剂还通过降低血清hbsag水平和hbv病毒血症显示出抗病毒作用,这表明在受感染的人类中,这些抗体可能在功能上很重要。大多数hbv中和抗体对各种病毒基因型具有广泛反应性,并识别位于“a”决定簇中的表位,尽管其他抗体也位于该区域之外。鉴定了几个中和表位,包括涉及由有效的交叉中和抗体bc1.187识别的s-hbs第二环的主要区域。在慢性hbv感染小鼠模型中,单次被动输注bc1.187在体内特别有效,可在几天内完全抑制血清hbsag和hbv病毒血症。有趣的是,我们在这里展示了bc1.187的种系版本仍然可以结合和中和ic
50
《0.1μg/ml的hbv。这表明表达这种免疫球蛋白的b细胞前体可以迅速亲和力成熟,因此很容易在中和hbv中发挥作用。
[0832]
目前治疗慢性hbv感染的疗法包括有效的直接抗病毒药物和peg-ifnα。然而,抗病毒治疗对血清hbsag水平没有显著影响,这主要是由于缺陷的亚病毒颗粒数量超过了传染性hbv病毒粒子。因此,绕过在慢性感染个体中观察到的免疫耐受,并诱导有效的抗hbv抗体应答仍然是一个重大挑战。一种有前途的策略是开发基于使用有效的hbv中和抗体的免疫疗法(corti等人,2018;gao等人,2017;tu和urban,2018)。小鼠和猴子的临床前模型,以及
慢性感染人类的几项i期临床试验表明中和hbv单克隆抗体的体内功效,当在受感染的受体中施用时,通过抑制hbsag并减少hbv dna含量而改变感染过程(eren等人,2000;galun等人,2002;lee等人,2019;lever等人,1990;li等人,2017;van nunen等人,2001;张等人,2016;朱等人,2016)。在这项研究中,我们使用两种不同的小鼠模型表明,用有效的人类交叉中和抗体治疗病毒血症动物对hbv感染有深远的影响。bc1.187疗法引起循环hbsag和hbv dna的快速丧失和/或显著减少,这种情况在治疗后在大多数小鼠中持续了数天至数周。体内实验还表明,低病毒血症小鼠可以在bc1.187抗体治疗后清除hbv感染。抗体是多功能的免疫效应物。除了中和作用外,它们还可以发挥多种免疫效应子功能,诸如抗体依赖性细胞毒性(adcc),它允许先天免疫细胞(诸如自然杀伤细胞(nk))杀伤受感染的细胞。adcc活性是人类中和抗体对病毒诸如hiv-1和流感的治疗特性的关键组成部分(bruel等人,2016;dilillo等人,2014)。早期,补体依赖性裂解和adcc参与了使用体外和体内系统对鼠抗s-hbs抗体的肝细胞杀伤活性(shouval等人,1982a;shouval等人,1982b)。最近,通过引发fc依赖性效应子功能,已显示针对前s1区的人类中和hbv抗体具有部分持续病毒学抑制的治疗活性(li等人,2017)。最后,通过利用宿主免疫系统进行抗体疗法可以刺激免疫应答,这是一种更好地理解并被称为疫苗样效应的特性(pelegrin等人,2015年),这种特性对于打破hbv诱导的免疫耐受方面可能是至关重要的。因此,我们建议除了阻断新发感染和可能通过fc依赖性机制消除受感染的肝细胞外,还可以在慢性感染的患者中使用本文描述的一些有效的人类交叉中和hbv抗体来大大降低血清hbsag水平。此类抗体确实可以充当强大的“抗原汇”,当与旨在恢复宿主先天性和适应性免疫应答的疗法,即,infα、治疗性疫苗、tlr激动剂、检查点抑制剂相结合时(fanning等人,2019;gehring和protzer,2019;maini和burton,2019),可以促进病毒清除并最终导致对hbv感染的长期控制。
[0833]
实例6-bc1.187和bc1.187工程化改造的构建体的体外和体内药代动力学(pk)评估
[0834]
用于测量抗体回收和转胞吞作用(抗体回收和清除(arc)测定)的体外脉冲追踪测定用于标记由两种已知机制驱动的潜在清除责任:1)非特异性清除-由非特异性结合/内化至细胞中驱动(ph=7.4时的arc分数),以及2)fcrn介导的效应(ph=6时的arc分数和arc倍数偏移)。该测定提供了相对于已在人类中显示类似igg的药代动力学的对照的这些参数的评估(有关该测定的进一步描述,请参阅mabs。2017 7月;9(5):781-791.doi:10.1080/19420862.2017。1320008)。野生型igg1 bc1.187在ph 7.4和ph 6下分别显示0.28和4.97的arc分数,导致17.8的arc倍数偏移。这些值表明非特异性结合/内化到细胞中的可能性低,以及与igg分子一致的fcrn循环。在测定中还评估了基于bc1.187 igg但具有额外fcrn修饰以增强fcrn结合(和再循环)的类似构建体,结果总结在表4中。数据显示,fcrn工程化改造可以增加arc倍数偏移,这预示着较低的体内清除率。
[0835]
第二个体外测定,大分子非特异性清除测定(luca)用于评估人原代内皮细胞中的抗体清除率。该测定与表达内源性fcrn的量的内皮细胞吸收mab的速率相关,并提供由非特异性吸收、fcrn循环和蛋白质降解产生的相对luca率。bc1.187的相对luca率为0.05,表明标准化化合物motavizumab-yte(相对luca率为0)和cd20-tcb(相对luca率为1)之间的细胞积累率。这也表明预测的人类bc1.187的类似igg特性。此外,在测定中测试了基于bc1.187的fcrn工程化改造的构建体,结果总结在表4中。至于arc测定,预计fcrn工程化改造的构建
体在体内具有较低的清除率。
[0836]
最后,在表达人类新生fc受体的转基因小鼠(hufcrn-tg小鼠)中评估了野生型bc1.187 igg和fcrn工程化改造的bc1.187 igg构建体的体内药代动力学,因为这些小鼠已被证明对人类pk具有预测性。(有关小鼠模型的进一步描述,请参阅28.proetzel等人,methods。2014;65:148
–
53;roopenian等人,methods mol biol.2016;1438:103
–
14;avery lb等人,mabs。2016;8:1064-78)。所有构建体均以5mg/kg的剂量静脉内施用,清除参数总结在表4中。对于所有测试的构建体,观察到这些小鼠中igg在典型范围内的清除。综合这些体外和体内药代动力学基准研究表明,基于bc1.187序列的中和抗体可能在人体中表现出类似igg的药代动力学。蛋白质工程化改造可导致较低的预计清除率,这将为中和抗体带来显著优势,因为它有望转化为更长的hbsag中和持续时间,或更长的临床给药间隔(即增加便利性和依从性)。
[0837]
表4:体外和体内测定的总结,以评估清除过程
[0838][0839]
尽管为了清楚理解的目的先前已通过举例说明和实施方案相当详细地描述了本发明,但是这些描述和实施方案不应解释为限制本发明的范围。本文引用的所有专利和科学文献的公开内容均全文以引用方式明确地并入。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1