一种具有抗氧化的积雪草提取物的提取工艺及应用的制作方法
1.本发明涉及中药制备的技术领域,特别涉及一种具有抗氧化的积雪草提取物的提取工艺及应用。
背景技术:
2.自由基是包含不成对价电子的各种原子、分子或离子,按其构成是否包含氧分子可将其分为氧自由基和非氧自由基。自由基可通过内源性或外源性两种途径产生。真核细胞中90%的内源性自由基是由线粒体电子逃逸产生的,线粒体电子与o2反应生成o-2
·
,进而转化为h2o2。剩下10%则在过氧化物酶体、血浆和核膜等处产生。而外源性自由基的产生途径较广,外部刺激如光、热、超声、辐射均可导致氧化还原反应和电解反应产生自由基,外环境致使心理压力和胁迫感增加也能使机体产生自由基。机体能够通过抗氧化防御系统阻止自由基的过度累积,平衡其破坏作用。自由基导致人体衰老的科学研究已被大多数人认可,致衰老机制和形式虽多种多样,但综合表现为各种与年龄相关的应激反应和炎症反应。
3.内源性和外源性刺激作用于机体后产生了自由基,自由基介入并干扰正常信号传导通路,但是能否引起损伤甚至衰老不仅取决于刺激的强度,还取决于机体的适应性。
4.积雪草苷(asiaticoside,as)是存在于积雪草中的一种三萜类化合物,其分子式为c
48h78o19
、分子量为959.12。as作为积雪草的主要药理活性成分之一,具有抗肿瘤、抗炎、保护神经系统功能、促进伤口愈合等多种药理作用。
5.积雪草苷元由积雪草提取物中的积雪草酸、羟基积雪草酸及三萜酸三种成分的组合而成,具有很强的对于皮肤清除自由基及抗氧化的功效应用价值。
6.羟基积雪草苷(madecassoside,mc)是积雪草中含量最高的五环类三萜化合物,分子式为c
48h78o20
,相对分子质量975.13,外观形状为白色结晶。羟基积雪草苷是积雪草由异戊二烯途径合成的皂苷类次生植物代谢产物。天然衍生化合物在生物医药领域通常具有广泛的生物学活性,在临床与日常生活中亦具有较广泛的应用。
技术实现要素:
7.针对现有技术中存在的不足之处,本发明的目的是提供一种具有抗氧化的积雪草提取物的提取工艺及应用,提取纯度高,分离成分精准,具有高效的清除自由基的能力。为了实现根据本发明的上述目的和其他优点,提供了
8.积雪草提取物在制备抗氧化产品中的应用。
9.优选的,包括羟基积雪草苷、积雪草苷以及积雪草苷元。
10.优选的,积雪草苷元包括积雪草酸、羟基积雪草酸及三萜酸。
11.优选的,羟基积雪草苷、积雪草苷以及积雪草苷元的质量分均为1%-100%。
12.优选的,羟基积雪草苷、积雪草苷以及积雪草苷元的质量分均为90%-100%。
13.一种清除自由基的羟基积雪草苷的提取工艺,包括:
14.s1、将积雪草全草粉碎进行搅拌提取;
15.s2、通过压滤,并进行药液上树脂柱吸附,用乙醇将有效成分从树脂柱洗脱出来;
16.s3、通过将药液上脱色树脂柱,对药液进行脱色,脱色液经刮板浓缩器浓缩至稠膏;
17.s4、转至d级洁净区的微波干燥箱进行烘干;
18.s5、通过粉碎、过筛、总混,即得积雪草总苷;
19.s6、将乙醇溶解分离积雪草苷,得到羟基积雪草苷粗品;
20.s7、通过95%乙醇溶解精制,烘干,粉碎过筛网后,即得羟基积雪草苷。
21.优选的,步骤s1中将将积雪草全草粉碎至60目细粉,投入提取罐中,每罐900kg细粉,加入4.5吨沸水搅拌提取2小时。
22.优选的,步骤s5与步骤s7中的过筛均为100目。
23.优选的,步骤s6中的乙醇为5倍95%乙醇。
24.羟基积雪草苷在制备抗过敏产品中的应用。
25.羟基积雪草苷在制备化学灼伤修护产品中的应用。
26.本发明与现有技术相比,其有益效果是:通过本技术的制备工艺提取出的积雪草苷元、羟基积雪草苷、积雪草苷三种积雪草成分,提取纯度高,分离成分精准,积雪草苷元、羟基积雪草苷、积雪草苷三种积雪草主要功效成分在清除自由基能力高。
附图说明
27.图1为根据本发明的具有抗氧化的积雪草提取物的提取工艺及应用的工艺流程图;
28.图2为根据本发明的具有抗氧化的积雪草提取物的提取工艺及应用的积雪草苷90%浓度对abts+自由基清除率曲线图;
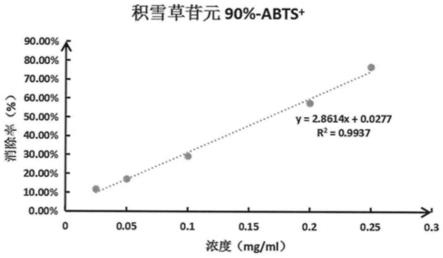
29.图3为根据本发明的具有抗氧化的积雪草提取物的提取工艺及应用的积雪草苷元90%浓度对abts+自由基清除率曲线图;
30.图4为根据本发明的具有抗氧化的积雪草提取物的提取工艺及应用的羟基积雪草苷90%浓度对abts+自由基清除率曲线图。
具体实施方式
31.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
32.参照图1-4,积雪草提取物在制备抗氧化产品中的应用。
33.进一步的,包括羟基积雪草苷、积雪草苷以及积雪草苷元。
34.进一步的,积雪草苷元包括积雪草酸、羟基积雪草酸及三萜酸。
35.进一步的,羟基积雪草苷、积雪草苷以及积雪草苷元的质量分均为1%-100%。
36.进一步的,羟基积雪草苷、积雪草苷以及积雪草苷元的质量分均为90%-100%。
37.一种清除自由基的羟基积雪草苷的提取工艺,包括:s1、将积雪草全草粉碎进行搅拌提取;
38.s2、通过压滤,并进行药液上树脂柱吸附,用乙醇将有效成分从树脂柱洗脱出来;
39.s3、通过将药液上脱色树脂柱,对药液进行脱色,脱色液经刮板浓缩器浓缩至稠膏;
40.s4、转至d级洁净区的微波干燥箱进行烘干;
41.s5、通过粉碎、过筛、总混,即得积雪草总苷;
42.s6、将乙醇溶解分离积雪草苷,得到羟基积雪草苷粗品;
43.s7、通过95%乙醇溶解精制,烘干,粉碎过筛网后,即得羟基积雪草苷。
44.一种清除自由基的积雪草苷的提取工艺,积雪草全草粉碎至60目细粉,投入提取罐中,每罐900kg细粉,加入4.5吨沸水搅拌提取2小时,经压滤后,药液上树脂柱吸附,用乙醇(60%-75%)将有效成分从树脂柱洗脱出来,再将药液上脱色树脂柱,对药液进行脱色,脱色液经刮板浓缩器(温度55~75℃,真空>0.06mpa)浓缩至稠膏(相对密度1.05~1.15(75℃)),转至d级洁净区的微波干燥箱(温度30~65℃真空>0.06mpa)进行烘干,烘干后再经粉碎、过筛100目、总混,即得积雪草总苷。再用5倍95%乙醇溶解分离积雪草苷,得到积雪草苷粗品,再通过95%乙醇溶解精制,烘干,粉碎过100目筛网后,即得积雪草。
45.一种清除自由基的积雪草苷元的提取工艺,积雪草全草粉碎至60目细粉,投入提取罐中,每罐900kg细粉,加入4.5吨沸水搅拌提取2小时,经压滤后,药液上树脂柱吸附,用乙醇(60%-75%)将有效成分从树脂柱洗脱出来,再将药液上脱色树脂柱,对药液进行脱色,脱色液经刮板浓缩器(温度55~75℃,真空>0.06mpa)浓缩至稠膏(相对密度1.05~1.15(75℃)),转至d级洁净区的微波干燥箱(温度30~65℃真空>0.06mpa)进行烘干,烘干后再经粉碎、过筛100目、总混,即得积雪草总苷。再经过水解后,静置沉淀,将沉淀物弃去,留上清液经过板框过滤,再进一步精制、烘干后粉碎、粉筛过100目筛网后,即得积雪草苷元。
46.abts+自由基清除测试
47.检测目的
48.检测待测样品为三个样品:积雪草苷90%、积雪草苷元90%、羟基积雪草苷90%的抗氧化就是清除自由基的能力。
49.检测仪器和设备
50.分析精密天平:称量0.1mg;
51.容量瓶:10ml、20ml、50ml、100ml;
52.可调节移液枪:1.00ml;
53.酶联免疫检测仪:紫外可见分光光度计uv-1800。
54.试剂
55.除有另外说明外,所有试剂均为分析纯,水为符合gb/t 6682规定的一级水。
56.95%乙醇;
57.2,2
′‑
联氮-双-3-乙基苯丙噻唑啉-6-磺酸(sigma公司);
58.阳性对照:维生素e,纯度≥96%。
59.样品信息
60.表4-1样品主要信息
[0061][0062]
实验步骤
[0063]
5.1abts+母液:量取等体积7.4mm的abts水溶液和2.6mm的过硫酸钾水溶液,混合均匀,于室温黑暗条件下反应12-16h。以棕色瓶配制,包裹锡纸,低温保存,即得;
[0064]
5.2abts+工作液:将abts+母液以95%乙醇稀释至吸光度为0.7
±
0.05,即得,避光待用;
[0065]
5.3阳性对照物用95%乙醇溶液稀释成:0.08mg/ml、0.04mg/ml、0.02mg/ml、0.01mg/ml系列浓度梯度用以验证试验系统。
[0066]
5.4待测样品处理:受试物用95%乙醇稀释为多级浓度样品。
[0067]
参照表5.4-1,使用10ml试管设立样品管(t)、样品本底(t0)、abts+管(c)和溶剂本底(c0),每一样品的每个受试浓度的样品管(t)需设立3支平行管,同时abts+管(c)也需设立3支平行管。
[0068]
在样品管(t)和样品本底(t0)中各加入1ml相同浓度的样品溶液。
[0069]
5.5在所有试管中(t、t0、c、c0)补充溶剂,待测样品用95%乙醇,补足3ml,混匀。
[0070]
5.6在样品管(t)和abts+管(c)中加入abts+乙醇溶液1ml,样品本底(t0)个溶剂本底(c0)用95%乙醇代替,轻轻摇匀,室温下静置5分钟。
[0071]
5.7将各支反应溶液移入1cm比色皿中,在734nm处测定吸光值。
[0072]
表5.4-1样品加液要求
[0073]
t-样品管t0-样品本底c-abts
+
管c0-溶剂本底样品溶液(ml)11
‑‑
95%乙醇溶剂(ml)2233abts
+
工作液(ml)1-1-95%乙醇(ml)-1-1平行次数3/样1/样3/试验1/试验
[0074]
6、实验结果
[0075]
6.1待测样品对abts+自由基的清除结果。
[0076]
6.2计算abts+自由基清除率:
[0077][0078]
式中:
[0079]
t-样品管吸光值,及样品与abts+反应后溶液吸光值;
[0080]
t0-样品本底吸光值;
[0081]
c-abts+管吸光值3次平均值,即未加样品时abts+溶液吸光值;
[0082]
c0-溶剂本底吸光值。
[0083]
6.3检测结果待测样品积雪草苷90%对abts+自由基的清除结果。
[0084]
表6.3-1积雪草苷90%对abts
+
自由基清除的检测结果
[0085][0086]
*表中数据为均值
±
相对偏差。
[0087]
*ic50为达到50%清除效果时对应样品的受试浓度。
[0088]
6.4检测结果待测样品积雪草苷元90%对abts+自由基的清除结果
[0089]
表6.4-1积雪草苷元90%对abts
+
自由基清除的检测结果
[0090][0091]
*表中数据为均值
±
相对偏差。
[0092]
*ic50为达到50%清除效果时对应样品的受试浓度。
[0093]
6.5检测结果待测样品羟基积雪草苷90%对abts+自由基的清除结果。
[0094]
表6.5-1羟基积雪草苷90%对abts
+
自由基清除的检测结果
[0095][0096]
*表中数据为均值
±
相对偏差。
[0097]
*ic50为达到50%清除效果时对应样品的受试浓度。
[0098]
每批次实验加入阳性对照的测试,阳性对照维生素e的ic
50
(达到50%清除效果时对应的样品受试浓度)均在0.02mg/ml-0.06mg/ml,本项目所有批次试验系统均有效。
[0099]
7检测结论
[0100]
7.1由表6.3-1及图2可得,积雪草苷90%样品对abts+自由基的清除率在测试浓度范围0.25-2.5mg/ml内抗氧化效果不明显,均未达50%清除率(即ic
50
);
[0101]
7.2由表6.4-1及图3可得,积雪草苷元90%样品对abts+自由基的清除率在测试浓度范围0.025-0.25mg/ml内具有抗氧化效果,且样品浓度与清除率呈线性关系,达50%清除率(即ic
50
)时浓度约为0.1651mg/ml;
[0102]
7.3由表6.5-1及图4可得,羟基积雪草苷90%样品对abts+自由基的清除率在测试
浓度范围0.25-2.5mg/ml;
[0103]
7.4使用abts+自由基清除检测方法,结果得积雪草苷元和羟基积雪草苷均具有一定的抗氧化效果,而积雪草苷抗氧化效果不明显,抗氧化效果;积雪草苷元》羟基积雪草苷》积雪草苷。
[0104]
这里说明的设备数量和处理规模是用来简化本发明的说明的,对本发明的应用、修改和变化对本领域的技术人员来说是显而易见的。
[0105]
尽管本发明的实施方案已公开如上,但其并不仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节和这里示出与描述的图例。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1