金属回收方法与流程
本发明涉及一种用于从水溶液或例如矿石和废料的固体原料中回收金属的方法。具体地说,在所述方法期间利用生物冶金技术。
背景技术:
全世界有大量含有痕量金属的材料,包括水溶液和固体材料。然而,由于相对于非金属基质,金属组分相对稀少,因此以有效、环境上安全的方式回收这些金属极具挑战性。举例来说,从水性液体废料流中去除毒性金属离子为广泛范围的工业的重大难题。
类似地,随着用于开采和精炼原生金属的矿石等级降低,人们越来越关注从例如低级开采矿石、冶炼厂尾矿和电子废料的来源中获得金属。然而,从这些原料中回收金属常常在经济上让人望而却步。影响任何回收方法的可行性的因素包括原料的金属浓度(和因此用于处理所需的原料的量);耐火材料的存在;和所产生废液的体积。因此,替代溶液有了一席之地,其旨在减轻这些问题中的至少一些,从而提高从低级或顽固原料中回收金属的经济性。
用于精炼金属的传统技术包括火法冶金和湿法冶金。在火法冶金中,在高温下(通常在合适的还原剂和/或催化剂存在下)熔炼原料。这需要大量的能量输入(和相关排放),并且因此原料中需要有实际最小金属浓度。在湿法冶金中,原料用浸滤剂溶液处理,所述浸滤剂溶液将所需金属(特定地或以其它方式)浸出成离子或络合可溶形式。需要后续步骤以从溶液中回收目标金属(例如,电解沉淀)。视浸出的温度和压力要求而定,这种方法与火法冶金相比可处理更低级原料。需要考虑可能使用腐蚀性(例如酸性)或毒性(例如氰化物)溶液;原料处理过程中任何溶液组分的消耗;和适当处理废液。火法冶金和湿法冶金技术不相互排斥,并且可在多个步骤中依序使用以精炼特定金属。
从含有金的矿石中回收金为具有多种问题的湿法冶金方法的典型实例。带有金的矿石中的金的量已经下降超过一百年,由于更容易回收,通过大规模开采已耗尽了金含量较高的资源。因此,湿法冶金技术已用于从大体积的岩石中回收痕量金。已成功地采用氰化物类浸滤剂多年,但有着毒性问题和处理某些矿石类型的难题。
废弃电子设备,例如来自计算机、手机、笔记本计算机和lcd显示器的印刷电路板也含有可观量的贵金属(包括金)。虽然已对使用火法冶金和湿法冶金方法从电子废料中回收金做出大量努力,但尚未取得可持续的成功。
生物冶金为最新的方法,其使用微生物以在环境条件下从原料中暴露、浸出、结合和/或回收金属(zhuang等人,《生物技术新见(currentopinioninbiotechnology)》33,第327-335页(2015))。使用微生物可以进一步降低原料所需的最低等级,或者更好地实现对火法冶金和/或湿法冶金工艺耐火的原料的经济加工。然而,常见的权衡是反应时间:生物冶金通常需要数周到数年才能从原料中回收金属(例如使用硫还原细菌对耐火的铜矿石进行生物氧化)。
本发明的目的为提供一种使用生物冶金技术回收金属的方法,其补充或替代传统的火法冶金和湿法冶金方法。希望这将导致从目前被忽视的低级或废弃金属流中获取价值,或者至少为公众提供这方面的有用选择。
技术实现要素:
本发明响应于所属领域的需要。本发明提供用于从含有金属离子的水溶液或含有金属的固体原料中回收金属的方法。
在第一方面,本发明提供一种从含有目标金属的水性富液中回收目标金属的方法,所述方法包含:
(a)生物吸附步骤,其包含使微生物与所述水性富液接触以使得至少一部分所述目标金属生物吸附到所述微生物上,其中所述微生物满载金属,并且所述水性富液变成贫液;
(b)分离步骤,其包含将所述金属满载微生物与所述贫液基本上分离;和(c)回收步骤,其包含从所述金属满载微生物中回收所述目标金属。
优选地,水性富液含有超过1000ppm、或超过500ppm、或超过200ppm、或超过100ppm、或超过50ppm、或超过20ppm、或超过10ppm、或超过5ppm、或超过1ppm的目标金属。
优选地,水性富液含有介于约0.1ppm到1500ppm之间、或介于约0.1ppm到1000ppm之间、或介于约0.1ppm到500ppm之间、或介于约0.1ppm到200ppm之间、或介于约0.1ppm到100ppm之间、或介于约0.1ppm到50ppm之间、或介于约0.1ppm到20ppm之间的目标金属。优选地,水性富液含有介于约0.5ppm到1500ppm之间、或介于约0.5ppm到1000ppm之间、或介于约0.5ppm到500ppm之间、或介于约0.5ppm到200ppm之间、或介于约0.5ppm到100ppm之间、或介于约0.5ppm到50ppm之间、或介于约0.5ppm到20ppm之间的目标金属。优选地,水性富液含有介于约1ppm到1500ppm之间、或介于约1ppm到1000ppm之间、或介于约1ppm到500ppm之间、或介于约1ppm到200ppm之间、或介于约1ppm到100ppm之间、或介于约1ppm到50ppm之间、或介于约1ppm到20ppm之间的目标金属。
优选地,贫液含有少于0.1ppm、或少于1ppm、或少于2ppm、或少于5ppm、或少于10ppm、或少于20ppm、或少于50ppm、或少于100ppm的目标金属。优选地,贫液含有介于约0.001与100ppm之间、或介于约0.001与50ppm之间、或介于约0.001与50ppm之间、或介于约0.01与50ppm之间的目标金属。
优选地,水性富液含有比贫液多至少10倍的目标金属。优选地,水性富液含有比贫液多至少20倍、或至少40倍、或至少45倍、或至少50倍的目标金属。
优选地,金属满载微生物包括大于100ppm、或大于200ppm、或大于500ppm、或大于1000ppm、或大于30,00ppm的目标金属。
优选地,水性富液到微生物的目标金属的浓度系数大于5、或大于10、或大于20、或大于50、或大于100、或大于900。
优选地,在生物吸附步骤中,微生物与水性富液接触介于约0.5与48小时之间。优选地,介于约0.5与24小时之间,或介于约0.5与12小时之间,或介于约0.5与4小时之间,或介于约1与3小时之间。
在特定实施例中,目标金属为金。
优选地,生物吸附步骤在例如介于约15与30℃之间的环境温度下进行。
优选地,微生物为藻或细菌。优选地,微生物为革兰氏阴性(gram-negative)或革兰氏阳性(gram-positive)细菌。优选地,微生物属于假单胞菌属(pseudomonas)、埃希氏杆菌属(escherichia)、芽孢杆菌属(bacillus)、脱硫弧菌属(desulfovibrio)、织线藻属(plectonema)、贪铜菌属(cupriavidus)、梭菌属(clostridium)或代尔夫特菌属(delftia)。
优选地,微生物选自发现呈生理相关量的目标金属的环境。
优选地,其中目标金属为金,微生物选自耐金属贪铜菌(cupriavidusmetalliduran)、食酸戴尔福特菌(delftiaacidovoran)、绿脓杆菌(pseudomonasaeruginosa)、恋臭假单孢菌(p.putida)、脱硫弧菌(desulfovibriodesulfurican)、枯草杆菌(bacillussubtilis)或鲍氏织线藻(plectonemaboryanum)。
优选地,其中目标金属为金,微生物选自以生理相关浓度发现金的环境。优选地,微生物选自耐金属贪铜菌或食酸戴尔福特菌。
在某些实施例中,分离步骤包括以下中的至少一个:
将所述金属满载微生物与所述贫液重力分离并且去除所述贫液,
离心并且去除所述贫液;
从所述贫液中过滤所述金属满载微生物。
在某些实施例中,分离步骤包含将金属满载微生物与贫液重力分离,其中去除至少50%的贫液。
优选地,去除至少60%、或至少70%、或至少80%、或至少90%、或至少95%的贫液。
在某些实施例中,分离步骤包含通过离心分离金属满载微生物,其中在离心期间,从金属满载微生物中去除至少50%的贫液。优选地,在离心期间去除至少60%、或至少70%、或至少80%、或至少90%、或至少95%的贫液。
在某些实施例中,分离步骤包含通过过滤分离金属满载微生物,其中在过滤期间,从金属满载微生物中去除至少50%的贫液。优选地,在过滤期间去除至少60%、或至少70%、或至少80%、或至少90%、或至少95%的贫液。
在某些实施例中,分离步骤包括干燥微生物。
在某些实施例中,回收步骤包括使金属满载微生物与触发微生物基本上解吸附目标金属的条件接触。
优选地,所述条件为含有触发目标金属的解吸附的化合物的溶液。优选地,所述溶液含有半胱氨酸或硫代硫酸盐或硫脲中的一种或多种。另外或或者,所述条件触发目标金属(呈金属或离子形式)的解吸附。借助于实例,所述条件可为ph小于5、或ph小于4、或ph小于3、或ph小于2。或者,所述条件可为ph介于1与5之间,或ph介于2与5之间,或介于2与4之间。借助于其它实例,所述条件可为ph大于8、或ph大于9、或ph大于10、或ph大于11、或ph大于12。或者可为ph介于8与13之间,或ph介于9与13之间,或介于10与13之间。另外或或者,所述条件可处于适用于解吸附目标金属的氧化还原电位下。或者,回收步骤包括燃烧或化学溶解金属满载微生物以解吸附所述目标金属。
在一特定实施例中,富液除目标金属之外,还包括至少一种其它金属。优选地,微生物比生物吸附步骤中的其它金属优先生物吸附目标金属,并且其它金属在分离步骤中保留在贫液中。优选地,微生物比生物吸附步骤中的其它金属优先生物吸附目标金属以使得在与富液中的质量比相比时,微生物中目标金属与其它金属的质量比增加了至少2倍,优选地,质量比增加了至少3倍、或至少5倍、或至少8倍、或至少10倍、或至少20倍、或至少50倍、或至少100倍、或至少200倍。优选地,目标金属为金。优选地,其它金属选自铜和镍中的一种或多种。
在第二方面中,本发明提供一种回收目标金属的方法,所述方法包含:
(a)溶解步骤,其包含用浸滤剂溶解来自固体原料的所述目标金属以形成含有目标金属离子的水性富液;
(b)生物吸附步骤,其包含使微生物与所述水性富液接触以使得至少一部分所述目标金属离子生物吸附到所述微生物上,其中所述微生物满载金属,并且所述水性富液变成贫液;
(c)分离步骤,其包含将所述金属满载微生物与所述贫液基本上分离;和(d)回收步骤,其包含从所述金属满载微生物中回收所述目标金属。
优选地,水性富液含有超过1000ppm、或超过500ppm、或超过200ppm、或超过100ppm、或超过50ppm、或超过20ppm、或超过10ppm、或超过5ppm、或超过1ppm的目标金属。
优选地,水性富液含有介于约0.1ppm到1500ppm之间、或介于约0.1ppm到1000ppm之间、或介于约0.1ppm到500ppm之间、或介于约0.1ppm到200ppm之间、或介于约0.1ppm到100ppm之间、或介于约0.1ppm到50ppm之间、或介于约0.1ppm到20ppm之间的目标金属。优选地,水性富液含有介于约0.5ppm到1500ppm之间、或介于约0.5ppm到1000ppm之间、或介于约0.5ppm到500ppm之间、或介于约0.5ppm到200ppm之间、或介于约0.5ppm到100ppm之间、或介于约0.5ppm到50ppm之间、或介于约0.5ppm到20ppm之间的目标金属。优选地,水性富液含有介于约1ppm到1500ppm之间、或介于约1ppm到1000ppm之间、或介于约1ppm到500ppm之间、或介于约1ppm到200ppm之间、或介于约1ppm到100ppm之间、或介于约1ppm到50ppm之间、或介于约1ppm到20ppm之间的目标金属。
优选地,贫液含有少于0.1ppm、或少于1ppm、或少于2ppm、或少于5ppm、或少于10ppm、或少于20ppm、或少于50ppm、或少于100ppm的目标金属。优选地,贫液含有介于约0.001与100ppm之间、或介于约0.001与50ppm之间、或介于约0.001与50ppm之间、或介于约0.01与50ppm之间的目标金属。
优选地,水性富液含有比贫液多至少10倍的目标金属。优选地,水性富液含有比贫液多至少20倍、或至少40倍、或至少45倍、或至少50倍的目标金属。
优选地,金属满载微生物包括大于100ppm、或大于200ppm、或大于500ppm、或大于1000ppm、或大于30,000ppm的目标金属。
优选地,水性富液到微生物的目标金属的浓度系数大于5、或大于10、或大于20、或大于50、或大于100、或大于900。
优选地,在生物吸附步骤中,微生物与水性富液接触介于约0.5与48小时之间。优选地,介于约0.5与24小时之间,或介于约0.5与12小时之间,或介于约0.5与4小时之间,或介于约1与3小时之间。
在特定实施例中,目标金属为金。
在某些实施例中,固体原料包含固体材料,其包含少于5%、或少于1%、或少于0.1%、或少于0.01%、或少于0.001%、或少于0.0001%的目标金属。在某些实施例中,固体原料为矿石、来自例如开采的工业过程的尾矿或废料、砂石、粘土、例如电子废料的废料中的任何一种或多种
在某些实施例中,溶解步骤和生物吸附步骤可能存在于相同容器中。
在某些实施例中,当目标金属为金时,优选地,固体原料为电子废料、或含金矿石、或含金砂石、或含金粘土。
在一特定实施例中,富液除目标金属之外,还包括至少一种其它金属。优选地,微生物比生物吸附步骤中的其它金属优先生物吸附目标金属,并且其它金属在分离步骤中保留在贫液中。优选地,微生物比生物吸附步骤中的其它金属优先生物吸附目标金属以使得在与富液中的质量比相比时,微生物中目标金属与其它金属的质量比增加了至少2倍,优选地,质量比增加了至少3倍、或至少5倍、或至少8倍、或至少10倍、或至少20倍、或至少50倍、或至少100倍、或至少200倍。优选地,目标金属为金。优选地,其它金属选自铜和镍中的一种或多种。
在某些实施例中,浸滤剂溶液为硫脲类溶液、或硫代硫酸盐类溶液、或硫氰酸盐类溶液、或氰化物类溶液、或卤素类溶液、或王水类溶液。
在某些实施例中,分离步骤包括以下中的至少一个:
将所述金属满载微生物与所述贫液重力分离并且去除所述贫液,
离心并且去除所述贫液;
从所述贫液中过滤所述金属满载微生物。
在某些实施例中,分离步骤包含将金属满载微生物与贫液重力分离,其中去除至少50%的贫液。
优选地,去除至少60%、或至少70%、或至少80%、或至少90%、或至少95%的贫液。
在某些实施例中,分离步骤包含通过离心分离金属满载微生物,其中在离心期间,从金属满载微生物中去除至少50%的贫液。优选地,在离心期间去除至少60%、或至少70%、或至少80%、或至少90%、或至少95%的贫液。
在另一实施例中,分离步骤包含通过过滤分离金属满载微生物,其中在过滤期间,从金属满载微生物中去除至少50%的贫液。优选地,在过滤期间去除至少60%、或至少70%、或至少80%、或至少90%、或至少95%的贫液。
在某些实施例中,分离步骤包括干燥微生物。
可能需要额外分离步骤以将金属满载微生物与贫液和剩余固体原料分离。
在某些实施例中,回收步骤包括使金属满载微生物与触发微生物基本上解吸附目标金属的条件接触。
优选地,所述条件为含有触发目标金属的解吸附的化合物的溶液。优选地,所述溶液含有半胱氨酸或硫代硫酸盐或硫脲中的一种或多种。另外或或者,所述条件触发目标金属(呈金属或离子形式)的解吸附。借助于实例,所述条件可为ph小于5、或ph小于4、或ph小于3、或ph小于2。或者,所述条件可为ph介于1与5之间,或ph介于2与5之间,或介于2与4之间。借助于其它实例,所述条件可为ph大于8、或ph大于9、或ph大于10、或ph大于11、或ph大于12。或者可为ph介于8与13之间,或ph介于9与13之间,或介于10与13之间。另外或或者,所述条件可处于适用于解吸附目标金属的氧化还原电位下。
或者,回收步骤包括燃烧或化学溶解金属满载微生物以解吸附目标金属。
在第三方面,提供通过第一和/或第二方面的方法回收的目标金属。优选地,所述金属为金。
在第四方面,提供一种用于从含有目标金属的水性富液中回收目标金属的系统,所述系统包含:
(a)容器,其配置成使微生物与所述水性富液接触以使得至少一部分所述目标金属生物吸附到所述微生物上,其中所述微生物满载金属,并且所述水性富液变成贫液;
(b)分离器,其配置成将所述金属满载微生物与所述贫液基本上分离;和(c)回收构件,其配置成从所述金属满载微生物中回收所述目标金属。
在某些实施例中,所述系统包括用于将含有金属满载微生物的贫液从(a)中的容器传递到(b)中的分离器的构件。在某些实施例中,所述系统包括用于将(b)中的金属满载微生物传递到(c)中的回收构件的构件。
在某些实施例中,分离器包含以下中的至少一个:
用于将金属满载微生物与贫液重力分离的构件,其中至少一部分贫液从金属满载微生物中去除,
用于通过离心分离金属满载微生物的构件,其中至少一部分贫液从金属满载微生物中去除;
用于通过过滤分离金属满载微生物的构件,其中至少一部分贫液从金属满载微生物中去除。
在某些实施例中,分离器包含用于将金属满载微生物与水性贫液重力分离并且去除至少一部分贫液的构件。
在某些实施例中,分离器包含用于通过离心分离金属满载微生物的构件,其中至少一部分贫液从金属满载微生物中去除。
在某些实施例中,分离器包含用于通过过滤分离金属满载微生物的构件,其中至少一部分贫液从金属满载微生物中去除。
在某些实施例中,回收构件包括用于使金属满载微生物与溶液接触的元件。
在某些实施例中,回收构件包括用于燃烧金属满载微生物以释放目标金属的元件。
在第五方面,提供用于从固体原料中回收目标金属的系统,所述系统包含:
(a)容器,其配置成用浸滤剂溶解来自固体原料的目标金属以形成含有所述目标金属的水性富液;
(b)容器,其配置成使微生物与所述水性富液接触以使得至少一部分所述目标金属生物吸附到所述微生物上,其中所述微生物满载金属,并且所述水性富液变成贫液;
(c)分离器,其配置成将所述金属满载微生物与所述贫液基本上分离;和(d)回收构件,其配置成从所述金属满载微生物中回收所述目标金属。
在某些实施例中,所述系统包括用于将水性富液从(a)中的容器传递到(b)中的容器的构件。在某些实施例中,(a)中所用的容器可能与(b)中所用的容器相同。在某些实施例中,所述系统包括将含有金属满载微生物的贫液从(b)中的容器传递到(c)中的分离器的构件。在某些实施例中,所述系统包括将(c)中的金属满载微生物传递到(d)中的回收构件的构件。
在某些实施例中,分离器包含用于将金属满载微生物与贫液重力分离并且倾析至少一部分贫液的构件。
在某些实施例中,分离器包含以下中的至少一个:
用于将金属满载微生物与贫液重力分离的构件,其中至少一部分贫液从金属满载微生物中去除,
用于通过离心分离金属满载微生物的构件,其中至少一部分水性贫液从金属满载微生物中去除;
用于通过过滤分离金属满载微生物的构件,其中至少一部分贫液从金属满载微生物中去除。
在某些实施例中,回收构件包括用于使金属满载微生物与溶液接触的构件。
在某些实施例中,回收构件包括用于燃烧金属满载微生物以释放目标金属的构件。
优选地,微生物为藻或细菌。优选地,微生物为革兰氏阴性或革兰氏阳性细菌。优选地,微生物属于假单胞菌属、埃希氏杆菌属、芽孢杆菌属、脱硫弧菌属、织线藻属、贪铜菌属、梭菌属或代尔夫特菌属。
优选地,微生物选自发现呈生理相关量的目标金属的环境。
广泛地说,本发明还可以在于单独地或共同地在本申请的说明书中提及或指示的部分、要素和特征,呈两个或更多个所述部分、要素或特征中的任何或所有组合形式,并且当具有本发明所涉及的领域中的已知等效物的特定整体在本文中被提到时,所述已知等效物被认为如单独地进行阐述一般并入本文中。
附图说明
本发明的这些和其它方面(应被视为在所有其新颖方面中)将从以下仅借助于实例给出的描述参考附图而变得显而易见,在所述附图中:
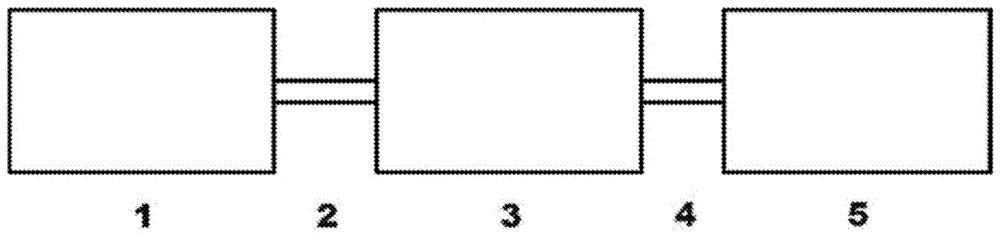
图1表示配置成根据本发明的第四方面从水性富液中回收目标金属的系统。
图2表示配置成根据本发明的第五方面从固体原料中回收目标金属的系统。
具体实施方式
定义
术语“目标金属”包括元素金属和特定目标金属的离子或多种特定金属。可以认识到,在本发明的方法或系统的不同部分中,特定的目标金属可以不同的离子状态(包括元素形式)或多个离子状态存在。目标金属可以呈离子(或多个离子)、盐或络合物或元素形式或其组合溶解或部分溶解于本发明的水溶液中。类似地,目标金属可以呈如上下文指示的离子(或多个离子)、盐或络合物或元素形式或其组合呈固体形式存在。
术语“水性富液”是指含有溶解的目标金属的水溶液。在一些极端例子中,水性富液还可含有至少一些未溶解的目标金属。
术语“贫液”是指与水性富液相比,含有耗尽量的溶解的目标金属的水溶液。认为在极端的情况下,目标金属可在贫液中完全缺失。
术语“接触”是指在两种或更多种溶液或物质之间混合和相互作用。这个的一个实例是水性富液与微生物之间的接触。这个的另一个实例是浸滤剂与固体原料之间的接触。
术语“生物吸附(biosorb)”和“生物吸附剂(biosorbent)”以及“生物吸附(biosorption)”以及其类似术语在与本发明的方法和系统相关地使用时是指用于吸附(adsorb/adsorp)或吸收金属的微生物或金属吸附(adsorbing/adsorping)或吸收到微生物的方法。
术语“原料”是指正在处理的输入材料。
术语“固体原料”是指可为用于处理的输入的各种金属来源的固态性质。实例包括开采矿石、尾矿和电子废料。
术语“微生物”是指藻、或细菌、或真菌、或原生生物(protoctist)、或古细菌。其可以多种意义用于微生物的混合物。
术语“金属满载微生物”意味已生物吸附一种或多种目标金属的微生物。
术语“ppm”是指百万分之一,并且涉及与另一底物相比底物的浓度。其是指两种底物之间的重量:重量比。对于水溶液,ppm和mg/l大致等效。
术语“rcf”意味相对离心力。
术语“倾析”或“倾析”或其类似术语是指从已使固体洗脱份沉降的固体/水性混合物中去除水溶液的上部部分。
术语“浸滤剂”是指能够将目标金属溶解成水性形式的水溶液。
术语“电子废料”是指电子废料或废弃电子电机设备(通常称为weee)。
“系统”包含通常将用于允许从原料中提取金属的管道和其它零件。借助于实例,“系统”可包括容器、导管、泵、压力阀、热交换器、过滤器、仪器(压力传感器、流量传感器、ph传感器)和混合球座(tee)(静态混合器)。
讨论
虽然以下描述关注本发明的特定实施例,即从水性富液或固体原料中回收金,但是应了解,本发明可适用于制造如将由所属领域的一般技术人员已知的本发明涉及的替代目标金属。
如上文所讨论,本发明人设计用于从含有金属离子的水溶液和/或固体原料中回收金属的方法。具体地说,本发明提供用于以比起现有方法具有多个成本和环境优势的方式从水溶液中回收金属的方法。
在本发明的一特定方面,提供一种从含有目标金属的水性富液中回收目标金属的方法,所述方法包含:
(a)生物吸附步骤,其包含使微生物与所述水性富液接触以使得至少一部分所述目标金属生物吸附到所述微生物上,其中所述微生物满载金属,并且所述水性富液变成贫液;
(b)分离步骤,其包含将所述金属满载微生物与所述贫液基本上分离;和(c)回收步骤,其包含从所述金属满载微生物中回收所述目标金属。
图1展示本发明的一实施例,在所述实施例中微生物在生物吸附容器1中与含有目标金属离子的水性富液接触。本发明对于浓缩目标金属离子的稀释流具有特定效用,因此在一些实施例中,水性富液含有超过1000ppm、或超过500ppm、或超过200ppm、或超过100ppm、或超过50ppm、或超过20ppm、或超过10ppm、或超过5ppm、或超过1ppm的目标金属。优选地,水性富液含有介于约0.1ppm到1500ppm之间、或介于约0.1ppm到1000ppm之间、或介于约0.1ppm到500ppm之间、或介于约0.1ppm到200ppm之间、或介于约0.1ppm到100ppm之间、或介于约0.1ppm到50ppm之间、或介于约0.1ppm到20ppm之间的目标金属。优选地,水性富液含有介于约0.5ppm到1500ppm之间、或介于约0.5ppm到1000ppm之间、或介于约0.5ppm到500ppm之间、或介于约0.5ppm到200ppm之间、或介于约0.5ppm到100ppm之间、或介于约0.5ppm到50ppm之间、或介于约0.5ppm到20ppm之间的目标金属。优选地,水性富液含有介于约1ppm到1500ppm之间、或介于约1ppm到1000ppm之间、或介于约1ppm到500ppm之间、或介于约1ppm到200ppm之间、或介于约1ppm到100ppm之间、或介于约1ppm到50ppm之间、或介于约1ppm到20ppm之间的目标金属。
根据本发明的方法,在某些实施例中,含有目标金属离子的浸滤剂溶液充当水性富液。借助于非限制性实例,当金为目标金属时,水性富液可通过将目标金属溶解于硫脲类溶液、或硫代硫酸盐类溶液、或硫氰酸盐类溶液、或氰化物类溶液、或卤素类溶液、或王水类溶液中而制得,并且合适条件的实例可见于aylmore,《矿物加工发展(developmentsinmineralprocessing)》15,第501-539页(2005)中。
在与富液接触时,微生物生物在生物吸附至少50%的目标金属所必要的一时间段内吸附目标金属。在特定实施例中,微生物与水性富液接触以使得生物吸附至少60%、或至少70%、或至少80%、或至少90%、或至少95%的目标金属。时间段优选介于约0.5与48小时之间、或介于约0.5与24小时之间、或介于约0.5与12小时之间、或介于约0.5与4小时之间、或介于约1与3小时之间。
在本发明的一特别优选实施例中,比起富液中的其它金属,微生物优先生物吸附目标金属。在分离步骤中其它金属随后与目标金属分离,同时其它金属保留在贫液中。实例7和8展示生物吸附步骤的优先性质。优先生物吸附的系数将部分地视富液中金属的比率而定,例如如果其已经呈类似量,那么质量比可能不会改变地与存在过量很多的其它金属的情况一样多。然而,优选地,在生物吸附步骤中比起其它金属,微生物优先生物吸附目标金属,以使得与生物吸附到微生物上的其它金属的目标金属的比率相比,富液中目标金属与其它金属的质量比增加了至少2倍、或至少3倍、或至少5倍、或至少8倍、或至少10倍、或至少20倍、或至少50倍、或至少100倍、或至少200倍。比率的增量的上限将部分地视起始比率而定,但可为1,000或更高。优选地,目标金属为金。优选地,其它金属选自铜和镍中的一种或多种。
多种微生物能够生物吸附金属离子。微生物优选为藻或细菌,优选为革兰氏阴性或革兰氏阳性细菌,例如来自假单胞菌属、埃希氏杆菌属、芽孢杆菌属、脱硫弧菌属、织线藻属、贪铜菌属、梭菌属或代尔夫特菌属。微生物优选地选自以生理相关量,例如低于0.5ppm发现目标金属的环境。能够生物吸附金属离子的微生物的实例包括革兰氏阴性细菌绿脓杆菌和大肠杆菌(escherichiacoli)、革兰氏阳性细菌枯草杆菌和真菌酿酒酵母(saccharomycescerevisiae)。以引用的方式并入本文中的nancharaiah等人(《生物技术趋势(trendsinbiotechnology)》34,第137-155页(2016))鉴别出广泛范围的微生物,其可用于根据本发明的方法生物吸附目标金属。大多数生物吸附事件在性质上为吸附性的(即金属离子通过与细胞壁或膜部分被动相互作用而与微生物的表面结合),但一些为吸收性的(即,金属离子通过微生物积极地内化)。
在目标金属离子为金的特定实施例中,例如革兰氏阴性细菌绿脓杆菌、恋臭假单孢菌和脱硫弧菌、革兰氏阳性细菌枯草杆菌和/或鲍氏织线藻的微生物已展示生物吸附金(reith等人,《国际微生物生态学会杂志(internationalsocietyformicrobialecologyjournal)》1,第567-584页(2007))。在某些优选实施例中,微生物选自以生理相关浓度发现金的环境,所述微生物例如革兰氏阴性细菌耐金属贪铜菌和食酸戴尔福特菌(rea等人,《欧洲微生物学会联合会微生物生态学(femsmicrobiologyecology)》92,第fiw082页(2016))。在其它优选实施例中,微生物选自其它工业过程中使用的那些,所述微生物例如革兰氏阳性细菌自产乙醇梭菌(clostridiumautoethanogenum)(abrini等人,《微生物学档案(archmicrobiol)》161,第345-351页(1994))。
在用于本发明而非环境中时,微生物一般为单一培养或至少两种到五种微生物的有限混合物。此外,在天然环境中,微生物一般仅暴露于低含量,例如少于0.5ppm的目标金属。在本发明的优选实施例中,富液含有相对高的量,例如大于0.5ppm或大于1ppm的目标金属。因此,出人意料地,微生物仍然具有生物吸附较高含量的目标金属的能力。另外或或者,出人意料地,微生物能够在相对较短时间段,例如少于12小时内生物吸附目标金属,即使在目标金属呈低或更高浓度时。
本发明人发现耐金属贪铜菌(cupriavidusmetallidurans/c.metallidurans)在本发明中在金为目标金属时尤其适用。本发明人发现耐金属贪铜菌相对易于生长,在生物吸附金下良好和/或相对快速地生物吸附目标金属和/或对优先生物吸附金有好处(参见实例7和8)和/或对富液中存在的其它金属具有相对耐受性。
在目标金属离子为金并且水性富液为硫代硫酸盐类溶液、或氰化物类溶液、或氯化物类溶液的特定实施例中,耐金属贪铜菌可用于分别生物吸附硫代硫酸金络合物或氰化亚金(aurocyanide)或氯金酸盐(reith等人,pnas106,第17757-17762页(2009);etschmann等人,《化学地质(chemicalgeology)》438,第103-111页(2016))。
在至少部分生物吸附目标金属离子时,溶液变成贫液,其中贫液含有比富液少的目标金属。在特定实施例中,贫液含有少于0.1ppm、或少于1ppm、或少于2ppm、或少于5ppm、或少于10ppm、或少于20ppm、或少于50ppm、或少于100ppm的目标金属。优选地,贫液含有介于约0.001与100ppm之间、或介于约0.001与50ppm之间、或介于约0.001与50ppm之间、或介于约0.01与50ppm之间的目标金属。在特定实施例中,水性富液比贫液含有多至少10倍的目标金属。优选地,水性富液含有比贫液多至少20倍、或至少40倍、或至少45倍、或至少50倍的目标金属。
已确认,微生物可在与水性富液在生物吸附容器1中接触之前由所属领域的技术人员熟悉的任何方法在分离容器中培养。借助于实例,微生物可在含有合适生长介质的生物反应器(未图示)中培养,并且转移到生物吸附容器1中。微生物可在不经进一步浓缩就直接转移或传递之前浓缩。在某些实施例中,微生物通过重力分离浓缩并且传递到生物吸附容器1中在最小体积的生长介质中作为浓缩微生物浆料。在一相关实施例中,浓缩微生物浆料可在传递到生物吸附容器1中之前在另一种溶液中洗涤。
在某些实施例中,微生物在富集液体介质(例如,营养肉汤或胰蛋白酶大豆肉汤)中培养直到达到生长的中期或静止期。
参看图1,在至少部分生物吸附目标金属时,在分离模组3中将金属满载微生物与贫液分离。预期,分离步骤的初始部分可能在与生物吸附步骤相同的容器中进行,其中仅仅通过重力分离使金属满载微生物浓缩。在其它实施例中,通过用于分离的导管构件2将金属满载微生物和贫液传递到分离模组3中。用于将微生物与贫液分离的构件的实例将对所属领域的技术人员而已是熟悉的。然而,借助于实例,金属满载微生物可通过重力分离、离心、过滤或其组合分离,以使得在各情况下贫液从金属满载微生物中去除。
应将提及基本上分离视为意味着将至少一部分贫液与金属满载微生物物理分离。物理分离涉及使其在分开的不接触位置,例如分离容器而非相同容器的接触层中。
在特定实施例中,在生物吸附容器1或分离模组3中,金属满载微生物与贫液在一时间段内重力分离。在重力分离后,至少一部分贫液可倾析、虹吸或者去除,静置浓缩金属满载微生物,其可传递到回收模组5中以进行回收步骤。
在某些实施例中,分离步骤包含将金属满载微生物与贫液重力分离,其中去除至少50%的贫液。优选地,去除至少60%、或至少70%、或至少80%、或至少90%、或至少95%的贫液。借助于实例,微生物的溶液可通过重力静置至沉降至多2小时、或至多6小时、或至多12小时、或至多24小时、或至多48小时、或至多72小时,随后去除贫液。
在一替代性实施例中,可通过离心在分离模组3中将金属满载微生物与贫液分离,并且去除贫液。熟悉所属领域的技术人员将认识到用于将贫液与金属满载微生物分离所必要的适当条件和设备,所述以下分离可通过导管构件4传递到回收模组5中。
在某些实施例中,分离步骤包含通过离心分离金属满载微生物,其中在离心期间,从金属满载微生物中去除至少50%的水性贫液。优选地,在离心期间去除至少60%、或至少70%、或至少80%、或至少90%、或至少95%的贫液。
所属领域的技术人员将认识到离心机的操作视所处理的液体体积和所需分离速率而定。还存在多种可与本发明的方法和系统一起采用的离心系统,包括合适的连续流离心或倾析式离心装置。
在另一实施例中,可通过过滤在分离模组3中将金属满载微生物与贫液分离。熟悉所属领域的技术人员将认识到用于将贫液与金属满载微生物分离所必要的适当条件和设备,所述以下分离可通过导管构件4传递到回收模组5中。
在某些实施例中,分离步骤包含通过过滤分离金属满载微生物,其中在过滤期间,从金属满载微生物中去除至少50%的贫液。优选地,在过滤期间去除至少60%、或至少70%、或至少80%、或至少90%、或至少95%的贫液。
作为一实例,含有金属满载微生物的溶液可通过孔径为大约0.45μm、或大约0.65μm、或大约0.8μm、或大约1μm的过滤器在真空下过滤以去除贫液。作为另一实例,交叉流过滤装置或膜生物反应器装置可用于去除贫液。
分离步骤由于多种原因是重要的。分离步骤从富液中的其它组分中去除金属满载微生物,并且因此去除金属。富液中的其它组分可为毒性或腐蚀性的,例如氰化物或酸。分离步骤还使目标金属浓缩。在分离步骤后,干燥的金属满载微生物优选地包括大于100ppm、或大于200ppm、或大于500ppm、或大于1000ppm、或大于30,00ppm的目标金属。本发明人进一步展示富液到分离的微生物的目标金属的显著浓度系数。水性富液到微生物的目标金属的浓度系数(即,在富液中更浓缩的目标金属在微生物中的倍数)大于5、或大于10、或大于20、或大于50、或大于100、或大于900。举例来说,实例1展示富液到微生物的目标金属的浓度系数为990。湿微生物生物质量通常估计是其干质量的五倍,即干质量为湿质量的约20%(luria,《细菌(thebacteria)》,第1卷.纽约学术出版社(academicpress,inc.,newyork),第1-34页(1960))。因此,如实例1和5中所使用的,对湿微生物生物质量计算的金属浓度系数可以乘以五倍以估计干燥微生物的浓度系数。实例8中例示微生物的干燥。这种浓度是重要的,因为例如尽管在湿法冶金中使用浸出剂来提取金属,但仍必须从浸滤剂中回收金属。
分离步骤可在一些情况下也使金属选择性分离和/或浓缩,例如,实例7证实优先生物吸附,并且随后将金与铜分离和/或浓缩。金选择性生物吸附到微生物上,以使得在分离步骤中将生物吸附到微生物上的金与贫液中的铜分离。
熟悉所属领域的技术人员将认识到用于从回收模组5中的金属满载微生物中回收目标金属的合适回收构件。然而,借助于非限制性实例,金属可通过改变微生物的条件从金属满载微生物中解吸附。举例来说,在本发明的某些实施例中,金属可通过改变微生物的ph,例如通过使微生物与含有酸或碱的溶液接触从金属满载微生物中解吸附。在这类实施例中,微生物将与具有特定ph的液体接触以引发目标金属解吸附到液体中。在特定实施例中,接触液体的ph为比贫液高的ph,而在其它实施例中,ph较低——视系统的特征而定。
借助于实例,所述条件可为ph小于5、或ph小于4、或ph小于3、或ph小于2。借助于其它实例,所述条件可为ph大于8、或ph大于9、或ph大于10、或ph大于11、或ph大于12。
在一替代性实施例中,金属满载微生物可与含有化合物的液体接触以引发目标金属解吸附到液体中。借助于实例,在某些实施例中可使用水性半胱氨酸以引发目标金属的解吸附。在目标金属为金的某些实施例中,大约0.3mm、或大约1mm、或大约10mm、或大约30mm、或大约60mm半胱氨酸溶液可与金属满载微生物接触(kenney等人,《地球化学与宇宙化学学报(geochimicaetcosmochimicaacta)》82,第51-60页(2012))。在一相关实施例中,水性硫代硫酸盐、硫脲、硫氰酸盐、氰化物或其它硫醇配体可用于引发金与微生物解吸附。如实例10中所示,氯气可用于改变条件。另外或或者,例如氧化还原电位或温度的变化的其它条件可用于促进目标金属的解吸附。
浓缩溶液可随后经历分离和纯化程序,例如沉淀杂质、溶剂提取、吸附和离子交换以使目标金属分离和/或进一步浓缩。随后,溶液可通过用于目标金属回收的电精炼工艺、化学还原或结晶或所属领域的技术人员将了解的其它方法来处理。
在一替代性实施例中,可将分离的金属满载微生物干燥并且燃烧以回收目标金属,使用所属领域的技术人员已知的常规火法冶金或湿法冶金技术可将所述目标金属与灰渣分离(hennebel等人,《新生物技术(newbiotechnology)》32,第121-127页(2015))。
很明显,回收步骤可回收呈金属或离子形式的目标金属。提及回收目标金属因此应视为包括回收金属金属或金属离子。
在本发明的方法和系统的特定实施例中,目标金属为金。在这类实施例中,分离的金满载微生物可在环境温度或30℃或50℃下干燥以使含水量最小化,并且随后例如通过气焊焊炬焚烧,从而逐渐使所产生灰渣的损失最小化。这种灰渣可随后用硝酸处理成可溶基本金属,过滤,并且含金残余物用王水(1份硝酸到3份盐酸)处理以产生氯金酸的溶液。在一相关实施例中,金满载微生物可能直接经历前述酸处理而不需要先前焚烧。可使用具有所属领域的普通知识的人员已知的方法从氯金酸中沉淀和熔炼金。
根据本发明的另一方面,提供一种回收目标金属的方法,所述方法包含:
(a)溶解步骤,其包含用浸滤剂溶解来自固体原料的目标金属以形成含有目标金属的水性富液;
(b)生物吸附步骤,其包含使微生物与所述水性富液接触以使得至少一部分所述目标金属离子生物吸附到所述微生物上,其中所述微生物满载金属,并且所述水性富液变成贫液;
(c)分离步骤,其包含将所述金属满载微生物与所述贫液基本上分离;和
(d)回收步骤,其包含从所述金属满载微生物中回收所述目标金属。
参看图2,通过与适当的浸滤剂接触,可将目标金属从固体原料中选择性溶解于溶解容器6中。所属领域的技术人员应了解用于选择性溶解特定目标金属的合适的浸滤剂。借助于非限制性实例,当金为目标金属时,浸滤剂可选自硫脲类溶液、或硫代硫酸盐类溶液、或硫氰酸盐类溶液、或氰化物类溶液、或卤素类溶液、或王水类溶液,并且合适条件的实例可见于aylmore,《矿物加工的发展(developmentsinmineralprocessing)》15,第501-539页(2005)中。
在特定实施例中,固体原料与浸滤剂接触溶解至少50%的目标金属、或至少60%的目标金属、或至少70%的目标金属、或至少80%的目标金属、或至少90%的目标金属、或至少95%的目标金属所必要的一段时间以产生水性富液。在特定实施例中,固体原料/浸滤剂混合物可能需要逐渐加热到超过30℃、或超过40℃、或超过50℃以帮助溶解。类似地,可搅动、超声波处理、振动或以其它方式处理混合物以帮助溶解。
固体原料可以是包含目标金属残余物的任何材料。借助于实例,固体原料可包含带有目标金属的金属矿石、砂、粘土、残余物或废料。借助于非限制性实例,在目标金属为金的本发明的某些实施例中,固体原料为从金开采过程或来自电子废料的印刷电路板中提取的金矿石。在某些实施例中,在与浸滤剂接触之前,可至少部分或完全地碾磨固体原料。然而,在所有情况下这可能始终没有必要,例如将目标金属表面涂布到固体原料上的实施例。
在某些实施例中,固体原料包含固体材料,其包含少于5%、或少于1%、或少于0.1%、或少于0.01%、或少于0.001%、或少于0.0001%的目标金属。在特定实施例中,目标金属为金。
在固体原料为金矿石或电子废料金的某些实施例中,浸滤剂可选自硫脲类溶液、或硫代硫酸盐类溶液、或硫氰酸盐类溶液、或氰化物类溶液、或卤素类溶液、或王水类溶液,并且合适条件的实例可见于aylmore,《矿物加工的发展》15,第501-539页(2005)中。
参看图2,当在溶解容器6中将目标金属至少部分溶解于浸滤剂中时,通过导管构件7将水性富液传递到生物吸附容器1中,其中可完成先前描述的生物吸附-分离-回收方法。所属领域的技术人员将认识到溶解容器6和生物吸附容器1可视所用方法和条件而为相同容器或不同容器。在本发明的特定实施例中,溶解容器6和生物吸附容器1为分离容器。
除非另外指示,否则本文所述的方法中所述的步骤顺序是极为优选的,并且已通过由本发明人进行的试验优化,以确保所述方法提供有效产率和经济上可行的回收方法。
实例
实例1生物吸附溶解于王水中的金
材料和方法:
根据无菌条件生长微生物培养物,但随后使用非无菌溶液和设备进行处理。
1.在30℃,约200rpm下将25ml的营养肉汤(0.5%蛋白胨,0.3%酵母提取物)用耐金属贪铜菌菌株ch34(莱布尼兹研究所(deutschesammlungvonmikroorganismenundzellkulturengmbh)#2839)接种,并且生长至少16小时到静止期。
2.将培养物在3,100rcf下离心15分钟,丢弃上清液,并且将丸粒(约0.1g)再悬浮于30ml的0.1m高氯酸钠中以洗涤。再次用10ml体积重复这一离心/洗涤步骤。
3.再次如上离心培养物,丢弃上清液,并且将丸粒再悬浮于25ml的0.1m高氯酸钠、25μm氯金酸(约5ppmau)中,ph为4(用氢氧化钠调节)(富液)。检查金/微生物混合物的ph,并且根据需要使用氢氧化钠或盐酸调节到4.0-4.5。
4.在室温下培育金/微生物混合物2小时。为将微生物保持在悬浮液中,始终在定轨振荡器上轻轻搅动混合物。
5.按照步骤2离心混合物,丢弃上清液(贫液),并且将丸粒储存在4℃下。
6.将来自步骤5的丸粒(生物吸附丸粒)(大约100μl体积)再悬浮于100ml水中,添加1ml的70%硝酸,并且随后通过电感耦合等离子体质谱分析(由新西兰奥克兰水力公司(watercareservicesltd,auckland,newzealand)提供的服务)分析金总含量。
结果:
在生物吸附时段(步骤4)结束时,检查混合物的ph,并且发现其处于4.5-5.0之间。
按为分析所提供的体积计,金总含量以mg/l为单位报导,并且用于计算生物吸附的量和生物吸附产率(表1)。金总含量的精确度估计在15-20%变化。
表1
按生物吸附的金的量计,富液含有比贫液多约4倍的目标金属(金)。
使用表1中的数据,反算留在贫液上清液中的金的浓度为约1ppm([0.125mg-0.099mg]/0.025l)。还使用约100μl(表2)的初始生物吸附丸粒体积计算生物吸附过程的浓度系数,即富液到生物吸附丸粒(湿的微生物)中的au的浓度的增量。湿的微生物生物质量通常估计是其干质量的五倍,即干质量为湿质量的约20%(luria,《细菌》,第1卷.纽约学术出版社,第1-34页(1960))。因此,这接近富液到干燥微生物的约990的au的浓度系数。
表2
实例2氯化金的生物吸附和解吸附
材料和方法:
根据无菌条件生长微生物培养物,但随后使用非无菌溶液和设备进行处理。
1.在30℃,约200rpm下将600ml的胰蛋白酶大豆肉汤(1.7%胰蛋白胨、0.3%大豆蛋白胨、0.25%葡萄糖、0.5%氯化钠、0.25%磷酸二钾)用枯草杆菌菌株(ehrenberg1835)cohn1872(新西兰兰德瑞研究有限公司(landcareresearchnewzealandltd)#20567)或恋臭假单孢菌菌株(trevisan1889)migula(新西兰兰德瑞研究有限公司#15057)接种,并且生长至少16小时到静止期。
2.在2,500rcf下使每种培养物离心10分钟,丢弃上清液,并且将丸粒再悬浮于300ml的水中。第二次重复这一离心/洗涤步骤。
3.再次如上离心每种培养物,丢弃上清液,并且将丸粒再悬浮于20ml的0.1m高氯酸钠中。第二次重复这一离心/洗涤步骤。
4.再次如上离心每种培养物,丢弃上清液,并且称重丸粒的湿质量。将每种丸粒再悬浮于0.1m高氯酸钠中,得到250g/l浓度。
5.向ph为4(用氢氧化钠调节)的117.5ml的25μm氯金酸(约5ppmau)(富液)中添加2.4ml的250g/l微生物溶液,得到微生物在120ml中的最终浓度为约5g/l。这分别对枯草杆菌和恋臭假单孢菌进行。检查金/微生物混合物的ph,并且根据需要使用氢氧化钠或盐酸调节到3.0-4.0。
6.在30℃下培育每种金/微生物混合物2小时。为将微生物保持在悬浮液中,始终在定轨振荡器上轻轻搅动每种混合物。
7.按照步骤2离心每种混合物,倾析上清液(贫液),并且储存在4℃下。
8.将每种丸粒再悬浮于7ml的上清液中,添加0.11g的l-半胱氨酸盐酸盐一水合物,并且用1mnaoh将ph调节到7.9-8.1。每种混合物顶部有上清液,最终体积为10ml,得到约62mm的半胱氨酸浓度。
9.按照步骤6在30℃下培育每种半胱氨酸/金/微生物混合物2小时。
10.按照步骤2离心每种混合物,并且倾析上清液。将上清液和丸粒储存在4℃下。
11.通过电感耦合等离子体质谱分析(由新西兰奥克兰水力公司提供的服务)分析以下枯草杆菌和恋臭假单孢菌样品的金总含量:
a.贫液上清液(步骤7):100ml,添加1ml的70%硝酸。
b.解吸附上清液(步骤10):用水将7ml补足到100ml(稀释约14.3倍),添加1ml的70%硝酸。
结果:
来自600ml的枯草杆菌培养物的洗涤丸粒的湿质量为3g,并且因此再悬浮于12ml0.1m高氯酸钠中,得到250g/l浓度;对于恋臭假单孢菌,质量和再悬浮液分别为2.6g和10.4ml。
在生物吸附时段(步骤6)结束时,检查每种混合物的ph,并且发现其处于3.0-4.0之间。
按为分析所提供的体积计,金总含量以mg/l为单位报导,并且用于计算生物吸附或解吸附的量和与金输入质量相比时的产率(表3)。金总含量的精确度估计在15-20%变化。
表3
对于枯草杆菌,富液含有比贫液多约49倍的目标金属。对于恋臭假单孢菌,富液含有比贫液多约16倍的目标金属。
表3中的结果示出枯草杆菌和恋臭假单孢菌两者都从富液中生物吸附大于90%的金。在回收步骤(步骤8-10)后,发现使用半胱氨酸条件,恋臭假单孢菌容易地解吸附金。使用半胱氨酸条件,枯草杆菌较不容易释放金,但认为如果需要,其它条件可用以提高回收率。
使用这些结果,使用体积为10ml的解吸附上清液计算来自生物吸附过程的浓度系数(表4)。在这个实例中,浓度系数为富液到所回收au(即,解吸附上清液)的浓度变化。枯草杆菌的更低值归因于上文所论述的较低解吸附速率而不是生物吸附步骤。
表4
实例3:金溶解浸滤剂
材料和方法:
从新西兰科罗曼德尔地区(coromandelregion,newzealand)的矿场获得含有约16ppmau和约260ppmag的带有金的石英矿石的样品(研磨到<100μm粒度)。从丢弃的台式计算机中收集印刷电路板,并且从板中切下具有镀金连接器销钉的部分,并且用作模型电子废料原料。
1.用于金的浸滤剂溶液按照以下制备:
a.硫代硫酸盐类浸滤剂:0.2m硫代硫酸钠五水合物,0.4m氨,12mm硫酸铜五水合物;使用1m硫酸将ph调节到9.5-10.0。
b.硫脲类浸滤剂:0.13m硫脲,5mm氯化铁(iii);使用1m硫酸将ph调节到1.0-1.5。
2.在用于每种原料/浸滤剂组合的分开的500ml平底玻璃瓶中,将100ml的浸滤剂添加到以下金原料中的每一种:
a.2到20mg金色粉末
b.25g研磨矿石(含有约0.4mgau)
c.电子废料的两个约0.5cm2的镀金销钉部分
3.在30℃,约100rpm下培育反应物20小时。保持瓶子的盖子松散以允许空气交换。
4.使反应物静置(以使研磨矿石固体沉降),并且倾析富液浸滤剂。通过电感耦合等离子体质谱分析(由新西兰奥克兰水力公司提供的服务)分析以下样品的金总含量:
a.金粉末(硫代硫酸盐类浸滤剂):用水将20ml补足到100ml(稀释约2倍),添加1ml的70%硝酸。
b.金粉末(硫脲类浸滤剂):用水将10ml补足到100ml(稀释约2倍),添加1ml的70%硝酸。
c.研磨矿石(硫代硫酸盐类浸滤剂):用水将50ml补足到100ml(稀释约2倍),添加1ml的70%硝酸。
d.研磨矿石(硫脲类浸滤剂):用水将50ml补足到100ml(稀释约2倍),添加1ml的70%硝酸。
e.电子废料(硫代硫酸盐类浸滤剂):用水将50ml补足到100ml(稀释约2倍),添加1ml的70%硝酸。
结果:
对于硫代硫酸盐类浸滤剂,测量初始氧化还原电位处于230与260mv之间(相对于标准氢电极);在浸出结束时,这处于160与180mv之间。对于硫脲类浸滤剂,这些值分别在360-400mv之间和340-370mv之间。硫代硫酸盐类浸滤剂的初始颜色为浅蓝色,在浸出结束之前变为深蓝色。硫脲类浸滤剂的初始颜色为浅橙色,在浸出结束(形成白色沉淀)之前变为无色。
可观察到金色粉末溶解于浸滤剂中;对于研磨矿石,无明显变化;而对于电子废料,可观察到金电镀的变色和溶解。虽然没有理由相信不会得到与另一种所列举原料类似的结果,但是电子废料并未用硫脲类浸滤剂进行试验。
按为分析所提供的体积计,金总含量以mg/l为单位报导,并且用于计算从原料中浸出的量和与适用时金输入质量相比时的产率(表5)。金总含量的精确度估计在15-20%变化。
表5
lix.,浸滤剂;*,估计电子废料au输入。
实例4:氯浸滤剂
材料和方法:
作为模型电子废料原料,从丢弃的台式计算机中收集印刷电路板,并且从板中切下具有镀金连接器销钉的部分。
1.将电子废料的五个约1cm2的镀金销钉部分(1.21g总质量)放置在平底反应烧瓶中,并且添加100ml的水。将烧瓶放置在磁性搅拌板上,并且添加搅拌蚤(stirringflea)。以适于保持电子废料围绕烧瓶移动的速度进行搅拌。
2.将氯气缓慢鼓泡到反应物液体中以形成氯类浸滤剂。
a.氯气由使用注射泵以9毫升/小时在分开的烧瓶中将12ml的32%盐酸滴到3g的高锰酸钾上而产生。
b.使来自电子废料反应烧瓶的过量氯气通过鼓泡到50ml的7mm硫代硫酸钠五水合物溶液中逸出以中和。
3.7小时后,观察到反应待完成,并且将富液浸滤剂倾析到分离的烧瓶中。
4.通过电感耦合等离子体质谱分析(由新西兰奥克兰的奥克兰大学质谱中心(universityofaucklandmassspectrometrycentre,auckland,newzealand)提供的服务)传送5ml的富液浸滤剂以用于分析金总含量。
结果:
按为分析所提供的体积计,金总含量以mg/l为单位报导,并且用于计算从原料中浸出的量(表6)。金总含量的精确度估计在15-20%变化。
表6
虽然从原料中浸出的金的量作为电子废料的全部质量的百分比相对较低,但是这反映出可用于浸出的金的量;0.8%相当于按质量计8,000ppm,这对于所属领域的技术人员是高浓度。
实例5:从氯溶液中生物吸附
材料和方法:
根据无菌条件生长微生物培养物,但随后使用非无菌溶液和设备进行处理。
按照实例4产生富有来自电子废料原料的金的氯类浸滤剂。
1.按照实例1培养25ml的耐金属贪铜菌菌株ch34。
2.将培养物在4,000rcf下离心12分钟,丢弃上清液,并且将丸粒(约0.1g)再悬浮于30ml的0.85%生理盐水溶液中以洗涤。第二次重复这一离心/洗涤步骤。
3.再次如上离心培养物,并且丢弃上清液。
4.用空气轻轻地鼓泡30ml的富有来自电子废料原料(约95ppmau)的金的氯类浸滤剂45分钟以驱除剩余氯气,并且用氢氧化钠将ph调节到4.5-5.0。这个溶液随后用于使来自步骤3的微生物丸粒再悬浮。
5.在室温下培育金/微生物混合物22小时。为将微生物保持在悬浮液中,始终在定轨振荡器上轻轻搅动混合物。
6.按照步骤2离心混合物,并且将上清液倾析并且储存在4℃下。按照步骤2将丸粒再悬浮于30ml的水中以洗涤和离心。
7.丢弃上清液,并且将丸粒再悬浮于2ml水中。这储存在4℃下。
8.通过电感耦合等离子体质谱分析(由新西兰奥克兰的奥克兰大学质谱中心提供的服务)分析以下样品的金总含量:
a.贫液上清液(步骤6):5ml。
b.生物吸附丸粒(步骤7):1ml。
结果:
按为分析所提供的体积计,金总含量以mg/l为单位报导,并且用于计算生物吸附的量和生物吸附产率(表7)。金总含量的精确度估计在15-20%变化。
表7
富液含有比贫液多约2倍的目标金属。
使用这些结果,计算来自生物吸附过程的浓度系数(表8),即富液到湿的生物吸附丸粒的au的浓度的增量。这接近富液到干燥生物质量的约34.5的au的浓度系数。
表8
实例6:将满载微生物与贫液分离
材料和方法:
根据无菌条件生长微生物培养物,但随后使用非无菌溶液和设备进行处理。
作为一实例,按照实例6制备金/微生物混合物。
1.为了将金满载微生物与贫液浸滤剂分离,样品通过离心或过滤处理:
a.离心:在3,000到8,000rcf下离心混合物至少10分钟,并且从金满载微生物丸粒中倾析贫液浸滤剂上清液。为了洗涤,将丸粒再悬浮于一定体积的洗涤溶液中,并且随后通过另一离心步骤回收。
b.过滤:在约20cmhg真空下将混合物应用于0.45μmpvdf过滤器几分钟,直到所有液体都通过。滤液为贫液浸滤剂,并且残余物为金满载微生物。为了洗涤,将一定体积的洗涤溶液添加到残余物中并且在真空下过滤通过。残余物通过用一定体积的洗涤溶液在50mlfalcon管中洗涤过滤器回收,直到金满载微生物再悬浮,并且随后丢弃过滤器。
结果:
离心或过滤都充分地用于将贫液浸滤剂与金满载微生物分离。
实例7:从金/铜溶液中优先生物吸附金
材料和方法:
根据无菌条件生长微生物培养物,但随后使用非无菌溶液和设备进行处理。
1.按照实例1培养120ml的耐金属贪铜菌菌株ch34。
2.将培养物分成6个相等的等分试样,在4,350rcf下离心10分钟,丢弃上清液,并且将丸粒再悬浮于30ml的0.85%生理盐水溶液中以洗涤。总计重复2次这一离心/洗涤步骤,丢弃最后洗涤上清液。
3.将丸粒(平均0.15g湿重)再悬浮于30ml的2次氯金酸连续稀释中,在初始调节的ph为5.5下在0.85%生理盐水溶液中补足的325μm(约64ppm)到10μm(约2ppm)氯金酸的范围内。
4.在丸粒再悬浮到32.5mm(2,060ppm)的最终浓度之前,还将氯化铜添加到每种稀释样品中。
5.在室温下培育金/铜/微生物混合物4小时。为将微生物保持在悬浮液中,始终在定轨振荡器上轻轻搅动混合物。
6.按照步骤2离心混合物,并且将上清液放在一旁。按照步骤2将丸粒再悬浮/用水洗涤,并且最终再悬浮于1.2ml水中(总体积估计为1.3ml)。
7.将来自步骤6的每种样品的一半(0.65ml)浸煮于4ml的酸混合物(3ml69%硝酸,1ml)中并且随后通过电感耦合等离子体质谱分析(由新西兰奥克兰的奥克兰大学质谱中心提供的服务)分析金和铜总含量。
结果:
按为分析所提供的体积计,金属总含量以mg/l为单位报导,并且用于计算生物吸附的量和生物吸附产率(表9)。金总含量的精确度估计在15-20%变化。
表9
这示出微生物(在这种情况下为耐金属贪铜菌)可选择性生物吸附金属。在这种情况下,并且铜,完全选择性生物吸附金。这使金属在分离步骤中选择性分离,即将金属满载微生物与贫液分离。在这种情况下,可将金满载微生物与保留大量铜的贫液分离。
可从表9中看出,生物吸附后金与铜的质量比变化。举例来说,在样品“325μmau”中,金属输入中金与铜比率为大约1:32;生物吸附后,发现比率为大约9:1,有利于金。这导致质量比提高288倍。以与样品“10μmau”类似的方式,金与铜比率从1:1,000增加到1:3,相对于铜增浓超过300倍。
实例8:从金/铜/镍溶液中优先生物吸附金并且干燥金属满载微生物
材料和方法:
1.在轻轻搅动下在22℃下使84g的湿的耐金属贪铜菌生物质量(以与实例5类似的方式产生)与250ml的富有金、铜和镍的浸滤剂溶液(以与实例4类似的方式由浸出电子废料而产生)接触2.25小时。
2.在离心罐中在4,000rcf下离心混合物40分钟,并且将上清液放在一旁。将丸粒再悬浮于1.1l水中以如上洗涤和离心,并且将洗涤上清液放在一旁。
3.将沉淀的金属满载生物质量散布在塔盘上,并且使其干燥超过72小时,得到大约22g的干质量。
4.将125mg的这一干燥生物质量碾磨,在4ml王水中浸煮,并且按照制造商的说明书通过使用岛津(shimadzu)aa-6300(日本京都岛津公司(shimadzucorp,kyoto,japan))的原子吸收质谱分析来分析金、铜和镍总含量。
结果:
金属总含量以mg/l为单位报导,并且用于计算每种生物吸附的金属的量和生物吸附产率(表10)。金属总含量的精确度估计在15-20%变化。
表10
*,在富液浸滤剂(250ml)中含有的金属总质量。
使用表10中的数据,使用22克的干燥金属满载生物质量计算来自250ml浸滤剂和随后干燥的生物吸附方法的浓度系数(表11)。
表11
可看出,虽然金的浓度增加路约10倍,但是铜的浓度仅增加了约3倍,而发现类似含量的镍。
实例9:通过熔炼从微生物中回收金属
材料和方法:
焚烧金属满载微生物的样品(先前通过原子吸收质谱分析确定含有36,250mg/kg[ppm]金,1,686mg/kg铜和82mg/kg镍;参见实例8)以去除有机物质并且回收生物吸附的金属。
1.将0.5g的干燥金属满载微生物粉末与相等部分的四硼酸钠焊剂混合,并且放置在坩埚中。
2.混合物谨慎地用甲基乙炔丙二烯丙烷气体焊炬加热,直到焊剂开始液化。随后逐渐增大火焰的强度,并且缓慢燃烧有机物质。
3.将残留在坩埚中的熔融金属残余物凝聚成单一质量,使其冷却,并且随后称重。
4.将冷却的金属纽扣浸煮在4ml王水中,并按照制造商的说明书通过使用岛津aa-6300(日本京都岛津公司)的原子吸收质谱分析来分析所得溶液的金、铜和镍总含量。
结果:
熔炼后达到的金属纽扣的的为20.94mg。金属总含量以mg/l为单位报导,并且用于计算金属产率(表10)。金属总含量的精确度估计在15-20%变化。
表12
实例10:通过化学溶解和沉淀从微生物中回收金
材料和方法:
类似于实例9,通过使用氯类浸滤剂提取,从金属满载微生物中回收生物吸附金属。
1.将100ml的水放置在反应容器中,并且装入气态氯维持45分钟。
2.将0.3g的干燥的金属满载微生物粉末(参见实例8)添加到浸滤剂中,并且使其反应隔夜,同时轻轻地搅拌。
3.随后用空气鼓泡溶液以去除过量氯,并且添加0.5g的偏亚硫酸氢钠以将例如金的金属离子沉淀出溶液。
结果:
金属满载微生物粉末的金属含量先前确定为36,250ppmau、1,688ppmcu和82ppmni(参见实例8)。在22℃下静置24小时后在溶液中形成可见沉淀,其为金色粉末。
综述
本文中已经参考某些优选实施例描述本发明,以便读者无需过度实验就能实践本发明。然而,所属领域的技术人员将易于认识到,许多组分和参数可以在不脱离本发明的范围的情况下在一定程度上加以改变或修改或取代成已知等效物。应了解,这类修改和等效物如同单独阐述般并入本文中。提供标题、小标题或其类似物以增强读者对本文件的理解,并且不应被解读为限制本发明的范围。
上文和下文(如果存在的话)提出的所有申请案、专利和公开案的全部公开内容特此以引用的方式并入。
本说明书中对任何现有技术的提及不应理解为对现有技术在美国或世界上任何国家形成公共常识的一部分的认可或任何形式的暗示。
除非上下文另有要求,否则在整个本说明书和随附的任何权利要求中,词语“包含(comprise)”、“包含(comprising)”以及其类似词语应以与排它性意义相反的包括性意义(也就是说,在“包括但不限于”的意义上)理解。
- 还没有人留言评论。精彩留言会获得点赞!