一种水循环系统保护剂及其制备工艺的制作方法
本发明涉及化学腐蚀及电化学腐蚀防护
技术领域:
,具体来说,涉及一种水循环系统保护剂及其制备工艺。
背景技术:
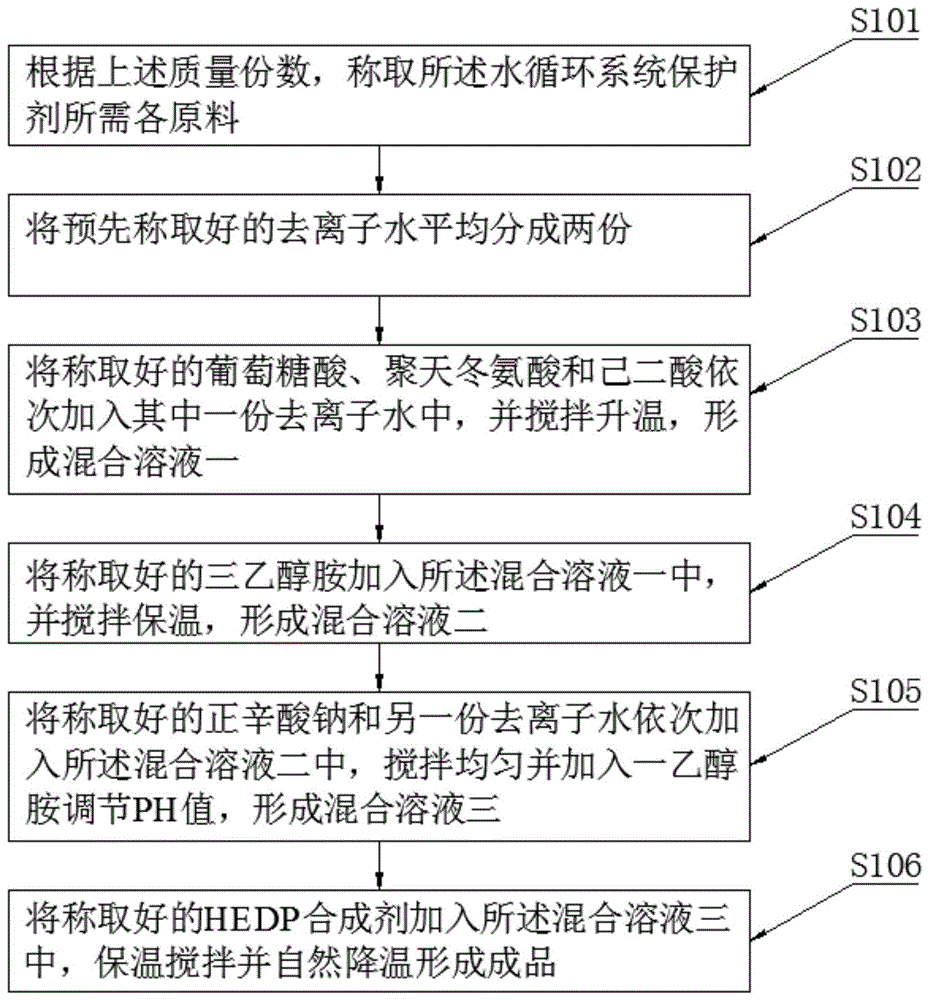
:金属材料受周围介质的作用而损坏,称为金属腐蚀。金属的锈蚀是最常见的腐蚀形态。腐蚀时,在金属的界面上发生了化学或电化学多相反应,使金属转入氧化(离子)状态。这会显著降低金属材料的强度、塑性、韧性等力学性能,破坏金属构件的几何形状,增加零件间的磨损,恶化电学和光学等物理性能,缩短设备的使用寿命,甚至造成火灾、爆炸等灾难性事故。金属在自然界淡水中的腐蚀可分为电化学腐蚀和化学腐蚀。其中,金属在淡水中电化学腐蚀的特征为:淡水以中性居多,在淡水中金属的腐蚀通常是以氧去极化为主的电化学腐蚀。氧的存在是淡水中金属腐蚀的根本原因。纯水中如果不存在o2,钢铁一般不腐蚀,但是通常天然水中总溶解有足够的氧,且表层水常被氧饱和,所以总能导致腐蚀。除电负性很高的镁在淡水中发生析氢腐蚀外,绝大多数金属和钢铁相似,在淡水中一般都发生受氧的扩散所控制的氧去极化腐蚀。金属在淡水中化学腐蚀的特征为:我国地域辽阔地下水差异较大,部分地区地下水中含有不同含量的腐蚀性离子。如:硫酸盐,氯化物,氟化物等。在受到水温和周围介质的作用而发生的腐蚀特征,如:氟化物在水温升到40度以上时与水中的钙,在氢的作用下会生成氟化钙(氢氟酸),会对金属和玻璃产生严重腐蚀。水温的影响:水温对活化态金属在开放系统中腐蚀速度的影响呈现两面性,一方面水温升高,水体的电导率增大,水体对流和扩散速度增大,金属腐蚀的阴阳极共振速度都将加快,从而使腐蚀过程的总速度加快;另一方面,温度升高,水体中含氧量减少,又会使腐蚀速度减少。因此,金属的腐蚀速度在某一温度下将达到最大值,如铁在喊3%nac1的水中,水温为80℃时的腐蚀速度最大。一般江河湖沼等自然水的温度在0-30℃之间,在此温度范围内,钢铁的腐蚀随温度的升高而加快(当腐蚀速度受水中氧扩散控制室,水温上升10℃,钢的腐蚀速度约加大30%)。ph值的影响:对铝、铁、钢、铜等金属而言,不同金属在不同的ph值范围内,腐蚀速度与ph值的关系有较大变化,在ph值4-6范围内铝的表面变化极小,当ph值<9时,有利于氢氧化物膜的形成,因此腐蚀速度随碱性的增加而降低;当ph值<13时,膜溶解破坏,腐蚀速度随碱性的增加而增大;当ph值<7时,膜亦发生溶解,腐蚀速度随酸度的增加急剧增大。流速的影响:在流速较低的阶段,当流速增大时,氧向金属表面扩散加快,钢的腐蚀速度增加;当流速增大到一定程度,氧的扩散速度使钢进入钝态,腐蚀速度急剧下降;而当流速增大到更大数值时,水对金属表面的冲击破坏了金属表面的钝化保护层,金属发生冲击腐蚀,从而又加速了腐蚀。针对相关技术中的问题,目前尚未提出有效的解决方案。技术实现要素:针对相关技术中的问题,本发明提出一种水循环系统保护剂及其制备工艺,以克服现有相关技术所存在的上述技术问题。为此,本发明采用的具体技术方案如下:根据本发明的一个方面,提供了一种水循环系统保护剂。该水循环系统保护剂包括以下原料组份:葡萄糖酸8-12份、hedp合成剂15-25份、聚天冬氨酸8-12份、已二酸3-7份、正辛酸钠8-12份、三乙醇胺10-20份、去离子水25-35份和一乙醇胺5-7份。可选的,一种水循环系统保护剂,包括以下原料组份:葡萄糖酸8份、hedp合成剂15份、聚天冬氨酸8份、已二酸3份、正辛酸钠8份、三乙醇胺10份、去离子水25份和一乙醇胺5份。可选的,一种水循环系统保护剂,包括以下原料组份:葡萄糖酸10份、hedp合成剂20份、聚天冬氨酸10份、已二酸5份、正辛酸钠10份、三乙醇胺15份、去离子水30份和一乙醇胺6份。可选的,一种水循环系统保护剂,包括以下原料组份:葡萄糖酸12份、hedp合成剂25份、聚天冬氨酸12份、已二酸7份、正辛酸钠12份、三乙醇胺20份、去离子水35份和一乙醇胺7份。根据本发明的另一方面,提供了一种水循环系统保护剂的制备工艺。该水循环系统保护剂的制备包括以下步骤:根据上述质量份数,称取所述水循环系统保护剂所需各原料;将预先称取好的去离子水平均分成两份;将称取好的葡萄糖酸、聚天冬氨酸和己二酸依次加入其中一份去离子水中,并搅拌升温,形成混合溶液一;将称取好的三乙醇胺加入所述混合溶液一中,并搅拌保温,形成混合溶液二;将称取好的正辛酸钠和另一份去离子水依次加入所述混合溶液二中,搅拌均匀并加入一乙醇胺调节ph值,形成混合溶液三;将称取好的hedp合成剂加入所述混合溶液三中,保温搅拌并自然降温形成成品。进一步的,所述混合溶液一在制备过程中搅拌升温的温度为85摄氏度。进一步的,所述混合溶液二在制备过程中搅拌保温的时间为80分钟。进一步的,所述混合溶液三在制备过程中ph值的范围为9.4-9.6。进一步的,所述混合溶液三在制备成品过程中保温搅拌时间为4小时,降温至37摄氏度以下。本发明的有益效果为:(1)、该水循环系统保护剂在金属表面要形成坚固而有弹性的保护膜,隔绝水与金属表面的接触,避免水流对金属表面造成的破坏,寿命长,抗酸碱,抗高温性极佳,对金属表面创伤有一定的修复功能,良好的防渗透,增加水系统的密封性,防止设备、管路细微渗漏。(2)、该水循环系统保护剂有很强的抗硬水功能,能快速分解水中的钙、镁,并可以和多种金属螯合,不会结垢,保持水质稳定。(3)、该水循环系统保护剂具有良好的储备碱度,让ph值保持在9-10.5之间当水的ph值在9以上时会有效的抑制微生物的生长不会产生微生物腐蚀,并会有利于金属成膜,保持膜的稳定性。(4)、具有优良的润滑性,抗气泡性和分散性,减少设备的噪音和分解系统中的水垢、污垢、残余助焊剂和有机物残渣。附图说明为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。图1是根据本发明实施例的一种水循环系统保护剂的制备工艺流程图。具体实施方式为进一步说明各实施例,本发明提供有附图,这些附图为本发明揭露内容的一部分,其主要用以说明实施例,并可配合说明书的相关描述来解释实施例的运作原理,配合参考这些内容,本领域普通技术人员应能理解其他可能的实施方式以及本发明的优点,图中的组件并未按比例绘制,而类似的组件符号通常用来表示类似的组件。根据本发明的实施例,提供了一种水循环系统保护剂及其制备工艺。现结合附图和具体实施方式对本发明进一步说明,根据本发明实施例的水循环系统保护剂,该水循环系统保护剂包括以下原料组份:葡萄糖酸8-12份、hedp合成剂15-25份、聚天冬氨酸8-12份、已二酸3-7份、正辛酸钠8-12、三乙醇胺10-20份、去离子水25-35份和一乙醇胺5-7份。为了更清楚的理解本发明的上述技术方案,以下通过具体实例对本发明的上述方案进行详细说明。实施例一一种水循环系统保护剂,该水循环系统保护剂包括以下原料组份:葡萄糖酸8g、hedp合成剂15g、聚天冬氨酸8g、已二酸3g、正辛酸钠8g、三乙醇胺10g、去离子水25g和一乙醇胺5g。该水循环系统保护剂的制备,包括以下步骤:根据上述质量份数,称取所述水循环系统保护剂所需各原料;将预先称取好的去离子水平均分成两份;将称取好的葡萄糖酸8g、聚天冬氨酸8g和己二酸3g依次加入其中一份去离子水12.5g中,并搅拌升温,形成混合溶液一;将称取好的三乙醇胺10g加入所述混合溶液一中,并搅拌保温,形成混合溶液二;将称取好的正辛酸钠8g和另一份去离子水12.5g依次加入所述混合溶液二中,搅拌均匀并加入一乙醇胺5g调节ph值,形成混合溶液三;将称取好的hedp合成剂15g加入所述混合溶液三中,保温搅拌并自然降温形成成品。实施例二一种水循环系统保护剂,该水循环系统保护剂包括以下原料组份:葡萄糖酸10g、hedp合成剂20g、聚天冬氨酸10g、已二酸5g、正辛酸钠10g、三乙醇胺15g、去离子水30g和一乙醇胺6g。该水循环系统保护剂的制备,包括以下步骤:根据上述质量份数,称取所述水循环系统保护剂所需各原料;将预先称取好的去离子水平均分成两份;将称取好的葡萄糖酸10g、聚天冬氨酸10g和己二酸5g依次加入其中一份去离子水15g中,并搅拌升温,形成混合溶液一;将称取好的三乙醇胺15g加入所述混合溶液一中,并搅拌保温,形成混合溶液二;将称取好的正辛酸钠10g和另一份去离子水15g依次加入所述混合溶液二中,搅拌均匀并加入一乙醇胺6g调节ph值,形成混合溶液三;将称取好的hedp合成剂20g加入所述混合溶液三中,保温搅拌并自然降温形成成品。实施例三一种水循环系统保护剂,该水循环系统保护剂包括以下原料组份:葡萄糖酸12g、hedp合成剂25g、聚天冬氨酸12g、已二酸7g、正辛酸钠12g、三乙醇胺20g、去离子水35g和一乙醇胺7g。该水循环系统保护剂的制备,包括以下步骤:根据上述质量份数,称取所述水循环系统保护剂所需各原料;将预先称取好的去离子水平均分成两份;将称取好的葡萄糖酸12g、聚天冬氨酸12g和己二酸7g依次加入其中一份去离子水17.5g中,并搅拌升温,形成混合溶液一;将称取好的三乙醇胺20g加入所述混合溶液一中,并搅拌保温,形成混合溶液二;将称取好的正辛酸钠12g和另一份去离子水17.5g依次加入所述混合溶液二中,搅拌均匀并加入一乙醇胺7g调节ph值,形成混合溶液三;将称取好的hedp合成剂25g加入所述混合溶液三中,保温搅拌并自然降温形成成品。为了方便理解本发明的上述技术方案,以下结合附图对本发明的上述方案的流程进行详细说明,具体如下:根据本发明的实施例,还提供了一种水循环系统保护剂的制备工艺。如图1所示,在实际生产过程中,该水循环系统保护剂的制备,包括以下步骤:步骤s101,根据上述质量份数,称取所述水循环系统保护剂所需各原料;步骤s102,将预先称取好的去离子水平均分成两份;步骤s103,将称取好的葡萄糖酸、聚天冬氨酸和己二酸依次加入其中一份去离子水中,并搅拌升温,形成混合溶液一;步骤s104,将称取好的三乙醇胺加入所述混合溶液一中,并搅拌保温,形成混合溶液二;步骤s105,将称取好的正辛酸钠和另一份去离子水依次加入所述混合溶液二中,搅拌均匀并加入一乙醇胺调节ph值,形成混合溶液三;步骤s106,将称取好的hedp合成剂加入所述混合溶液三中,保温搅拌并自然降温形成成品。在一个实施例中,所述混合溶液一在制备过程中搅拌升温的温度为85摄氏度。在一个实施例中,所述混合溶液二在制备过程中搅拌保温的时间为80分钟。在一个实施例中,所述混合溶液三在制备过程中ph值的范围为9.4-9.6。在一个实施例中,所述混合溶液三在制备成品过程中保温搅拌时间为4小时,降温至37摄氏度以下。为了方便理解本发明的上述技术方案,以下结合实验数据对本发明的上述方案的进行详细说明,具体如下:实验方案:实验一、普通地下水加热蒸发实验普通地下水加热蒸发试验(参照地下水标注gb/t14848-2017),试验结果为:加热至沸腾,冷却后有沉淀析出。实验二、水循环系统保护剂(1:30)加热蒸发实验实验内容:水循环系统保护剂25g(1:30)地下水,加热蒸发(98℃-100℃)。表1为水循环系统保护剂加热蒸发表序号蒸发水量/g补加水量/g结果1107107透明均一2112112透明均一3127127透明均一49595透明均一5141141透明均一6132132透明均一7104104有微量絮状物实验结果:当地下水超过818g时,有微量絮状物生成。通过上述实验一和实验二的结果可以得出水循环系统保护剂对硬水有很强的络合能力,再一次说明了水循环系统保护剂在暖通设备上的突出表现。实验三、水循环系统保护剂金属腐蚀试验本次试验设备:发动机冷却液腐蚀测定仪本次试验方法依据gb/t18175-2014标准实验条件:温度88℃±2℃,时间236h±2h,水循环系统保护剂与腐蚀水的比例为1:30表二为水循环系统保护剂金属腐蚀表实验后试剂无沉淀,玻璃器皿腐蚀试验结果各种金属符合防腐防锈标准。实验四、水循环系统保护剂储备碱度值缓冲能力测试表3为水循环系统保护剂储备碱度值缓冲能力测试表起始ph9.2终了ph9.1ph值变化+0.1起始储备碱度ml4.2终了储备碱度ml4.1储备碱度变化率%-0.1溶液澄清无沉淀实验结论:水循环系统保护剂在高温,高氧的作用下良好的抗衰减能力。证明水循环系统保护剂的良好ph值缓冲能力。实验室数据说明:水循环系统保护剂在水循环系统中对抗硬水和防锈防腐方面以及ph值的缓冲能力有着优异的表现,体现出优异的长使用寿命和无需经常添加的特点。综上所述,借助于本发明的上述技术方案,该水循环系统保护剂在金属表面要形成坚固而有弹性的保护膜,隔绝水与金属表面的接触,避免水流对金属表面造成的破坏,寿命长,抗酸碱,抗高温性极佳,对金属表面创伤有一定的修复功能,良好的防渗透,增加水系统的密封性,防止设备、管路细微渗漏。该水循环系统保护剂有很强的抗硬水功能,能快速分解水中的钙、镁,并可以和多种金属螯合,不会结垢,保持水质稳定。该水循环系统保护剂具有良好的储备碱度,让ph值保持在9-10.5之间当水的ph值在9以上时会有效的抑制微生物的生长不会产生微生物腐蚀,并会有利于金属成膜,保持膜的稳定性。具有优良的润滑性,抗气泡性和分散性,减少设备的噪音和分解系统中的水垢、污垢、残余助焊剂和有机物残渣。以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1