使UO3和/或U3O8转化为水合UO4的方法与流程
本发明涉及一种使UO3或U3O8转化为水合UO4(UO4水合物)的方法。
背景技术:
铀矿的处理具有从矿石中提炼铀、纯化铀以及使铀化合的目的,从而得到被称为精矿或铀酸盐的产品,或进一步得到富铀的“黄饼(yellowcake)”,例如包括高于70wt%的铀。首先,将铀矿压碎,并且随后磨碎,然后使经磨碎的铀矿承受被称为腐蚀或浸出的操作,以通过碱或酸(例如碳酸钠或硫酸)使铀进入溶液。在将来自矿石浸出物的溶液纯化和浓缩之后,例如在硫酸根介质中铀以通常为含铀的、铀酸盐化的(uraniated)的酸、液体、溶液形式回收。根据预先纯化-浓缩步骤,这些溶液也可能是在氯化物介质,氨水介质,硝酸盐介质或碳酸盐介质中。通过用沉淀剂,例如苏打、氧化镁、氨水、三碳酸铀酰胺以及过氧化氢H2O2的沉淀,通过过滤和干燥可从这些含铀的醇溶液得到铀精矿或“黄饼”。根据所使用的沉淀剂,铀精矿或“黄饼”将因此分别基于铀酸钠、铀酸镁、重铀酸铵、三碳酸铀酰胺或过氧化铀。因此,随后使制备的铀精矿或“黄饼”转变,尤其转变为UF4且随后转变为UF6。上面描述了含铀精矿,例如“黄饼”的制备,但是其他含铀的三氧化铀或六氧化铀的含铀精矿不能直接显著地被转化为UF6。事实上,一方面,相对于ASTM富集标准的接续的同位素分离步骤(也被称为富集),他们含铀过多的杂质;另一方面,某些化合物的存在可能使氟化方法恶化(redhibitory)。此外,某些氧化物对于产生UF4的还原/氢氟化步骤没有足够的反应性。为了找到对所有这些问题的改进,在使精矿转化之前,对其进行纯化。因此,纯化方法是已知的,其中,首先,将“黄饼”溶解在硝酸中,并且然后将溶液输送至逆流液-液抽提器,在逆流液-液抽提器中,使用TBP和火油的混合物抽提硝酸铀酰的溶液。该方法是复杂的,且使用必须进行处理过的硝酸盐和挥发性有机化合物。尤其必须进行用过的溶剂和硝酸盐废水的处理。用H2O2使铀沉淀是已知能够净化许多杂质污染的方法。然而,用H2O2使铀沉淀的所有已知的方法在通过加入充氧水(oxygenatedwater)使UO4·4H2O再沉淀之前,对铀进行预先溶解。然而,该技术具有下述两个主要不足:在溶解步骤中酸的加入以及因此例如硫酸根、氯根离子、硝酸根等关联阴离子(associatedanion)的引入。这些阴离子被证明在连续的转化步骤中是令人讨厌的杂质;在水合UO4的沉淀中,为了维持pH恒定的碱的加入以及因此例如钠、钾、铵阳离子的关联阳离子的加入。这些阳离子是对于UF4的形成是非常令人讨厌的杂质(Na、K...),或还产生气体流出物。尽管进行重复的洗涤,某些加入的杂质可能部分随同铀,并且对于UF4转化法是令人讨厌的。具体地,硫酸根释放腐蚀性H2S的同时,钠和钾形成低共熔物。在描述用H2O2使精矿沉淀的文献中,WO-A1-2009/013759提及了用于纯化目的,该文献描述了一种用于精炼“黄饼”的方法,以制备核纯度的铀,在该方法中,为了同时去除重金属、硼和其他稀土金属,在单一步骤中实现沉淀。在该方法中,开始于在适度搅拌下,使“黄饼”溶解在硝酸中以产生硝酸铀酰的溶液,并且在预定温度和pH下加入过氧化氢以选择性地沉淀水合过氧化铀。该文献的方法包括上文中列出的硝酸溶解精矿的预先步骤的所有不足。文献FR-A-2438623涉及一种用于纯化水合过氧化铀(VI)的方法,其中,在氟络合剂的存在下,在酸性水溶液中,尤其是硝酸的溶液中消化铀精矿,从而得到铀的水性溶液,并且铀的该水性溶液与过氧化氢反应以使水合过氧化铀(VI)沉淀。再一次,该文献的方法包括上文中列出用酸,例如用硝酸溶解精矿的预先步骤的所有不足。文献FR-A-2429747涉及一种用于从水合四氟化铀制备水合过氧化铀(VI)的方法,其中,在起沉淀作用的氟化物的试剂的存在下,在酸性水溶液中,尤其是硝酸的溶液中消化水合四氟化铀,用于使氟离子沉淀并且得到铀的水性溶液,过滤该铀的水性溶液,并且调节pH,并且使水性铀溶液与过氧化氢反应以使水合过氧化铀(VI)沉淀。这里再一次的,该文献的方法包括上文中列出用酸,例如用硝酸溶解精矿的预先步骤的所有不足。因此,考虑上文,存在对使UO3或U3O8转化为水合UO4的方法的需要,该方法将能实现水合过氧化铀的制备,该水合过氧化铀具有较低的杂质含量,尤其是杂质的含量足够低,以使得该水合过氧化铀可直接转化为UF4并随后转化为UF6。更具体地,存在对这样方法的需要,该方法允许UO4水合物的制备完全或大致符合ASTMC-787标准,该ASTMC-787标准涉及用于转化为UF6的水合UO4的纯度。该方法还应该允许具有高比表面积和对UF4的转化具有良好反应性的水合过氧化铀的制备。这里进一步存在对这样方法的需要,该方法是简单的、可靠的、安全且包括有限数目的步骤。这里还存在对这样方法的需要,该方法使用无毒的试剂,并且不会引起对环境任何不利,而且是低成本的。本发明的目的是提供一种用于使UO3或U3O8转化为水合UO4的方法,并且该方法符合上文列出的全部需要和要求。本发明的目的还是提供这样的一种方法,该方法不具有现有技术的方法的不足、缺陷、限制和不利,例如尤其是通过上述文献示出的不足、缺陷、限制和不利,并且该方法解决现有技术的方法的问题。
技术实现要素:
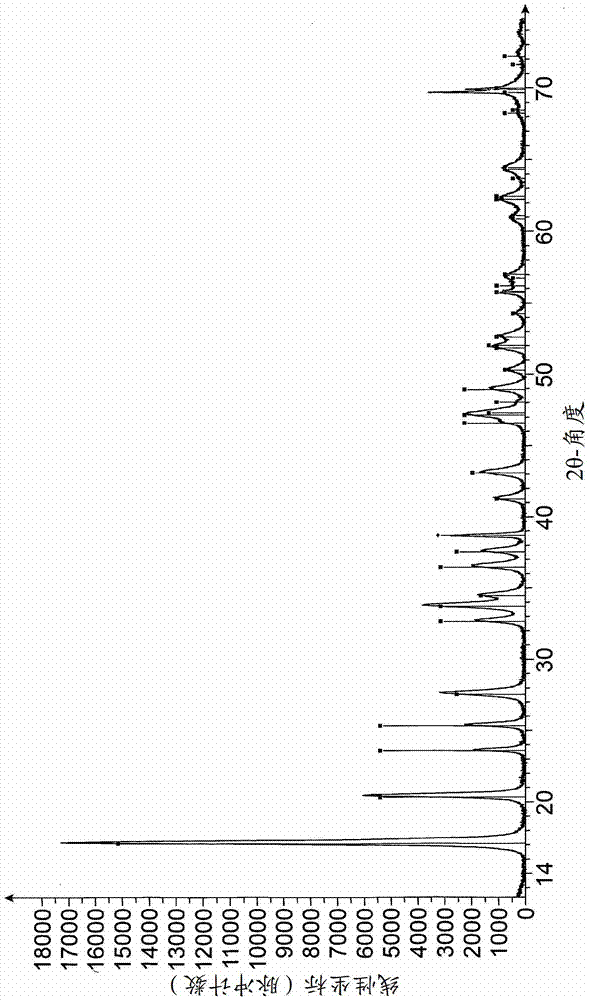
用根据本发明的使UO3和/或U3O8转化为分子式为UO4·nH2O的水合UO4的方法可达到该目的以及进一步的其他目的,其中n为2或4,包括下列连续步骤:a)制备UO3粉末和/或U3O8粉末的水性悬浮液;b)将过氧化氢H2O2加入到UO3粉末和/或U3O8粉末的所述水性悬浮液,使UO3和/或U3O8转化为水合UO4,以及使所述水合UO4在该悬浮液中沉淀、结晶;c)回收UO4水合物的沉淀、晶体;d)可选地,洗涤该回收的UO4水合物的沉淀、晶体;e)可选地,重复步骤d);f)可选地,干燥该沉淀、晶体;其中,进行将H2O2加入到水性悬浮液,从而使得相对于起始于UO3的反应:UO3+nH2O+H2O2→UO4·nH2O+H2O(1)或起始于U3O8的反应UO2.67+1.33H2O2+nH2O→UO4·nH2O+H2O(2)的化学计量,所述悬浮液含有化学计量过剩的H2O2,并且所述悬浮液的pH在步骤a)和b)中保持为包括在2和3之间的值(包括2和3)处。有利地,所述悬浮液的pH在步骤a)中通过将酸加入至所述悬浮液而被调节至包括在2和3之间的值。有利地,所述酸选自草酸、硫酸以及它们的混合物。有利地,相对于反应(1)的化学计量,H2O2的化学计量过量为大于1至10,优选为1.5至3;相对于反应(2)的化学计量,H2O2的化学计量过量为大于1.33至10。有利地,过氧化氢以浓度为30wt%至70wt%的水性溶液形式加入。有利地,UO3和/或U3O8的所述水性悬浮液对于UO3具有的铀浓度为10至500g/L(gU/L),优选100至200g/L;对于U3O8具有的铀浓度为10至500g/L,优选100至200g/L,例如250g/L。有利地,可在搅拌下进行步骤a)和步骤b)。有利地,在步骤a)和/或步骤b)中,将络合阴离子引入到所述悬浮液中。有利地,所述络合阴离子选自硫酸根离子、草酸根离子以及它们的混合物。有利地,选择步骤b)的持续时间以使得UO3和/或U3O8完全或基本上完全,例如高于99%,或甚至99.9%转化为UO4水合物。在实施方式中,步骤b)可包括下列连续步骤b1)和b2):b1)优选地在搅拌下,将过氧化氢H2O2加入到UO3粉末和/或U3O8粉末的所述水性悬浮液,并且,然后停止该加入;b2)优选地在搅拌下,使所述悬浮液熟化(ripen)。有利地,所述步骤b1)的持续时间可为1至8小时,优选为1至3小时;以及步骤b2)的持续时间可为1至24小时,优选为1至3小时。在另一个实施方式中,在步骤b)的整个持续时间中进行过氧化氢H2O2的加入,即省略步骤b2)。在该实施方式中,步骤b)的持续时间通常为1至8小时,优选为1至5小时。有利地,在步骤a)和/或步骤b)中,使所述悬浮液经受超声波的作用。尤其在这种情况下,通过蒸发可去除所述悬浮液中的水,然后回收作为干固体的UO4水合物的沉淀、晶体,所述干固体例如具有以质量计少于7%的水分含量,通常由UO4·2H2O组成,或者,在步骤c)中,通过固/液分离操作,例如过滤操作或离心操作将UO4水合物的沉淀、晶体作为湿固体从所述悬浮液中分离,所述湿固体例如具有以质量计30至80%的水分含量,通常由UO4·4H2O组成。另一方面,蒸发通常不能实现杂质的去除。有利地,用洗涤液将所述湿固体至少洗涤一次。有利地,所述洗涤液选自软化水,优选pH为2至3的例如用硫酸酸化的酸化水性溶液,含有与所述湿固体中含有的杂质络合的试剂的溶液。有利地,洗涤比为1至30,优选为1至10,所述洗涤比通过所述洗涤液的质量与所述湿固体的质量的比率来界定。有利地,氧化物UO3和/或氧化物U3O8呈现为被称为“黄饼”的含铀精矿的形式,或者氧化物UO3和/或氧化物U3O8来源于铀精矿的干燥以及随后的煅烧,该铀精矿基于例如在反应器中,尤其是流化床反应器中从含铀溶液中通过沉淀得到的水合UO4、重铀酸铵或三碳酸铀。根据本发明的方法通过将H2O2加入至U3O8粉末和/或UO3粉末的水性悬浮液中可被限定为直接转化法,而不需要预先溶解U3O8和/或UO3。根据本发明的方法,包括:具体步骤的次序,这在现有技术中未曾描述。根据本发明的方法与现有技术中的方法的基本区别是:在通过加入过氧化氢实现U3O8和/或UO3的转化之前,不需要进行U3O8和/或UO3的预先溶解。因此,根据本发明的方法,在分散系中而不是在溶液中实现U3O8和/或UO3转化为水合UO4(UO4水合物)。根据本发明的方法,该方法并不包括用于溶解铀的任何预先步骤,以及由于该预先溶解步骤引起的所有不足。具体地,因此根据本发明的方法避免了许多杂质的形成,而这些杂质在UO4水合物的转化(例如转化为UF4)的后续步骤中是极其令人讨厌的。现有技术中的所有对比方法包括这种溶解步骤,并且在现有技术中并不存在任何迹象使得本领域的技术人员来取消该溶解步骤。根据本发明的方法进一步通过这样的事实来限定,该事实是:该悬浮液含有相对于反应(1)和(2)化学计量过量的H2O2,这就使得能够得到全部转化或类似全部转化。根据本发明的方法进一步的特征在于,在步骤a)和b)中悬浮液的pH保持为包括在2和3之间的具体值。这个非常窄的pH范围的选定一方面能够避免UO4水合物在酸性太强的pH下(通常小于2)再溶解的风险,另一方面,避免了在碱性更强的pH下(通常大于3),形成不是UO4水合物的其他化合物以及杂质随着铀沉淀的风险。根据本发明的方法并不具有现有技术的方法中的不足,并且提供了现有技术中的问题的解决方案。因此,根据本发明的方法允许含有少量杂质,尤其是足够低杂质含量的过氧化铀或过氧化铀水合物的沉淀,从而该过氧化铀或过氧化铀水合物可直接转化为UF4,并且然后转化为UF6。根据本发明的方法有利地允许UO4水合物的制备完全或大致符合ASTMC-787标准,该ASTMC-787标准涉及用于转化为UF6的水合UO4的纯度。根据本发明的方法进一步允许具有快速转化为UF4的高反应性的过氧化铀的制备。事实上,根据本发明的方法能够得到具有高比表面积(高达30m2/g)的UO4水合物。现将尤其参照优选的实施方式详细描述本发明。参照附图的该描述以示例性给出而不是作为限定。附图说明图1示出了在实施例1中得到的UO4·2H2O形式的纯化的铀粉末的DRX图谱;图2示出了在实施例2中得到的UO4·2H2O形式的纯化的铀粉末的DRX图谱;图3示出了在实施例4中得到的UO4·2H2O形式的纯化的铀粉末的DRX图谱;图4为用扫描电子显微镜(SEM)拍摄的如在实施例1得到的200nm的尺寸的纳米针状物UO4·2H2O的照片,图4中表示的比例尺为200nm;图5为用扫描电子显微镜拍摄如在实施例2中得到的1μm至2μm的尺寸的纳米针状物UO4·2H2O的照片,图5中表示的比例尺为200nm;图6为用扫描电子显微镜拍摄如在实施例6中得到的100nm至200nm的尺寸的纳米针状物UO4·2H2O的照片,图6中表示的比例尺为200nm。具体实施方式在根据本发明的方法的第一步骤中,制备三氧化铀UO3粉末和/或八氧化铀U3O8粉末的水性悬浮液。根据本发明的方法可用所有类型的三氧化铀UO3和/或八氧化铀U3O8实施,而无关它们的来源和它们呈现出的形状。例如,这些氧化物可呈现为被称作“黄饼”的精矿。例如,这些氧化物也可来源于铀精矿的干燥以及随后的煅烧,该铀精矿基于例如水合UO4,重铀酸铵,或在反应器中,尤其是流化床反应器中从含铀溶液中通过沉淀得到的三碳酸铀。在文献WO-A1-2010/051855中描述了在流化床反应器中从含铀溶液中通过沉淀预先得到的水合UO4、重铀酸铵或三碳酸铀的铀精矿的干燥以及随后的煅烧来制备UO3粉末或U3O8粉末的方法,可引用该文献的描述。由于在流化床中制备该铀精矿,在该文献中得到的UO3粉末或U3O8粉末具有尤其有利的性质。被称为“黄饼”的精矿形式的氧化物或来源于优选地通过在流化床中沉淀得到的铀精矿的干燥和煅烧的氧化物通常呈现为粉末,并且该氧化物可被直接用于根据本发明的方法中,并且可悬浮在水中。然而,可能有利的是,进行氧化物粉末的预先磨碎以得到具体的细晶粒,例如1微米的数量级。悬浮的粉末通常含有杂质且根据本发明的方法尤其具有在得到的水合过氧化铀(过氧化铀水合物)中降低这些杂质的含量的目的。优选地,根据本发明的方法,其寻求得到一种水合过氧化铀,对于该水合过氧化铀,杂质含量与其转化为UF6是兼容的,并且对于该水合过氧化铀,该杂质含量符合ASTMC-787标准。U3O8粉末可含有下列一种或多种杂质,例如,用ppm/U表示下列含量:As:102Ca:1383Si:2312Zr:316SO4:29205Mo:1109Na:20UO3粉末含有一种或多种下列杂质,例如,用ppm/U表示下列含量:Na:404Ca:407Mo:9V:5W:2Cr:30用于实施根据本发明的方法的反应器,并且尤其用于进行步骤a)和步骤b)的反应器通常为优选地进行搅拌的反应器,该搅拌的反应器通常提供有螺旋式搅拌器,例如三叶螺旋桨。该反应器可进一步提供有反浆片(counter-blade)或挡板(baffle)。本领域技术人员根据需要制备的悬浮液体积可容易地选择反应器的体积。反应器可进一步提供有用于测定参数值(例如悬浮液的温度和pH)的传感器和装置。通常,通过将已知量的氧化物粉末引入至反应器来制备悬浮液。然后,将预计量的软化水加入到该已知量的氧化物中,以得到具有所需浓度的悬浮液。相当明显的是,也可能以将软化水引入到反应器中来开始,且然后将氧化物粉末加入到软化水中。悬浮液的氧化物的浓度通常为10至500gU/L,优选100至200gU/L。通过加入酸或酸的混合物,将软化水的pH调节到2到3的值。该酸(这些酸)可为任何的无机酸和有机酸。将在下文中看到,优选阴离子对其进一步具有络合作用的酸,该络合作用促进反应的动力学。优选的酸是硫酸、草酸和它们的混合物。此外,也可使用其它酸来调节pH,然而硫酸具有不会引入对UF6的核纯度(nuclearpurity)不利的元素,由于没有关于硫存在的ASTM规范。此外,通过反应中间体(铀酰离子UO22+)的形成来限制向水合UO4的转化速率,然而也可使用类似硫酸根离子或草酸根阴离子或进一步的柠檬酸根离子,和/或将在下文提到的,通过施加超声波来加速该转化速率。因此,可能的是加入在根据本发明的步骤a)和步骤b)期间提供络合阴离子的化合物。在硫的情况下,S/U的最佳比例为0.125。优选地,硫酸将被用作提供络合阴离子的化合物,用于使氧化铀悬浮以得到快速的转化动力学。在粉末和软化水已经被引入到反应器后,开始搅拌以使粉末悬浮在软化水中。调节搅拌速度以允许粉末有效悬浮。在转化至水合UO4的整个持续时间中,持续搅拌以使得起始铀完全结晶化。然后,可能的是首先将充氧水加入到该悬浮液中。可通过能够控制充氧水被引入反应器的流速的任何合适的装置来完成充氧水的加入。优选地,在搅拌下完成充氧水的加入。通常,过氧化氢以浓度为30wt%至70wt%的水性溶液形式加入。根据本发明,加入的充氧水的总量为使得相对于起始铀,相对于下列反应(1)的化学计量,H2O2的化学计量过量为大于1至10,优选为1.5至3,相对于下列反应(2)的化学计量,H2O2的化学计量过量为大于1....
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1