导电性钙铝石型化合物的制造方法与流程
本发明涉及一种导电性钙铝石型化合物的制造方法。导电性钙铝石型化合物作为显示导电性的陶瓷而适合用于燃料电池材料、储氢容器材料、传感器、电子设备、离子发射器等技术领域。
背景技术:
钙铝石型化合物为源自产于德国的mayen地区的水泥(cement)矿物的化合物,为具有代表性晶体骨架12cao·7al2o3(以下,有时也记为“c12a7”)的氧化物离子包合铝硅酸盐。
关于导电性钙铝石,专利文献1中记载了一种通过利用由稀有气体生成的等离子体对钙铝石型化合物进行处理来制造导电性钙铝石的方法。
此外,专利文献2中记载了一种对钙铝石(ca24a128o644+·2o2-)的游离氧被氢置换的氢置换钙铝石(ca24a128o644+·4h-)照射紫外线从而制造导电性钙铝石(ca24a128o644+·4e-)的方法。
现有技术文献
专利文献
专利文献1:日本专利第5347345号公报
专利文献2:日本专利公开2014-136661号公报
技术实现要素:
(一)要解决的技术问题
然而,专利文献1的方法中,由于对稀有气体照射微波而生成等离子体后,需要在真空中对钙铝石型化合物进行处理,因此存在反应时间长及操作繁杂、难以控制反应的问题。
此外,专利文献2的方法中,为了得到氢置换钙铝石(ca24a128o644+·4h-),需要在氢氛围中将加藤石(katoite)于500~1500℃下烧成处理约2小时,而要制造导电性钙铝石,还需要约1小时的紫外线照射处理,除了能源成本增加以外,还存在操作繁杂的问题。
本发明鉴于上述的现有技术问题,其课题在于提供一种导电性钙铝石型化合物的制造方法,其反应在短时间完结,操作简化且易于控制反应,能够实现能源成本的节约。
(二)技术方案
本发明是在为了解决上述技术问题而反复深入研究而完成的,本发明提供一种导电性钙铝石型化合物的制造方法,其特征在于,将钙铝石型化合物与碳成分混合,并将得到的混合物收纳于密封容器,在非活性气体气氛下或真空气氛下对所述混合物照射微波而将该混合物加热。
在本发明的导电性钙铝石型化合物的制造方法中,用作原料的钙铝石型化合物只要是氧化物离子包合铝硅酸盐,可以是任意物质。作为钙铝石型化合物,优选钙与铝的摩尔比在11~13:12~16的范围内。
钙铝石型化合物(c12a7)既可以为在由晶格的骨架形成的笼结构被保持的范围内,将晶体骨架的ca原子和/或al原子的一部分或者全部置换成其他原子的化合物,也可以为将笼结构中的游离氧离子的一部分或者全部置换成其他阴离子的同型化合物。钙铝石型化合物(c12a7)有时也被标记为ca12al14o33或者ca24al28o66。
钙铝石型化合物(c12a7)优选为具有代表组成(ca12al14o33)、且具有由三维连结而成的空隙(笼)构成的晶体结构的化合物。
在本发明的导电性钙铝石型化合物的制造方法中,作为另一方的原料而使用的碳成分,只要是由碳原子构成的碳成分,可使用任意物质,例如可列举出碳化硅、活性炭、石墨、炭黑、ru/碳、石墨烯、玻璃碳、乙炔黑。
在本发明的导电性钙铝石型化合物的制造方法中,钙铝石型化合物与碳成分的混合比按重量比计优选为3~9:1~4,更优选为4~7:1~4。
在本发明的导电性钙铝石型化合物的制造方法中使用的密封容器优选为石英玻璃制容器,例如安瓿管。在将钙铝石型化合物与碳成分的混合物收纳于密封容器后,对容器内进行气体置换或者抽真空,然后将容器密封。
在本发明的导电性钙铝石型化合物的制造方法中,要将已容纳至密封容器内的钙铝石型化合物在加热下还原使其导电性化,使密封容器内为非活性气体气氛或者真空气氛。非活性气体气氛中的氧浓度优选为1(v/v)%以下,更优选为0.9(v/v)%以下,最优选为0.8(v/v)%以下。密封容器内的非活性气体气氛也可以为氮、氩、氦等。真空气氛中的气压例如可以为使用真空泵减压至10torr以下、优选减压至3~10torr的气压。
微波是基于电波频率的分类之一,是指电波中最短的波长范围(通常为波长1m至100μm、频率0.3~300ghz的电磁波)。微波的振荡中可使用采用了磁控管、速调管、行波管(twt)、回旋管(gyrotron)、耿氏二极管(gunndiode)的电路等。微波的照射使用微波发生装置进行。产生在日本的电波法中允许用于工业加热的频率即910mhz、2.45ghz、5.8ghz的微波发生装置容易获得,故而优选使用。例如,如图1所示,将收纳有该混合物的密封容器(1)配置于密封状的反应容器(2)内,利用半导体或者磁控管发生器(3)向反应容器(2)内照射微波。这样,利用微波发生装置(4)对该混合物照射微波,其结果为,通过对钙铝石型化合物(c12a7)加热从而对该化合物赋予导电性。
基于微波照射的混合物的加热条件优选为于600~1200℃下加热5~60分钟,特别优选为于气氛温度为800~900℃下进行时间为10~40分钟的加热,从而制造导电性钙铝石型化合物。
认为赋予钙铝石型化合物导电性的机理为:若对所述混合物照射微波,则微波被该混合物吸收,其能量变成热并对该混合物加热,碳成分从钙铝石型化合物中争夺氧而将该化合物还原,而产生导电性钙铝石型化合物。
(三)有益效果
根据本发明的导电性钙铝石型化合物的制造方法,将钙铝石型化合物与碳成分混合,将得到的混合物收纳于密封容器中,在非活性气体气氛下或者真空气氛下对所述混合物照射微波从而对该混合物加热,由此制造导电性钙铝石型化合物,因此不需要高温或者长时间的反应以及繁杂的反应控制,能够容易且稳定地以低成本制造具有良好特性的导电性钙铝石型化合物。
这样,利用本发明的方法,反应在短时间完结,操作简化,易于控制反应,能够实现能源成本的节约。
附图说明
图1是示意性地表示微波发生装置的照射状态的微波发生装置的垂直剖视图。
图2是拉曼分析光谱。
图3是表示拉曼分析光谱的d/g值的曲线图。
图4是esr分析光谱。
图5是esr分析光谱。
图6是表示xrd分析结果的图。
具体实施方式
接下来,与比较例一起对本发明的实施例进行说明,但本发明并不限定于这些实施例。
本发明中使用的钙铝石型化合物(c12a7)的制造方法没有特别限定。例如,本实施例中,如下所述,通过向氧化钙添加氧化铝来制造钙铝石型化合物。
除此之外,通过包括将铝粉体与氢氧化钙作为原料的加藤石的制造工序、和转化成钙铝石型化合物的工序的制造工序,可制造该化合物。
<本实施例中的钙铝石型化合物的制造方法>
用电子天秤称取4.00g的caco3(kishidachemicalco.,ltd.、≧99.5%)的粉末、2.38g的γ-al2o3(alfaaesar、≧99.9%)的粉末,用研钵充分混合。将混合后的粉末转移至氧化铝坩埚,并在大气气氛下使用电炉(koyothermosystemsco.,ltd.、kbf314n)于1300℃下熔融12小时后自然放冷,制作了钙铝石型化合物(c12a7)。
实施例1(作为碳成分使用玻璃碳以及进行氮气氛下的微波照射)将0.22g钙铝石型化合物与0.035g玻璃碳(aldrich公司)混合,将得到的混合物容纳于安瓿管(直径2.5cm、长度15cm)中。接着,对该安瓿管内进行氮气置换从而使该管内的氧浓度为小于1%(v/v),并将该管密封。接着,将该安瓿管配置于微波发生装置的反应容器内,利用该发生装置的磁控管于温度为800~900℃下对安瓿管内的混合物照射频率为2.45ghz的微波20分钟。
实施例2(作为碳成分使用玻璃碳以及进行氩气氛下的微波照射)
除了进行了氩气置换来代替氮气置换以外,进行了与实施例1相同的操作。
实施例3(作为碳成分使用乙炔黑以及进行氮气氛下的微波照射)
除了使用0.029g乙炔黑(stremchemicals公司)代替玻璃碳以外,进行了与实施例1相同的操作。
实施例4(作为碳成分使用石墨烯以及进行氮气氛下的微波照射)除了使用0.0251g石墨烯(stremchemicals公司)代替玻璃碳以外,进行了与实施例1相同的操作。
实施例5(作为碳成分使用玻璃碳以及进行真空气氛下的微波照射)
将0.22g钙铝石型化合物(c12a7)与0.035g玻璃碳(aldrich公司)混合,将得到的混合物容纳于安瓿管(直径2.5cm、长度15cm)中。接着,将该安瓿管密封后,使用真空泵将该管内减压至10~3torr。接着,将该安瓿管配置于微波发生装置的反应容器内,并利用该发生装置的磁控管于温度800~900℃下对安瓿管内的混合物照射频率为2.45ghz的微波20分钟。
比较例1(现有技术的导电性钙铝石)
按照日本特开2014-136661号公报中记载的方法,制备了导电性钙铝石型化合物。
比较例2(作为碳成分使用玻璃碳以及进行空气气氛下的微波照射)
除了不进行安瓿管内的氮置换而直接保持为空气气氛以外,进行了与实施例1相同的操作。
比较例3(作为碳成分使用玻璃碳,空气气氛,无微波照射)
除了不进行安瓿管内的氮置换而直接保持为空气气氛,也未进行微波照射以外,进行了与实施例1相同的操作。
产品分析
(1)拉曼光谱分析
在下述的条件下,对在上述实施例和比较例中得到的产品进行了拉曼光谱分析。
分析装置:日本分光公司(jascocorporation)制造的“nrs-3100”
(分析条件)
·激励波长:532nm
·曝光时间:30秒
·累计次数:2
·物镜:100x
·激光功率:约1mw
·对各试样进行5点测定,取得所得到的测定值的平均值。
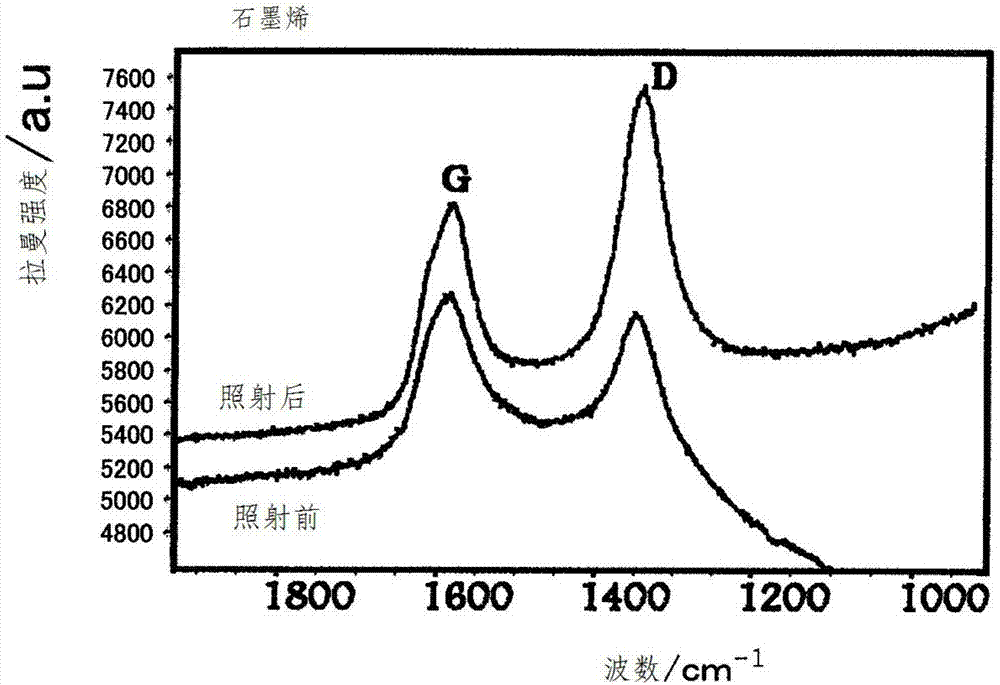
将实施例4中的微波照射前后的石墨烯的拉曼分析光谱示于图2。
将从实施例1和实施例4中的微波照射前后的碳成分的拉曼分析光谱中得到的d/g值示于图3。
图3中,对于d/g,若该值高,则表示测定试样中的碳的缺陷增加了。
根据图3,确认了:实施例1(使用玻璃碳)和实施例4(使用石墨烯)中被微波照射的试样中的碳的d/g高、晶体缺陷多,钙铝石型化合物被部分还原。
(2)电子自旋共振(esr)分析
在下述的条件下,对在上述实施例和比较例中得到的产品进行电子自旋共振分析。esr分析为用于未成对电子的检测的方法。
分析装置:日本电子公司(jeolltd.)制造的“jes-re3x(jes-px1000)”
(分析条件):
·测定温度:室温
·微波频率:9.2ghz
·微波功率:1mw
·磁场调制宽度:0.1mt
·标准物质:mn2+/mno2
将对于在实施例1~4和比较例1~3中得到的产品的试样的电子自旋共振分析结果示于图4及图5。
如图4及图5所示,在进行了微波照射的实施例1~4的产品中,与无微波照射的比较例3的产品相比,324mt附近的峰归属于e-,可知实施例1~4和比较例1的产品成为导电性钙铝石型化合物。在比较例2(空气气氛下)的产品中,在322mt附近检测到o2-的峰,可知未生成导电性钙铝石型化合物。
(3)x射线衍射(xrd)分析
在下述的条件下,对在上述实施例和比较例中得到的产品进行x射线衍射(xrd)分析。
x射线衍射装置(日本理学公司(rigakucorporation)制造,“rint2500hf+/pc-fa”)
(分析条件):
·cu/40kv/40ma
·扫描速度:10°/min
·扫描范围:10~70.0°
将对于在实施例1、2、5以及比较例1、2中得到的产品的试样的x射线衍射分析结果示于图6。
根据这些x射线衍射分析结果,确认了:上述实施例中得到的产品保持钙铝石型化合物结构。
另外,可知:通过于约500℃以上对钙铝石型化合物的原料进行烧成,从而获得钙铝石型化合物。因此,本发明中,由于通过用微波对钙铝石型化合物的原料进行照射而加热,从而获得钙铝石型化合物,因此本发明中使用的钙铝石型化合物例如既可以为作为钙铝石型化合物的前体的加藤石,也可以为氧化铝和氧化钙、氧化铝和氢氧化钙。
- 还没有人留言评论。精彩留言会获得点赞!