钴在富锂正极材料中增大正极材料的电荷容量和抑制在充电循环期间从正极材料的气体放出的用途的制作方法
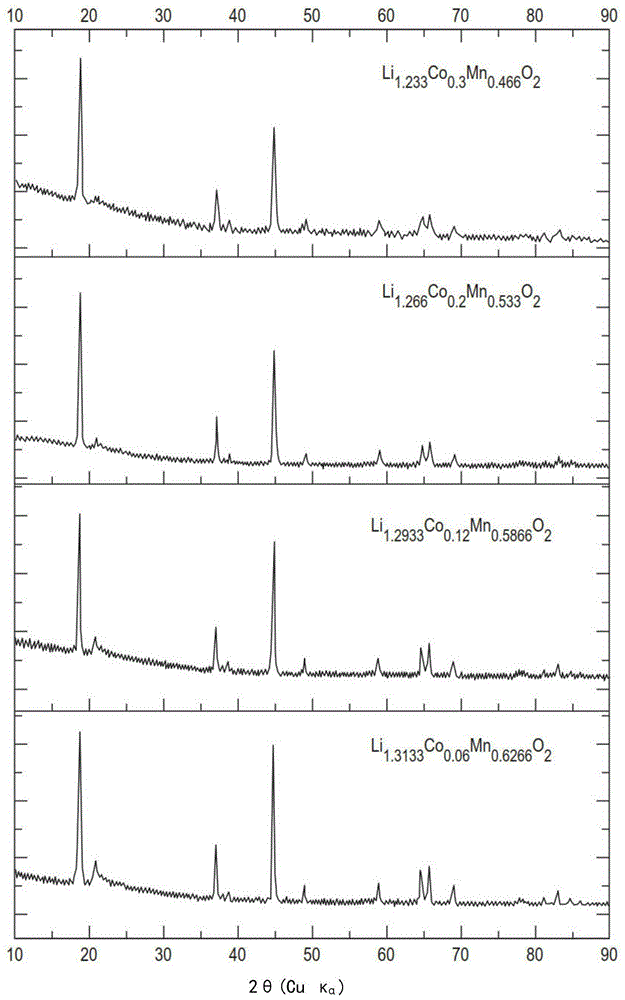
本发明涉及一组电活性正极化合物。更具体地,本发明涉及一组高容量富锂mc化合物的用途。常规的锂离子电池(battery)因用于制成正极(positiveelectrode,cathode)的材料的容量而在性能方面受限。包含镍锰钴氧化物的共混物的正极材料的富锂共混物在安全性和能量密度之间存在折衷。认识到,电荷储存在这样的正极材料内的过渡金属阳离子中。已经建议,如果电荷可储存在阴离子(例如氧)上,则能显著地提升正极材料的容量和由此的能量密度,减少对这样大量的过渡金属重离子的需要。然而,提供如下材料的挑战依旧存在:其可依赖于阴离子和阳离子两者的氧化还原化学性来储存电荷,并且经受住充电/放电循环,而不损害该材料的安全性或造成会使该材料分解的不期望的氧化还原反应。在第一方面中,本发明涉及钴在如下通式的正极材料中用于增大所述材料的电荷容量(chargecapacity)的用途:在第二方面中,本发明涉及钴在如下通式的正极材料中用于增大所述材料的电荷容量的用途:在所述用途的示例中,x大于或等于0且小于0.2;和y大于0.12。已经发现,可通过如下实现容量改善的化合物:减少过量的锂量,并且增加钴和/或镍的量。如上定义的特定化合物因钴和/或镍的氧化程度并还因晶格内氧根离子(oxideion)的氧化而展现在容量方面的大幅增加。在不希望局限于理论的情况下,认识到,特定量的钴和/或镍取代(替换)的存在实现氧的氧化还原活性,并且因此改善该材料的电化学容量。另外,当与现有技术的过渡金属取代的nmc富锂材料相比时,本发明的化合物在电化学循环期间展现改善的稳定性。分子氧的放出(evolution)普遍存在于如下的富锂材料第三行过渡金属氧化物(li1+xm1-xo2,其中m为ti、v、cr、mn、fe、co、ni、cu或zn):其中锂已经被过渡金属离子的一些所交换。这些材料通常依赖于氧的氧化还原来改善它们的电荷容量性质。均质材料可遭受分子氧在循环期间因氧根阴离子的氧化还原而从晶体结构逃逸。进而,这使该材料的容量和可用寿命缩减。认识到,当由锂离子的移出(removal)导致的电荷不平衡因电子从氧阴离子移出而平衡时,所得的氧阴离子是不稳定的,这导致在充电循环期间不期望的氧化还原反应和分子氧气的放出。在不希望局限于理论的情况下,认识到,所述材料中相对于锂含量特定的钴和/或镍含量避免晶格内的欠键合(under-bonding),使得各氧阴离子仍键合到~3个阳离子。本发明的化学途径使用特定量的过渡金属调节晶格结构,其改善所述材料的容量并且提高所述材料的经过若干充电/放电循环的稳定性。在本发明的实例中,x为0。也就是说,所述化合物的镍含量实际上为零。在该实例中,y(即钴含量)大于0.12。在一种甚至更具体的实例中,y可等于或大于0.2。已经证明,当y等于或大于0.2时,显著改善所述材料的容量。另外,y可等于或小于0.4。认识到,高于该阈值,所述材料的容量下降到预期值。已经证明,当y为0.3时实现改善的容量。更特别地,y的值可以说是大于0.2且等于或小于0.4。更特别地,y的值可以说是大于0.2且等于或小于0.3。在两个具体实例中,y可等于0.2或0.3。当x为零时,x+y的值(即,y的值)可以说是0.2或0.3。在本发明实例中,x具有大于0的值。也就是说,所述化合物包含镍级分。已经表明,镍的加入使在充电和放电循环期间从所述材料逃逸的分子氧的量减少。可以说,掺杂(doing)到富锂材料中的镍和钴的值与总量有关。这意味着,镍和钴掺杂的总量在这两种金属之间分配(即,值为x+y的函数)。x可具有等于或大于0.175且等于或小于0.275的值;和,y具有等于或大于0.1且等于或小于0.35的值。x+y的值可等于或大于0.3。x值和y值两者均可大于0.13。更特别地,当x为0.175时,y具有等于或大于0.2且等于或小于0.35的值;当x为0.2时,y具有等于或大于0.15且等于或小于0.3的值;当x为0.225时,y具有等于或大于0.1且等于或小于0.25的值;当x为0.25时,y具有等于或大于0.05且等于或小于0.2的值,更特别地y具有等于或大于0.1且等于或小于0.2的值;当x为0.275时,y具有等于或大于0.05且等于或小于0.15的值,优选地y具有等于0.15的值;当x为0.3时,y具有等于或大于0.05且等于或小于0.1的值;和,当x为0.325时,y具有等于0.05的值。替代地,当y为0.05时,x具有等于或大于0.25且等于或小于0.325的值;当y为0.1时,x具有等于或大于0.225且等于或小于0.3的值,更特别地x具有等于或大于0.225且等于或小于0.25的值;当y为0.15时,x具有等于或大于0.2且等于或小于0.275的值;当y为0.2时,x具有等于或大于0.175且等于或小于0.25的值;当y为0.25时,x具有等于或大于0.175且等于或小于0.225的值;当y为0.3时,x具有等于或大于0.175且等于或小于0.2的值;和,当y为0.35时,x具有等于0.175的值。一种特定的材料组成(即li1.2ni0.13co0.13mn0.54o2)展现与只有钴的系列材料(即,当x等于0时)相同的在容量改善方面的益处。本发明化合物可被限定为具有层状结构。典型地,层状结构已经显示出具有最高的能量密度。当以层状形式时,经仅钴掺杂的材料可进一步使用如下通式定义:ali2mno3·(1-a)licoo2,使得a可等于或小于0.88。更优选地,a等于或大于0.7且等于或小于0.8。具体地,所述材料可为0.8li2mno3·0.2licoo2.,或者所述材料可为0.7li2mno3·0.3licoo2。这些特定的层状结构展现改善的容量和提高的经过若干次充电循环的稳定性。当以层状形式时,经镍-钴掺杂的材料可进一步使用如下通式定义:(1-a-b)li2mno3·alicoo2·blini0.5mn0.5o2,使得a等于或大于0.15且等于或小于0.2;且b为0.4。所关注的两种具体组成为a=0.2b=0.4;和a=0.15b=0.4。特别地,所述材料可为0.45li2mno3·0.15licoo2·0.4lini0.5mn0.5o2,或所述材料可为0.4li2mno3·0.2licoo2·0.4lini0.5mn0.5o2。这些特定的层状结构呈现改善的容量和提高的在经过若干次充电循环的稳定性。为了使本发明可更容易地被理解,现将通过示例的方式参考附图描述本发明的实施方式,在图中:图1显示按照实施例1的合成材料的粉末x-射线衍射图案;图2显示按照实施例1的合成材料的第一次循环的恒电流负荷曲线;图3显示按照实施例1的替代性合成材料的另外的粉末x-射线衍射图案;和图4显示按照实施例1的替代性合成材料的第一次循环的恒电流负荷曲线、和经过若干循环的容量测量;图5显示绘制了本发明材料以30℃、c/10、相对于li/li+为2-4.8v时在放电期间的容量和能量图的三元等高线(ternarycontour);图6显示绘制了本发明材料以55℃、c/10、相对于li/li+为2-4.8v时在放电期间的容量和能量图的三元等高线;和图7显示绘制了本发明材料以30℃、c/10、相对于li/li+为2-4.8v时在放电期间气体漏失(gasloss)图的三元等高线。现将参考以下实施例对本发明进行说明。实施例1–经钴和钴-镍取代的富锂材料的合成对于仅用钴掺杂的材料(即,x=0),使用甲醛-间苯二酚溶胶凝胶合成途径合成具有通式的材料,其中y=0、0.06、0.12、0.2和0.3;为了获得0.01mol的最终产物,计算所有的试剂比率。将按化学计量的量的ch3cooli·2h2o(98.0%,sigmaaldrich(rtm))、(ch3coo)2mn·4h2o(>99.0%,sigmaaldrich(rtm))和(ch3coo)2co·4h2o(99.0%sigmaaldrich(rtm))溶解在50ml水中,其中0.25mmol的ch3cooli·2h2o(99.0%,sigmaaldrich(rtm))对应于相对于0.01摩尔所合成的材料5摩尔%的锂。同时,将0.1mol的间苯二酚(99.0%,sigmaaldrich(rtm))溶解在0.15mol甲醛(36.5%w/w水溶液,fluka(rtm))中。所有试剂在它们各自的溶剂中一旦完全溶解,就将这两种溶液混合并将混合物剧烈搅拌一小时。随后,将包含5%摩尔过量的锂的所得溶液在油浴中在80℃下加热直至形成均匀的白色凝胶。最后,将凝胶在90℃干燥过夜并且然后在500℃以15小时和在800℃以20小时进行热处理。对于用钴-镍掺杂的材料,使用甲醛-间苯二酚溶胶凝胶合成途径合成通式为的具有其中x=0.2y=0.2的组成和其中x=0.2y=0.15的组成的材料。为了获得0.01mol的最终产物,计算所有的试剂比率。将按化学计量的量的ch3cooli·2h2o(98.0%,sigmaaldrich(rtm)),(ch3coo)2mn·4h2o(>99.0%,sigmaaldrich(rtm))(ch3coo)2ni·4h2o(99.0%sigmaaldrich(rtm)和(ch3coo)2co·4h2o(99.0%sigmaaldrich(rtm))溶解在50ml水中,其中0.25mmolch3cooli·2h2o(99.0%,sigmaaldrich(rtm))对应于相对于0.01摩尔合成材料5摩尔%的锂。同时,将0.1mol的间苯二酚(99.0%,sigmaaldrich(rtm))溶解在0.15mol甲醛(36.5%w/w水溶液,fluka(rtm))中。所有试剂在它们各自的溶剂中一旦完全溶解,就将这两种溶液混合并将混合物剧烈搅拌一小时。随后,将包含5%摩尔过量的锂的所得溶液在油浴中在80℃下加热直至形成均匀的白色凝胶。最后,将凝胶在90℃干燥过夜并且然后在500℃以15小时和在800℃以20小时进行热处理。实施例2–经钴和钴-镍取代的富锂材料的结构分析和表征通过粉末x-射线衍射(pxrd)考察根据实施例1的材料,粉末x-射线衍射(pxrd)采用装备有9kwcu旋转阳极的rigaku(rtm)smartlab实施。图1(掺杂钴的)以及图3a和图3b(分别为掺杂镍-钴的组成1和2)显示所合成的材料的粉末x-射线衍射图案。它们以在过渡层中具有一定的阳离子排序的层状材料为特征。所有图案似乎显示与具有r-3m空间群的密堆积层状结构例如litmo2一致的主峰。在范围为20-30的2θ角度下观察到另外峰,其无法被归属为r-3m空间。该排序源于在li+ni+2和mn4+之间的原子半径和电荷密度的差异并且在低镍掺杂的氧化物的结构中似乎最强。所述峰不及在完美排序存在于其中的材料中(如在li2mno3中)那么强。观察不到由于杂质引起的多余峰的存在。实施例3–经钴和钴-镍取代的富锂材料的电化学分析通过用biologicvmp3和maccor4600系列的恒电位仪进行的恒电流循环对根据实施例1的材料进行电化学表征。将所有样品组装到相对于金属锂的不锈钢纽扣电池中,并且在相对于li+/li为2v和4.8v之间以100次循环在50mag-1电流比率(currentrate)下循环。所使用的电解质为lp30(lipf6在1:1重量比的ec:dmc中的1m溶液)。图2(掺杂钴的)和图4(分别为掺杂镍-钴的组成1和2)显示根据实施例1的材料在第一次循环的充电和随后的放电期间的电位曲线。两个样品均呈现不同长度的以相对于li+/li0的4.5v为中心的高电压平台、和在充电开始时的倾斜区域。该区域的长度可归因于镍从ni+2向ni+4和co+3向co+4的氧化并且似乎与仅对过渡金属的氧化还原活性负责的将被提取的锂(即电荷)的量良好一致。在第一次放电期间,所述材料均未显示可逆平台的存在,表明在锂离子从各样品的晶格中提取(充电)和插入到其中(放电)期间所遵循的热力学途径的不同。对于实施例1的材料,第一次循环呈现由于不可逆的高电位平台的存在引起的最低库伦效率值。库伦效率似乎在前五次循环内从第一次循环值(大约60-80%)快速地提升至高于98%的值。下面详述按照实施例和本发明的展现技术效果的组成。组成limnconio11.150.550.050.25221.150.5250.10.225231.150.50.150.2241.150.4750.20.175251.1333330.5416670.050.275261.1333330.5166670.10.25271.1333330.4916670.150.225281.1333330.4666670.20.2291.1333330.4416670.250.1752101.1166670.5333330.050.32111.1166670.5083330.10.2752121.1166670.4833330.150.252131.1166670.4583330.20.2252141.1166670.4333330.250.22151.1166670.4083330.30.1752161.10.5250.050.3252171.10.50.10.32181.10.4750.150.2752191.10.450.20.252201.10.4250.250.2252211.10.40.30.22221.10.3750.350.1752下面详述按照实施例和本发明的展现技术效果的组成。组成limnconio11.150.5250.10.225221.150.50.150.2231.150.4750.20.175241.1333330.5166670.10.25251.1333330.4916670.150.225261.1333330.4666670.20.2271.1333330.4416670.250.175281.1166670.4833330.150.25291.1166670.4583330.20.2252101.1166670.4333330.250.22111.1166670.4083330.30.1752121.10.4750.150.2752131.10.450.20.252141.10.4250.250.2252151.10.40.30.22161.10.3750.350.1752按照上述方法测试这些材料,并且结果作为绘制了本发明材料以30℃和55℃、c/10、相对于li/li+为2-4.8v在放电期间的容量和能量图的三元等高线显示在图5和图6中。实施例4–在经镍-钴取代的富锂材料的第一次循环期间的气体放出将根据本发明的各材料的一个圆片组装到el-cellpat-cell-press(rtm)单个单元电池中。将所有样品相对于金属锂组装并且从ocv循环至相对于li+/li为4.8v并且然后以50mag-1的电流比率放电到2v。所使用的电解质为lp30(lipf6在1:1重量比的ec:dmc中的1m溶液)。该单元电池专门设计用于记录顶部空间内的压力变化,其于是可与从正极放出的气体的摩尔数关联。该单元电池中的压力传感器经由控制器箱连接,该控制器箱经由usb接口连接到计算机。然后,其经由由el-cell(rtm)提供的datalogger和ec-link软件进行记录。该数据作为电压、电流、时间和压力记录。这些值可通过理想气体定律组合以计算循环时所放出的气体摩尔数,其可用于计算在环境条件下放出的气体体积。计算各材料在充电期间的总气体漏失并且生成作为图7的等高线图,其显示作为三元空间内的组成的函数的气体漏失。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1