抑制性tRNA通读提前终止密码子疾病中的截短蛋白的制作方法
本发明属于生物制药领域,具体涉及利用构建抑制性trna延长致病基因无义突变体的截短蛋白,使哺乳动物细胞中产生全长有功能的蛋白,从而恢复突变体的正常结构和功能。本发明主要涉及构筑对应三种终止密码子的19种抑制性trna,在哺乳动物细胞中通读dystrophin蛋白并在肿瘤细胞通读无义突变蛋白,作用显著。
背景技术:
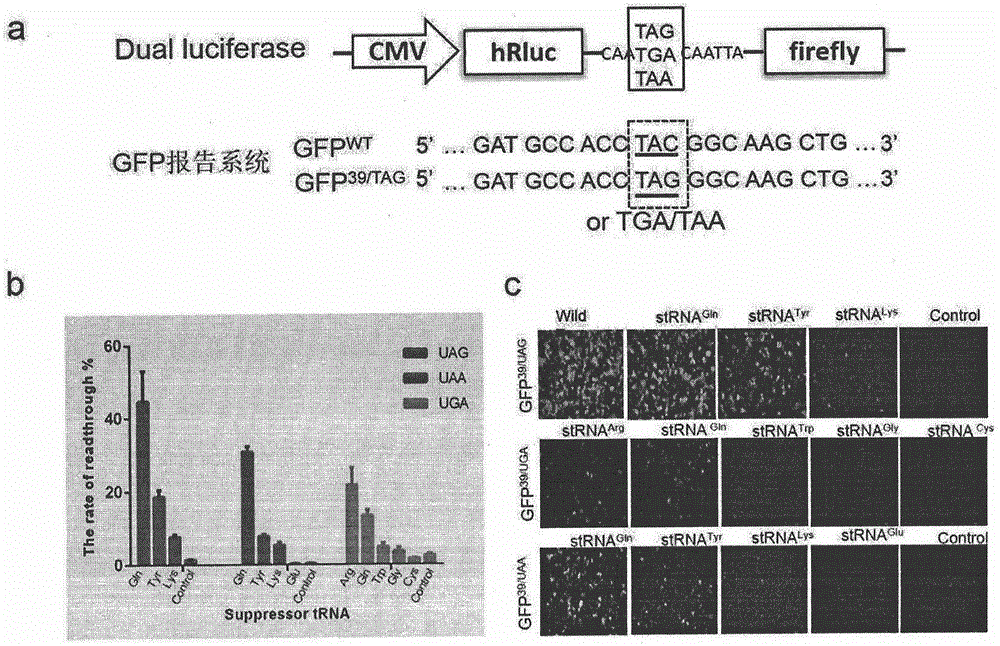
:无义突变及其引起的遗传性疾病人类基因组中的存在许多种基因突变类型,无义突变是基因突变中的一类。基因突变是基因组dna分子发生的可遗传的变异现象,其中包括移码突变和碱基置换。移码突变包括碱基的插入和缺失,碱基置换主要为错义突变和无义突变。无义突变是指编码基因的某个碱基发生突变,产生终止密码子uag、uaa和uga,终止密码子不编码任何氨基酸。终止密码子不能与转移rna(trna)的反密码子配对,但能被终止因子或释放因子识别,终止肽键的合成,使蛋白质合成终止,因而生成不完整和没有功能的蛋白质。无义突变的发生使基因框内产生提前终止密码子(prematureterminationcodons,ptc),导致基因编码的两种结果,一种即产生截短型蛋白,另一种则导致含有ptc的mrna的稳定性降低,从而引发相应的遗传性疾病。据统计,大约有11.2%的单基因遗传性疾病会产生ptc突变,被称作提前终止密码子病(prematureterminationcodonsdiseases,ptcdiseases),另一方面,许多癌症发生也会产生ptc突变(keelingk.m.etal.criticalreviewsinbiochemistryandmolecularbiology,2012,47:444-463.)。杜氏肌营养不良(duchennemusculardystrophy,dmd)是ptc疾病中的一个典型代表。dmd是一种严重的肌肉萎缩疾病,也是最常见的x连锁隐性遗传性疾病,以进展性、致死性为主要特点。dmd基因的无义突变则是导致dmd发生的主要原因之一。无义突变产生提前终止密码子uag、uaa、uga,生成截短了的多肽产物,使患者缺失或缺少功能性的抗萎缩蛋白(dystrophin),致使肌肉萎缩。据报道,duchenne型肌营养不良症在活产男婴中的发病率为1/6300~1/3500[dooleyj.etal.clinpediatr(phila),2010,49:177-179.]。该病目前尚无有效治愈方法,多于幼年期发病,青少年期丧失行走能力,成年早期死亡,给患者个人、家庭和社会造成沉重心理和经济负担抑制性trna通读无义突变人类基因组中的61种密码子可以被trna识别,编码20种氨基酸,三种终止密码子(uag、uaa、uga)没有相应的trna识别,不编码氨基酸,进而终止翻译。但是有研究发现,存在可以识别终止密码子的trna,使终止密码子编码氨基酸,蛋白翻译正常进行。这种能够识别终止密码子的trna,即为无义突变抑制性trna。抑制性trna存在广泛,无论在植物细胞还是动物细胞中,都发现了抑制性trna。但由于抑制性trna在细胞中含量极少,因此抑制性trna不易被检测到。无义突变抑制性trna由正常编码氨基酸trna反密码子环碱基突变产生,突变后的trna能识别终止密码子并与终止密码子完全互补配对,同时仍能携带氨基酸,能够在提前终止密码子处插入特定氨基酸,通读无义突变。基于抑制性trna能够通读无义突变的特性,有文献报道应用抑制性trna通读原核和真核细胞中含有提前终止密码子的蛋白,恢复蛋白表达。由于大约30%人类遗传性疾病中存在ptc,但抑制性trna对于人类遗传性疾病相关蛋白通读情况研究仍不清楚,因此,利用构建抑制性trna延长致病基因无义突变体的截短蛋白,使哺乳动物细胞中产生全长有功能的蛋白,从而恢复突变体的正常结构和功能显得十分重要。另一方面,虽然抑制性trna能够恢复含无义突变蛋白表达,但是,不同抑制性trna通读效率有何差异,仍不得而知。因此,构建多种抑制性trna,比较在哺乳动物细胞中通读效率差异,需找高效抑制性trna也十分重要。技术实现要素:发明人经过对现有技术的思考和研究,构建19种无义突变抑制性trna(序列如seqidno:1-19),抑制性trna携带对应氨基酸并与提前终止密码子完全互补配对,通读无义突变,恢复ptc疾病中致病蛋白表达,并比较得通读无义突变效率最高的抑制性trna。发明人首先确定了人类遗传性疾病中19种无义突变频率较高的氨基酸密码子,改变识别这19种密码子的相应trna反密码子环碱基,通过soepcr的方法构建无义突变抑制性trna,并在抑制性trna5’端连接7sk启动子。再将抑制性trna与含有提前终止密码子的dystrophin蛋白基因转染至293t细胞,在哺乳细胞中恢复dystrophin蛋白表达。同时,应用含有终止密码子的双荧光素酶报告基因和gfp报告基因比较不同抑制性trna促进通读效率,比较得到通读效率最高的抑制性trna分别为amber抑制性trna(gln);ocher抑制性trna(gln);opal抑制性trna(arg)。本发明的优点可体现在如下中的一个或几个:1、通过soepcr的方法,实现任意一种抑制性trna的快速构建。2、获得了三种能够高效通读无义突变的抑制性trna-amber抑制性trna(gln);ocher抑制性trna(gln);opal抑制性trna(arg)。3、利用多种抑制性trna,实现通读单基因遗传性疾病和肿瘤中的无义突变,恢复截短蛋白的正常结构和功能。具体地,在本发明的一个实施方案中,构建抑制性trna并在293t细胞中恢复dmd疾病相关蛋白dystrophin蛋白表达,主要通过:(1)构建含有7sk启动子的19种抑制性trna的表达载体bjmu-strnagln-uag;bjmu-strnatyr-uag;bjmu-strnalys-uag;bjmu-strnaleu-uag;bjmu-strnaglu-uag;bjmu-strnatrp-uag;bjmu-strnaarg-uga;bjmu-strnagln-uga;bjmu-strnatrp-uga;bjmu-strnagly-uga;bjmu-strnacys-uga;bjmu-strnaleu-uga;bjmu-strnaser-uga;bjmu-strnagln-uaa;bjmu-strnatyr-uaa;bjmu-strnalys-uaa;bjmu-strnaglu-uaa;bjmu-strnaleu-uaa;bjmu-strnaser-uaa,19种抑制性trna对应19种较易发生无义突变的119种氨基酸密码子;(2)构建中间含有终止密码子的双荧光素酶报告系统pgl4-2luc-tag;pgl4-2luc-taa;pgl4-2luc-tga和含有提前终止密码子的gfp报告基因pcdna3.1-gfp-39tag;pcdna3.1-gfp-39taa;pcdna3.1-gfp-39tga;(3)根据dmd病人中无义突变位点,利用点突变技术在dystrophin蛋白的同源异构体蛋白dp71b蛋白相应位点引入提前终止密码子,构建分别含有提前终止密码子uag,uaa,uga的dp71b蛋白质粒dp71b3115tag;dp71b3216taa;dp71b3112tga;(4)将步骤(1)和步骤(2)中载体分别对应共转染至293t细胞中,利用双荧光素酶和gfp报告-系统比较不同抑制性trna通读效率差异;(5)将步骤(1)的抑制性trna分别与步骤(3)中的含有提前终止密码子的dp71b蛋白共同转染至293t细胞,westernblot方法检测dp71b表达恢复情况,最终确定多种抑制性trna能够恢复无义突变的dp71b蛋白表达,其中抑制性trna(gln)对于uag、uaa、uga三种终止密码子的无义突变均有较高的通读效率;(6)将步骤(1)的抑制性trna转染至肿瘤细胞系a549和du145,培养48小时后提取蛋白,经westernblot证明在肿瘤细胞系a549和du145中stk11蛋白和全长ephb2蛋白恢复表达抑制性trna通读无义突变的原理在于:(1)在细胞正常的翻译过程中,提前终止密码子被第一类肽链释放因子erf1识别,而正常trna不能识别终止密码子,erf3是一类依赖于核糖体和第一类肽链释放因子的gtpase,协同erf1促进肽链从核糖体上释放,翻译过程终止(zhouravleva,g.etal.emboj,1995,14,4065-72.)。而构建的抑制性trna为正常trna通过反密码子环改造而来,其反密码子环能够与终止密码子uag、uaa、uga完全互补配对,与erf1竞争识别提前终止密码子,改变反密码子环的trna仍能携带对应的氨基酸,因此,抑制性trna在提前终止密码子位置插入氨基酸,使翻译过程继续进行,通读无义突变;(2)所构建的抑制性trna5’段连有7sk启动子,能够启动抑制性trna在哺乳动物细胞中大量表达,最终恢复蛋白表达。在本发明的一个具体实施方案中,利用soepcr方法实现任意一种带有7sk启动子的抑制性trna的快速构建。原理在于,抑制性trna只是正常trna单个碱基的替换,大小一般在80bp左右,长度较小,可以设计部分互补配对的上下游两段引物直接pcr合成,合成的抑制性trna进行第二步pcr,连接于7sk启动子3’端。具体地为,设计覆盖全部抑制性trna并部分互补的上下游引物,其余引物设计按照soepcr常规方法设计。第一步pcr分别合成抑制性trna及7sk启动子序列,第二步pcr实现抑制性trna与7sk启动子的连接,实现带有7sk启动子的抑制性trna的合成。在本发明的一个具体的实施方案中,利用中间分别含有终止密码子uag、uaa、uga的renila荧光素酶和firefly酶双荧光素酶报告基因pgl4-2luc-tag;pgl4-2luc-taa;pgl4-2luc-tga,检测不同抑制性trna的通读效率。即在293t细胞中转染抑制性trna和相应双荧光素酶报告基因,通过分别测定firefly和renila的荧光读值,根据firefly相对于renila的荧光相对值,反应通读效率差异。同时,利用点突变技术将gfp荧光基因第39位氨基酸密码子分别点突变为uag、uaa、uga三种提前终止密码子得到pcdna3.1-gfp-39tag;pcdna3.1-gfp-39taa;pcdna3.1-gfp-39tga载体,通过测定293t细胞中gfp荧光强度,确定抑制性trna通读效率,最终确定通读uag、uaa、uga效率最高的抑制性trna分别为amber抑制性trna(gln);ocher抑制性trna(gln);opal抑制性trna(arg)。在本发明的一个具体的实施方案中,将抑制性trna应用于恢复人类遗传性疾病相关无义突变蛋白表达。根据人类dmd疾病中无义突变位置,在正常dp71b序列对应位置进行点突变,模拟人类dmd疾病中dmd基因序列,含有提前终止密码子uag的dp71b3115tag,突变为c.9346c>t,含有提前终止密码子uaa的dp71b3216taa,突变为c.9651c>a;含有提前终止密码子uga的dp71b3112tga,突变为c.9337c>t。将突变后的dp71b蛋白质粒与不同的抑制性trna共转染至293t细胞中,恢复dp71b的表达。在本发明的一个具体的实施方案中,将抑制性trna用于通读肿瘤细胞中抑癌基因的无义突变位点。将bjmu-strnagln-uag转染肿瘤细胞系a549和du145(人肺癌细胞a549基因组上stk11发生无义突变c.109c>t,p.q37x,为终止密码子uag;人前列腺癌细胞du145基因组上ephb2基因发生无义突变c.2167c>t,p.q723x,为终止密码子uag)。加入非天然氨基酸培养48小时后提取蛋白,经westernblot证明基因密码子扩展技术在肿瘤细胞系a549和du145中恢复了全长stk11蛋白和全长ephb2蛋白的表达。更为具体地,本发明提供了1.含有7sk启动子的19种抑制性trna的表达载体bjmu-strnagln-uag;bjmu-strnatyr-uag;bjmu-strnalys-uag;bjmu-strnaleu-uag;bjmu-strnaglu-uag;bjmu-strnatrp-uag;bjmu-strnaarg-uga;bjmu-strnagln-uga;bjmu-strnatrp-uga;bjmu-strnagly-uga;bjmu-strnacys-uga;bjmu-strnaleu-uga;bjmu-strnaser-uga;bjmu-strnagln-uaa;bjmu-strnatyr-uaa;bjmu-strnalys-uaa;bjmu-strnaglu-uaa;bjmu-strnaleu-uaa;bjmu-strnaser-uaa,其可实现不同抑制性trna的过表达。2.含有终止密码子的双荧光素酶报基因pgl4-2luc-tag;pgl4-2luc-taa;pgl4-2luc-tga,其序列如seqidno:22所示。可通过测定该基因的firely相对于renila荧光强度,反映抑制性trna通读效率。3.携带tyr39位分别突变为uag、uaa、uga的绿色荧光蛋白报告基因载体pcdna3.1-gfp-39tag;pcdna3.1-gfp-39taa;pcdna3.1-gfp-39tga,该载体可通过荧光强度反映通读效率,未经突变的序列如seqidno:21所示。4.含有提前终止密码子uag,uaa,uga的dp71b蛋白质粒dp71b3115tag;dp71b3216taa;dp71b3112tga。未经突变的dp71b序列如seqidno:23所示。附图说明:图1:抑制性trna质粒构建a:正常trna改造反密码子环合成抑制性trna;b:抑制性trna通读ptc示意图,携带氨基酸的抑制性trna反密码子环与提前终止密码子完全互补配对,通读ptc;c:soepcr方法将7sk启动子连接至抑制性trna5’端;d:用bamhi和bglii双酶切抑制性trna,bamhi单酶切bjmu载体,将酶切产物连接,得到连有7sk-抑制性trna的bjmu载体。图2:双荧光素酶报告基因及gfp报告基因检测抑制性trna通读效率a:双荧光素酶报告基因及gfp报告基因构建,双荧光素酶中间连有含有终止密码子的linker,野生型gfp基因通过点突变将39为氨基酸突变为提前终止密码子;b:双荧光素酶报告基因检测不同抑制性trna通读效率,不同抑制性trna通读效率不同,通读uag、uaa、uga效率最高的抑制性trna分别为amber抑制性trna(gln);ocher抑制性trna(gln);opal抑制性trna(arg);c:gfp报告基因荧光强度检测不同抑制性trna通读效率,进一步验证了抑制性trna不同通读效率。图3:抑制性trna恢复ptc疾病中及肿瘤细胞无义突变蛋白表达a:抑制性trna能够恢复dp71b蛋白表达,但恢复效率不同;b:转染抑制性trnagln-uag,a549中stk11蛋白表达恢复;c:转染抑制性trnagln-uag,du145中ephb2蛋白表达恢复。为了更好地理解本发明,发明人用实施例对具体试验进行阐述和说明,其中所述实施例仅用于说明,并不限定本发明的保护范围。任何与本发明等价的变体或者实施方案都包括在本发明中。实施例1:19种抑制性trna的获得(1)确定19种抑制性trna根据人类ptc疾病突变特点,确定19种可发生无义突变的氨基酸密码子所对应trna的序列,改变trna反密码子环得到与提前中终止密码子完全互补配对的抑制性trna,19种抑制性trna分别为,amber抑制性trna:抑制性trna(gln/uag)、抑制性trna(tyr/uag)、抑制性trna(lys/uag)、抑制性trna(leu/uag)、抑制性trna(glu/uag)、抑制性trna(trp/uag);opal抑制性trna:抑制性trna(arg/uga)、抑制性trna(gln/uga)、抑制性trna(trp/uga)、抑制性trna(gly/uga)、抑制性trna(cys/uga)、抑制性trna(leu/uga)、抑制性trna(ser/uga);ocher抑制性trna:抑制性trna(gln/uaa)、抑制性trna(tyr/uaa)、抑制性trna(lys/uaa)、抑制性trna(glu/uaa)、抑制性trna(leu/uaa)、抑制性trna(ser/uaa)。(2)soepcr引物及点突变引物设计根据以确定的19中抑制性trna序列合成19种5’端连接有7sk启动子的19种抑制性trna其中3种抑制性trna,抑制性trna(gln/uag)、抑制性trna(tyr/uag)、抑制性trna(lys/uag)由序列全合成得到,其余13种由soepcr法合成抑制性trna并在5‘端连接7sk启动子,3种由得到的抑制性trna点突变获得。表17sk启动子序列表2soepcr引物序列表3抑制性trna点突变引物设计点突变引物名称引物序列(5’-3’方向)7sk-gln-ugaforctcggatcgctggatttgaagtccagagtgctaac7sk-gln-ugarevgttagcactctggacttcaaatccagcgatccgag7sk-tyr-uaaforgcgacctaaggatctaaagtcctccgctctacc7sk-tyr-uaarevggtagagcggaggactttagatccttaggtcgc7sk-trp-uag-forgcaacggcagcgcgtctgactctagatcagaaggtuag-trp-revaccttctgatctagagtcagacgcgctgccgttgc(3)抑制性trna连接至bjmu载体在得到抑制性trna的基础上,用bamhi和bglii双酶切抑制性trna,bamhi单酶切bjmu载体,将酶切产物连接,得到连有7sk-抑制性ttrna的bjmu载体。实施例2:利用双荧光素报告基因和点突变的gfp报告基因检测19种抑制性trna通读效率(1)构建含有提前终止密码子的gfp报告基因绿色荧光蛋白gfp是最常用的报告基因,也是指示非天然氨基酸插入的有力工具,其由238个氨基酸组成,其基因序列如seqidno:21。将gfp序列插入pcdna3.1商业质粒上,将gfp荧光基因第39位氨基酸密码子分别点突变为uag、uaa、uga三种提前终止密码子。设计能够使编码所述氨基酸的密码子分别突变为三种终止密码子的引物,具体引物如下表所示。表4gfp突变引物列表gfp-39-uag-forggcgagggcgatgccacctagggcaagctgaccctgaagttcgfp-39-uag-forgaacttcagggtcagcttgccctaggtggcatcgccctcgccgfp-39-uaa-forggcgagggcgatgccacctaaggcaagctgaccctgaagttcgfp-39-uaa-forgaacttcagggtcagcttgccttaggtggcatcgccctcgccgfp-39-uag-forggcgagggcgatgccacctgaggcaagctgaccctgaagttcgfp-39-uag-forgaacttcagggtcagcttgcctcaggtggcatcgccctcgcc利用定点突变试剂盒(lightningsite-directedmutagenesiskits,catalog#210518),按说明书操作,以野生型gfp表达载体pcdna3.1-gfp-wt为模板将第39位的氨基酸密码子分别突变为三种终止密码子,构建得到表达质粒(pcdna3.1-gfp-39tag、pcdna3.1-gfp-39taa和pcdna3.1-gfp-39tga),经测序验证突变成功。(2)293t细胞中分别转染不同抑制性trna质粒和双荧光素酶报基因验证抑制性trna通读效率将抑制性trna载体与和双荧光素报告基因pgl4-2luc-tag;pgl4-2luc-taa;pgl4-2luc-tga质粒按表5的分组以1∶2比例混合,再与转染试剂megatrans1.0按1∶3比例混合,共同加入293t细胞,6小时后换液,至细胞于37℃,5%co2的孵箱中继续培养48小时后裂解细胞,向细胞裂解液加入荧光素酶底物,检测荧光读值。结果如图2b所示。加入抑制性trna后,可以得到全长有活性的突变型萤火虫荧光素酶蛋白。最终确定通读uag、uaa、uga效率最高的抑制性trna分别为amber抑制性trna(gln):ocher抑制性trna(gln);opal抑制性trna(arg)。表5双荧光素酶报告基因转染质粒分组(3)293t细胞中分别转染19种抑制性trna和pcdna3.1-gfp质粒验证抑制性trna通读效率将实施例2的步骤1获得的pcdna3.1-gfp-39txx,以及实施例1的步骤3的19种抑制性trna质粒按表6的分组按照实施例2步骤2所述转染方式转染至293t细胞,48小时后后用荧光显微镜观察绿色荧光,结果如图2c所示。最终进一步验证通读uag、uaa、uga效率最高的抑制性trna分别为amber抑制性trna(gln);ocher抑制性trna(gln);opal抑制性trna(arg)。表6gfp报告基因转染质粒分组实例3:293t细胞系中通读疾病蛋白dystrophin(1)构建含有提前终止密码子uag、uaa、uga的dp71b突变质粒dystrophin蛋白的同源异构体dp71b序列如seqidno:23所示,发明人根据杜氏肌营养不良病人无义突变的位点,对野生型dp71b序列进行点突变,在不同位置引入提前终止密码子,构建含有提前终止密码子uag的dp71b3115tag,突变为c.9346c>t,含有提前终止密码子uaa的dp71b3216taa,突变为c.9651c>a;含有提前终止密码子uga的dp71b3112tga,突变为c.9337c>t,经测序验证突变成功。(2)293t细胞系中通读疾病蛋白dystrophin将实施例3的步骤1获得的dp71b3115tag,dp71b3216taa,dp71b3112tga质粒与对应的抑制性trna按照实施例2步骤2所述转染方式转染至293t细胞,继续培养48小时后提取蛋白,westernblot检测(一抗为anti-dystrophin,为抗dystrophin蛋白c末端抗体,货号12715-1-ap)到全长dystrophin蛋白的产生,如图3a。证明抑制性trna能够通读不同类型提前终止密码子,恢复疾病蛋白的表达。实施例4:抑制性trna通读肿瘤细胞系基因组上的提前终止密码子经查阅文献,人肺癌细胞a549基因组上stk11发生无义突变c.109c>t,p.q37x,为琥珀型终止密码子uag;人前列腺癌细胞du145基因组上ephb2基因发生无义突变c.2167c>t,p.q723x,为琥珀型终止密码子uag。将bjmu-strnagln-uag质粒与转染试剂megatrans1.0按1∶3比例混合,分别转染a549和du145细胞,6小时后换液,置细胞于37℃,5%co2的孵箱中继续培养48小时后提取蛋白,westernblot检测(一抗分别为anti-stk11和anti-ephb2)到全长蛋白的stk11和ephb2产生,如图3b和3c。验证抑制性能够通读内源性基因组上的提前终止密码子,恢复抑癌基因蛋白表达。以上所述的仅是本发明的一些实施方式。对于本领域的普通技术人员来说,在不脱离本发明创造构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1