用于改善病毒载体效率的组合物和方法与流程
本发明涉及用于改善病毒在靶细胞中的转导效率的肽和组合物。
背景技术:
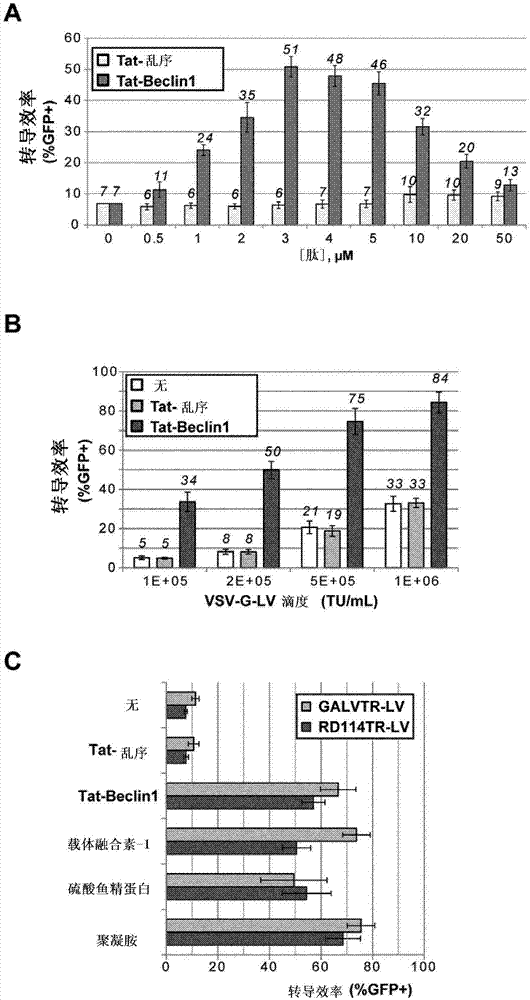
:基因治疗途径经常受到重组病毒载体对靶细胞的低转导效率的阻碍。逆转录病毒载体,特别是基于人免疫缺陷病毒1(HIV-1)的慢病毒载体(LV)是基因治疗的有希望的运载工具(D'Costa等,2009)。这些载体目前用于临床应用以治疗各种疾病,例如免疫缺陷、神经变性或神经疾病、贫血、HIV感染。逆转录病毒载体的一些应用依赖于离体转导特异性靶细胞,例如表达CD34标志物的造血干细胞/祖细胞。使用重组慢病毒粒子的一个限制因素是在生产重组慢病毒载体粒子期间获得高感染性滴度的能力。规避这种限制的一种方式是在提纯步骤期间浓缩病毒上清液(Rodrigues等,2007)。然而,对于一些LV来说,难以像GALVTR-LV(将长臂猿白血病病毒包膜糖蛋白与双嗜性鼠白血病病毒(MLV-A)包膜糖蛋白的胞质尾区融合而假型化的LV(Sandrin等,2002))那样,根据用于假型病毒粒子的包膜糖蛋白来制定提纯方案。因此,许多慢病毒载体制剂滴度较低并且转导效能有限。另一个限制因素是慢病毒载体本身感染靶细胞的能力。几种包膜糖蛋白如VSV-G、RD114TR、GALVTR可用于假型慢病毒载体,并对靶细胞例如CD34+细胞具有可变的感染性(Sandrin等,2002)。规避这些限制的一个策略是添加辅因子来优化转导方案,如阳离子聚合物(例如聚凝胺)或纤连蛋白片段(例如纤维连接蛋白)(Davis等,2004;Pollok等,1999)。美国专利号7,759,467描述了用于提高逆转录病毒对造血细胞的转导效率的方法,该方法包括在纤连蛋白或纤连蛋白片段存在下感染所述细胞。但是,由于至少两个原因,所提出的方法并不完全令人满意。首先,用于改善逆转录病毒效率的纤连蛋白片段存在显著的经济弊端,因为它们通常包含约270个或更多个氨基酸。此外,使用纤连蛋白或纤连蛋白片段需要包被培养板并将病毒上清液预加载到固定的纤连蛋白片段上。这两个步骤难以标准化,并且取决于所使用的纤连蛋白片段和病毒上清液的浓度而可能导致靶细胞转导的某种饱和(Novelli等,1999)。有趣的是,最近在人精液中鉴定出被称为SEVI的天然阳离子肽为HIV-1感染性的强增强剂(Munch等,2007;Roan等,2009)。国际申请号PCT/EP2007/050727中也公开了这种肽家族,其描述了促进细胞的病毒感染的人前列腺酸性磷酸酶的氨基酸残基240-290的片段。申请人以前还在申请号PCT/EP2012/06264中提出了使用LAH4肽或其功能性衍生物来促进病毒或病毒载体对真核细胞的感染,这提供了非常好的结果,特别是关于用LV载体感染hCD34+细胞而言。因此本发明人的目的是为了提供用于提高病毒或病毒载体在靶细胞中的转导效率的改进手段。技术实现要素:本发明提供了用于改善病毒在靶细胞中的转导的组合物和方法。本发明人已经发现,包含细胞穿透肽(CPP)部分和Beclin衍生肽部分(这两个部分在下文中定义)的肽,并特别是MAP-Beclin-1、Tat-Beclin-1或Tat-Beclin-2肽,具有促进病毒在真核细胞中的转导效率的性质。该观察结果是非常出人意料的,因为Tat-Beclin1(TB1)肽以前已被描述为诱导自噬,一种参与病毒抑制的细胞机制(WO2013/119377;Shoji-Kawata等,2013)。同样地,在2013年,HeC.等鉴定了Beclin2(HeC.等,2013),一种参与自噬的哺乳动物特异性蛋白,像Beclin1。然而,Beclin2,但不是Beclin1,在另外的溶酶体降解途径中起作用。但是,本文公开了包含CPP部分和Beclin衍生肽部分的肽,包括Tat-Beclin2肽、Tat-Beclin-1肽和MAP-Beclin-1肽,显著改善许多不同的病毒类型在不同的真核靶细胞中的转导效率。因此,本发明的一个方面提供了促进病毒感染细胞的方法,包括使所述细胞与所述病毒和肽接触,所述肽包含:(i)CPP部分;和(ii)Beclin衍生肽部分,特别是Beclin-1或Beclin-2衍生肽部分。在一个具体实施方式中,本发明的方法是体外方法。更特别地,实施所述方法是为了增加用于检测样品中病毒的存在或不存在的基于细胞的分析的灵敏度。的确,得益于本发明中实现的肽的转导增强性质,甚至可以检测到样品中低量的病毒,因为它们的感染性改善了。此外,也可以实施本发明的方法用于诊断对象中病毒的感染,包括将所述对象的样品与细胞以及包含CPP部分和Beclin衍生肽部分的本发明肽一起温育,以便增强所述样品中含有的任何病毒进入所述细胞,并随后鉴定已进入细胞的病毒。更优选地,本发明涉及如上定义的包含CPP部分和Beclin衍生肽部分(例如Beclin-1-或Beclin-2衍生肽部分)的肽,与编码治疗性基因的病毒载体组合在基因治疗方法中的应用。在一个具体实施方式中,与本发明的肽一起使用的病毒或病毒载体是逆转录病毒,特别是慢病毒,例如假型慢病毒。在另一个实施方式中,所述病毒或病毒载体是细小病毒,特别是腺相关病毒(AAV)。在一个具体实施方式中,本发明的肽促进病毒感染细胞,其中所述细胞是造血干细胞/祖细胞,优选hCD34+细胞。本发明的肽也可以与另一种病毒转导增强剂例如载体融合素(vectofusin)、人纤连蛋白片段、各种精液来源的病毒感染增强剂或由HIV-1包膜糖蛋白衍生的肽一起使用。此外,本发明涉及包含CPP部分和Beclin衍生肽部分(例如Beclin-1-或Beclin-2衍生肽部分)的肽。特别地,本发明涉及包含MAP部分和Beclin-1衍生肽部分的肽。本发明的另一个方面涉及病毒或病毒载体与包含细胞穿透肽(CPP)部分和Beclin衍生肽部分的肽的复合物。在另一个方面,本发明涉及病毒或病毒载体与包含细胞穿透肽(CPP)部分和Beclin衍生肽部分的肽的混合物。在一个具体实施方式中,本发明的复合物或混合物中的病毒或病毒载体是逆转录病毒,特别是慢病毒。具体的慢病毒包括假型慢病毒。在另一个实施方式中,所述病毒或病毒载体是细小病毒,特别是腺相关病毒(AAV)。在另一个实施方式中,所述肽如上所定义,并且更具体地如权利要求中定义,或者所述肽包含SEQIDNO:75、SEQIDNO:77和SEQIDNO:98-101中所示的序列或由所述序列组成。.本发明也涉及包含编码本发明的肽的多核苷酸的核酸构建体。本发明的另一个方面涉及包含本发明的肽和病毒载体的试剂盒。根据以下详细描述,其他方面和实施方式将是显而易见的。附图说明图1.Tat-Beclin1促进各种慢病毒载体的细胞系转导。A)在不存在或存在指示浓度的Tat-乱序(Tat-Scrambled)肽或Tat-Beclin1肽的情况下,用VSV-G-LV(2x105TU/ml)转导HCT116细胞6小时。B)在不存在或存在Tat-乱序肽或Tat-Beclin1肽(5μM)的情况下,用各种滴度的VSV-G-LV转导HCT116细胞。C)在不存在或存在Tat-乱序肽(5μM)、Tat-Beclin1(5μM)、载体融合素-1(6μg/ml)、硫酸鱼精蛋白(4μg/ml)或聚凝胺(3μg/ml)的情况下,用GALVTR-LV或RD114TR-LV(106TU/ml)转导HCT116细胞。在这三组中,转导效率在三至四天后通过监测GFP表达来评价。所有数据均表示为以一式两份进行的三个独立实验的平均值±标准误差均值(SEM)。图2.Tat-Beclin1提高hCD34+HSPC的慢病毒转导而没有明显的细胞毒性。A)在不存在(无)或存在纤维连接蛋白(7μg/cm2)或指示浓度的Tat-乱序肽或Tat-Beclin1肽的情况下,用高度纯化的VSV-G-LVs(2x107ig/ml,MOI240)感染hCD34+细胞。三至五天后,通过监测GFP表达评价转导效率。数据表示为以一式两份进行的三个独立实验(三个UCB供体)的平均值±SEM。B)在不存在或存在Tat-Beclin1(10μM)的情况下,用VSV-G-LV(2x105TU/ml)一式两份转导hCD34+细胞(六个UCB供体)。数据表示为每个UCB供体的平均转导水平。棒指示分布的平均值。P-值利用Mann-Whitney检验确定(**P<0.01)。C)在集落形成细胞(CFC)分析中转导的hCD34+细胞的分化。结果表示在不存在或存在纤维连接蛋白(7μg/cm2)、Tat-乱序肽(10μM)或Tat-Beclin1肽(10μM)的情况下用VSV-G-LV(5x107ig/ml)转导后,对1000个铺板细胞获得的不同类型集落的平均数。数据是以一式两份进行的三个独立实验(三个UCB供体)的平均值±SEM。图3.Tat-Beclin1促进慢病毒粒子与靶细胞的粘附和融合。A)病毒融合分析。在不存在(无)或存在10μM的Tat-乱序肽或Tat-Beclin1的情况下,将细胞与VSV-G-BLAM-LV一起在37℃下温育2.5hr。接着,通过使用流式细胞术监测靶细胞中切割的CCF2底物的百分比来评估病毒融合效率。数据表示为以一式两份进行的三个独立实验(三个用于hCD34+细胞的UCB供体)的平均值±SEM。B)粘附分析。在不存在或存在Tat-乱序肽或Tat-Beclin1(5μM)的情况下,将HCT116细胞在37℃下预温育30min。接着,在不存在或存在Tat-乱序肽或Tat-Beclin1(5μM)的情况下,将细胞与VSV-G-LV(75ng的p24)一起在4℃下温育2.5hr。作为阳性对照,将一种条件的HCT116细胞与混合有聚集肽载体融合素-1(12μg/ml)的VSV-G-LV的冷溶液一起温育。数据表示为以一式两份进行的三个独立实验的平均值±SEM。C)病毒下拉(pull-down)分析。VSV-G-LV粒子与Tat-乱序肽(10μM)、Tat-Beclin1(10μM)或阳性对照载体融合素-1(10μM)混合。短暂离心(15,000g)后,使用HIV-1p24ELISA试剂盒定量沉淀的病毒粒子的百分比。数据针对p24输入水平归一化并表示为以一式两份进行的三个独立实验的平均值±SEM。图4.Tat-Beclin1和各种衍生物的病毒转导增强剂活性。HCT116细胞如图1A中所述,在不存在(无)或存在2.5μM(浅灰色柱状图)或5μM(黑色柱状图)的指示肽的情况下被转导。数据表示为以一式两份进行的三个独立实验的平均值±SEM。图5.Tat-Beclin1变体的病毒转导效率。A)人类Beclin1蛋白从残基246至322的一级序列(智人(homosapiens),NP_003757)。突变H275E、S279D和Q281E以粗斜体突出显示。二级结构元件在序列上方指示(α螺旋(α)、环(L)和β片层(β))。在所述结构元件上方,黑线表示各Tat-Beclin1变体的蛋白质序列覆盖度。B)HCT116细胞如图1A中所述在下述情况下被转导:不存在(无)或存在2.5μM(浅灰色柱状图)或5μM(黑色柱状图)的指示肽,或C)与浓度递增的Tat-Bec(267-296)一起,或D)与2.5μM的指示肽一起。对于所有组,数据均表示为以一式两份进行的三个独立实验的平均值±SEM。图6.Tat-Beclin1提高重组腺相关病毒的细胞系转导。A)在不存在或存在指示浓度的Tat-乱序肽或Tat-Beclin1肽的情况下,将293T细胞用表达GFP的重组AAV8(MOI1000)转导6小时。3至4天后,通过监测GFP表达评价转导效率。数据表示为以一式两份进行的三个独立实验的平均值±SEM并利用线性回归建模进行分析。图7.Tat-Beclin1促进慢病毒转导的最佳剂量不诱导自噬。将表达mCherry-eGFP-LC3融合蛋白的HEK293T细胞在不存在或存在Tat-Beclin1(5μM)的情况下或在Earle's平衡盐溶液(EBSS)中温育6小时。接着,使用成像流式细胞仪分析细胞。在明视野中、在mCherry荧光中和在SSC通道中获取细胞的图像。数据表示为在每个单个细胞中观察到的mCherry斑点的数量。棒表示从三个独立实验获得的分布的平均值。P-值利用Mann-Whitney检验确定。n.s.未统计。图8.Beclin2衍生肽在非常低的剂量下促进VSV-G-LV的细胞系转导。A)Tat-Beclin1、Tat-Beclin1野生型(Tat-BecWT)和Tat-Beclin2野生型(Tat-Bec2WT)肽的一级序列。B)在不存在或存在指示浓度的Tat-乱序肽(Tat-Scr)、Tat-Beclin1、Tat-Beclin1野生型肽(Tat-BecWT)、Tat-乱序肽2(Tat-Scr2WT)和Tat-Beclin2野生型(Tat-Bec2WT)肽的情况下,将HCT116细胞用VSV-G-LV(2x105TU/ml)转导六小时。所有数据均表示为以一式两份进行的三个独立实验的平均值±标准误差均值(SEM)。具体实施方式本发明涉及非天然存在的合成肽,其包含以下各项或由以下组成:(i)CPP部分;和(ii)Beclin衍生肽部分。这两个部分共价结合,任选地经由氨基酸或非氨基酸接头共价结合。另外,根据本发明,所述肽可以按任何取向包含这两个部分(例如,从N-端到C-端:CPP部分–Beclin衍生部分;或Beclin衍生部分–CPP部分)。细胞穿透肽(CPP)部分在本发明的环境下,术语“细胞穿透肽”或“CPP”是指可变长度的肽链,不限于且独立于所述肽执行其功能的机制,已知或可以证明它提高或促进货物(例如肽、核酸、病毒或任何其他货物)从细胞外室跨细胞膜的传递,从而将货物运送到细胞中,在此所述货物可以引起至少一种可测量的生物反应或功能。CPP通常可以具有含有高相对丰度的带正电荷氨基酸例如赖氨酸或精氨酸的氨基酸组成,或可以具有包含极性/带电氨基酸和非极性疏水氨基酸的交替模式的序列。因此,在本发明的一个具体实施方式中,所述CPP部分由具有5至50个氨基酸残基、特别是10至20个氨基酸残基的氨基酸序列组成。在一个进一步的具体实施方式中,所述CPP部分具有包含带正电荷的残基例如赖氨酸和精氨酸残基的氨基酸序列。在另一个实施方式中,所述CPP部分具有带正电荷的残基例如赖氨酸或精氨酸残基和非极性的疏水性残基例如丙氨酸和亮氨酸残基相互交替的氨基酸序列。所述CPP部分可以源自于能够跨细胞膜易位的天然存在的蛋白质,例如果蝇同源框蛋白质触角足(Antennapedia)(转录因子)、病毒蛋白质如HIV-1转录因子TAT和来自HSV的衣壳蛋白VP22-1,和/或它们可以是合成来源的,例如源自于嵌合蛋白或合成多肽例如聚精氨酸。关于CPP的综述可以在Milletti,2012中找到。在一个具体实施方式中,所述CPP部分是由人免疫缺陷病毒(HIV)1型的反式转录激活因子(tat)肽衍生的肽。在本发明的环境下,由tat肽衍生的肽是包含具有细胞穿透性质的氨基酸序列的tat片段。特别地,所述tat衍生肽是包含tat的氨基酸47-57(SEQIDNO:1)、48-60(SEQIDNO:2)或49-57(SEQIDNO:3)或由所述氨基酸组成的肽。在本发明的实践中可以没有限制地使用其他CPP,包括MAP-或触角足衍生的肽。表1列出了可以使用的各种代表性肽。表1:CPP列表在一个具体实施方式中,所述CPP部分包含选自SEQIDNO:1-62中任一种的肽序列、或其与SEQIDNO:1-62中的任一种具有至少50%、至少60%、至少70%、至少80%、至少85%、至少90%或至少95%序列同一性并保留至少一部分所述序列增强货物分子传递到细胞内的能力的变体,或由所述肽序列或变体组成。在一个具体实施方式中,所述CPP部分选自由SEQIDNO:1至SEQIDNO:4组成的组,特别选自SEQIDNO:1和SEQIDNO:4。Beclin肽部分在本发明的环境下,所述Beclin衍生肽部分与来源于Beclin蛋白的氨基酸序列相对应。在本发明的环境下,Beclin肽的“功能性变体”或“衍生物”是当所述功能性变体或所述衍生物与CPP部分融合时,能够改善病毒的转导效率的肽。特别地,当与CPP部分融合时,所述功能性变体能够将病毒的转导效率改善至少10%、至少20%或至少30%或更多,优选至少30%。更特别地,当与CPP部分融合时,所述功能性变体能够将用来自水疱性口炎病毒(VSV-G)的包膜糖蛋白(GP)假型化的HIV-1衍生的慢病毒载体(LV)的转导效率改善至少10%、至少20%或至少30%或更多,优选至少30%。更加特别地,当与CPP部分融合时,所述功能性变体能够将用来自水疱性口炎病毒(VSV-G)的包膜糖蛋白(GP)假型化的HIV-1衍生的慢病毒载体(LV)对hCD34+细胞的转导效率改善至少10%、至少20%或至少30%或更多。在一个进一步的具体实施方式中,Beclin肽的功能性变体还与亲本Beclin肽(即,其所源自的肽)的序列,例如与SEQIDNO:65或89所示的Beclin肽的序列,具有至少50%、至少60%、至少70%、至少75%、至少80%和最特别至少83%的序列同一性。在一个具体实施方式中,所述Beclin衍生肽部分的序列包含下述氨基酸序列,其中在亲本Beclin肽中,例如在SEQIDNO:65或89所示的序列中,做出了1至6个氨基酸残基的添加、缺失或取代。在一个具体方面,所述Beclin衍生肽部分是在SEQIDNO:65或89中包含1、2、3、4、5或6个氨基酸取代、例如4、5或6个氨基酸取代的Beclin-1或Beclin-2肽部分。根据一个具体实施方式,所述Beclin衍生部分长度在14至22个氨基酸残基之间,例如16至20个氨基酸残基长度,特别是由长度为16、17、18、19或20个氨基酸残基组成的肽。在一个具体实施方式中,所述Beclin衍生部分长度是18个氨基酸残基。在一个具体方面,所述Beclin衍生肽部分包含通式(I)的序列或由通式(I)的序列组成:N1N2N3N4N5N6TFN9IN11N12N13GN15N16N17N18(I)其中:N1是极性氨基酸或是I,特别是T或I,更特别是I;N2是极性氨基酸,特别是N、D或S,更特别是N;N3是疏水性氨基酸或C,特别是V、C或I,更特别是C;N4是疏水性氨基酸,特别是F或L,更特别是F;N5是极性氨基酸,特别是N、T、S、R或Q,更特别是T;N6是疏水性氨基酸,特别是A或V,更特别是A;N9是极性氨基酸,特别是H、E或T,更特别是E;N11是W,S,G或R,特别是W;N12是极性氨基酸或是V,特别是H、V、D、Q或E,更特别是V;N13是极性氨基酸或是A,特别是S、E、D、A,更特别是E;N15是Q、P、S或E,特别是P;N16是疏水性氨基酸,特别是F、L、V或I,更特别是L;N17是疏水性氨基酸,特别是G、A或P,更特别是G;N18是T、V或I,特别是V。在另一个具体方面,所述Beclin衍生肽部分包含通式(II)的序列或由通式(II)的序列组成:N1N2N3FN5N6TFN9IN11N12N13GN15N16N17N18(II)其中:N1是极性氨基酸或isI,特别是T或I,更特别是I;N2是极性氨基酸,特别是N、D或S,更特别是N;N3是疏水性氨基酸,特别是V、C或I,更特别是C;N5是极性氨基酸,特别是N、T、S、R或Q,更特别是T;N6是疏水性氨基酸,特别是A或V,更特别是A;N9是极性氨基酸,特别是E或T,更特别是E;N11是W、S、G或R,特别是W;N12是极性氨基酸或是V,特别是H、V、D、Q或E,更特别是V;N13是极性氨基酸或是A,特别是S、E、D、A,更特别是E;N15是P或S,特别是P;N16是疏水性氨基酸,优选L、V或I,更特别是L;N17是疏水性氨基酸,优选G、A或P,更特别是G;N18是疏水性氨基酸,特别是V或I,更特别是V.术语“极性氨基酸”是指包含偏好驻留在含水(即水)环境中的亲水侧链的氨基酸。因此这些侧链因此可以参与氢键相互作用。术语“极性氨基酸”包括“极性带电氨基酸”例如D、E、K、R、H和“极性不带电氨基酸”例如S、T、Y、C、N和Q。术语“疏水性氨基酸”是指包含在生理pH下不带电荷的非极性侧链的氨基酸。疏水性侧链是化学无反应性的,倾向于聚集而不是暴露于水性环境。术语“疏水性氨基酸”包含G、A、L、I、V、P、F、W和M。用于本文中时,“氨基酸”有时使用标准单字母代码来指定:丙氨酸(A),丝氨酸(S),苏氨酸(T),天冬氨酸(D),谷氨酸(E),天冬酰胺(N),谷氨酰胺(Q),精氨酸(R),赖氨酸(K),异亮氨酸(I),亮氨酸(L),甲硫氨酸(M),缬氨酸(V),苯丙氨酸(F),酪氨酸(Y),色氨酸(W),脯氨酸(P),甘氨酸(G),组氨酸(H),半胱氨酸(C)。包括合成和非天然存在的氨基酸类似物(和/或肽连接)。在一个具体实施方式中,所述Beclin衍生部分源自于人Beclin蛋白,例如SEQIDNO:63所示的人Beclin-1蛋白或SEQIDNO:64所示的人Beclin-2蛋白:SEQIDNO:63:MEGSKTSNNSTMQVSFVCQRCSQPLKLDTSFKILDRVTIQELTAPLLTTAQAKPGETQEEETNSGEEPFIETPRQDGVSRRFIPPARMMSTESANSFTLIGEASDGGTMENLSRRLKVTGDLFDIMSGQTDVDHPLCEECTDTLLDQLDTQLNVTENECQNYKRCLEILEQMNEDDSEQLQMELKELALEEERLIQELEDVEKNRKIVAENLEKVQAEAERLDQEEAQYQREYSEFKRQQLELDDELKSVENQMRYAQTQLDKLKKTNVFNATFHIWHSGQFGTINNFRLGRLPSVPVEWNEINAAWGQTVLLLHALANKMGLKFQRYRLVPYGNHSYLESLTDKSKELPLYCSGGLRFFWDNKFDHAMVAFLDCVQQFKEEVEKGETRFCLPYRMDVEKGKIEDTGGSGGSYSIKTQFNSEEQWTKALKFMLTNLKWGLAWVSSQFYNKSEQIDNO:64:MSSIRFLCQRCHQALKLSGSSESRSLPAAPAPTSGQAEPGDTREPGVTTREVTDAEEQQDGASSRSPPGDGSVSKGHANIFTLLGELGAMHMLSSIQKAAGDIFDIVSGQAVVDHPLCEECTDSLLEQLDIQLALTEADSQNYQRCLETGELATSEDEAAALRAELRDLELEEARLVQELEDVDRNNARAAADLQAAQAEAAELDQQERQHYRDYSALKRQQLELLDQLGNVENQLQYARVQRDRLKEINCFTATFEIWVEGPLGVINNFRLGRLPTVRVGWNEINTAWGQAALLLLTLANTIGLQFQRYRLIPCGNHSYLKSLTDDRTELPLFCYGGQDVFLNNKYDRAMVAFLDCMQQFKEEAEKGELGLSLPYGIQVETGLMEDVGGRGECYSIRTHLNTQELWTKALKFMLINFKWSLIWVASRYQK在一个具体实施方式中,所述Beclin-2衍生肽部分包括SEQIDNO:64中的氨基酸249至266(下划线序列:INCFTATFEIWVEGPLGV被称为SEQIDNO:89)。在一个具体实施方式中,所述Beclin-2衍生肽部分包含SEQIDNO:89中所示的序列或由所述序列组成,或包含对应于如上定义的其功能性变体的序列或由所述序列组成。在一个具体实施方式中,所述Beclin-2衍生肽的功能性变体在其对应于SEQIDNO:64的氨基酸252和256的位置具有苯丙氨酸残基。在一个具体实施方式中,所述Beclin-2衍生肽部分或其功能性变体源自于任何物种的Beclin-2,包括但不限于人、小鼠、兔、猪、马、熊猫或牛Beclin-2。下表2对应于人Beclin-2序列的249至266位氨基酸与小鼠、兔、猪、马,熊猫和牛的相应序列的比对。表2:Beclin-2序列的比对人Beclin-2(249-266)INCFTATFEIWVEGPLGVSEQIDNO:89小鼠Beclin-2(262-279)TNIFNATFTISDEGPLGVSEQIDNO:92马Beclin-2(253-270)INVFSVTFEIGHSGPVGVSEQIDNO:93熊猫Beclin-2(645-662)TNVFNATFEIRHDGPVGISEQIDNO:94猪Beclin-2(244-261)TNVFRATFEIRHAGPIAISEQIDNO:95牛Beclin-2(248-265)TDVFNATFEIWQDGPLPVSEQIDNO:96兔Beclin-2(238-255)TSIFQVTFEIREEGSVGISEQIDNO:97在一个具体实施方式中,所述Beclin衍生肽源自于选自表2的序列的Beclin-2肽。在一个具体实施方式中,所述Beclin-1衍生肽部分包括Beclin-1的β1片层,或Beclin-1的β1片层的功能性变体,其位于SEQIDNO:63中的氨基酸274至279。在另一个具体实施方式中,所述Beclin-1衍生肽部分包括Beclin-1的L1环和β1片层。在另一个实施方式中,所述Beclin-1衍生肽部分包括SEQIDNO:63的氨基酸250-262(对应于Beclin-1的α1螺旋)的至少C末部分或全部、Beclin的L1环和β1片层。SEQIDNO:63中下划线的序列在下面的描述中被称为SEQIDNO:65(SEQIDNO:65:TNVFNATFHIWHSGQFGT)。它对应于Beclin-1的进化保守结构域(ECD267-284)的片段。在一个具体实施方式中,所述Beclin-1衍生肽部分包含SEQIDNO:65中所示的序列或由所述序列组成,或包含对应于如上定义的其功能性变体的序列或由所述序列组成。在一个具体实施方式中,所述Beclin-1衍生肽的功能性变体在它对应于SEQIDNO:63的氨基酸270和274的位置具有苯丙氨酸残基。SEQIDNO:66所示的Beclin-1衍生肽是本发明的说明性功能性变体,其对应于在SEQIDNO:65的9、13和15位(对应于SEQIDNO:63的275、279和281位)处有取代并在对应于SEQIDNO:65的270和274位的氨基酸位置处维持苯丙氨酸残基的SEQIDNO:65:TNVFNATFEIWHDGEFGTSEQIDNO:66在一个具体方面,所述Beclin-1衍生肽部分可包含10至60个氨基酸,特别是15至55个,特别是18至50个,特别是18至49个氨基酸(例如18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48和49个氨基酸),特别是18至35个氨基酸,更特别是18至33个氨基酸(例如18、19、20、21、22、23、24、25、26、27、28、29、30、31、32和33个氨基酸)。在一个具体实施方式中,Beclin-1衍生肽部分包含SEQIDNO:63的氨基酸270-282,特别是氨基酸267-284(即SEQIDNO:65),或其如上所述的变体,以及与氨基酸267-284的任一端或两端邻接的所述Beclin-1蛋白的至少一个或多个氨基酸。例如,除了SEQIDNO:65中所示的序列之外,所述Beclin-1衍生肽部分还可以特别包含与SEQIDNO:63中的氨基酸267-284邻接的1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16或17个氨基酸。例如,所述Beclin-1衍生部分还可以包括氨基酸250-266或256-266。可选地或在前面句子中提及的氨基酸之外,它可以在SEQIDNO:65的序列或其功能性变体例如SEQIDNO:66之外,还包括SEQIDNO:63的氨基酸285-296或285-298。此外,本发明还设想了SEQIDNO:65的功能性变体,其包含SEQIDNO:65中显示的所述序列的一部分,例如包含SEQIDNO:63的氨基酸268-284、269-284、270-284、267-283或267-282的功能性变体。另外,所述功能性变体可以是SEQIDNO:66中所示序列的变体,其中从其N端或C端或从两端缺失了1、2或3个氨基酸。本发明的Beclin-1肽的示例性功能性变体包括:FNATFEIWHDGEFGTSEQIDNO:67TNVFNATFEIWHDGEFSEQIDNO:68YAQTQLDKLKKTNVFNATFEIWHDGEFGTSEQIDNO:69TNVFNATFEIWHDGEFGTINNFRLGRLPSVSEQIDNO:70VENQMRYAQTQLDKLKKTNVFNATFEIWHDGEFSEQIDNO:71FNATFEIWHDGEFGTINNFRLGRLPSVPVSEQIDNO:72FEIWHDGEFGTINNFRLGRLPSVPVSEQIDNO:73融合肽如上所述,本发明的肽包含共价连接在一起的CPP部分和Beclin衍生部分,因此是融合肽。所述肽的这两个部分的连接可以通过共价键直接完成或经由接头部分完成。SEQIDNO:74的肽是所述两个肽部分直接连接的例子,其中所述CPP部分是SEQIDNO:1中所示的Tat序列,并且所述Beclin衍生的肽部分由SEQIDNO:66中所示的氨基酸序列与SEQIDNO:63的氨基酸285-296融合组成:YGRKKRRQRRRTNVFNATFEIWHDGEFGTINNFRLGRLPSVSEQIDNO:74SEQIDNO:90的肽是所述两个肽部分的直接连接的例子,其中所述CPP部分是SEQIDNO:1中所示的Tat序列,并且所述Beclin衍生肽部分由SEQIDNO:89中所示的氨基酸序列组成:YGRKKRRQRRRINCFTATFEIWVEGPLGVSEQIDNO:90在一个具体实施方式中,所述肽包含接头。所述接头可以是包含1至25个氨基酸、特别是1至5个氨基酸的肽。在一个具体实施方式中,所述接头是单个中性(即在生理pH下为中性)氨基酸,例如G、A、V、S、Y或T,特别是G。或者,所述接头可以是中性氨基酸的二肽,例如选自GG、AA、GA、AG、AS、AY、GS、GT、GV、AV、SV、TV、VG、VA和VT的二肽。在另一个具体实施方式中,所述接头是非肽接头,例如-(CH2)n-接头,其中n是在1和6之间的整数。从N-端到C-端,本发明的肽可依次包含:-CPP部分和Beclin衍生部分,任选地经由如上所述的接头连接;或-Beclin衍生部分和CPP部分,任选地经由如上所述的接头连接。在一个具体实施方式中,本发明的肽从其N-端到其C-端包含CPP部分和Beclin衍生部分,任选地经由如上所述的接头连接。在一个进一步的具体实施方式中,本发明的肽依次包含CPP部分、接头(特别是二肽接头,例如GG二肽)和Beclin衍生部分。在另一个具体实施方式中,本发明的肽从其N-端到其C-端包含Beclin衍生部分和CPP部分,任选地经由如上所述的接头连接。在一个进一步的具体实施方式中,本发明的肽依次包含Beclin衍生部分、接头(特别是二肽接头,例如GG二肽)和CPP部分。在一个具体实施方式中,本发明的肽是一种融合肽,其依次包含:(i)为Tat序列的CPP部分(例如SEQIDNO:1、2和3所示序列之一,特别是SEQIDNO:1所示的序列)或MAP序列(例如SEQIDNO:4或5),(ii)二肽接头例如GG二肽,和(iii)式(I)或(II)的Beclin衍生部分,例如Beclin-1衍生部分如SEQIDNO:65-73之一或Beclin-2衍生部分如SEQIDNO:89。特别地,本发明中实施的肽是以下各项所示的肽:SEQIDNO:75:YGRKKRRQRRRGGTNVFNATFEIWHDGEFGT;SEQIDNO:76:KLALKLALKALKAALKAGTNVFNATFEIWHDGEFGT;SEQIDNO:77:YGRKKRRQRRRGGTNVFNATFHIWHSGQFGT;SEQIDNO:78:YGRKKRRQRRRGGYAQTQLDKLKKTNVFNATFEIWHDGEFGT;SEQIDNO:79:YGRKKRRQRRRGGTNVFNATFEIWHDGEFGTINNFRLGRLPSV;SEQIDNO:80:YGRKKRRQRRRGGTNVFNATFHIWHSGQFGTINNFRLGRLPSV;SEQIDNO:81:YGRKKRRQRRRGGVENQMRYAQTQLDKLKKTNVFNATFEIWHDGEF;SEQIDNO:82:YGRKKRRQRRRGGFEIWHDGEFGTINNFRLGRLPSVPV;SEQIDNO:83:YGRKKRRQRRRGGFNATFEIWHDGEFGTINNFRLGRLPSVPV;或SEQIDNO:91:YGRKKRRQRRRGGINCFTATFEIWVEGPLGV.根据一个具体实施方式,本发明还包括上文定义的肽的逆向、反转或逆向反转(retro-inverso)衍生物,其保留了本文公开的转导促进性质。在一个具体实施方式中,本发明涉及如上定义的肽的逆向反转衍生物。特别地,本发明的肽的逆向反转衍生物适合于体内使用,因为它们更耐蛋白水解性降解。所述肽可以包含至少一个D氨基酸以及亚氨氨基酸和稀有氨基酸。本发明也涉及根据本发明的肽的肽模拟物。这些可以例如通过修饰一个或多个肽键为特征,例如通过反向肽键或通过酯键。本发明还包括上述肽的衍生物,其包含不同于α-氨基酸的氨基酸,例如β或γ-氨基酸。融合肽的用途本发明的肽促进细胞的病毒感染。用于本文中时,“病毒”涉及天然存在的病毒以及人造病毒。例如,副粘病毒(例如呼吸道合胞病毒、麻疹病毒)、正粘病毒(例如流感病毒)、黄病毒(例如丙型肝炎病毒)、嗜肝DNA病毒(例如乙型肝炎病毒)、弹状病毒(例如狂犬病病毒、VSV)、冠状病毒(例如SARS)、披膜病毒(例如辛德毕斯(Sindbis)病毒、基孔肯雅(Chikungunya)病毒)、丝状病毒(例如埃博拉病毒)、砂粒病毒、痘病毒、疱疹病毒、布尼亚病毒、博尔纳病毒(bornavirus)、动脉炎病毒、杆状病毒、细小病毒例如腺相关病毒。根据一个具体实施方式,所述病毒是人造病毒,其可以例如包含货物,例如可用于治疗、诊断或任何其他目的(例如可用于在靶细胞内进行功能研究)的货物。说明性的货物包括核酸货物,例如编码产物、特别是基因治疗产物(例如蛋白质或RNA,例如反义RNA或shRNA)或诊断产物的DNA或RNA序列。此外,根据本发明,所述病毒可以是病毒样粒子(或VLP),其还可以含有货物例如蛋白质货物、核酸货物(例如DNA或RNA货物)、诊断货物或药物货物。在本发明的环境下,病毒是有包膜或无包膜病毒。细小病毒例如腺相关病毒(或AAV)是说明性的无包膜病毒。在一个优选实施方式中,所述病毒是包膜病毒。在优选实施方式中,所述病毒是逆转录病毒,特别是慢病毒。本发明人已经表明,本发明的肽可促进用来自水泡性口炎病毒(VSV-G)、修饰的猫内源性逆转录病毒(RD114TR)和修饰的长臂猿白血病病毒(GALVTR)的包膜糖蛋白(GP)假型化的HIV-1衍生的慢病毒载体(LV)感染真核细胞。本发明人甚至已经表明,本发明的肽有效地促进其他病毒例如细小病毒、包括腺相关病毒的进入,由此证明它们的广泛效率。鉴于用本发明的肽获得的转导效率和在所公开的实验中使用的病毒载体和GP的多样性,显然本发明的肽可用作提高包膜和无包膜病毒在真核细胞中的转导效率的通用工具。因此,也预期本发明的肽可以促进用许多其他病毒或其他假型病毒,例如用各种包膜糖蛋白诸如兼嗜性鼠白血病病毒GP(A-MLV)或修饰的狒狒内源性病毒GP(BaEVTR)假型化的慢病毒(Levy,2015),或用无包膜病毒例如细小病毒、特别是AAV例如重组AAV载体,感染真核细胞。所述靶细胞可以是任何种类的真核细胞,例如哺乳动物细胞,特别是人、小鼠、大鼠、猴、狗或仓鼠细胞。在一个具体实施方式中,所述靶细胞是CD34+细胞,特别是从他/她的造血谱系需要基因治疗的患者采集的CD34+细胞。其他代表性的非限制性靶组织/细胞是皮肤、肌肉、肝脏、眼睛、神经元、淋巴细胞、成纤维细胞、角化细胞、脂肪细胞、成肌细胞、肝细胞、肿瘤细胞并更通常是任何已知或将被鉴定为病毒的靶标的真核细胞。本发明人在下面的实验部分中表明,得益于本发明的肽,可以获得多种多样的细胞的转导,从而证明了它们的广泛效率和适用性。在本文公开的方法中,本发明的肽以有效量使用。术语肽的“有效量”在本文中表示显著增加病毒载体的转导效率所需的量。这种有效量通常将取决于所测试的特定肽、靶细胞和实施的病毒载体。特别地,所述有效量是诱导病毒载体的转导效率增加而不诱导或增加自噬过程的肽量。该量可以根据本领域公知的方法确定,特别是根据实施报道基因分析的上述方法和实施例中所示。例如,本发明人意外表明以前公开的Tat-Beclin1肽(Shoji-Kawata等,2013)以低浓度,通常取决于被转导的细胞类型而以在1和20μM、例如2.5和20μM之间的浓度,最佳地促进VSV-G-LV或GALVTR-LV对HCT116细胞或CD34+细胞的病毒转导。此外,本发明人已经表明,所述Tat-Beclin-2肽在0.01μM至约10μM之间、特别是0.1和5μM之间的甚至更低剂量下,也是慢病毒转导的有效增强剂。使用本发明肽的典型浓度范围包括0.01μM和20μM之间的浓度,例如1和20μM之间,例如2.5和20μM之间,特别是3和15μM之间,更特别是4和12μM之间,例如4、5、6、7、8、9或10μM的浓度。在一个具体实施方式中,本发明的肽以约5μM或约10μM的浓度使用。在一个具体实施方式中,本发明的肽,特别是Tat-Beclin-1肽,以0.01μM和5μM之间、特别是1μM和5μM之间的有效量使用。根据另一个方面,本发明涉及本发明的肽与病毒粒子的复合物,所述病毒粒子特别是非包膜(例如细小病毒,例如AAV载体)或包膜病毒粒子,更特别是用于基因治疗的包膜病毒载体。此外,本发明的另一个方面涉及这样的复合物的制备方法,其包含将所述肽与病毒粒子混合。根据另一个方面,本发明涉及本发明的肽与病毒粒子(特别是包膜病毒粒子或无包膜病毒粒子,更特别是与用于基因治疗的包膜病毒载体)和细胞的混合物。此外,本发明的另一个方面涉及这样的混合物的制备方法,其包含将所述肽与病毒粒子和所述细胞混合。本发明的肽可用于药物组合物中。因此,本发明涉及包含如上定义的肽和合适的可药用运载工具的组合物。本发明的药物组合物含有一种或多种本发明的肽或所述肽的生理可接受的盐。本发明的药物组合物也可以含有药物常用的助剂,其例如对所述组合物的溶解度、稳定性或无菌性有贡献或增加摄入体内的效率。本发明的一个方面也涉及如上定义的肽,其用作药物。在一个具体实施方式中,所述药物用于增加基因治疗病毒载体的效率(D'Costa等,2009)。含有所述肽的药物组合物的形式和含量取决于施用途径。优选地,选择其中所述肽在非降解条件下到达靶位点的盖仑制剂(galenicformulations)和应用形式。所述药物可以作为注射剂、滴剂、喷雾剂、片剂、栓剂、乳膏剂、软膏剂、凝胶剂等局部施用。有可能作为单次大剂量(bolus)给药或在一段时间内反复施用。本发明的肽、复合物或药物组合物或药物可以经由局部或全身途径体内施用,例如通过将其经由肌内、静脉内、动脉内、腹膜内或颅内途径施用注射。因此,本发明也涉及一种用于基因治疗的方法,其包含向有需要的患者施用如上所述的肽、复合物或药物组合物。所述方法还包含在施用本发明的肽之前、之后或一起施用用于基因治疗的病毒载体。如本领域中充分理解的,本发明的用于基因治疗的病毒或病毒载体包含治疗基因。根据一个方面,所述肽、复合物或药物组合物或药物用于细胞治疗的离体方法中。在这个方面,所述肽、复合物、药物组合物或药物用于增强基因治疗病毒载体进入从患者采集的细胞中,其中所述细胞旨在由于所述基因治疗病毒载体而被遗传修饰。在一个具体实施方式中,所述细胞是造血干/祖细胞,如hCD34+细胞。所述细胞可以与本发明的肽和基因治疗病毒载体混合,以校正在所述细胞中检测到的任何缺陷。特别地,这种离体方法可用于在用肽和病毒载体例如HIV-1衍生的慢病毒载体的混合物转导之后给患者静脉注射遗传修饰的hCD34+细胞,表达编码可用于治疗疾病的产物(例如蛋白质或治疗性RNA)的目标基因。例如,所述治疗性产物可以是纠正WiskottAldrich综合征的Wiskott-Aldrich综合症蛋白质、纠正严重联合免疫缺陷1的IL2受体γ链、纠正慢性肉芽肿病的gp91phox蛋白质、纠正腺苷脱氨酶缺乏症(或ADA-SCID)的腺苷脱氨酶(ADA)、纠正地中海贫血的β-珠蛋白、纠正镰状细胞病的β-珠蛋白或γ-珠蛋白、纠正Fanconi贫血的Fanconi贫血蛋白(例如FA-A)、纠正儿童脑部肾上腺脑白质营养不良的ATP结合盒蛋白或纠正异染性脑白质营养不良的芳基硫酸酯酶A。本发明还可以用于其他离体基因治疗,例如基于嵌合抗原受体(CAR)-T细胞的治疗。在一个具体方面,本发明也涉及在培养基中包含如上所述的肽的组合物,所述组合物旨在用作促进病毒或病毒载体、特别是无包膜的或有包膜的病毒或病毒载体对细胞的转导的感染促进剂。因此,本发明也涉及在合适的基质中、特别是在合适的培养基中包含本发明的肽的病毒感染促进剂。根据另一个方面,本发明也涉及编码本发明的肽的分离的多核苷酸。本发明的多核苷酸可以包含不同的核苷酸化学,例如DNA、RNA或化学修饰的核苷酸。在另一个方面,本发明涉及包含与至少一个控制序列操作性连接的多核苷酸的核酸构建体,所述控制序列指导所述肽在表达宿主中的产生。术语“可操作地连接”在本文中表示这样一种构造:其中控制序列被置于相对于多核苷酸序列的编码序列的适当位置,使得所述控制序列指导本发明的肽的编码序列的表达。在本发明环境中的核酸构建体是单链或双链的核酸分子,其是从天然存在的基因中分离的、或者被修饰而含有原本不会天然存在的核酸链段、或者是合成的。当核酸构建体含有表达本发明的肽编码序列所需的控制序列时,术语核酸构建体与术语“表达盒”同义。根据本发明,控制序列包含表达编码本发明的肽的多核苷酸所必需的所有组分。每个控制序列对于编码多肽的核苷酸序列而言可以是天然的或外来的,或者对于彼此可以是天然的或外来的。这样的控制序列包括但不限于前导序列、聚腺苷酸化序列、前肽序列、启动子、信号肽序列和转录终止子。至少,所述控制序列包括启动子、以及转录和翻译终止信号。为了引入便于所述控制序列与编码多肽的所述核苷酸序列的编码区进行连接的特定限制性位点,所述控制序列可以配有接头。在又一个方面,本发明涉及包含所述核酸构建体的重组表达载体。说明性的重组表达载体包括例如质粒、粘粒和病毒载体。在另一个方面,本发明涉及包含所述核酸或所述重组表达载体的重组宿主细胞。所述宿主细胞可以是原核细胞(例如大肠杆菌(EscherichiaColi)细胞)或真核细胞。在另一个方面,本发明涉及生产本发明的肽的方法,所述方法包含以下步骤:(i)在有利于产生所述肽的条件下培养包含本发明的核酸构建体的宿主细胞;和(ii)回收所述肽。或者,可以使用本领域已知的常规方法通过体外合成产生本发明的肽。各种商业合成仪器是现有的,例如AppliedBiosystemsInc.,Beckman的自动合成器等。下面在实验部分中给出说明性的体外合成,其中通过标准芴基甲氧基-碳酰氯固相肽合成产生所述肽,通过制备型反相HPLC提纯,并通过HPLC和质谱进行分析。通过使用合成仪,天然存在的氨基酸可以被非天然氨基酸取代,所述非天然氨基酸特别是D-异构体(或D-形式)例如D-丙氨酸和D-异亮氨酸、非对映异构体、具有不同长度或官能性的侧链等。制备的具体顺序和方式将由方便性、经济性、纯度要求等来确定。本文中所述的肽用于广泛的应用,例如治疗和诊断应用,并且是用于执行和研究病毒进入细胞的有价值的实验室工具。因此,在一个方面,本发明涉及用于促进病毒或病毒载体对细胞的转导的方法,特别是体外方法,所述方法包含使所述细胞与病毒和如上定义的肽接触,所述肽包含:-细胞穿透肽(CPP)部分;和-Beclin衍生肽部分。在一个具体实施方式中,所述肽不是SEQIDNO:75和SEQIDNO:77中所示的肽。在这个方面的具体实施方式中,所述方法还包含验证所述病毒对细胞的有效转导或转导水平。此外,根据这个方面,本文公开的肽被用于改善目标病毒或病毒载体的感染或转导,其具有如下所述的许多应用。本发明的优选实施方式是本发明的肽作为病毒感染或转导效率的通用增强剂在基于病毒载体系统的常规实验室实践或基因治疗途径中的用途。所述肽在体外、离体或体内增强载体例如为基因治疗、诊断或任何其他目的设计的载体(例如用于功能研究的载体)进入细胞。所述肽可以与病毒载体、例如用于基因治疗或诊断的载体组合施用,并介导所述病毒载体进入靶细胞。所述肽在体外也有用,因为它们促进病毒被细胞摄入。因此它们可用作研究病毒以及它们的作用机制的工具。本发明的另一个实施方式是本发明的肽在诊断方法、特别是如HIV-1和其他包膜病毒的病毒的诊断方法中的用途。因此,本发明也涉及用于增加检测样品中病毒的存在或不存在的基于细胞的分析的灵敏度的体外方法,所述方法包含使样品或来自样品的提取物与细胞和如上定义的肽接触,其中所述肽包含:-细胞穿透肽(CPP)部分;和-Beclin衍生肽部分。在该接触步骤之后,将所述细胞在适当的培养条件下培养。然后可以通过本领域已知的任何方法进行病毒的存在或不存在的检测,例如通过测定细胞中和/或细胞培养基中的病毒水平。本发明的肽增强了病毒粒子的感染滴度并因此增强了它们的细胞摄取,允许检测残余的病毒污染物。因此,它可用于从样品如血清、血液、血浆、精子或组织中分离病毒粒子,所述样品来源于对象,特别是怀疑被病毒、更具体而言是被包膜病毒感染的人类对象。本发明的肽也可用于研究来自水、食物的病毒粒子(禽流感,SARS)或用于生物恐怖主义的任何(包膜或非包膜)病毒。与常规诊断方法相比,可以数倍有利于成功的病毒分离。优选的方法是结合亲和力分析以及从怀疑或已知包含病毒的溶液中定量除去病毒以获得安全溶液的方法。在这样的方法中,本发明的肽优选与载体或柱共价结合。本发明的肽通常可用于增强病毒粒子进入靶细胞。所述肽也可用作病毒粒子感染/转导速率的一般增强剂,所述病毒粒子例如无包膜病毒粒子如细小病毒例如AAV载体,或病毒包膜粒子例如带有外来包膜糖蛋白如VSV-G、GALVTR、RD114TR等的粒子(假粒子)。本发明的上述肽促进所有被分析的包膜病毒粒子的感染率。这允许进行感染实验,特别是在原代细胞中,这在以前是不可行的。因此本发明的肽可用作体外的实验室工具。本发明的肽也可用于增强基于载体系统、特别是基于无包膜或包膜载体系统的离体或体内基因治疗方法中的基因递送率。因此,本发明也涉及如上所述的肽用于基因疗法以促进在有此需要的对象中病毒或病毒载体对真核细胞的感染。本发明的肽可以与病毒或病毒载体组合用于基因治疗。特别地,本发明涉及本发明的肽用于通过基因疗法来治疗疾病的方法,其中本发明的肽与病毒或病毒载体组合使用,所述病毒或病毒载体在其基因组中包含用于治疗所述疾病的适当的治疗性转基因。在一个具体实施方式中,所述治疗通过施用包含上述转基因之一的病毒或病毒载体来进行,用于治疗上面列出的相应疾病。所述肽可以与基因治疗载体同时、分开或相继施用。生成用于基因治疗、尤其是用于干细胞的离体基因治疗的高感染性病毒载体,是困难的程序。特别地,病毒载体、例如用于干细胞的逆转录病毒载体(例如慢病毒载体)的转导效率低。然而,在本发明的肽存在下,干细胞和细胞系可以被病毒载体有效地转导,导致与不含肽的样品相比,基因递送到靶细胞中的效率更高。本发明的肽的另一个优点是它允许使用具有低(或低于最佳)感染滴度的病毒批次,或者允许使用与未实施本发明的肽时相比更少的病毒载体。在本发明的体外和离体方法中,肽可以在有或没有事先固定在固体载体上的情况下使用。有利地,为了获得增加的转导效率,不需要固定。在本发明的体外方法的一个具体实施方式中,将另一种转导改进工具与本发明的肽一起使用。例如,在一个具体实施方式中,用本发明的肽和另一种病毒转导增强剂二者来增加转导效率,所述另一种病毒转导增强剂例如前述的病毒转导增强剂如载体融合素-1(KKALLHAALAHLLALAHHLLALLKKA-NH2:SEQIDNO:84)、人纤连蛋白片段(例如纤维连接蛋白,其是可从例如Clontech商购的)、各种精液来源的病毒感染增强剂(例如,SEVI(GIHKQKEKSRLQGGVLVNEILNHMKRATQIPSYKKLIMY;SEQIDNO:85)、精胶蛋白1肽SEM1(86-107)(DLNALHKTTKSQRHLGGSQQLL;SEQIDNO:86))或衍生自HIV-1包膜糖蛋白的肽(例如EF-C肽(QCKIKQIINMWQ;SEQIDNO:87),P16肽(Ac-NWFDITNWLWYIKKKK-NH2;SEQIDNO:88))。在另一个实施方式中,本发明提供了包含如上定义的肽的试剂盒。所述试剂盒还可以包含病毒或病毒载体。通过以下实施例进一步描述本发明。实施例材料和方法肽和试剂载体融合素-1、Tat-乱序肽、Tat-Beclin1及其衍生物通过标准芴基甲氧基-碳酰氯固相肽合成制备,通过制备型反相HPLC提纯,并通过HPLC和质谱(Genecust,Dudelange,卢森堡)进行分析。7-氨基-放线菌素D(7-AAD)、聚凝胺,硫酸鱼精蛋白和TritonX-100得自Sigma-Aldrich(St-Quentin-Fallavier,法国)。细胞系培养来源于人类结直肠癌的HCT116细胞(CCL-247;ATCC,Manassas,VA)和人胚胎肾HEK293T细胞(Merten,2011)在37℃、5%CO2下在补充有10%热灭活的胎牛血清(FCS)的Dulbecco’s改良Eagle’s培养基(DMEM+Glutamax)(LifeTechnologies,St-Aubin,法国)中培养。病毒载体产生和载体滴定LV如前所述产生(Fenard,2013)。简而言之,利用磷酸钙转染,用四种质粒瞬时转染HEK293T细胞:gagpol(pKLgagpol)和rev(pKrev)表达质粒,转移质粒(pCCLsin.cPPT.hPGK.eGFP.WPRE),和编码VSV-G(pMDG)包膜糖蛋白(GP)、GALVTRGP(pBA.GALV/Ampho-Kana)或RD114TRGP(pHCMV-RD114TR)的质粒。产生24小时后,收获原病毒上清液,过滤(0.45μm)并在-80℃冷冻。通过若干膜类和色谱步骤提纯GFP表达VSV-G-LV已在以前描述(Merten,2011)。使用商业化的ELISA试剂盒(PerkinElmer,Courtaboeuf,法国),通过测量HIV-1p24衣壳含量来确定实体粒子滴度。利用通过流式细胞术(FACSCalibur,BDBiosciences,LePontdeClaix,法国)检测GFP,滴度表示为每毫升的转导单位(TU/ml),或利用滴度表示为每ml的感染性基因组(ig/ml)的Q-PCR(Merten,2011),对HCT116细胞测定感染滴度。细胞系转导对于慢病毒转导,将HCT116细胞在48孔板中在不存在或存在培养添加剂的情况下用所需量的慢病毒载体上清液在6小时期间转导。接下来,将细胞在新鲜培养基中温育并进一步培养3至4天。对于用重组腺相关病毒血清型8(AAV8-GFP)进行的转导实验,将293T细胞在12孔板中在不存在或存在培养添加剂的情况下以感染复数(MOI)为1000进行转导。16小时后,洗涤细胞并在新鲜培养基中进一步培养24小时。在这些实验中,利用流式细胞术(FACSCalibur,BDBiosciences)通过随后的GFP表达来评估转导效率。人CD34+细胞培养和转导根据国际伦理原则和法国国家法律(生命伦理法n°2011-814),按照法国高等研究部(FrenchMinistryofResearchandHigherStudies)的声明N°DC-201-1655,在法国Evry的CentreHospitalierSudFrancilien于无并发症分娩后有知情同意书的情况下采集脐带血(UCB)样本。通过免疫磁性选择分离人CD34+细胞(MiltenyiBiotec,Paris,法国)。如以前所述(Ingrao等,2014),过夜进行hCD34+细胞的预活化。将预活化的细胞铺在96孔板中,并通过添加所需量的混有或未混有目标肽的LV粒子来启动转导。在转导后6小时,通过在每个孔中添加分化培养基来稀释反应物。4-6天后,通过7-AAD标记和测量GFP表达分别评价细胞死亡率和转导效率。病毒下拉分析将在存在培养添加剂的情况下LV粒子的下拉根据以前描述的方案(Yolamanova,2013)进行调整。简而言之,用在室温下平衡的X-Vivo20培养基将VSV-G-LV上清液稀释至p24为100ng/ml。接下来,将1.5ml试管加载500μl不存在或存在10μM所指示的培养添加剂的LV悬液。均化后,将样品在室温下低速(15,000g)离心5分钟。然后,弃去上清液,将沉淀悬浮于100μl新鲜培养基中并在-20℃冷冻。对于每种条件,如上所述使用商业HIV-1p24ELISA试剂盒评价沉淀的p24的量。粘附和BLAM-LV融合分析LV粘附于靶细胞的方案根据以前的研究(Fenard,2013)进行调整。简而言之,将HCT116细胞在不存在或存在Tat-乱序肽或Tat-Beclin1(5μM)的情况下在37℃预温育30min。然后,将细胞在4℃下与不存在或存在培养添加剂的病毒上清液一起进一步温育2.5hr。接着,将细胞用冷PBS1x洗涤3次并在含有1%TritonX-100和蛋白酶混合抑制剂Complete(Rochediagnostics,Meylan,法国)的PBS1x中裂解。使用商业HIV-1p24ELISA试剂盒评价裂解液中的p24含量,并利用DC蛋白分析(Biorad,Ivry-sur-Seine,法国)将数据针对总蛋白质含量归一化。对于病毒融合分析(BLAM-LV),方案以前已被广泛描述(Ingrao等,2014)。CFC分析CFC分析根据制造商的说明书,通过铺板500个转导或未转导的细胞/毫升Methocult(H4434,StemcellTechnologies),一式两份进行。培养2周后,使用倒置显微镜以标准视觉判据计数红系爆式集落形成单位(BFU-E);粒细胞-单核细胞集落形成单位(CFU-GM)以及粒细胞、红细胞、巨噬细胞、巨核细胞集落形成单位(CFU-GEMM)。基于成像流式细胞术(ImageStream)的自噬分析利用瞬时磷酸钙转染方法,用pBABE-puro-mCherry-eGFP-LC3表达质粒转染HEK293T细胞。细胞(5×10E5细胞/孔),在存在或不存在Tat-Beclin1(5μM)下或在Earle's平衡盐溶液(EBSS)中于37℃、5%CO2下温育6h。接着,将细胞在PBS1X中洗涤,固定(1.2%PFA)并用ImageStream(Amniscorporation,Seattle,WA,美国)分析。使用40X放大目镜和最低流速以优化灵敏度,在明视野通道中、在mCherry荧光通道中、和最后SSC通道(742nm)中获取细胞的图像。一旦获取,就用软件处理图像。在直方图上对聚焦图像进行门控,显示在40和90之间的明视野通道的Gradient_RMS特征值。然后使用面积对长宽比的散点图(在明视野通道中)对单个细胞进行门控并去除二联细胞。一旦对单个细胞门控,就利用软件中包含的自动斑点计数向导(automaticspotcountingwizard),在mCherry通道中计数每个细胞上的斑点数。数据作为文本文件输出并用GraphPadPrism处理。结果和讨论低剂量的Tat-Beclin1强烈改善各种假型的慢病毒对细胞系的转导。为了评价TB1(SEQIDNO:75)肽对慢病毒转导的效应,将HCT116细胞在低或高剂量的TB1或对照肽Tat-乱序肽(TS)存在下,用被广泛使用的VSV-G糖蛋白包膜(VSV-G-LV)假型化的慢病毒载体(LV)转导(图1A)。有趣的是,使用低剂量的TB1强烈改善了慢病毒转导效率(10倍)。此外,所述TB1效应在VSV-G-LV从10E5到10E6TU/ml(相当于MOI为0.5至5)的一个对数浓度范围内不可饱和,达到高达84%的转导效率(图1B)。利用LV进行基因转移的一大优势是它们支持用许多异种包膜糖蛋白进行假型化以靶向特定细胞的能力(Levy,2015)。因此,评估了TB1对各种LV假型、即修饰的长臂猿白血病病毒糖蛋白假型化LV(GALVTR-LV)和修饰的RD114猫内源性逆转录病毒糖蛋白假型化LV(RD114TR-LV)的效应。非常重要的是,众所周知这些造血嗜性(hematopoietic-tropic)假型需要培养添加剂来促进有效转导。在粘着性细胞系上,用于促进LV的经典可溶性添加剂是聚凝胺、硫酸鱼精蛋白或最近鉴定的载体融合素-1(Fenard,2013)。如图1C所示,TB1促进GALVTR和RD114TR-LV转导的程度比得上其他培养添加剂。因此,TB1是其他许多细胞系和慢病毒假型的一种有效的慢病毒转导增强剂。Tat-Beclin1促进造血干/祖细胞的安全慢病毒转导。尽管促进细胞系的慢病毒转导对于基础研究是感兴趣的,但另一个强烈的兴趣是优化当前的慢病毒转导临床方案,为了离体基因治疗途径而靶向造血干/祖细胞(HSPC)。如图2A所示,使用高度纯化的VSV-G-LV粒子来转导人CD34+HSPC。在TB1存在下,观察到慢病毒转导增加两倍。TB1促进HSPC的慢病毒转导的最佳剂量限定在10μM左右(图2A-B)。由于以前已经表明TB1肽能够引发称为自死亡(autosis)的特定细胞死亡(Liu,2013),所以对HSPC进行了安全性研究。为此,从在慢病毒转导期间暴露于最佳浓度的纤维连接蛋白、TS或TB1肽的人CD34+细胞实施集落形成细胞(CFC)分析。对于这些实验,我们使用高度纯化的VSV-G-LV来转导CD34+细胞,因为这些载体在这种分析中表现不出可测量的造血毒性(Merten,2011)。如图2C所示,没有所述分析中使用的任何培养添加剂有毒性的证据。CD34+细胞暴露于TB1不影响它们随后作为CFC的生长和髓红样分化。Tat-Beclin1作用于LV与靶细胞膜的粘附和融合步骤。LV进入靶细胞是限速步骤。因此,我们决定测试低剂量的TB1是否能够增强LV与靶细胞膜的粘附和融合。为此,采用BLAM-LV分析(Ingrao,2014)。如图3A所示,TB1强烈增进病毒与细胞系(HCT116)或相关的原代细胞如hCD34+HSPC的融合步骤。接着,通过在4℃下定量与靶细胞相互作用的病毒粒子的数量,我们已经表明,在TB1存在下病毒粘附水平强烈增加,达到比得上使用载体融合素-1的对照条件的水平(图3B)。然而,使用病毒下拉分析,我们已经表明病毒粘附的这种增加不是TB1诱导病毒粒子聚集的结果,就像纳米纤维肽载体融合素-1正是这种情况(图3C)。因此,TB1肽能够通过不涉及病毒粒子聚集的分子机制来增进病毒粘附和融合步骤。设计多种Tat-Beclin1变体及对其在慢病毒转导上的评价。为了评估TB1对慢病毒转导的作用的特异性,合成并在用VSV-G-LV转导HCT116细胞期间测试了Tat转导结构域(Tat)和267-284修饰的beclin1结构域(Bec)。如图4所示,Tat和Bec肽都不能促进慢病毒转导。因此,TB1对慢病毒转导的正面效应不是由于Tat的细胞穿透肽(CPP)活性。同样,Beclin1结构域必须与转导结构域连接才能发挥其效应,提示它在细胞内起作用,必然是通过如Shoji-Kawata研究中所述与GAPR-1蛋白的特异性相互作用或通过与有待鉴定的另一种细胞配偶体的相互作用。为了增加它的肽溶解度,Shoji-Kawata和同事在TB1的267-284Beclin1结构域中引入了三个突变,即H275E、S279D和Q281E(WO2013/119377,Shoji-Kawata等,2013)。为了评价这些突变对病毒转导增强剂活性的影响,将人Beclin1蛋白的野生型267-284结构域与Tat融合(Tat-BecWT)。如图4所示,Tat-BecWT能够在2.5μM的浓度下与TB1同样有效地促进慢病毒转导。然而,与TB1相比,这种肽在5μM的浓度下不再有活性。不排除这三个突变可以改善与GAPR-1蛋白或另一种关键配偶体的相互作用,导致更好的病毒转导增强剂活性。实际上,这些突变使Beclin1结构域与病毒因子HIV-1Nef蛋白的相互作用增加了25至30%(参见Shoji-Kawata等,2013,补充图1d)。为了进一步了解TB1对病毒转导的作用机制,评价了两个苯丙氨酸残基在TB1肽中的作用。以前,Shoji-Kawata和同事已经表明Tat-Bec(F270S)和Tat-Bec(F274S)肽不再能够诱导自噬途径(Shoji-Kawata等,2013)。在我们的病毒转导实验中,这些肽也不能促进慢病毒转导(图4),表明苯丙氨酸残基对于这些功能中的任何一个都是关键的。在过去的几年中已经发现了许多细胞穿透肽(CPPs)(Milletti等,2012)。因此,测试不同于广泛使用的Tat肽的CPP可以是有趣的。一个有趣的候选物是MAP(模型两性肽)。我们设计了MAP-乱序阴性对照和MAP-Beclin1肽(MAP部分具有SEQIDNO:4所示的序列)。如图4所示,MAP-Beclin1(SEQIDNO:76)与TB1同样有效地促进慢病毒转导,表明可以使用各种CPP来允许所述修饰的Beclin1结构域进入靶细胞细胞质。所述TB1肽的修饰的Beclin1结构域对应于人Beclin1蛋白(智人(homosapiens),NP_003757)的氨基酸残基267至284。这种结构域据描述具有人GAPR-1和HIV-1Nef蛋白结合结构域。然而,能够高效促进慢病毒转导的最佳Beclin1肽序列尚未被评价。为此,设计了许多肽(图5A)。这些肽允许Beclin1蛋白的更好覆盖度。例如,Tat-Bec(250-282)(SEQIDNO:81)完全覆盖α1螺旋、L1环和β1片层(基于晶体结构,Huang等,2012)。而Tat-Bec(274-298)(SEQIDNO:82)完全覆盖β1和β2片层以及L2环(图5A)。所有这些TB1衍生物已经在慢病毒转导分析中进行了测试。如图5B所示,尽管程度不同,但所有肽均能够促进慢病毒转导。在2.5μM下,除了Tat-Bec(274-298),大多数衍生物都比TB1有效率得多。然而,在5μM下,看起来所述肽序列移向所述蛋白质的C端侧越多,它对慢病毒转导的有效性就越小。使用Tat-Bec(267-296)(SEQIDNO:83)的剂量响应实验显示,非常低剂量的这种肽(低至1μM)就能够促进最佳的慢病毒转导(图5C)。有趣的是,含有267-296Beclin1片段的野生型序列(Tat-Bec(267-296)WT)(SEQIDNO:80)的肽促进慢病毒转导,但是没有含有三个修饰H275E、S279D和Q281E的Tat-Bec(267-296)肽有效(图5D)。该结果令人联想到用Tat-BecWT(SEQIDNO:77)获得的结果(图4)。最后,Tat-Bec(267-296)dGG(SEQIDNO:74),其中GG接头已被缺失的Tat-Bec(267-296)的肽变体,增加近5倍的病毒转导水平,提示该接头对于观察到所述肽对慢病毒转导的正面作用并没有严格的依赖性。总而言之,这些beclin1结构域变体突出了覆盖人Beclin1序列中氨基酸残基270至282的区域对促进慢病毒转导的非常重要的作用。低剂量(2.5μM)下的最高性能肽是Tat-Bec(250-282),提示了α1螺旋、L1环和β1片层结构域的重要作用。TB1对腺伴随病毒载体作用的评价腺相关载体(AAV)属于基因治疗途径中最经常使用的病毒载体。在不同的血清型中,AAV-8已成功用于临床,并且对于肝脏定向基因治疗具有很大的希望(Nathwani等,2014)。因此,体外评价了TB1对AAV8转导效率的效应。如图6所示,TB1能够以剂量依赖性方式增强重组AAV8感染性,而Tat-乱序肽对照肽没有效应。该结果突出了TB1的广谱作用,既作用于包膜病毒载体,也作用于无包膜病毒载体。对自噬过程的TB1最佳剂量的评价为了更好地了解TB1的作用机制,我们设法研究了慢病毒转导的增加是否是激活自噬过程的结果。为了监测单细胞水平下的自噬,用表达mCherry-eGFP-LC3融合蛋白的质粒转染HEK293T细胞。接着,将细胞与TB1(5μM)或EBSS饥饿溶液一起温育并用成像流式细胞仪分析。正如预期,EBSS增加了每个细胞的自噬溶酶体(mCherry斑点)的数量(图7)。相反,在TB1处理的HEK293T细胞中自噬溶酶体的数量与肽不存在(无)时的对照条件相当。这些数据表明,在TB1存在下观察到的慢病毒转导的改善决不是诱导自噬流的结果。设计Tat-Beclin2及对其在慢病毒转导上的评价人Beclin1和Beclin2蛋白的序列比对显示了ECD结构域中的同源性。因此,我们决定设计Tat-Bec2WT肽,即Tat(47-57)转导肽与人Beclin2ECD249-266结构域的融合物(图8A)。由于TB1含有三个突变(H275E,S279D和Q281E),因此还设计了与Tat(47-57)肽和野生型人Beclin1ECD267-284结构域的融合物相对应的Tat-BecWT肽,并在序列比对中表示(图8A)。已经测试了这三种肽在大范围浓度下促进慢病毒产生的能力。如图8B所示,所有肽均能够有效促进慢病毒转导,但它们的最佳剂量有很大的可变性:TB1为3μM,Tat-BecWT为1μM,和Tat-Bec2WT为500nM。只有100nM的Tat-Bec2WT能够将慢病毒转导增加三倍,从10到30%(8B),而TB1和Tat-BecWT在该浓度下没有效应。Tat-Scr2WT是Tat-Bec2WT的乱序版本,它促进慢病毒转导,但在对应于Tat-Bec2WT的效应幅度降低的剂量下,肯定是Tat依赖性活性。总之,Tat-Bec2WT在很低剂量下是慢病毒转导的强效增强剂。参考文献D'Costa,J.,S.G.Mansfield,和L.M.Humeau.2009.临床试验中的慢病毒载体:现状(Lentiviralvectorsinclinicaltrials:Currentstatus).Curr.Opin.Mol.Ther.11:554-564.Davis,H.E.,M.Rosinski,J.R.Morgan,和M.L.Yarmush.2004.带电聚合物经由膜电荷中和和病毒聚集调节逆转录病毒转导(Chargedpolymersmodulateretrovirustransductionviamembranechargeneutralizationandvirusaggregation).Biophys.J.86:1234-1242.Fenard,D.,D.Ingrao,A.Seye,J.Buisset,S.Genries,S.Martin,A.Kichler,和A.Galy.2013.载体融合素-1,一种新的病毒进入增强剂,强烈促进人造血干细胞的慢病毒转导(载体融合素-1,anewviralentryenhancer,stronglypromoteslentiviraltransductionofhumanhematopoieticstemcells).Mol.Ther.NucleicAcids2:e90.He,C.,Y.Wei,K.Sun,B.Li,X.Dong,Z.Zou,Y.Liu,LN.Kinch,S.Khan,S.Sinha,RJ.Xavier,NV.Grishin,G.Xiao,EL.Eskelinen,PE.Scherer,JL.Whistler和B.Levine.2013.Beclin2在自噬、G蛋白偶联受体降解、和代谢中起作用(Beclin2FunctionsinAutophagy,DegradationofGProtein-CoupledReceptors,andMetabolism).Cell.154(5):1085-99.Huang,W.,W.Choi,W.Hu,N.Mi,Q.Guo,M.Ma,M.Liu,Y.Tian,P.Lu,F.L.Wang,H.Deng,L.Liu,N.Gao,L.Yu,和Y.Shi.2012.晶体结构和生化分析揭示Beclin1为一种新型的膜结合蛋白(CrystalstructureandbiochemicalanalysesrevealBeclin1asanovelmembranebindingprotein).CellRes.22:473-489.Ingrao,D.,S.Majdoul,A.K.Seye,A.Galy,和D.Fenard.2014.同时测量原代CD34+细胞与基于人类免疫缺陷病毒1型慢病毒载体的融合和转导效率揭示转导增强剂的不同效应(ConcurrentMeasuresofFusionandTransductionEfficiencyofPrimaryCD34+CellswithHumanImmunodeficiencyVirus1-BasedLentiviralVectorsRevealDifferentEffectsofTransductionEnhancers).Hum.GeneTher.Methods25:48-56.Levy,C.,E.Verhoeyen,和F.L.Cosset.2015.用于基因转移到基因治疗靶细胞的慢病毒载体的表面工程(Surfaceengineeringoflentiviralvectorsforgenetransferintogenetherapytargetcells).Curr.Opin.Pharmacol.24:79-85.Liu,Y.,S.Shoji-Kawata,R.M.Sumpter,Jr.,Y.Wei,V.Ginet,L.Zhang,B.Posner,K.A.Tran,D.R.Green,R.J.Xavier,S.Y.Shaw,P.G.Clarke,J.Puyal,和B.Levine.2013.自死亡是由自噬诱导肽、饥饿和缺氧缺血引发的Na+,K+-ATP酶调节的细胞死亡形式(AutosisisaNa+,K+-ATPase-regulatedformofcelldeathtriggeredbyautophagy-inducingpeptides,starvation,andhypoxia-ischemia).Proc.Natl.Acad.Sci.U.S.A110:20364-20371.Merten,O.W.,S.Charrier,N.Laroudie,S.Fauchille,C.Dugue,C.Jenny,M.Audit,M.A.Zanta-Boussif,H.Chautard,M.Radrizzani,G.Vallanti,L.Naldini,P.Noguiez-Hellin,和A.Galy.2011.为临床离体基因治疗应用产生的慢病毒载体的大规模制造和表征(Large-scalemanufactureandcharacterizationofalentiviralvectorproducedforclinicalexvivogenetherapyapplication).Hum.GeneTher.22:343-356.Milletti,F.2012.细胞穿透肽:类别,起源和当前概貌(Cell-penetratingpeptides:classes,origin,andcurrentlandscape).DrugDiscov.Today17:850-860.Munch,J.,E.Rucker,L.Standker,K.Adermann,C.Goffinet,M.Schindler,S.Wildum,R.Chinnadurai,D.Rajan,A.Specht,G.Gimenez-Gallego,P.C.Sanchez,D.M.Fowler,A.Koulov,J.W.Kelly,W.Mothes,J.C.Grivel,L.Margolis,O.T.Keppler,W.G.Forssmann,和F.Kirchhoff.2007.精液来源的淀粉样原纤维极大增强HIV感染(Semen-derivedamyloidfibrilsdrasticallyenhanceHIVinfection).Cell131:1059-1071.Nathwani,A.C.,U.M.Reiss,E.G.Tuddenham,C.Rosales,P.Chowdary,J.McIntosh,M.DellaPeruta,E.Lheriteau,N.Patel,D.Raj,A.Riddell,J.Pie,S.Rangarajan,D.Bevan,M.Recht,Y.M.Shen,K.G.Halka,E.Basner-Tschakarjan,F.Mingozzi,K.A.High,J.Allay,M.A.Kay,C.Y.Ng,J.Zhou,M.Cancio,C.L.Morton,J.T.Gray,D.Srivastava,A.W.Nienhuis,A.M.Davidoff.因子IX基因治疗在血友病B中的长期安全性和功效(Long-termsafetyandefficacyoffactorIXgenetherapyinhemophiliaB).2014.N.Engl.J.Med.371(21):1994-2004.Novelli,E.M.,L.Cheng,Y.Yang,W.Leung,M.Ramirez,V.Tanavde,C.Enger,和C.I.Civin.1999.脐血CD34+细胞的离体培养扩增祖细胞数量,保留非肥胖糖尿病/重症联合免疫缺陷小鼠的移植能力,并增强逆转录病毒转导效率(ExvivocultureofcordbloodCD34+cellsexpandsprogenitorcellnumbers,preservesengraftmentcapacityinnonobesediabetic/severecombinedimmunodeficientmice,andenhancesretroviraltransductionefficiency).Hum.GeneTher.10:2927-2940.Pollok,K.E.,和D.A.Williams.1999.利用重组纤连蛋白片段促进逆转录病毒介导的基因转移至造血干细胞和祖细胞以及外周血T淋巴细胞中(Facilitationofretrovirus-mediatedgenetransferintohematopoieticstemandprogenitorcellsandperipheralbloodT-lymphocytesutilizingrecombinantfibronectinfragments).Curr.Opin.Mol.Ther.1:595-604.Roan,N.R.,J.Munch,N.Arhel,W.Mothes,J.Neidleman,A.Kobayashi,K.Smith-McCune,F.Kirchhoff,和W.C.Greene.2009.SEVI的阳离子性质是其增强人类免疫缺陷病毒感染的能力的基础(ThecationicpropertiesofSEVIunderlieitsabilitytoenhancehumanimmunodeficiencyvirusinfection).J.Virol.83:73-80Rodrigues,T.,M.J.Carrondo,P.M.Alves,和P.E.Cruz.2007.用于临床应用的逆转录病毒载体的纯化:生物学意义和技术挑战(ThecationicpropertiesofSEVIunderlieitsabilitytoenhancehumanimmunodeficiencyvirusinfection).J.Biotechnol.127:520-541.Sandrin,V.,B.Boson,P.Salmon,W.Gay,D.Negre,R.LeGrand,D.Trono,和F.L.Cosset.2002.用修饰的RD114包膜糖蛋白假型化的慢病毒载体表现出在血清中的增加的稳定性,以及来源于人和非人灵长类动物的原代淋巴细胞和CD34+细胞的增强的转导(LentiviralvectorspseudotypedwithamodifiedRD114envelopeglycoproteinshowincreasedstabilityinseraandaugmentedtransductionofprimarylymphocytesandCD34+cellsderivedfromhumanandnonhumanprimates).Blood100:823-832.Shoji-Kawata,S.,R.Sumpter,M.Leveno,G.R.Campbell,Z.Zou,L.Kinch,A.D.Wilkins,Q.Sun,K.Pallauf,D.MacDuff,C.Huerta,H.W.Virgin,J.B.Helms,R.Eerland,S.A.Tooze,R.Xavier,D.J.Lenschow,A.Yamamoto,D.King,O.Lichtarge,N.V.Grishin,S.A.Spector,D.V.Kaloyanova,和B.Levine.2013.候选治疗性自噬诱导肽的鉴定(Identificationofacandidatetherapeuticautophagy-inducingpeptide).Nature494:201-206.Yolamanova,M.,C.Meier,A.K.Shaytan,V.Vas,C.W.Bertoncini,F.Arnold,O.Zirafi,S.M.Usmani,J.A.Muller,D.Sauter,C.Goffinet,D.Palesch,P.Walther,N.R.Roan,H.Geiger,O.Lunov,T.Simmet,J.Bohne,H.Schrezenmeier,K.Schwarz,L.Standker,W.G.Forssmann,X.Salvatella,P.G.Khalatur,A.R.Khokhlov,T.P.Knowles,T.Weil,F.Kirchhoff,和J.Munch.2013.肽纳米原纤维促进逆转录病毒基因转移并提供浓缩病毒的快速手段(Peptidenanofibrilsboostretroviralgenetransferandprovidearapidmeansforconcentratingviruses).Nat.Nanotechnol.8:130-136.序列表<110>吉尼松公司等<120>用于改善病毒载体效率的组合物和方法<130>B2148PC00<160>101<170>PatentInversion3.3<210>1<211>11<212>PRT<213>人工<220><223>Tat(47-57)<400>1TyrGlyArgLysLysArgArgGlnArgArgArg1510<210>2<211>13<212>PRT<213>人工<220><223>Tat(48-60)<400>2GlyArgLysLysArgArgGlnArgArgArgProProGln1510<210>3<211>9<212>PRT<213>人工<220><223>Tat(49-57)<400>3ArgLysLysArgArgGlnArgArgArg15<210>4<211>17<212>PRT<213>人工<220><223>MAP肽<400>4LysLeuAlaLeuLysLeuAlaLeuLysAlaLeuLysAlaAlaLeuLys151015Ala<210>5<211>18<212>PRT<213>人工<220><223>MAP肽<400>5LysLeuAlaLeuLysLeuAlaLeuLysAlaLeuLysAlaAlaLeuLys151015LeuAla<210>6<211>16<212>PRT<213>人工<220><223>触角足(或穿透素)<400>6ArgGlnIleLysIleTrpPheGlnAsnArgArgMetLysTrpLysLys151015<210>7<211>7<212>PRT<213>人工<220><223>穿透素衍生物<400>7ArgArgMetLysTrpLysLys15<210>8<211>8<212>PRT<213>人工<220><223>穿透素衍生物<400>8AsnArgArgMetLysTrpLysLys15<210>9<211>9<212>PRT<213>人工<220><223>穿透素衍生物<400>9GlnAsnArgArgMetLysTrpLysLys15<210>10<211>10<212>PRT<213>人工<220><223>穿透素衍生物<400>10PheGlnAsnArgArgMetLysTrpLysLys1510<210>11<211>7<212>PRT<213>人工<220><223>穿透素衍生物<400>11ArgArgGluLysTrpLysLys15<210>12<211>7<212>PRT<213>人工<220><223>穿透素衍生物<400>12ArgArgGlnLysTrpLysLys15<210>13<211>7<212>PRT<213>人工<220><223>穿透素衍生物<400>13LysArgMetLysTrpLysLys15<210>14<211>7<212>PRT<213>人工<220><223>穿透素衍生物<400>14ArgLysMetLysTrpLysLys15<210>15<211>7<212>PRT<213>人工<220><223>穿透素衍生物<220><221>MISC_FEATURE<222>(3)..(3)<223>Xaa=Orn<400>15ArgArgXaaLysTrpLysLys15<210>16<211>7<212>PRT<213>人工<220><223>穿透素衍生物<400>16ArgArgMetLysGlnLysLys15<210>17<211>7<212>PRT<213>人工<220><223>穿透素衍生物<400>17ArgArgMetLysTrpPheLys15<210>18<211>7<212>PRT<213>人工<220><223>穿透素衍生物<220><221>MISC_FEATURE<222>(2)..(2)<223>Xaa=Orn<400>18ArgXaaArgLysTrpLysLys15<210>19<211>7<212>PRT<213>人工<220><223>穿透素衍生物<400>19ArgArgMetTrpLysLysLys15<210>20<211>7<212>PRT<213>人工<220><223>穿透素衍生物<400>20ArgArgMetLysLysTrpLys15<210>21<211>16<212>PRT<213>人工<220><223>D-穿透素<220><221>MISC_FEATURE<222>(1)..(16)<223>D-氨基酸<400>21ArgGlnIleLysIleTrpPheGlnAsnArgArgMetLysTrpLysLys151015<210>22<211>18<212>PRT<213>人工<220><223>Pegelin(SynB)<400>22ArgGlyGlyArgLeuSerTyrSerArgArgArgPheSerThrSerThr151015GlyArg<210>23<211>33<212>PRT<213>人工<220><223>VP22<400>23AspAlaAlaThrAlaThrArgGlyArgSerAlaAlaSerArgProThr151015GluArgProArgAlaProAlaArgSerAlaSerArgProArgArgVal202530Asp<210>24<211>27<212>PRT<213>人工<220><223>运输蛋白<400>24GlyTrpThrLeuAsnSerAlaGlyTyrLeuLeuGlyLysIleAsnLeu151015LysAlaLeuAlaAlaLeuAlaLysLysIleLeu2025<210>25<211>21<212>PRT<213>人工<220><223>运输蛋白-10<400>25AlaGlyTyrLeuLeuGlyLysIleAsnLeuLysAlaLeuAlaAlaLeu151015AlaLysLysIleLeu20<210>26<211>30<212>PRT<213>人工<220><223>KALA<400>26TrpGluAlaLysLeuAlaLysAlaLeuAlaLysAlaLeuAlaLysHis151015LeuAlaLysAlaLeuAlaLysAlaLeuLysAlaCysGluAla202530<210>27<211>21<212>PRT<213>人工<220><223>Pep-1<400>27LysGluThrTrpTrpGluThrTrpTrpThrGluTrpSerGlnProLys151015LysLysArgLysVal20<210>28<211>21<212>PRT<213>人工<220><223>Pep-2<400>28LysGluThrTrpPheGluThrTrpPheThrGluTrpSerGlnProLys151015LysLysArgLysVal20<210>29<211>27<212>PRT<213>人工<220><223>MPG<400>29GlyAlaLeuPheLeuGlyPheLeuGlyAlaAlaGlySerThrMetGly151015AlaTrpSerGlnProLysSerLysArgLysVal2025<210>30<211>19<212>PRT<213>人工<220><223>Vectocell肽<400>30ValLysArgGlyLeuLysLeuArgHisValArgProArgValThrArg151015MetAspVal<210>31<211>14<212>PRT<213>人工<220><223>Vectocell肽<400>31SerArgArgAlaArgArgSerProArgHisLeuGlySerGly1510<210>32<211>16<212>PRT<213>人工<220><223>Vectocell肽<400>32LeuArgArgGluArgGlnSerArgLeuArgArgGluArgGlnSerArg151015<210>33<211>22<212>PRT<213>人工<220><223>Vectocell肽<400>33GlyAlaTyrAspLeuArgArgArgGluArgGlnSerArgLeuArgArg151015ArgGluArgGlnSerArg20<210>34<211>29<212>PRT<213>人工<220><223>Wr-T转运子<220><221>MISC_FEATURE<222>(22)..(29)<223>D-氨基酸<400>34LysGluThrTrpTrpGluThrTrpTrpThrGluTrpTrpThrGluTrp151015SerGlnGlyProGlyArgArgArgArgArgArgArgArg2025<210>35<211>7<212>PRT<213>人工<220><223>R7<400>35ArgArgArgArgArgArgArg15<210>36<211>26<212>PRT<213>人工<220><223>LAH4<400>36LysLysAlaLeuLeuAlaLeuAlaLeuHisHisLeuAlaHisLeuAla151015LeuHisLeuAlaLeuAlaLeuLysLysAla2025<210>37<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>37LysLysAlaLeuLeuAlaHisAlaLeuHisLeuLeuAlaLeuLeuAla151015LeuHisLeuAlaHisAlaLeuLysLysAla2025<210>38<211>24<212>PRT<213>人工<220><223>LAH4衍生物<400>38LysLysAlaLeuLeuAlaHisAlaLeuHisLeuLeuAlaLeuLeuAla151015LeuHisLeuAlaHisAlaLeuAla20<210>39<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>39ArgArgAlaLeuLeuAlaHisAlaLeuHisLeuLeuAlaLeuLeuAla151015LeuHisLeuAlaHisAlaLeuArgArgAla2025<210>40<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>40LysLysAlaLeuLeuAlaHisAlaLeuAlaHisLeuAlaLeuLeuAla151015LeuHisLeuAlaLeuHisLeuLysLysAla2025<210>41<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>41LysLysAlaLeuLeuAlaLeuAlaLeuHisHisLeuAlaLeuLeuAla151015LeuHisLeuAlaHisAlaLeuLysLysAla2025<210>42<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>42LysLysAlaLeuLeuAlaLeuAlaLeuHisHisLeuAlaLeuLeuAla151015HisHisLeuAlaLeuAlaLeuLysLysAla2025<210>43<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>43LysLysAlaLeuLeuHisLeuAlaLeuLeuHisAlaAlaLeuLeuAla151015HisHisLeuAlaLeuAlaLeuLysLysAla2025<210>44<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>44LysLysAlaLeuLeuHisLeuAlaLeuLeuHisAlaAlaLeuLeuAla151015HisLeuAlaAlaLeuHisLeuLysLysAla2025<210>45<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>45LysLysAlaLeuLeuHisLeuAlaLeuLeuLeuAlaAlaLeuHisAla151015HisLeuAlaAlaLeuHisLeuLysLysAla2025<210>46<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>46LysLysAlaLeuLeuAlaHisAlaLeuHisLeuLeuAlaAlaLeuAla151015LeuHisLeuAlaHisLeuLeuLysLysAla2025<210>47<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>47LysLysAlaLeuLeuLeuAlaAlaLeuHisHisLeuAlaAlaLeuAla151015LeuHisLeuAlaHisLeuLeuLysLysAla2025<210>48<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>48LysLysAlaLeuLeuLeuAlaAlaLeuHisHisLeuLeuAlaLeuAla151015HisHisLeuAlaAlaLeuLeuLysLysAla2025<210>49<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>49LysLysAlaLeuLeuHisAlaAlaLeuAlaHisLeuLeuAlaLeuAla151015HisHisLeuLeuAlaLeuLeuLysLysAla2025<210>50<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>50LysLysAlaLeuLeuHisAlaLeuLeuAlaHisLeuAlaAlaLeuLeu151015HisAlaLeuLeuAlaHisLeuLysLysAla2025<210>51<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>51LysLysAlaLeuLeuHisAlaLeuLeuAlaAlaLeuLeuAlaHisLeu151015HisAlaLeuLeuAlaHisLeuLysLysAla2025<210>52<211>25<212>PRT<213>人工<220><223>LAH4衍生物<400>52LysAlaLeuLeuHisAlaAlaLeuAlaHisLeuLeuAlaLeuAlaHis151015HisLeuLeuAlaLeuLeuLysLysAla2025<210>53<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>53LysLysLysLeuLeuHisAlaAlaLeuAlaHisLeuLeuAlaLeuAla151015HisHisLeuLeuAlaLeuLeuLysLysAla2025<210>54<211>24<212>PRT<213>人工<220><223>LAH4衍生物<400>54LysLysAlaLeuLeuHisAlaAlaLeuAlaHisLeuLeuAlaLeuAla151015HisHisLeuLeuAlaLeuLeuAla20<210>55<211>25<212>PRT<213>人工<220><223>LAH4衍生物<400>55LysLysAlaLeuLeuHisAlaAlaLeuAlaHisLeuLeuAlaLeuAla151015HisHisLeuLeuAlaLeuLeuLysLys2025<210>56<211>24<212>PRT<213>人工<220><223>LAH4衍生物<400>56LysLysLeuLeuHisAlaAlaLeuAlaHisLeuLeuAlaLeuAlaHis151015HisLeuLeuAlaLeuLeuLysLys20<210>57<211>24<212>PRT<213>人工<220><223>LAH4衍生物<400>57LysLysAlaLeuLeuHisAlaAlaLeuAlaHisLeuLeuAlaLeuAla151015HisHisLeuLeuAlaLeuLysLys20<210>58<211>23<212>PRT<213>人工<220><223>LAH4衍生物<400>58LysLysLeuHisAlaAlaLeuAlaHisLeuLeuAlaLeuAlaHisHis151015LeuLeuAlaLeuLeuLysLys20<210>59<211>21<212>PRT<213>人工<220><223>LAH4衍生物<400>59LysLysLeuHisAlaAlaLeuAlaHisLeuLeuAlaLeuAlaHisHis151015LeuLeuAlaLysLys20<210>60<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>60LysLysAlaLeuLeuHisAlaAlaLeuAlaHisLeuLeuAlaLeuAla151015AlaAlaLeuLeuAlaLeuLeuLysLysAla2025<210>61<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>61LysLysAlaLeuLeuAlaAlaAlaLeuAlaAlaLeuLeuAlaLeuAla151015AlaAlaLeuLeuAlaLeuLeuLysLysAla2025<210>62<211>26<212>PRT<213>人工<220><223>LAH4衍生物<400>62LysLysLeuLeuLeuHisAlaLeuLeuAlaHisLeuLeuAlaLeuLeu151015HisHisLeuLeuAlaLeuLeuLysLysLeu2025<210>63<211>450<212>PRT<213>智人(Homosapiens)<400>63MetGluGlySerLysThrSerAsnAsnSerThrMetGlnValSerPhe151015ValCysGlnArgCysSerGlnProLeuLysLeuAspThrSerPheLys202530IleLeuAspArgValThrIleGlnGluLeuThrAlaProLeuLeuThr354045ThrAlaGlnAlaLysProGlyGluThrGlnGluGluGluThrAsnSer505560GlyGluGluProPheIleGluThrProArgGlnAspGlyValSerArg65707580ArgPheIleProProAlaArgMetMetSerThrGluSerAlaAsnSer859095PheThrLeuIleGlyGluAlaSerAspGlyGlyThrMetGluAsnLeu100105110SerArgArgLeuLysValThrGlyAspLeuPheAspIleMetSerGly115120125GlnThrAspValAspHisProLeuCysGluGluCysThrAspThrLeu130135140LeuAspGlnLeuAspThrGlnLeuAsnValThrGluAsnGluCysGln145150155160AsnTyrLysArgCysLeuGluIleLeuGluGlnMetAsnGluAspAsp165170175SerGluGlnLeuGlnMetGluLeuLysGluLeuAlaLeuGluGluGlu180185190ArgLeuIleGlnGluLeuGluAspValGluLysAsnArgLysIleVal195200205AlaGluAsnLeuGluLysValGlnAlaGluAlaGluArgLeuAspGln210215220GluGluAlaGlnTyrGlnArgGluTyrSerGluPheLysArgGlnGln225230235240LeuGluLeuAspAspGluLeuLysSerValGluAsnGlnMetArgTyr245250255AlaGlnThrGlnLeuAspLysLeuLysLysThrAsnValPheAsnAla260265270ThrPheHisIleTrpHisSerGlyGlnPheGlyThrIleAsnAsnPhe275280285ArgLeuGlyArgLeuProSerValProValGluTrpAsnGluIleAsn290295300AlaAlaTrpGlyGlnThrValLeuLeuLeuHisAlaLeuAlaAsnLys305310315320MetGlyLeuLysPheGlnArgTyrArgLeuValProTyrGlyAsnHis325330335SerTyrLeuGluSerLeuThrAspLysSerLysGluLeuProLeuTyr340345350CysSerGlyGlyLeuArgPhePheTrpAspAsnLysPheAspHisAla355360365MetValAlaPheLeuAspCysValGlnGlnPheLysGluGluValGlu370375380LysGlyGluThrArgPheCysLeuProTyrArgMetAspValGluLys385390395400GlyLysIleGluAspThrGlyGlySerGlyGlySerTyrSerIleLys405410415ThrGlnPheAsnSerGluGluGlnTrpThrLysAlaLeuLysPheMet420425430LeuThrAsnLeuLysTrpGlyLeuAlaTrpValSerSerGlnPheTyr435440445AsnLys450<210>64<211>431<212>PRT<213>智人(Homosapiens)<400>64MetSerSerIleArgPheLeuCysGlnArgCysHisGlnAlaLeuLys151015LeuSerGlySerSerGluSerArgSerLeuProAlaAlaProAlaPro202530ThrSerGlyGlnAlaGluProGlyAspThrArgGluProGlyValThr354045ThrArgGluValThrAspAlaGluGluGlnGlnAspGlyAlaSerSer505560ArgSerProProGlyAspGlySerValSerLysGlyHisAlaAsnIle65707580PheThrLeuLeuGlyGluLeuGlyAlaMetHisMetLeuSerSerIle859095GlnLysAlaAlaGlyAspIlePheAspIleValSerGlyGlnAlaVal100105110ValAspHisProLeuCysGluGluCysThrAspSerLeuLeuGluGln115120125LeuAspIleGlnLeuAlaLeuThrGluAlaAspSerGlnAsnTyrGln130135140ArgCysLeuGluThrGlyGluLeuAlaThrSerGluAspGluAlaAla145150155160AlaLeuArgAlaGluLeuArgAspLeuGluLeuGluGluAlaArgLeu165170175ValGlnGluLeuGluAspValAspArgAsnAsnAlaArgAlaAlaAla180185190AspLeuGlnAlaAlaGlnAlaGluAlaAlaGluLeuAspGlnGlnGlu195200205ArgGlnHisTyrArgAspTyrSerAlaLeuLysArgGlnGlnLeuGlu210215220LeuLeuAspGlnLeuGlyAsnValGluAsnGlnLeuGlnTyrAlaArg225230235240ValGlnArgAspArgLeuLysGluIleAsnCysPheThrAlaThrPhe245250255GluIleTrpValGluGlyProLeuGlyValIleAsnAsnPheArgLeu260265270GlyArgLeuProThrValArgValGlyTrpAsnGluIleAsnThrAla275280285TrpGlyGlnAlaAlaLeuLeuLeuLeuThrLeuAlaAsnThrIleGly290295300LeuGlnPheGlnArgTyrArgLeuIleProCysGlyAsnHisSerTyr305310315320LeuLysSerLeuThrAspAspArgThrGluLeuProLeuPheCysTyr325330335GlyGlyGlnAspValPheLeuAsnAsnLysTyrAspArgAlaMetVal340345350AlaPheLeuAspCysMetGlnGlnPheLysGluGluAlaGluLysGly355360365GluLeuGlyLeuSerLeuProTyrGlyIleGlnValGluThrGlyLeu370375380MetGluAspValGlyGlyArgGlyGluCysTyrSerIleArgThrHis385390395400LeuAsnThrGlnGluLeuTrpThrLysAlaLeuLysPheMetLeuIle405410415AsnPheLysTrpSerLeuIleTrpValAlaSerArgTyrGlnLys420425430<210>65<211>18<212>PRT<213>人工<220><223>beclin-1267-284<400>65ThrAsnValPheAsnAlaThrPheHisIleTrpHisSerGlyGlnPhe151015GlyThr<210>66<211>18<212>PRT<213>人工<220><223>修饰的beclin-1267-284<400>66ThrAsnValPheAsnAlaThrPheGluIleTrpHisAspGlyGluPhe151015GlyThr<210>67<211>15<212>PRT<213>人工<220><223>修饰的beclin-1270-284<400>67PheAsnAlaThrPheGluIleTrpHisAspGlyGluPheGlyThr151015<210>68<211>16<212>PRT<213>人工<220><223>修饰的beclin-1267-282<400>68ThrAsnValPheAsnAlaThrPheGluIleTrpHisAspGlyGluPhe151015<210>69<211>29<212>PRT<213>人工<220><223>修饰的beclin-1256-284<400>69TyrAlaGlnThrGlnLeuAspLysLeuLysLysThrAsnValPheAsn151015AlaThrPheGluIleTrpHisAspGlyGluPheGlyThr2025<210>70<211>30<212>PRT<213>人工<220><223>修饰的beclin-1267-296<400>70ThrAsnValPheAsnAlaThrPheGluIleTrpHisAspGlyGluPhe151015GlyThrIleAsnAsnPheArgLeuGlyArgLeuProSerVal202530<210>71<211>33<212>PRT<213>人工<220><223>修饰的beclin-1250-282<400>71ValGluAsnGlnMetArgTyrAlaGlnThrGlnLeuAspLysLeuLys151015LysThrAsnValPheAsnAlaThrPheGluIleTrpHisAspGlyGlu202530Phe<210>72<211>29<212>PRT<213>人工<220><223>修饰的beclin-1270-298<400>72PheAsnAlaThrPheGluIleTrpHisAspGlyGluPheGlyThrIle151015AsnAsnPheArgLeuGlyArgLeuProSerValProVal2025<210>73<211>25<212>PRT<213>人工<220><223>修饰的beclin-1274-298<400>73PheGluIleTrpHisAspGlyGluPheGlyThrIleAsnAsnPheArg151015LeuGlyArgLeuProSerValProVal2025<210>74<211>41<212>PRT<213>人工<220><223>修饰的Tat-Beclin-1+beclin-1285-296<400>74TyrGlyArgLysLysArgArgGlnArgArgArgThrAsnValPheAsn151015AlaThrPheGluIleTrpHisAspGlyGluPheGlyThrIleAsnAsn202530PheArgLeuGlyArgLeuProSerVal3540<210>75<211>31<212>PRT<213>人工<220><223>TB1<400>75TyrGlyArgLysLysArgArgGlnArgArgArgGlyGlyThrAsnVal151015PheAsnAlaThrPheGluIleTrpHisAspGlyGluPheGlyThr202530<210>76<211>36<212>PRT<213>人工<220><223>MAP-B1<400>76LysLeuAlaLeuLysLeuAlaLeuLysAlaLeuLysAlaAlaLeuLys151015AlaGlyThrAsnValPheAsnAlaThrPheGluIleTrpHisAspGly202530GluPheGlyThr35<210>77<211>31<212>PRT<213>人工<220><223>TBWT<400>77TyrGlyArgLysLysArgArgGlnArgArgArgGlyGlyThrAsnVal151015PheAsnAlaThrPheHisIleTrpHisSerGlyGlnPheGlyThr202530<210>78<211>42<212>PRT<213>人工<220><223>TB1256-284<400>78TyrGlyArgLysLysArgArgGlnArgArgArgGlyGlyTyrAlaGln151015ThrGlnLeuAspLysLeuLysLysThrAsnValPheAsnAlaThrPhe202530GluIleTrpHisAspGlyGluPheGlyThr3540<210>79<211>43<212>PRT<213>人工<220><223>TB1267-296<400>79TyrGlyArgLysLysArgArgGlnArgArgArgGlyGlyThrAsnVal151015PheAsnAlaThrPheGluIleTrpHisAspGlyGluPheGlyThrIle202530AsnAsnPheArgLeuGlyArgLeuProSerVal3540<210>80<211>43<212>PRT<213>人工<220><223>TBWT267-296<400>80TyrGlyArgLysLysArgArgGlnArgArgArgGlyGlyThrAsnVal151015PheAsnAlaThrPheHisIleTrpHisSerGlyGlnPheGlyThrIle202530AsnAsnPheArgLeuGlyArgLeuProSerVal3540<210>81<211>46<212>PRT<213>人工<220><223>TB1250-282<400>81TyrGlyArgLysLysArgArgGlnArgArgArgGlyGlyValGluAsn151015GlnMetArgTyrAlaGlnThrGlnLeuAspLysLeuLysLysThrAsn202530ValPheAsnAlaThrPheGluIleTrpHisAspGlyGluPhe354045<210>82<211>38<212>PRT<213>人工<220><223>TB1274-298<400>82TyrGlyArgLysLysArgArgGlnArgArgArgGlyGlyPheGluIle151015TrpHisAspGlyGluPheGlyThrIleAsnAsnPheArgLeuGlyArg202530LeuProSerValProVal35<210>83<211>42<212>PRT<213>人工<220><223>TB1270-298<400>83TyrGlyArgLysLysArgArgGlnArgArgArgGlyGlyPheAsnAla151015ThrPheGluIleTrpHisAspGlyGluPheGlyThrIleAsnAsnPhe202530ArgLeuGlyArgLeuProSerValProVal3540<210>84<211>26<212>PRT<213>人工<220><223>载体融合素-1<400>84LysLysAlaLeuLeuHisAlaAlaLeuAlaHisLeuLeuAlaLeuAla151015HisHisLeuLeuAlaLeuLeuLysLysAla2025<210>85<211>39<212>PRT<213>人工<220><223>SEVI<400>85GlyIleHisLysGlnLysGluLysSerArgLeuGlnGlyGlyValLeu151015ValAsnGluIleLeuAsnHisMetLysArgAlaThrGlnIleProSer202530TyrLysLysLeuIleMetTyr35<210>86<211>22<212>PRT<213>人工<220><223>SEM1(86-107)<400>86AspLeuAsnAlaLeuHisLysThrThrLysSerGlnArgHisLeuGly151015GlySerGlnGlnLeuLeu20<210>87<211>12<212>PRT<213>人工<220><223>EF-C肽<400>87GlnCysLysIleLysGlnIleIleAsnMetTrpGln1510<210>88<211>16<212>PRT<213>人工<220><223>P16肽<400>88AsnTrpPheAspIleThrAsnTrpLeuTrpTyrIleLysLysLysLys151015<210>89<211>18<212>PRT<213>人工<220><223>Beclin-2249-266<400>89IleAsnCysPheThrAlaThrPheGluIleTrpValGluGlyProLeu151015GlyVal<210>90<211>29<212>PRT<213>人工<220><223>TAT+beclin-2<400>90TyrGlyArgLysLysArgArgGlnArgArgArgIleAsnCysPheThr151015AlaThrPheGluIleTrpValGluGlyProLeuGlyVal2025<210>91<211>31<212>PRT<213>人工<220><223>TAT+GG+Beclin2<400>91TyrGlyArgLysLysArgArgGlnArgArgArgGlyGlyIleAsnCys151015PheThrAlaThrPheGluIleTrpValGluGlyProLeuGlyVal202530<210>92<211>18<212>PRT<213>人工<220><223>小鼠Beclin-2262-279<400>92ThrAsnIlePheAsnAlaThrPheThrIleSerAspGluGlyProLeu151015GlyVal<210>93<211>18<212>PRT<213>人工<220><223>马Beclin-2253-270<400>93IleAsnValPheSerValThrPheGluIleGlyHisSerGlyProVal151015GlyVal<210>94<211>18<212>PRT<213>人工<220><223>熊猫Beclin-2645-662<400>94ThrAsnValPheAsnAlaThrPheGluIleArgHisAspGlyProVal151015GlyIle<210>95<211>18<212>PRT<213>人工<220><223>猪Beclin-2244-261<400>95ThrAsnValPheArgAlaThrPheGluIleArgHisAlaGlyProIle151015AlaIle<210>96<211>18<212>PRT<213>人工<220><223>牛Beclin-2248-265<400>96ThrAspValPheAsnAlaThrPheGluIleTrpGlnAspGlyProLeu151015ProVal<210>97<211>18<212>PRT<213>人工<220><223>兔Beclin-2238-255<400>97ThrSerIlePheGlnValThrPheGluIleArgGluGluGlySerVal151015GlyIle<210>98<211>31<212>PRT<213>人工<220><223>tat-beclin1H275E<400>98TyrGlyArgLysLysArgArgGlnArgArgArgGlyGlyThrAsnVal151015PheAsnAlaThrPheGluIleTrpHisSerGlyGlnPheGlyThr202530<210>99<211>31<212>PRT<213>人工<220><223>tat-beclin1S279D<400>99TyrGlyArgLysLysArgArgGlnArgArgArgGlyGlyThrAsnVal151015PheAsnAlaThrPheHisIleTrpHisAspGlyGlnPheGlyThr202530<210>100<211>31<212>PRT<213>人工<220><223>tat-beclin1Q281E<400>100TyrGlyArgLysLysArgArgGlnArgArgArgGlyGlyThrAsnVal151015PheAsnAlaThrPheHisIleTrpHisSerGlyGluPheGlyThr202530<210>101<211>31<212>PRT<213>人工<220><223>tat-beclin1F274W277<400>101TyrGlyArgLysLysArgArgGlnArgArgArgGlyGlyThrAsnVal151015PheAsnAlaThrPheHisIleTrpHisSerGlyGlnPheGlyThr202530当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1