用于益生菌负载和肠道递送的再生纤维素微球及其制备方法与流程
本发明涉及高分子材料领域,具有涉及用于负载、递送益生菌的再生纤维素微球及其制备方法。
背景技术:
益生菌是一类通过改善寄主肠道微生态平衡而有益于寄主的一类微生物,具有调节肠道菌群结构、促进肠道中有益菌的繁殖、提高机体免疫力、调节胆固醇水平、抑制肿瘤生长等功效。然而,益生菌最大的缺点是活菌期时间短,从加工、贮藏、运输,再经口服从消化道到达肠道期间,因外界条件的影响,达到肠道的活菌数大大减少,因此,使用微胶囊技术将足够量的活菌递送到肠道成为研究热点。目前常见的益生菌包埋材料有海藻酸钠、淀粉和蛋白质等,但这几种壁材在益生菌包埋上都有各自的不足之处,如海藻酸钠致密性低,蛋白质易变性、稳定性差等,为此,新型益生菌递送材料的发掘受到广泛关注。
纤维素是地球上最丰富的多糖,因具有生物相容性和可生物降解性而广泛应用于许多领域。许多纤维素衍生物如羟丙基纤维素和羧甲基纤维素已被广泛用作益生菌包埋材料,但是这些衍生物是水溶性的,可物理降解,因此在益生菌的递送过程中不能实现益生菌的有效保护。
技术实现要素:
本发明所要解决的技术问题是针对上述现有技术存在的不足而提供一种再生纤维素微球,具有良好的孔径结构、ph响应和益生菌负载及肠道递送等性能。
本方案为解决上述所提出的问题所采用的技术方案为:
再生纤维素微球,它是由纤维素和纳米纤维素共混经溶解及再生制备得到的多孔微球,平均孔径为1~3μm,其中纤维素和纳米纤维素的质量比为1:(0~9),且纳米纤维素不为0。
按上述方案,所述纤维素的粘均分子量为3万~37万道尔顿。
按上述方案,纳米纤维素是纤维素通过tempo(2,2,6,6-四甲基哌啶-氮-氧化物)媒介氧化体系制备得到表面富含羧基的纳米纤维素,表面羧基含量为0.1~1.6mmol/g。
按上述方案,再生制备过程在盐酸溶液中进行,整个再生制备过程体系ph不超过5。
本发明同时提供一种上述再生纤维素微球的制备方法,主要步骤如下:
1)按纤维素和纳米纤维素制备成共混溶液;
2)将步骤1)所得纤维素和纳米纤维素共混溶液滴加到盐酸溶液中进行再生,得到再生纤维素微球粗产品;
3)将步骤2)所得再生纤维素微球粗产品浸泡于水中,除去残留的盐酸,得到再生纤维素微球。
按上述方案,步骤1)中,所述纤维素和纳米纤维素的质量比为1:(0~9),且纳米纤维素不为0。
按上述方案,步骤1)中,共混溶液中纤维素和纳米纤维素的总浓度为2%~6%。
按上述方案,步骤1)中,共混溶液为纤维素和纳米纤维素混合溶解在尿素和碱的水溶液。其中,纤维素和纳米纤维素的总量的质量百分含量为1~5wt.%,尿素的质量百分含量为2~30wt.%,碱的质量百分含量为6~10wt.%。碱优选碱金属的氢氧化物等。进一步地,碱优选氢氧化钠,共混溶液中尿素和氢氧化钠的质量百分含量分别为4~30wt.%、7~9wt.%;或者,碱优选氢氧化锂,共混溶液中尿素和氢氧化锂的质量百分含量分别为2~20wt.%、6~10wt.%。
进一步地,步骤1)中,共混溶液的配制方法是:将尿素和碱的混合水溶液预冷至-12~-20℃,然后加入纤维素和纳米纤维素混合物搅拌溶解,离心脱泡、除杂制得纤维素溶液。其中,离心采用转速为5000~10000rpm,时间为15~20min。
按上述方案,步骤1)中,共混溶液置于1~7℃条件储藏。
按上述方案,步骤2)中,盐酸溶液的浓度为5~10%,整个再生过程体系ph不超过5。共混溶液与盐酸溶液的体积比大约为(15-25)~(40-60)。
按上述方案,步骤2)中,滴加的速度是10ml/h~30ml/h。
按上述方案,步骤3)中,浸泡时间为3~5天。
本发明所述再生纤维素微球可以在益生菌的负载和/或肠道递送等方面广泛应用。
与现有技术相比,本发明的有益效果是:
(1)本发明选用纤维素作为基础原料,及tempo媒介氧化体系改性制备得到的纳米纤维素为原料,其中纤维素起到骨架支撑作用,纳米纤维素可用于调节微球的孔径和ph响应性能;所得的再生纤维素微球具有良好的孔径结构和ph响应性能,具有平均孔径为1~3μm,能实现益生菌的有效负载及肠道递送,对益生菌的有效负载量可达到2.68×108cfu/ml,有效递送量达到2.5×107cfu/ml,表现出良好的益生菌负载及肠道递送能力;
(2)本发明所述再生纤维素微球为益生菌包埋和递送提供了新的解决方案,且属环境友好材料,可广泛的应用于功能因子肠道递送领域,且具有应用到递送其他功能因子领域的应用前景,易于功能化拓展及应用。
(3)本发明采用绿色溶剂溶解纤维素和纳米纤维素,并通过简单的再生过程制备得到再生纤维素微球,制备过程简单环保无污染,所用原料来源广泛,价格低廉,可生物降解,无毒无污染,且具有良好的生物相容性。
附图说明
图1中,再生纤维素微球的制备流程及所得复合微球的宏观形貌图;
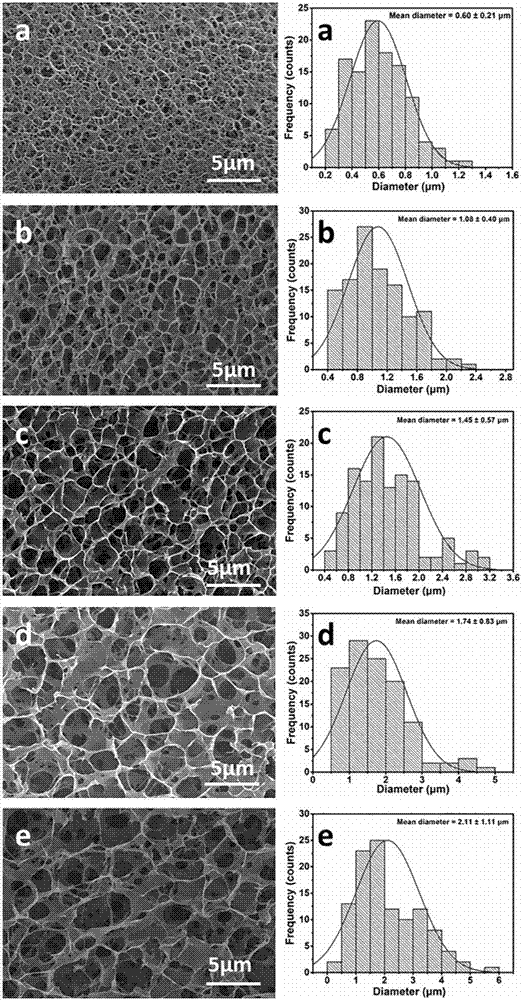
图2中,a,b,c,d,e分别代表对比例、实施例1~4所得再生纤维素微球扫描电镜图和孔径分布图;
图3中,cfm,ccnm-1,ccnm-2,ccnm-3,ccnm-4分别代表对比例、实施例1~4所得再生纤维素微球;其中,a是再生纤维素微球的孔隙率和载菌量的关系图,b为再生纤维素微球总载菌量释放曲线;
图4为对比例、实施例1~4所得再生纤维素微球在模拟肠道中益生菌释放曲线。
具体实施方式
为了更好地理解本发明所解决的技术问题、技术方案及技术效果,以下结合实施例和附图,对本发明的内容进一步详细说明,但不应理解为对本发明的限制。
下述实施例中纤维素均为棉短绒纤维素,它的粘均分子量为3万~37万道尔顿。
对比例
再生纤维素微球,其是由纤维素溶解所得共混溶液在盐酸溶液的作用下,经过再生制备得到的微球,具有平均孔径为~0.6μm的多孔网络结构,益生菌负载量达到~9.7×107cfu/ml,有效递送量达到~5.3×106cfu/ml。
上述再生纤维素微球的制备方法,具体步骤如下:
1)将4g纤维素立即加入预冷至-12.5℃的96g含8.7%lioh和12wt.%尿素的组合水溶液中,机械搅拌5min,在8000rpm条件下,离心15min,得到纤维素溶液,置于4℃条件储藏;
2)设置注射泵流速为20ml/h,将20ml纤维素溶液利用注射泵匀速滴加至50ml10%hcl溶液中,滴加过程中持续磁力搅拌,得到再生纤维素微球粗产品;
3)从盐酸溶液中过滤再生纤维素微球粗产品后,反复水洗得到纯净的再生纤维素微球微球。
实施例1
再生纤维素微球,其是由纤维素和纳米纤维素混合溶解所得共混溶液在盐酸溶液的作用下,经过再生制备得到的微球,具有平均孔径为~1.08μm的多孔网络结构,益生菌负载量达到~1.23×108cfu/ml,有效递送量达到~8×106cfu/ml,其中纤维素和纳米纤维素的质量比为3:7。
上述再生纤维素微球的制备方法,具体步骤如下:
1)将2.8g纤维素与1.2g纳米纤维素混合后,立即加入预冷至-12.5℃的96g含8.7%lioh和12wt.%尿素的组合水溶液中,机械搅拌5min,在8000rpm条件下,离心15min,得到纤维素和纳米纤维素共混溶液,置于4℃条件储藏;
2)设置注射泵流速为20ml/h,将20ml纤维素和纳米纤维素混合溶液利用注射泵匀速滴加至50ml10%hcl溶液中,滴加过程中持续磁力搅拌,得到再生纤维素微球粗产品;
3)从盐酸溶液中过滤再生纤维素微球粗产品后,反复水洗得到纯净的再生纤维素微球微球。
实施例2
再生纤维素微球,其是由纤维素和纳米纤维素混合溶解所得共混溶液在盐酸溶液的作用下,经过再生制备得到的微球,具有平均孔径为~1.45μm的多孔网络结构,益生菌负载量达到~1.4×108cfu/ml,有效递送量达到~1×107cfu/ml,其中纤维素和纳米纤维素的质量比为5:5。
上述再生纤维素微球的制备方法,具体步骤如下:
1)将2g纤维素与2g纳米纤维素混合后,立即加入预冷至-12.5℃的96g含8.7%lioh和12wt.%尿素的组合水溶液中,机械搅拌5min,在8000rpm条件下,离心15min,得到纤维素和纳米纤维素混合溶液,置于4℃条件储藏。
2)设置注射泵流速为20ml/h,将20ml纤维素和纳米纤维素混合溶液利用注射泵匀速滴加至50ml10%hcl溶液中,滴加过程中持续磁力搅拌,得到再生纤维素微球粗产品;
3)从盐酸溶液中过滤再生纤维素微球粗产品后,反复水洗得到纯净的再生纤维素微球微球。
实施例3
再生纤维素微球,其是由纤维素和纳米纤维素混合溶解所得共混溶液在盐酸溶液的作用下,经过再生制备得到的微球,具有平均孔径为~1.74μm的多孔网络结构,益生菌负载量达到~2.0×108cfu/ml,有效递送量达到~1.7×107cfu/ml,其中纤维素和纳米纤维素的质量比为3:7。
上述再生纤维素微球的制备方法,具体步骤如下:
1)将1.2g纤维素与2.8g纳米纤维素混合后,立即加入预冷至-12.5℃的96g含8.7%lioh和12wt.%尿素的组合水溶液中,机械搅拌5min,在8000rpm条件下,离心15min,得到纤维素和纳米纤维素混合溶液,置于4℃条件储藏。
2)设置注射泵流速为20ml/h,将20ml纤维素和纳米纤维素混合溶液利用注射泵匀速滴加至50ml10%hcl溶液中,滴加过程中持续磁力搅拌,得到再生纤维素微球粗产品;
3)从盐酸溶液中过滤再生纤维素微球粗产品后,反复水洗得到纯净的再生纤维素微球微球。
实施例4
再生纤维素微球,其是由纤维素和纳米纤维素混合溶解所得共混溶液在盐酸溶液的作用下,经过再生制备得到的微球,具有平均孔径为~2.11μm的多孔网络结构,益生菌负载量达到~2.7×108cfu/ml,有效递送量达到~2.3×107cfu/ml,其中纤维素和纳米纤维素的质量比为1:9。
上述再生纤维素微球的制备方法,具体步骤如下:
1)将0.4g纤维素与3.6g纳米纤维素混合后,立即加入预冷至-12.5℃的96g含8.7%lioh和12wt.%尿素的组合水溶液中,机械搅拌5min,在8000rpm条件下,离心15min,得到纤维素和纳米纤维素混合溶液,置于4℃条件储藏。
2)设置注射泵流速为20ml/h,将20ml纤维素和纳米纤维素混合溶液利用注射泵匀速滴加至50ml10%hcl溶液中,滴加过程中持续磁力搅拌,得到再生纤维素微球粗产品;
3)从盐酸溶液中过滤再生纤维素微球粗产品后,反复水洗得到纯净的再生纤维素微球微球。
如图2所示,对比例与实施例1~实施例4再生纤维素微球孔径分别是0.6μm,1.08μm,1.45μm,1.74μm,2.11μm,平均孔径呈现逐渐增大的趋势,再生纤维素微球平均孔径随着纳米纤维素含量增高而逐渐增大。
为了进一步验证再生纤维素微球益生菌负载性能和孔径大小的关系,对比例、实施例1~4所得再生纤维素微球的孔隙率和载菌量的关系图、总载菌量释放曲线结果如图3所示,可知:随着纳米纤维素含量增多,再生纤维素微球孔径变大,载菌能力显著增强,总载菌量从9.7×107cfu/ml增加至2.7×108cfu/ml,证实了再生纤维素微球具有良好的益生菌负载性能。
在此基础上,验证了再生纤维素微球对益生菌的肠道递送性能,将载菌微球在模拟胃液中浸泡2小时后转移至模拟肠液中进行释放试验。图4为对比例、实施例1~4所得再生纤维素微球在模拟肠道中益生菌释放曲线,递送量从5.3×106cfu/ml增加至2.3×107cfu/ml,证实了再生纤维素微球可有效保护足量益生菌到达肠道。
以上所述仅是本发明的优选实施方式,应当指出,对于本领域的普通技术人员来说,在不脱离本发明创造构思的前提下,还可以做出若干改进和变换,这些都属于本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!