Nω-Asp-Nα-(17β-雌二醇-3-乙酰基)-Lys,其制备,活性和应用的制作方法
本发明涉及nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys,涉及它的制备方法,涉及它与ca2+络合的逐级稳定常数,进一步涉及它在小鼠骨质疏松模型上的抗骨质疏松作用,因而本发明涉及它在制备抗骨质疏松药物中的应用。本发明属于生物医药领域。
背景技术:
骨质疏松症是以骨量低和骨组织微结构破坏为特征的全身性疾病。药源性骨质疏松症普遍出现在服用可的松,氢化可的松和地塞米松的患者。糖皮质激素,例如可的松,氢化可的松和地塞米松,是临床抗炎和免疫抑制的一线药物。虽然可的松,氢化可的松和地塞米松有很好的抗炎和免疫抑制作用,但是它们引起骨质疏松副作用严重限制了它们的临床应用。虽然普遍使用的17β-雌二醇可以拮抗糖皮质激素引起的骨质疏松症,但是抗骨质疏松症药物都存在子宫内膜增生和凝血两种副反应。这种状态使得发明拮抗糖皮质激素的骨质疏松症副作用的新型抗骨质疏松药物,一直是药物研究的兴趣之一。不过,始终没有找到实质性解决办法。例如2006年美国公开的一项专利(us7067505b2)虽然涉及了一个天冬氨酸的主链和侧链羧基连接两个雌二醇的化合物(简称1-天冬缀2-雌醇)的合成方法,但是没有评价它的活性和副作用。2000年发明人就开始研究雌二醇的结构修饰,发现用天冬氨酸连接雌二醇的关键技术有两点。一点是asp连接到lys的侧链氨基,另一点是lys的α-氨基通过羰亚甲基连接到雌二醇的3-位酚羟基上,才能既增强雌二醇的抗骨质疏松活性又消除雌二醇的子宫内膜增生和凝血两个副作用。根据这个发现,发明人提出了本发明。本发明的突出创造性在于,1)nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的骨靶向性质导致的优秀的抗骨质疏松作用;2)nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys可释放17β-雌二醇;3)nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys没有17β-雌二醇的毒副作用。
技术实现要素:
本发明的第一个内容是提供下式的nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys。
本发明的第二个内容是提供nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的制备方法,该方法包括以下步骤:
1)17β-雌二醇与溴乙酸乙酯在丙酮中和k2co3存在下于65℃回流3-乙氧羰亚甲基-17β-雌二醇;
2)在氢氧化钠水溶液中3-乙氧羰亚甲基-17β-雌二醇水解为3-羧亚甲基-17β-雌二醇;
3)在dcc存在下3-羧亚甲基-17β-雌二醇与lys(boc)-obzl缩合生成17β-雌二醇-3-亚甲基甲酰-lys(boc)-obzl;
4)在氯化氢的乙酸乙酯溶液中17β-雌二醇-3-亚甲基甲酰-lys(boc)-obzl脱boc生成17β-雌二醇-3-亚甲基甲酰-lys-obzl;
5)在dcc存在下17β-雌二醇-3-亚甲基甲酰-lys-obzl与boc-asp(obzl)缩合生成17β-雌二醇-3-亚甲基甲酰-lys[boc-asp(obzl)]-obzl;
6)在乙醇水溶液中17β-雌二醇-3-亚甲基甲酰-lys[boc-asp(obzl)]-obzl氢解脱除苄基生成17β-雌二醇-3-亚甲基甲酰-lys(boc-asp);
7)在氯化氢的乙酸乙酯溶液中17β-雌二醇-3-亚甲基甲酰-lys(boc-asp)脱boc生成nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys。
本发明的第三个内容是评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的抗骨质疏松活性。
本发明的第四个内容是评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的子宫内膜增生副作用。
本发明的第五个内容是评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的凝血副作用。
附图说明
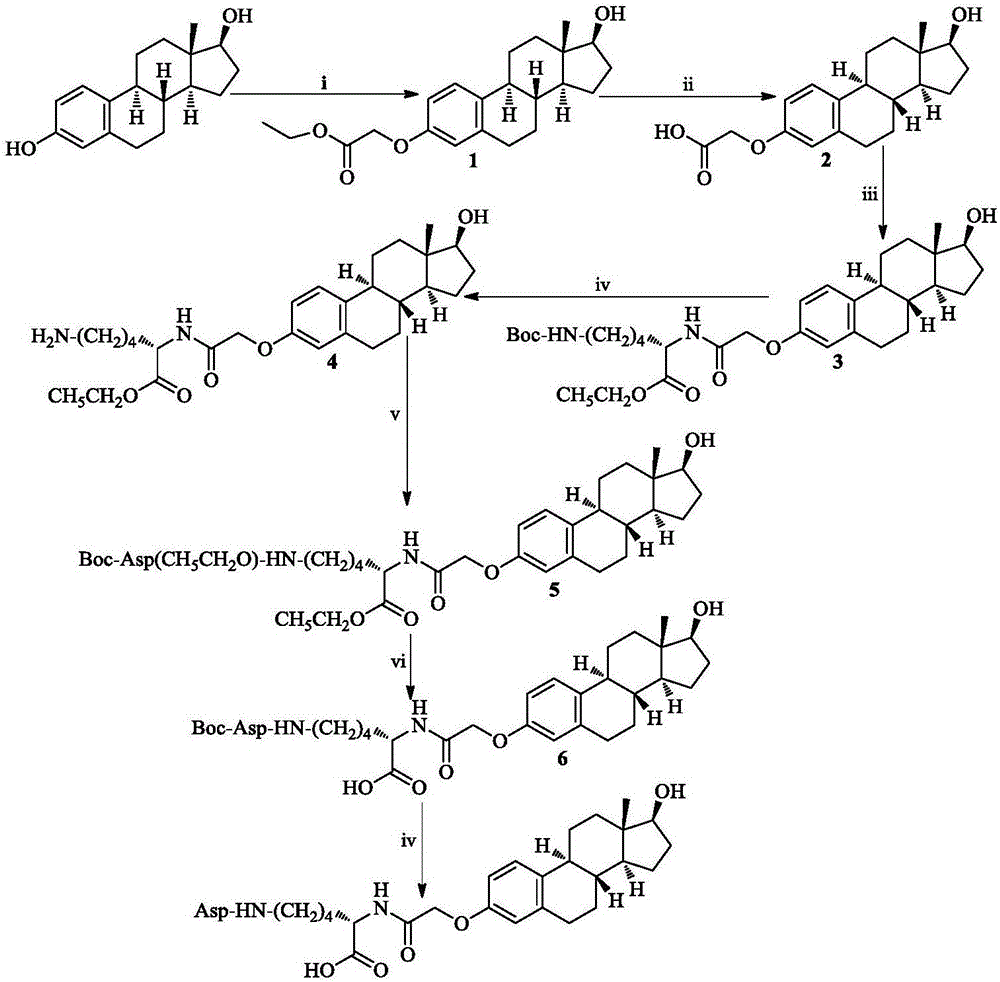
图1.nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的合成路线,i溴乙酸乙酯,k2co3,丙酮,回流,65℃;ii2nnaoh;iiik(boc)-obzl,hobt/dcc,thf,nmm;iv4nhcl/ea;vboc-d(obzl),hobt/dcc,thf,nmm;vih2,pd/c。
实施方式
为了进一步阐明本发明下面给出一系列实施例。必须指出,这些实施例完全是例证性的。给出这些实施例的目的是为了充分明示本发明的意义和内容,决不对本发明造成任何形式的限制。
实施例1制备3-乙氧羰亚甲基-17β-雌二醇(1)
向10.0g(36.76mmol)17β-雌二醇与100ml丙酮的溶液中加入5.60g(40.58mmol)k2co3和4.5ml(40.42mmol)溴乙酸乙酯。混合物于65℃回流12h,tlc板监测(石油醚/乙酸乙酯,2/1)17β-雌二醇消失,过滤除去k2co3,滤液减压浓缩,残留物通过硅胶柱层析纯化(二氯甲烷/甲醇,100/1)得7.80g(59%)标题化合物,为无色固体。esi-ms(m/e):359.22235[m+h]+;1hnmr(300mhz,dmso-d6):δ/ppm=7.16(d,j=8.4hz,1h),6.65(dd,j1=8.4hz,j2=2.7hz,1h),6.58(d,j=2.7hz,1h),4.68(s,2h),4.50(d,j=4.5hz,1h),4.16(q,j=3.3hz,2h),3.52(m,1h),2.74(m,2h),2.26(d,j=13.5hz,1h),2.11(m,1h),1.87-1.78(m,3h),1.53(m,1h),1.39-1.21(m,10h),0.66(s,3h)。
实施例2制备3-羧亚甲基-17β-雌二醇(2)
0℃向7.00g(19.55mmol)3-乙氧羰亚甲基-17β-雌二醇(1)与150ml甲醇的溶液中加入naoh水溶液(2n)调节ph值到12。混合物0℃搅拌2小时,tlc监测(石油醚/乙酸乙酯,1/1;含2滴冰醋酸)至1消失。反应混合物于0℃用稀盐酸调节ph值至2,用乙酸乙酯萃取。乙酸乙酯层用无水na2so4干燥12小时,过滤,滤液减压浓缩得5.89g(91%)标题化合物,为无色固体。esi-ms(m/e):329.17532[m-h]-;1h-nmr(300mhz,dmso-d6):δ/ppm=12.95(s,1h),7.16(d,j=8.4hz,1h),6.65(dd,j1=8.4hz,j2=2.1hz,1h),6.58(d,j=2.7hz,1h),4.68(s,2h),4.50(d,j=4.5hz,1h),3.52(m,1h),2.75(m,2h),2.26(d,j=13.5hz,1h),2.11(m,1h),1.91-1.77(m,3h),1.53(m,1h),1.36-1.06(m,7h),0.67(s,3h)。
实施例3制备17β-雌二醇-3-亚甲基甲酰-lys(boc)-obzl(3)
0℃向3.60g(10.91mmol)3-羧亚甲基-17β-雌二醇(2)与50ml无水四氢呋喃的溶液中加1.51g(11.19mmol)1-羟基苯并三唑(hobt)和2.52g(12.23mmol)二环己基碳二亚胺(dcc)并搅拌0.5小时,得到反应液i。0℃向4.81g(13.26mmol)hcl·lys(boc)-obzl与50ml无水四氢呋喃的溶液中加n-甲基吗啉(nmm)调节ph值为8,得到反应液ii。0℃将反应液ii加到反应液i中,搅拌0.5小时,用nmm调节ph值为8,室温反应6h,tlc板监测(二氯甲烷/甲醇,20/1)2消失。反应液过滤除去二环己基脲(dcu),滤液减压浓缩,残留物用乙酸乙酯溶解,过滤除去残留的dcu,乙酸乙酯层依次用5%碳酸氢钠溶液洗3次,饱和氯化钠溶液洗3次,5%硫酸氢钾溶液洗3次,饱和氯化钠溶液洗3次,5%碳酸氢钠溶液洗3次及饱和氯化钠溶液洗3次。乙酸乙酯层用无水硫酸钠干燥12小时,过滤,滤液减压浓缩,残留物用柱层析纯化(二氯甲烷/甲醇,40/1),得5.33g(75%)标题化合物,为无色固体。esi-ms(m/e):589.38532[m+h]+;1hnmr(300mhz,dmso-d6):δ/ppm=8.34(d,j=7.8hz,1h),7.34(m,5h),7.15(d,j=8.4hz,1h),6.75(s,1h),6.69(dd,j1=8.4hz,j2=2.7hz,1h),6.62(d,j=2.7hz,1h),5.13(s,2h),4.49(s,3h),4.34(m,1h),3.52(m,1h),2.84(d,j=6.3hz,2h),2.74(m,2h),2.26(d,j=13.5hz,1h),2.11(m,1h),1.87-1.57(m,6h),1.36-1.13(m,20h),0.66(s,3h)。
实施例4制备17β-雌二醇-3-亚甲基甲酰-lys-obzl(4)
0℃将2.40g(3.70mmol)17β-雌二醇-3-亚甲基甲酰-lys(boc)-obzl(3)与25ml无水乙酸乙酯的溶液搅拌并加入30ml氯化氢的乙酸乙酯溶液(4m)。搅拌2h后,tlc显示(二氯甲烷/甲醇,15/1)3消失。反应溶液减压浓缩,除净氯化氢气体。残留物用无水乙醚研磨,得到1.83g(85%)标题化合物,为无色固体。esi-ms(m/e):489.33292[m+h]+;1h-nmr(300mhz,dmso-d6):δ/ppm=8.43(d,j=7.5hz,1h),7.35(m,5h),7.14(d,j=8.7hz,1h),6.68(dd,j1=8.7hz,j2=2.1hz,1h),6.62(d,j=2.1hz,1h),5.13(s,2h),4.49(s,3h),4.38(m,1h),3.52(m,1h),2.73(s,2h),2.47(m,2h),2.34(d,j=13.5hz,1h),2.11(m,1h),1.89-1.51(m,6h),1.36-1.13(m,11h),0.66(s,3h)。
实施例5制备17β-雌二醇-3-亚甲基甲酰-lys[boc-asp(obzl)]-obzl(5)
0℃向3.23g(10.00mmol)boc-asp(obzl)与50ml无水四氢呋喃的溶液加1.35g(10.00mmol)hobt和2.47g(11.99mmol)dcc并搅拌0.5小时,得到反应液i。0℃向6.00g(10.95mmol)n-(3-羧亚甲氧基-雌二醇)-lys-obzl与50ml无水四氢呋喃的溶液中加nmm调节ph值为8,得到反应液ii。0℃将反应液ii加到反应液i中,搅拌0.5小时,用nmm调节ph值为8,室温反应6h,tlc板监测(二氯甲烷/甲醇,10/1)4消失。反应液过滤除去dcu,滤液减压浓缩,残留物用乙酸乙酯溶解,过滤除去残留的dcu,乙酸乙酯层依次用5%碳酸氢钠溶液洗3次,饱和氯化钠溶液洗3次,5%硫酸氢钾溶液洗3次,饱和氯化钠溶液洗3次,5%碳酸氢钠溶液洗3次及饱和氯化钠溶液洗3次。乙酸乙酯层用无水硫酸钠干燥12小时,过滤,滤液减压浓缩,残留物用柱层析纯化(二氯甲烷/甲醇,20/1),得6.07g(71.1%)标题化合物,为无色固体。esi-ms(m/e):854.45135[m+h]+;1h-nmr(300mhz,dmso-d6):/ppm=8.33(d,j=7.5hz,1h),7.38-7.28(m,10h),7.15(d,j=8.4hz,1h),6.85(s,1h),6.76(dd,j1=8.4hz,j2=3.0hz,1h),6.65(d,j=3.0hz,1h),5.23(s,2h),5.12(s,2h),4.82(m,1h),4.27(s,3h),4.17(m,1h),3.62(m,1h),2.94(m,1h),2.79(d,j=6.0hz,2h),2.70(m,2h),2.64(m,1h),2.23(d,j=13.2hz,1h),2.05(m,1h),1.77-1.55(m,6h),1.37-1.11(m,20h),0.72(s,3h)。
实施例6制备17β-雌二醇-3-亚甲基甲酰-lys(boc-asp)(6)
将853mg(1.00mmol)17β-雌二醇-3-亚甲基甲酰-lys[boc-asp(obzl)]-obzl(5)用20ml乙醇溶解,加50mg钯碳,室温通12小时氢气。结束反应并滤除钯碳,滤液减压浓缩得到639.1g(95%)标题化合物,无色固体。esi-ms(m/e):674.36535[m+h]+。
实施例7制备nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys
按照实施例4的方法从600mg(0.89mmol)17β-雌二醇-3-亚甲基甲酰-lys(boc-asp)(6)得到515mg(90%)标题化合物,为无色固体。esi-ms(m/e):574.31288[m+h]+;
实施例8评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys对卵巢切除雌性小鼠骨小梁密度的影响
卵巢切除雌性小鼠的骨小梁密度是抗骨质疏松活性重要指标。为评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的抗骨质疏松活性,本发明首先评价了它对卵巢切除的雌性小鼠骨小梁密度的影响。icr小鼠(体重25.0±2.0g)随机分为假手术组(sham组),卵巢切除组加羧甲基纤维素钠(cmcna)组,巢切除组加雌二醇组(口服剂量为2.3μmol/kg),卵巢切除加nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys(口服剂量为100,10和1nmol/kg),每组11只小鼠。所有小鼠都连续治疗4周。最后一次给药后的次日在小鼠称体重和眼眶取血之后,乙醚麻醉,处死。取小鼠左侧股骨,剔除干净肌肉组织,用氯仿/甲醇(2/1)浸泡两次(每次3小时)脱脂,在断层扫描仪上测定股骨关节头下方0.2-0.4mm处测定骨小梁密度。表1的结果表明,nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys剂量依赖地抑制卵巢切除小鼠骨小梁密度降低。nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的最低有效剂量是1mol/kg。在230nmol/kg剂量下17β-雌二醇没有活性。也就是说nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的活性比17β-雌二醇至少强230倍,体现了本发明意想不到的技术效果。
表1口服nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys小鼠的骨小梁密度
a)与卵巢切除加cmcna组小鼠比p<0.01,与假手术组小鼠比p<0.05;b)与卵巢切除加cmcna组,卵巢切除加2300nmol/kg17β-雌二醇组及卵巢切除加剂量为10nmol/kgnω-asp-nα-(17β-雌二醇-3-乙酰基)-lys组的小鼠比p<0.01,与假手术组小鼠比p>0.05;c)与卵巢切除加剂量为1nmol/kg的nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys组的小鼠比p<0.05;c)与卵巢切除加cmcna组小鼠和卵巢切除加剂量为100nmol/kg的nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys组的小鼠比p<0.01,与卵巢切除加剂量为1nmol/kg的nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys组的小鼠比p<0.05;d)与卵巢切除加cmcna组的小鼠比p<0.05;n=11。
实施例9评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys对卵巢切除雌性小鼠股骨干重的影响
卵巢切除的雌性小鼠股骨干重是抗骨质疏松活性的重要指标。为评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的抗骨质疏松活性,本发明评价了它对卵巢切除的雌性小鼠股骨干重的影响。实施例8测定了骨小梁密度的小鼠左侧股骨置烘箱中于120℃烘6小时,称股骨干重。结果见表2。结果表明,在三种剂量下nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys都能有效地抑制卵巢切除小鼠股骨减重。nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的最低有效剂量是1nmol/kg。在230nmol/kg剂量下17β-雌二醇没有活性。也就是说nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的活性比17β-雌二醇至少强230倍,体现了本发明意想不到的技术效果。
表2口服nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys小鼠的股骨干重
a)与卵巢切除加cmcna组小鼠比p<0.01,与假手术组小鼠比p>0.05;b)与卵巢切除加cmcna组小鼠比p>0.05;n=11.
实施例10评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys对卵巢切除雌性小鼠股骨灰重的影响
卵巢切除的雌性小鼠股骨煅烧之后的灰重是抗骨质疏松活性的重要指标。为评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的抗骨质疏松活性,本发明评价了它对卵巢切除的雌性小鼠股骨煅烧遗留的灰重量的影响。实施例8测定了骨小梁密度的小鼠左侧股骨置烘箱中于120℃烘6小时之后,置800℃马福炉煅烧8小时,称股骨的灰重。结果见表3。结果表明,nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys剂量依赖地抑制卵巢切除小鼠股骨灰减重。nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的最低有效剂量是1nmol/kg。在230nmol/kg剂量下17β-雌二醇没有活性。也就是说nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的活性比17β-雌二醇至少强230倍,体现了本发明意想不到的技术效果。
表3口服nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys小鼠的股骨灰重
a)与卵巢切除加cmcna组小鼠比p<0.01,与假手术组小鼠比p>0.05;b)与卵巢切除加cmcna组小鼠比p>0.05;c)与卵巢切除加cmcna组小鼠比p<0.01,与卵巢切除加剂量为10nmol/kg的nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys组的小鼠比p<0.05,与卵巢切除加剂量为1nmol/kg的nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys组的小鼠比p<0.01,与假手术组小鼠比p>0.05;d)与卵巢切除加cmcna组小鼠比p<0.01,与卵巢切除加剂量为1nmol/kg及100nmol/kg的nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys组的小鼠比p<0.05;e)与卵巢切除加cmcna组小鼠比p<0.05;n=11.
实施例11评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys对卵巢切除雌性小鼠股骨的矿物质含量的影响
卵巢切除的雌性小鼠股骨的矿物质含量(bmc)是抗骨质疏松活性的重要指标。股骨矿物质含量是指股骨灰重与干重的比值。为评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的抗骨质疏松活性,本发明计算了nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys对卵巢切除的雌性小鼠股骨灰重与干重的比值的影响。将实施例10测定的小鼠左侧股骨灰重除以实施例9测定的小鼠左侧股骨干重得到股骨灰重与干重的比值,即股骨中的矿物质含量。结果见表4。结果表明,nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys剂量依赖地抑制卵巢切除小鼠股骨中的矿物质含量降低。nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的最低有效剂量是10nmol/kg。在230nmol/kg剂量下17β-雌二醇没有活性。也就是说nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的活性比17β-雌二醇至少强23倍,体现了本发明意想不到的技术效果。
表4口服nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys小鼠股骨的矿物质密度
a)与卵巢切除加cmcna组小鼠比p>0.05;b)与卵巢切除加cmcna组小鼠比p<0.01,与假手术组小鼠比p<0.05;c)与卵巢切除加cmcna组小鼠比p<0.01,与假手术组小鼠比p<0.05,与卵巢切除加剂量为10nmol/kg的nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys组的小鼠比p<0.05,与卵巢切除加剂量为1nmol/kg的nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys组的小鼠比p<0.01;d)与卵巢切除加cmcna组及卵巢切除加剂量为10nmol/kg的nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys组的小鼠比p<0.05;n=11.
实施例12评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys对卵巢切除雌性小鼠股骨灰重与股骨长度比值的影响
为澄清nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys在三种剂量下都能有效地抑制卵巢切除小鼠股骨灰减重是否与小鼠股骨生长有关,本发明测定了股骨长度并计算了小鼠股骨灰重与长度的比值。结果见表5。结果表明,nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys虽然能有效地抑制卵巢切除小鼠股骨灰重与长度比值降低,但对股骨长度没有影响。可见nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys对股骨生长没有影响,它有效地抑制卵巢切除小鼠股骨灰重与长度比值降低是有效抑制股骨中矿物质丢失的结果。
表5口服nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys小鼠股骨灰重与长度的比值
a)与cmcna组小鼠比p<0.01;b)与卵巢切除加cmcna组小鼠比p>0.05;n=11.
实施例13评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys对卵巢切除雌性小鼠股骨中钙含量的影响
卵巢切除的雌性小鼠骨中钙含量是抗骨质疏松活性的重要指标。为评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的抗骨质疏松活性,本发明评价了它对卵巢切除的雌性小鼠骨中钙含量的影响。卵巢切除小鼠连续治疗4周,最后一次给药后的次日眼眶取血,静置30min,3000g/min离心20min得血清,用邻甲酚酞络合酮法测定骨钙和血钙含量,用钼蓝法测定骨磷和血磷含量,用磷酸苯二钠为底物测定血清碱性磷酸酶含量。测定发现nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys对卵巢切除的雌性小鼠的血钙含量,骨磷含量,血磷含量和血清碱性磷酸酶含量都没有影响。对卵巢切除的雌性小鼠的骨钙含量的影响见表6。结果表明,nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys剂量依赖地抑制卵巢切除的雌性小鼠骨钙含量降低,最低有效剂量是10nmol/kg。也就是说nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的活性比17β-雌二醇至少强23倍,体现了本发明意想不到的技术效果。
表6口服nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys小鼠股骨的钙含量
a)与卵巢切除加cmcna组小鼠p<0.01,与假手术组小鼠比p>0.05;b)与卵巢切除加cmcna组小鼠及卵巢切除加剂量为1nmol/kg的nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys组的小鼠比p<0.01,与卵巢切除加剂量为10nmol/kg的nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys组的小鼠比p<0.05,与假手术组小鼠比p>0.05;c)与卵巢切除加cmcna组小鼠比p<0.01,与卵巢切除加剂量为1nmol/kg的nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys组的小鼠比p<0.05;d)与卵巢切除加cmcna组小鼠比p>0.05;n=11.
实施例14评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys治疗卵巢切除雌性小鼠的子宫内膜增生副作用
子宫内膜增生是17β-雌二醇治疗的主要副作用之一。为考察nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys是否能够避免这种副作用,本发明评价了它对卵巢切除的雌性小鼠的子宫重量的影响。表7的结果表明,在2300nmol/kg和230nmol/kg两种剂量下17β-雌二醇显著增加卵巢切除的雌性小鼠的子宫重量。在100nmol/kg,10nmol/kg和1nmol/kg三种剂量下nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys都可有效地抑制卵巢切除雌性小鼠的子宫增重。可见nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys能够避免17β-雌二醇的子宫内膜增生副作用。表7的结果还表明,cmcna治疗的卵巢切除的雌性小鼠出现预期的子宫萎缩的现象。
表7口服nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys小鼠股骨的钙含量
a)与卵巢切除加cmcna组小鼠及假手术组小鼠比p<0.01;b)与假手术组小鼠比p>0.05;n=11.
实施例15评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys治疗卵巢切除雌性小鼠的血栓形成副作用
血栓形成是17β-雌二醇治疗的另一个主要副作用。为考察nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys是否能够避免这种副作用,本发明评价了它治疗的卵巢切除雌性小鼠的尾出血时间。最后一次给药30min后,将小鼠装入固定装置内并使尾巴外露,在尾末端2mm处快速剪尾让切口自然流血并开始计时。每隔30秒用滤纸轻轻拭去切口的血滴,直至自然止血。从出血到止血的时间即为出血时间。表8的结果表明,表8的结果表明,在2300nmol/kg和230nmol/kg两种剂量下17β-雌二醇显著缩短卵巢切除的雌性小鼠的尾出血时间。在100nmol/kg,10nmol/kg和1nmol/kg三种剂量下nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys都不影响卵巢切除的雌性小鼠的尾出血时间。可见,nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys没有17β-雌二醇治疗的血栓形成风险。
表8口服nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys小鼠的尾出血时间
a)与卵巢切除加cmcna组小鼠及假手术组小鼠比p<0.05;b)与卵巢切除加cmcna组小鼠及假手术组小鼠比p>0.05;n=11.
实施例16评价nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys治疗卵巢切除雌性小鼠的脂肪肝副作用
脂肪肝是17β-雌二醇治疗的一个次要副作用。为考察nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys是否能够避免这种副作用,本发明评价了它对卵巢切除的雌性小鼠的肝重的影响。最后一次给药的次日,小鼠乙醚麻醉,处死,取肝,称重。表9的结果表明,在2300nmol/kg和230nmol/kg两种剂量下17β-雌二醇显著显著增加卵巢切除的雌性小鼠的肝重。在100nmol/kg,10nmol/kg和1nmol/kg三种剂量下nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys都不影响卵巢切除的雌性小鼠的肝重。可见,nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys没有17β-雌二醇治疗的脂肪肝风险。
表9口服nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys小鼠的肝重
a)与卵巢切除加cmcna组小鼠及假手术组小鼠比p<0.05;b)与假手术组小鼠比p>0.05;n=11.
实施例17测定nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys与二价钙络合物的逐级稳定常数采用ph计(211a,hanna,italy),用ph6.86和ph4.01的标准缓冲溶液分别校准仪器。配制koh标准溶液(45.90mm),盐酸标准溶液(91.2mm),ca2+标准溶液(109.46mm),kcl标准溶液(0.5m)。首先精密称量10.01mgnω-asp-nα-(17β-雌二醇-3-乙酰基)-lys,用移液管分别移取1.5ml盐酸标准溶液,6.0mlkcl标准溶液,7.5mlh2o于50ml烧杯中,加入搅拌子,在电磁搅拌器上搅拌均匀,测量ph值。用20ml碱式滴定管,装入koh标准溶液,进行滴定。每滴0.2mlkoh,测一次溶液ph值。其次称量10.01mgnω-asp-nα-(17β-雌二醇-3-乙酰基)-lys,用移液管分别移取1.5ml盐酸标准溶液,6.0mlkcl标准溶液,7.5mlh2o,3.75mlcacl2于50ml烧杯中,按以上同样方法以koh标准溶液滴定。用origin7.5软件计算nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys的加质子常数
表10.nω-asp-nα-(17β-雌二醇-3-乙酰基)-lys与ca2+络合物的逐级稳定常数
- 还没有人留言评论。精彩留言会获得点赞!