经标记的核苷酸组合物及用于核酸测序的方法与流程
根据35u.s.c.§119(e),本申请要求2016年11月23日提交的美国临时申请62/426,144和2016年5月20日提交的美国临时申请62/339,790的优先权,其通过引用整体并入本文。
【技术领域】
本申请整体涉及用于进行生物学及/或化学样品的快速的大规模并行定量分析的方法、组合物及装置;及制造该装置的方法。
背景技术:
生物样品的检测及分析可使用生物学分析(“生物分析”)。生物分析通常涉及昂贵的大型实验室设备,该设备需要经培训的研究科学家操作并进行生物分析。此外,生物分析通常以大量进行,因此大量特定类型的样品为检测及定量所必需的。
藉由用发射特定波长的光的发光标记物标记样品来进行一些生物分析。用光源照明标记物以使得发光,且用光检测器检测发光光源以对标记物发射的发光光源的量进行定量。使用发光标记物的生物分析通常涉及昂贵的雷射光源以照射样品和复杂的发光检测光学装置及电子装置以自照明的样品采集发光。
技术实现要素:
在其他方面中,本发明提供一种经发光标记的核苷酸,其包含一或多个经由核酸连接至一或多个多磷酸核苷的发光标记,其中该核酸包含保护组件。在一些实施例中,保护组件涉及核酸的一或多个特征和/或修饰,其当所述一或多个多磷酸核苷的多磷酸核苷在聚合酶的活性位点中或附近时,保护聚合酶免受一或多个发光标记的损伤作用。
在一些实施例中,核酸为单链的。在一些实施例中,核酸为双链的。在一些实施例中,本发明的双链核酸包含:第一寡核苷酸链,其包含连接在沿着第一寡核苷酸链的任一侧面上具有一或多个核苷酸的内部位置处的一或多个发光标记;及第二寡核苷酸链,其包含一或多个多磷酸核苷,其中该第二寡核苷酸链退火至第一寡核苷酸链。
在一些实施例中,本发明的经发光标记的核苷酸包含两种或更多个经由包含多个胸苷核苷酸的连接子连接至核酸的多磷酸核苷。在一些实施例中,连接子包含支链连接子,例如支链胸苷连接子。在一些实施例中,支链连接子包含支链胸苷连接子。举例而言,在一些实施例中,各核苷多磷酸包含式nu-t(t)nt-r的胸苷连接子,其中nu代表多磷酸核苷,t代表胸苷核苷酸,n为1与30间的值的整数,且r代表连接一或多个额外多磷酸核苷的汇合点。在一些实施例中,汇合点进一步直接连接至核酸的寡核苷酸链。在一些实施例中,汇合点例如经由其他胸苷连接子和/或其他汇合点进一步间接连接至寡核苷酸链。
在一些实施例中,核酸的保护组件包含至少一种能量吸收修饰。在一些实施例中,至少一种能量吸收修饰包含三重态淬灭剂。在一些实施例中,至少一种能量吸收修饰包含树枝状修饰。在一些实施例中,至少一种能量吸收修饰包含单糖-teg、双糖、n-乙酰基单糖、tempo-teg、trolox-teg或甘油树状体。在一些实施例中,保护组件包含一或多个茎-环。在一些实施例中,一或多个茎-环为未标记的,例如一或多个茎-环并不包含连接在茎-环的环和/或茎的发光标记。在一些实施例中,一或多个茎-环在一或多个发光标记与一或多个多磷酸核苷之间的核酸上的位置中。在此类实施例中,一或多个未标记茎-环可提供产生聚合酶保护作用的立体阻挡物和/或吸收阻挡物。
在一些实施例中,一或多个发光标记可连接在至少一或多个茎-环的环。然而,在一些实施例中,保护组件(例如一或多个未标记的茎-环)将一或多个发光标记与一或多个多磷酸核苷分离。
在一些实施例中,经发光标记的核苷酸的核酸进一步包含退火至第一及第二寡核苷酸链中的至少一者的第三寡核苷酸链。在一些实施例中,核酸进一步包含退火至第一、第二及第三寡核苷酸链中的至少一者的第四寡核苷酸链。在一些实施例中,寡核苷酸链形成霍利迪连结体(hollidayjunction)。
在一些方面中,本发明提供测定模板核酸序列的方法。在一些实施例中,该等方法包括以下步骤:其包含使目标体积中的复合物曝露于多种类型经发光标记的核苷酸,该复合物包含模板核酸、引物及聚合酶。在一些实施例中,各类型的经发光标记的核苷酸包含一或多个经由核酸连接至一或多个多磷酸核苷的发光标记。在一些实施例中,核酸包含保护组件。因此,在一些方面中,本发明提供核酸测序方法,其利用本文所描述的经发光标记的多磷酸核苷组合物中的任一者。
在一些实施例中,该等方法进一步包含将一系列一或多个激发能脉冲引向目标体积附近的步骤。在一些实施例中,该等方法进一步包含在连续并入包含引物的核酸期间检测自经发光标记的核苷酸的多个发射光子的步骤。在一些实施例中,该等方法进一步包含藉由测定发射光子的时序及任选的频率鉴别并入的核苷酸的序列的步骤。
在一些实施例中,反应混合物中的四种不同类型的核苷酸(例如腺嘌呤、鸟嘌呤、胞嘧啶、胸腺嘧啶/尿嘧啶)可各自用一或多个发光分子(例如一或多个发光标记)标记。在一些实施例中,各类型的核苷酸可连接至多于一个相同发光分子(例如两个或更多个相同荧光染料连接至核苷酸)。在一些实施例中,各发光分子可连接至多于一个核苷酸(例如两个或更多个相同核苷酸)。在一些实施例中,多于一个核苷酸可连接(例如经由包含一或多个保护组件的核酸连接子)至多于一个发光分子。在一些实施例中,所有四个核苷酸用在相同光谱范围(例如520-570nm)内吸收及发射的发光分子标记。
在一些实施例中,一组四个核苷酸中的发光标记可选自包含芳族或杂芳族化合物的染料,且可为芘、蒽、萘、吖啶、芪、吲哚、苯并吲哚、噁唑、咔唑、噻唑、苯并噻唑、啡啶、啡噁嗪、卟啉、喹啉、乙锭、苯甲酰胺、花青、羰花青、水杨酸酯、邻胺基苯甲酸酯、香豆素、荧光素、若丹明或其他类似化合物。例示性染料包括二苯并哌喃染料,诸如荧光素;或若丹明染料、萘染料、香豆素染料、吖啶染料、花青染料、苯并噁唑染料、芪染料、芘染料、酞菁染料、藻胆蛋白染料、方酸染料、bodipy染料及其类似物。
在一些实施例中,一组四个核苷酸中的发光标记包含alexa
在某些实施例中,至少一种类型、至少两种类型、至少三种类型或至少四种类型经发光标记的核苷酸包含选自由以下组成的组的发光染料:6-tamra、5/6-羧基若丹明6g、alexa
在一些实施例中,至少一种类型、至少两种类型、至少三种类型或至少四种类型的经发光标记的核苷酸各自包含选自由以下组成的组的发光染料:alexa
在一些实施例中,第一类型的经发光标记的核苷酸包含alexa
在一些实施例中,第一类型的经发光标记的核苷酸包含alexa
在一些实施例中,第一类型的经发光标记的核苷酸包含alexa
在一些实施例中,第一类型的经发光标记的核苷酸包含alexa
在一些实施例中,第一类型的经发光标记的核苷酸包含alexa
在一些实施例中,第一类型的经发光标记的核苷酸包含alexa
在一些实施例中,第一类型的经发光标记的核苷酸包含
在一些实施例中,至少一种类型、至少两种类型、至少三种类型或至少四种类型经发光标记的核苷酸包含选自由以下组成的组的发光染料:alexa
在一些实施例中,第一及第二类型的经发光标记的核苷酸包含选自由以下组成的组的发光染料:alexa
在某些实施例中,至少一种类型、至少两种类型、至少三种类型或至少四种类型经发光标记的核苷酸分子包含选自由以下组成的组的发光蛋白质:tagbfp、mtagbfp2、蓝铜矿(azurite)、ebfp2、mkalama1、天狼星(sirius)、宝石蓝(sapphire)、t-宝石蓝、ecfp、蔚蓝(cerulean)、scfp3a、mturquoise、mturquoise2、单体midoriishi-cyan、tagcfp、mtfp1、egfp、祖母绿(emerald)、superfoldergfp、单体azamigreen、taggfp2、mukg、mwasabi、clover、mneongreen、eyfp、柠檬色(citrine)、金星(venus)、syfp2、tagyfp、单体kusabira-orange、mkok、mko2、morange、morange2、mraspberry、mcherry、mstrawberry、mtangerine、tdtomato、tagrfp、tagrfp-t、mapple、mruby、mruby2、mplum、hcred-tandem、mkate2、mneptune、nirfp、tagrfp657、ifp1.4、irfp、mkeimared、lss-mkate1、lss-mkate2、mberfp、pa-gfp、pamcherry1、patagrfp、kaede(绿色)、kaede(红色)、kikgr1(绿色)、kikgr1(红色)、ps-cfp2、meos2(绿色)、meos2(红色)、psmorange或dronpa。
本申请的方面提供用于将激发能递送至待鉴别分子(例如经发光标记的多磷酸核苷)及在激发之后检测发射光子的方法。在某些实施例中,检测包含记录各检测发光的发光与激发能前一脉冲之间的持续时间。在某些实施例中,检测包含记录多个检测的发光中的每一者的发光与前一激发能脉冲之间的持续时间。在某些实施例中,递送多个激发能脉冲。待鉴别分子的发光标记物(例如一或多个发光标记)可藉由各脉冲或一部分该等脉冲激发。在某些实施例中,多次发光藉由一或多个传感器检测。待鉴别分子的发光标记物可在各激发或一部分激发之后发光。产生发光的激发事件的部分是基于标记物的发光量子产率。在一些实施例中,提高发光标记的数目可提高量子产率(例如提高发光发射的数目)。另外,并非标记物发射的所有发光均将检测到,例如一些发光将远离传感器定向。在某些实施例中,基于发光标记物的发光特性选择激发能,包括吸收光谱及在给定光谱范围内激发之后标记物发射光子所处的波长。
在某些实施例中,基于待检测的经发光标记的分子(例如经发光标记的多磷酸核苷)的发光特性(例如发光寿命)选择脉冲式激发能的频率。在一些实施例中,脉冲之间之间隙长于激发的一或多个经发光标记的分子的发光寿命。在一些实施例中,间隙比激发的一或多个经发光标记的分子的发光寿命长约两倍与约十倍之间,在约十倍与约100倍之间,或在约100倍与约1000倍之间。在一些实施例中,间隙比激发的一或多个经发光标记的分子的发光寿命长约10倍。
在某些实施例中,基于监测的化学方法选择脉冲式激发能(pulsedexcitationenergy)的频率。对于测序反应,当并入经发光标记的核苷酸时递送至目标体积的脉冲的数目将部分地确定检测到的发射光子的数目。在一些实施例中,选择频率以在并入经发光标记的核苷酸期间允许足够数目个待检测光子,其中足够数目为区别经发光标记的核苷酸与多种类型经发光标记的核苷酸所必要的光子的数目。在一些实施例中,基于发射光子的波长,区别经发光标记的核苷酸。在一些实施例中,基于发光发射寿命,例如脉冲激发与发射检测之间的时间,区别经发光标记的核苷酸。在一些实施例中,基于发射光子的波长及发射寿命,区别经发光标记的核苷酸。在一些实施例中,基于发射信号的发光强度(例如基于时间段内发射频率或发射事件总数),区别经发光标记的核苷酸。在一些实施例中,基于发射信号的发光强度及发光寿命,区别经发光标记的核苷酸。在一些实施例中,基于发光强度及波长,区别经发光标记的核苷酸。在一些实施例中,基于发光强度、波长及发光寿命,区别经发光标记的核苷酸。
根据本申请的另一方面,提供一种对靶核酸进行测序的方法。在一些实施例中,对靶核酸进行测序的方法包含以下步骤:(i)提供包含(a)该靶核酸、(b)与该靶核酸互补的引物、(c)核酸聚合酶及(d)用于并入与该靶核酸互补的生长核酸链中的核苷酸的混合物,其中该等核苷酸包括不同类型的经发光标记的核苷酸,其中该等经发光标记的核苷酸在连续并入该生长核酸链中期间产生可检测信号,不同类型的经发光标记的核苷酸的该等可检测信号在时域(timedomain)(例如藉由测定可检测信号的时序(timing)和/或频率)方面可彼此区分;(ii)使(i)的该混合物在足以藉由该引物延伸产生该生长核酸链的条件下进行聚合反应;(iii)在连续并入该生长核酸链中期间自该等经发光标记的核苷酸测量该等可检测信号;及(iv)在连续并入该生长核酸链中后自该等经发光标记的核苷酸测定该等测量到的可检测信号的时序和/或频率,以鉴别该等经发光标记的核苷酸并入该生长核酸链中的时间顺序,进而测定该靶核酸的序列。
在一些实施例中,靶核酸或核酸聚合酶连接至支撑物。在一些实施例中,在使(i)的混合物进行聚合反应之后鉴别并入的时间顺序。在一些实施例中,可检测信号为光学信号。在一些实施例中,光学信号为发光信号。在一些实施例中,测定量测到的可检测信号的时序和/或频率包含(i)在一或多个传感器处接收该等可检测信号;及(ii)将响应于在该一或多个传感器处接受的该等可检测信号产生的多个电荷载子中的电荷载子基于产生该等电荷载子所处的时间选择性地引导至至少一个电荷载子存储区域中。
在一些实施例中,该等量测到的可检测信号的时序和/或频率包含衰变寿命的量测结果。在一些实施例中,量测到的可检测信号的时序和/或频率包含可检测信号在检测可检测信号的一或多个传感器处的到达时间的量测结果。在一些实施例中,该方法进一步包含基于可检测信号到达时间将可检测信号产生的电荷载子分离成与一或多个传感器相关的频段(bin)。在一些实施例中,量测到的可检测信号的时序和/或频率为非光谱量测结果。
【附图说明】
熟习此项技术者将理解,本文所描述的图仅用于说明性目的。应理解,在一些情况下,可放大或增大展示本发明的各种方面以便于本发明的理解。在附图中,在各种图通篇,相同参考标号一般指相同特征、功能上类似和/或结构上类似的元素。图式未必为按比例的,实际上重点在于说明教导内容的原理。图式不意欲以任何方式限制本公开内容的范畴。
本发明的特征及优点将结合附图自下文的详述而变得更显而易见。
当参考图式描述实施例时,可使用方向参考(“上”、“下”、“顶部”、“底部”、“左侧”、“右侧”、“水平”、“垂直”等)。此类参考仅旨在帮助读者在正常方向观看图式。此等方向参考不意欲描述实施装置的较佳或唯一方向。装置可实施于其他定向中。
如自具体实施方式显而易见,在本申请通篇,图(例如图1-9)中描绘及出于说明的目的进一步描述的实例描述了非限制性实施例,且在一些情况下可出于更清楚说明的目的简化某些方法或省略特征或步骤。
图1显示含有用于核酸测序的各种组分的样品槽的非限制性示意图。
图2显示用于四个阶段的核酸测序的非限制性例示性实验;(a)在并入经发光标记的核苷酸前;(b)第一并入事件;(c)第一及第二并入事件之间的时间段;及(d)第二并入事件;以及在阶段(a)-(d)期间原始及经处理数据的对应实例。
图3描绘具有不同发光寿命的四种发光分子的非限制性信号与发射时间图以及针对衰变机率标准化的累积分布函数。
图4展示例示性经发光标记的核苷酸的发光寿命的非限制性图表及发光强度的图表。
图5描绘四个经发光标记的核苷酸的非限制性测序实验:(a)自绿色及红色脉冲检测到的发光的迹线;(b)基于各核苷酸并入的发光寿命及强度,来自绿色脉冲的数据减少;及(c)以实验方式测定的序列与模板序列的比对。
图6描绘四个经发光标记的核苷酸的非限制性测序实验:(a)自绿色脉冲检测到的发光的迹线;(b)基于各核苷酸并入的发光寿命及强度,来自绿色脉冲的数据减少;及(c)以实验方式测定的序列与模板序列的比对。
图7描绘非限制性测序实验,其中经发光标记的核苷酸的发光特性用于鉴别并入测序反应物中的碱基。
图8a及图8b描绘藉由核酸保护分子分离的发光分子及核苷酸的非限制性实例。
图8c描绘包含对接在聚合酶活性位点中的核酸保护分子的非限制性经发光标记的核苷酸。如所示,经由5'-胺-染料连接子将染料分子连接至核酸,且核苷酸包含经由叠氮基-丙醇连接子连接至核酸的六磷酸核苷。
图8d描绘核酸保护分子的非限制性实例。
图8e描绘用包含15碱基对核酸保护分子的经发光标记的六磷酸脱氧胸苷进行的测序反应的非限制性实例。
图8f描绘用各自包含25碱基对核酸保护分子的cy3标记腺苷及alexafluor-546标记胞苷进行的测序反应的非限制性实例。
图8g描绘在20碱基对核酸保护分子上使用内部发光标记或外部发光标记获得的强度迹线的非限制性比较。
图8h描绘具有连接在相同寡核苷酸链的相对端处的发光标记及核苷酸的核酸保护分子的非限制性实例。
图8i描绘具有连接至不同寡核苷酸链的发光标记及核苷酸的核酸保护分子的非限制性实例。
图8j描绘将多个染料连接至核酸保护分子链的非限制性方法。
图8k描绘包含三个茎环及连接在寡核苷酸链主链内的两个cy3.5染料的非限制性单链核酸保护分子。
图8l描绘包含可在染料与多磷酸核苷之间提供距离和/或本体结构(bulkstructure)以保护聚合酶不与染料接触的茎环结构的非限制性双链寡核苷酸保护分子。
图8m描绘形成霍利迪连结体的核酸保护分子的非限制性实例。
图8n描绘包含双链核酸保护分子的经发光标记的多磷酸核苷的非限制性构型。
图8o描绘经由支链胸苷寡核苷酸连接子在核苷酸结构域中具有多于一个核苷酸(nu)的非限制性未标记链的构型。
图8p-8q描绘具有多个能量吸收修饰(修饰的非限制性实例展示连接至寡核苷酸链的5'端)的非限制性寡核苷酸结构。
图9描绘用于核苷酸连接子合成及例示性结构的非限制性反应流程。
【发明详述】
本发明的方面涉及用于将发光标记连接至多磷酸核苷的核酸连接子。此类组合物宜用于涉及多磷酸核苷作为反应物物质的用途的技术中。举例而言,某些dna测序技术可涉及在合成测序反应中使用聚合酶,从而可基于生长链中特定类型的标记核苷酸的并入产生的独特信号,获得序列信息。在一些实施例中,聚合酶活性可决定测序结果的稳固性。因此,通常需要保护聚合酶免受光诱导损伤以便保存恰当的官能性及总活性,例如以便优化读数参数,诸如读取长度及准确度。因此,本文所描述的核酸连接子提供聚合酶保护官能性使光子诱导的损伤消除或最小化,否则则可能由于经发光标记的核苷酸非常接近于聚合酶活性位点而产生。
在一些方面中,本发明提供经发光标记的核苷酸,其包含经由核酸连接子连接至多磷酸核苷的发光标记。在一些实施例中,多磷酸核苷用作合成反应物中的聚合酶底物,且核酸连接子在经发光标记的核苷酸上赋予聚合酶保护特性。在一些实施例中,核酸连接子在发光标记与多磷酸核苷之间提供分离距离以在涉及多磷酸核苷的酶催化反应期间使标记与聚合酶或其他酶之间的相互作用的程度降至最低。然而,本发明人进一步识别和了解可提供保护作用的核酸连接子的额外特征。在一些实施例中,核酸连接子包含位于发光标记与多磷酸核苷之间的一或多个保护组件,以在涉及多磷酸核苷的酶催化反应期间进一步保护聚合酶或其他酶。举例而言,在一些实施例中,核酸连接子包含一或多个结构基序(例如茎-环、霍利迪连结体)、多个杂交寡核苷酸链、在杂交区域内的一或多个交联碱基对(例如在两个或更多个将发光标记连接至多磷酸核苷的寡核苷酸链之间),和/或一或多个能量吸收修饰(例如三重态淬灭剂、支链聚合结构、支链树枝状结构),以提供进一步聚合酶保护作用。在一些实施例中,本文所描述的核酸连接子(及相关标记核苷酸)不连接至材料粒子(例如不连接至金属、磁性、聚合或其他材料的粒子)。在一些实施例中,核酸连接子为线性分子。在一些实施例中,核酸连接子为环状分子。在一些实施例中,核酸连接子为单链的(例如具有或不具有茎-环结构)。在一些实施例中,核酸连接子为双链的(例如具有或不具有茎环结构)。在一些实施例中,双链核酸连接子的两个链为杂交的(归因于互补序列)和非共价连接的。然而,在一些实施例中,一或多个共价键可引入(例如使用一或多个化学连接子)至双链连接子的共价连接的两个链。在一些实施例中,核酸连接子可包括如本文所描述的一或多个额外部分。在一些实施例中,核酸连接子包括i)在糖磷酸酯主链内或末端的一或多个额外部分,ii)一或多个修饰(例如一或多个经修饰的碱或糖)或i)及ii)的组合。然而,在一些实施例中,核酸连接子不包括i)、ii)或i)或ii)中的任一者。
在一些实施例中,核酸连接子包含一或多个结构基序,诸如茎环,其在发光标记与多磷酸核苷之间提供立体阻挡物。茎环或发夹环为当寡核苷酸链与相同链的另一部分折叠并形成碱基对时在寡核苷酸链上形成的核苷酸的未配对环。在一些实施例中,茎-环的未配对环包含三至十个核苷酸。因此,茎-环可藉由具有杂交形成茎的反向互补序列的寡核苷酸链的两个区域形成,其中这两个区域由形成未配对环的三至十个核苷酸间隔开。在一些实施例中,茎可经设计具有一或多个g/c核苷酸,其可藉由相比于a/t核苷酸形成的增加的氢键相互作用而提供增加的稳定性。在一些实施例中,茎包含紧邻未配对环序列的g/c核苷酸。在一些实施例中,茎在靠近未配对环序列的前2、3、4或5个核苷酸内包含g/c核苷酸。在一些实施例中,一或多个发光标记连接至茎-环的未配对环,其中茎区域在一或多个发光标记与多磷酸核苷之间提供刚性及距离。在一些实施例中,一或多个发光标记连接至茎-环的茎。在一些实施例中,核酸连接子的茎-环不包含发光标记。在一些实施例中,核酸连接子的茎-环在茎(例如“凸出部分”)内包含未配对区域。在一些实施例中,一或多个未标记结构基序,诸如茎-环,包括于核酸连接子中(例如一或多个发光标记与一或多个多磷酸核苷之间的核酸连接子上的位置中)。在此类实施例中,一或多个未标记结构基序可提供立体阻挡物和/或提供聚合酶保护作用的吸收阻挡物。
在一些实施例中,核酸连接子包含一或多个能量吸收修饰,诸如淬灭部分,以吸收或另外缓和对聚合酶的光诱导损伤。在一些实施例中,核酸连接子可包含提供聚合酶保护作用的额外特征。举例而言,在一些实施例中,可选择核酸连接子上的发光标记的连接位置以提供聚合酶保护作用。在一些实施例中,发光标记连接在核酸连接子上的内部位点处,以使得标记相对于末端连接标记以更大程度保持临近于核酸连接子。在此类实施例中,发光标记在其与空间中的聚合酶相互作用的可用性方面相对受限。
在一些实施例中,核酸连接子为双链的。在一些实施例中,双链核酸连接子包含连接至发光标记的第一寡核苷酸链和连接至多磷酸核苷的第二寡核苷酸链。在一些实施例中,第二寡核苷酸链进一步包含靠近退火的第一寡核苷酸链的发光标记的一或多个能量吸收修饰。举例而言,在一些实施例中,核酸连接子的一或多个能量吸收修饰相比于多磷酸核苷更接近发光标记。因此,在此类实施例中,一或多个能量吸收修饰充当与发光分子发射的辐射和/或非辐射衰变相交的立体和/或吸收阻挡物。
如本文所使用,“核酸连接子”指将发光标记连接至多磷酸核苷的核酸。在一些实施例中,核酸连接子提供聚合酶保护作用。因此,在一些实施例中,核酸连接子替代地称为“核酸保护分子”或更一般称为“保护分子”。在一些实施例中,视情形而定,术语核酸及寡核苷酸可互换使用。因而,核酸连接子、寡核苷酸连接子、核酸保护分子及寡核苷酸保护分子可指相同或类似概念。
应理解,在核酸连接子(例如寡核苷酸二聚体)的情况下,连接于其上的“核苷酸”或“多磷酸核苷”指经配置以并入生长核酸链中(例如在测序反应期间)的一或多个核苷酸(例如磷酸核苷)。在一些实施例中,所述一或多个核苷酸包含一或多个单磷酸核苷或多磷酸核苷(例如二或三磷酸核苷或具有超过三个5'磷酸的核苷等)。在一些实施例中,所述一或多个磷酸核苷(例如多磷酸核苷)可经由末端磷酸酯连接至形成部分本申请中所描述的保护分子的寡核苷酸(例如未标记寡核苷酸链)。在本申请中描述的组合物或方法中的任一者的一些实施例中,磷酸核苷(例如多磷酸核苷)的磷酸酯部分(例如多磷酸酯部分)包括一或多个磷酸酯或其变体。举例而言,在一些实施例中,磷酸核苷(例如多磷酸核苷)的磷酸酯部分(例如多磷酸酯部分)可包括磷酸酯、硫酯、胺基磷酸酯、烷基膦酸酯键、其他适合的键或大于一种此类修饰或其两者或更多者的组合。在一些实施例中,核酸连接子的标记及未标记链基本上彼此互补(例如在二聚结构域的长度内,其中二聚结构域内的链可具有例如至少60%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少98%、至少99%或100%彼此互补)。
如本文所描述,本发明的方面涉及具有聚合酶保护作用的组合物。应了解,操作人员可藉由多种参数评估聚合酶保护作用。一般而言,可藉由在具有保护组件的组合物与不具有保护性组件的组合物之间进行比较性评定来评估保护组件的作用。举例而言,在一些实施例中,相对于在除不具有一或多个保护组件但另外类似或相同的核酸连接子的外相同条件及相同试剂下进行的测序反应,聚合酶保护组件可将序列读数长度提高例如10%-25%、25-50%、50-75%、75-100%或大于100%,例如约2倍、3倍、4倍、5倍或更多倍。在一些实施例中,保护组件可提高序列准确度(例如相对于在如上文所描述的比较性条件下进行的测序反应,提高约5%、约10%、约15%或更多)。在一些实施例中,聚合酶的保护可藉由降低的程度(例如降低约10%、20%、30%、40%、50%或更多)量测,其为在上文所描述的比较性条件下评估的在链合成期间聚合酶因光诱导损伤而失活的程度。
在一些实施例中,本发明提供基于那些分子的一或多个发光特性来鉴别单分子的新型方法及组合物。在一些实施例中,基于其发光寿命、吸收光谱、发射光谱、发光量子产率、发光强度或其两者或更多者的组合,鉴别分子(例如经发光标记的多磷酸核苷)。鉴别可表示给分子分配准确的分子身份,或可表示将特定分子与一组可能的分子区别或区分开来。在一些实施例中,基于不同发光寿命、吸收光谱、发射光谱、发光量子产率、发光强度或其两者或更多者的组合,多个单分子可彼此区别开来。在一些实施例中,藉由使分子曝露于一系列单独的光脉冲及评估自分子发射的各光子的时序或其他特性,鉴别单分子(例如与其他分子区别开来)。在一些实施例中,汇总自单分子依次发射的多个光子的信息且进行评估以鉴别分子。在一些实施例中,由自分子依次发射的多个光子测定分子的发光寿命,且发光寿命可用于鉴别分子。在一些实施例中,由自分子依次发射的多个光子测定分子的发光强度,且发光强度可用于鉴别分子。在一些实施例中,由自分子依次发射的多个光子测定分子的发光寿命及发光强度,且发光寿命及发光强度可用于鉴别分子。
本申请的方面适用于检测和/或鉴别一或多种生物学或化学分子。在一些实施例中,可藉由在一或多个时间点测定一或多种试剂或产物的存在或不存在来评估化学或生物学反应物。
本申请的方面藉由使分子曝露于光和测定自分子发射的一或多个光子的一或多个特性来查询分子。在某些实施例中,藉由使分子曝露于光脉冲和测定自分子发射的光子的一或多个特性询问分子。在一些实施例中,使分子曝露于多个单独的光脉冲事件且测定在单独的光脉冲事件之后发射的单独的光子的一或多个特性。在一些实施例中,分子不响应于每个光脉冲而发射光子。然而,可藉由使分子曝露于一系列单独的光脉冲和评估在光脉冲事件的子集之后发射的单独的光子(例如在约10%脉冲事件之后发射光子或在约1%脉冲事件之后发射光子)评估多个发射光子。
本申请的方面适用于藉由测定在一或多个时间点一或多个反应的试剂、中间物和/或产物的存在或不存在来监测化学或生物学反应物。在一些实施例中,反应随时间推移的进程可藉由使反应样品曝露于一系列单独的光脉冲以及分析在各光脉冲之后检测到的任何发射光子分析。
因此,在本申请的一些方面中,使反应样品曝露于多个单独的光脉冲且检测和分析一系列发射光子。在一些实施例中,该系列发射光子提供关于在实验时间内在反应样品中存在且不改变的单分子的信息。然而,在一些实施例中,该系列发射光子提供关于在不同时间存在于反应样品中(例如当反应或方法进行时)的一系列不同分子的信息。
在一些实施例中,本申请的方面可用于分析生物样品,例如测定样品中的一或多种核酸或多肽的序列和/或测定样品中一或多种核酸或多肽变体(例如相关基因中的一或多个突变)的存在或不存在。在一些实施例中,可对患者样品(例如人类患者样品)进行测试以提供核酸序列信息或出于诊断、预后和/或治疗目的,测定一或多种相关核酸的存在或不存在。在一些实例中,诊断测试可包括对个体的生物样品中的核酸分子进行测序,例如藉由对个体的生物样品中的无细胞脱氧核糖核酸(dna)分子和/或表达产物(例如核糖核酸(rna))进行测序。
在一些实施例中,使用发光寿命和/或强度分析(例如询问和/或鉴别)的一或多种分子可为标记分子(例如已用一或多个发光标记物标记的分子)。在一些实施例中,生物分子的单独亚单元可使用标记物鉴别。在一些实例中,发光标记物用于鉴别生物分子的单独亚单元。一些实施例使用发光标记物(在本文中亦称为“标记物”),其可为外源性或内源性标记物。外源性标记物可为用作报导子的外部发光标记物和/或用于发光标记的标签。外源性标记物的实例可包括但不限于荧光分子、荧光团、荧光染料、荧光染色剂、有机染料、荧光蛋白质、参与荧光共振能量转移(fret)的物质、酶和/或量子点。其他外源性标记物为本领域已知的。此类外源性标记物可结合到特异性结合特定靶标或组分的探针或官能基(例如分子、离子和/或配体)。将外源性标签或报导子连接至探针可以通过检测外源性标签或报导子的存在来鉴别靶标。探针的实例可包括蛋白质、核酸(例如dna、rna)分子、脂质及抗体探针。外源性标记物和官能基的组合可形成用于检测的任何适合的探针、标签和/或标记,其包括分子探针、标记探针、杂交探针、抗体探针、蛋白质探针(例如生物素结合探针)、酶标记、荧光探针、荧光标签和/或酶报导子。
虽然本发明提及发光标记物,但其他类型的标记物也可与本文所提供的装置、系统及方法一起使用。此类标记物可为质量标签、静电标签、电化学标记或其任意组合。
尽管可将外源性标记物添加至样品中,内源性标记物可已为样品的一部分。内源性标记物可包括存在的任何发光标记物,其可在激发能存在下发光或“自体荧光”。内源性荧光团的自体荧光可在不需要引入外源性荧光团的情况下提供无标记且非侵入性的标记。藉助于实例而非限制,此类内源性荧光团的实例可包括血红蛋白、氧血红素、脂质、胶原蛋白及弹性蛋白交联、还原的烟碱酰胺腺嘌呤二核苷酸(nadh)、经氧化的黄素类(fad及fmn)、脂褐质、角蛋白和/或卟啉。
已认识到需要简单、较不复杂的设备进行单分子检测和/或核酸测序,本发明人构想使用发光标签组(例如发光标记物(luminescentmarker)、发光标记(luminescentlabel))标记不同分子来检测单分子的技术。此类单分子可为具有标签的核苷酸或氨基酸。标签可在键结至单分子时、在自单分子释放后、或在键结至单分子和自单分子释放后检测。在一些实例中,标签为发光标签。所选组中的各发光标签与各自的分子相关。举例而言,一组四个标签可用于“标记”dna中存在的核碱基,组中的每个标签与不同的核碱基关联,例如第一标签与腺嘌呤(a)相连,第二标签与胞嘧啶(c)相连,第三标签与鸟嘌呤(g)相连,且第四标签与胸腺嘧啶(t)相连。此外,该组标签中的发光标签中的每一者具有不同特性,其可用于将该组的第一标签与该组中的其他标签区别开来。以此方式,各标签可通过使用这些区别性特征中的一或多者得到唯一鉴别。藉助于实例而非限制,可用于将一个标签与另一个区别开来的标签的特征可包括标签响应于激发能发射的光的发射能量和/或波长、由特定标签吸收以使标签处于激发态下的激发光的波长和/或标签的发射寿命。
测序
本申请的一些方面适用于对生物学聚合物,诸如核酸及蛋白质进行测序。在一些实施例中,本申请中描述的方法、组合物及装置可用于鉴别并入核酸或蛋白质中的一系列核苷酸或氨基酸单体(例如藉由检测一系列标记核苷酸或氨基酸单体的并入时程)。在一些实施例中,本申请中描述的方法、组合物和装置可用于鉴别并入藉由聚合酶合成的模板依赖性核酸测序反应产物中的一系列核苷酸。
在某些实施例中,藉由天然存在的核酸聚合酶进行模板依赖性核酸测序产物。在一些实施例中,聚合酶为天然存在的聚合酶的突变体或经修饰的变体。在一些实施例中,模板依赖性核酸序列产物将包含与模板核酸链互补的一或多个核苷酸段。在一个方面中,本申请提供一种藉由测定其互补核酸链的序列来测定模板(或靶)核酸链的序列的方法。
如本文所使用,术语“聚合酶”一般指能够催化聚合反应的任何酶(或聚合反应酶)。聚合酶的实例包括(但不限于)核酸聚合酶、转录酶或连接酶。聚合酶可为聚合反应酶。
针对单分子核酸延伸部分(例如用于核酸测序)的实施例可使用能够合成与靶核酸分子互补的核酸的任何聚合酶。在一些实施例中,聚合酶可为dna聚合酶、rna聚合酶、逆转录酶和/或其一或多种突变体或改变形式。
聚合酶的实例包括(但不限于)dna聚合酶、rna聚合酶、热稳定聚合酶、野生型聚合酶、经修饰聚合酶、大肠杆菌dna聚合酶i、t7dna聚合酶、噬菌体t4dna聚合酶
在靶核酸的核碱基与互补dntp之间碱基配对后,聚合酶藉由在新合成的链的3'羟基末端与dntp的α磷酸酯之间形成磷酸二酯键将dntp并入新合成的核酸链中。在共轭至dntp的发光标签为荧光团的实例中,通过激发使其发出存在信号且在并入步骤期间或之后检测发射的脉冲。对于共轭至dntp的末端(γ)磷酸酯的检测标记物,将dntp并入新合成的链中使得β及γ磷酸酯及检测标记释放,其自由扩散于样品槽中,导致自荧光团检测的发射降低。
在一些实施例中,聚合酶为具有较高持续合成能力的聚合酶。然而,在一些实施例中,聚合酶为具有降低的持续合成能力的聚合酶。聚合酶持续合成能力一般指聚合酶将dntp连续并入核酸模板中而不释放核酸模板的能力。在一些实施例中,聚合酶为具有较低5'-3'外切核酸酶活性和/或3'-5'核酸外切酶的聚合酶。在一些实施例中,相对于对应的野生型聚合酶,聚合酶经修饰(例如藉由氨基酸取代)以具有降低的5'-3'外切核酸酶活性和/或3'-5'活性。dna聚合酶的其他非限制性实例包括9°nmtmdna聚合酶(新英格兰生物实验室(newenglandbiolabs))及克列诺外聚合酶的p680g突变体(tuske等人(2000)jbc275(31):23759-23768)。在一些实施例中,具有降低的持续合成能力的聚合酶提供对含有一或多个核苷酸重复序列的段(例如两个或更多个相同类型的依序碱基)的模板进行测序的提高的准确度。在一些实施例中,聚合酶为相比于未经标记的核酸对标记核苷酸具有更高亲和性的聚合酶。
在另一方面中,本申请提供藉由对多个核酸片段进行测序来测序靶核酸的方法,其中靶核酸包含片段。在某些实施例中,该方法包含组合多个片段序列以提供亲代靶核酸的序列或部分序列。在一些实施例中,组合步骤藉由计算机硬件及软件进行。本文所描述的方法可允许对一组相关靶核酸,诸如整个染色体或基因组进行测序。
在测序期间,聚合酶可偶联(例如连接)至靶核酸分子的引发位置。引发位置可以是与靶核酸分子的一部分互补的引物。作为替代方案,引发位置为提供于靶核酸分子的双链段内的间隙或切口。间隙或切口可具有0至至少1、2、3、4、5、6、7、8、9、10、20、30或40个核苷酸长度。切口可在双链序列的一个链中提供断裂,其可为聚合酶提供引发位置,诸如链置换聚合酶。
在一些情况下,测序引物可退火至靶核酸分子,其可固定或可不固定化于固体载体。固体载体可包含例如用于核酸测序的芯片上的样品槽(例如纳米孔口、反应腔室)。在一些实施例中,测序引物可固定化于固体载体且靶核酸分子的杂交亦使靶核酸分子固定化于固体载体。在一些实施例中,聚合酶固定化于固体载体且使可溶性引物和靶核酸与聚合酶接触。然而,在一些实施例中,包含聚合酶、靶核酸和引物的复合物在溶液中形成且使复合物固定化于固体载体(例如经由聚合酶、引物和/或靶核酸的固定化)。在一些实施例中,样品槽(例如纳米孔口、反应腔室)中的组分中无一者固定化于固体载体。举例而言,在一些实施例中,包含聚合酶、靶核酸及引物的复合物在溶液中形成且复合物不固定化于固体载体。
在适当的条件下,与退火的引物/靶核酸接触的聚合酶可将一或多个核苷酸添加或并入引物中,且核苷酸可以5'至3'的模板依赖性方式添加至引物中。此类核苷酸并入引物上(例如经由聚合酶的作用)可一般称作引物延伸反应。各核苷酸可与可检测标签相关联,该标签可在核酸延伸反应期间检测和鉴别出(例如基于其发光寿命和/或其他特性)且用于测定并入延伸的引物并因此并入新合成的核酸分子的序列中的各核苷酸。经由新合成的核酸分子的序列互补性,亦可测定靶核酸分子的序列。在一些情况下,测序引物退火至靶核酸分子以及核苷酸并入至测序引物可在类似反应条件(例如相同或类似反应温度)下或在不同反应条件(例如不同反应温度)下进行。在一些实施例中,藉由合成方法进行测序可包括靶核酸分子群体(例如靶核酸的复本)的存在和/或扩增靶核酸以获得靶核酸的群体的步骤。然而,在一些实施例中,藉由合成进行的测序用于测定正在评估的各反应物中的单分子的序列(且不需要核酸扩增以制备用于测序的靶模板)。在一些实施例中,根据本申请的方面,并行(例如在单个芯片上)进行多个单分子测序反应。举例而言,在一些实施例中,多个单分子测序反应各自在单一芯片上单独的反应腔室(例如纳米孔口、样品槽)中进行。
实施例能够以较高准确度和长的读取长度对单核酸分子进行测序,诸如准确度为至少约50%、60%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%、99.9%、99.99%、99.999%或99.9999%,和/或读取长度大于或等于约10个碱基对(bp)、50bp、100bp、200bp、300bp、400bp、500bp、1000bp、10,000bp、20,000bp、30,000bp、40,000bp、50,000bp或100,000bp。在一些实施例中,单分子测序中使用的靶核酸分子为单链靶核酸(例如脱氧核糖核酸(dna)、dna衍生物、核糖核酸(rna)、rna衍生物)模板,其被添加或固定于含有固定化或连接至固体载体(诸如样品槽的底部或侧壁)的测序反应物的至少一种额外组分(例如聚合酶,诸如dna聚合酶、测序引物)的样品槽(例如纳米孔口)。靶核酸分子或聚合酶可直接或经由连接子连接至样品壁,诸如样品槽的底部或侧壁。样品槽(例如纳米孔口)亦可含有经由引物延伸反应的核酸合成所需的任何其他试剂,诸如适合的缓冲剂、辅助因子、酶(例如聚合酶)以及多磷酸脱氧核苷,诸如例如三磷酸脱氧核苷,包括三磷酸脱氧腺苷(datp)、三磷酸脱氧胞苷(dctp)、三磷酸脱氧鸟苷(dgtp)、三磷酸脱氧尿苷(dutp)及三磷酸脱氧胸苷(dttp)的dntp,其包括诸如荧光团的发光标签。在一些实施例中,各类别dntp(例如含有腺嘌呤的dntp(例如datp)、含有胞嘧啶的dntp(例如dctp)、含有鸟嘌呤的dntp(例如dgtp)、含有尿嘧啶的dntp(例如dutp)及含有胸腺嘧啶的dntp(例如dttp))共轭至不同发光标签以使得自标签发射的光的检测指示出并入新合成的核酸中的dntp的身份。经由任何适合的装置和/或方法,包括用于本文中其他处描述的检测的此类装置及方法,可检测到自发光标签发射的光且归于其适当的发光标签(及因此相关的dntp)。发光标签可在任何位置处共轭至dntp以使得发光标签的存在不抑制dntp并入新合成的核酸链中或聚合酶的活性。在一些实施例中,发光标签共轭至dntp的末端磷酸酯(例如γ磷酸酯)。
在一些实施例中,单链靶核酸模板可与测序引物、dntp、聚合酶及核酸合成所必需的其他试剂接触。在一些实施例中,所有适当的dntp可与单链靶核酸模板同时(例如所有dntp同时存在)接触以使得dntp的并入可持续进行。在其他实施例中,dntp可与单链靶核酸模板依次接触,其中单链靶核酸模板与各适当的dntp单独接触,其中洗涤步骤在单链靶核酸模板与不同dntp接触之间。对于待鉴别的单链靶核酸模板的各连续碱基位置,可重复使单链靶核酸模板与各dntp单独接触继而洗涤的此类循环。
在一些实施例中,测序引物退火至单链靶核酸模板且聚合酶基于单链靶核酸模板连续地将dntp(或其他多磷酸脱氧核苷)并入引物中。与各并入的dntp相关联的独特发光标签可在dntp并入引物期间或之后用适当的激发光激发,且可随后使用任何适合的装置和/或方法(包括本文中其他处描述的用于检测的装置及方法)检测其发射。特定光发射(例如具有特定发射寿命、强度、光谱和/或其组合)的检测可归因于并入的特定dntp。获自检测到的发光标签的采集的序列可随后用于经由序列互补性确定单链靶核酸模板的序列。
尽管本发明提到dntp,本文所提供的装置、系统及方法可与各种类型的核苷酸,诸如核糖核苷酸及脱氧核糖核苷酸(例如具有至少4、5、6、7、8、9或10个磷酸酯基团的多磷酸脱氧核苷)一起使用。此类核糖核苷酸及脱氧核糖核苷酸可包括各种类型的标签(或标记物)及连接子。在一些实施例中,本发明提供可有利地用于同在申请中的美国专利申请第14/543,865号、第14/543,867号、第14/543,888号、第14/821,656号、第14/821,686号、第14/821,688号、第15/161,067号、第15/161,088号、第15/161,125号、第15/255,245号、第15/255,303号、第15/255,624号、第15/261,697号、第15/261,724号、第62/289,019号、第62/296,546号、第62/310,398号、第62/339,790号、第62/343,997号、第62/344,123号及第62/426,144号中所描述的技术中的方法及组合物,其中的每一者的内容以引用的方式并入本文中。
核酸测序的实例
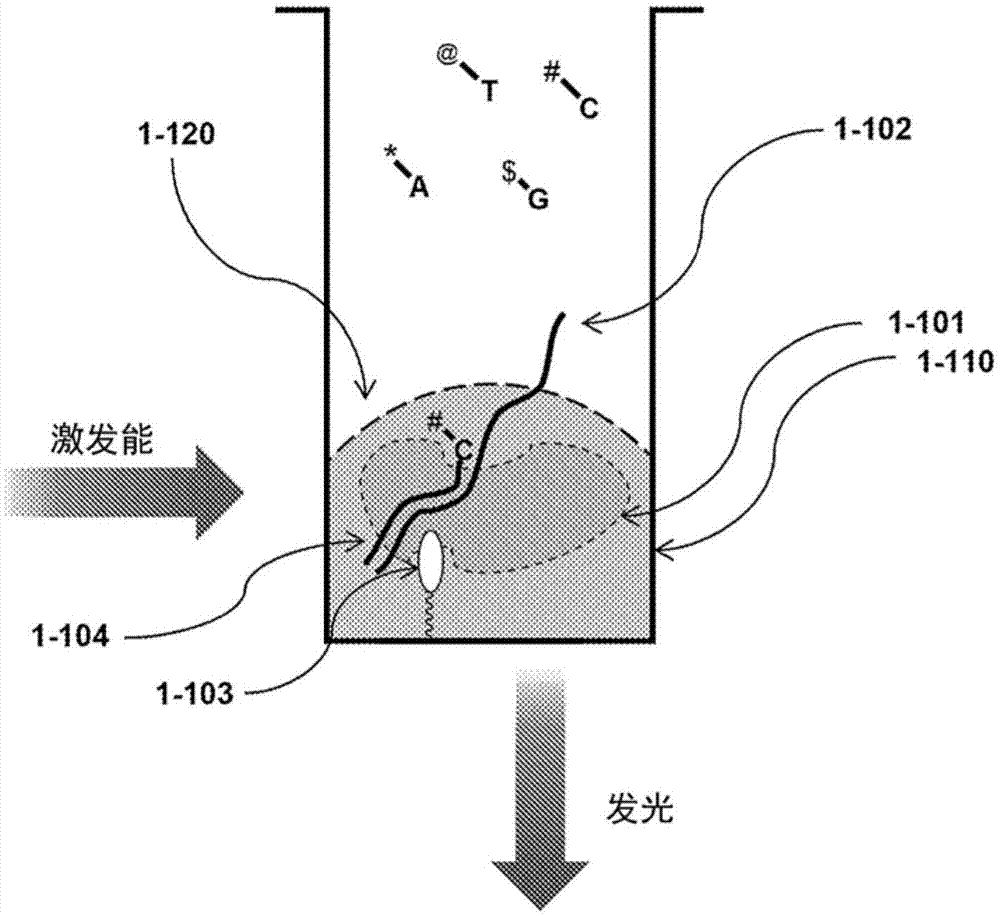
以下实例意在说明本文所描述的一些方法、组合物及装置。实例的所有方面为非限制性的。图1示意性地说明单分子核酸测序方法的设备。1-110为经配置以含有单一复合物的样品槽(例如纳米孔口、反应腔室),该复合物包含核酸聚合酶1-101、待测序靶核酸1-102及引物1-104。在本实例中,样品槽1-110的底部区描述为目标体积(例如激发区域)1-120。
如本文中其他处所描述,目标体积为激发能被引导朝向的体积。在一些实施例中,体积为样品槽体积和激发能偶合至样品槽的特性。目标体积可经配置以限制目标体积中限制的分子或复合物的数目。在一些实施例中,目标体积经配置以限制单分子或复合物。在一些实施例中,目标体积经配置以限制单聚合酶复合物。在图1中,包含聚合酶1-101的复合物受限于目标体积1-120中。复合物可任选地藉由连接至样品槽表面而固定化。用于样品槽表面处理及官能化的例示性方法进一步详细论述于本申请中的其他处。在本实例中,藉由包含适于将连接子连接至聚合酶1-101的一或多个生物分子(例如生物素)的连接子1-103,使复合物固定化。
孔口的体积亦含有具有聚合酶复合所必需的适合的溶剂、缓冲剂及其他添加剂的反应混合物,以合成核酸链。反应混合物亦含有多种类型经发光标记的核苷酸。各类型核苷酸由符号*-a、@-t、$-g、#-c表示,其中a、t、g及c表示核苷酸碱基,且符号*、@、$及#表示经由连接子-连接至各核苷酸的独特发光标记。在图1中,#-c核苷酸目前正在并入互补链1-102中。并入的核苷酸在目标体积1-120内。
图1亦用箭头指示递送至目标体积附近的激发能以及朝向检测器发射的发光的概念。箭头为示意性的,且不意指示激发能递送或发光的特定方向。在一些实施例中,激发能为来自光源的光脉冲。激发能可行进通过一或多个装置组件,诸如在光源与目标体积附近之间的波导或滤光器。发射能亦可行进通过一或多个装置组件,诸如在发光分子与检测器之间的波导或滤光器。一些发光可发射在载体上,其未引导至检测器(例如朝向样品槽的侧壁)且可不被检测到。
图2示意性地说明随时间推移单样品槽(例如纳米孔口)中的测序方法。阶段a至d描绘具有如图1中的聚合酶复合物的样品槽。阶段a描绘在任何核苷酸添加至引物中之前的初始状态。阶段b描绘经发光标记的核苷酸(#-c)的并入事件。阶段c描绘并入事件之间的时间段。在本实例中,核苷酸c已添加至引物中,且先前连接至经发光标记的核苷酸(#-c)的标记及连接子已裂解。阶段d描绘经发光标记的核苷酸(*-a)的第二并入事件。在阶段d之后的互补链由引物、c核苷酸及a核苷酸组成。
阶段a及c均描绘并入事件之前或之间的时间段,其在本实例中显示持续约10毫秒。在阶段a及c中,因为没有正在并入核苷酸,所以在目标体积中不存在经发光标记的核苷酸(图2中未绘出),但可检测出背景发光或来自未并入的经发光标记的核苷酸的伪发光。阶段b及d显示不同核苷酸(分别#-c及*-a)的并入事件。在本实例中,此等事件亦如所示持续约10毫秒。
列标记“原始频段数据(rawbindata)”描绘在各阶段期间产生的数据。在实例实验通篇,将多个光脉冲递送至目标体积附近。对于各脉冲,检测器经配置以记录检测器接受的任何发射光子。当检测器接受发射的光子时,将其分离成多个时间频段(在本实例中存在3个)中的一者。在一些实施例中,检测器经配置有2与16个之间的时间频段。“原始频段数据”记录分别对应于最短、中间及最长频段的数值1(最短条柱)、2(中等条柱)或3(最长条柱)。各条柱表示发射光子的检测。
因为对于阶段a或c,目标体积中不存在经发光标记的核苷酸,所以未检测到光子。对于阶段b及d中的每一者,在并入事件期间检测到多个光子发射事件(如本文所使用的发光事件或“发光”)。发光标记#具有比发光标记*更短的发光寿命。因此阶段b数据描绘为记录有低于频段值更高的阶段d的平均频段值。
列标记“处理数据”描绘已经处理以指示相对于各脉冲的时间发射的光子的数目(计数)的原始数据。因为各条柱对应于特定时间频段的光子计数,所以描绘经处理数据的例示性曲线对应于包含比图中描述的三个时间频段更多的时间频段的原始频段数据。在本实例中,该数据仅经处理以测定发光寿命,但该数据亦可评估其他发光特性,诸如吸收或发射的光子的发光强度或波长。例示性经处理数据接近目标体积中发光标记的发光寿命的指数衰变曲线特征。因为发光标记#具有比发光标记*更短的发光寿命,阶段b的经处理数据在更长持续时间具有更少计数,而阶段d的经处理数据在更长持续时间具有相对更多的计数。
图2的实例实验将鉴别作为ca添加至互补链中的前两个核苷酸。对于dna,紧接在退火至引物的区域之后的靶链的序列将因此鉴别为gt。在本实例中,单独基于发光寿命,核苷酸c及a可与多个c、g、t及a区别开来。在一些实施例中,诸如吸收或发射的光子的发光强度或波长的其他特性可为区别一或多个特定核苷酸所必要的。
在核苷酸并入后发射的信号可储存于内存中且在稍候的时间处理,以测定靶核酸模板的序列。这可包括将信号与参考信号进行比较,以确定随时间变化并入的核苷酸的身份。替代地或另外,可实时采集和处理(例如在核苷酸并入后)在核苷酸并入后发射的信号,以实时测定靶核酸模板的序列。
如本文所使用,术语“核酸”一般指包含一或多个核酸亚单位的分子。核酸可包括一或多个选自腺嘌呤(a)、胞嘧啶(c)、鸟嘌呤(g)、胸腺嘧啶(t)及尿嘧啶(u)或其变体的亚单位。在一些实例中,核酸为脱氧核糖核酸(dna)或核糖核酸(rna)或其衍生物。核酸可为单链或双链的。核酸可为环状的。
如本文所使用,术语“核苷酸”一般指核酸亚单位,其可包括a、c、g、t或u或其变体或类似物。核苷酸可包括可并入生长核酸链中的任何亚单位。此类亚单位可为a、c、g、t或u,或特异于一或多个互补性a、c、g、t或u的任何其他亚单位,或互补于嘌呤(例如a或g或其变体或类似物)或嘧啶(例如c、t或u或其变体或类似物)。亚单位可使得单独的核酸碱基或碱基组(例如aa、ta、at、gc、cg、ct、tc、gt、tg、ac、ca或其尿嘧啶对应物)得到解析。
核苷酸一般包括核苷及至少1、2、3、4、5、6、7、8、9、10或更多个磷酸酯(po3)基团。核苷酸可包括核碱基、五碳糖(核糖或脱氧核糖)及一或多个磷酸酯基团。核糖核苷酸为核苷酸,其中糖为核糖。脱氧核糖核苷酸为核苷酸,其中糖为脱氧核糖。核苷酸可为单磷酸核苷或多磷酸核苷。核苷酸可为多磷酸脱氧核苷,诸如例如三磷酸脱氧核苷,其可选自三磷酸脱氧腺苷(datp)、三磷酸脱氧胞苷(dctp)、三磷酸脱氧鸟苷(dgtp)、三磷酸脱氧尿苷(dutp)及三磷酸脱氧胸苷(dttp)的dntp,其包括诸如发光标签或标记物(例如荧光团)的可检测标签。
多磷酸核苷可具有“n”个磷酸酯基团,其中“n”为大于或等于2、3、4、5、6、7、8、9或10的数目。多磷酸核苷的实例包括二磷酸核苷及三磷酸核苷。核苷酸可为末端磷酸酯标记的核苷,诸如末端磷酸酯标记的多磷酸核苷。此类标记可为发光标记(luminescentlabel)(例如荧光或化学发光)、荧光标记、着色标记(coloredlabel)、显色标记(chromogeniclabel)、质量标签(masslabel)、静电标记(electrostaticlabel)或电化学标记。标记(或标记物)可经由连接子偶联至末端磷酸酯。连接子可包括例如至少一个或多个羟基、硫氢基、胺基或卤烷基,其可适于在天然或经修饰的核苷酸的末端磷酸酯处形成例如磷酸酯、硫酯、胺基磷酸酯或烷基膦酸酯键。连接子可为可裂解的以便自末端磷酸酯分离标记,诸如藉助于聚合反应酶。核苷酸及连接子的实例提供于美国专利第7,041,812号中,其全部以引用的方式并入本文中。
核苷酸(例如多磷酸核苷酸)可包含甲基化核碱基。举例而言,甲基化核苷酸可为包含连接至核碱基(例如直接连接至核碱基的环,连接至核碱基的环的取代基)的一或多个甲基的核苷酸。例示性甲基化核碱基包括1-甲基胸腺嘧啶、1-甲基尿嘧啶、3-甲基尿嘧啶、3-甲基胞嘧啶、5-甲基胞嘧啶、1-甲基腺嘌呤、2-甲基腺嘌呤、7-甲基腺嘌呤、n6-甲基腺嘌呤、n6,n6-二甲基腺嘌呤、1-甲基鸟嘌呤、7-甲基鸟嘌呤、n2-甲基鸟嘌呤及n2,n2-二甲基鸟嘌呤。
如本文所使用,术语“引物”一般指核酸分子(例如寡核苷酸),其可包括包含a、c、g、t和/或u或其变体或类似物的序列。引物可为包含dna、rna、pna或其变体或类似物的合成寡核苷酸。引物可经设计以使得其核苷酸序列与靶链互补,或引物可包含随机苷酸序列。在一些实施例中,引物可包含尾部(例如聚a尾部、索引衔接子、分子条形码等)。在一些实施例中,引物可包含5至15个碱基,10至20个碱基,15至25个碱基,20至30个碱基,25至35个碱基,30至40个碱基,35至45个碱基,40至50个碱基,45至55个碱基,50至60个碱基,55至65个碱基,60至70个碱基,65至75个碱基,70至80个碱基,75至85个碱基,80至90个碱基,85至95个碱基,90至100个碱基,95至105个碱基,100至150个碱基,125至175个碱基,150至200个碱基,或大于200个碱基。
发光特性
如本文所描述,发光分子为吸收一或多个光子且可随后在一或多个持续时间之后发射一或多个光子的分子。藉由若干参数描述分子的发光,该等参数包括(但不限于)发光寿命、吸收光谱、发射光谱、发光量子产率及发光强度。术语吸收及激发在本申请通篇可互换使用。典型的发光分子可吸收多个波长处的光或藉由多个波长处的光进行激发。在某些波长处或在某些光谱范围内的激发可藉由发光发射事件弛豫,而在某些其他波长或光谱范围处的激发可不藉由发光发射事件弛豫。在一些实施例中,发光分子仅适当地在单一波长处或在单一光谱范围内激发发光。在一些实施例中,发光分子适当地在两个或更多个波长处或在两个或更多个光谱范围内激发发光。在一些实施例中,藉由量测激发光子或吸收光谱的波长鉴别分子。
来自发光发射事件的发射光子将在可能的波长的光谱范围内的波长处发射。典型地,相比于激发光子的波长,发射光子具有更长波长(例如具有更小能量或红移)。在某些实施例中,藉由量测发射光子的波长鉴别分子。在某些实施例中,藉由量测多个发射光子的波长鉴别分子。在某些实施例中,藉由量测发射光谱鉴别分子。
发光寿命指激发事件与发射事件之间的持续时间。在一些实施例中,发光寿命表示为指数衰变的等式中的常数。在一些实施例中,其中存在递送激发能的一或多个脉冲事件,持续时间为该脉冲与后续发射事件之间的时间。
分子的“发光寿命测定”可使用任何适合的方法(例如藉由使用适合的技术量测寿命或藉由测定发射的时间依赖性特征)进行。在一些实施例中,测定分子的发光寿命包含相对于一或多个分子(例如测序反应中不同的经发光标记的核苷酸)测定寿命。在一些实施例中,测定分子的发光寿命包含测定相对于参照寿命。在一些实施例中,测定分子的发光寿命包含量测寿命(例如荧光寿命)。在一些实施例中,测定分子的发光寿命包含测定指示寿命的一或多个时间特征。在一些实施例中,分子的发光寿命可基于相对于激发脉冲横跨一或多个时间闸控窗发生的多个发射事件的分布(例如1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、30、40、50、60、70、80、90、100或更多个发射事件)而测定。举例而言,基于相对于激发脉冲量测的光子到达时间的分布,单分子的发光寿命可区别于具有不同发光寿命的多个分子。
应了解,单分子的发光寿命指示在单分子达到激发态之后发射的光子的时序,且单分子因指示光子时序的信息而得到区分。一些实施例可包括藉由量测与分子发射的光子相关的时间,基于分子的发光寿命,从多个分子区别分子。时间分布可提供可自分布测定的发光寿命的指示。在一些实施例中,基于时间分布,诸如藉由将时间分布与对应于已知分子的参考分布进行比较,单分子可区别于多个分子。在一些实施例中,发光寿命的值由时间分布测定。
发光量子产率指在产生发射事件的给定波长处或给定光谱范围内激发事件的分数且典型地低于1。在一些实施例中,本文所描述的分子的发光量子产率在0与约0.001之间,在约0.001与约0.01之间,在约0.01与约0.1之间,在约0.1与约0.5之间,在约0.5与0.9之间,或在约0.9与1之间。在一些实施例中,藉由测定或估算发光量子产率鉴别分子。
如本文针对单分子所使用,发光强度系指每单位时间藉由递送脉冲激发能激发的分子所发射的发射光子的数目。在一些实施例中,发光强度系指每单位时间藉由递送脉冲激发能激发的分子所发射的发射光子的检测数目且藉由特定传感器或传感器组检测。
在不同条件下,给定分子的发光寿命、发光量子产率及发光强度可各自变化。在一些实施例中,单分子将具有与分子集合不同的观测到的发光寿命、发光量子产率或发光强度。在一些实施例中,受限于样品槽(例如纳米孔口)中的分子将具有与未受限于样品槽中的分子不同的观测到的发光寿命、发光量子产率或发光强度。在一些实施例中,连接至另一分子的发光标记或发光分子将具有与未连接至另一分子的发光标记或发光分子不同的发光寿命、发光量子产率或发光强度。在一些实施例中,与大分子复合物(例如蛋白质复合物(例如核酸聚合酶))相互作用的分子将具有与不与大分子复合物相互作用的分子不同的发光寿命、发光量子产率或发光强度。
在某些实施例中,本申请中描述的发光分子在持续时间之后吸收一个光子且发射一个光子。在一些实施例中,可藉由量测持续时间测定或估算分子的发光寿命。在一些实施例中,可藉由量测多个脉冲事件及发射事件的多个持续时间来测定或估算分子的发光寿命。在一些实施例中,可藉由量测持续时间,在多种类型分子的发光寿命中区分分子的发光寿命。在一些实施例中,可藉由量测多个脉冲事件及发射事件的多个持续时间,在多种类型分子的发光寿命中区分分子的发光寿命。在某些实施例中,藉由测定或估算分子的发光寿命,在多种类型分子中鉴别或区分分子。在某些实施例中,藉由在多种类型分子的多个发光寿命中区分分子的发光寿命,在多种类型分子中鉴别或区分分子。
在某些实施例中,发光发射事件为荧光。在某些实施例中,发光发射事件为磷光。如本文所使用,术语发光涵盖包括荧光及磷光两者的所有发光事件。
在一个方面中,本申请提供一种测定单发光分子的发光寿命的方法,其包含:在目标体积中提供发光分子;将多个激发能脉冲递送至目标体积附近;及检测来自发光分子的多个发光。在一些实施例中,所述方法进一步包含评估各对脉冲与发光之间的多个持续时间的分布。在一些实施例中,该方法进一步包含使单发光分子固定化于目标体积中。
在另一方面中,本申请提供一种测定多个分子的发光寿命的方法,其包括:在目标体积中提供多个发光分子;将激发能的多个脉冲递送至目标体积附近;及检测来自发光分子的多个发光。在一些实施例中,所述方法进一步包含评估各对脉冲与发光之间的多个持续时间的分布。在一些实施例中,该方法进一步包含使发光分子固定化于目标体积中。在一些实施例中,所述多个由以下组成:在2与约10个分子之间,在约10与约100个分子之间,或在约100与约1000个分子之间。在一些实施例中,所述多个由以下组成:在约1000与约106个分子之间,在约106与约109个分子之间,在约109与约1012个分子之间,在约1012与约1015个分子之间,或在约1015与约1018个分子之间。在一些实施例中,所述多个的所有分子为相同类型的分子。
图3展示具有不同发光寿命(最长至最短,顶部至底部)的四个发光分子的例示性衰变曲线3-1。幅值可指来自包含多种分子的样品的发光强度,其基于发光寿命在初始激发之后随时间推移以指数方式降低。幅值可替代地指在例如单分子的多个激发能脉冲后的持续时间之后检测到的发射的数目或计数。对于具有不同发光寿命的四个发光分子(最短至最长,顶部至底部),标准化累积分布函数3-2对应于3-1。cdf可表示,基于发光寿命在初始激发之后随时间推移达到零(例如已发光的所有激发分子的累积机率)的发光幅值的标准化机率。cdf可替代地表示,在激发能的单脉冲之后或多个脉冲中的每一者之后,特定持续时间发射发光的单分子的标准化机率。
在一个方面中,本申请提供一种测定单发光分子的发光强度的方法,其包括:在目标体积中提供发光分子;将激发能的多个脉冲递送至目标体积附近;及检测来自发光分子的多个发光。在一些实施例中,该方法进一步包含测定每单位时间多个检测到的发光的数目。在一些实施例中,该方法进一步包含使单发光分子固定化于目标体积中。
在另一方面中,本申请提供一种测定多个分子的发光强度的方法,其包括:在目标体积中提供多个发光分子;将激发能的多个脉冲递送至目标体积附近;及检测来自发光分子的多个发光。在一些实施例中,该方法进一步包含测定每单位时间多个检测到的发光的数目。在一些实施例中,该方法进一步包含使发光分子固定化于目标体积中。在一些实施例中,所述多个由以下组成:在2与约10个分子之间,在约10与约100个分子之间,或在约100与约1000个分子之间。在一些实施例中,所述多个由以下组成:在约1000与约106个分子之间,在约106与约109个分子之间,在约109与约1012个分子之间,在约1012与约1015个分子之间,或在约1015与约1018个分子之间。在一些实施例中,所述多个的所有分子为相同类型的分子。
激发能
在本文所描述的方法的一个方面中,一或多个激发能用于激发待鉴别或区别(例如在测序反应期间)的分子的发光标记。在一些实施例中,激发能在可见光谱中。在一些实施例中,激发能在紫外线光谱中。在一些实施例中,激发能在红外线光谱中。在一些实施例中,一种激发能用于激发经发光标记的分子。在一些实施例中,两种激发能用于激发经发光标记的分子。在一些实施例中,三种或大于三种激发能用于激发经发光标记的分子。在一些实施例中,各经发光标记的分子仅藉由递送的激发能中的一者激发。在一些实施例中,经发光标记的分子藉由递送的激发能中的两者或更多者激发。在某些实施例中,激发能可为单色或受限于光谱范围。在一些实施例中,光谱范围具有约0.1nm与约1nm之间,约1nm与约2nm之间,或约2nm与约5nm之间的范围。在一些实施例中,光谱范围具有约5nm与约10nm之间,约10nm与约50nm之间,或约50nm与约100nm之间的范围。
在某些实施例中,激发能递送为光脉冲。在某些实施例中,激发能递送为多个光脉冲。在某些实施例中,两个或更多个激发能用于激发经发光标记的分子。在一些实施例中,各激发能同时递送(例如在各脉冲中)。在一些实施例中,各激发能在不同时间递送(例如在各能量的单独脉冲中)。不同激发能可以足以允许检测来自靶分子的发光的任何模式递送。在一些实施例中,两个激发能在各脉冲中递送。在一些实施例中,第一激发能及第二激发能在交替脉冲中递送。在一些实施例中,第一激发能在一系列依序脉冲中递送,且第二激发能在后续系列依序脉冲或以此类系列的交替模式递送。
在某些实施例中,基于经发光标记的分子的发光特性,选择光脉冲的频率。在某些实施例中,基于多个经发光标记的核苷酸的发光特性,选择光脉冲的频率。在某些实施例中,基于多个经发光标记的核苷酸的发光寿命,选择光脉冲的频率。在一些实施例中,选择频率以使得脉冲之间之间隙长于一或多个经发光标记的核苷酸的发光寿命。在一些实施例中,基于多个经发光标记的核苷酸的最长发光寿命,选择频率。举例而言,若四个经发光标记的核苷酸的发光寿命为0.25、0.5、1.0及1.5ns,则可选择光脉冲的频率以使得脉冲之间之间隙超过1.5ns。在一些实施例中,间隙比一或多个激发的经发光标记的分子的发光寿命长约两倍与约十倍之间,在约十倍与约100倍之间,或在约100倍与约1000倍之间。在一些实施例中,间隙比一或多个激发的经发光标记的分子的发光寿命长约10倍。在一些实施例中,间隙在约0.01ns与约0.1ns之间,在约1ns与约5ns之间,在约5ns与约15ns之间,在约15ns与约25ns之间,或在约25ns与约50ns之间。在一些实施例中,选择间隙以使得该脉冲激发的分子将以发光方式衰变或激发态将藉由另一机制弛豫的机率为50%、75%、90%、95%或99%。
在某些实施例中,其中存在多个激发能,各激发能的脉冲的频率相同。在某些实施例中,其中存在多个激发能,各激发能的脉冲的频率不同。举例而言,若红色雷射用于激发寿命为0.2及0.5ns的发光分子且绿色雷射用于激发寿命为5ns及7ns的发光分子,则在各红色激光脉冲之后之间隙可比各绿色激光脉冲(例如20ns)之后之间隙短(例如5ns)。
在某些实施例中,基于监测的化学方法选择脉冲式激发能的频率。对于测序反应,可选择频率以使得递送的多个脉冲足以允许检测足够数目的待检测发射光子。在检测到的光子的情况下,足够数目系指自多个经发光标记的核苷酸鉴别或区别经发光标记的核苷酸所必要的多个光子。举例而言,dna聚合酶可平均每20毫秒并入额外核苷酸一次。经发光标记的核苷酸与复合物相互作用的时间可为约10毫秒,且发光标记物裂解时与下一经发光标记的核苷酸开始相互作用之间的时间可为约10毫秒。可随后选择脉冲激发能的频率以历经10毫秒递送足够脉冲,从而使得在并入经发光标记的核苷酸时的10毫秒期间检测足够数目个发射光子。举例而言,在100mhz的频率下,在10毫秒(并入事件的大致长度)内将存在1百万脉冲。若此等脉冲的0.1%产生检测的光子,则将存在1,000个可分析的发光数据点以测定并入的经发光标记的核苷酸的身份。上述值中的任一者为非限制性的。在一些实施例中,并入事件可进行1ms与20ms之间,20ms与100ms之间,或100ms与500ms之间。在一些实施例中,其中在单独定时的脉冲中递送多个激发能,经发光标记的核苷酸可仅藉由该等脉冲的一部分激发。在一些实施例中,选择多个激发能脉冲的频率及模式以使得脉冲的数目足以激发多个经发光标记的核苷酸中的任一者,以允许检测足够数目个发射光子。
在一些实施例中,脉冲频率在约1mhz与约10mhz之间。在一些实施例中,脉冲频率在约10mhz与约100mhz之间。在一些实施例中,脉冲频率在约100mhz与约1ghz之间。在一些实施例中,脉冲频率在约50mhz与约200mhz之间。在一些实施例中,脉冲频率为约100mhz。在一些实施例中,频率为随机的。
在某些实施例中,激发能在约500nm与约700nm之间。在一些实施例中,激发能在约500nm与约600nm之间,或约600nm与约700nm之间。在一些实施例中,激发能在约500nm与约550nm之间,在约550nm与约600nm之间,在约600nm与约650nm之间,或在约650nm与约700nm之间。
在某些实施例中,本文所描述的方法包含递送两个激发能。在一些实施例中,两个激发能间隔约5nm与约20nm之间,约20nm与约40nm之间,约40nm与约60nm之间,约60nm与约80nm之间,约80nm与约100nm之间,约100nm与约150nm之间,约150nm与约200nm之间,约200nm与约400nm之间,或至少约400nm之间。在一些实施例中,两个激发能间隔约20nm与约80nm之间,或约80nm与约160nm之间。
当激发能提及为在特定范围内时,激发能可包含单一波长以使得波长在范围端点之间或范围端点处,或激发能可包含具有最大强度的波长的光谱以使得最大强度在范围端点之间或范围端点处。
在某些实施例中,第一激发能在450nm至500nm范围内,且第二激发能在500nm至550nm,550nm至600nm,600nm至650nm,或650nm至700nm范围内。在某些实施例中,第一激发能在500nm至550nm范围内,且第二激发能在450nm至500nm,550nm至600nm,600nm至650nm,或650nm至700nm范围内。在某些实施例中,第一激发能在550nm至600nm范围内,且第二激发能在450nm至500nm,500nm至550nm,600nm至650nm,或650nm至700nm范围内。在某些实施例中,第一激发能在600nm至650nm范围内,且第二激发能在450nm至500nm,500nm至550nm,550nm至600nm,或650nm至700nm范围内。在某些实施例中,第一激发能在650nm至700nm范围内,且第二激发能在450nm至500nm,500nm至550nm,550nm至600nm,或600nm至650nm范围内。
在某些实施例中,第一激发能在450nm至500nm范围内,且第二激发能在500nm至550nm范围内。在某些实施例中,第一激发能在450nm至500nm范围内,且第二激发能在550nm至600nm范围内。在某些实施例中,第一激发能在450nm至500nm范围内,且第二激发能在600nm至670nm范围内。在某些实施例中,第一激发能在500nm至550nm范围内,且第二激发能在550nm至600nm范围内。在某些实施例中,第一激发能在500nm至550nm范围内,且第二激发能在600nm至670nm范围内。在某些实施例中,第一激发能在550nm至600nm范围内,且第二激发能在600nm至670nm范围内。在某些实施例中,第一激发能在470nm至510nm范围内,且第二激发能在510nm至550nm范围内。在某些实施例中,第一激发能在470nm至510nm范围内,且第二激发能在550nm至580nm范围内。在某些实施例中,第一激发能在470nm至510nm范围内,且第二激发能在580nm至620nm范围内。在某些实施例中,第一激发能在470nm至510nm范围内,且第二激发能在620nm至670nm范围内。在某些实施例中,第一激发能在510nm至550nm范围内,且第二激发能在550nm至580nm范围内。在某些实施例中,第一激发能在510nm至550nm范围内,且第二激发能在580nm至620nm范围内。在某些实施例中,第一激发能在510nm至550nm范围内,且第二激发能在620nm至670nm范围内。在某些实施例中,第一激发能在550nm至580nm范围内,且第二激发能在580nm至620nm范围内。在某些实施例中,第一激发能在550nm至580nm范围内,且第二激发能在620nm至670nm范围内。在某些实施例中,第一激发能在580nm至620nm范围内,且第二激发能在620nm至670nm范围内。
用于将激发能脉冲递送至目标体积的激发能来源及装置的某些实施例描述在本文中其他处。
经发光标记的核苷酸
在一个方面中,本文所描述的方法及组合物包含一或多个经发光标记的核苷酸(例如经由包含一或多种保护组件的核酸连接子连接至一或多个标记物的一或多个多磷酸核苷)。在某些实施例中,一或多个核苷酸包含脱氧核糖核苷。在一些实施例中,所有核苷酸包含脱氧核糖核苷。在某些实施例中,一或多个核苷酸包含核糖核苷。在一些实施例中,所有核苷酸包含核糖核苷。在一些实施例中,一或多个核苷酸包含经修饰的核糖或核糖类似物(例如锁核酸)。在一些实施例中,一或多个核苷酸包含天然存在的碱基(例如胞嘧啶、鸟嘌呤、腺嘌呤、胸腺嘧啶、尿嘧啶)。在一些实施例中,一或多个核苷酸包含胞嘧啶、鸟嘌呤、腺嘌呤、胸腺嘧啶或尿嘧啶的衍生物或类似物。
在某些实施例中,一种方法包含使聚合酶复合物曝露于多个经发光标记的核苷酸的步骤。在某些实施例中,组合物或装置包含反应混合物,其包含多个经发光标记的核苷酸。在一些实施例中,多个核苷酸包含四种类型的核苷酸。在一些实施例中,四种类型核苷酸各自包含胞嘧啶、鸟嘌呤、腺嘌呤及胸腺嘧啶中的一者。在一些实施例中,四种类型核苷酸各自包含胞嘧啶、鸟嘌呤、腺嘌呤及尿嘧啶中的一者。
在某些实施例中,反应混合物中各类型经发光标记的核苷酸的浓度在约50nm与约200nm,约200nm与约500nm,约500nm与约1μm,约1μm与约50μm,或约50μm与250μm之间。在一些实施例中,反应混合物中各类型经发光标记的核苷酸的浓度在约250nm与约2μm之间。在一些实施例中,反应混合物中各类型经发光标记的核苷酸的浓度为约1μm。
在某些实施例中,反应混合物含有用于测序反应的额外试剂。在一些实施例中,反应混合物包含缓冲液。在一些实施例中,缓冲液包含3-(n-吗啉基)丙磺酸(mops)。在一些实施例中,缓冲液以约1mm之间及约100mm之间的浓度存在。在一些实施例中,mops的浓度为约50mm。在一些实施例中,反应混合物包含一或多种盐。在一些实施例中,盐包含乙酸钾。在一些实施例中,乙酸钾的浓度为约140mm。在一些实施例中,盐以约1mm与约200mm之间的浓度存在。在一些实施例中,反应混合物包含镁盐(例如乙酸镁)。在一些实施例中,乙酸镁的浓度为约20mm。在一些实施例中,镁盐以约1mm与约50mm之间的浓度存在。在一些实施例中,反应混合物包含还原剂。在一些实施例中,还原剂为二硫苏糖醇(dtt)。在一些实施例中,还原剂以约1mm与约50mm之间的浓度存在。在一些实施例中,dtt的浓度为约5mm。在一些实施例中,反应混合物包含一或多种光稳定剂。在一些实施例中,反应混合物包含抗氧化剂、氧气清除剂或三重态淬灭剂。在一些实施例中,光稳定剂包含原儿茶酸(pca)。在一些实施例中,光稳定剂包含4-硝基苯甲基醇(nba)。在一些实施例中,光稳定剂以约0.1mm与约20mm之间的浓度存在。在一些实施例中,pca的浓度为约3mm。在一些实施例中,nba的浓度为约3mm。具有光稳定剂(例如pca)的混合物亦可包含酶以再生光稳定剂(例如原儿茶酸二加氧酶(pcd))。在一些实施例中,pcd的浓度为约0.3mm。
本申请涵盖用于区分多个核苷酸中的核苷酸的不同方法。在某些实施例中,经发光标记的核苷酸中的每一者具有不同发光寿命。在某些实施例中,经发光标记的核苷酸中的两者或更多者具有相同发光寿命或大体上相同发光寿命(例如无法藉由方法或装置区别的寿命)。
在某些实施例中,经发光标记的核苷酸中的每一者吸收不同光谱范围内的激发能。在某些实施例中,经发光标记的核苷酸中的两者吸收相同光谱范围内的激发能。在某些实施例中,经发光标记的核苷酸中的三者吸收相同光谱范围内的激发能。在某些实施例中,经发光标记的核苷酸中的四者或更多者吸收相同光谱范围内的激发能。在某些实施例中,经发光标记的核苷酸中的两者吸收不同光谱范围内的激发能。在某些实施例中,经发光标记的核苷酸中的三者吸收不同光谱范围内的激发能。在某些实施例中,经发光标记的核苷酸中的四者或更多者吸收不同光谱范围内的激发能。
在某些实施例中,经发光标记的核苷酸中的每一者发射不同光谱范围内的光子。在某些实施例中,经发光标记的核苷酸中的两者发射相同光谱范围内的光子。在某些实施例中,经发光标记的核苷酸中的三者发射相同光谱范围内的光子。在某些实施例中,经发光标记的核苷酸中的四者或更多者发射相同光谱范围内的光子。在某些实施例中,经发光标记的核苷酸中的两者发射不同光谱范围内的光子。在某些实施例中,经发光标记的核苷酸中的三者发射不同光谱范围内的光子。在某些实施例中,经发光标记的核苷酸中的四者或更多者发射不同光谱范围内的光子。
在某些实施例中,四种经发光标记的核苷酸中的每一者具有不同发光寿命。在某些实施例中,两种或更多种经发光标记的核苷酸具有不同发光寿命且吸收和/或发射第一光谱范围内的光子,且一或多种经发光标记的核苷酸吸收和/或发射第二光谱范围内的光子。在一些实施例中,三种经发光标记的核苷酸中的每一者具有不同发光寿命且发射第一光谱范围内的发光,且第四经发光标记的核苷酸吸收和/或发射第二光谱范围内的光子。在一些实施例中,两种经发光标记的核苷酸中的每一者具有不同发光寿命且发射第一光谱范围内的发光,且第三及第四经发光标记的核苷酸各自具有不同发光寿命且发射第二光谱范围内的发光。
在某些实施例中,四种经发光标记的核苷酸中的每一者具有不同发光强度。在某些实施例中,两种或更多种经发光标记的核苷酸具有不同发光强度且发射第一光谱范围内的发光,且一或多种经发光标记的核苷酸吸收和/或发射第二光谱范围内的光子。在一些实施例中,三种经发光标记的核苷酸中的每一者具有不同发光强度且发射第一光谱范围内的发光,且第四经发光标记的核苷酸吸收和/或发射第二光谱范围内的光子。在一些实施例中,两种经发光标记的核苷酸中的每一者具有不同发光强度且发射第一光谱范围内的发光,且第三及第四经发光标记的核苷酸各自具有不同发光强度且发射第二光谱范围内的发光。
在某些实施例中,四种经发光标记的核苷酸中的每一者具有不同发光寿命或发光强度。在某些实施例中,两种或更多种经发光标记的核苷酸具有不同发光寿命或发光强度且发射第一光谱范围内的发光,且一或多种经发光标记的核苷酸吸收和/或发射第二光谱范围内的光子。在一些实施例中,三种经发光标记的核苷酸中的每一者具有不同发光寿命或发光强度且发射第一光谱范围内的发光,且第四经发光标记的核苷酸吸收和/或发射第二光谱范围内的光子。在一些实施例中,两种经发光标记的核苷酸中的每一者具有不同发光寿命或发光强度且发射第一光谱范围内的发光,且第三及第四经发光标记的核苷酸各自具有不同发光寿命或发光强度且发射第二光谱范围内的发光。
在某些实施例中,两种或更多种经发光标记的核苷酸具有不同发光寿命且吸收第一光谱范围内的激发能,且一或多种经发光标记的核苷酸吸收第二光谱范围内的激发能。在一些实施例中,三种经发光标记的核苷酸中的每一者具有不同发光寿命且吸收第一光谱范围内的激发能,且第四经发光标记的核苷酸吸收第二光谱范围内的激发能。在一些实施例中,两种经发光标记的核苷酸中的每一者具有不同发光寿命且吸收第一光谱范围内的激发能,且第三及第四经发光标记的核苷酸各自具有不同发光寿命且吸收第二光谱范围内的激发能。
在某些实施例中,两种或更多种经发光标记的核苷酸具有不同发光寿命或发光强度且吸收第一光谱范围内的激发能,且一或多种经发光标记的核苷酸吸收第二光谱范围内的激发能。在一些实施例中,三种经发光标记的核苷酸中的每一者具有不同发光寿命或发光强度且吸收第一光谱范围内的激发能,且第四经发光标记的核苷酸吸收第二光谱范围内的激发能。在一些实施例中,两种经发光标记的核苷酸中的每一者具有不同发光寿命或发光强度且吸收第一光谱范围内的激发能,且第三及第四经发光标记的核苷酸各自具有不同发光寿命或发光强度且吸收第二光谱范围内的激发能。
在测序期间,核苷酸鉴别方法可随着序列中的各种碱基对变化。在某些实施例中,两种类型核苷酸可经标记以吸收第一激发能,且基于不同发光强度区别那两种类型的核苷酸(例如a、g),而两种额外类型的核苷酸(例如c、t)可经标记以吸收第二激发能,且那两种额外类型核苷酸基于不同发光寿命而区别。对于此类实施例,在测序期间,可仅基于发光强度测定序列的某些链段(例如仅并入a及g的链段),而可仅基于发光寿命测定所述序列的其他链段(例如仅并入c及t的链段)。在一些实施例中,基于发光寿命区分2与4种之间的经发光标记的核苷酸。在一些实施例中,基于发光强度区分2与4种之间的经发光标记的核苷酸。在一些实施例中,基于发光寿命及发光强度区分2与4种之间的经发光标记的核苷酸。
图4展示例示性经发光标记的核苷酸的发光寿命4-1以及相同例示性核苷酸的发光强度4-2。举例而言,第四列显示了连接至荧光团alexa
发光检测
在本文所描述的方法的一个方面中,藉由一或多个传感器检测一个发射光子(发光)或多个发射光子。对于多种经发光标记的分子或核苷酸,分子中的每一者可发射单一光谱范围内的光子,或一部分分子可发射第一光谱范围内的光子且另一部分分子可发射第二光谱范围内的光子。在某些实施例中,藉由单一传感器检测发射光子。在某些实施例中,藉由多个传感器检测发射光子。在一些实施例中,第一光谱范围内发射的光子藉由第一传感器检测,且第二光谱范围内发射的光子藉由第二传感器检测。在一些实施例中,多个光谱范围中的每一者内发射的光子藉由不同传感器检测。
在某些实施例中,各传感器经配置以基于激发能与发射光子之间的持续时间为发射的光子指定时间频段。在一些实施例中,在较短持续时间之后发射的光子将指定为较早时间频段,且在较长持续时间之后发射的光子将指定为较晚时间频段。
在一些实施例中,将多个激发能脉冲递送至目标体积附近且检测可包括光子发射事件在内的多个光子。在一些实施例中,多种发光(例如光子发射事件)对应于经发光标记的核苷酸并入核酸产物中。在一些实施例中,经发光标记的核苷酸的并入持续约1ms与约5ms之间,约5ms与约20ms之间,约20ms与约100ms之间,或约100ms与约500ms之间。在一些实施例中,在经发光标记的核苷酸的并入期间检测到约10与约100之间,约100与约1000,约1000与约10000,或约10000与约100000之间的发光。
在某些实施例中,若未并入经发光标记的核苷酸,则未检测到发光。在一些实施例中,存在发光背景。在一些实施例中,当未并入经发光标记的核苷酸时,检测到伪发光。在激发能脉冲期间,若一或多个经发光标记的核苷酸在目标体积中(例如扩散至目标体积中,或与聚合酶相互作用,但未并入),则可发生此类伪发光,但未藉由测序反应并入。在一些实施例中,自目标体积中但未并入的经发光标记的核苷酸检测到的多次发光少于来自经发光标记的核苷酸的多次发光(例如十倍、100倍、1000倍、10000倍)。
在一些实施例中,对于对应于经发光标记的核苷酸的并入的各多种检测到的发光,基于脉冲与发射光子之间的持续时间,给发光指定时间频段。针对并入事件的此多个在本文中称为“爆发(burst)”。在一些实施例中,爆发系指高于基线(例如噪声阈值)的一系列信号(例如量测结果),其中该等信号对应于经发光标记的核苷酸在激发区域内时发生的多个发射事件。在一些实施例中,爆发与前一和/或后一爆发间隔了代表基线的信号的时间间隔。在一些实施例中,藉由基于多个持续时间测定发光寿命来分析爆发。在一些实施例中,藉由基于每单位时间检测到的发光的数目测定发光强度来分析爆发。在一些实施例中,藉由测定检测到的发光的光谱范围来分析爆发。在一些实施例中,分析爆发数据将允许给并入的经发光标记的核苷酸分配身份,或允许自多个经发光标记的核苷酸区分一或多个经发光标记的核苷酸。所述分配或区分可依赖于发光寿命、发光强度、发射光子的光谱范围或其任何组合中的任一者。
图5描绘例示性模板核酸的测序。用以下4种经发光标记的核苷酸运行测序实验:连接至alexa
图5展示一种还原原始数据以使用强度-寿命曲线5-2区分相同颜色的爆发(例如t、g与c之间的紫色迹线中的爆发)的方法。各圆圈代表紫色迹线的爆发。已分析各爆发以基于脉冲与各检测到的光子的发射之间的持续时间测定经发光标记的核苷酸的发光寿命。另外,已分析各爆发以基于每秒检测到的光子的数目测定经发光标记的核苷酸的发光强度。并入事件聚集在对应于三种经发光标记的核苷酸中的每一者的三组中。曲线底部中的深色集群(虚线下曲线区域)分配给具有最长发光寿命及最低发光强度的c-d530r2。曲线底部中的浅色集群(虚线下曲线区域)分配给具有中等寿命及强度的g-d554r1。且曲线上部中的浅色集群(虚线上曲线区域)分配给具有最短寿命及最高强度的t-af555。图5展示自数据测定的序列与模板核酸的已知序列之间的比对5-3。垂直条柱指示以实验方式测定的碱基与靶序列之间的匹配。短划线指示经测测序列中未分配核苷酸的模板序列中的位置或与模板序列中的任何位置均不对应的经测定序列中的额外位置。
图6描绘模板核酸测序的第二实例。用以下4种经发光标记的核苷酸运行测序实验:连接至alexa
图6展示一种还原原始数据以使用强度-寿命曲线6-2区分t及c的方法。各圆圈代表强度迹线6-1的爆发。已分析各爆发以基于脉冲与各检测到的光子的发射之间的持续时间测定经发光标记的核苷酸的发光寿命。另外,已分析各峰值以基于每秒检测到的光子的数目测定经发光标记的核苷酸的发光强度。并入事件聚集在对应于两种经发光标记的核苷酸中的每一者的两组中。曲线右部中的深色集群(虚线右侧曲线区域)分配给具有最长发光寿命及最低发光强度的c-af546。曲线右部中的浅色集群(虚线右侧曲线区域)分配给具有最短寿命及最高强度的t-af555。图6展示自数据测定的序列与模板核酸的已知序列之间的比对6-3。垂直条柱指示以实验方式测定的碱基与靶序列之间的匹配。短划线指示经测测序列中未分配核苷酸的模板序列中的位置或与模板序列中的任何位置均不对应的经测定序列中的额外位置。
发光标记
术语发光标签、发光标记及发光标记物通篇可互换使用且涉及包含一或多个发光分子的分子。在某些实施例中,并入的分子为发光分子,例如未连接不同发光标记的发光分子。典型的核苷酸及氨基酸不发光,或在激发及发射能量的适合的范围内不发光。在某些实施例中,并入的分子包含发光标记。在某些实施例中,并入的分子为经发光标记的核苷酸。在某些实施例中,并入的分子为经发光标记的氨基酸或经发光标记的trna。在一些实施例中,经发光标记的核苷酸包含核苷酸及发光标记。在一些实施例中,经发光标记的核苷酸包含核苷酸、发光标记及连接子。在一些实施例中,发光标记为荧光团。
在某些实施例中,发光标记及任选的连接子保持连接至并入的分子。在某些实施例中,发光标记及任选的连接子在并入过程期间或之后自分子裂解。
在某些实施例中,发光标记为花青染料或其类似物。在一些实施例中,花青染料具有下式:
或其盐、立体异构体或互变异构体,其中:
a1及a2接合形成任选的经取代的芳族或非芳族单环或多环杂环;
b1及b2接合形成任选的经取代的芳族或非芳族单环或多环杂环;
r1及r2中的每一者独立地为氢、任选的经取代的烷基;及
l1及l2中的每一者独立地为氢、任选的经取代的烷基,或l1及l2接合形成任选的经取代的芳族或非芳族单环或多环碳环。
在某些实施例中,发光标记为若丹明染料或其类似物。在一些实施例中,若丹明染料具有下式:
或其盐、立体异构体或互变异构体,其中:
a1及a2中的每一者独立地为氢、任选的经取代的烷基、任选的经取代的芳族或非芳族杂环基、任选的经取代的芳族或非芳族碳环基或任选的经取代的羰基,或a1及a2接合形成任选的经取代的芳族或非芳族单环或多环杂环;
b1及b2中的每一者独立地为氢、任选的经取代的烷基、任选的经取代的芳族或非芳族杂环基、任选的经取代的芳族或非芳族碳环基或任选的经取代的羰基,或b1及b2接合形成任选的经取代的芳族或非芳族单环或多环杂环;
r2及r3中的每一者独立地为氢、任选的经取代的烷基、任选的经取代的芳基或任选的经取代的酰基;及
r4为氢、任选的经取代的烷基、任选的经取代的任选的经取代的芳族或非芳族杂环基、任选的经取代的芳族或非芳族碳环基或任选的经取代的羰基。
在一些实施例中,r4为任选的经取代的苯基。在一些实施例中,r4为任选的经取代的苯基,其中至少一个取代基为任选的经取代的羰基。在一些实施例中,r4为任选的经取代的苯基,其中至少一个取代基为任选的经取代的磺酰基。
典型地,发光标记包含芳族或杂芳族化合物且可为芘、蒽、萘、吖啶、芪、吲哚、苯并吲哚、噁唑、咔唑、噻唑、苯并噻唑、啡啶、吩噁嗪、卟啉、喹啉、乙锭、苯甲酰胺、花青、羰花青、水杨酸盐、邻胺基苯甲酸盐、香豆素、荧光素、若丹明或其他类似化合物。例示性染料包括二苯并哌喃染料,诸如荧光素或若丹明染料,包括5-羧基荧光素(fam)、2'7'-二甲氧基-4'5'-二氯-6-羧基荧光素(joe)、四氯荧光素(tet)、6-羧基若丹明(r6g)、n,n,n',n'-四甲基-6-羧基若丹明(tamra)、6-羧基-x-若丹明(rox)。例示性染料亦包括在α或β位置中具有氨基的萘胺染料。举例而言,萘胺基化合物包括1-二甲基氨基萘基-5-磺酸酯、1-苯氨基-8-萘磺酸酯及2-p-甲苯烷基-6-萘磺酸酯、5-(2'-氨基乙基)氨基萘-1-磺酸(edans)。其他例示性染料包括香豆素,诸如3-苯基-7-异氰酸酯基香豆素;吖啶,诸如9-异硫氰基香豆素及吖啶橙;n-(p-(2-苯并噁唑基)苯基)顺丁烯二酰亚胺;花青,诸如吲哚二羰菁3
对于核苷酸测序,经发光标记的核苷酸的某些组合为优选的。在一些实施例中,经发光标记的核苷酸中的至少一者包含花青染料或其类似物。在一些实施例中,至少一种经发光标记的核苷酸包含若丹明染料或其类似物。在一些实施例中,至少两种经发光标记的核苷酸各自包含花青染料或其类似物。在一些实施例中,至少两种经发光标记的核苷酸各自包含若丹明染料或其类似物。在一些实施例中,至少三种经发光标记的核苷酸各自包含花青染料或其类似物。在一些实施例中,至少三种经发光标记的核苷酸各自包含若丹明染料或其类似物。在一些实施例中,至少四种经发光标记的核苷酸各自包含花青染料或其类似物。在一些实施例中,至少四种经发光标记的核苷酸各自包含若丹明染料或其类似物。在一些实施例中,三种经发光标记的核苷酸包含花青染料或其类似物,且第四种经发光标记的核苷酸包含若丹明染料或其类似物。在一些实施例中,两种经发光标记的核苷酸包含花青染料或其类似物,且第三及任选的第四种经发光标记的核苷酸包含若丹明染料或其类似物。在一些实施例中,三种经发光标记的核苷酸包含若丹明染料或其类似物,且第三及任选的第四种经发光标记的核苷酸包含花青染料或其类似物。
在一些实施例中,至少一种经标记的核苷酸连接至两个或更多个染料(例如相同染料的两个或更多个拷贝和/或两个或更多个不同染料)。
在一些实施例中,至少两种经发光标记的核苷酸吸收第一激发能,其中经发光标记的核苷酸中的至少一者包含花青染料或其类似物,且经发光标记的核苷酸中的至少一者包含若丹明染料或其类似物。在一些实施例中,至少两种经发光标记的核苷酸吸收第二激发能,其中经发光标记的核苷酸中的至少一者包含花青染料或其类似物,且经发光标记的核苷酸中的至少一者包含若丹明染料或其类似物。在一些实施例中,至少两种经发光标记的核苷酸吸收第一激发能,其中经发光标记的核苷酸中的至少一者包含花青染料或其类似物,且经发光标记的核苷酸中的至少一者包含若丹明染料或其类似物,且至少两种额外经发光标记的核苷酸吸收第二激发能,其中经发光标记的核苷酸中的至少一者包含花青染料或其类似物,且经发光标记的核苷酸中的至少一者包含若丹明染料或其类似物。
在一些实施例中,至少两种经发光标记的核苷酸吸收第一激发能,其中经发光标记的核苷酸中的至少一者具有小于约1ns的发光寿命,且经发光标记的核苷酸中的至少一者具有超过1ns的发光寿命。在一些实施例中,至少两种经发光标记的核苷酸吸收第二激发能,其中经发光标记的核苷酸中的至少一者具有小于约1ns的发光寿命,且经发光标记的核苷酸中的至少一者具有超过1ns的发光寿命。在一些实施例中,至少两种经发光标记的核苷酸吸收第一激发能,其中经发光标记的核苷酸中的至少一者具有小于约1ns的发光寿命,且经发光标记的核苷酸中的至少一者具有超过1ns的发光寿命,且至少额外两种经发光标记的核苷酸吸收第二激发能,其中经发光标记的核苷酸中的至少一者具有小于约1ns的发光寿命,且经发光标记的核苷酸中的至少一者具有超过1ns的发光寿命。
在某些实施例中,发光标记为选自表1的染料。表1中列出的染料为非限制性的,且本申请的发光标记可包括表1中未列出的染料。在某些实施例中,一或多种经发光标记的核苷酸的发光标记选自表1。在某些实施例中,四种或更多种经发光标记的核苷酸的发光标记选自表1。
表1.例示性荧光团.
染料亦可基于最大吸收或发射发光的波长进行分类。表2提供根据最大吸收的大致波长分成列的例示性荧光团。表2中列出的染料为非限制性的,且本申请的发光标记可包括表2中未列出的染料。准确的最大吸收或发射波长可不对应于所示的光谱范围。在某些实施例中,一或多种经发光标记的核苷酸的发光标记选自表2中列出的“红色”组。在某些实施例中,一或多种经发光标记的核苷酸的发光标记选自表2中列出的“绿色”组。在某些实施例中,一或多种经发光标记的核苷酸的发光标记选自表2中列出的“黄色/橙色”组。在某些实施例中,选择四种核苷酸的发光标记以使得所有选自表2中列出的“红色”、“黄色/橙色”或“绿色”组中的一者。在某些实施例中,选择四种核苷酸的发光标记以使得三种选自表2中列出的“红色”、“黄色/橙色”及“绿色”组之第一组,且第四种选自表2中列出的“红色”、“黄色/橙色”及“绿色”组之第二组。在某些实施例中,选择四种核苷酸的发光标记以使得两种选自表2中列出的第一“红色”、“黄色/橙色”及“绿色”组,且第三及第四种选自表2中列出的“红色”、“黄色/橙色”及“绿色”组之第二组。在某些实施例中,选择四种核苷酸的发光标记以使得两种选自表2中列出的第一“红色”、“黄色/橙色”及“绿色”组,且第三选自表2中列出的“红色”、“黄色/橙色”及“绿色”组的第二组,且第四选自表2中列出的“红色”、“黄色/橙色”及“绿色”组的第三组。
表2.例示性荧光团光谱范围.
在某些实施例中,发光标记可为具有下式的(染料101)、(染料102)、(染料103)、(染料104)、(染料105)或(染料106)(呈nhs酯形式):
或其类似物。在一些实施例中,各磺酸酯或羧酸酯独立地任选的为质子化的。在一些实施例中,上述染料藉由在所示连接点处形成酰胺键而连接至连接子或核苷酸。
在某些实施例中,发光标记可包含第一及第二发色团。在一些实施例中,第一发色团的激发态能够经由能量传递至第二发色团弛豫。在一些实施例中,能量传递为福斯特共振能量转移(
对于一组经发光标记的分子(例如经发光标记的核苷酸),经发光标记的fret对的特性可允许选择多个可区别的分子(例如核苷酸)。在一些实施例中,fret对的第二发色团具有与多个其他经发光标记的分子不同的发光寿命。在一些实施例中,fret对的第二发色团具有与多个其他经发光标记的分子不同的发光强度。在一些实施例中,fret对的第二发色团具有与多个其他经发光标记的分子不同的发光寿命及发光强度。在一些实施例中,fret对的第二发色团发射与多个其他经发光标记的分子不同的光谱范围内的光子。在一些实施例中,fret对的第一发色团具有与多个经发光标记的分子不同的发光寿命。在某些实施例中,fret对可吸收与多个其他经发光标记的分子不同的光谱范围内的激发能。在某些实施例中,fret对可吸收与多个其他经发光标记的分子中的一或多者相同光谱范围内的激发能。
在一些实施例中,两个或更多个核苷酸可连接至发光标记,其中核苷酸连接至发光标记上的不同位置。非限制性实例可包括含有两个与核苷酸类似物上的反应性部分兼容的独立反应性化学部分(例如叠氮基、乙炔基、羧基、氨基)的发光分子。在此类实施例中,发光标记可经由独立键连接至两个核苷酸分子。在一些实施例中,发光标记可包含两个或更多个独立接至两个或更多个核苷酸。
在一些实施例中,两或更多个核苷酸可经由连接子(例如具有两个或更多个反应性位点的分支链连接子(branchedlinker)或连接子,其上可连接核苷酸和/或染料)连接至发光染料。因此,在一些实施例中,两个或更多个核苷酸(例如相同类型)可连接至两个或更多个染料(例如相同类型)。
在一些实施例中,发光标记可包含具有发光特性的蛋白质。在一些实施例中,一或多个核苷酸连接至发光蛋白质。在一些实施例中,一或多个核苷酸经由蛋白质的不同位点的接点连接至发光蛋白质。在某些实施例中,选择四种核苷酸的发光标记以使得一种核苷酸用荧光蛋白质标记,而其余三种核苷酸用荧光染料(例如表1及2中的非限制性实例)标记。在某些实施例中,选择四种核苷酸的发光标记以使得两种核苷酸用荧光蛋白质标记,而其余两种核苷酸用荧光染料(例如表1及2中的非限制性实例)标记。在某些实施例中,选择四种核苷酸的发光标记以使得三种核苷酸用荧光蛋白质标记,而其余核苷酸用荧光染料(例如表1及2中的非限制性实例)标记。在一些实施例中,选择四种核苷酸的发光标记以使得所有四种核苷酸用荧光蛋白质标记。
根据本申请的一些方面,发光标记(例如染料,例如荧光团)可损伤曝露于激发光的测序反应中的聚合酶。在一些方面中,当发光分子保持非常接近于聚合酶时,此损伤在经发光标记的核苷酸并入期间发生。损伤反应的非限制性实例包括在聚合酶与发光分子之间形成共价键以及辐射或非辐射衰变自发光分子发射至酶。这可减少聚合酶的有效性并缩短测序运行长度。
在一些实施例中,藉由相对较长连接子或连接子构造连接核苷酸及发光标记,以在标记核苷酸的并入期间保持发光标记远离聚合酶。术语“连接子构造”在本文中用于指将发光分子连接至核苷酸且不涵盖发光分子或核苷酸的整个结构。
在一些实施例中,单连接子将发光分子连接至核苷酸。在一些实施例中,连接子含有一或多个分叉点以使得两个或更多个(例如2、3、4、5、6、7、8、9、10或更多个)核苷酸连接至各发光分子,两个或更多个(例如2、3、4、5、6、7、8、9、10或更多个)发光分子连接至各核苷酸,或两个或更多个(例如2、3、4、5、6、7、8、9、10或更多个)核苷酸连接至两个或更多个(例如2、3、4、5、6、7、8、9、10或更多个)发光分子。
在一些实施例中,连接子构造决定发光标记与核苷酸之间的距离。在一些实施例中,距离为约1nm或2nm至约20nm。举例而言,超过2nm,超过5nm,5-10nm,超过10nm,10-15nm,超过15nm,15-20nm,超过20nm。然而,发光标记与核苷酸之间的距离不能过长,因为当核苷酸保持在酶的活性位点内时,发光标记需要在待激发照射体积内。因此,在一些实施例中,总体连接子长度小于30nm,小于25nm,约20nm,或小于20nm。
在一些实施例中,保护分子包括在连接子构造内。保护分子可保护聚合酶免受可能在酶与发光标记之间发生的损伤反应。保护分子的非限制性实例包括核酸(例如脱氧核糖核酸、核糖核酸),例如包含一或多个保护组件的核酸。在一些实施例中,保护分子为寡核苷酸(例如dna寡核苷酸、rna寡核苷酸或其变体)。
在一些实施例中,保护分子连接至一或多个发光分子及一或多个核苷酸分子。如本文所使用,核苷酸在此情形下系指可并入生长核酸中的多磷酸核苷,例如在测序反应的情形下。在一些实施例中,发光分子不靠近核苷酸。举例而言,一或多个发光分子可连接在保护分子的第一侧面上且一或多个核苷酸可连接至保护分子的第二侧面,其中保护分子的第一及第二侧面彼此远离。在一些实施例中,它们在保护分子的大约相对侧面上。
保护分子与发光标记连接的位置和保护分子与核苷酸连接的位置之间的距离可为经由空间的线性量测结果或横跨保护分子表面的非线性量测结果。保护分子上发光标记与核苷酸连接点之间的距离可藉由建立保护分子的三维结构模型来量测。在一些实施例中,此距离可为2、4、6、8、10、12、14、16、18、20nm或大于20nm。可选地,保护分子上发光标记及核苷酸的相对位置可藉由将保护分子的结构作为二次曲面(例如椭球、椭圆形圆柱)来描述。在一些实施例中,发光标记及核苷酸相隔的距离为环绕代表保护分子的椭球形形状的距离的至少八分之一。在一些实施例中,发光标记及核苷酸相隔的距离为环绕代表保护分子的椭球形形状的距离的至少四分之一。在一些实施例中,发光标记及核苷酸相隔的距离为环绕代表保护分子的椭球形形状的距离的至少三分之一。在一些实施例中,发光标记及核苷酸相隔的距离为环绕代表保护分子的椭球形形状的距离的一半。
在一些实施例中,在保护分子包含核酸(例如具有一或多个保护组件的核酸连接子)的情况下,可基于发光标记与核苷酸之间产生的核酸内碱基的数目量测核酸上发光标记(例如一或多个发光标记)与核苷酸(例如一或多个多磷酸核苷)连接点之间的距离。在一些实施例中,将标记的连接点与多磷酸核苷的连接点分离的连接子中的核酸亚单位的数目(例如单链连接子中的核苷酸或双链连接子中的碱基对的数目)可为10-100(例如10-25、25-50、50-75、75-100)或更多。举例而言,在一些实施例中,核酸连接子为双链的。在此类实施例中,发光标记及核苷酸的连接点之间的距离可藉由双链核酸内产生的碱基对的数目量测(例如核酸连接子的第一及第二寡核苷酸链的核碱基之间的碱基配对)。在一些实施例中,核酸连接子(例如线性核酸连接子)上发光标记及核苷酸连接点相隔至少5个碱基对,5与10个之间的碱基对,至少10个碱基对,10与15个之间的碱基对,至少15个碱基对,15与20个之间的碱基对,至少20个碱基对,20与25个之间的碱基对,至少25个碱基对,25与30个之间的碱基对,至少30个碱基对,30与35个之间的碱基对,至少35个碱基对,35与40个之间的碱基对,至少40个碱基对,40与45个之间的碱基对,至少45个碱基对,45与50个之间的碱基对,至少50个碱基对,50与75个之间的碱基对,至少75个碱基对,75与100个之间的碱基对,或更多个。在一些实施例中,预期包括一或多个结构基序保护组件(例如茎-环)可使得在发光标记与核苷酸之间产生更大数目的碱基和/或碱基对。因此,在一些实施例中,核酸连接子上发光标记及核苷酸连接点间隔至少50个碱基对,50与60个之间的碱基对,至少60个碱基对,60与70个之间的碱基对,至少70个碱基对,70与80个之间的碱基对,至少80个碱基对,80与90个之间的碱基对,至少90个碱基对,90与100个之间的碱基对,至少100个碱基对,100与150个之间的碱基对,至少150个碱基对,150与200个之间的碱基对,至少200个碱基对,或更多个。在一些实施例中,双链核酸连接子(或单链核酸连接子中的核苷酸)中的碱基对的数目小于500,小于450,小于400,小于350,小于300,或小于250。
保护分子,诸如包含一或多个保护组件的核酸连接子可用于提供立体阻挡以防止发光标记接近聚合酶。保护分子可用于吸收或保护聚合酶免受发光分子发射的辐射及非辐射性衰变。保护分子可用于在发光标记与聚合酶之间提供立体阻挡及衰变阻挡两者。
当核苷酸保持在酶的活性位点内时,保护分子的尺寸应使得发光标记不能或不大可能直接接触聚合酶。当核苷酸保持在酶的活性位点内时,保护分子的尺寸亦应使得连接的发光标记在待激发的照射体积内。应考虑将发光标记连接至保护分子的所选连接子以及将核苷酸连接至保护分子的所选连接子,来选择保护分子的尺寸。用于连接发光标记和核苷酸(例如多磷酸核苷)的保护分子及连接子包含连接子构造,其中连接子构造的尺寸应使得当核苷酸保持在酶的活性位点内时,发光标记不能直接接触聚合酶。
保护分子(和/或包含保护分子的连接子构造)优选为水可溶的。在一些实施例中,优选保护分子(和/或包含保护分子的连接子构造)具有净负电荷。
图7进一步说明测序实验的非限制性实例以及独特发光特性如何可用于区别多个经发光标记的核苷酸7-1。连接至各碱基(胸腺嘧啶、腺嘌呤、胞嘧啶、鸟嘌呤)的发光标记具有允许各标记核苷酸区别于多个标记核苷酸的发光特性(例如发光寿命、发光强度和/或发射波长)。引入多个相同类型的核苷酸用以加快测序反应中的并入速率。
利用经发光标记的核苷酸7-1的测序实验可在例示性反应容器7-2中进行。反应在波导上方的腔室中进行,波导用作激发能管道,藉由自波导的消散波将激发能递送至反应腔室底部中的样品。孔口阻挡自波导的光辐射至本体样品以及环境光和/或传感器的杂散光,并为反应腔室提供制造路径。反应腔室为将样品置放在底部以及波导的消散波的高激发区域内的蚀刻结构。选择性表面化学用于提供具有不同组成的反应腔室的底部及侧壁,以使得样品可选择性地定位于反应腔室底部。
在一些实施例中,可使用选择性表面官能化和/或表面钝化的不同技术获得选择性表面化学,例如如例示性反应容器7-2中一般所描绘。举例而言,反应容器7-2可包含金属叠层(metalstack),其中侧壁表面处金属的曝露部分包含金属氧化物。在一些实施例中,金属氧化物表面可钝化以使得其为惰性的或针对官能化试剂和/或样品为反应性最低。如所示,在一些实施例中,“氧化物”层可指由其曝露表面上的二氧化硅构成的透明层。在一些实施例中,氧化物或二氧化硅表面可选择性地官能化以将样品限制在反应容器7-2的底部表面处或附近。
在每例示性工作流程7-3的测序反应期间,特定核苷酸的并入可区别于四种经发光标记的核苷酸。在实验整个过程,存在两个不同时间段:脉冲时间段及检测时间段。在脉冲时间段期间,持续20皮秒,未采集到发射光。在脉冲时间段之后为检测时间段,持续10奈秒,其中四个时间频段捕获历经检测时间段(i)发生的发射事件。脉冲及检测时间段包含一个循环。发射事件历经1百万循环(ii)的时程被持续分段和累积。横跨时间频段的发射事件的总体分布代表发光寿命,且可用于使特定数据组匹配已知寿命分布(iii)。在一些实施例中,发射事件(例如发光寿命)的分布不使一个经发光标记的碱基区别于多个其他标记分子。除了发射事件的分布外,发射事件(例如发光强度)的数量可用于自多个其他分子鉴别单分子。
图8a为由非蛋白质(例如核酸)保护分子(101)间隔开的发光分子及核苷酸的非限制性实例。非蛋白质保护分子的非限制性实例可包括核酸分子,例如脱氧核糖核酸、核糖核酸及其组合。在一些实施例中,核酸保护分子包含一或多个保护组件(例如位于一或多个核苷酸的连接位点与一或多个标记物之间)。如所示,发光分子及核苷酸直接连接至非蛋白质保护分子(例如共价连接)。在一些实施例中,发光分子及核苷酸直接连接至非蛋白质保护分子的连续部分。举例而言,在一些实施例中,非蛋白质保护分子为核酸分子,且发光分子和/或核苷酸直接结合至核酸分子的核苷酸。在一些实施例中,发光分子和/或核苷酸经之连接至非蛋白质保护分子的连接子不是非蛋白质保护分子的连续部分。举例而言,在一些实施例中,非蛋白质保护分子为核酸分子,且发光分子和/或核苷酸经由连接子连接至核酸。
在一些实施例中,发光分子及核苷酸可经由反应性部分连接至非蛋白质(例如核酸)保护分子,如图8b中所描绘。在本实例中,发光分子上的反应性部分(550)经由非蛋白质保护分子上的对应的反应性部分(500)共价连接至非蛋白质保护分子。核苷酸上的反应性部分(551)经由非蛋白质保护分子上的对应的反应性部分(501)共价连接至非蛋白质保护分子(101)。在一些实施例中,反应性部分500和/或反应性部分501直接连接至非蛋白质保护分子的连续部分。在一些实施例中,反应性部分500和/或反应性部分501经之连接至非蛋白质保护分子的连接子不是非蛋白质保护分子的连续部分。
在一些实施例中,一或多个发光标记和/或一或多个多磷酸核苷可使用本领域已知的化学偶联技术连接至核酸连接子(例如非蛋白质保护分子)。举例而言,在一些实施例中,点击化学技术(例如铜催化、应变促进、无铜点击化学方法等)可用于将一或多个发光标记及一或多个多磷酸核苷连接至核酸。因此,在一些实施例中,图8b中描绘的反应性部分配对501/551及500/550可包括反应性胺、叠氮化合物、炔烃、硝酮、烯烃(例如环烯烃)、四嗪、四唑及适于点击反应及类似偶联技术的其他反应性部分。
在一些实施例中,非蛋白质保护分子为寡核苷酸(例如dna寡核苷酸、rna寡核苷酸或其变体)。在一些实施例中,寡核苷酸为单链的。在一些实施例中,发光标记直接地或间接地连接至单链寡核苷酸的一端(例如5'端或3'端),且一或多个核苷酸直接地或间接地连接至单链寡核苷酸的另一端(例如3'端或5'端)。举例而言,单链寡核苷酸可包含连接至寡核苷酸5'端的发光标记及连接至寡核苷酸3'端的一或多个核苷酸(例如相同类型)。可选地,在一些实施例中,单链寡核苷酸可包含连接至寡核苷酸3'端的发光标记及连接至寡核苷酸5'端的一或多个核苷酸(例如相同类型)。
在一些实施例中,寡核苷酸为双链的(例如寡核苷酸包含两条退火互补的寡核苷酸链)。在一些实施例中,发光标记直接地或间接地连接至双链寡核苷酸的一端,且一或多个核苷酸直接地或间接地连接至双链核苷酸的另一端。在一些实施例中,发光标记直接地或间接地连接至双链寡核苷酸的一个链,且一或多个核苷酸(例如相同类型)直接地或间接地连接至双链核苷酸的另一链。举例而言,双链寡核苷酸可包含连接至寡核苷酸的一个链的5'端的发光标记及连接至另一链的5'端的一或多个核苷酸(例如相同类型)。可选地,在一些实施例中,双链寡核苷酸可包含连接至寡核苷酸的一个链的3'端的发光标记及连接至另一链的3'端的一或多个核苷酸(例如相同类型)。
在一些实施例中,一或多个发光标记和/或一或多个核苷酸(例如相同类型)可连接在单链或双链寡核苷酸上的一或多个不同位置处,包括在寡核苷酸的一或多个末端和/或内部位置处。
例示性实施例描绘在图8c中,其中经发光标记的核苷酸包含寡核苷酸保护分子。如所示,当核苷酸结合至聚合酶时,寡核苷酸在发光标记(例如一或多个染料)与聚合酶之间提供距离。因此,在一些实施例中,寡核苷酸可用于充当立体阻挡,以防止或限制发光标记与聚合酶之间的相互作用的程度。另外,寡核苷酸可吸收发光分子发射的辐射性和/或非辐射性衰变。此类功能可有利地保护聚合酶免受降解或功能缺失。
图8c中所示的非限制性实例描绘包含连接至一个链的一端(例如5'端)的发光标记及连接至同一链的另一端(例如3'端)的核苷酸的双链寡核苷酸保护分子。在一些实施例中,双链寡核苷酸包含连接至第一链的发光标记及连接至第二链的一或多个核苷酸,如图8d中所描绘。如所示,核酸815(例如双链寡核苷酸)包含15个碱基对。核酸815包含经由连接子815-2连接至核酸的第一寡核苷酸链的发光标记815-1以及经由连接子815-4连接至核酸的第二寡核苷酸链的核苷酸815-3(例如描绘为六磷酸核苷的多磷酸核苷)。将核苷酸815-3连接至核酸815的连接子815-4的化学结构展示于图9-2中,但可根据本文中其他处描述的连接子分子设计任何适合的连接子。
图8d进一步描绘核酸820及822,各自包含具有20个碱基对的双链寡核苷酸。如所示,核酸820包含外部发光标记820-1。在一些实施例中,“外部”发光标记系指连接至寡核苷酸链的末端(例如5'或3'端)的发光标记。在一些实施例中,外部发光标记连接在寡核苷酸链上最5'或最3'的碱基处。然而,在一些实施例中,寡核苷酸链可包含额外碱基作为悬端区域,在此额外碱基不与核酸的相对链碱基配对。在此类实施例中,可认为外部发光标记在与相对链形成最5'-或最3'的碱基配对的寡核苷酸链上的碱基处连接。核酸822包含内部发光标记822-1。在一些实施例中,“内部”发光标记系指发光标记连接在寡核苷酸链内的位置处,沿着寡核苷酸链在任一侧上具有一或多个碱基配对的核苷酸。因此,若沿着所述链的连接位点上游的至少一个核苷酸及下游的至少一个核苷酸与相对链碱基配对,则发光标记可称为内部发光标记。在一些实施例中,内部发光标记经由无碱基位点或核碱基连接至寡核苷酸链。在一些实施例中,内部发光标记整合于寡核苷酸主链内。
应了解,寡核苷酸保护分子可具有任何长度,如图8d中的例示性构建体的不同长度所示(例如15个碱基对的核酸815、20个碱基对的核酸820、30个碱基对的核酸830及45个碱基对的核酸845)。举例而言,由15个碱基对及25个碱基对组成的例示性寡核苷酸分别展示于图8e及图8f中,随附测序实验的例示性结果。在一些实施例中,寡核苷酸可具有约10或大于10,约20或大于20,约30或大于30,约40或大于40,约50或大于50,约60或大于60,约70或大于70,约80或大于80,约90或大于90,约100或大于100,约125或大于125,约150或大于150,约175或大于175,约200或大于200,约250或大于250,约300或大于300,约350或大于350,约400或大于400,约450或大于450,约500或大于500的长度。在一些实施例中,寡核苷酸具有小于20,小于30,小于40,小于50,小于60,小于70,小于80,小于90,小于100,小于125,小于150,小于175,小于200,小于250,小于300,小于350,小于400,小于450,小于500,或小于600个碱基的长度。在一些实施例中,寡核苷酸连接子足够长以保护聚合酶免于连接至寡核苷酸连接子的标记的发射,亦足够短以允许在测序反应期间激发且检测标记。
应了解,发光标记和/或一或多个核苷酸可连接在寡核苷酸中的任何位置处。在一些实施例中,发光标记和/或一或多个核苷酸连接在5'或3'端处或大约在5'或3'端处。在一些实施例中,发光标记连接在寡核苷酸的内部位置处以使得发光标记非常接近于寡核苷酸的较大部分。举例而言,图8g描绘包含内部染料的例示性寡核苷酸以及包含外部染料的例示性寡核苷酸以及在测序实验中利用任一者的例示性结果。在一些实施例中,内部发光标记(例如内部染料)一般系指当相比于外部发光标记(例如外部染料)时紧密接近的寡核苷酸的较大部分包围的发光标记。在一些实施例中,包围发光标记的寡核苷酸的较大部分提供用于吸收发光标记发射的辐射性和/或非辐射性衰变的更大阻挡。
可使用本领域已知的任何方法产生包含寡核苷酸保护分子的经发光标记的核苷酸。举例而言,图8h描绘一种非限制性途径,其中发光标记及核苷酸连接在寡核苷酸的同一链的相对端处。在此实施例中,发光标记及核苷酸使用反应性基团化学方法连接至第一链,且第二互补链随后退火至第一链。如上文所指示,在一些实施例中,发光标记及一或多个核苷酸可连接至寡核苷酸保护分子的不同链(例如在3'和/或5'端处)。图8i描绘例示性方法,其中包含发光标记的第一链退火至包含核苷酸的第二互补链。
如本文所描述,保护分子可包含发光标记(例如具有一或多个染料的标记)。在一些实施例中,保护分子可包含一或多个用于吸收发光标记发射的辐射性和/或非辐射性衰变的部分(例如能量吸收部分)。举例而言,图8j描绘将多个染料连接至例示性寡核苷酸保护分子的链的非限制性方法,其中反应性基团化学方法用于将两个染料共价连接至寡核苷酸上的连接子。如所示,连接子包含三重态淬灭剂,其可吸收由激发成高反应状态的发光标记产生的任何潜在有害作用。在图8j中所示的实例中,展示能量吸收部分共价连接至同一链作为发光标记(例如染料分子)。在一些实施例中,能量吸收部分可靠近发光标记,但连接至互补链,该互补链退火至具有如下文所描述的发光标记的链。
除了提供聚合酶保护作用的化学部分外,本文涵盖了寡核苷酸结构基序。在一些实施例中,一或多个未标记结构基序(例如能够形成稳定茎-环或其他结构的寡核苷酸序列)位于发光标记与多磷酸核苷之间的核酸连接子上(例如未标记茎结构存在于标记的位置与多磷酸核苷的位置之间)。举例而言,图8k描绘包含三个茎环结构的寡核苷酸保护分子。在一些实施例中,寡核苷酸保护分子可包含一或多个茎环结构(例如2、3、4、5、6、7、8、9或大于9个)且可为单链的。在一些实施例中,寡核苷酸保护分子可包含一或多个茎环结构(例如2、3、4、5、6、7、8、9或大于9个)且可为双链的。举例而言,图8l描绘包含茎环结构的例示性双链寡核苷酸保护分子。在一些实施例中,茎环提供的发光标记与一或多个核苷酸之间的区域中的增加的结构提供较大区域,其中寡核苷酸可空间上阻碍发光标记与聚合酶之间的相互作用。
在一些实施例中,寡核苷酸保护分子包含一个茎环(例如发夹结构)。在一些实施例中,寡核苷酸保护分子包含两个茎环。在一些实施例中,寡核苷酸保护分子包含三个茎环。在一些实施例中,寡核苷酸保护分子包含四个茎环。在一些实施例中,寡核苷酸保护分子包含5、6、7、8、9或10或更多个茎环。
本文所描述的寡核苷酸保护分子涵盖额外的核酸结构基序。在一些实施例中,寡核苷酸保护分子包含三个或更多个核酸链(例如3、4、5、6、7或8或更多个核酸链)。在一些实施例中,寡核苷酸保护分子包含四个核酸链。举例而言,寡核苷酸保护分子可包含霍利迪连结体,如图8m中所描绘。在一些实施例中,一或多个结构基序(例如茎环、霍利迪连结体)可提高寡核苷酸保护分子的刚性以使发光标记与聚合酶之间的平均距离最大化。在一些实施例中,相关平均距离系指当连接至标记的多磷酸核苷在聚合酶活性位点(例如在并入生长链中期间)中时发光标记与聚合酶之间的距离。
在一些实施例中,额外的结构基序(例如基于寡核苷酸保护分子的序列赋予的物理特性和/或基于寡核苷酸保护分子的一或多个部分的一或多个化学修饰)可包括于单链或双链寡核苷酸保护分子中,例如以提高刚性或提供特定的3维构造。在一些实施例中,一或多个退火区域(例如两个寡核苷酸的茎结构或杂交互补区域)可经稳定化(例如藉由共价修饰)。
在一些实施例中,寡核苷酸保护分子上的一或多个位置可经修饰以包括一或多个能量吸收部分。在一些实施例中,一或多个能量吸收部分可添加至连接标记的同一核酸链中(参见作为非限制性实例的图8j)。在一些实施例中,一或多个能量吸收部分可添加至与在双链寡核苷酸保护分子(例如一或多个能量吸收部分可包括在连接至一或多个核苷酸的互补链上)的情况下的标记链不同的链中,例如如下文更详细地描述。
因此,在一些实施例中,经发光标记的核苷酸可以图8n中描绘的通用形式8-100提供。如所示,发光标记结构域(星形形状的点线)经由二聚结构域非共价连接至核苷酸结构域(圆圈形状的点线)。在一些实施例中,二聚结构域系指在发光标记结构域与核苷酸结构域之间提供非共价连接的区域。举例而言,在一些实施例中,通用结构8-100为互补寡核苷酸二聚体,其包含:包含发光标记结构域的标记寡核苷酸链8-110以及包含核苷酸结构域的未标记寡核苷酸链8-120。应理解,在寡核苷酸保护分子(例如寡核苷酸二聚体)的情况下,核苷酸结构域系指经配置以并入生长核酸链(例如在测序反应期间)中的一或多个核苷酸(例如磷酸核苷)。在一些实施例中,所述一或多个核苷酸包含一或多个单磷酸核苷或多磷酸核苷(例如二或三磷酸核苷或具有超过三种5'磷酸酯的核苷等)。在一些实施例中,所述一或多个磷酸核苷(例如多磷酸核苷)可经由末端磷酸酯连接至寡核苷酸(例如未标记寡核苷酸链),其形成如本申请中所描述的保护分子的一部分。在本申请中描述的组合物或方法中的任一者的一些实施例,磷酸核苷(例如多磷酸核苷)的磷酸酯部分(例如多磷酸酯部分)包括一或多个磷酸酯或其变体。举例而言,在一些实施例中,磷酸核苷(例如多磷酸核苷)的磷酸酯部分(例如多磷酸酯部分)可包括磷酸酯、硫酯、氨基磷酸酯、烷基膦酸酯键、其他适合的键或大于一种此类修饰或其两者或更多者的组合。在一些实施例中,标记及未标记链实质上彼此互补(例如在二聚结构域的长度内,其中二聚结构域内的链可彼此互补例如至少60%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少98%、至少99%或100%)。在此类实施例中,标记及未标记链可经退火以形成双链结构,其中退火部分构成二聚结构域,且两个链的退火产生经发光标记的核苷酸8-100。在一些实施例中,二聚结构域含有5至100个碱基对,例如10至50个碱基对,15至45个碱基对,或其他范围内的碱基对,例如基于以下非限制性尺寸中的任一者的组合。在一些实施例中,二聚结构域含有至少5、至少10、至少15、至少20、至少25、至少30、至少35、至少45、至少50、至少55、至少60、至少65、至少70、至少75、至少100、至少250个碱基对。在一些实施例中,二聚结构域含有不超过500、不超过300、不超过200、不超过150、不超过100、不超过75、不超过70、不超过65、不超过60、不超过55、不超过50、不超过45、不超过40、不超过35、不超过30、不超过25、不超过20、不超过15、不超过10个碱基对。在一些实施例中,二聚结构域含有15个碱基对。在一些实施例中,二聚结构域含有30个碱基对。在一些实施例中,二聚结构域含有45个碱基对。
在一些实施例中,发光标记结构域及核苷酸结构域可有利地藉由二聚结构域间隔开。举例而言,在一些实施例中,在通用形式8-100系指双链寡核苷酸结构的情况下,发光标记结构域及核苷酸结构域描绘在退火的寡核苷酸二聚体的相反末端处。因此,在一些实施例中,发光标记结构域及核苷酸结构域各自分别连接在标记及未标记链的3'端处或附近(例如连接在寡核苷酸序列中最3'核苷酸处,连接在位于寡核苷酸序列中最3'的1%、2%、5%、10%、15%、20%、25%、30%、35%、40%或45%的核苷酸内的核苷酸处)。在一些实施例中,发光标记结构域及核苷酸结构域各自连接在标记及未标记链的5'端处或附近(例如连接在寡核苷酸序列的最5'核苷酸处,连接最5'的1%、2%、5%、10%、15%、20%、25%、30%、35%、40%或45%的核苷酸内的核苷酸处)。
如图8n中所示,标记链8-110包含发光标记结构域(星形形状点线)。在一些实施例中,发光标记结构域系指具有一或多个发光分子的标记链的区域。举例而言,在一些实施例中,标记链8-111的发光标记结构域由一个发光分子(星形形状实线)组成。在一些实施例中,标记链8-112的发光标记结构域由两个发光分子组成。如结构8-112中所描绘,具有多于一个发光分子的发光标记结构域可类似分支链结构。应了解,医师可基于所需特性(例如发光特性,诸如寿命、强度、量子产率等)确定待包括在单标记链上的发光分子的数目。连接至发光标记结构域的发光分子的数目的非限制性实例包括2-10(例如2、3、4、5、6、7、8、9、10)、10-15、15-20或其他适合的数目。发光分子可以线性、分支链、线性及分支链的组合或其他构造连接。因此,通用标记链8-113展示有具有第一发光分子以及两个额外分支的发光标记部分(点线)的发光标记结构域,各发光标记部分具有一或多个发光分子。
在一些实施例中,未标记链的核苷酸结构域可以类似方式设计。举例而言,如图8n中所示,在一些实施例中,未标记链8-120包含核苷酸结构域(圆圈形状点线)。在一些实施例中,核苷酸结构域系指具有一或多个核苷酸(例如一或多个多磷酸核苷)的未标记链的区域。在一些实施例中,未标记链8-121的核苷酸结构域由一个核苷酸(圆圈形状实线)组成。在一些实施例中,未标记链8-122的核苷酸结构域由两个核苷酸组成。如结构8-122中所描绘,具有多于一个核苷酸的核苷酸结构域可类似分支链结构。应了解,医师可基于所需特性(例如核酸测序反应中的特性,诸如反应动力学、读段长度、与聚合酶的接近度等)确定待包括于单未标记链上的核苷酸结构域中的核苷酸的数目。连接至核苷酸结构域的核苷酸的数目的非限制性实例包括2-10(例如2、3、4、5、6、7、8、9、10)、10-15、15-20或其他适合的数目。核苷酸可以线性、分支链、线性及分支链的组合或其他构造连接。因此,通用未标记链8-123展示有具有第一核苷酸及两个额外分支链核苷酸部分(点线)的核苷酸结构域,各核苷酸部分具有一或多个核苷酸。分支链核苷酸的非限制性实例展示于图8o中,其描绘经由分支的胸苷寡核苷酸连接子在核苷酸结构域中具有多于一个核苷酸(nu)的各种未标记链的构造。尽管藉助于实例在连接子中描绘胸苷,但在一些实施例中,可使用可选的寡核苷酸连接子(例如胞苷、尿苷、腺苷、鸟苷或其任何组合)。在一些实施例中,未标记链可包含可用于例如核酸测序反应中的额外修饰。
如图8n中所描绘,包含核苷酸结构域的未标记链8-131可进一步包含能量吸收修饰(正方形形状实线)。在一些实施例中,能量吸收修饰系指保护核酸测序反应完整性(例如避免对标记激发态产生的反应性物质对聚合酶的损伤作用)的任何化学部分。举例而言,在一些实施例中,能量吸收修饰藉由以下中的任一者保护测序反应的完整性:吸收、淬灭或以其他方式缓解反应性物质(例如反应性氧物质、自由基或任何三重态分子)的作用;在发光标记结构域与核苷酸结构域之间提供立体阻挡;相比于在能量吸收修饰不存在下进行的反应,提高测序反应中的读段长度;相比于在能量吸收修饰不存在下进行的反应,提高测序反应的读段准确度;或其任何组合。
如所示,在一些实施例中,能量吸收修饰在与核苷酸结构域相对的未标记链的末端处或附近。如自通用寡核苷酸二聚体8-100应了解,未标记链8-131中的能量吸收修饰可有利地定位成邻近于退火结构体中的发光标记结构域。因此,在一些实施例中,在发光标记结构域及核苷酸结构域连接在其各自链的3'端处或附近的情况下,能量吸收修饰连接在未标记链的5'端处或附近(例如连接在寡核苷酸序列中最5'核苷酸处,连接在位于寡核苷酸序列中最5'的1%、2%、5%、10%、15%、20%、25%、30%、35%、40%或45%的核苷酸内的核苷酸处)。在一些实施例中,在发光标记结构域及核苷酸结构域连接在其各自链的5'端处或附近的情况下,能量吸收修饰连接在未标记链的3'端处或附近(例如连接在最3'核苷酸处,连接在位于寡核苷酸序列中最3'的1%、2%、5%、10%、15%、20%、25%、30%、35%、40%或45%的核苷酸内的核苷酸处)。在一些实施例中,未标记链可包含多于一个能量吸收修饰。在一些实施例中,能量吸收修饰可包括在不为互补二聚结构域的部分的寡核苷酸悬端(例如3'或5'悬端)内。悬端可具有任何适合的长度,例如长度为1至10(例如约5)或10至20个核苷酸(或其他适合的长度)。
举例而言,在一些实施例中,未标记链8-132包含两个能量吸收修饰。如结构8-132中所描绘,具有多于一个能量吸收修饰的未标记链可类似分支链结构。应了解,未标记链可包含任何数目的能量吸收修饰,其可例如根据给定能量吸收修饰的特性或发光标记结构域中的发光分子的特性和/或数目而变化。能量吸收修饰(例如连接至任一个或两个链)的数目的非限制性实例包括2-10(例如2、3、4、5、6、7、8、9、10)、10-15、15-20或其他适合的数目。能量吸收修饰可以线性、分支链、线性及分支链的组合或其他构造连接。因此,通用未标记链8-133展示具有第一能量吸收修饰及两个额外的分支能量吸收结构域(点线),各能量吸收结构域具有一或多个能量吸收修饰。
在一些实施例中,可根据图8p-8q中所描绘的非限制性结构对未标记链作出一或多个能量吸收修饰。在一些实施例中,可根据下文描绘的非限制性结构对未标记链作出一或多个能量吸收修饰。在此等实例中,一或多个能量吸收修饰展示连接至寡核苷酸链(例如未标记寡核苷酸链)的5'端。
在一些实施例中,核酸连接子包含一或多个能量吸收修饰。在一些实施例中,一或多个能量吸收修饰包含多种淬灭部分(例如三重态淬灭剂)。淬灭部分可包含可检测地淬灭本文所描述的一或多个发光标记的发射的任何染料分子。可基于一或多个发光标记的染料分子的特定类型选择适合的淬灭部分。举例而言,在一些实施例中,适当的淬灭部分具有展现与发光标记的发射谱带至少一些光谱重叠的吸收谱带。在一些实施例中,此重叠的发生可伴随供体的在与淬灭部分的最大吸收波长相比更低或甚至更高波长发射最大值处的发射,限制条件为存在足够的光谱重叠。在一些实施例中,能量传递亦可经由供体发射转移至受体的更高电子状态进行。在一些实施例中,适当的淬灭部分能够自可能损伤聚合酶的一或多个发光标记吸收特定能阶发射。在此类实施例中,可选择淬灭部分以优选(例如选择性地)吸收发射光谱的一部分,其包括潜在地损伤聚合酶、而不会吸收检测为信号(例如在测序反应期间)的发射光谱的部分的发射能阶。
适用作淬灭部分的广泛多种化学反应染料及荧光团为本领域中已知的(参见例如molecularprobeshandbook,第六版,richardp.haugland编(1996),尤其第1-3章;molecularprobeshandbook,第七版,richardp.haugland编;bioprobes26(1997年10月);bioprobes27(1998年2月);bioprobes28(1998年5月);bioprobes29(1998年11月);bioprobes30(1999年1月);bioprobes31(1999年5月):bioprobes32(1999年12月);及bioprobes33(2000年2月);全部以引用的方式并入本文中)。溶液中或共轭至寡核苷酸时的候选染料的光谱特性是已知的或易于使用光谱荧光计来量测。
在一些实施例中,淬灭部分为芘、蒽、萘、吖啶、芪、吲哚或苯并吲哚、噁唑或苯并噁唑、噻唑或苯并噻唑、4-氨基-7-硝基苯-2-氧杂-1,3-二唑(nbd)、花青、羰花青、卡波帝(carbostyryl)、卟啉、水杨酸盐、邻氨基苯甲酸盐、薁、苝、吡啶、喹啉、香豆素(包括羟基香豆素及氨基香豆素及其氟化及磺化衍生物(如gee等人(1998)的美国专利第5,830,912号及wang等人(1997)的美国专利第5,696,157号中所描述,其以引用的方式并入本文中)、聚氮杂阴丹(polyazaindacene)(例如haugland等人(1988)的美国专利第4,774,339号;kang等人(1993)的美国专利第5,187,288号;haugland等人(1993)的美国专利第5,248,782号;kang等人(1993)的美国专利第5,274,113号;kang等人(1995)的第5,433,896号;wu等人(1999)的美国专利第6,005,113号,全部以引用的方式并入本文中)、二苯并哌喃、噁嗪或苯并噁嗪、卡巴嗪(corey(1989)的美国专利第4,810,636号,以引用的方式并入)或芴酮或苯芴酮(babb等人(1989)的美国专利第4,812,409号,以引用的方式并入)。
在一些实施例中,淬灭部分为非荧光染料。举例而言,在一些实施例中,淬灭部分可选自偶氮染料(诸如dabcyl或dabsyl染料及其结构类似物);三芳基甲烷染料,诸如孔雀绿或酚红;经4',5z-二醚取代的荧光素(美国专利第4,318,846号(1982))或不对称花青染料淬灭剂(pct国际申请wo9937,717(1999))。
在一些实施例中,核酸连接子包含具有两个或更多个(例如三个)淬灭部分的未标记链。举例而言,在一些实施例中,未标记链包含下文描绘的经tris-trolox修饰的链。然而,可使用其他类似结构且并入核酸连接子中(例如在发光标记与多磷酸核苷之间的位置处)。
在一些实施例中,包含三种淬灭部分的未标记链为经tris-tempo修饰的链:
在一些实施例中,核酸连接子包含一或多个并不充当发色团的能量吸收修饰。在此类实施例中,所述一或多个能量吸收修饰可藉由在发光标记与多磷酸核苷之间提供立体阻挡而起作用,该等阻挡阻止了发光标记与聚合酶的相互作用。在一些实施例中,核酸连接子包含充当立体阻挡物的分支链聚合结构。在一些实施例中,分支链聚合结构包含两个或更多个基于聚醚的结构。举例而言,在一些实施例中,分支链聚合结构包含基于聚乙二醇(peg)的结构,如以下结构中所示描绘了未标记链的末端修饰。然而,应了解,可使用其他类似分支结构且并入核酸连接子中(例如在发光标记与多磷酸核苷之间的位置处)。
在一些实施例中,核酸连接子包含充当立体阻挡物的树枝状结构。举例而言,在一些实施例中,核酸连接子包含具有聚酯-16-羟基双-mpa树枝状修饰的未标记链,如以下结构中所示描绘了末端经修饰的未标记链。应了解,任何数目的分支适用于此等及类似实施例,因为可根据特定标记核苷酸构造使分支数目优化。举例而言,在一些实施例中,具有多个发光标记的核酸连接子可能需要更大数目的分支,以提供相对于具有单发光标记的类似连接子更大的立体阻挡。
在一些实施例中,末端经修饰的未标记链为聚酯-8-羟基双-mpa树枝状经修饰的链:
如上文中所描述,在一些实施例中,能量吸收修饰为保护测序反应完整性的未标记链的修饰。根据本发明中所提供的技术,核酸测序反应可使用多种类型经发光标记的核苷酸进行,其中核苷酸的发光特性为某些类型核苷酸独有的。因此,在一些实施例中,此等独特发光特性中的一或多者的检测允许鉴别特定类型的核苷酸。因而,在一些实施例中,对一或多个经发光标记的核苷酸作出的任何能量吸收修饰不应干扰基于各自独特发光特性检测特定类型核苷酸的能力。举例而言,各种染料(chromis530n、dylight554r1及cy3b)各自连接至标记链,且各标记链退火至具有6-单糖(6-glycose)-悬端能量吸收修饰或6-甘油树状体悬端能量吸收修饰的未标记链,且量测各寡核苷酸二聚体的发光强度及寿命值。如表3中所呈现的结果中所示,发光特性的任何归因于能量吸收修饰的改变大约随染料分子调整。因此,经发光标记的寡核苷酸二聚体保留将允许各自在混合物中的鉴别的独特发光特性。
表3.能量吸收修饰对经标记的寡核苷酸的作用。
因此,发光标记可直接例如藉由键连接至分子,或可经由连接子或连接子构造连接。在某些实施例中,连接子包含一或多个磷酸酯。在一些实施例中,核苷酸藉由包含一或多个磷酸酯的连接子连接至发光标记。描述为具有一或多个磷酸酯的连接子系指包含存在连接子结构内的一或多个磷酸酯(不直接连接至核苷酸的一或多个磷酸酯)的连接子。在一些实施例中,核苷酸藉由包含三个或更多个磷酸酯的连接子连接至发光标记。在一些实施例中,核苷酸藉由包含四个或更多个磷酸酯的连接子连接至发光标记。
在某些实施例中,连接子包含脂族链。在一些实施例中,连接子包含-(ch2)n-,其中n为1至20(包括端点)的整数。在一些实施例中,n为1至10(包括端点)的整数。在某些实施例中,连接子包含杂脂族链。在一些实施例中,连接子包含聚乙二醇部分。在一些实施例中,连接子包含聚丙二醇部分。在一些实施例中,连接子包含-(ch2ch2o)n-,其中n为1至20(包括端点)的整数。在一些实施例中,连接子包含-(ch2ch2o)n-,其中n为1至10(包括端点)的整数。在某些实施例中,连接子包含-(ch2ch2o)4-。在某些实施例中,连接子包含一或多个亚芳基。在一些实施例中,连接子包含一或多个亚苯基(例如对位取代亚苯基)。在某些实施例中,连接子包含手性中心。在一些实施例中,连接子包含脯氨酸或其衍生物。在一些实施例中,连接子包含脯氨酸六聚体或其衍生物。在一些实施例中,连接子包含香豆素或其衍生物。在一些实施例中,连接子包含萘或其衍生物。在一些实施例中,连接子包含蒽或其衍生物。在一些实施例中,连接子包含聚苯基酰胺或其衍生物。在一些实施例中,连接子包含苯并二氢吡喃酮(chromanone)或其衍生物。在一些实施例中,连接子包含4-氨基炔丙基-l-苯丙氨酸或其衍生物。在某些实施例中,连接子包含多肽。
在一些实施例中,连接子包含寡核苷酸。在一些实施例中,连接子包含两个退火寡核苷酸。在一些实施例中,一或多个寡核苷酸包含脱氧核糖核苷酸、核糖核苷酸或锁核糖核苷酸。
在某些实施例中,连接子包含光稳定剂。在一些实施例中,连接子具有下式:
其中ps为光稳定剂,位置标记d连接至发光标记,且位置标记b连接至核苷酸。在一些实施例中,位置标记d藉由如本文所描述的连接子连接至发光标记。在一些实施例中,位置标记b藉由如本文所描述的连接子连接至核苷酸。
在某些实施例中,连接子包含一或多个磷酸酯、脂族链、杂脂族链及一或多种酰胺(例如-c(=o)nh-)。在某些实施例中,包含一或多个磷酸酯及脂族链的连接子可经由图9中描绘的例示性反应流程9-1合成。在某些实施例中,连接子含有一或多个官能化反应性部分(例如乙炔基、叠氮基)。
等效物及范畴
本申请的各种方面可单独、组合或以前文中所描述的实施例中未具体论述的多种配置使用,且因此不限于应用至前文描述中所阐述或图式中所说明的组件的细节及配置。举例而言,一个实施例中所描述的方面可以任何方式与其他实施例中所描述的方面组合。
此外,本发明可体现为方法,已提供其至少一个实例。作为方法的部分所执行的动作可以任何适合的方式排序。因此,可建构如下实施例:其中动作以不同于所说明的次序的次序执行,可包括同时执行一些动作,即使此等动作在说明性实施例中被展示为连续动作。
在申请专利范围中使用诸如“第一”、“第二”、“第三”等序数术语修饰权利要求要素本身不意味着一个权利要求要素相对于另一权利要求要素的任何优先权、优先性或次序或执行方法动作的时间次序,而是仅用作标签以区分具有某一名称的一个权利要求要素与具有相同名称(但使用序数术语)的另一要素,以区分该等权利要求要素。
此外,本文所使用的措词及术语出于描述的目的且不应视为限制性。本文中对“包括”、“包含”或“具有”、“含有”、“涉及”及其变化的使用意谓涵盖在其之后所列举的项目及其等效物以及额外项目。
- 还没有人留言评论。精彩留言会获得点赞!