一种巯基化羟乙基淀粉及其修饰的纳米材料和制备方法与流程
本发明涉及活性淀粉及纳米材料,更具体地,涉及一种巯基化羟乙基淀粉及其修饰的纳米材料和制备方法。
背景技术:
近些年来,随着纳米技术的蓬勃发展,一系列纳米药物载体材料被应用到抗肿瘤药物的研究中。这些材料可以增强药物在肿瘤部位的渗透以及滞留、延长药物在体内的循环时间和降低化疗药物的毒副作用。但是许多纳米药物载体在实际应用往往很难收获以上提到的优良效果,其中一个重要原因就是人体复杂的生理环境会限制纳米材料发挥正常的作用。纳米药物载体在进入体内后会面临许多的生物屏障,包括血浆蛋白的非特异性吸附以及巨噬细胞的吞噬等。为了克服这些生物屏障,必须要对纳米药物载体进行改性。
目前,对纳米药物载体改性的方法中,最常用的一种方法就是使用表面修饰剂对纳米药物载体进行改性,即通过一些大分子材料对纳米药物载体表面进行适当修饰,增强载体表面的空间位阻,最终稳定纳米药物载体。
聚乙二醇(PEG)是由环氧乙烷在一定条件下聚合而成的一类高分子材料,是最常用的表面修饰高分子,具有结构简单、分子量可调、反应活性强、水溶性好、生物相容性好等特点。PEG也是美国食品药品监督管理局(FDA)批准能用于体内的少数人工合成高分子聚合物之一。目前,在药剂学研究中,PEG的一个重要应用就是对蛋白质、多肽或者纳米药物载体进行修饰(Pascal Bailon,CheeYoub Won. PEG-modified biopharmaceuticals[J].Expert opinion on drug delivery, 2009,6(1):1)。PEG修饰后,药物载体的稳定性提高,免疫原性降低,体内循环时间延长。
但是PEG也存着一些缺陷。首先,作为一种人工合成的聚合物, PEG不能在体内降解,因此长期或者大量使用可能会产生毒副作用。其次,PEG的可修饰位点少,这不利于其偶联一些药物分子以及靶向配体。最后,PEG的长期使用会带来严重的免疫毒性。考虑到目前PEG 存在的诸多不足,寻找一种更加优良的修饰剂就成为了一件非常重要的事。
技术实现要素:
本发明提供一种克服上述问题或者至少部分地解决上述问题的巯基化羟乙基淀粉及其修饰的纳米材料和制备方法。
本发明中的重量份的单位可以是本领域常规重量/质量单位。
根据本发明的一个方面,提供一种巯基化羟乙基淀粉,该巯基化羟乙基淀粉中巯基的摩尔取代度为0.05~0.2。
在一个优选实施方式中,其化学结构式可表述为:
其中,R为H或CH2CH2OH。可以理解的是,由于羟乙基取代度的不同,上述羟乙基淀粉的化学结构式仅表示羟乙基淀粉较优的或可能的结构形式,并不表示羟乙基淀粉唯一的结构形式。
在一个优选实施方式中,巯基化羟乙基淀粉的分子量为 10~480kDa;优选为20~50kDa;可进一步优选为25kDa。
在一个优选实施方式中,巯基化羟乙基淀粉的分子量为 10~480kDa;优选为20~50kDa;可进一步优选为25kDa;
巯基的摩尔取代度为0.05-0.2;优选为0.08~0.15;进一步优选为 0.1。
本发明的巯基化羟乙基淀粉具有高反应活性以及良好的水溶性;同时,其还具有良好的生物降解性能。所得巯基化羟乙基淀粉中巯基的摩尔取代度保持在该范围,能够有效地提高巯基化羟乙基淀粉的活性,又不会影响巯基化羟乙基淀粉的稳定性。同时,所得巯基化羟乙基淀粉的分子量保持在合适的范围,利于其保持良好的稳定性和生物降解能力。
根据本发明的另一个方面,提供一种巯基化羟乙基淀粉的制备方法,包括:
步骤S1、将羟乙基淀粉在碱性条件下羧基化得到羧甲基羟乙基淀粉;
步骤S2、羧甲基羟乙基淀粉与2-(吡啶二硫)-乙胺盐酸盐反应得到羟乙基淀粉-2-(吡啶二硫);
步骤S3、羟乙基淀粉-2-(吡啶二硫)巯基化得到巯基化羟乙基淀粉。
本发明的巯基化羟乙基淀粉(简称:HES-SH)制备方法,所选用的试剂安全性高,制备过程简单,不会产生副产物,巯基化羟乙基淀粉的产率高,便于大批量生产。
在步骤S1中,将羟乙基淀粉(简称:HES)溶在去离子水中,搅拌至完全溶解。再加入含有碱性溶液以调节pH值,得到淀粉溶液。在碱性条件下,便于提高羟乙基淀粉羧基化的反应效率。上述淀粉溶液经羧基化反应后,即可得到羧甲基羟乙基淀粉(简称:HES-COOH)。
在一个优选实施方式中,羟乙基淀粉的化学结构式可表述为:
其中,R为H或CH2CH2OH。可以理解的是,由于羟乙基取代度的不同,上述羟乙基淀粉的化学结构式仅表示羟乙基淀粉可能的结构形式,并不表示羟乙基淀粉唯一的结构形式。
其中,羟乙基淀粉的分子量为20000~30000;优选为25000。
其中,羟乙基淀粉中羟乙基的摩尔取代度为0.4~0.6;优选为0.5。
在一个优选实施方式中,淀粉溶解于去离子水中后,所得淀粉水溶液的质量浓度为10~100mg/mL;优选50mg/mL。
在一个优选实施方式中,用于调节pH值的碱性物质可以为NaOH。加入NaOH水溶液,将淀粉溶液的pH值调节至合适的范围,有利于调控淀粉的羧基化反应,以便于调控巯基化羟乙基淀粉活性基团的取代度。
在一个优选实施方式中,将淀粉溶液的pH值调节至合适范围后,向淀粉溶液中添加羧基化试剂,以使淀粉溶液中的淀粉发生羧基化反应,向淀粉上接入活性基团。
在一个优选实施方式中,羧基化试剂为具有羧甲基基团的化合物。羧基化试剂中的羧甲基与淀粉发生羧基化反应,以在淀粉的碳链上接入羧甲基,得到含有羧甲基羟乙基淀粉的溶液。
在一个优选实施方式中,羧基化试剂为α-卤代羧酸;优选为氯乙酸(简称:MCA)。
在一个优选实施方式中,羟乙基淀粉中的糖单元与羧基化试剂的摩尔比为1:(1~4);优选为1:(2~3)。
在一个优选实施方式中,羟乙基淀粉中的糖单元、碱性物质、羧基化试剂的摩尔比为1:(1~5):(1~4);优选为1:4:2。该投料比例可以获得合适羧甲基取代度的羧基化羟乙基淀粉,并且降低羟乙基淀粉在碱性条件下的水解程度,以利于所制备的巯基化羟乙基淀粉中巯基的取代度保持在合适的范围。
在一个优选实施方式中,向淀粉溶液中加入羧基化试剂后,所得第一混合液在60~80℃条件下持续搅拌1~6h,即得到含有羧甲基羟乙基淀粉的第二混合液。
在一个优选实施方式中,将第二混合液添加到甲醇或乙醚中,得到第三混合液。第三混合液为悬浮液。第三混合液经离心分离处理,得到白色沉淀。
在一个优选实施方式中,将上述白色沉淀用洗涤剂洗涤数次。洗涤剂可选用甲醇、乙醚等。
洗涤后的白色沉淀再用去离子水透析2~3天。透析所采用透析袋的节流分子量为800~1200Da。所得白色沉淀经冷冻干燥后,即得到白色固体羧甲基羟乙基淀粉。
在一个优选实施方式中,羧甲基羟乙基淀粉的化学结构式可表述如下:
其中,R为H或CH2CH2OH。可以理解的是,由于羧甲基和/或羟乙基取代度的不同,上述羧甲基羟乙基淀粉的化学结构式仅表示羧甲基羟乙基淀粉可能的结构形式,并不表示羧甲基羟乙基淀粉唯一的结构形式。
含有羧甲基羟乙基淀粉的第二混合液经离心分离、洗涤后,再经透析和冷冻干燥处理,能够有效的去除制备过程中未反应完全的原料或中间产物等杂质,提高所得固体羧甲基羟乙基淀粉的纯度。
步骤S2中,将羧甲基羟乙基淀粉溶于去离子水中,形成羧甲基羟乙基淀粉溶液。向羧甲基羟乙基淀粉溶液中添加2-(吡啶二硫)-乙胺盐酸盐,使羧甲基羟乙基淀粉与2-(吡啶二硫)-乙胺盐酸盐反应而生成羟乙基淀粉-2-(吡啶二硫)(简称:HES-PA)。
在一个优选实施方式中,羧甲基羟乙基淀粉溶液中,羧甲基羟乙基淀粉中的游离羧基的质量浓度为10~100mg/mL,优选50mg/mL。
在一个优选实施方式中,在1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐与N-羟基琥珀酰亚胺的催化作用下,能够有效地提高羧甲基羟乙基淀粉与2-(吡啶二硫)-乙胺盐酸盐的反应效率,提高产物的产率。
在一个优选实施方式中,羧甲基羟乙基淀粉中的游离羧基与2-(吡啶二硫)-乙胺盐酸盐的摩尔比为1:(0.5~3)。优选为1:2。羧甲基羟乙基淀粉中的游离羧基为羧基化过程中接入到羟乙基淀粉上的羧基。羧甲基羟乙基淀粉与2-(吡啶二硫)-乙胺盐酸盐的比例保持在合适的范围,以使羧甲基羟乙基淀粉中的羧基能够完全反应,以提高反应效率。
在一个优选实施方式中,羧甲基羟乙基淀粉中的游离羧基、1-(3- 二甲氨基丙基)-3-乙基碳二亚胺盐酸盐、N-羟基琥珀酰亚胺与2-(吡啶二硫)-乙胺盐酸盐的摩尔比为1:(3.5~4.5):(1.5~2.5):(0.5~3),优选为1:4:2:2。催化剂1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐与N- 羟基琥珀酰亚胺的用量在合适的范围,便于羧甲基羟乙基淀粉中的羧基与2-(吡啶二硫)-乙胺盐酸盐充分反应。
在一个优选实施方式中,羧甲基羟乙基淀粉溶于去离子水中后,再加入2-(吡啶二硫)-乙胺盐酸盐、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐和N-羟基琥珀酰亚胺得到第四混合液。
第四混合液在5~50℃条件下反应24~48h,得到含有羟乙基淀粉 -2-(吡啶二硫)的第五混合液。
在一个优选实施方式中,第五混合液经离心分离处理后,取其上清液采用去离子水透析2~3天。其中,透析处理所采用的透析袋的截留分子量为800~1200Da。透析后所得溶液经冷冻干燥后,即得到白色固体羟乙基淀粉-2-(吡啶二硫)。
羟乙基淀粉-2-(吡啶二硫)的化学结构式可表示如下:
其中,R为H或CH2CH2OH。可以理解的是,由于羟乙基和/或2-(吡啶二硫)的取代度的不同,上述羟乙基淀粉-2-(吡啶二硫)的化学结构式仅表示羟乙基淀粉-2-(吡啶二硫)可能的结构形式,并不表示羟乙基淀粉 -2-(吡啶二硫)唯一的结构形式。
在步骤S3中,将白色固体羟乙基淀粉-2-(吡啶二硫)复溶于有机溶剂中,得到羟乙基淀粉-2-(吡啶二硫)溶液。
其中,有机溶剂可以为二甲亚砜。
在一个优选实施方式中,羟乙基淀粉-2-(吡啶二硫)溶液中,羟乙基淀粉-2-(吡啶二硫)的质量浓度为10~100mg/mL;优选为30~70mg/mL;进一步优选50mg/mL。
在一个优选实施方式中,向羟乙基淀粉-2-(吡啶二硫)溶液中加入巯基化试剂,便于形成巯基基团。具体地,巯基化试剂可以为二硫苏糖醇(简称:DTT)、谷胱甘肽,巯基乙醇等。巯基化试剂可优选为二硫苏糖醇。
羟乙基淀粉-2-(吡啶二硫)与巯基化试剂反应,以使羟乙基淀粉 -2-(吡啶二硫)中的二硫键断裂,形成巯基,得到最终产物巯基化羟乙基淀粉。
在一个优选实施方式中,羟乙基淀粉-2-(吡啶二硫)中的2-(吡啶二硫)基团与巯基化试剂的摩尔比为1:(5~20);优选为1:(8~15);进一步优选为1:10。
羟乙基淀粉-2-(吡啶二硫)中的吡啶基团与巯基化试剂的摩尔比保持在合适的范围,使羟乙基淀粉-2-(吡啶二硫)中的-2-(吡啶二硫)基团与巯基化试剂充分反应,以使羟乙基淀粉-2-(吡啶二硫)中的二硫键能够完全断开以形成巯基,避免产物中含有-2-(吡啶二硫)基团或其他杂质。
在一个优选实施方式中,向羟乙基淀粉-2-(吡啶二硫)溶液中加入巯基化试剂得到第六混合液。第六混合液中通入N2,并在5-50℃条件下反应24~48h,得到含有巯基化羟乙基淀粉的、黄褐色的第七混合液。
在一个优选实施方式中,第七混合液采用截留分子为800~1200Da 的透析袋经去离子水透析2-3天,再经冷冻干燥后得到的固体物质即为巯基化羟乙基淀粉。
在一个优选实施方式中,本发明的巯基化羟乙基淀粉的制备方法,包括:
步骤S1、将所述羟乙基淀粉与所述羧基化试剂羧基化得到羧甲基羟乙基淀粉;其中,所述羟乙基淀粉中的糖单元与所述羧基化试剂的摩尔比为1:(2~3);
步骤S2、将羧甲基羟乙基淀粉、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐、N-羟基琥珀酰亚胺与2-(吡啶二硫)-乙胺盐酸盐反应得到羟乙基淀粉-2-(吡啶二硫);
步骤S3、羟乙基淀粉-2-(吡啶二硫)巯基化得到巯基化羟乙基淀粉。
在一个优选实施方式中,本发明的巯基化羟乙基淀粉的制备方法,包括:
步骤S1、所述羟乙基淀粉与所述羧基化试剂在60~80℃条件下反应1-6h的条件下羧基化反应得到羧甲基羟乙基淀粉;
步骤S2、将羧甲基羟乙基淀粉、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐、N-羟基琥珀酰亚胺与2-(吡啶二硫)-乙胺盐酸盐反应得到羟乙基淀粉-2-(吡啶二硫);其中,羧甲基羟乙基淀粉中的游离羧基、1-(3- 二甲氨基丙基)-3-乙基碳二亚胺盐酸盐、N-羟基琥珀酰亚胺与2-(吡啶二硫)-乙胺盐酸盐的摩尔比为1:(3.5~4.5):(1.5~2.5):(0.5~3);
步骤S3、羟乙基淀粉-2-(吡啶二硫)与二硫苏糖醇的混合物中通入 N2,并在5~50℃条件下反应24~48h得到巯基化羟乙基淀粉。
具体地,以羧基化试剂为氯乙酸、巯基化试剂为二硫苏糖醇为例,由羟乙基淀粉制备巯基化羟乙基淀粉的过程可表述如下:
本发明的巯基化羟乙基淀粉的制备方法,其制备过程简单,反应效率高,反应条件易于调控,能够制备得到杂质含量少、产率高、生物降解性好,且其具有高反应活性以及良好的水溶性。
根据本发明的另一个方面,还提供一种巯基化羟乙基淀粉,其由上述方法制备得到。
根据本发明的另一个方面,还提供一种由上述巯基化羟乙基淀粉修饰的聚多巴胺纳米材料。优选在聚多巴胺表面修饰一层巯基化羟乙基淀粉。经巯基化羟乙基淀粉修饰的聚多巴胺纳米材料(简称: HES-PDA),其稳定性好,冻干复溶能力强,可以作为一种纳米药物载体应用于抗肿瘤药物的靶向输送。
在一个优选实施方式中,上述由巯基化羟乙基淀粉修饰的聚多巴胺纳米材料的粒径为100~300nm。
在一个优选实施方式中,上述由巯基化羟乙基淀粉修饰的聚多巴胺纳米材料的zeta电位为-20~0mV。
根据本发明的另一个方面,还提供一种由巯基化羟乙基淀粉修饰的聚多巴胺(简称:PDA)纳米材料的制备方法,包括:巯基化羟乙基淀粉与聚多巴胺在碱性条件下反应。将反应所得产物采用超滤过滤处理后,即得到由巯基化羟乙基淀粉修饰的聚多巴胺纳米材料。
其制备过程可表述如下:
本发明的聚多巴胺纳米材料制备方法中,将聚多巴胺分散于去离子水中得到聚多巴胺水溶液,并采用超声搅拌10~30min,以增强聚多巴胺在水中的分散性。向聚多巴胺水溶液中添加碱性溶液以调节聚多巴胺水溶液的pH值,得到第八混合液。第八混合液的pH值为8~12。该pH值优选为10。
在一个优选实施方式中,第八混合液中聚多巴胺的质量浓度为 0.5~5mg/mL;优选为4mg/mL。
在一个优选实施方式中,所用碱性溶液可以为NaOH水溶液等。具体地,碱性溶液中碱性物质的摩尔浓度为0.05~0.15mol/L;优选为 0.1mol/L。
在一个优选实施方式中,将上述巯基化羟乙基淀粉分散于去离子水中得到巯基化羟乙基淀粉溶液。巯基化羟乙基淀粉溶液中巯基化羟乙基淀粉的质量浓度为2~50mg/mL;优选为20mg/mL。
配制得到第八混合液和巯基化羟乙基淀粉溶液以后,将二者混合,以使巯基化羟乙基淀粉与聚多巴胺反应,得到经巯基化羟乙基淀粉修饰的聚多巴胺纳米材料。
在一个优选实施方式中,巯基化羟乙基淀粉与聚多巴胺的质量比为(1~10):1;优选为5:1。巯基化羟乙基淀粉与聚多巴胺的质量比调控在合适的范围,该质量比可以使得聚多巴胺表面充分与巯基化羟乙基淀粉反应,很好的稳定聚多巴胺,而且该投料比还可以减少巯基化羟乙基淀粉的用量,简化了后续的纯化过程。
在一个优选实施方式中,第八混合液与巯基化羟乙基淀粉溶液混合反应后得到含有经巯基化羟乙基淀粉修饰的聚多巴胺纳米材料的第九混合液。第九混合液采用超滤以去除未反应完全的巯基化羟乙基淀粉和/或聚多巴胺。
其中,超滤所采用超滤管的截留分子量为30~100kDa;超滤转速为3000~5000转/分钟;超滤时间为5~25min。第九混合液采用上述超滤过程超滤3~6次,所得悬浮液经冷冻干燥处理,得到的黑色固体即为经巯基化羟乙基淀粉修饰的聚多巴胺纳米材料。
根据本发明的另一个方面,还提供一种由巯基化羟乙基淀粉修饰的聚多巴胺纳米材料,其由上述方法制备得到。
根据本发明的另一个方面,还提供一种由巯基化羟乙基淀粉修饰的金纳米材料。优选在金纳米粒表面修饰一层巯基化羟乙基淀粉。经巯基化羟乙基淀粉修饰得到的金纳米材料(简称:HES-GNP)比未经修饰的金纳米材料具有更高的稳定性。
其中,优选每平方纳米的金纳米颗粒上修饰的巯基化羟乙基淀粉颗粒的个数为30~80个;优选为50个。
在一个优选实施方式中,由巯基化羟乙基淀粉修饰的金纳米材料的粒径为30~150nm。
在一个优选实施方式中,由巯基化羟乙基淀粉修饰的金纳米材料的zeta电位为-20~0mV。
根据本发明的另一个方面,还提供一种由巯基化羟乙基淀粉修饰的金纳米材料的制备方法,包括:将巯基化羟乙基淀粉与金纳米材料在50~70℃条件下孵育1~6h即得。
本发明的由巯基化羟乙基淀粉修饰的金纳米材料的制备方法中,将金纳米材料分散于去离子水中,得到第十混合液。第十混合液中,金纳米材料的摩尔浓度为0.1~1nmol/L。
在一个优选实施方式中,将上述巯基化羟乙基淀粉分散于去离子水中,得到第十一混合液。在第十一混合液中,巯基化羟乙基淀粉的质量浓度为0.1~0.5mg/mL。
在一个优选实施方式中,将第十混合液逐滴滴加到第十一混合液中得到第十二混合液。第十二混合液在50~70℃条件下孵育1~6h,得到含有经巯基化羟乙基淀粉修饰的金纳米材料的第十三混合液。
在一个优选实施方式中,第十三混合液经离心分离处理,以去除未反应完全的巯基化羟乙基淀粉,得到含有由巯基化羟乙基淀粉修饰的金纳米材料的悬浮液。其中,离心处理的转速为10000~15000转/分钟,离心处理的时间5-20min。第十三混合液经上述离心处理方式处理 2~4次。
根据本发明的另一个方面,还提供一种由巯基化羟乙基淀粉修饰的金纳米材料,其由上述制备方法制备得到。其中,优选每平方纳米的金纳米材料上修饰的巯基化羟乙基淀粉颗粒的个数为30~80个;优选为50个。该比例可以实现较好的修饰效果,得到的羟乙基淀粉稳定的金纳米粒的稳定性较好。
本发明的有益效果主要如下:
本发明所涉及的巯基化羟乙基淀粉巯基化取代度合适,富含具有高反应活性的巯基,可以解决目前羟乙基淀粉缺少高活性官能团的缺陷,又能够具有良好地稳定性,而且巯基化羟乙基淀粉依然保持着良好的水溶性,可以对一些纳米材料的表面进行修饰,从而改善该材料的相关性能。
本发明所涉及的巯基化羟乙基淀粉具有α-淀粉酶响应性,在体内可以被逐渐降解,之后通过肾脏排出,因为不会在体内蓄积,不会产生毒副作用。
本发明提供了一种巯基化羟乙基淀粉的制备方法,该方法反应条件温和,操作简单,产率高,有利于批量放大生产,此外,该方法反应机理明确,不会产生副产物,安全性好,最终产物巯基化羟乙基淀粉的质量能得到保障。
本发明的巯基化羟乙基淀粉修饰聚多巴胺,其具有制备方法简单,稳定性好,冻干复溶能力强等优点,可以作为一种纳米药物载体应用于抗肿瘤药物的靶向输送。
本发明的羟乙基淀粉修饰的金纳米粒,其制备方法简单,而且与未修饰的金纳米粒相比,巯基化羟乙基淀粉的修饰的金纳米粒具有更高的稳定性。
附图说明
图1为本发明实施例1制备的巯基化羟乙基淀粉的核磁共振谱图 (氢谱);
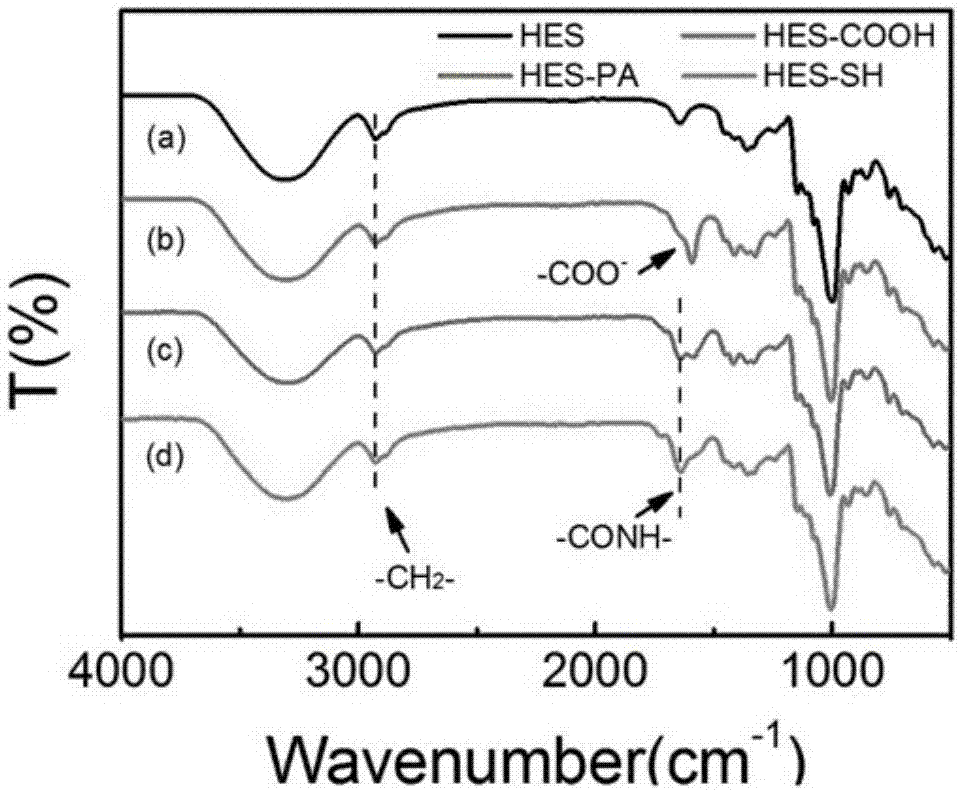
图2为本发明实施例1制备的巯基化羟乙基淀粉的红外光谱图;
图3为本发明实施例2制备的巯基化羟乙基淀粉修饰的聚多巴胺和聚乙二醇修饰的聚多巴胺的透射电镜图;
图4为本发明实施例2制备的巯基化羟乙基淀粉修饰的聚多巴胺和聚乙二醇修饰的聚多巴胺的粒径分布图(水合粒径);
图5为本发明实施例2制备的巯基化羟乙基淀粉修饰的聚多巴胺和聚乙二醇修饰的聚多巴胺红外光谱图;
图6为本发明实施例2制备的巯基化羟乙基淀粉修饰的聚多巴胺和聚乙二醇修饰的聚多巴胺的水合粒径随时间变化图;
图7为本发明实施例2制备的巯基化羟乙基淀粉修饰的聚多巴胺和聚乙二醇修饰的聚多巴胺在不同分散介质中的图片;
图8为本发明实施例3制备的金纳米粒和巯基化羟乙基淀粉修饰的金纳米粒的粒径分布图(水合粒径);
图9为本发明实施例3制备的金纳米粒和巯基化羟乙基淀粉修饰的金纳米粒的透射电镜图片;
图10为本发明实施例3制备的金纳米粒和巯基化羟乙基淀粉修饰的金纳米粒的紫外吸收光谱图;
图11为本发明实施例3制备的金纳米粒和巯基化羟乙基淀粉修饰的金纳米粒在不同分散介质中的图片;
图12为本发明实施例3制备的在不同浓度的氯化钠溶液中的紫外吸收光谱图;
图13为本发明实施例3制备的巯基化羟乙基淀粉修饰的金纳米粒在0.8mol/L的氯化钠中的水合粒径随时间变化图。
具体实施方式
下面结合实施例,对本发明的具体实施方式作进一步详细描述。以下实施例用于说明本发明,但不用来限制本发明的范围。
实施例1
本实施例提供一种巯基化羟乙基淀粉及其制备方法,该方法包括以下三个步骤:
(1)取分子量为25000Da、羟乙基摩尔取代度为0.5的羟乙基淀粉1g溶在20mL去离子水中,搅拌至完全溶解;再加入0.8g已经溶解完全的氢氧化钠溶液,充分搅拌,得到反应液A;之后再向反应液A 中加入氯乙酸1g,在70摄氏度下持续搅拌反应3h,得到反应液B;将反应液B倒入至甲醇,搅拌,得混悬液C;将混悬液C离心,得到白色沉淀,所述白色沉淀用甲醇洗涤数次;将所述白色沉淀复溶于去离子水,之后采用截留分子量为1000Da的透析袋去离子水透析3天,冷冻干燥得到的白色固体为HES-COOH;
(2)取上述HES-COOH 0.5g溶于10mL去离子水中,之后加入 1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐210mg、N-羟基琥珀酰亚胺 62.5mg和2-(吡啶二硫)-乙胺盐酸盐121mg,25℃搅拌反应24h,得到反应液D;将反应液D离心,离心的转速为5000转/分钟,离心时间为10分钟,取上清采用截留分子量为3500Da的透析袋去离子水透析 3天,冷冻干燥得到的白色固体为HES-PA;
(3)取上述HES-PA 0.5g复溶于10mL二甲亚砜中,之后加入二硫苏糖醇420mg,充入氮气,室温搅拌反应24h,得到黄褐色的反应液 E;将反应液E采用截留分子量为3500Da的透析袋去离子水透析3天,冷冻干燥,即得到固体物质HES-SH。所得HES-SH中巯基的取代度为 0.081。
实施例2
本实例提供一种由巯基化羟乙基淀粉修饰的聚多巴胺纳米材料及其制备方法,该制备方法包括:取40mg PDA分散在10mL去离子水中,搅拌超声30分钟,使用氢氧化钠(浓度为0.1mol/L)调节pH到 10,得到的混悬液A;取实施例1制备的HES-SH 200mg分散于10mL 水中,得到溶液B;将溶液B缓慢滴加至混悬液A中,之后持续超声 30分钟,再室温搅拌反应24h,得到反应液C;将反应液C超滤以除去未反应的HES-SH,得到HES-PDA混悬液D,超滤管的截留分子量为100kDa,超滤转速为4000转/分钟,超滤时间为10min,超滤次数为4次;将混悬液D冷冻干燥,得到黑色的固体为HES-PDA。
实施例3
本实施例提供一种由巯基化羟乙基淀粉修饰的金纳米材料及其制备方法,该制备方法包括:将1nMGNP分散在2mL去离子水中,得到液体A;取实施例1制备的HES-SH 5mg分散于25mL水中,得到溶液B;将溶液A缓慢滴加至混悬液B中,之后在60摄氏度下孵育2 小时,得到反应液C;将反应液C离心以除去未反应的HES-SH,得到分散液D,所述离心转速为12000转/分钟,所述离心时间为10min,离心次数优选为3次即得。
试验例1
采用核磁共振氢谱和红外光谱确认实施例1制备的HES-SH的化学结构。图1和图2为本发明实施例1制备的HES-SH的核磁共振氢谱图和红外光谱图。由图1可知,与HES的核磁谱图相比,HES-COOH 在4~4.3处出现了一组新的峰,对应羧甲基上的两个氢的峰。与 HES-COOH相比,HES-PA在7~8.5和2.5~3.1处出现了新的峰,分别对应PA*HCl的吡啶上氢的峰和亚甲基上氢的峰。与HES-PA相比, HES-SH在7~8.5处没有峰出现,说明HES-PA中的二硫键已经断开。
由图2可知,与HES的红外光谱图相比,HES-COOH的红外吸收在1593cm-1处出现了一个新的吸收峰,归属于羧甲基上的羧酸根离子的羰基吸收峰。与HES-COOH相比,HES-PA的红外吸收在1641cm-1处出现了新的吸收峰,归属于HES-PA结构中酰胺键的中C-N伸缩振动峰。与HES-PA相比,HES-SH没有新的吸收峰出现,说明结构中的酰胺键依然完整。以上这些结果与合成路线所设想的结果相符,以上核磁共振氢谱和红外吸收光谱的结果确证了本实施例1制备的 HES-SH的化学结构。
试验例2
HES-PDA的表征,通过激光粒度仪来测量PDA在修饰前后的粒径变化,通过红外光谱确证所得到纳米载药系统的结构。图3是PDA 在修饰前的透射电镜图片,图4是HES-PDA和聚PEG-PDA的粒径分布图(水合粒径),图5是HES-PDA和PEG-PDA的红外光谱图。
由图3可知,实施例3所制备的PDA为尺寸均一的纳米粒,是一种优良的纳米材料。
由图4可知,与PDA的平均粒径134.1±2.7nm相比,HES-PDA的平均粒径增大到156.5±1.2nm,而PEG-PDA的平均粒径增大到 156.2±1.4nm,二者的粒径均有明显的增加,说明了修饰反应的成功。
由图5可知,与PDA相比,HES-PDA在2877cm-1处出现了一个更强的吸收峰,归属于HES结构中亚甲基的伸缩振动,同时,HES-PDA 在1101cm-1处出现了一个更强的吸收峰,这是HES存在所引起的吸收;同样的,对于PEG-PDA来说,其红外吸收峰与PDA相比,也发生了明显的变化,以上红外光谱的结果确证了HES-SH和PEG是修饰在 PDA表面的。
试验例3
巯基化羟乙基淀粉修饰的聚多巴胺稳定性的评价,
实验过程:分别取1mg冻干之后的HES-PDA与PEG-PDA分散于 2mL的0.01M的磷酸盐酸盐缓冲液中,之后定时用DLS测量水合粒径。此外,分别取1mg冻干之后的HES-PDA与PEG-PDA分散于适量的 DMEM培养基和20%血清中,之后观察稳定性。
图6是HES-PDA和PEG-PDA在磷酸盐缓冲液(PBS)中的粒径随时间变化曲线。图7是PDA、HES-PDA和PEG-PDA在不同分散介质中的图片。
由图6可知,HES-PDA和PEG-PDA在PBS中具有很好的稳定性,在连续12天的测量中,其粒径与分散性并没有发生明显的变化。
由图7可知,与PDA相比,HES-PDA与PEG-PDA在水、PBS、 DMEM和20%血清中依然能保持稳定而不发生聚沉。
以上结果表明HES-SH能和PEG一样具有稳定PDA的作用。
试验例4
巯基化羟乙基淀粉修饰的金纳米粒(HES-GNP)的表征,通过激光粒度仪测量GNP在修饰前后的粒径变化,通过透射电镜表征GNP 在修饰前后的形态。
图8是GNP在修饰前后的粒径分布图(水合粒径),图9是GNP 在修饰前后的透射电镜图片,图10是GNP在修饰前后的紫外吸收光谱,表1是GNP和HES-GNP的粒径、分散度、Zeta电位和紫外吸收峰等参数的总结。
表1 GNP和HES-GNP的粒径、分散度、Zeta电位和紫外吸收峰等参数的总结
由表1和图8可以看出,与GNP相比,HES-GNP的水合半径增大了约7nm,这与25000分子量的HES分子的大小较为接近,而且 HES-GNP的多分散指数(PDI)依然较好,说明没有发生聚集的现象。
对于通过柠檬酸钠还原法制备的金纳米粒来说,其在水中能保持稳定的原因是金纳米粒表面存在很多的柠檬酸根,通过电荷之间的互斥作用稳定金纳米粒。由表1可知,HES-GNP的Zeta-电位发生明显的下降,由-30mV下降到约-10mV,这是由于羟乙基淀粉存在于金纳米粒表面,取代了原有的柠檬酸根,使得纳米粒的表面电荷减少,Zeta-电位下降。
由图9可知,使用磷钨酸对HES-GNP进行染色,从透射电镜所拍得的图片中可以看到,金纳米粒表面存在一层聚合物包裹层,形貌非常清晰,由此可以确定金纳米粒表面存在着羟乙基淀粉。
由图10和表1可知,在修饰了羟乙基淀粉后,金纳米粒的紫外吸收发生了明显的红移,最大吸收波长从525.8nm偏移到528.8nm,这是由于金纳米粒表面存在的羟乙基淀粉,使金纳米粒表面的介电常数发生了改变,物理性质发生改变。
以上水合粒径,透射电镜,Zeta-电位和紫外吸收光谱的结果结合在一起可以证实巯基化羟乙基淀粉可以成功修饰到金纳米粒上。
试验例5
HES-GNP稳定性的评价,图11是GNP、HES-GNP在不同浓度的氯化钠溶液中的图片,图12是HES-GNP在不同浓度的氯化钠溶液中的紫外吸收光谱。图13是GNP、HES-GNP在氯化钠溶液、磷酸盐缓冲液中的粒径随时间变化曲线。图13中,实心黑点代表粒径,空心圆点代表多分散指数。
前面提到,对于通过柠檬酸钠还原法制备的金纳米粒来说,其在水中能保持稳定的原因是金纳米粒表面存在很多的柠檬酸根,通过电荷之间的互斥作用稳定金纳米粒。当存在一定浓度的电解质离子时,金纳米粒表面的双电层厚度被电解质离子压缩而产生静电屏蔽效应,最终使得金纳米粒丧失稳态而发生聚沉。因此通过检测HES-GNP在高电解质环境下的理化性质就可以反映出HES-GNP的稳定性。
实验药物的配制,首先配制浓度为4mol/L和1mol/L的NaCl浓溶液,之后将浓度为0.5nM的GNP和HES-GNP分散液与前面配制的NaCl 浓溶液以适当比例混合,并且保持总体积一定,这样就可以获得金纳米粒浓度相同,而NaCl浓度不同的一系列液体,在室温下静置1小时后,测量样品的紫外吸收光谱,水合粒径等理化参数。
为了研究HES-GNP长期稳定性,选取浓度为0.8mol/L的NaCl溶液和浓度为0.01mol/L,pH为7.4的磷酸盐缓冲液作为分散介质,之后通过定时测量HES-GNP在两种分散介质中的粒径来反映材料的稳定性。
由图11可知,对于GNP来说,在氯化钠浓度为0.02mol/L时,颜色由原来的酒红色变成了紫色,这说明此时就发生了明显的聚沉现象,金纳米粒丧失稳定性。随着氯化钠浓度继续升高,金纳米粒聚集沉淀的情况就会更加严重。而对于HES-GNP,其形态在不同浓度的氯化钠溶液中均没有发生明显的改变。由图12可知,HES-GNP在不同浓度的氯化钠溶液中的紫外吸收光谱也没有发生显著的改变。由图13可知,在0.8mol/L的NaCl溶液和浓度为0.01mol/L,pH为7.4的磷酸盐缓冲液中,HES-GNP可以保持长期稳定状态而不发生聚沉。
以上结果说明HES-GNP即使在高浓度的电解质溶液中也可以保持稳定,具有很好的物理稳定性。进一步分析,当羟乙基淀粉修饰到金纳米粒表面后,金纳米粒表面的电荷部分被羟乙基淀粉取代。此时,羟乙基淀粉的存在削弱了电荷之间的相互作用,但是却提供了一种新的空间稳定作用。这是由于羟乙基淀粉存在于金纳米粒表面,产生了一种新的空间斥力势能,使金纳米粒之间不会直接碰撞,对胶体的稳定起主要作用。
最后,本发明的方法仅为较佳的实施方案,并非用于限定本发明的保护范围。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!