一种阿洛酮糖的生产工艺的制作方法
本发明属于食品原料加工领域,具体涉及一种阿洛酮糖的生产工艺。
背景技术
d-阿洛酮糖是果糖的一种差向异构体,在自然界存在但含量极少的一种单糖,其甜味和蔗糖类似,但其热量远低于蔗糖,对于肥胖以及糖尿病患者是一种理想的蔗糖代替物;与d-葡萄糖和d-果糖相比,还具有较强的清除活性氧的能力等。
由于d-阿洛酮糖在自然界存在稀少,不适宜工业化大生产,而且化学合成会产生较多副产物,成本高,污染大,并且生物合成技术发展至今较为成熟;生成的产物较为单一。但是目前的生产技术普遍存在产生污染物多,环保压力大,底物转化率低,生产成本高等诸多不利因素。如果能够减少离子交换产生的废水,回收利用昂贵的金属离子,实现循环再反应,必将大大降低生产成本和环境污染。
综上所述,本领域迫切需要开发可有效利用金属离子并循环使用,减少离子交换产生的废水,生成成本低、环境污染污染少的一种生产阿洛酮糖的方法。
技术实现要素:
本发明的目的就是提供可有效利用金属离子并循环使用,减少离子交换产生的废水,生成成本低、环境污染污染少的一种生产阿洛酮糖的方法。
在本发明的第一方面,提供了一种由淀粉生产阿洛酮糖的方法,包括下述步骤:
(1)对淀粉进行液化糖化处理,从而得到含糖化产物的第一混合物,所述糖化产物包括:葡萄糖;
(2)向所述的第一混合物中加入酶促金属离子,形成含酶促金属离子的第一混合物;
(3)对步骤(2)中的含酶促金属离子的第一混合物,进行异构化处理,将葡萄糖异构化为果糖进而异构化为d-阿洛酮糖,从而形成含d-阿洛酮糖的第二混合物;
(4)从所述第二混合物中分离并回收酶促金属离子,并获得除去了酶促金属离子的第三混合物;
(5)对所述第三混合物进行色谱分离,从而得到含d-阿洛酮糖的分离产品;
其中,步骤(4)中回收的酶促金属离子,作为步骤(2)中的酶促金属离子循环使用。
在另一优选例中,所述糖化产物还包括麦芽糖、异麦芽糖、麦芽三糖和/或麦芽四糖。
在另一优选例中,所述方法还包括步骤(6)浓缩步骤(5)中含d-阿洛酮糖的分离产品,得到浓缩的含d-阿洛酮糖的分离产品。
在另一优选例中,步骤(6)采用mvr方式进行蒸发浓缩。
在另一优选例中,所述蒸发浓缩为减压(优选地,真空度为-0.07~-0.1mpa)蒸发浓缩。
在另一优选例中,所述蒸发浓缩的温度为74~76℃。
在另一优选例中,所述方法还包括步骤(7)使步骤(6)中浓缩的含d-阿洛酮糖的分离产品中的d-阿洛酮糖通过结晶(优选地,降温结晶)析出,分离得到d-阿洛酮糖晶体。
在另一优选例中,步骤(5)中,所述的色谱分离为模拟移动床色谱分离。
在另一优选例中,步骤(5)包括步骤:
(5.1)提供所述第三混合物作为进料f;以及
(5.2)色谱分离:通过基于移动床色谱的色谱分离设备对所述含糖混合液进行分离,得到所述含d-阿洛酮糖的分离产品;
所述色谱分离包括:
(5.2.1)进料步骤:将所述的所述第三混合物通入的色谱柱中;
(5.2.2)洗脱步骤:将洗脱液d通入色谱柱中进行洗脱,且所述洗脱液d为水;
(5.2.3)出料步骤:收集出料液,其中,所述出料液包括所述含d-阿洛酮糖的分离产品;
其中,所述色谱分离设备包括2~20个(优选地,包括4~12个;更优选地包括5~10个)所述色谱柱和/或色谱柱段,且所述色谱柱和/或色谱柱段的填料为阳离子树脂,所述的各个色谱柱和/或色谱柱段串联连接。
在另一优选例中,步骤(5.2.1)及步骤(5.2.2)间歇进行;和/或步骤(5.2.3)连续进行。
在另一优选例中,料水比为1:(0.5~3.0);其中,所述料水比为进料f:洗脱液d的质量比;优选地,料水比为1:(0.8~2.5);优选地,为1:(1.0~2.0)。
在另一优选例中,d-阿洛酮糖的分离产品与进料f总量的质量比为(0.9~1.5):1;优选地,(1.0~1.3):1。
在另一优选例中,步骤(5.2.1)中,所述方法的进料的流量为0.002~0.150bv(床体积)/h;优选地,所述方法的进料的流量为0.005~0.10bv/h;更优选地,为0.01~0.05bv/h。
在另一优选例中,步骤(5.2.2)中,洗脱液的流量为0.005~0.375bv(床体积)/h,;优选地,所述方法的进料的流量为0.0125~0.10bv/h;更优选地,为0.025~0.125bv/h。
在另一优选例中,步骤(5.2.3)中,所述出料液的流量为0.002~0.150bv(床体积)/h。
在另一优选例中,步骤(5)中,所述色谱柱和/或色谱柱段的柱温为20~80℃;优选地,为30~70℃;更优选地,为50~65℃。
在另一优选例中,所述的阳离子树脂选自:钙型阳离子树脂、钠型阳离子树脂、钾型阳离子树脂、镁型阳离子树脂、锂型阳离子树脂,或其组合;优选地,为钙型阳离子树脂、镁型阳离子树脂,或其组合。
在另一优选例中,步骤(5)中,所述阳离子树脂的粒径为:50~500um。
在另一优选例中,步骤(5)中,单个所述色谱柱和/或色谱柱段填充的所述阳离子树脂的密度为0.85~0.95g/cm3。
在另一优选例中,步骤(5)中,所述色谱柱的单柱和/或色谱柱段的单段长度为50~200cm;
在另一优选例中,步骤(5)中,所述色谱柱的单柱和/或色谱柱段的单段径高比1/20~1/0.4;优选地,为1/15~1/1。
在另一优选例中,所述方法的色谱柱和/或色谱柱段的切换时间为3~15min;优选地,为5~8min。
在另一优选例中,所述的含d-阿洛酮糖的分离产品中,d-阿洛酮糖的纯度≥95%,以干物质总质量为基准;优选地,纯度为96~99%;更优选地,纯度为98~99%。
在另一优选例中,所述酶促金属离子选自:mn2+、co2+、mg2+、fe2+、ca2+-或其组合;优选地,所述酶促金属离子选自:mn2+、co2+、mg2+、fe2+或其组合;更优选地,所述酶促金属离子为mn2+、co2+或其组合。
在另一优选例中,步骤(4)中,通过下述步骤回收酶促金属离子:
(i)使用离子交换树脂吸附所述第二混合物中的酶促金属离子,得到吸附了酶促金属离子的树脂;其中,所述离子交换树脂为钙型阳离子树脂;
(ii)用含ca2+的水溶液,洗脱所述吸附了酶促金属离子的离子交换树脂,得到回收的酶促金属离子。
在另一优选例中,步骤(ii)中,得到的回收的酶促金属离子是水溶液的形式的回收的酶促金属离子。
在另一优选例中,步骤(ii)中,得到的的回收的酶促金属离子以水溶液形式直接用于步骤(2)中。
在另一优选例中,所述含ca2+的溶液的ca2+浓度为0.1~1.0m。
在另一优选例中,所述含ca2+的溶液中的溶质为cacl2。
在另一优选例中,步骤(ii)中所述离子交换树脂经洗脱后,可继续作为步骤(i)中的离子交换树脂使用。
在另一优选例中,所述的离子交换树脂装填于离子交换柱中,且所述的离子交换柱的填料密度为0.7~1.2g/ml。
在另一优选例中,所述离子交换树脂为钙型阳离子树脂。
在另一优选例中,所述第二混合物以10~30kg/min流过所述离子交换柱。
在另一优选例中,步骤(1)包括下述步骤:
(1.1)将淀粉乳化,得到经乳化的淀粉;
(1.2)将所述经乳化的淀粉在淀粉酶的存在下,经过液化处理,得到液化淀粉;
(1.3)所述的液化淀粉在糖化酶的存在下,经糖化处理,得到含葡萄糖的第一混合物。
在另一优选例中,步骤(1.1)为将所述淀粉加水配制成含25wt%~30wt%淀粉的混合物后进行乳化。
在另一优选例中,所述淀粉酶为a-淀粉酶。
在另一优选例中,步骤(1)具有下述一个或多个特征:
步骤(1.2)中,液化处理的ph为5.5~6.5(优选地ph,为5.8~6.2);
步骤(1.2)中,液化处理温度为100~120℃(优选地,为105~115℃);
步骤(1.2)中,液化处理后的de值为15~25%(优选地为15~20%);
步骤(1.3)中,糖化处理的ph为4.1~4.9;
步骤(1.3)中,糖化处理温度为50~70℃;和/或
步骤(1.3)中,糖化处理后的de值为97~100%。
在另一优选例中,步骤(1)中还包括步骤(1.4)对第一混合物进行浓缩处理,得到经浓缩的第一混合物。
在另一优选例中,未经浓缩的所述第一混合物中干物质的浓度为10~70wt%,较佳地,20~65wt%,更佳地,30~60wt%,所述浓度为总干物质的浓度,以所述第一混合物总质量为基准。
在另一优选例中,所述经浓缩的第一混合物中干物浓度为45~60wt%(优选地,50~60wt%),以所述第一混合物总质量为基准。
在另一优选例中,所述浓缩处理,采用mvr蒸发器进行。
在另一优选例中,所述第一混合物在浓缩前还包括步骤:升温灭活、活性炭脱色、过滤、除去离子蛋白质和/或除去氨基酸。
在另一优选例中,步骤(3)中,所述异构化处理是指,所述含酶促金属离子的第一混合物在葡萄糖异构化酶和果糖异构化酶的存在下,形成含d-阿洛酮糖的第二混合物。
在另一优选例中,所述果糖异构化酶为c-3差向异构酶。
在另一优选例中,所述果糖异构化酶为类芽孢杆菌(paenibacillussenegalensis)的d-阿洛酮糖-3-差向异构酶。
在另一优选例中,所述的c-3差向异构酶选自下组:
(i)氨基酸序列如seqidno.:1所示的多肽;
(ii)将seqidno.:1所示氨基酸序列的多肽经过一个或多个氨基酸残基(较佳地,1-50个,更佳地,1-30个,更佳地,1-10个,最佳地,1-6个)的取代、缺失或添加而形成的、或是添加信号肽序列后形成的、并具有催化产生阿洛酮糖活性的衍生多肽;
(iii)序列中含有(i)或(ii)中所述按氨基酸序列的衍生多肽;
(iv)氨基酸序列与seqidno.:1所示氨基酸序列的同源性≥70%(较佳地≥80%,更佳地≥90%),并具有催化产生阿洛酮糖活性的衍生多肽。
在另一优选例中,所述葡萄糖异构化酶和果糖异构化酶预先固定于反应柱。
在另一优选例中,步骤(3)中,所述异构化处包括步骤:所述含酶促金属离子的第一混合物依次流过固定有葡萄糖异构化酶的反应柱及固定有果糖异构化酶的反应柱。
在另一优选例中,步骤(3)中,所述酶催化的温度为55~65℃。
在另一优选例中,所述含酶促金属离子的第一混合物流过固定有葡萄糖异构化酶的反应柱的流速为10~30kg/min;和/或
流过固定有果糖异构化酶的反应柱的流速为10~30kg/min。
在另一优选例中,在流经不同的反应柱时,流速是相同的或不同的。
在另一优选例中,第一混合物一次流过固定有葡萄糖异构化酶的反应柱及固定有果糖异构化酶的反应柱后直接流过所述离子交换柱得到第三混合液。
在另一优选例中,所述第二混合物和/或所述第三混合物含10~20wt%的阿洛酮糖、30~50wt%的果糖及30~50wt%的葡萄糖,以总干物质质量为基准。
在另一优选例中,步骤(5)中,还能分离得到含果糖和葡萄糖的分离产物;回收所得的含果糖和葡萄糖的分离产物,并用作第一混合物。
在另一优选例中,步骤(5.2.2)中,所述出料还包括含果糖和葡萄糖的分离产物。
在另一优选例中,步骤(5)中回收所得的含果糖和葡萄糖的分离产物经浓缩处理(优选地,mvr浓缩处理)后用作第一混合物。
在另一优选例中,在所述含果糖和葡萄糖的分离产物中,葡萄糖和果糖的总浓度为20~40wt%,优选地,为25~35wt%,以含果糖和葡萄糖的分离产物的质量为基准。
在另一优选例中,所述含果糖和葡萄糖的分离产物包括:40~70wt%的葡萄糖及30~55wt%的果糖,优选地,50~60wt%的葡萄糖及40~50wt%的果糖,以含果糖和葡萄糖的分离产物中干物质总质量为基准。
在另一优选例中,还包括步骤:对所述含果糖和葡萄糖的分离产物进行浓缩处理。
在另一优选例中,所述的浓缩处理为通过mvr进行浓缩处理。
在另一优选例中,所述经浓缩的含果糖和葡萄糖的分离产物中果糖和葡萄糖的总浓度为30~60wt%,以含果糖和葡萄糖的分离产物的总质量计。
在另一优选例中,在第一混合物中,葡萄糖的含量≥70%,较佳地≥80%,更佳地≥90%,最佳地≥95%,按所述第一混合物中干物质的总质量计。
在另一优选例中,所述第一混合物包含90~99wt%的葡萄糖,优选地,包含95~99wt%的葡萄糖,以第一混合物中干物质总质量为基准。
在另一优选例中,所述第二混合物的糖类物质的总浓度为30~68wt%(优选地,为50~65wt%),以第二混合物的总质量为基准。
在另一优选例中,所述第二混合物中阿洛酮糖纯度大于5wt%,优选地,大于11wt%;更优选地,大于14wt%,以第二混合物中干物质总质量为基准。
在另一优选例中,所述第二混合物包括:阿洛酮糖、葡萄糖、果糖、及低聚糖(包括二糖),以第二混合物中干物质总质量为基准。
在另一优选例中,所述方法中,阿洛酮糖的转化率为60~85g阿洛酮糖/100g淀粉(算上葡萄糖果糖再利用)。
在另一优选例中,在步骤(a)中,所述的原料淀粉的量为0.1~2.0吨。
在另一优选例中,所述的方法的d-阿洛酮糖的生产量为100~1500kg/天;优选地,为100~750kg/天;更优选地,为200~500kg/天。
应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
附图说明
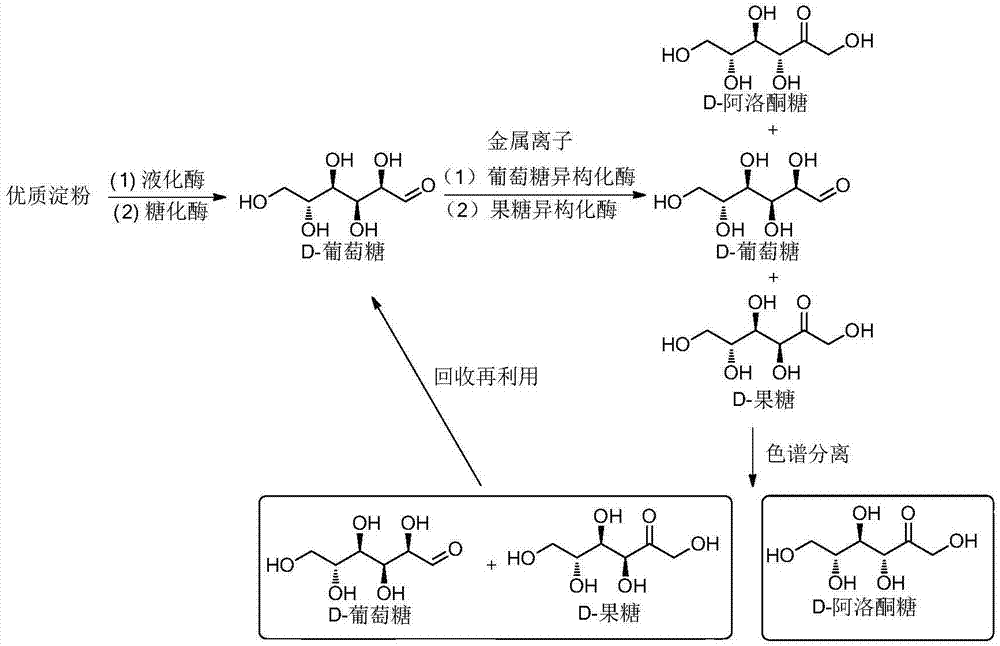
图1为本发明方法的反应流程图。
图2为本发明方法的工艺流程图。
图3为本发明方法的所得混合液的液相色谱图。
图4为本发明的色谱分离流程示意图。
具体实施方式
发明人经过广泛而深入地研究,开发了一种独特的阿洛酮糖的生产方法。本方法通过循环利用各种原料等(例如,循环利用催化用离子和循环利用分离阿洛酮糖后剩余的含糖溶液等)使本发明的生成方法污染减少,成本降低,产能提高,从而实现环保和高效生产阿洛酮糖。基于此发明人完成了本发明。
术语
如本文所用“de值”又称“葡萄糖值”,是指糖化液中还原糖全部以葡萄糖计所占干物质的百分比;de值=还原糖含量/干物质含量*100%,其中,还原糖含量(g/100ml糖化液)指100ml糖化液中还原糖的质量,干物质含量(g/100g)指100g糖化液中含有干物质的质量。
如本文所用“淀粉酶”是指能水解淀粉、糖原和有关多糖中的o-葡萄糖键的酶(例如,α-淀粉),其作用于淀粉时从淀粉分子内部以随机的方式切断α-1,4糖苷键。
如本文所用术语“糖化酶”,又称葡萄糖淀粉酶[glucoamylase,ec.3.2.1.3.],这种酶能把淀粉从非还原性未端水解a-1.4葡萄糖苷键产生葡萄糖,也能缓慢水解a-1.6葡萄糖苷键,转化为葡萄糖的酶。同时也能水解糊精,糖原的非还原末端释放β-d-葡萄糖。
如本文所用果糖异构化酶为c-3差相异构酶。
如本文所用,“c-3差相异构酶”和“d-阿洛酮糖-3-差向异构酶”可互换使用,指可高效催化产生阿洛酮糖的酶。例如在本发明中使用的果糖异构化酶为seqidno.:1所示的蛋白(即野生型d-阿洛酮糖-3-差向异构酶)或其衍生蛋白(例如,seqidno.:2所示的突变型d-阿洛酮糖-3-差向异构酶),所示果糖异构化酶来自类芽孢杆菌(paenibacillussenegalensis)。本领域技术人员还应明白“c-3差相异构酶”还应包括所述蛋白的变异形式,所述变异形式具有与“本发明的c-3差相异构酶”相同或相似的功能,但其氨基酸序列与野生型c-3差相异构酶所示氨基酸序列有少量差异。这些变异形式包括(但不限于):一个或多个(通常为1-50个,较佳地1-30个,更佳地1-20个,最佳地1-10个,还更佳如1-8个、1-6个)氨基酸的缺失、插入和/或取代,以及在c末端和/或n末端添加一个或多个(通常为20个以内,较佳地为10个以内,更佳地为6个以内)氨基酸。例如,本领域技术人员熟知,用性能相近或相似的氨基酸进行取代时,通常不会改变蛋白质的功能。又比如,在c末端和/或n末端添加一个或数个氨基酸通常也不会改变蛋白质的功能。该术语还包括c-3差相异构酶的活性片段和活性衍生物。多肽的变异形式包括:同源序列、保守性变异体、等位变异体、天然突变体、诱导突变体、在高或低的严格性条件下能与“本发明的d-阿洛酮糖-3-差向异构酶”的编码dna杂交的dna所编码的蛋白。本发明还包括其他多肽,如包含“本发明的d-阿洛酮糖-3-差向异构酶”或其片段的融合蛋白。除了几乎全长的多肽外,本发明还应包括“本发明的d-阿洛酮糖-3-差向异构酶”的活性片段。通常,该片段具有“本发明的d-阿洛酮糖-3-差向异构酶”的氨基酸序列的至少约10个连续氨基酸,通常至少约30个连续氨基酸,较佳地至少约50个连续氨基酸,更佳地至少约80个连续氨基酸,最佳地至少约100个连续氨基酸。本发明还提供“d-阿洛酮糖-3-差向异构酶”的类似物。这些类似物与天然“本发明的d-阿洛酮糖-3-差向异构酶”的差别可以是氨基酸序列上的差异,也可以是不影响序列的修饰形式上的差异,或者兼而有之。这些多肽包括天然或诱导的遗传变异体。诱导变异体可以通过各种技术得到,如通过辐射或暴露于诱变剂而产生随机诱变,还可通过定点诱变法或其他已知分子生物学的技术。类似物还包括具有不同于天然l-氨基酸的残基(如d-氨基酸)的类似物,以及具有非天然存在的或合成的氨基酸(如β、γ-氨基酸)的类似物。应理解,本发明的蛋白并不限于上述例举的代表性蛋白。修饰(通常不改变一级结构)形式包括:体内或体外的多肽的化学衍生形式如乙酰化或羧基化。修饰还包括糖基化。修饰形式还包括具有磷酸化氨基酸残基(如磷酸酪氨酸,磷酸丝氨酸,磷酸苏氨酸)的序列。还包括被修饰从而提高了其抗蛋白水解性能或优化了溶解性能的蛋白。在本发明中,“d-阿洛酮糖-3-差向异构酶”的保守性变异多肽指与野生型d-阿洛酮糖-3-差向异构酶所示氨基酸序列相比,有至多20个,较佳地至多10个,更佳地至多5个,最佳地至多3个氨基酸被性质相似或相近的氨基酸所替换而形成多肽,但所述保守性变异多肽依然具有与氨基酸序列如seqidno:1所示蛋白相同或相似的活性,即,催化产生阿洛酮糖的活性。因此,鉴于本发明的教导和现有技术,本领域技术人员可根据,例如下表所示进行氨基酸替换而产生保守性变异的突变体。
因此,本文所用的“含有”,“具有”或“包括”包括了“包含”、“主要由……构成”、“基本上由……构成”、和“由……构成”;“主要由……构成”、“基本上由……构成”和“由……构成”属于“含有”、“具有”或“包括”的下位概念。本发明的蛋白可以是重组蛋白、天然蛋白、合成蛋白,优选重组蛋白。本发明的蛋白可以是天然纯化的产物,或是化学合成的产物,或使用重组技术从原核或真核宿主(例如,细菌、酵母、高等植物、昆虫和哺乳动物细胞)中产生。根据重组生产方案所用的宿主,本发明的蛋白可以是糖基化的,或可以是非糖基化的。本发明的蛋白还可包括或不包括起始的甲硫氨酸残基。本领域技术人员明白,本发明的“d-阿洛酮糖-3-差向异构酶”还包括“d-阿洛酮糖-3-差向异构酶”的片段、衍生物和类似物。如本文所用,术语“片段”、“衍生物”和“类似物”是指基本上保持本发明的“d-阿洛酮糖-3-差向异构酶”相同的生物学功能或活性的多肽。本发明的多肽片段、衍生物或类似物可以是(i)有一个或多个保守或非保守性氨基酸残基(优选保守性氨基酸残基)被取代的多肽,而这样的取代的氨基酸残基可以是也可以不是由遗传密码编码的,或(ii)在一个或多个氨基酸残基中具有取代基团的多肽,或(iii)成熟多肽与另一个化合物(比如延长多肽半衰期的化合物,例如聚乙二醇)融合所形成的多肽,或(iv)附加的氨基酸序列融合到此多肽序列而形成的多肽(如前导序列或分泌序列或用来纯化此多肽的序列或蛋白原序列,或融合蛋白)。根据本文的定义这些片段、衍生物和类似物属于本领域熟练技术人员公知的范围。鉴于本领域现有技术和本发明的教导,本领域技术人员不难获得本发明d-阿洛酮糖-3-差向异构酶的活性片段。因此,任何一种“d-阿洛酮糖-3-差向异构酶”的生物活性片段都可以应用于本发明。在本文中,“d-阿洛酮糖-3-差向异构酶”的生物活性片段是指“d-阿洛酮糖-3-差向异构酶”的片段,但其仍然能保持全长“d-阿洛酮糖-3-差向异构酶”的全部或部分功能。通常情况下,所述的生物活性片段至少保持全长“d-阿洛酮糖-3-差向异构酶”的50%的活性。在更优选的条件下,所述活性片段能够保持全长“d-阿洛酮糖-3-差向异构酶”的60%、70%、80%、90%、95%、99%、或100%的活性。基于本发明的教导和现有技术,本领域技术人员还可以明白,可以将d-阿洛酮糖-3-差向异构酶制成固定化酶等其它利用形式。
如本文所用,术语“干物质”是指混合物中除水以外的组分,在本发明中主要为糖类物质。
如本文所用,术语“浓度”是指特定物质重量占溶液总重量的百分比,例如,阿洛酮糖的浓度为阿洛酮糖重量/溶液总重量*100%。
如本文所用,术语“纯度”是指特定物质重量占除水以外物质总重量的百分比,例如,阿洛酮糖的纯度为阿洛酮糖重量/溶液中干物质的重量*100%。
如本文所用,术语“糖类物质”由c、h、o三种元素组成的分子化合物,在本申请中所述糖类物质为阿洛酮糖、果糖、葡萄糖等。
如本文所用,术语“重量比”在一定时间段内或者分离一定量的物料时各物质之间的平均重量比。
如本文所用,术语“酶活”是指每分钟转化为1umol相对应产品的酶量,为1u。
如本文所用,术语“mvr”是指机械式蒸汽再压缩蒸发器。
为了克服这些不利因素,本发明提供可了一整套高效、环保的生产工艺。
本发明提供一种高效环保生物催化转化阿洛酮糖的生产工艺(如图1所示)。利用廉价的优质淀粉转化为葡萄糖(例如,依次用淀粉液化酶、糖化酶,将淀粉转化为葡萄糖),经葡萄糖异构化酶和果糖异构化酶催化转化生成阿洛酮糖(优选地,阿洛酮糖经过离子交换去除多余的金属离子,然后经过色谱分离纯化得到阿洛酮糖纯品)。本工艺采用循环利用技术,减少污染,降低成本,提高产能,从而达到环保和高效生产阿洛酮糖。
本发明利用传统的淀粉制糖技术生产葡萄糖,经生物酶催化进一步转化为阿洛酮糖,该过程用到金属离子(即酶促金属离子)mn2+、co2+、mg2+、fe2+和ca2+中的一种或几种促进酶的催化效率,并使酶的稳定性得到提高,延长酶的使用寿命;在纯化阿洛酮糖的过程中,需要分离或回收这些金属离子、和中间体与原料,便于循环再使用,从而避免这些金属离子、中间体及原料的遗弃对环境的污染。回收金属离子的过程,采用廉价的离子交换树脂(如钙型阳离子树脂),用氯化钙水溶液洗脱和回收反应中用到的金属离子,回收的金属离子在生物催化过程中,重复使用,避免了传统的阴阳离子法中既要用强碱又要用强酸的过程,减少了树脂的用量和大量的废酸废碱;回收中间体和原料的过程,采用色谱分离和减压浓缩相结合的系统,经固定化的葡萄糖异构化酶和果糖异构化(例如,葡萄糖异构化酶和果糖异构化酶均使用固定化酶,并装在带夹套的反应柱内使用)酶反复转化,经多次(如10次及以上)循环转化,葡萄糖转化率可以达到75%以上,从而大大提高生产效率。
在另一优选例中,所述工艺,所用到的a淀粉酶、糖化酶、葡萄糖异构化酶和果糖异构化酶可以商业采购,也可以自行生产。
在另一优选例中,所述工艺,生物酶催化反应过程中,加入催化量的金属离子mn2+、co2+、mg2+、fe2+和ca2+中的一种或几种,以提高转化效率和提高固定化酶的稳定性。
在另一优选例中,所述工艺,优质淀粉依次用淀粉液化酶、糖化酶、葡萄糖异构化酶和果糖异构化酶生物催化转化之后,得到葡萄糖、果糖和阿洛酮糖的混合液(即第二混合物)。
在另一优选例中,所得混合液(即第二混合物)包含有金属离子mn2+、co2+、mg2+、fe2+和ca2+中的一种或几种。
在另一优选例中,所述工艺,所得葡萄糖、果糖和阿洛酮糖的混合液(即第二混合物)在进行色谱分离前,用钙型阳离子树脂回收添加的金属离子,再循环利用。
在另一优选例中,所述工艺,所用色谱分离填料为阳离子树脂(例如钙型树脂),分离得到的阿洛酮糖水溶液经过减压浓缩,得到高纯度的阿洛酮糖,纯度在98%以上。
在另一优选例中,经色谱分离得到的葡萄糖和阿洛酮糖溶液(即含果糖和葡萄糖的分离产物),经过减压浓缩后做为葡萄糖异构化和果糖异构化的原料再使用。
在另一优选例中,所回收金属离子返回前述葡萄糖异构化和果糖异构化生物催化过程。
在另一优选例中,所用钙型阳离子树脂,用氯化钙水溶液洗脱回收添加的金属离子后,再重复使用。
在另一优选例中,葡萄糖和果糖的异构化以及进一步的纯化分离采用串联循环反应器。
下面结合工艺流程图(如图2所示),对本发明做进一步说明。
第一步:制备葡萄糖溶液(即第一混合物)
把优质淀粉按25~30%的进行乳化,用na2co3调节ph=6.0±0.2,加入a~淀粉酶调浆均匀后,控制温度(110±5℃)进行喷射液化,液化de值控制在15%~20%。然后将液化液冷却至60℃附近,调节ph值为4.5左右,加人糖化酶,进行保温糖化(例如50~70℃下糖化),反应到所需de值(例如,97~100%)时,升温灭酶,加入活性炭吸附过滤,用树脂脱除盐和氨基酸后,经mvr浓缩(浓缩得到的水可作为洗脱剂用于第三步的色谱分离)得到一定浓度的葡萄糖溶液,加入催化量的金属离子mn2+、co2+、mg2+、fe2+中的一种或几种,即可进入下一步转化。
第二步:葡萄糖的异构化(即得到第二混合物或第三混合物的步骤)
将第一步所得到的含金属离子的葡萄糖溶液(即第一混合物)保温60±5度,同时把固定好的葡萄糖异构化酶和果糖异构化酶预热并保温60±5度,把第一步所得到的葡萄糖溶液以一定的速度(例如,10~30kg/min)依次通过葡萄糖异构化酶、果糖异构化酶和钙型阳离子树脂,所得反应转化溶液包含有葡萄糖、果糖和阿洛酮糖。
第三步:色谱分离
把第二步所得反应转化液(已去除第一步中加入的金属离子)利用模拟移动床进行色谱分离,色谱柱的填料采用钙型树脂,控制一定的料水比,进行纯化分离,可以得到两份溶液:第一份,阿洛酮糖的水溶液(即含d-阿洛酮糖的分离产品),纯度在98%以上;第二份,含有葡萄糖和果糖的水溶液(即含果糖和葡萄糖的分离产物),糖度为20~30%,(葡萄糖及果糖的总浓度约为20~30%)。
具体地,采用4~8个装有专用色谱分离树脂并用氯化钙再生好的柱子,流程如图4所示,以4柱为例。
如图4所示,出料连续进行,进行间歇性进料(进料间隔时间比如30~60min,与树脂的量和填充密度等有关)和洗脱(洗脱间隔时间比如30~60min,与树脂的量和填充密度等有关),分别收集快组分(主要成分是阿洛酮糖,即含d-阿洛酮糖的分离产品)和慢组分(主要成分是葡萄糖和果糖,即含果糖和葡萄糖的分离产物)。
具体地,4个色谱柱串联连接,流动相依次流过(流速为0.002~0.150bv/h)这4个色谱柱,同时色谱柱可向流动相流动方向移动。
首先进料(进料流量0.002~0.150bv/h),进料0.01~0.02bv后进水洗脱,且通过移动色谱柱来使进水点(加入洗脱剂的位置)位于快组分出料位置和慢组分出料位置之间,色谱柱的切换时间t为5~8min。其中,所述切换时间是指,色谱柱在某一位置,在t时间时,色谱柱开始沿流动相流动方向移动并移动到流动相流动方向上下一个位置;例如,如图1所示,某一色谱柱移动到色谱柱1位置后,再经过t时间后,该色谱柱由色谱柱1位置快速移动到了图中色谱柱2的位置。
在另一优选例中,所述色谱分离方法的料水比(物料质量:洗脱水的质量)为1:(1.5~3)、快组分/慢组分(阿洛酮糖溶液)为(2~3):1。
例如,色谱条件可以为:
进料f=0.4kg/h(与树脂量有关)、洗脱剂d=0.6kg/h、出料ad(慢组分,阿洛酮糖的水溶液)=0.33kg/h、bd(快组分,含有葡萄糖和果糖的水溶液)=0.66kg/h、处理量0.03kg料液/kg树脂、料水比1:1.5、bd/ad=2;
瞬时操作条件:f→b=33ml/min(进料时快组分出料)、d→a(洗脱时慢组分出料)=33ml/min、循环量(与切换时间成反比)r=33ml/min、d→b(洗脱时快组分出料)=33ml/min。
第四步:阿洛酮糖的结晶纯化
阿洛酮糖溶液经过浓缩后(浓缩得到的水可作为洗脱剂用于第三步的色谱分离)梯度降温析晶,离心过滤即可得到阿洛酮糖的白色结晶,纯度在99%以上。
第五步:金属离子的回收利用
经葡萄糖异构化酶和果糖异构化酶转化的反应液(即第二步中反应转化溶液,即第二混合物)用钙型阳离子树脂处理后,所添加的金属离子被交换吸附在阳离子树脂上,当有金属离子从流出液被检测到时,钙型树脂已被交换完成,更换备用树脂;将已用树脂用氯化钙洗脱,可以富集回收被吸附的金属离子。把该回收离子加入第三步所得葡萄糖和果糖溶液或加入第一步得到的葡萄糖溶液,即可进入循环再转化。
第六步:回收葡萄糖和果糖溶液的再利用
往第五步所得葡萄糖和果糖溶液中加入一定量的葡萄糖溶液,经过预热之后,即可进入生物酶催化转化的工序,即回到第二步的生物催化转化。
在另一优选例中,回收葡萄糖和果糖溶液的再利用3~20次,优选地,5~15次,更优选地,8~12次。
本发明的主要优点包括:
(a)本发明方法中的金属离子可以循环使用;
(b)未转化的的葡萄糖和果糖经色谱分离后可以循环再转化;
(c)减压浓缩得到的水用于淀粉液化和色谱分离。
(d)本发明产率高。
(e)本发明采用循环利用技术,减少污染,降低成本,提高产能,并环保和高效生产阿洛酮糖。
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(newyork:coldspringharborlaboratorypress,1989)中所述的条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数是重量百分比和重量份数。
实施例中所用的葡萄糖异构酶、淀粉酶和糖化酶购自诺维信。
实施例中所用的果糖异构化酶为c-3差向异构酶,其序列如seqidno.:2所示。
实施例1.1
(1)把500kg优质淀粉用1200kg去离子水进行乳化,用十水碳酸钠调节ph到6.0,加入耐高温的a-淀粉酶水溶液20kg,均匀调浆后在110摄氏度喷射液化,液化de值约为18%;经过冷却降温,在60摄氏度,调节ph到4.5;加入糖化酶开始保温糖化,反应的de值达到97时,终止糖化,升温灭酶;在80度,加入活性炭,搅拌半小时后,经板框过滤得到葡萄糖溶液,依次经阳离子交换树脂和阴离子交换树脂处理,除去残余的离子、蛋白质和氨基酸,得到浓度约为25%的葡萄糖溶液;
(2)把25wt%的葡萄糖溶液利用mvr蒸发器浓缩至55wt%,加入coso4.7h2o,co2+浓度为1mm(即co2+在葡萄糖溶液中的浓度为1mm),预热并保温在60度,以20kg/min的速度自下至上流经控温60摄氏度的葡萄糖异构化酶和果糖异构化酶,然后再自上而下流经钙型阳离子树脂,去除金属离子co2+,得到阿洛酮糖、果糖和葡萄糖的混合溶液,三者的比例为15.3/40.9/43.8;用示差检测器检测的液相图谱如图3所示,自左至右三个主要的峰依次是葡萄糖、果糖和阿洛酮糖。
(3)阿洛酮糖、果糖和葡萄糖的混合溶液用模拟移动床进行色谱分离(使用专用钙型阳离子树脂树脂),得到纯度大于98%的阿洛酮糖溶液和葡萄糖与果糖的混合溶液。经减压浓缩得到80%的阿洛酮糖浓缩液,梯度降温析晶之后得到纯度大于99%阿洛酮糖晶体。得到阿洛酮糖晶体37.5kg,单程收率约为7.5%(以重量计算)
实施例1.2
在实施例1中,当钙型阳离子树脂被co2+交换吸附饱和后,用10wt%cacl2水溶液进行洗脱,收集co2+溶液,返回实施例1再利用;钙型树脂再循环使用。经测试,co2+离子回收率95%。
实施例1.3
在实施例1中,色谱分离的得到的葡萄糖和果糖的混合水溶液(浓度27%)经减压浓缩至糖度达到55%,与新生产的葡萄糖溶液混合,加入回收的co2+预热保温在60摄氏度,即可进入新的催化循环反应。
重复实施例1.1及实施例1.3的步骤10次。循环利用产生并分离得到葡萄糖和果糖的混合水溶液
整体循环利用后,淀粉转化为d-阿洛酮糖的转化率为85%,产率为80%,即500kg淀粉能产生了约400kg阿洛酮糖。
实施例2.1
过程基本同实施例1.1,其中将步骤(2)
其中,将coso4.7h2o换为mnso4.h2o
得到阿洛酮糖晶体35kg,单程收率约为7.0%(以重量计算)。
实施例2.2
过程基本同实施例1.2,其中,回收co2+改为回收mn2+。
经测试,mn2+离子回收率85%。
实施例2.3
过程基本同实施例1.3。
重复实施例2.1及实施例2.3的步骤10次。循环利用产生并分离得到葡萄糖和果糖的混合水溶液。
整体循环利用后,淀粉转化为d-阿洛酮糖的转化率为95%,产率为76%,即500kg淀粉能产生了约380kg阿洛酮糖
在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
序列表
<110>上海立足生物科技有限公司
<120>一种阿洛酮糖的生产工艺
<130>p2016-1250
<160>2
<170>patentinversion3.5
<210>1
<211>292
<212>prt
<213>类芽孢杆菌(paenibacillussenegalensis)
<400>1
metlyspheglythrtyrphealatyrtrpgluglnsertrpaspthr
151015
asptyrleulystyrvallyslysvalalaaspleuglypheaspval
202530
leugluvalglyalaalaglyilevalasnmetseraspaspalaleu
354045
seralaleulysserglualagluasntyralailethrleuthrala
505560
glyileglyleuprolysglnpheaspvalsersergluasngluser
65707580
valargglnaspglyilealaphemetlyslysileleuaspalaleu
859095
hislysalaglyilelysalaileglyglythriletyrsertyrtrp
100105110
provalasptyrseralaproileasnlysproalavalarglysgln
115120125
serilelyssermetglngluleualaasptyralaalaglntyrasp
130135140
ilethrleuleuvalgluserleuasnargphegluglnpheleuval
145150155160
asnaspalalysglualavalasptyrvallysalavalasnlyspro
165170175
asnvallysvalmetleuaspserphehismetasnileglugluasp
180185190
tyrleuglyaspalaileargtyrthrglyasptyrleuglyhisphe
195200205
hisileglyglucysasnarglysvalproglylysglyhismetpro
210215220
trpsergluileglyglnalaleuargaspileglntyraspglycys
225230235240
valvalmetgluprophevalargproglyglyilevalglyserasp
245250255
ilelysvaltrpargaspleuseraspasnalaaspglualalysleu
260265270
aspalaaspilelysgluserleugluphevallysglnthrpheleu
275280285
lysserthrpro
290
<210>2
<211>292
<212>prt
<213>人工序列(artificialsequence)
<400>2
metlyspheglythrtyrphealatyrtrpgluglnsertrpaspthr
151015
asptyrleulystyrvallyslysvalalaaspleuglypheaspval
202530
leugluvalglyalaalaglyilevalasnmetseraspaspalaleu
354045
seralaleulysserglualagluasntyralailethrleuthrala
505560
glyileglyleuprolysglnpheaspvalsersergluasngluser
65707580
valargglnaspglyilealaphemetlyslysileleuaspalaleu
859095
hislysalaglyilelysalaileglyglythriletyrsertyrtrp
100105110
provalasptyrseralaproileasnalaproalavalarglysgln
115120125
serilelyssermetglngluleualaasptyralaalaglntyrasp
130135140
ilethrleuleuvalgluserleuasnargphegluglnpheleuval
145150155160
asnaspalalysglualavalasptyrvallysalavalasnlyspro
165170175
asnvallysvalmetleuaspserphehismetasnileglugluasp
180185190
tyrleuproaspalaileargtyrthrglyasptyrleuglyhisphe
195200205
hisileglyglucysasnarglysvalproglylysglyhismetpro
210215220
trpsergluileglyglnalaleuargaspileglntyraspglycys
225230235240
valvalmetgluprophevalargproglyglyilevalglyserasp
245250255
ilelysvaltrpargaspleuseraspasnalaaspglualalysleu
260265270
aspalaaspilelysgluserleugluphevallysglnthrpheleu
275280285
lysserthrpro
290
- 还没有人留言评论。精彩留言会获得点赞!