一种脐带间充质干细胞复合外泌体及其制备方法与流程
本发明涉及干细胞技术领域,更具体地,涉及一种脐带间充质干细胞复合外泌体及其制备方法。
背景技术:
脐带间充质干细胞分离于新生儿出生后的废弃组织-脐带。因其来源广泛,易获取、无伦理性争议、免疫原性低、对供者无伤害等优势,现已成为最具有转化应用前景的间充质干细胞。脐带间充质干细胞可用于治疗糖尿病足,中枢神经损伤,风湿性关节炎,红斑狼疮等疾病。间充质干细胞具有的多种生物学功能在临床上得到了广泛的关注,其治疗机制成为近年干细胞领域相关研究的热点。外泌体被认为是间充质干细胞发挥旁分泌作用的载体,通过将分子包裹在膜内,外泌体可以保护酶或者rna免于降解,并通过细胞内吞作用来促进细胞内摄取。此外,外泌体是一种纳米大小的颗粒,易于在血液以及其他体液中转移。
目前大量研究表明,间充质干细胞来源的外泌体可以通过其内容的蛋白、rna成分胞间转移,发挥与间充质干细胞相类似的组织修复、免疫抑制、调节免疫功能等作用。然而与间充质干细胞相比,间充质干细胞外泌体还具有以下优势:
1、间充质干细胞外泌体没有细胞的活性,并且不存在形成肿瘤的风险。此外,由于膜结合蛋白含量较低,外泌体的免疫原性低于间充质干细胞。
2、间充质干细胞外泌体对维持细胞内稳态以及对外界刺激作出反应起到了重要的作用。当组织微环境稳态因疾病或损伤而遭到破坏时,这种作用就显得更加重要了。
3、间充质干细胞外泌体富含生物活性分子,如蛋白质和rna。存在于外泌体中的许多蛋白质都属于酶类,具有催化活性,并且这些活性与所处的环境有关,如底物浓度和ph。因而,若用于治疗,外泌体中的酶也许可以缓解药物剂量不足或过量的问题。
除此之外,间充质干细胞来源的外泌体性质更稳定,保存运输方便,因此间充质干细胞外泌体有望成为一种新的皮肤修复治疗策略。然而现有脐带间充质干细胞外泌体在修复皮肤真皮层时效果不佳,在疾病治疗领域的针对性不强。
技术实现要素:
针对现有技术中存在的技术问题,本发明提出了一种脐带间充质干细胞复合外泌体及其制备方法,该方法将具有促进人血管内皮细胞增殖、迁移和血管生成功能的mir-181b包载于人脐带间充质干细胞外泌体内形成复合外泌体,使形成的复合外泌体的治疗针对性更强,该方法简单易行,包载成功率高。
为实现上述目的,本发明是通过以下技术方案实现的:
本发明的第一个目的在于提出一种脐带间充质干细胞复合外泌体,所述复合外泌体为内部包载有mir-181b的脐带间充质干细胞外泌体。
本发明的第二个目的在于提出一种脐带间充质干细胞复合外泌体的制备方法,该制备方法用于制备上述的复合外泌体,包括如下步骤:
(1)人脐带间充质干细胞的培养;
(2)人脐带间充质干细胞外泌体提取、纯化;
(3)合成mir-181b;
(4)电穿孔mir-181b包载于步骤(1)中纯化的脐带间充质干细胞外泌体获取复合外泌体样品;
(5)复合外泌体样品进行膜修复;
(6)复合外泌体的抽取、纯化与保存。
进一步地,所述步骤(1)人脐带间充质干细胞的培养,具体操作是:取生长良好的人脐带间充质干细胞,用dmem/f12培养液进行细胞计数,达到106/ml后原代培养,按5×106cells/ml接种到t75细胞培养瓶,置于co2体积浓度为5%的37℃培养箱中培养,细胞达80%融合时,用质量浓度0.25%胰酶于37℃下消化,以1×104cells/ml传代扩增,取p2~p5代的人脐带间充质干细胞;p2~p5代的人脐带间充质干细胞置于o2体积比浓度为21%的37℃培养箱中,用dmem/f12培养液进行培养,直到细胞达70%融合时,改用无血清的饥饿培养液,培养12h,将无血清的饥饿培养液换为含有10ng/ml表皮细胞生长因子的dmem/f12培养液,培养至细胞处于对数生长期,收集细胞培养上清液。
进一步地,所述步骤(4)的方法为:向1ml含50mm海藻糖的磷酸缓冲盐溶液中分别加入步骤(2)纯化的脐带间充质干细胞外泌体和步骤(3)合成的mir-181b,均匀混合形成混合反应液,混合反应液加入穿孔皿中进行电穿孔;所述混合反应液包括脐带间充质干细胞外泌体100μg~300ug、mir-181b5~20μl。
更进一步地,所述步骤(4)中电穿孔的穿孔条件为:电压100v、电容125μf、放电时间1ms、放电次数为1次。
进一步地,所述步骤(6)的方法为:复合外泌体样品经10万~14万g(rcf)离心力超速离心两次,每次70~90min,弃尽上清,沉淀物即为同时负载mir-181b的复合外泌体,复合外泌体-80℃保存备用。
与现有技术相比,本发明的有益效果在于:
(1)本发明将mir-181b包载于人脐带间充质干细胞外泌体,充分结合了人脐带间充质干细胞外泌体具有的组织修复功能和mir-181具有的促进人血管内皮细胞的增殖、迁移和血管生成功能,通过电穿将mir-181包载于人脐带间充质干细胞外泌体内,该复合外泌体的治疗针对性更强。该方法简单易行,包载成功率高该方法简单易行,成功率高。
(2)脐带间充质干细胞取材方便,无道德伦理争议,可获取的细胞数量多、活力强,便于扩增和传代,同时又没有配型、排异等问题,极其适合于临床研究和应用。
(3)本发明制备的复合外泌体在发挥治疗的作用的基础上,为临床应用研究提供可靠的实验研究数据及理论基础。
附图说明
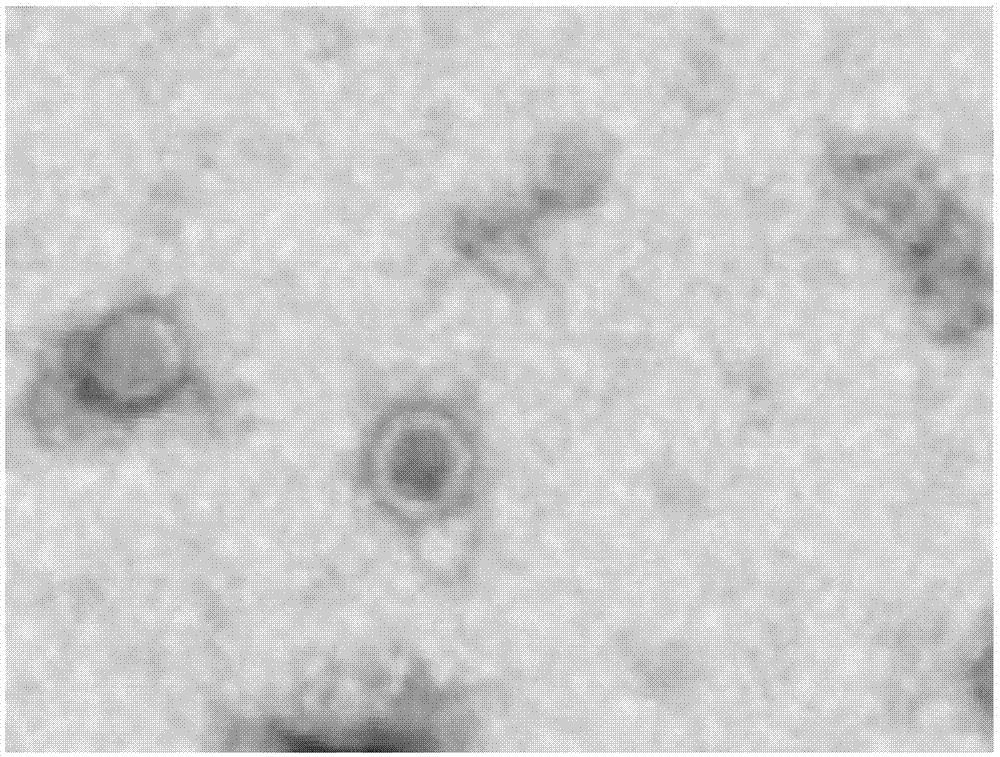
图1为实施例1中穿孔前的脐带间充质干细胞外泌体的电镜照片。
图2为实施例1中穿孔后的脐带间充质干细胞外泌体的电镜照片。
图3为实施例3中westernblotcd81、cd63鉴定复合外泌体蛋白。
具体实施方式
展示一下实例来具体说明本发明的某些实施例,且不应解释为限制本发明的范围。对本发明公开的内容可以同时从材料、方法和反应条件进行改进,所有这些改进,均应落入本发明的的精神和范围之内。本发明所用试剂和原料均市售可得或可按文献方法制备。下列实施例中未注明具体条件的实验方法,通常按照工具书(著[美]j.莎姆布鲁克,黄培堂译,《分子克隆实验指南》,科学出版社)中所述的条件,或按照制造厂商所建议的条件。
实施例1:复合外泌体的制备
一、人脐带间充质干细胞外泌体的制备
配制dmem/f12培养液,培养液含质量浓度20%fbs、100u/ml青霉素和100μg/ml链霉素。
将脐带用75%乙醇浸泡4min,pbs浸泡清洗3次,剔除血管后剪成1cm2小块,浸没于质量浓度0.1%的ⅱ型胶原酶,37℃消化50分钟,加入0.25%胰酶,37℃消化10分钟,加入血清终止胰酶消化,将前述细胞组织液过滤,离心,弃去上层清液,取下层细胞。
将下层细胞加dmem/f12培养液进行细胞计数,达到106/ml后原代培养,按5×106cells/ml接种到t75细胞培养瓶,每个细胞培养瓶中dmem/f12培养液体积为20ml,置于co2体积比浓度5%的37℃培养箱中培养,3d后换液去除非贴壁细胞,以后每4d半量换液1次,10d时细胞达80%融合时,用质量浓度0.25%胰酶于37℃下消化,以1×104cells/ml传代扩增,取p2~p5代的人脐带间充质干细胞。
p2代的人脐带间充质干细胞置于o2体积比浓度为21%的37℃培养箱中,用dmem/f12培养液进行培养,直到细胞达70%融合时,改用无血清的饥饿培养液,培养12h,将无血清的饥饿培养液换为含有10ng/ml表皮细胞生长因子的dmem/f12培养液,培养至细胞处于对数生长期,收集细胞培养上清液300g~10000g梯度离心60-120min,沉底得到的外泌体重悬于含50mm海藻糖的pbs溶液中,-80℃保存备用。
二、合成mir-181b
查找序列信息
>hsa-mir-181b-5pmimat0000257aacauucauugcugucggugggu,
>hsa-mir-181b-3pmimat0022692cucacugaacaaugaaugcaa。
由上海吉玛制药技术有限公司合成合成mir-181b并pcr富集。
三、电穿孔获取复合外泌体样品
按下列比例,将1ml含50mm海藻糖的磷酸缓冲盐溶液中分别加入纯化的脐带间充质干细胞外泌体和合成的mir-181b,均匀混合形成混合反应液,混合反应液加入穿孔皿中采用invitrogen公司neon电穿孔仪,100v、电容125μf、1ms条件下1次脉冲完成电穿孔包载;所述混合反应液包括脐带间充质干细胞外泌体100μg~300ug、mir-181b5~20μl。穿孔后立即取样,在紫外-可见光分光光度计上检测样品在260nm处的吸光值,并与未穿孔样品对比,判断穿孔是否成功。穿孔前和穿孔后的脐带间充质干细胞外泌体的电镜照片分别如图1和图2所示,从图中可以看出,本发明的方法应用于复合外泌体的制备简单易行,成功率高。
四、复合外泌体样品进行膜修复
穿孔后样品立即放入细胞培养箱中孵育1个小时,以促进外泌体膜修复。
五、复合外泌体的抽取与纯化
复合外泌体样品经10万~14万g(rcf)离心力超速离心两次,每次70~90min,弃尽上清,沉淀物即为同时负载mir-181b的复合外泌体,复合外泌体-80℃保存备用。
实施例2:pbs重悬复合外泌体用bca法测外泌体含量(以蛋白计)
1、试剂a包括:1%bca二钠盐、2%无水碳酸钠0.16%酒石酸钠、0.4%氢氧化钠、0.95%碳酸氢钠,混合调ph值至11.25。
2、试剂b:4%硫酸铜。
3、bca工作液:试剂a100ml+试剂b2ml混合。
4、蛋白质标准液:用结晶牛血清白蛋白根据其纯度用生理盐水配制成1.5mg/ml的蛋白质标准液。(纯度可经凯氏定氮法测定蛋白质含量而确定)
5、待测样品:用双缩脲测定法的样品稀释而成。
6、pbs重悬复合外泌体用bca法测外泌体含量为0.5ug/ul。
实施例3:western-blot检测外泌体膜表面特征性蛋白表达
1、收集蛋白样品使用细胞裂解液样品进行裂解,然后测定每个蛋白样品的蛋白浓度。
2、电泳、转膜。
3、浸没于5%bsa封闭液中室温缓慢摇荡两小时。孵育一抗4℃过夜。
4、根据一抗来源选择合适的二抗,按相应比例稀释(1:1000~1:10000),室温轻摇两小时。
5、tbs洗涤后,使用ecl发光试剂显色。结果外泌体特异性标志物cd81和cd63清晰可见(如图3所示)。
实施例4:复合外泌体对成纤维细胞增殖及分化调控能力的细胞学研究
以流式细胞周期检测其对成纤维细胞的细胞增殖能力的影响
1、将成纤维细胞铺于六孔板中,待细胞密度在70%时,一孔加入tgfβ细胞因子的同时加入实施例1制备的复合外泌体(100ug/ml)(实验组)、一孔加入tgfβ细胞因子的同时加入nc外泌体、一孔只加入tgfβ细胞因子(阳性对照组),一孔为不加任何干预。
2、48h后以0.25%胰酶消化细胞,进行流式细胞周期实验。
3、结果可见:
加入实施例1的复合外泌体的成纤维细胞在g2期的比例为20.85%,加入nc外泌体的成纤维细胞在g2期的比例20.69%,而阳性对照组g2期为14.84%,空白对照组为14.08%。表明含实施例1的脐带间充质干细胞复合外泌体的成纤细胞增殖最快。
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!