一种海绵来源杂萜类化合物及其制备方法与应用与流程
本发明涉及医药技术领域,具体涉及一种海绵来源杂萜类化合物septosonea及其制备方法与应用。
背景技术:
海绵是一种低等的多细胞动物,有5亿多年的演化史,在海洋严酷的竞争环境中形成了独特的化学防御机制,能够高效地产生活性物质,每年从海绵中发现结构新颖的活性物质约占海洋天然产物的三分之一以上,目前美国fda批准上市的7个海洋药物中,有3个源自海绵,因此,海绵已成为海洋药物的重要来源,一直是海洋天然产物化学家的研究热点。
倔海绵(dysideaseptosa)为海绵属寻常纲(demospongiae)网角海绵(dictyoceratida)掘海绵科(dysideidae)海绵。国内外学者已经对该属海绵进行过较为系统的化学成分和生物活性研究。具有21个碳的杂萜是倔海绵属海绵最重要的一类代谢产物,其混合的生源合成途径和多变的结构引起了国内外学者的广泛关注。该类型杂萜类化合物具有广泛的生物活性,包括抗菌1、抗真菌2、抗肿瘤3、抗氧化4、抗炎5以及抗过敏活性6。该类型化合物广泛的生物活性和多变的结构引起了化学家和生物学家的持续关注。(文献:[1](a)urban,s.;capon,r.j.5-epi-isospongiaquinone,anewsesquiterpene/quinoneantibioticfromanaustralianmarinesponge,spongiahispida.j.nat.prod.1992,55,1638–1642.(b)schmalzbauer,b.;herrmann,j.;müller,r.;menche,d.totalsynthesisandantibacterialactivityofdysidavaronea.org.lett.2013,15,964-967.;[2]ciavatta,m.l.;lopezgresa,m.p.;gavagnin,m.;romero,v.;melck,d.;manzo,e.;guo,y.w.;vansoest,r.;cimino,g.studiesonpuupehenone-metabolitesofadysideasp.:structureandbiologicalactivity.tetrahedron2007,63,1380–1384.;[3](a)daletos,g.;devoogd,n.j.;müller,w.e.g.;wray,v.;lin,w.;feger,d.;kubbutat,m.;aly,a.h.;proksch,p.cytotoxicandproteinkinaseinhibitingnakijiquinonesandnakijiquinolsfromthespongedactylospongiametachromia.j.nat.prod.2014,77,218-226.(b)hwang,i.h.;oh,j.;zhou,w.;park,s.;kim,j.h.;chittiboyina,a.g.;ferreira,d.;song,g.y.;oh,s.;na,m.;hamann,m.t.cytotoxicactivityofrearrangeddrimanemeroterpenoidsagainstcoloncancercellsviadown-regulationofβ-cateninexpression.j.nat.prod.2015,78,453-461.;[4]utkina,n.k.;denisenko,v.a.;krasokhin,v.b.sesquiterpenoidaminoquinonesfromthemarinespongedysideasp.j.nat.prod.2010,73,788–791.;[5]mcnamara,c.e.;larsen,l.;perry,n.b.;harper,j.l.;berridge,m.v.;chia,e.w.;kelly,m.;webb,v.l.anti-inflammatorysesquiterpene-quinonesfromthenewzealandspongedysideacf.cristagalli.j.nat.prod.2005,68,1431–1433.;[6]jiao,w.h.;cheng,b.h.;shi,g.h.;chen,g.d.;gu,b.b.;zhou,y.j.;hong,l.l.;yang,f.;liu,z.q.;qiu,s.q.;liu,z.g.;yang,p.c.;lin,h.w.dysivillosinsa–d,unusualantiallergicmeroterpenoidsfromthemarinespongedysideavillosa.sci.rep.2017,7,8947.)
但是至今未见从该属海绵中获得对转基因斑马鱼炎症具有治疗作用的杂萜化合物的报道。
技术实现要素:
本发明的第一目的在于公开一种海绵来源杂萜类化合物(本发明中命名为septosonea),其化学结构式如下:
本发明的第二目的在于公开所述的海绵来源杂萜类化合物的制备方法,其包括步骤:
(a)用60-95%(优选95%)乙醇冷浸提取倔海绵,再将提取液浓缩得到浸膏;
(b)将浸膏用水混悬,然后用有机溶剂萃取,萃取液减压浓缩后依次经:
减压硅胶柱色谱分离,采用石油醚-乙酸乙酯梯度洗脱,合并含有倍半萜醌类化合物的馏分;
sephadexlh-20凝胶柱分离,采用石油醚-二氯甲烷-甲醇系统洗脱,进一步富集倍半萜醌类化合物;
反相中压ods柱色谱分离,采用甲醇-水系统梯度洗脱,获得含有倍半萜类化合物的精细馏分;
高效液相色谱法分离,采用65~75%优选70%甲醇水洗脱,得到化合物septosonea。
较佳的,步骤(a)中,倔海绵浸提前先经冷冻并切碎。
较佳的,步骤(b)中,萃取用的有机溶剂为二氯甲烷、正己烷、乙酸乙酯和环己烷中的一种或者两种及以上;优选二氯甲烷或正己烷。
步骤(b)中,sephadexlh-20凝胶柱的中文全称为:羟丙基葡聚糖凝胶柱,为常用市售产品。
较佳的,sephadexlh-20凝胶柱采用的石油醚-二氯甲烷-甲醇体积比为4:1:5。
步骤(b)中,ods柱为常用的市售的填料为十八烷基硅烷键合硅胶的反向色谱柱。
较佳的,反相中压ods柱采用的甲醇-水系统梯度为10:90~100:0。优选梯度为10:90、30:70、50:50、70:30、80:20、90:10和100:0。
较佳的,高效液相色谱法分离时,流速2.0ml/min,检测波长240nm。
本发明的第三目的在于公开所述的海绵来源杂萜类化合物septosonea的应用,尤其是在制备抗炎药物或抗肿瘤药物中的应用。
体外活性试验证明,本发明化合物septosonea对核因子nf-κb信号通路具有很强的抑制活性,nf-κb信号通路对炎症的发生、对肿瘤的血管生成和凋亡都具有密切的关系,因此可用于制备抗炎和抗肿瘤药物。其体内抗炎活性已在转基因斑马鱼模型中得以确证。
所述的海绵来源杂萜化合物septosonea在制备抗炎药物和抗肿瘤药物中的应用是指直接用于预防、诊断、检测、保护、治疗和研究机体炎症反应及其直接相关疾病的产品中的一种或多种,所述的炎症包括与nf-κb信号通路相关或可能相关的炎症,指变质性炎症、渗出性炎症、增生性炎症、妇科炎症或特异性炎症中的一种或多种。
所述的渗出性炎症是浆液性炎、纤维素性炎、化脓性炎、出血性炎、坏死性炎或卡他性炎中的一种或多种。
所述的特异性炎症是结核、梅毒、麻风或淋巴肉芽肿中的一种或多种。
所述的妇科性炎症是盆腔炎、阴道炎或宫颈炎中的一种或多种。
所述的海绵来源杂萜化合物septosonea的应用,其他特征在于,所述的抗肿瘤药物是指直接用于预防、诊断、检测、保护、治疗和研究肿瘤及其直接相关疾病的药物中的一种或多种,是抗肺癌药物、抗宫颈癌药物或抗结肠癌药物中的一种或多种;所述的肿瘤是肺癌、宫颈癌或结肠癌中的一种或多种。
所述的抗肺癌药物是指直接用于预防、诊断、检测、保护、治疗和研究肺癌及其直接相关疾病的药物中的一种或多种,所述的肺癌是指非小细胞肺癌和小细胞肺癌中的一种或多种,所述的非小细胞肺癌是磷癌、腺癌或大细胞肺癌中的一种或多种。
所述的抗宫颈癌药物是指直接用于预防、诊断、检测、保护、治疗和研究宫颈癌及其直接相关疾病的药物中的一种或多种,所述的宫颈癌是非典型增生、原位癌、镜下早期浸润癌或浸润癌中的一种或多种。
所述的抗结肠癌药物是指直接用于预防、诊断、检测、保护、治疗和研究结肠癌及其直接相关疾病的药物中的一种或多种,所述的结肠癌是指左半结肠癌、右半结肠癌或直肠癌中的一种或多种。
本发明的有益效果在于:本发明制备方法简单,通过该方法制备得到的化合物septosonea对nf-κb信号通路抑制活性显著,同时在体内对转基因斑马鱼炎症具有明显的抑制活性。本发明为研究和开发新的抗炎、抗肿瘤药物提供了新的先导化合物,为开发利用我国海洋药用资源提供了科学依据。
附图说明
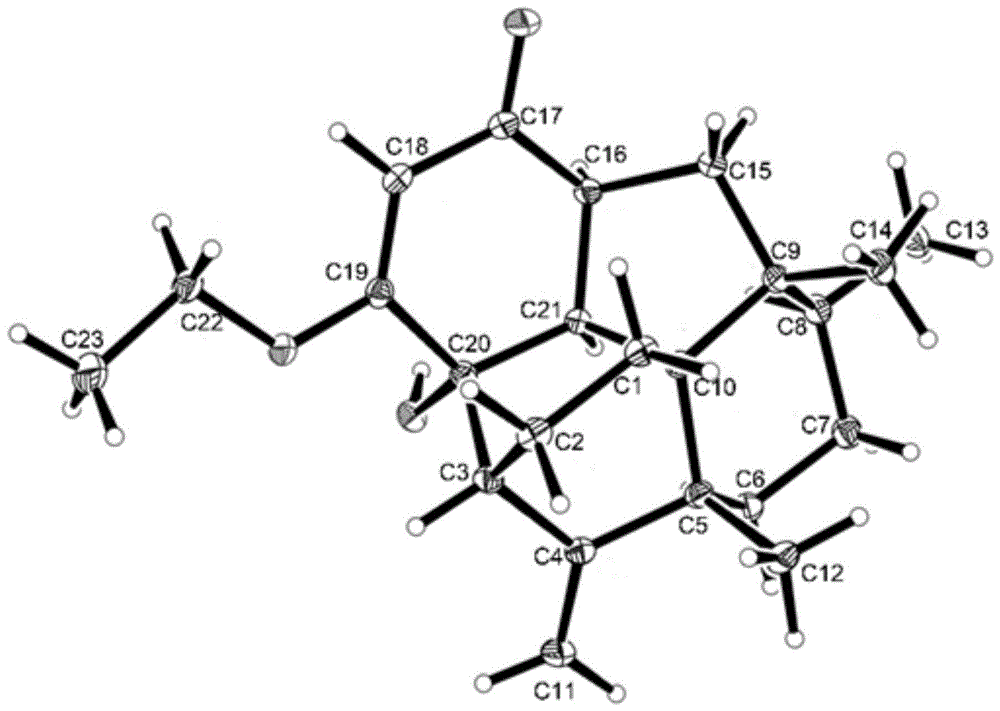
图1为本发明化合物septosonea的x-ray单晶衍射结构图;
图2为本发明化合物septosonea的实测ecd曲线和两种构型计算ecd曲线;
图3为效果实施例1中各组斑马鱼幼苗的荧光显微镜照片;
图4为效果实施例1中各组斑马鱼幼苗中的巨噬细胞计算结果示意图;
图5为效果实施例2中各组的荧光素酶活性测试结果示意图。
具体实施方式
以下结合具体实施例,对本发明作进一步说明。应理解,以下实施例仅用于说明本发明而非用于限定本发明的范围。
实施例1化合物septosonea的制备
取预先冷冻并切碎的倔海绵(湿重700g),分别用95%乙醇(1l)冷浸提取5次,每次一周,合并提取液,提取液经减压浓缩得总浸膏,将总浸膏混悬到水中,再用等体积正己烷和二氯甲烷各进行萃取5次,合并萃取液,减压浓缩,得到正己烷萃取物(2.4g),二氯甲烷萃取物(3.2g),lc-ms在两个萃取物中均检测到septosonea的存在。
将上述萃取物用减压硅胶柱色谱分离,采用石油醚-乙酸乙酯梯度洗脱,根据薄层色谱tlc分析结果,得到含有倍半萜醌类化合物的馏分,再用sephadexlh-20凝胶柱对该馏分进行进一步富集,采用石油醚-二氯甲烷-甲醇(4:1:5)系统,得到进一步富集倍半萜醌类化合物的馏分,然后对该馏分再进行反相中压ods柱色谱分离,采用甲醇-水系统梯度洗脱(10:90、30:70、50:50、70:30、80:20、90:10和100:0),对于获得的含有倍半萜类化合物的精细馏分,再用高效液相色谱法进行分离(70%甲醇水,流速2.0ml/min,检测波长240nm),得到化合物septosonea(c23h32o3)。
septosonea的理化性质和核磁共振数据如下:
无色针晶;mp183–185℃;
表1化合物septosonea的核磁共振谱数据(cdcl3)
图1所示为化合物septosonea的x-ray单晶衍射结构,图2所示为化合物septosonea的实测ecd曲线(exptlfor1)以及两种构型的计算ecd曲线(1a和1b),确定该化合物的绝对构型为3r,5r,8s,9r,10r,16s,20s,21s,结构式如下:
效果实施例1体内抑制硫酸铜诱导的转基因斑马鱼炎症实验
对本发明化合物septosonea进行体内抑制硫酸铜诱导的转基因斑马鱼炎症实验,同时以indomethacin(吲哚美辛,人工合成抗炎药)作为对比进行平行实验。样品用dmso溶解,低温保存,dmso在最终体系中的浓度控制在不影响检测活性的范围之内。每个样品在测试中均设置3个复孔。
具体实验步骤:
巨噬细胞中绿色荧光蛋白表达的转基因斑马鱼(tg:zlyz-egfp)(购自山东省科学院)被用于该活性测试,培养条件按照oecd(theorganizationforeconomicco-operationanddevelopment)规范进行,斑马鱼培养在28±0.5℃、14/10h光照/非光照循环条件下培养。挑选健康的斑马鱼幼苗放入24孔板中,每孔添加2ml胚胎培养基,每孔10条幼苗,共分成6组:对照组(水)、模型组(10μmcuso4)、阳性对照组(10μmcuso4+5μmindomethacin(购自solarbio,china))、3个加药组(10μmcuso4+(10μm,5μm,2.5μm)septosonea)。每条斑马鱼幼苗都用荧光显微镜(axio,zoom.v16)拍照,巨噬细胞的数目用image-proplus软件获得。
结果如下:
图3为各组斑马鱼幼苗的荧光显微镜照片,其中control表示空白组,cuso4表示模型组,indomethacin表示阳性对照组,2.5μm、5μm和10μm表示3个加药组。图4为各组巨噬细胞数目计算结果。
由图3和图4可知,本发明化合物septosonea对硫酸铜诱导的转基因斑马鱼急性炎症发生和扩散具有抑制活性,其活性与吲哚美辛相当,且具有良好的剂量依赖关系。
效果实施例2体外抑制tnf-α诱导的人hek-293t细胞中核因子nf-κb信号通路实验
对本发明化合物septosonea进行体外抑制tnf-α诱导的hek-293t细胞nf-κb信号通路实验。样品用dmso溶解,低温保存,dmso在最终体系中的浓度控制在不影响检测活性的范围之内。每个样品在测试中均设置3个复孔。
具体实验步骤:
hek-293t(购自中国科学院)培养在96孔板中。12小时之后,细胞共转染到荧光素酶报告质粒pgl4.32[luc2p/nf-κb-re/hy-gro]vector(30ng/ml)和pc-dna-renilla(10ng/ml)(购自promega,madison,wi,usa)12小时。核因子nf-κb信号通路被tnf-α(20ng/ml)(购自promega,madison,wi,usa)活化,加入3个浓度(1.25μm、5μm、20μm)的septosonea,用tpca(2-[(aminocarbonyl)amino]-5-(4-fluorophenyl)-3-thiophenecarboxamide,购自promega,madison,wi,usa)(0.5μm)作为阳性对照药。6小时后,使用荧光素酶测定试剂盒(购自promega,madison,wi,usa)测量荧光素酶活性。
结果如下:
图5为各组的荧光素酶活性测试结果,显示septosonea在1.25-20μm浓度下对tnf-α诱导的人源hek-293t细胞中核因子nf-κb活化具有显著的抑制活性,ic50为6.8μm,并呈现良好的浓度依赖性。
以上已对本发明创造的较佳实施例进行了具体说明,但本发明创造并不限于所述实施例,熟悉本领域的技术人员在不违背本发明创造精神的前提下还可做出种种的等同的变型或替换,这些等同的变型或替换均包含在本申请权利要求所限定的范围内。
- 还没有人留言评论。精彩留言会获得点赞!