一种用于肝癌诊断的生物标志物的制作方法
本发明属于生物医药领域,涉及一种用于肝癌诊断的生物标志物,具体的涉及生物标志物ac239809.3。
背景技术:
肝细胞肝癌(hepatocellularcarcinoma,hcc)是最常见的恶性肿瘤之一,具有侵袭性强、死亡率高的特点,位列癌症相关死亡原因的第二位(esther,cidon.systemictreatmentofhepatocellularcarcinoma:past,presentandfuture[j].worldjournalofhepatology,2017,9(18):797-807.)。目前认为乙型肝炎病毒(hbv)、丙型肝炎病毒(hcv)、酒精性及非酒精性肝硬化、黄曲霉毒素、肥胖等均与肝癌的发生相关。肝癌的发病机制尚未完全明确,研究认为与基因突变、肝癌干细胞、微环境、非编码rna、代谢异常等有关(farazipa,depinhora.hepatocellularenvironment.[j].naturereviewscancer,2006,carcinomapathogenesis:fromgenesto6(9):674-687.)。由于我国肝癌多发生于欠发达地区,使得很多患者被诊断时多已处于进展期或晚期,错过了最佳的手术时机。肝移植被认为是治疗肝癌和潜在肝疾病最有效的方法,但由于其手术费用昂贵,而且有严格的适应症,肝源相对短缺,虽然近年来肝移植技术已非常成熟,但肝癌的总体死亡率仍未有很大的改善。靶向口服化疗药物索拉菲尼被认为是晚期肝癌患者的唯一选择,但其价格昂贵,不是所有患者都能承受,而且远期疗效有限,所以中晚期肝癌患者的预后依然很差。过去的几十年中,随着科学技术的进步,肿瘤的免疫治疗、基因治疗等取得了巨大的进展,因此,深入研究肝癌细胞的基因谱及寻找新的治疗靶点至关重要。
肝癌的发病是一个涉及多种调控和分子通路的复杂过程,目前尚不十分清楚。以往对肝癌发病的分子机制研究主要集中在蛋白质编码基因上,因为一直以来蛋白质被认为是各种生物学过程的中心。相比之下,rna被认为是蛋白质合成的中间环节(mrna)或平台(trna和rrna)。然而随着近年来高通量测序技术的发展,人们逐渐认识到过去被认为是转录组“噪音”的非编码rna,无论在数量上还是功能上都比蛋白质编码基因要丰富和重要。长链非编码rna(longnon-codingrna,lncrna)是一类转录本长度超过200nt的rna分子,由于缺少有效的开放式阅读框,不具有编码蛋白的功能。科学家们已经认识到了非编码rna,尤其是lncrna对于破解各种科学难题的重要意义。目前有越来越多的研究报道其具有复杂的生物学功能,lncrna能够在表观遗传学、转录及转录后等多个水平调控基因表达,也与疾病的发展息息相关。lncrna在多种癌症中差异表达,多个研究证实其可参与肿瘤的发生、发展、侵袭和转移的各个阶段,是肿瘤发生和进展的关键因素。
目前,在乳腺癌和大肠癌的诊断中,分子标志物检测已经成为标准,是治疗过程的重要步骤。然而,目前还没有统一的肝细胞癌分子标志物标准。寻找肝细胞癌发生发展相关的lncrna对肿瘤的诊断和治疗具有重要的意义。
技术实现要素:
为了弥补现有技术的不足,本发明的目的在于提供一种用于肝癌诊断的生物标志物,通过检测生物标志物的表达水平,可以判断受试者是否患有肝癌,同时所述生物标志物也可以作为分子靶标应用于肝癌的个性化治疗。
为了实现上述目的,本发明采用如下技术方案:
本发明提供了检测ac239809.3的试剂在制备诊断肝细胞癌的产品中的应用。
进一步,所述产品包括通过测序技术、核酸杂交技术、核酸扩增技术检测样本中ac239809.3的表达水平的试剂。
进一步,所述试剂选自:
特异性识别ac239809.3的探针;
或特异性扩增ac239809.3的引物。
进一步,所述特异性扩增ac239809.3的引物序列如seqidno.1~2所示。
本发明提供了一种体外检测ac239809.3表达水平的产品,所述产品包括芯片、试剂盒、核酸膜条。
进一步,所述芯片包括特异性识别ac239809.3的寡核苷酸探针;所述试剂盒包括特异性扩增ac239809.3的引物,或特异性识别ac239809.3的寡核苷酸探针;所述核酸膜条包括特异性识别ac239809.3的寡核苷酸探针。
进一步,所述特异性扩增ac239809.3的引物序列如seqidno.1~2所示。
本发明提供了体外检测ac239809.3表达水平的产品在制备诊断肝细胞癌的工具中的应用。
本发明提供了ac239809.3在构建预测肝细胞癌的计算模型中的应用。
本发明提供了ac239809.3在制备治疗肝细胞癌的药物组合物中的应用。
进一步,所述药物组合物包括ac239809.3的抑制剂,所述抑制剂可以降低ac239809.3的表达水平。
附图说明
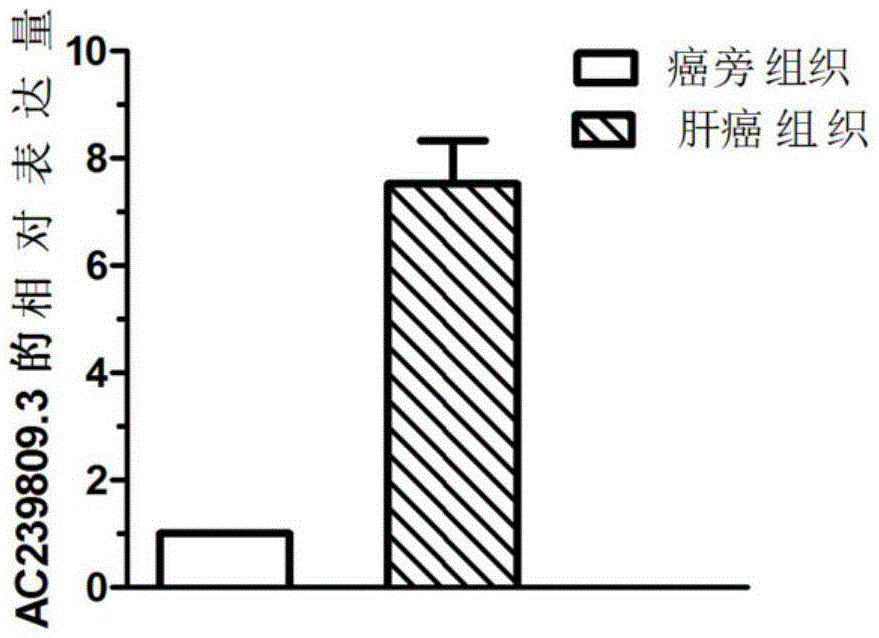
图1是利用qpcr检测ac239809.3基因在肝细胞癌组织中的表达情况图。
具体的实施方式
本发明通过采用高通量测序和生物信息学相结合的方法,筛选在肝细胞癌组织和相对应的癌旁组织中呈现差异表达的lncrna,然后通过大样本进一步验证所述差异表达的lncrna与肝细胞癌的关系,进而确定该lncrna应用于肝细胞癌诊断和治疗的可能性。本发明通过实验首次发现了ac239809.3在肝癌组织中表达上调。
ac239809.3基因位于人1号染色体上,ensemblid为ensg00000227733本发明中的ac239809.3包括野生型、突变型或其片段。目前已经公开的ac239809.3存在18个转录本,ac239809.3-201(转录id:enst00000599640.5)、ac239809.3-214(转录id:enst00000496508.1)、ac239809.3-209(转录id:enst00000629702.3)、ac239809.3-211(转录id:enst00000464343.6)、ac239809.3-213(转录id:enst00000634551.1)、ac239809.3-215(转录id:enst00000611617.5)、ac239809.3-203(转录id:enst00000611286.4)、ac239809.3-218(转录id:enst00000616018.1)、ac239809.3-212(转录id:enst00000628063.2)、ac239809.3-217(转录id:enst00000620213.4)、ac239809.3-207(转录id:enst00000599387.5)、ac239809.3-206(转录id:enst00000596091.5)、ac239809.3-202(转录id:enst00000628902.1)、ac239809.3-216(转录id:enst00000622642.4)、ac239809.3-210(转录id:enst00000596220.1)、ac239809.3-208(转录id:enst00000611452.4)、ac239809.3-204(转录id:enst00000614606.4)、ac239809.3-205(转录id:enst00000482381.2)。其中,一种代表性的ac239809.3基因如ac239809.3-201(转录id:enst00000599640.5)的序列所示。
本领域技术人员知道,在对原始测序结果进行生物信息学分析时,通常会将测序结果和已知的基因进行比对,只要测序片段可以比对到相关基因上,就可以看做是该基因的表达,因此,在提及差异表达的基因时,该基因的不同的转录本同时包含在本发明中。
本领域技术人员应当理解,测定基因表达的手段不是本发明的重要方面。可以在转录水平上检测生物标志物的表达水平。本发明可以利用本领域内已知的任何方法测定基因表达。
检测技术
本发明的lncrna使用本领域普通技术人员已知的多种核酸技术进行检测,这些技术包括但不限于:核酸测序、核酸杂交和核酸扩增技术。
核酸测序技术的示例性非限制性实例包括但不限于链终止子(sanger)测序和染料终止子测序。本领域的普通技术人员将认识到,由于rna在细胞中不太稳定并且在实验中更易受到核酸酶攻击,因此在测序前通常将rna逆转录成dna。
核酸测序技术的另一示例性非限制性实例包括下一代测序(深度测序/高通量测序),高通量测序技术是一种基于单分子簇的边合成边测序技术,基于专有的可逆终止化学反应原理。测序时将基因组的dna的随机片段附着到光学透明的玻璃表面,这些dna片段经过延伸和桥式扩增后,在玻璃表面形成数以亿计的簇,每个簇是具有数千份相同模板的单分子簇,然后利用带荧光基团的四种特殊脱氧核糖核苷酸,通过可逆性的边合成边测序技术对待测的模板dna进行测序。
核酸杂交技术的示例性非限制性实例包括但不限于原位杂交(ish)、微阵列和southern或northern印迹。原位杂交(ish)是一种使用标记的互补dna或rna链作为探针以定位组织一部分或切片(原位)或者如果组织足够小则为整个组织(全组织包埋ish)中的特异性dna或rna序列的杂交。dnaish可用于确定染色体的结构。rnaish用于测量和定位组织切片或全组织包埋内的mrna和其他转录本(例如,ncrna)。通常对样本细胞和组织进行处理以原位固定靶转录本,并增加探针的进入。探针在高温下与靶序列杂交,然后将多余的探针洗掉。分别使用放射自显影、荧光显微术或免疫组织化学,对组织中用放射、荧光或抗原标记的碱基标记的探针进行定位和定量。ish也可使用两种或更多种通过放射性或其他非放射性标记物标记的探针,以同时检测两种或更多种转录本。
将southern和northern印迹分别用于检测特异性dna或rna序列。使从样本中提取的dna或rna断裂,在基质凝胶上通过电泳分离,然后转移到膜滤器上。使滤器结合的dna或rna与和所关注的序列互补的标记探针杂交。检测结合到滤器的杂交探针。该程序的一种变化形式是反向northern印迹,其中固定到膜的底物核酸为分离的dna片段的集合,而探针是从组织提取并进行了标记的rna。
核酸扩增技术的示例性非限制性实例包括但不限于:聚合酶链式反应(pcr)、逆转录聚合酶链式反应(rt-pcr)、转录介导的扩增(tma)、连接酶链式反应(lcr)、链置换扩增(sda)和基于核酸序列的扩增(nasba)。本领域的普通技术人员将认识到,某些扩增技术(例如,pcr)需要在扩增前将rna逆转录成dna(例如,rt-pcr),而其他扩增技术则直接扩增rna(例如,tma和nasba)。
通常称为pcr的聚合酶链式反应使用变性、引物对与相反链的退火以及引物延伸的多个循环,以指数方式增加靶核酸序列的拷贝数;tma的转录介导的扩增(在基本上恒定的温度、离子强度和ph的条件下自身催化地合成靶核酸序列的多个拷贝,其中靶序列的多个rna拷贝自身催化地生成另外的拷贝;lcr的连接酶链式反应使用与靶核酸的相邻区域杂交的两组互补dna寡核苷酸;其他扩增方法包括例如:通常称为nasba的基于核酸序列的扩增;使用rna复制酶(通常称为qβ复制酶)扩增探针分子本身的扩增;基于转录的扩增方法;以及自我维持的序列扩增。
本发明中非扩增或扩增的核酸可通过任何常规的手段检测。
芯片、核酸膜条、试剂盒
本发明提供了检测中ac239809.3基因的表达水平的产品,所述产品包括(但不限于)芯片、核酸膜条或试剂盒。其中芯片包括:固相载体;以及有序固定在所述固相载体上的寡核苷酸探针,所述的寡核苷酸探针特异性地对应于ac239809.3所示的部分或全部序列。
所述固相载体包括无机载体和有机载体,所述无机载体包括但不限于有硅载体、玻璃载体、陶瓷载体等;所述有机载体包括聚丙烯薄膜、尼龙膜等。
本发明提供了核酸膜条包括基底和固定于所述基底上的针对ac239809.3的寡核苷酸探针;所述基底可以是任何适于固定寡核苷酸探针的基底,例如尼龙膜、硝酸纤维素膜、聚丙烯膜、玻璃片、硅胶晶片、微缩磁珠等
本发明提供了一种试剂盒,所述试剂盒包括检测ac239809.3表达的试剂,以及选自下组的一种或多种物质:容器、使用说明书、阳性对照物、阴性对照物、缓冲剂、助剂或溶剂。
本发明的试剂盒中还可附有试剂盒的使用说明书,其中记载了如何采用试剂盒进行检测,和如何利用检测结果对肿瘤发展进行判断、对治疗方案进行选择。试剂盒的组分可以以水介质的形式或以冻干的形式来包装。试剂盒中适当的容器通常至少包括一种小瓶、试管、长颈瓶、宝特瓶、针筒或其它容器,其中可放置一种组分,并且优选地,可进行适当地等分。在试剂盒中存在多于一种的组分时,试剂盒中通常也将包含第二、第三或其它附加的容器,其中分离地放置附加的组分。然而,不同组合的组分可被包含在一个小瓶中。本发明的试剂盒通常也将包括一种用于容纳反应物的容器,密封以用于商业销售。这种容器可包括注模或吹模的塑料容器,其中可保留所需的小瓶。
作为一种优选的实施方式,所述试剂盒为荧光定量pcr检测试剂盒,所述引物适用于sybrgreen、taqman探针、分子信标、双杂交探针、复合探针的检测。
在一个更优选的实施方案中,所述试剂盒中的pcr反应液为荧光定量pcr反应液,并一步包含荧光染料。
本发明提供了ac239809.3在制备预测肝细胞癌的计算模型中的应用。正如熟练技术人员可以领会的,可以使用两种或更多种标志物的测量来改进调查中的诊断问题。生化标志物可以个别测定,或者在本发明的一个实施方案中,它们可以同时测定,例如使用芯片或基于珠的阵列技术。然后独立解读生物标志物的浓度,例如使用每种标志物的个别截留,或者它们组合进行解读。
在本发明中,可以以不同方式实施和实现将标志物水平与某种可能性或风险关联起来的步骤。优选地,在数学上组合基因和一种或多种其它标志物的测定浓度,并将组合值与根本的诊断问题关联起来。可以通过任何适宜的现有技术数学方法将标志物值的测定组合。
优选地,在标志物组合中应用的数学算法是一种对数函数。优选地,应用此类数学算法或此类对数函数的结果是单一值。根据根本的诊断问题,能容易地将此类值与例如个体关于肝细胞癌的风险或与有助于评估肝细胞癌松患者的其它有意诊断用途关联起来。以一种优选的方式,此类对数函数是如下获得的:a)将个体分类入组,例如正常人、有肝细胞癌风险的个体、具有肝细胞癌的患者等等,b)通过单变量分析来鉴定在这些组之间差异显著的标志物,c)对数回归分析以评估标志物的可用于评估这些不同组的独立差别值,并d)构建对数函数来组合独立差别值。在这种类型的分析中,标志物不再是独立的,而是代表一个标志物组合。
本发明提供了ac239809.3在制备治疗肝细胞癌的药物组合物中的应用,所述药物组合物包含ac239809.3的抑制剂以及药学上可接受的载体,所述抑制剂选自以ac239809.3或其转录本为靶序列、且能够抑制ac239809.3基因表达或基因转录的干扰分子,包括:shrna(小发夹rna)、小干扰rna(sirna)、dsrna、微小rna、反义核酸,或能表达或形成所述shrna、小干扰rna、dsrna、微小rna、反义核酸的构建物。所药学上可接受的载体包括(但并不限于)稀释剂、粘合剂、表面活性剂、致湿剂、吸附载体、润滑剂、填充剂、崩解剂。
下面结合附图和实施例对本发明作进一步详细的说明。以下实施例仅用于说明本发明而不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。
实施例1筛选与肝细胞癌相关的基因标志物
1、样品收集
收集35例原发性肝细胞癌患者的癌组织及相对应的癌旁组织样本,从中随机选取5例进行高通量测序,患者均知情同意,上述所有标本的取得均通过组织伦理委员会的同意。
2、rna样品的制备及质量分析
用剪刀组织剪碎,加入1mltrizol,振荡器上震荡1min;常温放置10min,使核蛋白体完全分解;然后加入200μl三氯甲烷(氯仿),盖紧管盖,剧烈震荡15s,常温静置10min后,4℃,11000rpm离心15min;将水样层转移到一个新的离心管中,加入500μl异丙醇;颠倒混匀后,常温静置10min后4℃,11000rpm离心15min;用枪小心吸走液体,留沉淀在管底,加入1ml75%的乙醇,在振荡器上震荡5s,洗涤沉淀一次,4℃,8000rpm离心5min;然后将上清小心去掉,干燥沉淀10min,加入适量的水溶解沉淀10min。
3、总rna定量与纯度分析
将提取的rna进行琼脂糖凝胶电泳,利用nanodrop2000对所提rna的浓度和纯度进行检测,琼脂糖凝胶电泳检测rna完整性,agilent2100测定rin值。单次建库要求rna总量5μg,浓度≥200ng/μl,od260/280介于1.8~2.2之间。
4、构建cdna文库
使用epicentre的ribo-zero试剂盒除去总rna中的核糖体rna;利用金属离子将完整的rna随机打断成200bp左右的小片段;利用illumina的truseqtmrnasampleprepkit进行cdna文库的构建。
5、测序
使用illuminax-ten测序平台对cdna文库进行测序。
6、高通量转录组测序数据分析
删除不易检测到的lncrna,使用工具r-3.3.3中的deseq2进行生信分析。用cutadapt对reads的5’和3’段进行trim,trim掉质量<20的碱基,并且删掉n大于10%的reads;然后使用tophat将测序结果比对到参考基因组上。所用的参考基因组版本为hg38;cuffquant定量lncrna的表达量并标准化输出,cuffdiff比较对照组跟疾病组lncrna的表达差异,差异表达lncrna的筛选标准:fdr<0.05,abs(log2fc)>1。
7、结果
高通量测序结果显示,ac239809.3基因在肝细胞癌组织中的表达量显著高于癌旁组织(p<0.001),提示ac239809.3可以作为可能的检测靶标应用于肝细胞癌的早期诊断。
实施例2qpcr测序验证ac239809.3基因的差异表达
1、利用前面收集的35例患者肝癌组织样本和癌旁组织样本对ac239809.3基因差异表达进行大样本qpcr验证。
2、rna提取步骤参见实施例1
3、qpcr检测
1)逆转录反应
a.将1μg的总rna模板与2μl10×缓冲液、2μldatp(10mm)、0.5μlpolya多聚酶、0.5μl核糖核酸酶(rnase)抑制剂和无核糖核酸酶水(rnasefreewater)混合,体积最后为20μl,37℃孵育1h;
b.向反应管中加入1μl0.5μg/μloligo(dt)特异性rt引物,70℃孵育5min,立即置冰上孵育至少2min;
c.将反应混合物与4μl5×缓冲液、1μldntp(10mm),0.5μlm-mlv逆转录酶,0.5μl核糖核酸酶(rnase)抑制剂,10μlpolya反应混合液和4μl无核糖核酸酶水(rnasefreewater)混合,42℃孵育1h。
2)引物设计
根据ac239809.3基因和gapdh基因的编码序列设计qpcr扩增引物,具体引物序列如下:
ac239809.3基因:
正向引物为5’-tcttctatcctggtgttc-3’(seqidno.1);
反向引物为5’-agatgattcagatgatgttac-3’(seqidno.2)。
gapdh基因:
正向引物为5’-aatcccatcaccatcttccag-3’(seqidno.3);
反向引物为5’-gagccccagccttctccat-3’(seqidno.4)。
3)qpcr扩增检验
配制25μl反应体系:sybrgreen聚合酶链式反应体系12.5μl,正反向引物(5μm)各1μl,模板cdna2.0μl,ddh2o8.5μl。各项操作均于冰上进行。
反应条件:95℃10min,(95℃15s,60℃60s)×45个循环。以sybrgreen作为荧光标记物,在lightcycler荧光定量pcr仪上进行pcr反应,以gapdh作为参照基因,在60-95℃进行溶解曲线分析,通过融解曲线分析和电泳确定目的条带,δδct法进行相对定量。
4、结果
qpcr结果如图1所示,与癌旁组织相比,ac239809.3在肝癌组织中表达上调,差异具有统计学意义(p<0.05);ac239809.3在检测的所有样本中均表达上调,提示ac239809.3在肝癌的诊断中具有较高的应用价值。
上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。
序列表
<110>河北医科大学第二医院
<120>一种用于肝癌诊断的生物标志物
<160>4
<170>siposequencelisting1.0
<210>1
<211>18
<212>dna
<213>人工序列(artificialsequence)
<400>1
tcttctatcctggtgttc18
<210>2
<211>21
<212>dna
<213>人工序列(artificialsequence)
<400>2
agatgattcagatgatgttac21
<210>3
<211>21
<212>dna
<213>人工序列(artificialsequence)
<400>3
aatcccatcaccatcttccag21
<210>4
<211>19
<212>dna
<213>人工序列(artificialsequence)
<400>4
gagccccagccttctccat19
- 还没有人留言评论。精彩留言会获得点赞!