一种索玛鲁肽的制备方法与流程
本发明属于多肽药物制备方法
技术领域:
,具体涉及一种索玛鲁肽的制备方法。
背景技术:
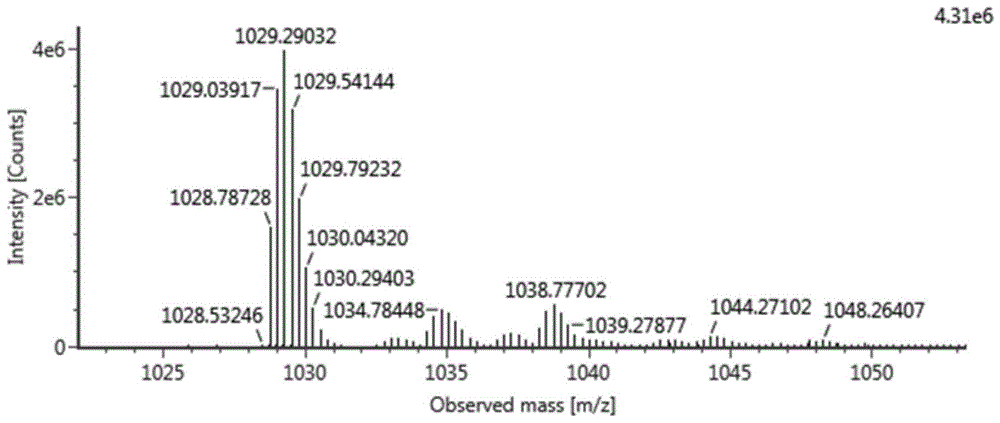
:索玛鲁肽是一种glp-1(胰高血糖素样肽)类似物,其具有以下结构:his-aib-glu-gly-thr-phe-thr-ser-asp-val-ser-ser-tyr-leu-glu-gly-gln-ala-ala-lys(aeea-aeea-γ-glu-nα-octa-oh)-glu-phe-ile-ala-trp-leu-val-arg-gly-arg-gly-oh,与人glp-1具有97%的序列同源性。人glp-1可以结合并激活glp-1受体。glp-1受体为天然glp-1的靶点,glp-1是一种内源性肠促胰岛素激素,能够促进胰腺β细胞葡萄糖浓度依赖性地分泌胰岛素。与天然glp-1不同的是,索玛鲁肽在人体中的药代动力学和药效动力学特点均适合每周一次的给药方案。皮下注射给药后,其作用时间延长的机理包括:使吸收减慢的自联作用;与白蛋白结合;对二肽基肽酶iv(dpp-iv)和中性内肽酶(nep)具有更高的酶稳定性,从而具有较长的血浆半衰期。索玛鲁肽的活性由其与glp-1受体间特定的相互作用介导,导致环磷酸腺苷(camp)的增加。索玛鲁肽能够以葡萄糖浓度依赖的模式刺激胰岛素的分泌,同时以葡萄糖浓度依赖的模式降低过高的胰高糖素的分泌。因此,当血糖升高时,胰岛素分泌受到刺激,同时胰高糖素分泌受到抑制。与之相反,在低血糖时索玛鲁肽能够减少胰岛素分泌,且不影响胰高糖素的分泌。索玛鲁肽的降血糖机理还包括轻微延长胃排空时间。索玛鲁肽能够通过减轻饥饿感和能量摄入降低体重和体脂量。每周皮下注射一次,可使2型糖尿病患者血糖水平大幅改善,并且低血糖风险较低。同时,索玛鲁肽还能够通过降低食欲和减少食物摄入量,诱导减肥。与利拉鲁肽相比,索玛鲁肽的脂肪连更长,疏水性强,但是索玛鲁肽经过短链的peg修饰,亲水性大大增强。peg修饰后不但可以与白蛋白紧密结合,掩盖dpp-4酶水解位点,还能降低肾排泄,可延长生物半衰期,达到长循环的效果。索马鲁肽与艾塞那肽相比,提供了更好的血糖控制及体重减轻。索玛鲁肽具有降低血糖、减轻体重、促进胰岛细胞再生以及心血管系统保护等多种效应,临床应用前景广阔。本品用于成人2型糖尿病患者控制血糖:适用于单用二甲双胍或磺脲类药物最大可耐受剂量治疗后血糖仍控制不佳的患者,与二甲双胍或磺脲类药物联合应用。国内外关于索玛鲁肽制备报道的报道很多,如中国专利cn201811590004.4提供了一种固相合成法,以wang树脂为起始原料,以fmoc保护的氨基酸为单体,依次逐个接上氨基酸得到线性索玛鲁肽树脂,采用tfa裂解获得粗品,最后采用反相高效液相色谱法纯化,获得索玛鲁肽,未规避thr13-ser14-asp15困难片段序列的缺失肽杂质;中国专利cn201811466181.1采用片段法合成,片段过多,氨基酸原料使用过多,成本高。上述制备方法存在以下不足,在制备索玛鲁肽过程中,序列thr13-ser14-asp15处由于β折叠,氨基酸缩合困难,出现大量缺失杂质,另外,主链脱lys保护基后偶联侧链aeea及glu-otbu等非天然氨基酸时存在空间位阻过大,缩合不完全等现象,这些因缩合不完全产生的杂质极性与索玛鲁肽非常接近,给粗品纯化带来困难,降低了产品收率。技术实现要素:为了解决上述技术问题,本发明提供了一种索玛鲁肽的制备方法,它包括如下步骤:(1)取fmoc-gly-树脂,通过多肽固相合成法,按索玛鲁肽c端至n端顺序,在该树脂上依次偶联具有n端fmoc保护的氨基酸至第22位val,得到如下序列肽树脂:fmoc-val-ser(tbu)-ser(tbu)-tyr(tbu)-leu-glu(otbu)-gly-gln(trt)-ala-ala-lys(r1)-glu(otbu)-phe-ile-ala-trp(boc)-leu-val-arg(pbf)-gly-arg(pbf)-gly-树脂;其中,r1为alloc、dde、mtt或mmt中的一种;(2)脱除第22位val的fmoc保护基后,偶联短肽链fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh,并按索玛鲁肽c端至n端顺序,继续偶联具有n端fmoc保护的氨基酸至第29位his(trt),得到如下序列肽树脂:boc-his(trt)-aib-glu(otbu)-gly-thr(tbu)-phe-thr(tbu)-ser(tbu)-asp(otbu)-val-ser(tbu)-ser(tbu)-tyr(tbu)-leu-glu(otbu)-gly-gln(trt)-ala-ala-lys(r1)-glu(otbu)-phe-ile-ala-trp(boc)-leu-val-arg(pbf)-gly-arg(pbf)-gly-树脂;(3)脱除第12位lys的保护基r1后,采用两步法在lys侧链偶联短肽链fmoc-aeea-aeea-oh和octa(otbu)-glu(α-otbu)-γ-cooh;其中,先偶联短肽链fmoc-aeea-aeea-oh,再偶联短肽链octa(otbu)-glu(α-otbu)-γ-cooh;或者,采用一步法在lys侧链偶联短肽链octa(otbu)-glu(α-otbu)-aeea-aeea-oh;即获得索玛鲁肽全保护肽树脂,结构为:boc-his(trt)-aib-glu(otbu)-gly-thr(tbu)-phe-thr(tbu)-ser(tbu)-asp(otbu)-val-ser(tbu)-ser(tbu)-tyr(tbu)-leu-glu(otbu)-gly-gln(trt)-ala-ala-lys(aeea-aeea-γ-glu(α-otbu)-octa(otbu))-glu(otbu)-phe-ile-ala-trp(boc)-leu-val-arg(pbf)-gly-arg(pbf)-gly-树脂;(4)索玛鲁肽全保护肽树脂经裂解液裂解后即得索玛鲁肽粗品;(5)索玛鲁肽粗品经反相高效液相色谱法纯化,再经换盐,即得索玛鲁肽精品。进一步地,步骤(1)中,所述fmoc-gly-树脂为fmoc-gly-wang或fmoc-gly-ctc;当为fmoc-gly-wang时,替代度为0.15~0.45mmol/g,优选为0.28mmol/g;当为fmoc-gly-ctc时,替代度为0.25~0.45mmol/g。进一步地,步骤(2)中,所述偶联短肽链fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh的缩合剂选自cl-hobt/dic、hobt/dic、pybop/cl-hobt/diea、pybop/hoat/diea或comu/diea;所述偶联短肽链fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh的溶剂选自dmf、dcm、nmp或dmso中的一种或多种。进一步地,步骤(2)中,所述缩合剂为cl-hobt/dic;所述溶剂由dmf、dcm和dmso组成;其中,所述缩合剂中cl-hobt和dic的摩尔比为2:3~5,优选为2:3;所述溶剂中dmf、dcm和dmso的体积比为2:1~2:1~2,优选为2:1:1。进一步地,步骤(3)中,所述脱除保护基r1的方法如下:当r1为alloc时,保护基脱除选用5~10当量的吗啡啉或5~10当量的苯硅烷,再加入0.1~0.3当量的四(三苯基膦)钯,选用dcm为溶剂,脱除反应3分钟,将反应液抽滤后,重复操作1遍;当r1为dde时,选用含2%水合肼的dmf溶液,脱除反应3分钟,将反应液抽滤后,再重复操作1遍;当r1为mtt时,选用含5%tfa的dcm溶液,脱除反应30分钟,将反应液抽滤后,再重复操作1遍;当r1为mmt时,选用含5%tfa的dcm溶液,脱除反应30分钟,将反应液抽滤后,再重复操作1遍。进一步地,步骤(3)中,所述采用两步法在lys侧链偶联短肽链fmoc-aeea-aeea-oh和octa(otbu)-glu(α-otbu)-γ-cooh时,偶联的缩合剂选自pybop/cl-hobt/diea、pybop/hoat/diea、comu/diea;所述采用一步法在lys侧链偶联短肽链octa(otbu)-glu(α-otbu)-aeea-aeea-oh时,偶联的缩合剂选自cl-hobt/dic、hobt/dic、comu/diea。进一步地,步骤(3)中,所述采用两步法在lys侧链偶联短肽链fmoc-aeea-aeea-oh和octa(otbu)-glu(α-otbu)-γ-cooh时,偶联的缩合剂选自pybop/hoat/diea;优选地,所述pybop、hoat和diea的摩尔比为2:2:3。进一步地,步骤(3)中,所述两步法和一步法所选溶剂均选自dmf、dcm、nmp或dmso中的一种或多种,溶剂中加入以下表面活性剂:1~3%(v/v)的曲拉通或10-15%(v/v)的硫氢化钾。进一步地,步骤(4)中,所述裂解液由tfa与苯甲硫醚、甲硫醚、苯酚、1,2-乙二硫醇、三异丙基硅烷和水中的一种或多种组成;优选地,所述裂解液由tea、苯酚、1,2-乙二硫醇和三异丙基硅烷组成;其中tea、苯酚、1,2-乙二硫醇和三异丙基硅烷的体积比为90:5:2.5:2.5。进一步地,步骤(5)中,所述换盐方法为:流动相a:0.5-2%醋酸/水溶液(v/v);流动相b:乙腈;色谱柱:10μm的反相c18,77mm*250mm的色谱柱;检测波长:220nm;梯度洗脱:使用a相和b相的混合液,先用体积比为5-15%的乙腈平衡30-80min,再将b相的体积比在30-60min之内由10%上升至80%,并保持20-60min。本发明中v/v代表体积与体积的比。本发明中多肽固相合成法为本领域常用的方法,即为将前一步反应得到的保护氨基酸-树脂脱去fmoc保护基后,再与下一个保护氨基酸偶联反应。本发明中“-氨基酸(rx)-”括号里的rx为氨基酸的侧链保护基团;本发明中“fomc-氨基酸(rx)-oh”为保护氨基酸,fomc和oh为氨基酸的保护基团。与现有技术相比,本发明具有下述优点:(1)本发明采用片段法合成短肽链,使用短肽链fmoc-thr13-ser14-asp15-oh,直接避免了因14位点ser困难反应位点导致的缺失杂质,有利于剩余氨基酸的继续偶联,大大提高了索玛鲁肽粗品的纯度和收率,降低合成成本。(2)以往公开的专利中普遍使用逐一法偶联侧链或者直接偶联片段,但这些方法都无法避免片段难溶或者反应活性低导致的收率和纯度偏低的问题。本发明使用两步法偶联侧链,即使用的保护氨基酸为fmoc-aeea-aeea-oh和octa(otbu)-glu(α-otbu)-γ-cooh,改善了片段溶解性问题,表面活性剂的引入,更是极大提高了反应活性,提高了终产品的收率和纯度,提高了后端纯化制备的回收率和较低了难度。综上,本发明索玛鲁肽制备方法直接避免了thr13-ser14-asp15及aeea-aeea两处困难缩合位点单一氨基酸缺失质类杂质产生,使索玛鲁肽纯化难度大大降低,提高了产品收率和纯度,所得产品纯度大于99.0%,也降低了制备索玛鲁肽的成本,具有广泛的实用价值和应用前景。显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。附图说明图1为本发明制备的索玛鲁肽的ms图谱。图2为本发明制备的索玛鲁肽的hplc图谱。具体实施方式本发明具体实施方式中部分使用的原料、设备均为已知产品,通过购买市售产品获得。本发明中涉及的英文缩写所对应的中文名称见表1所示:表1本发明中涉及的英文缩写所对应的中文名称实施例1、本发明索玛鲁肽的制备使用均一替代度为0.28mmol/g的fmoc-gly-wang(购买自西安蓝晓科技新材料有限公司,批号un104f08-190221)为起始树脂载体,通过去fmoc保护和偶联反应,依次与表2所示的保护氨基酸偶联,制得索玛鲁肽肽树脂。表2本发明使用的保护氨基酸接肽顺序n=保护氨基酸分子量2fmoc-arg(pbf)-oh6483fmoc-gly-oh2974fmoc-arg(pbf)-oh6485fmoc-val-oh3396fmoc-leu-oh3537fmoc-trp(boc)-oh5268fmoc-ala-oh3119fmoc-ile-oh35310fmoc-phe-oh38711fmoc-glu(otbu)-oh42512fmoc-lys(alloc)-oh45213fmoc-ala-oh31114fmoc-ala-oh31115fmoc-gln(trt)-oh61016fmoc-gly-oh29717fmoc-glu(otbu)-oh42518fmoc-leu-oh35319fmoc-tyr(tbu)-oh45920fmoc-ser(tbu)-oh38421fmoc-ser(tbu)-oh38422fmoc-val-oh33923自制片段fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh71224fmoc-phe-oh38725fmoc-thr(tbu)-oh39726fmoc-gly-oh29727fmoc-glu(otbu)-oh42528fmoc-aib-oh32529boc-his(trt)-oh49830自制片段fmoc-aeea-aeea-oh53131自制片段octa(otbu)-glu-(α-otbu)-oh556具体制备方法如下:1、自制片段的制备(1)fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh的制备a.溶胀:将100g(90mmol)替代度为0.9mmol/g的ctcresin树脂(购买自吉尔生化(上海)有限公司,批号gls190202-48101),加入1500ml二氯甲烷,混合40min后,滤除二氯甲烷,该树脂备用。b.替代树脂:将100mmol的fmoc-asp(otbu)-oh溶于1500ml二氯甲烷,加入300mmol的diea,将溶液于0-10℃下搅拌激活5min后,倒入步骤a得到的ctc树脂中,于20-25℃条件下混合10min后,补加20ml的diea,继续混合50min。待反应结束后,加入甲醇100ml,继续混合30min。反应结束后,抽滤,树脂用二氯甲烷洗5次,每次1500ml。即得到fmoc-asp(otbu)-ctc。c.去保护:在fmoc-asp(otbu)-ctc中加入20%哌啶/dmf溶液(v/v)1000ml,于20-30℃条件下混合5min后,抽干;加入dmf1000ml,混合5min后,抽干;加入20%哌啶/dmf溶液(v/v)1000ml,于20-30℃条件下混合10min后,抽干;加入dmf1500ml,混合5min后,抽干。重复用dmf洗涤8次,每次1500ml,每次混合5min。d.偶联:依次加入300mmol的fmoc-ser(tbu)-oh、300mmoltbtu和300mmolhobt,加入3:1的dmf/dcm溶液1200ml,于0-10℃条件下加入400mmol的diea,激活5min。将以上激活液缓慢加入到反应釜中,于20-25℃条件下混合2h。待反应结束后,抽干,加入dmf1500ml,混合5min后,抽干。重复用dmf洗涤6次,每次1500ml,每次混合5min。最后用茚三酮检测为阴性,即得到fmoc-ser(tbu)-asp(otbu)-ctc。e.偶联fmoc-thr(tbu)-oh:重复上述c和d操作,将上述d操作中的fmoc-ser(tbu)-oh改为fmoc-thr(tbu)-oh,加入量为300mmol,其余试剂及其比例均不变,即得到181g的fmoc-thr(tbu)-ser(tbu)-asp(otbu)-ctc。f.裂解:加入1000ml三氟乙醇/dcm溶液(v/v=1:3),在25℃条件下搅拌反应2h后,过滤,滤饼用三氟乙醇的dcm溶液抽洗3次,合并滤液,于30℃条件下浓缩至剩余体积约200ml体积的浓缩液。将该浓缩液缓慢倒入冷冻的甲叔醚中,搅拌30min充分析固体后,过滤,滤渣用甲叔醚抽洗3次后,将该固体真空干燥,即得到75g短肽链fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh,收率为94.50%,hplc纯度为98.51%。(2)fmoc-aeea-aeea-oh的制备a.溶胀:将100g(90mmol)替代度为0.9mmol/g的ctcresin树脂(购买自吉尔生化(上海)有限公司,批号gls190202-48101)加入1500ml二氯甲烷,混合40min后,滤除二氯甲烷,该树脂备用。b.替代树脂:将100mmol的fmoc-aeea-oh溶于1500ml二氯甲烷,其余步骤与“(1)fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh的制备”中步骤b操作完全相同,即得到fmoc-aeea-ctc。c.去保护:与“(1)fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh的制备”中步骤c操作完全相同。d.偶联:依次加入300mmol的fmoc-aeea-oh、300mmoltbtu和300mmolhobt,其余步骤与“(1)fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh的制备”中步骤d操作完全相同。最后用茚三酮检测为阴性,即得到155g的fmoc-aeea-aeea-ctc。e.裂解:与“(1)fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh的制备”中步骤f操作完全相同,即得到51g短肽链fmoc-aeea-aeea-oh,收率为89.61%,hplc纯度为99.13%。(3)octa(otbu)-glu-(α-otbu)-oh的制备a.溶胀:将100g(90mmol)替代度为0.9mmol/g的ctcresin树脂(购买自吉尔生化(上海)有限公司,批号gls190202-48101)加入1500ml二氯甲烷,混合40min后,滤除二氯甲烷,该树脂备用。b.替代树脂:将100mmol的fmoc-glu-(α-otbu)-oh溶于1500ml二氯甲烷,其余步骤与“(1)fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh的制备”中步骤b操作完全相同,即得到fmoc-glu-(α-otbu)-ctc。c.去保护:与“(1)fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh的制备”中步骤c操作完全相同。d.偶联:依次加入300mmol的fmoc-octa(otbu)-oh、300mmol的cl-hobt和400mmoldic,其余步骤与“(1)fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh的制备”中步骤d操作完全相同。最后用茚三酮检测为阴性,即得到166g的fmoc-octa(otbu)-glu-(α-otbu)-ctc。e.裂解:与“(1)fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh的制备”中步骤f操作完全相同,即得到55g的fmoc-octa(otbu)-glu-(α-otbu)-oh,收率为91.1%,hplc纯度为98.97%。2、索玛鲁肽肽树脂的合成1)fmoc-val-ser(tbu)-ser(tbu)-tyr(tbu)-leu-glu(otbu)-gly-gln(trt)-ala-ala-lys(r1)-glu(otbu)-phe-ile-ala-trp(boc)-leu-val-arg(pbf)-gly-arg(pbf)-gly-wang(中间体1)的制备取用40mmol的0.28mmol/g的fmoc-gly-wang,全部倒入反应釜中,用1500mldcm溶胀混合15min后抽干,按如下去保护和偶联操作进行:a.去保护:加入20%哌啶/dmf溶液(v/v)1000ml,于20-30℃条件下混合5min后,抽干,加入dmf1000ml,混合5min后,抽干。加入20%哌啶/dmf溶液(v/v)1000ml,于20-30℃条件下混合10min后,抽干。加入dmf1500ml,混合5min后,抽干。重复用dmf洗涤8次,每次1500ml,每次混合5min。b.偶联:依次加入80mmol的fmoc-arg(pbf)-oh、80mmoltbtu和80mmolhobt,加入3:1的dmf/dcm溶液1200ml,于0-10℃条件下加入120mmol的diea,激活5min。将以上激活液缓慢加入到反应釜中,于20-25℃条件下混合2h。待反应结束后,抽干,加入dmf1500ml,混合5min后,抽干。重复用dmf洗涤6次,每次1500ml,每次混合5min。最后用茚三酮检测为阴性,即得到fmoc-arg(pbf)-gly-wang。c.按上述a的去保护方法和b的偶联方法,依主链从c端至n端顺序,按照表2顺序,依次分别偶联剩余保护氨基酸,即从表2接肽顺序3开始,逐个偶联至22号val,即得到索玛鲁肽中间体a的wang肽树脂,备用。2)接入短肽链fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh,即为中间体2的制备将上述索玛鲁肽中间体a的wang肽树脂按照“1)中间体1的制备”中步骤a所述方法去保护操作后,依次加入80mmol的短肽链fmoc-thr(tbu)-ser(tbu)-asp(otbu)-oh、80mmol的cl-hobt,加入dmf/dcm/dmso(v:v:v=2:1:1)溶液1200ml,于0-10℃条件下加入120mmol的dic,激活5min。将以上激活液缓慢加入到反应釜中,于20-25℃条件下混合2h。待反应结束后,抽干,加入dmf1500ml,混合5min后,抽干。重复用dmf洗涤6次,每次1500ml,每次混合5min。最后用茚三酮检测为阴性即得到中间体2,备用。3)主链(中间体3)的制备按上述“1)中间体1的制备”中步骤a的去保护方法和步骤b的偶联方法,依主链从c端至n端顺序,按照表2顺序,依次分别偶联剩余保护氨基酸,即从表2接肽顺序24开始,逐个偶联至29号his,即得到索玛鲁肽主链(中间体3)的wang肽树脂,备用。(4)接入侧链短肽链fmoc-aeea-aeea-oh,制备中间体4a.脱alloc于中间体3中加入1500ml的dcm,依次加入150ml苯硅烷和15g四(三苯基膦)钯,于20-30℃条件下通氮气鼓泡30min后,抽干,用1500ml的dcm抽洗1次。再加入150ml苯硅烷和8g四(三苯基膦)钯,于20-30℃条件下通氮气鼓泡30min后,抽干,用1500ml的dcm抽洗5次,树脂备用。b.接入侧链短肽链fmoc-aeea-aeea-oh按“1)中间体1的制备”中步骤a的去保护操作后,依次加入80mmol的短肽链fmoc-aeea-aeea-oh、80mmol的pybop,80mmol的hoat,溶于dmf/dcm/nmp(v:v:v=5:3:2)溶液1200ml,溶液中加入表面活性剂为2%(v/v)的曲拉通,于0-10℃条件下加入120mmol的diea,激活5min。将以上激活液缓慢加入到反应釜中,于20-25℃条件下混合2h。待反应结束后,抽干,加入dmf1500ml,混合5min后,抽干。重复用dmf洗涤6次,每次1500ml,每次混合5min。最后用茚三酮检测为阴性即得到中间体4,备用。(5)接入侧链短肽链fmoc-octa(otbu)-glu-(α-otbu)-oh将中间体4按“1)中间体1的制备”中步骤a的去保护操作后,依次加入80mmol的短肽链fmoc-octa(otbu)-glu-(α-otbu)-oh,80mmol的pybop,200mmol的hoat,溶于dmf/dcm/nmp(v:v:v=5:3:2)溶液1200ml,溶液中加入表面活性剂为2%(v/v)的曲拉通,于0-10℃条件下加入120mmol的diea,激活5min。将以上激活液缓慢加入到反应釜中,于20-25℃条件下混合2h。待反应结束后,抽干,加入dmf1500ml,混合5min后,抽干。重复用dmf洗涤6次,每次1500ml,每次混合5min。最后用茚三酮检测为阴性。最后用二氯甲烷洗5次,每次800ml;洗毕,用甲醇洗两次,每次800ml;再用二氯甲烷洗2次,每次800ml;最后用醇洗3次,每次800ml,直至树脂充分分散开。将该树脂于20-30℃条件下真空干燥箱中干燥4h,直至恒重(连续两次称重,误差低于1%),得到wang树脂的全保护肽树脂324g。即得到索玛鲁肽的肽树脂,备用。3、索玛鲁肽粗品的制备取上述制备得到的索玛鲁肽的肽树脂,加入3240ml体积比为tfa:苯酚:1,2-乙二硫醇:三异丙基硅烷=90:5:2.5:2.5的裂解试剂(裂解试剂10ml/克树脂),搅拌均匀,室温搅拌反应3小时,反应混合物使用砂芯漏斗过滤,收集滤液,树脂再用少量tfa洗涤3次,合并滤液后减压浓缩,加入无水乙醚沉淀,再用无水乙醚洗沉淀3次,抽干得类白色粉末,即为索玛鲁肽粗品174g,收率为98.71%,粗品的hplc纯度为73.35%。4、索玛鲁肽精品的制备a.取上述制备得到的索玛鲁肽粗品,加水搅拌,用氨水调ph8.5至完全溶解,溶液用0.45μm混合微孔滤膜过滤,纯化备用;采用高效液相色谱法进行纯化,纯化用色谱填料为10μm的反相c18,流动相系统为0.1%tfa/水溶液-0.1%tfa/乙腈溶液,77mm*250mm的色谱柱流速为90ml/min,采用梯度系统洗脱,循环进样纯化,取粗品溶液上样于色谱柱中,启动流动相洗脱,收集主峰蒸去乙腈后,得索玛鲁肽纯化中间体浓缩液,含量45.9mg/ml,hplc纯度为99.25%。b.取索玛鲁肽纯化中间体浓缩液,用0.45μm滤膜滤过备用;采用高效液相色谱法进行换盐:流动相a:1%醋酸/水溶液(v/v);流动相b:乙腈;色谱柱:10μm的反相c18,77mm*250mm的色谱柱;检测波长:220nm;梯度洗脱:洗脱剂为a相与b相的混合液,先用10%的乙腈平衡60min,再将b相的体积比在45min之内由10%上升至80%,并保持30min。色谱柱流速为90ml/min(可根据不同规格的色谱柱,调整相应的流速);采用梯度洗脱,循环上样方法,上样于色谱柱中,启动流动相洗脱,采集图谱,观测吸收度的变化,收集换盐主峰并用分析液相检测纯度,合并换盐主峰溶液,减压浓缩,得到索玛鲁肽醋酸水溶液,冷冻干燥,得索玛鲁肽精品94.83g,总收率为54.5%。对制备得到索玛鲁肽精品进行ms和hplc检测,所得ms图如1所示,hplc图谱如图2所示。该索玛鲁肽纯品分子量:1029.29([m+4h]/4);纯度:99.41%;最大单一杂质0.3%。综上,本发明索玛鲁肽制备方法直接避免了thr13-ser14-asp15及aeea-aeea两处困难缩合位点单一氨基酸缺失质类杂质产生,使索玛鲁肽纯化难度大大降低,提高了产品收率和纯度,所得产品纯度大于99.0%,也降低了制备索玛鲁肽的成本,具有广泛的实用价值和应用前景。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1