一种甲酰氨基嘧磺隆或其衍生物中间体的制备方法与流程
本发明涉及精细化工技术领域,具体而言,涉及一种甲酰氨基嘧磺隆或其衍生物中间体的制备方法。
背景技术:
甲酰氨基嘧磺隆(试验代号:aef130360,通用名称:foramsulfuron,商品名称:cornstar、康施它,其它名称:甲酰氨磺隆)是由安万特公司开发的新型磺酰脲类除草剂。化学名称为1-(4,6-二甲氧基嘧啶-2-基)-3-(2-二甲基氨基羰基-5-甲酰氨基苯基磺酰基)脲,英文化学名称为1-(4,6-dimethoxypyrimidin-2-y1)-3-(2-dimethoxylcarbamoyl-5-formamidophenylsulfonyl)urea。
甲酰氨基嘧磺隆是支链氨基酸生物合成关键酶als(乙酰乳酸合成酶)抑制剂,其能够被杂草的根和叶吸收,并在植株体内迅速传导,阻碍缬氨酸、异亮氨酸、亮氮酸合成,抑制细胞分裂和生长。敏感杂草根和叶在吸收药剂后,幼芽和根部迅会速停止生长,幼嫩组织发黄,随后枯死。
现有2-二甲基氨基-5-硝基苯磺酰胺的制备方法主要是:以对硝基甲苯邻磺酸为起始原料,硝酸高温氧化制得2-羧酸-5-硝基苯磺酸,再以二氯亚砜、盐酸二甲胺为原料得到2-二甲氨基-5-硝基苯磺酸,然后以三光气作为卤化试剂,制得2-二甲氨基-5-硝基苯磺酰氯,再以氨水氨化得到2-二甲氨基-5-硝基苯磺酰胺。
如上的制备方法中,需要采用冰乙酸为溶剂硝酸高温氧化法,危险性较大,而且由于需要以三光气作为卤化试剂,工业生产安全隐患较大。
有鉴于此,特提出本发明。
技术实现要素:
本发明的第一目的在于提供一种甲酰氨基嘧磺隆中间体的制备方法,本发明制备方法反应步骤少工艺安全简便,不仅能够减少了三废的排放,而且对环境友好。
本发明的第二目的在于提供一种甲酰氨基嘧磺隆的制备方法。
为了实现本发明的上述目的,特采用以下技术方案:
一种甲酰氨基嘧磺隆或其衍生物中间体的制备方法,包括:以糖精为原料,经氨化和硝化反应后,得到2-二甲基氨基羰基-5-硝基苯磺酰胺,即为甲酰氨基嘧磺隆中间体。
同时,本发明还提供了一种甲酰氨基嘧磺隆的制备方法,所述制备方法包括:先按照本发明方法制备2-二甲基氨基羰基-5-硝基苯磺酰胺;然后,再以所制得的2-二甲基氨基羰基-5-硝基苯磺酰胺为原料,制备甲酰氨基嘧磺隆或其衍生物。
与现有技术相比,本发明的有益效果为:
本发明中,以糖精为原料制备甲酰氨基嘧磺隆中间体化合物,不仅污染少,成本低,而且制备反应步骤少,反应条件温和,安全易操作,生产更为环保,适于大规模工业化生产。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,以下将对实施例或现有技术描述中所需要使用的附图作简单地介绍。
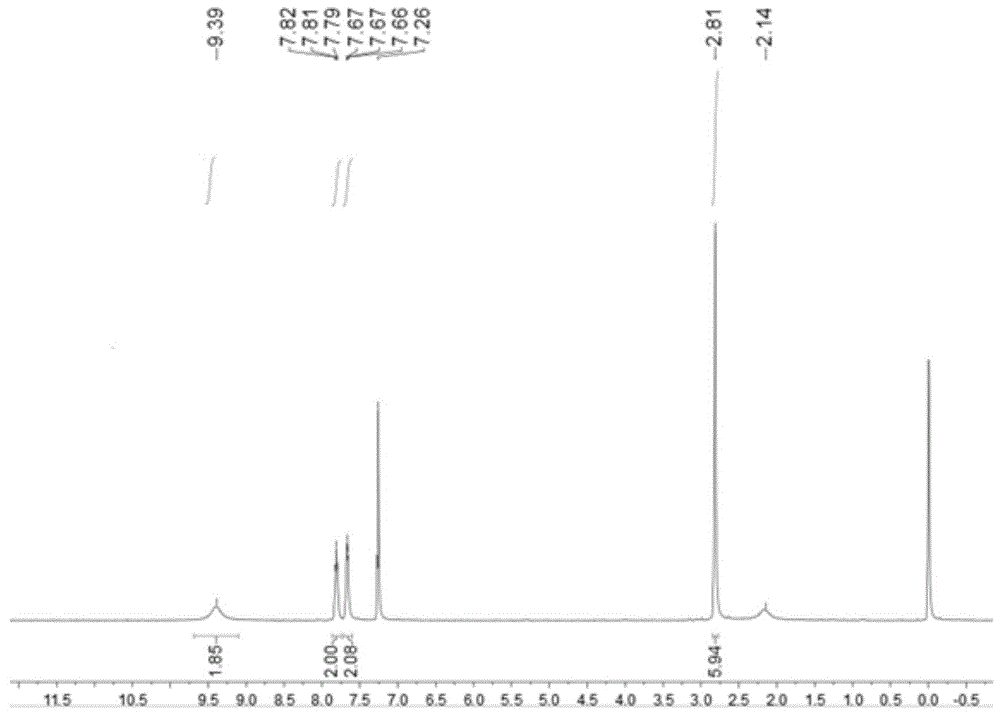
图1为实施例1产物2-二甲基氨基羰基-5-硝基苯磺酰胺的核磁谱图;
图2为实施例2步骤(a)产物化合物iv核磁图谱。
具体实施方式
下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
本发明所提供的制备方法,是一种制备甲酰氨基嘧磺隆中间体化合物的方法,更具体而言,是一种是制备2-二甲基氨基羰基-5-硝基苯磺酰胺的方法。
不同于传统的以对硝基甲苯类化合物为起始原料的制备方法,本发明中,创造性的以糖精为起始原料,并经两步反应得到目标化合物,从而简化了反应流程,而且反应条件更为温和,污染小。
本发明所提供的甲酰氨基嘧磺隆或其衍生物中间体的制备方法可参考如下:以糖精为原料,经氨化和硝化反应后,得到2-二甲基氨基羰基-5-硝基苯磺酰胺,即为甲酰氨基嘧磺隆中间体。
在本发明的一些实施方式中,如上所述甲酰胺基嘧磺隆中间体可以由如下所示反应路线(i)得到:
具体反应步骤包括:
(a)向溶有化合物i的溶液中,加入催化剂和氨化试剂,反应得到化合物ii;
(b)向溶有化合物ii的溶液中,加入催化剂和硝化试剂,反应得到化合物iii。
在本发明优选的一些实施方式中,如上反应路线(i)步骤(a)中,用以溶解化合物i的溶剂包括甲醇,乙腈,1,4-二氧六环,n,n-二甲基甲酰胺,苯,甲苯或者二甲苯中的一种或几种;
优选的,溶剂的摩尔用量为原料化合物i摩尔用量的5~90倍。
在本发明优选的一些实施方式中,如上反应路线(i)步骤(a)中,所述催化剂包括:硫酸,盐酸,醋酸以及对甲苯磺酸中的至少一种;
优选的,催化剂与化合物i摩尔比为(0.01-4):1,二者的摩尔比例可以为,但不限于0.05:1,0.1:1,0.3:1,0.5:1,1:1,1.5:1,2:1,2.5:1,3:1,4:1等。
在本发明优选的一些实施方式中,如上反应路线(i)步骤(a)中,所述氨化试剂包括:二甲胺以及二甲胺盐酸盐中的至少一种;
优选的,二甲胺盐酸盐可以以固体形式加料;
优选的,二甲胺可以以固体形式加料,或者以二甲胺溶液的形式加料,例如可以以二甲胺甲醇溶液,二甲胺乙醇溶液,二甲胺四氢呋喃溶液等形式进行加料。
优选的,氨化试剂与化合物i的摩尔比为(1-20):1,二者的摩尔比里可以为,但不限于1:1,2:1,3:1,4:1,5:1,7:1,10:1,12:1,15:1,17:1,20:1等。
在本发明优选的一些实施方式中,如上反应路线(i)步骤(a)中,反应温度为-10℃-150℃(例如可以为,但不限于0℃,10℃,20℃,50℃,70℃,90℃,100℃,120℃,150℃等),反应时间为0.5-24h(例如可以为,但不限于1h,3h,5h,7h,10h,12h,15h,18h,24h等);
优选的,步骤(a)中,还包括在反应后,将反应液减压蒸馏,重结晶得到化合物ii的步骤。
在本发明优选的一些实施方式中,如上反应路线(i)步骤(b)中,用以溶解化合物ii的溶剂包括:硫酸,醋酸,醋酸酐,二氯甲烷,1.2-二氯乙烷,丙酮中的一种或多种;
优选的,溶剂摩尔用量为原料ⅱ摩尔量的2~95倍。
在本发明优选的一些实施方式中,如上反应路线(i)步骤(b)中,所述催化剂包括:醋酸酐,kno3,nano3,agno3,ca(no3)2,ni(no3)2中的一种或多种;
优选的,催化剂与化合物ⅱ的摩尔比为(0.01-4):1,二者的摩尔比例可以为,但不限于0.05:1,0.1:1,0.3:1,0.5:1,1:1,1.5:1,2:1,2.5:1,3:1,4:1等。
在本发明优选的一些实施方式中,如上反应路线(i)步骤(b)中,所述硝化试剂包括:硝酸(浓硝酸,优选为发烟硝酸),kno3,nano3,agno3,ca(no3)2以及ni(no3)2中的一种或多种;
优选的,硝化试剂与化合物ⅱ的摩尔比为(1-20):1,二者的摩尔比里可以为,但不限于1:1,2:1,3:1,4:1,5:1,7:1,10:1,12:1,15:1,17:1,20:1等。
在本发明优选的一些实施方式中,如上反应路线(i)步骤(b)中,包括:控制温度在-10℃-10℃(例如可以为,但不限于-5℃,0℃,5℃等),然后将硝化试剂加入溶剂(所用溶剂包括硫酸,醋酸,醋酸酐,二氯甲烷,1.2-二氯乙烷,丙酮中的一种或多种)中,混合(例如采用搅拌等方式)得到混合溶液;
将催化剂加入溶有化合物ii的溶液中,然后加入含有硝化试剂的混合溶液,在-20℃-80℃(例如可以为,但不限于-10℃,0℃,10℃,20℃,30℃,40℃,50℃,60℃,70℃,80℃等)条件下,反应0.5h-24h(例如可以为,但不限于1h,2h,4h,6h,12h,18h,24h等),反应结束后,将反应液倒入冰水混合物中,所得沉淀物经分离(例如采用过滤分离)后干燥,重结晶得到化合物iii(2-二甲基氨基羰基-5-硝基苯磺酰胺),即为甲酰氨基嘧磺隆中间体。
在本发明的一些实施方式中,如上所述甲酰胺基嘧磺隆中间体可以由如下所示反应路线(ii)得到:
具体步骤包括:
(a)向溶有化合物i的溶液中,加入催化剂,反应得到化合物iv;
(b)向溶有化合物iv的溶液中,加入氨化试剂,反应得到化合物ii;
(c)向溶有化合物ii的溶液中,加入催化剂和硝化试剂,得到化合物iii。
在本发明优选的一些实施方式中,如上反应路线(ii)步骤(a)中,用以溶解化合物i的溶剂包括:甲醇以及任选的其他溶剂;
其中,所述其他溶剂包括:乙腈,1,4-二氧六环,n,n-二甲基甲酰胺,苯,甲苯或者二甲苯中的一种或几种;
优选的,溶剂的摩尔用量为原料化合物i摩尔用量的5倍以上。
在本发明优选的一些实施方式中,如上反应路线(ii)步骤(a)中,所述催化剂包括硫酸或盐酸中的一种或两种;
优选的,催化剂与化合物i的摩尔比为(0.01-4):1,二者的摩尔比例可以为,但不限于0.05:1,0.1:1,0.3:1,0.5:1,1:1,1.5:1,2:1,2.5:1,3:1,4:1等。
在本发明优选的一些实施方式中,如上反应路线(ii)步骤(a)中,包括:控制温度在0℃-25℃(例如可以为,但不限于5℃、10℃、15℃、20℃等),向溶有化合物i的溶液中,加入催化剂,加料完成后,在0℃-80℃(例如可以为,但不限于5℃、10℃、15℃、20℃、30℃、40℃、50℃、60℃、70℃等等)条件下反应0.5-24h(例如可以为,但不限于1h,2h,4h,6h,12h,18h,24h等),反应结束后,降温至室温,重结晶得化合物iv。
在本发明优选的一些实施方式中,如上反应路线(ii)步骤(b)中,用以溶解化合物iv的溶剂包括:甲醇,乙醇,二氯甲烷,1.2-二氯乙烷,四氢呋喃,乙腈中的一种或多种;
优选的,溶剂摩尔用量为原料ⅳ摩尔量的2倍以上。
在本发明优选的一些实施方式中,如上反应路线(ii)步骤(b)中,所述氨化试剂包括:二甲胺以及二甲胺盐酸盐中的至少一种;
优选的,二甲胺盐酸盐可以以固体形式加料;
优选的,二甲胺可以以固体形式加料,或者以二甲胺溶液的形式加料,例如可以以二甲胺甲醇溶液,二甲胺乙醇溶液,二甲胺四氢呋喃溶液等形式进行加料。
优选的,氨化试剂与化合物iv的摩尔比为(1-20):1,二者的摩尔比里可以为,但不限于1:1,2:1,3:1,4:1,5:1,7:1,10:1,12:1,15:1,17:1,20:1等。
在本发明优选的一些实施方式中,如上反应路线(ii)步骤(b)包括:向溶有化合物iv的溶液中,加入氨化试剂,然后在在0℃-80℃(例如可以为,但不限于5℃、10℃、15℃、20℃、30℃、40℃、50℃、60℃、70℃等等)条件下反应0.5-48h(例如可以为,但不限于1h,2h,4h,6h,12h,18h,24h,30h,36h等),反应结束后,将反应液减压蒸馏,得到化合物ii。
在本发明优选的一些实施方式中,如上反应路线(ii)中,步骤(c)可以参照反应路线(i)中步骤(b)的操作进行。
在本发明优选的一些实施方式中,如上反应路线(ii)步骤(c)中,用以溶解化合物ii的溶剂包括:硫酸,醋酸,醋酸酐,二氯甲烷,1.2-二氯乙烷,丙酮中的一种或多种;
优选的,溶剂摩尔用量为原料ⅱ摩尔量的2~95倍。
在本发明优选的一些实施方式中,如上反应路线(ii)步骤(c)中,所述催化剂包括:醋酸酐,kno3,nano3,agno3,ca(no3)2,ni(no3)2中的一种或多种;
优选的,催化剂与化合物ⅱ的摩尔比为(0.01-4):1,二者的摩尔比例可以为,但不限于0.05:1,0.1:1,0.3:1,0.5:1,1:1,1.5:1,2:1,2.5:1,3:1,4:1等。
在本发明优选的一些实施方式中,如上反应路线(ii)步骤(c)中,所述硝化试剂包括:硝酸(浓硝酸,优选为发烟硝酸),kno3,nano3,agno3,ca(no3)2以及ni(no3)2中的一种或多种;
优选的,硝化试剂与化合物ⅱ的摩尔比为(1-20):1,二者的摩尔比里可以为,但不限于1:1,2:1,3:1,4:1,5:1,7:1,10:1,12:1,15:1,17:1,20:1等。
在本发明优选的一些实施方式中,如上反应路线(ii)步骤(c)中,包括:控制温度在-10℃-10℃(例如可以为,但不限于-5℃,0℃,5℃等),然后将硝化试剂加入溶剂(所用溶剂包括硫酸,醋酸,醋酸酐,二氯甲烷,1.2-二氯乙烷,丙酮中的一种或多种)中,混合(例如采用搅拌等方式)得到混合溶液;
将催化剂加入溶有化合物ii的溶液中,然后加入含有硝化试剂的混合溶液,在-20℃-80℃(例如可以为,但不限于-10℃,0℃,10℃,20℃,30℃,40℃,50℃,60℃,70℃,80℃等)条件下,反应0.5h-24h(例如可以为,但不限于1h,2h,4h,6h,12h,18h,24h等),反应结束后,将反应液倒入冰水混合物中,所得沉淀物经分离(例如采用过滤分离)后干燥,重结晶得到化合物iii(2-二甲基氨基羰基-5-硝基苯磺酰胺),即为甲酰氨基嘧磺隆中间体。
进一步的,基于如上的制备方法,本发明还可以提供一种甲酰氨基嘧磺隆的制备方法,该制备方法中,首先按照如上方法得到2-二甲基氨基羰基-5-硝基苯磺酰胺,然后再以其为原料,得到最终产品甲酰氨基嘧磺隆(具体可参考现有技术,例如cn1414955a等中所公开的方法)。
以cn1414955a中所公开的方法为例,2-二甲基氨基羰基-5-硝基苯磺酰胺为原料,制备甲酰氨基嘧磺隆的反应方程可参考如下:
实施例1甲酰氨基嘧磺隆中间体制备:
(a)在500ml三口瓶中,室温下加入糖精(化合物i)25g,乙腈250ml,开启搅拌,缓慢滴加浓硫酸2.68g,然后加入二甲胺盐酸盐55.75g,加料完毕,开始升温至70℃,反应8小时;反应完毕,开始减压蒸馏,残余物采用硅胶层析柱法纯化,得到白色固体(化合物ii)26.5g,收率85%。
产品核磁共振氢谱分析如下:
1hnmr(400mhz,cdcl3):δ9.39(s,2h),7.87–7.75(m,2h),7.71–7.60(m,2h),2.81(s,6h)。
反应方程如下:
(b)在150ml三口瓶中,加入30ml冰乙酸,降温至0℃,开始滴加浓硝酸30ml,制成混酸。
将24g化合物ii加入到100ml三口瓶中,加入48ml冰醋酸,恒速下搅拌,降温至0℃,开始滴加混酸,控制反应温度0℃到15℃之间,反应4小时。将反应液倒在碎冰上,沉淀物经过滤,真空干燥,采用硅胶层析柱法纯化得到灰色固体(化合物iii,2-二甲基氨基羰基-5-硝基苯磺酰胺)24.5g,收率85%,产物核磁如图1所示。
反应方程如下:
实施例2
(a)在250ml三口瓶中,室温下加入ⅰ25g,甲醇100ml,开启搅拌,控制温度10℃-25℃之间,缓慢滴加浓硫酸8.03g,加料完毕,反应体系开始升温至70℃,反应12小时;反应完毕,降温至室温,重结晶得到白色固体ⅳ26.14g,收率89%,产物核磁如图2所示。
反应方程如下:
核磁共振氢谱分析如下:
1hnmr(400mhz,cdcl3)δ8.16(d,j=7.2hz,1h),7.87(d,j=7.2hz,1h),7.71–7.59(m,2h),5.72(s,2h),4.00(s,3h)。
(b)在500ml三口瓶中,加入ⅳ25g,四氢呋喃100ml,开启搅拌,控制温度10℃~25℃之间,缓慢滴加2m的二甲胺四氢呋喃溶液290ml,加料完毕,反应20小时;反应完毕,开始减压蒸馏,重结晶得到白色固体ⅱ23.86g,收率90%。
反应方程如下:
(c)在150ml三口瓶中,加入30ml冰乙酸,降温至0℃,开始滴加浓硝酸30ml,制成混酸。
将24g化合物ii加入到100ml三口瓶中,加入20ml冰醋酸,恒速下搅拌,降温至0℃,开始滴加混酸,控制反应温度0℃到15℃之间,反应4小时。将反应液倒在碎冰上,沉淀物经过滤,真空干燥,采用硅胶层析柱法纯化得到灰色固体(化合物iii,2-二甲基氨基羰基-5-硝基苯磺酰胺)24.5g,收率85%,产物核磁如图1所示。
反应方程如下:
实施例3
(a)在500ml三口瓶中,室温下加入糖精(化合物i)25g,n,n-二甲基甲酰胺150ml,开启搅拌,缓慢滴加浓盐酸11.06g,然后加入二甲胺盐酸盐55.75g,加料完毕,开始升温至100℃,反应6小时;反应完毕,开始减压蒸馏,残余物采用硅胶层析柱法纯化,得到白色固体(化合物ii)21.81g,收率70%。
反应方程如下:
(b)将20g化合物ii加入到250ml三口瓶中,加入120ml浓硫酸,恒速下搅拌,降温至0℃,开始加入11.18gnano3,控制反应温度0℃到15℃之间,反应6小时。将反应液倒在碎冰上,沉淀物经过滤,真空干燥,采用硅胶层析柱法纯化得到灰色固体(化合物iii,2-二甲基氨基羰基-5-硝基苯磺酰胺)17.96g,收率75%。
反应方程如下:
实施例4
(a)在250ml三口瓶中,室温下加入ⅰ25g,甲醇100ml,开启搅拌,控制温度10℃-25℃之间,缓慢滴加浓硫酸13.39g,加料完毕,反应体系开始升温至70℃,反应10小时;反应完毕,降温至室温,重结晶得到白色固体ⅳ23.5g,收率80%;
反应方程如下:
(b)在250ml三口瓶中,加入ⅳ20g,四氢呋喃120ml,开启搅拌,控制温度10℃~25℃之间,加入二甲胺盐酸盐22.74g,加料完毕,反应体系升温至70℃,反应12小时;反应完毕,开始减压蒸馏,重结晶得到白色固体ⅱ11.67g,收率55%。
反应方程如下:
(c)将20g化合物ii加入到250ml三口瓶中,加入120ml浓硫酸,恒速下搅拌,降温至0℃,开始加入11.18gnano3,控制反应温度0℃到15℃之间,反应6小时。将反应液倒在碎冰上,沉淀物经过滤,真空干燥,采用硅胶层析柱法纯化得到灰色固体(化合物iii,2-二甲基氨基羰基-5-硝基苯磺酰胺)17.96g,收率75%。
反应方程如下:
尽管已用具体实施例来说明和描述了本发明,然而应意识到,在不背离本发明的精神和范围的情况下可以作出许多其它的更改和修改。因此,这意味着在所附实施例中包括属于本发明范围内的所有这些变化和修改。
- 还没有人留言评论。精彩留言会获得点赞!