一种高稳定性的磺胺类药物抗体hAb4D11及其应用
本发明涉及生物技术和免疫检测领域,具体涉及一种高稳定性的磺胺类药物抗体hab4d11及其应用。
背景技术:
磺胺类药物(sulfonamides,sas)是一类抗菌谱较广、价格低廉、种类较多的化学合成抗菌剂,目前广泛用于兽医临床、畜牧和水产养殖中,来预防和治疗细菌感染性疾病。但其不合理使用甚至滥用,易造成sas在动物源食品中残留,继而威胁人类健康和食品安全。除了从源头上控制sas的不合理使用外,对动物源食品中的药物残留进行检测及监控,是保障食品安全的重要措施。因此有必要建立简便、快速、灵敏、广谱的残留检测方法。
目前,sas残留的检测主要使用色谱-串联质谱联用(lc-ms/ms)的理化分析方法。而该方法需要的仪器较为昂贵、样品前处理较为复杂、人员及操作较为专业,繁琐费时、检测成本较高,且不能现场操作,不适于大批量样本的快速筛查。
以抗原和抗体的特异性、可逆性结合反应为基础的免疫分析技术,具有速度快、成本低、灵敏度高的特点,目前被新修订的《食品安全法》认可,并被广泛用于动物源食品中sas的快速筛查。
通过小鼠免疫、脾细胞与瘤细胞融合、单克隆筛选,制备获得的单克隆抗体(mab),通常其对有机溶剂的耐受性能和热稳定性较差。而乙腈和甲醇等有机溶剂为样本前处理常用的试剂,因此常常需要在提取后,经过氮吹、复溶、稀释等步骤来减弱有机溶剂对免疫分析的影响。通过基因重组来制备重组抗体(hab),以提升其对有机溶剂的耐受性能和热稳定性,则可减化样本的前处理流程,从而缩短检测时间,提高检测效率。
技术实现要素:
为了解决上述技术问题,本发明提供了一种具有高稳定性、且其识别磺胺类药物的性能并未改变的磺胺类药物抗体hab4d11及其应用。
为了实现上述目的,本发明首先提供了一种高稳定性的磺胺类药物抗体hab4d11,包括重链及轻链,
所述重链是基于seqidno.1所示的氨基酸序列,将包括第1、5–6、9–10、12–13、16、23、38、40、43、67–68、71、74、76–77、83–84、87–88、91和114位在内的一个或多个氨基酸残基置换为其他氨基酸所得到的;所述重链的氨基酸序列与seqidno.1所示的氨基酸序列有至少94%的一致性;
所述轻链是基于seqidno.2所示的氨基酸序列,将包括第3、9、12–13、15、17、19、22、46、62、64、72–73、78、80–85、87、104和108位在内的一个或多个氨基酸残基置换为其他氨基酸所得到的;所述轻链的氨基酸序列与seqidno.2所示的氨基酸序列有至少89%的一致性。
作为优选,所述重链在seqidno.1所示的氨基酸序列中,至少进行了下列一个位点的置换:
第1位的谷氨酰胺置换为谷氨酸(q1e);
第5位的谷氨酰胺置换为缬氨酸(q5v);
第6位的谷氨酰胺置换为谷氨酸(q6e);
第9位的丙氨酸置换为甘氨酸(a9g);
第10位的谷氨酸置换为甘氨酸(e10g);
第12位的丙氨酸置换为缬氨酸(a12v);
第13位的精氨酸置换为谷氨酰胺(r13q);
第16位的丙氨酸置换为甘氨酸(a16g);
第23位的赖氨酸置换为丙氨酸(k23a);
第38位的赖氨酸置换为精氨酸(k38r);
第40位的精氨酸置换为丙氨酸(r40a);
第43位的谷氨酰胺置换为赖氨酸(q43k);
第67位的谷氨酰胺置换为精氨酸(q67r);
第68位的丙氨酸置换为苯丙氨酸(a68f);
第71位的苏氨酸置换为丝氨酸(t71s);
第74位的精氨酸置换为苏氨酸(r74t);
第76位的丝氨酸置换为赖氨酸(s76k);
第77位的丝氨酸置换为天冬酰胺(s77n);
第83位的亮氨酸置换为甲硫氨酸(l83m);
第84位的丝氨酸置换为天冬酰胺(s84n);
第87位的丙氨酸置换为精氨酸(a87r);
第88位的丝氨酸置换为丙氨酸(s88a);
第91位的丝氨酸置换为苏氨酸(s91t);
第114位的丝氨酸置换为亮氨酸(s114l);
进一步优选所述重链在seqidno.1所示的氨基酸序列中还对第28、30位中的一个以上氨基酸残基进行了置换;更优选将第28位的苏氨酸置换为天冬酰胺(t28n);第30位的苏氨酸置换为赖氨酸(t30k)。
作为优选,所述轻链在seqidno.2所示的氨基酸序列中,至少进行了下列一个位点的置换:
第3位的缬氨酸置换为谷氨酰胺(v3q);
第9位的丙氨酸置换为丝氨酸(a9s);
第12位的丙氨酸置换为丝氨酸(a12s);
第13位的缬氨酸置换为丙氨酸(v13a);
第15位的亮氨酸置换为缬氨酸(l15v);
第17位的谷氨酰胺置换为天冬氨酸(q17d);
第19位的丙氨酸置换为缬氨酸(a19v);
第22位的丝氨酸置换为苏氨酸(s22t);
第46位的谷氨酰胺置换为赖氨酸(q46k);
第62位的异亮氨酸置换为缬氨酸(i62v);
第64位的丙氨酸置换为丝氨酸(a64s);
第72位的精氨酸置换为甘氨酸(r72g);
第73位的脯氨酸置换为苏氨酸(p73t);
第78位的丝氨酸置换为苏氨酸(s78t);
第80位的天冬酰胺置换为丝氨酸(n80s);
第81位的脯氨酸置换为丝氨酸(p81s);
第82位的缬氨酸置换为亮氨酸(v82l);
第83位的谷氨酸置换为谷氨酰胺(e83q);
第84位的丙氨酸置换为脯氨酸(a84p);
第85位的天冬氨酸置换为谷氨酸(d85e);
第87位的缬氨酸置换为苯丙氨酸(v87f);
第104位的甘氨酸置换为谷氨酰胺(g104q);
第108位的亮氨酸置换为缬氨酸(l108v)。
进一步优选所述轻链在seqidno.2所示的氨基酸序列中还对第113位的氨基酸残基进行了置换;更优选将第113位的丙氨酸置换为苏氨酸(a113t)。
作为本发明的一种优选方案,在所述磺胺类药物抗体hab4d11中,所述重链的氨基酸序列如seqidno.3所示,所述轻链的氨基酸序列如seqidno.4所示。
本发明进一步提供一种核酸,其编码所述的磺胺类药物抗体hab4d11。
本发明进一步提供一种包含所述核酸的生物材料,所述生物材料为载体、宿主细胞。
本发明进一步提供一种包含所述核酸或生物材料在制备检测磺胺类药物试剂盒或试纸条、或在动物源性食品安全评价中的应用。
本发明进一步提供所述的磺胺类药物抗体hab4d11制备得到的磺胺类药物检测试剂或试剂盒或试纸条。
本发明进一步提供磺胺类药物抗体hab4d11在磺胺类药物检测中的应用,优选为以下任一应用:
(1)在制备磺胺类药物的荧光偏振检测试剂盒中的应用;
(2)在制备磺胺类药物的酶联免疫检测试剂盒中的应用;
(3)在制备磺胺类药物的侧流层析检测试纸条中的应用。
本发明所述的所述磺胺类药物包括氨苯磺胺、磺胺醋酰、磺胺胍、磺胺苯吡唑、酞磺胺噻唑、磺胺二甲异噁唑、磺胺噻唑、磺胺甲基异噁唑、磺胺二甲噁唑、磺胺甲噻二唑、磺胺硝苯、柳氮磺胺吡啶、磺胺吡啶、磺胺氯哒嗪、磺胺甲氧哒嗪、磺胺乙氧哒嗪、磺胺喹噁啉、磺胺氯吡嗪、磺胺邻二甲氧嘧啶、磺胺苯酰、磺胺甲氧吡嗪、磺胺二甲基异嘧啶、磺胺间甲氧嘧啶、磺胺对甲氧嘧啶、磺胺嘧啶、磺胺二甲基嘧啶、磺胺间二甲氧嘧啶、磺胺甲基嘧啶、磺胺溴二甲嘧啶中的一种或几种。
本发明提供磺胺类药物包被抗原,是由所述磺胺半抗原hs(6-(4-aminophenylsulfonamido)hexanoicacid)与载体蛋白偶联后得到。其中,所述载体蛋白选自牛血清白蛋白(bsa)、卵清蛋白(ova)、钥孔血蓝蛋白(klh)、甲状腺球蛋白(tg)、人血清白蛋白(hsa);优选bsa、ova。
在本发明的一个具体实施方式中,所述磺胺类药物包被抗原,是将磺胺半抗原hs与bsa偶联得到的hs-bsa。
本发明提供磺胺类药物荧光标记半抗原,是由所述磺胺半抗原hs与荧光素偶联后得到。其中,所述荧光素选自5-氨基荧光素(5-af)、6-氨基荧光素(6-af)、5-氨甲基荧光素(5-amf)、4’-氨甲基荧光素(4’-amf)、异硫氰酸荧光素乙二胺衍生物(edf);优选5-amf、4’-amf、edf。
在本发明的一个具体实施方式中,所述磺胺类药物荧光标记半抗原,是将磺胺半抗原hs与5-af偶联得到的hs-5af。
借由上述技术方案,本发明至少具有下列优点及有益效果:
本发明中的抗体hab4d11在识别磺胺类药物的性能并未改变的情况下,同时具有耐热性和耐有机溶剂性,与seqidno.1~2所示的磺胺类药物抗体mab4d11相比,tm值可提高至少5~10℃,有机溶剂耐受性可提高至少5~18%。而且,该抗体hab4d11还具有较为广泛的识别范围。
利用本发明提供的重组抗体hab4d11,在样本前处理时无需氮吹、复溶,仅需提取后稀释,便可用于检测,有利于缩短检测时间,提高检测效率,在兽药残留检测中具有良好的应用前景。
除此之外,本发明提供的氨基酸突变位点及突变氨基酸,也可为其他抗体热稳定性和有机溶剂耐受性的改造提供一定参考。
附图说明
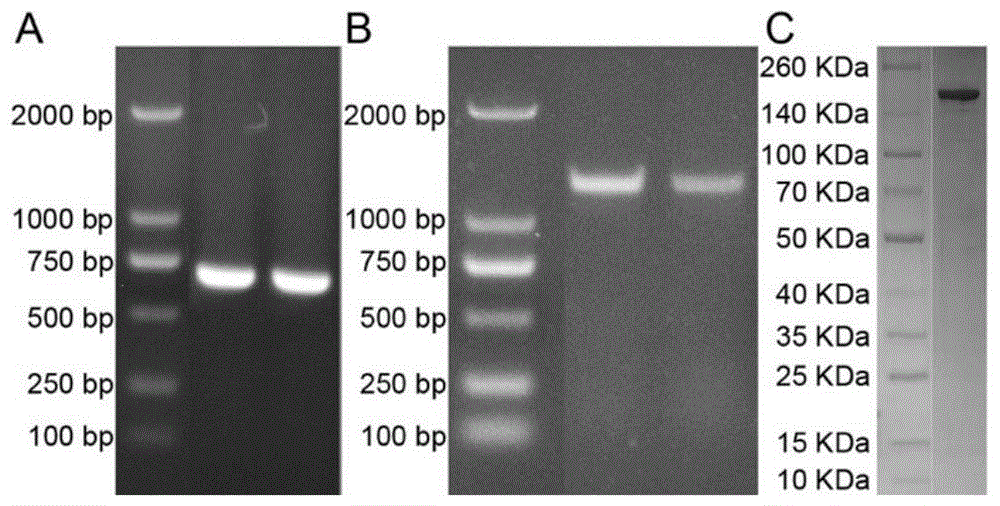
图1为本发明实施例1中轻链、重链dna片段电泳图,抗体sds-page电泳图;
图2为本发明实施例2中抗体溶解温度tm测定曲线;
图3为本发明实施例4中磺胺类药物包被原maldi-tof图;
图4为本发明实施例6中荧光标记半抗原与抗体结合曲线;
图5为本发明实施例6中磺胺类药物smz在fpia中的竞争标准曲线;
图6为本发明实施例7中磺胺类药物smz在elisa中的竞争标准曲线。
具体实施方式
以下实施例用于说明本发明,但不用来限制本发明的范围。若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段,所用原料均为市售商品。
实施例1重组抗体hab4d11的制备和鉴定
1、所述磺胺类药物重组抗体hab4d11的重链的氨基酸序列如seqidno.3所示,在seqidno.1的基础上进行了q1e、q5v、q6e、a9g、e10g、a12v、r13q、a16g、k23a、t28n、t30k、k38r、r40a、q43k、q67r、a68f、t71s、r74t、s76k、s77n、l83m、s84n、a87r、s88a、s91t、s114l的置换;所述磺胺类药物重组抗体hab4d11的轻链的氨基酸序列如seqidno.4所示,在seqidno.2的基础上进行了v3q、a9s、a12s、v13a、l15v、q17d、a19v、s22t、q46k、i62v、a64s、r72g、p73t、s78t、n80s、p81s、v82l、e83q、a84p、d85e、v87f、g104q、l108v、a113t。
2、选择全合成,分别合成获得重链和轻链的重组基因。
3、根据表达载体pcdna5多克隆位点和重链质粒上的酶切位点,使用hindiii和paci进行双酶切,将重链基因克隆至真核表达载体上。
4、使用bamhi和xhoi进行双酶切,将轻链基因克隆至上述表达载体上。
5、将载体转化进入dh5α感受态细胞中,借助氨苄西林抗性,挑取阳性单菌落,进行pcr和测序鉴定。
6、选择正确序列的菌株,提取质粒,用于下一步的转染及表达。
7、采用脂质体转染的方法,将上述质粒转染flp-in-cho细胞,培养过程中,加入潮霉素,来进行抗性筛选。
8、将稳定表达抗体的cho细胞传代培养,加入四环素诱导表达,并收集上清。
9、使用基于proteing的亲和色谱法,对重组抗体进行纯化。
10、重组质粒经pcr鉴定,重组抗体经sds-page鉴定,均成功,结果如图1所示,其中,轻链dna片段的大小为660bp左右(图1a),重链dna片段的大小为1350bp左右(图1b),大小正确;抗体大小在150kda左右(图1c),证明抗体表达成功。
实施例2重组抗体hab4d11的热稳定性测定
1、将hab4d11和mab4d11(重链序列如seqidno.1所示,轻链序列如seqidno.2所示)分别加入uni管中。
2、随着温度的升高,使用蛋白稳定性分析仪测定内源荧光光谱的变化。
3、软件拟合,得出荧光光谱随温度的变化规律曲线。
4、求取一介导数,其峰值即为tm值。
5、其结果如图2所示,其中mab4d11的tm值为65.7℃,而hab4d11的tm值为76.3℃,提升10.6℃。
实施例3重组抗体hab4d11的有机溶剂耐受性测定
1、将一定量的乙腈或者甲醇等试剂加入fpia的反应缓冲液中,配制成含0%、1%、2%、5%、10%和20%有机溶剂的缓冲液。
2、以磺胺二甲基嘧啶(smz)作为代表性sas,以hs-5af为荧光标记半抗原,用上述缓冲液分别配制成含有不同含量有机溶剂的标准品溶液。
3、建立smz在不同有机溶剂含量下的校正曲线,以ic50值(半数抑制浓度)、δfp值(最大与最小fp值的差值)和δfp/ic50值作为判断标准,以此考察hab和mab对有机溶剂的耐受能力。
4、其结果如表1所示,和mab4d11相比,hab4d11对甲醇的耐受性能增加10%,对乙腈的耐受性能增加18%。
表1hab4d11与mab4d11对甲醇和乙腈的耐受性能比较
实施例4磺胺类药物检测用包被原hs-bsa的制备
1、取0.5mmol的hs,155mg的n,n’-dicyclohexylcarbodiimide(dcc),85mg的n-hydroxysuccinimide(nhs),加入1mldmf中,室温过夜搅拌,对半抗原羧基进行酯化(活化)。
2、将活化产物取出,4000rpm离心10min。
3、称取660mg的bsa,溶于20ml预冷的pbs中。
4、取活化产物中离心后的上清液,逐滴缓慢加入bsa溶液中,4℃条件下过夜搅拌。
5、将上述反应产物置于透析袋中,透析三天,每8小时更换一次透析液。
6、取出产物,分装后冻存于-20℃冰柜,即为包被原hs-bsa。
7、取合成的磺胺类药物包被原经maldi-tof测定,如图3所示,hs-bsa主峰的m/z为68207.9(图3b),而bsa为64763.1(图3a),表明半抗原与载体蛋白bsa偶联成功,其偶联摩尔比分别为12.0:1。
实施例5磺胺类药物检测用荧光标记半抗原hs-5af的制备
1、取0.5mmol的hs,155mg的dcc,85mg的nhs,加入1mldmf中,室温过夜搅拌,对半抗原羧基进行酯化。
2、将活化产物取出,4000rpm离心10min。
3、称取210mg的5-af,溶于5ml的dmf中。
4、取活化产物中离心后的上清液,逐滴缓慢加入5-af溶液中,避光过夜搅拌。
5、将上述反应产物置于薄层色谱板上,使用chcl3:ch3oh:ch3cooh(6:1:0.07,v/v/v)为展开剂,分离纯化产物。
6、取迁移率(rf)为0.45的条带,经甲醇洗脱后冻存于-20℃冰柜,即为荧光标记半抗原hs-5af。
实施例6磺胺类药物fpia方法的建立
1、试剂配制
反应缓冲液:na2b4o710h2o5.72g,h3bo38.66g,加蒸馏水至1l,混匀。
2、抗体与荧光标记物结合曲线
使用反应缓冲液稀释荧光标记半抗原,选择荧光强度为反应缓冲液荧光强度的20倍时,为其最佳稀释度,以每孔70μl的体积加入96孔黑色、不透明、低结合酶标板中。使用反应缓冲液将抗体倍比稀释,依次加入96孔酶标板中。再加入70μl的反应缓冲液,使得每孔总体积为210μl。混匀,读取fp值。结果如图4所示,选择70%与荧光标记半抗原结合的抗体浓度为最佳浓度,其为1.6μg/ml。
3、标准曲线建立
将单环类磺胺(氨苯磺胺、磺胺醋酰、磺胺胍),五元杂环双环类磺胺(磺胺苯吡唑、酞磺胺噻唑、磺胺二甲异噁唑、磺胺噻唑、磺胺甲基异噁唑、磺胺二甲噁唑、磺胺甲噻二唑)和六元杂环双环类磺胺(磺胺硝苯、柳氮磺胺吡啶、磺胺吡啶、磺胺氯哒嗪、磺胺甲氧哒嗪、磺胺乙氧哒嗪、磺胺喹噁啉、磺胺氯吡嗪、磺胺邻二甲氧嘧啶、磺胺苯酰、磺胺甲氧吡嗪、磺胺二甲基异嘧啶、磺胺间甲氧嘧啶、磺胺对甲氧嘧啶、磺胺嘧啶、磺胺二甲基嘧啶、磺胺间二甲氧嘧啶、磺胺甲基嘧啶、磺胺溴二甲嘧啶)等标准品使用反应缓冲液配制8个浓度梯度,每个浓度3个平行孔,做竞争fpia,绘制标准曲线,计算ic50值,其中smz的标准曲线如图5所示。
4、交叉反应率测定
将上述ic50值与smz的ic50值对比,得到交叉反应率,结果如表2所示。本研究建立的竞争fpia方法对所测定的29种磺胺类药物均存在一定程度的交叉反应率。
表2fpia方法ic50值及抗体交叉反应率
实施例7磺胺类药物elisa方法的建立
1、试剂配制
包被缓冲液:na2co31.59g,nahco32.93g,加蒸馏水至1l,混匀。
封闭缓冲液:小牛血清50ml,蔗糖50g,酪蛋白2.5g,na2hpo4·12h2o5.8g,nah2po4·2h2o0.593g,proclin300300μl,加蒸馏水定容至1l,混匀,置4℃冰箱保存。
抗体稀释液:nah2po4·2h2o0.6g,na2hpo41.072g,nacl16g,kcl0.4g,proclin300200μl,tritonx-100500μl,加蒸馏水至1l,混匀,置4℃冰箱保存。
标准品稀释液:na2hpo4·12h2o2.9g,nah2po4·2h2o0.59g,nacl8.5g,kcl0.2g,加蒸馏水水定容至1l,混匀。
酶标抗体稀释液:nah2po4·2h2o0.6g,na2hpo41.072g,nacl16g,kcl0.4g,proclin300200μl,蒸馏水950ml,溶解后加入50ml已灭活小牛血清,混匀,置4℃冰箱保存。
洗涤缓冲液(20×):na2hpo4·12h2o23.2g,kh2po42g,nacl64g,kcl0.036g,tween-2020ml,proclin300300μl,加水980ml定容至1l。稀释20倍使用。
底物缓冲液:na2hpo4·12h2o3.68g,柠檬酸0.933g,加蒸馏水至100ml。
tmb储存液:取10mgtmb溶于4ml乙二醇,避光保存。
底物液:取tmb储存液0.4ml,底物缓冲液10ml,30%h2o210μl,避光保存。
终止缓冲液:取98%浓硫酸22.2ml,加蒸馏水177.8ml,混匀。
2、方阵滴定
采用方阵滴定法筛选最佳的包被原浓度和抗体稀释度。使用包被缓冲液将包被原稀释成1:75000,1:50000,1:25000和1:12500,从第1至第4列依次纵向加入96孔酶标板中,包被。使用抗体稀释液将抗体稀释成1:10000,1:7500,1:5000和1:2500,每个稀释度设置1个重复,从第1至第8行依次横向加入96孔酶标板。同时,每一个包被原、抗体浓度组合,加入5ng/ml的smz,进行竞争反应。
方阵滴定结果见表3,初步选择od值1.5,相邻两孔od值有较大变化,且竞争较好的包被浓度及对应的抗体稀释度组合。从表3中选择包被原1:25000的浓度和抗体1:7500的稀释度组合。
表3抗体hab4d11与hs-bsa方阵滴定法
3、标准曲线建立
将单环类磺胺(氨苯磺胺、磺胺醋酰、磺胺胍),五元杂环双环类磺胺(磺胺苯吡唑、酞磺胺噻唑、磺胺二甲异噁唑、磺胺噻唑、磺胺甲基异噁唑、磺胺二甲噁唑、磺胺甲噻二唑)和六元杂环双环类磺胺(磺胺硝苯、柳氮磺胺吡啶、磺胺吡啶、磺胺氯哒嗪、磺胺甲氧哒嗪、磺胺乙氧哒嗪、磺胺喹噁啉、磺胺邻二甲氧嘧啶、磺胺苯酰、磺胺甲氧吡嗪、磺胺二甲基异嘧啶、磺胺间甲氧嘧啶、磺胺对甲氧嘧啶、磺胺嘧啶、磺胺二甲基嘧啶、磺胺间二甲氧嘧啶、磺胺甲基嘧啶、磺胺溴二甲嘧啶)等标准品配制8个浓度梯度,每个浓度3个平行孔,做间接竞争elisa,绘制标准曲线,计算ic50值,其中smz的标准曲线如图6所示。
4、交叉反应率测定
将上述ic50值与smz的ic50值对比,得到交叉反应率,结果如表4所示。本研究建立的间接竞争elisa方法对所测定的29种磺胺类药物均存在一定程度的交叉反应率。
表4elisa方法ic50值及抗体交叉反应率
虽然,上文中已经用一般性说明、具体实施方式及试验,对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
序列表
<110>中国农业大学
<120>一种高稳定性的磺胺类药物抗体hab4d11及其应用
<130>khp191115471.0
<160>4
<170>siposequencelisting1.0
<210>1
<211>441
<212>prt
<213>人工序列(artificialsequence)
<400>1
glnileglnleuglnglnserglyalagluleualaargproglyala
151015
servalargleusercyslysalaserglytyrthrphethrthrtyr
202530
trpleuglntrpleulysglnargproglyglnglyleuglutrpile
354045
glyalailetyrproglyasnglyaspthrargtyrpheproasnphe
505560
lysglyglnalathrleuthralaaspargserserserthralatyr
65707580
leuglnleuserserleualasergluaspseralavaltyrtyrcys
859095
alaargleuleuargthraspphealametasptyrtrpglyglngly
100105110
thrservalthrvalserseralalysthrthrproproservaltyr
115120125
proleualaproglyseralaalaglnthrasnsermetvalthrleu
130135140
glycysleuvallysglytyrpheprogluprovalthrvalthrtrp
145150155160
asnserglyserleuserserglyvalhisthrpheproalavalleu
165170175
glnseraspleutyrthrleuserserservalthrvalproserser
180185190
thrtrpprosergluthrvalthrcysasnvalalahisproalaser
195200205
serthrlysvalasplyslysilevalproargaspcysglycyslys
210215220
procysilecysthrvalprogluvalserservalpheilephepro
225230235240
prolysprolysaspvalleuthrilethrleuthrprolysvalthr
245250255
cysvalvalvalaspileserlysaspaspprogluvalglnpheser
260265270
trpphevalaspaspvalgluvalhisthralaglnthrglnproarg
275280285
glugluglnpheasnserthrpheargservalsergluleuproile
290295300
methisglnasptrpleuasnglylysgluphelyscysargvalasn
305310315320
seralaalapheproalaproileglulysthrileserlysthrlys
325330335
glyargprolysalaproglnvaltyrthrileproproprolysglu
340345350
glnmetalalysasplysvalserleuthrcysmetilethraspphe
355360365
pheprogluaspilethrvalglutrpglntrpasnglyglnproala
370375380
gluasntyrlysasnthrglnproilemetaspthraspglysertyr
385390395400
phevaltyrserlysleuasnvalglnlysserasntrpglualagly
405410415
asnthrphethrcysservalleuhisgluglyleuhisasnhishis
420425430
thrglulysserleuserhisserpro
435440
<210>2
<211>218
<212>prt
<213>人工序列(artificialsequence)
<400>2
aspilevalleuthrglnserproalaserleualavalserleugly
151015
glnargalathrilesercysargthrsergluservalaspthrtyr
202530
glyileserpheilehistrptyrglnglnlysproglyglnpropro
354045
lysleuleuiletyrargalaserasnleugluserglyileproala
505560
argpheserglyserglyserargproaspphethrleuserileasn
65707580
provalglualaaspaspvalalathrtyrtyrcysglnglnserasp
859095
lysaspproglythrpheglyglyglythrlysleugluilelysarg
100105110
alaaspalaalaprothrvalserilepheproproserserglugln
115120125
leuthrserglyglyalaservalvalcyspheleuasnasnphetyr
130135140
prolysaspileasnvallystrplysileaspglysergluarggln
145150155160
asnglyvalleuasnsertrpthraspglnaspserlysaspserthr
165170175
tyrsermetserserthrleuthrleuthrlysaspglutyrgluarg
180185190
hisasnsertyrthrcysglualathrhislysthrserthrserpro
195200205
ilevallysserpheasnargasnglucys
210215
<210>3
<211>441
<212>prt
<213>人工序列(artificialsequence)
<400>3
gluileglnleuvalgluserglyglyglyleuvalglnproglygly
151015
servalargleusercysalaalaserglytyrasnphelysthrtyr
202530
trpleuglntrpleuargglnalaproglylysglyleuglutrpile
354045
glyalailetyrproglyasnglyaspthrargtyrpheproasnphe
505560
lysglyargphethrleuseralaaspthrserlysasnthralatyr
65707580
leuglnmetasnserleuargalagluaspthralavaltyrtyrcys
859095
alaargleuleuargthraspphealametasptyrtrpglyglngly
100105110
thrleuvalthrvalserseralalysthrthrproproservaltyr
115120125
proleualaproglyseralaalaglnthrasnsermetvalthrleu
130135140
glycysleuvallysglytyrpheprogluprovalthrvalthrtrp
145150155160
asnserglyserleuserserglyvalhisthrpheproalavalleu
165170175
glnseraspleutyrthrleuserserservalthrvalproserser
180185190
thrtrpprosergluthrvalthrcysasnvalalahisproalaser
195200205
serthrlysvalasplyslysilevalproargaspcysglycyslys
210215220
procysilecysthrvalprogluvalserservalpheilephepro
225230235240
prolysprolysaspvalleuthrilethrleuthrprolysvalthr
245250255
cysvalvalvalaspileserlysaspaspprogluvalglnpheser
260265270
trpphevalaspaspvalgluvalhisthralaglnthrglnproarg
275280285
glugluglnpheasnserthrpheargservalsergluleuproile
290295300
methisglnasptrpleuasnglylysgluphelyscysargvalasn
305310315320
seralaalapheproalaproileglulysthrileserlysthrlys
325330335
glyargprolysalaproglnvaltyrthrileproproprolysglu
340345350
glnmetalalysasplysvalserleuthrcysmetilethraspphe
355360365
pheprogluaspilethrvalglutrpglntrpasnglyglnproala
370375380
gluasntyrlysasnthrglnproilemetaspthraspglysertyr
385390395400
phevaltyrserlysleuasnvalglnlysserasntrpglualagly
405410415
asnthrphethrcysservalleuhisgluglyleuhisasnhishis
420425430
thrglulysserleuserhisserpro
435440
<210>4
<211>218
<212>prt
<213>人工序列(artificialsequence)
<400>4
aspileglnleuthrglnserproserserleuseralaservalgly
151015
aspargvalthrilethrcysargthrsergluservalaspthrtyr
202530
glyileserpheilehistrptyrglnglnlysproglylyspropro
354045
lysleuleuiletyrargalaserasnleugluserglyvalproser
505560
argpheserglyserglyserglythraspphethrleuthrileser
65707580
serleuglnprogluaspphealathrtyrtyrcysglnglnserasp
859095
lysaspproglythrpheglyglnglythrlysvalgluilelysarg
100105110
thraspalaalaprothrvalserilepheproproserserglugln
115120125
leuthrserglyglyalaservalvalcyspheleuasnasnphetyr
130135140
prolysaspileasnvallystrplysileaspglysergluarggln
145150155160
asnglyvalleuasnsertrpthraspglnaspserlysaspserthr
165170175
tyrsermetserserthrleuthrleuthrlysaspglutyrgluarg
180185190
hisasnsertyrthrcysglualathrhislysthrserthrserpro
195200205
ilevallysserpheasnargasnglucys
210215
- 还没有人留言评论。精彩留言会获得点赞!