噁二唑取代苯磺酰胺类化合物及其制备方法与作为碳酸酐酶抑制剂的应用与流程
本申请要求申请日为2019年12月6日,申请号为201911240568.x,发明名称为“噁二唑取代苯磺酰胺类化合物及其制备方法与作为碳酸酐酶抑制剂的应用”的中国专利申请的优先权,该申请文件的全部内容作为参考并入本申请文件中。
本发明属于药学研究领域,具体涉及一种噁二唑取代苯磺酰胺类化合物或其药学上可接受的盐,其制备方法,以及用于制备作为碳酸酐酶抑制剂的药物的用途。
背景技术:
碳酸酐酶(cas)是一类重要的含锌酶,能催化co2/h2o和hco3-/h+离子的相互转化。自然界中碳酸酐酶分为有7个大类,但在人体中只有α-ca存在。迄今为止,在人类碳酸酐酶中发现16个亚型,它们分布于不同的细胞、细胞器和组织中,具有多种独特的动力学性质,成为青光眼、高原缺氧、癫痫、癌症、白血病、肥胖、关节炎等病症重要的研究靶点。
近年来报道了大量的苯磺酰胺类化合物作为caⅰ、ⅱ、ix和xii抑制剂,研究表明苯磺酰胺类化合物是cas抑制剂设计的重要组成模块,同时苯磺酰胺类化合物的尾部对cas的抑制性和选择性至关重要。因此,合成不同理化性质尾部的化合物,成为改善药物药效、选择性和降低毒副作用的重要手段。
技术实现要素:
本发明专利的一方面是提供式i所示的一类噁二唑取代苯磺酰胺类化合物或其药学上可接受的盐。
其中,r为萘基、联苯基、二甲苯基、氯苯基、二甲氨基苯基、二甲氧基苯基、三甲氧基苯基、硝基苯基、丙氧基苯基、异丙氧基苯基、丁氧基苯基、异丁氧基苯基、甲磺酰基苯基、三氟甲氧基苯基、氟苯基甲氧基苯基;
由选自cl、br、f、c1至c3烷氧基和c1至c3烷基中的1个取代基取代的含有一个n原子的六元芳香杂环基;
羰基、甲氧基羰基、乙氧基羰基或丙氧基羰基;
甲基、乙基、丙基、丁基、苯甲基或苯乙基;或
c3至c6环烷基。
优选地,r为萘基、联苯基、二甲苯基、氯苯基、二甲氨基苯基、二甲氧基苯基、三甲氧基苯基、硝基苯基、丙氧基苯基、异丙氧基苯基、丁氧基苯基、异丁氧基苯基、甲磺酰基苯基、三氟甲氧基苯基、氟苯基甲氧基苯基;
由选自br、甲氧基、乙氧基、丙氧基、甲基、乙基、丙基中的1个取代基取代的含有一个n原子的六元芳香杂环基;
羰基、甲氧基羰基、乙氧基羰基或丙氧基羰基;
甲基、乙基、丙基、丁基、苯甲基或苯乙基;或
环丙基、环丁基、环戊基或环己基。
进一步优选地,根据本发明的式i所示的一类噁二唑取代苯磺酰胺类化合物选自如下化合物:
4-(5-(萘-2-基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(2,4-二甲基苯基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-([1,1'-联苯]-4-基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(2-氯苯基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(3-氯苯基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(4-(二甲氨基)苯基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(2,6-二甲氧基苯基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(2,4,6-三甲氧基苯基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(吡啶-4-基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(吡啶-3-基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(5-溴吡啶-2-基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(4-甲氧基吡啶-3-基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(2-甲氧基吡啶-3-基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-苯乙基-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-环丙基-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-环戊基-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-环己基-1,3,4-噁二唑-2-基)苯磺酰胺;
5-(4-氨磺酰苯基)-1,3,4-噁二唑-2-羧酸乙酯;
4-(5-(4-硝基苯基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(4-丙氧基苯基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(4-异丙氧基苯基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(4-异丁氧基苯基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(4-(甲磺酰基)苯基)-1,3,4-噁二唑-2-基)苯磺酰胺;
4-(5-(4-(三氟甲氧基)苯基)-1,3,4-噁二唑-2-基)苯磺酰胺;和
4-(5-(4-((3-氟苄基)氧基)苯基)-1,3,4-噁二唑-2-基)苯磺酰胺。
所述“药学上可接受的盐”为通式(i)化合物与无机酸或有机酸反应形成的常规的无毒盐。例如,所述常规的无毒盐可通过通式(i)化合物与无机酸或有机酸反应制得,所述无机酸包括盐酸、氢溴酸、硫酸、硝酸、胺基磺酸和磷酸等,以及所述有机酸包括柠檬酸、酒石酸、乳酸、丙酮酸、乙酸、苯磺酸、对甲苯磺酸、甲磺酸、萘磺酸、乙磺酸、萘二磺酸、马来酸、苹果酸、丙二酸、富马酸、琥珀酸、丙酸、草酸、三氟乙酸、硬酯酸、扑酸、羟基马来酸、苯乙酸、苯甲酸、水杨酸、谷氨酸、抗坏血酸、对胺基苯磺酸、2-乙酰氧基苯甲酸和羟乙磺酸等;或者通式(i)化合物与丙酸、草酸、丙二酸、琥珀酸、富马酸、马来酸、乳酸、苹果酸、酒石酸、柠檬酸、天冬氨酸或谷氨酸形成酯后再与无机碱形成的钠盐、钾盐、钙盐、铝盐或铵盐;或者通式(i)化合物与有机碱形成的甲胺盐、乙胺盐或乙醇胺盐;或者通式(i)化合物与赖氨酸、精氨酸、鸟氨酸形成酯后再与盐酸、氢溴酸、氢氟酸、硫酸、硝酸、磷酸形成的对应的无机酸盐或与甲酸、乙酸、苦味酸、甲磺酸和乙磺酸形成的对应的有机酸盐。
本发明专利的再一方面是提供了一种式i所示的噁二唑取代苯磺酰胺类化合物或其药学上可接受的盐的制备方法。反应流程如下:
以对羧基苯磺酰胺为原料,经过、肼解、希夫碱缩合和氧化环合,得到目标产物噁二唑取代苯磺酰胺类衍生物。其中酯化、肼解、希夫碱缩合各个步骤的具体反应条件可以按照本领域中常规的设计进行,例如所述酯化反应可以参照文献(europeanjournalofmedicinalchemistry,2018,156:430-443),所述肼解反应可以参照文献(bioorganic&medicinalchemistryletters,2018,28(14):2369-2374)、所述希夫碱缩合可以参照文献(acsmedicinalchemistryletters,2017,8(8):792-796)等。
可选择地,第四步骤环合反应可以以次氯酸钠或碘作为氧化剂,365-600nm的光照射,室温反应2-5小时,4-(2-亚甲基肼-1-羰基)苯磺酰胺类衍生物发生分子内环合反应,得到环合产物式i所示化合物,其中取代基r的定义如前所述。
本发明的另一方面是提供式i所示化合物或其药学上可接受的盐的在制备碳酸酐酶抑制剂的药物中的用途。所述碳酸酐酶抑制剂可以用于治疗青光眼、高原缺氧、癫痫、癌症、白血病、肥胖、关节炎等疾病。
本发明的第四方面是提供含有式i所示化合物或其药学上可接受的盐作为活性成分的药物组合物。
根据本发明的药物组合物,所述药物组合物包括治疗有效量的式i所示化合物或其药学上可接受的盐以及药物辅料。术语“有效量”可指为实现预期的效果所需的剂量和时段的有效的量。此有效量可能因某些因子而产生不同的变化,如疾病的种类或治疗时疾病的病症、被施用的特定标的器官的构造、病人个体大小、或疾病或症状的严重性。本领域具有通常知识者不需要过度实验即可凭经验决定特定化合物的有效量。所述“药物辅料”是指药物中常规采用的各种辅料,例如赋形剂、控释剂、稳定剂等,这属于本领域技术人员常规知识范围。
根据本发明的所述药物组合物可以是以下剂型:片剂例如但不限于普通片剂、速释片、缓释片、控释片、薄膜衣片、糖衣片、口含片、舌下片、生物粘附片等;胶囊剂例如但不限于硬胶囊、软胶囊等;注射剂例如但不限于无菌或者含抑菌剂的水性注射剂、油性注射剂、冷冻干粉针剂、注射用微球等;喷雾剂例如但不限于口腔喷雾剂、鼻腔喷雾剂、局部皮肤喷雾剂等;气雾剂例如但不限于肺吸入用气雾剂、局部皮肤气雾剂等;滴鼻剂例如但不限于滴鼻用溶液、滴鼻用凝胶等;粉雾剂例如但不限于空腔用粉雾剂、鼻腔用粉雾剂、局部皮肤用粉雾剂等;人体其他腔道如阴道、直肠、耳腔等用的栓剂、贴剂、凝胶剂。这些制剂的制备工艺是本领域技术人员根据已有的知识或者参考相关教科书或工具书或文献而可以制备的。
有益效果
本发明的化合物制备工艺简单,关键步骤反应条件温和、收率更高、能耗更低、更环保。本发明专利提供的制备式i所示的噁二唑取代苯磺酰胺类衍生物的方法科学合理,具有操作简便、成本低廉、反应易于控制等特点。本发明的化合物作为碳酸酐酶抑制剂,显示良好的开发潜力。
附图说明
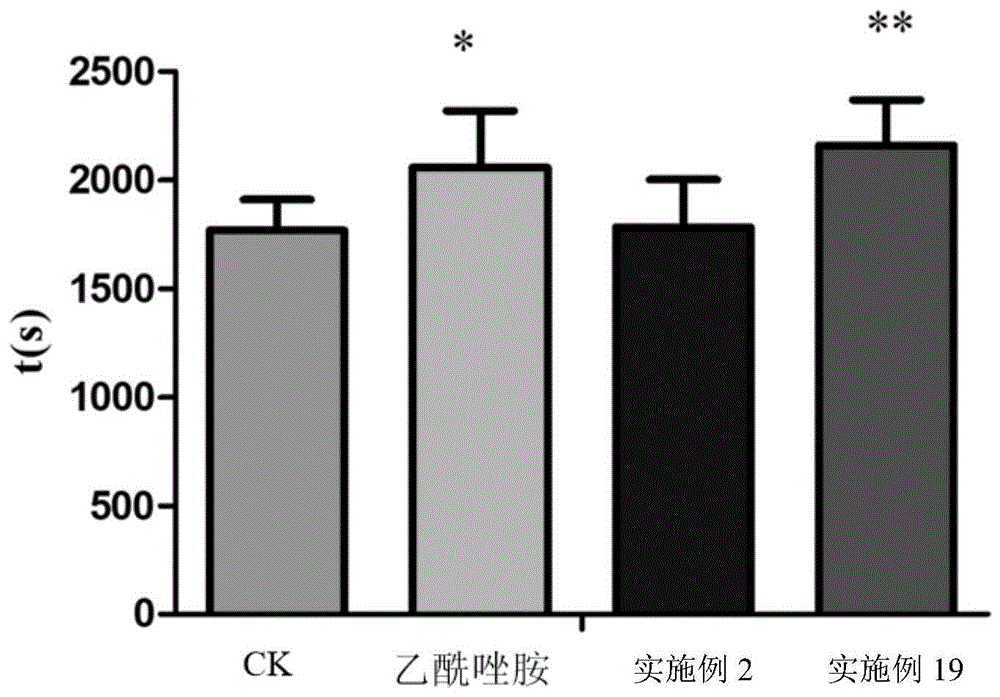
图1为试验实施例2中常压缺氧条件下小鼠耐受力实验。
具体实施方式
以下,将详细地描述本发明。在进行描述之前,应当理解的是,在本说明书和所附的权利要求书中使用的术语不应解释为限制于一般含义和字典含义,而应当在允许发明人适当定义术语以进行最佳解释的原则的基础上,根据与本发明的技术方面相应的含义和概念进行解释。因此,这里提出的描述仅仅是出于举例说明目的的优选实例,并非意图限制本发明的范围,从而应当理解的是,在不偏离本发明的精神和范围的情况下,可以由其获得其他等价方式或改进方式。
以下实施例仅是作为本发明的实施方案的例子列举,并不对本发明构成任何限制,本领域技术人员可以理解在不偏离本发明的实质和构思的范围内的修改均落入本发明的保护范围。
下述实施例中的实验方法,如无特殊说明,均为常规方法。
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径获得。
实施例1:4-(5-(萘-2-基)-1,3,4-噁二唑-2-基)苯磺酰胺的合成
第一步:4-氨磺酰苯甲酸甲酯的制备
将浓硫酸(1ml)滴加入到4-氨基磺酰苯甲酸(2.010g,10mmol)的甲醇(60ml)的混合物中,在回流下反应,直到tlc显示反应完成。然后,在减压下除去溶剂,将残留物加入氢氧化钠水溶液中和调节ph6-7。然后搅拌并过滤混合物,得到2.000g白色固体,产率为93.0%。1hnmr(dmso-d6)δppm:8.14(d,j=8.0hz,2h,ar-h),7.97(d,j=8.0hz,2h,ar-h),7.59(s,2h,so2nh2),3.90(t,3h,ch3);13cnmr(dmso-d6)δppm:165.81,148.54,132.85,130.43,126.61,53.19;esi-msm/z:计算值c8h9no4s[m+h]+:216.0286,实测值:216.0356。
第二步:4-(肼羰基)苯磺酰胺的制备
将水合肼(2.33g,46.5mmol)、4-氨磺酰苯甲酸甲酯(2.000g,9.3mmol)加入甲醇(70ml)中,在50℃下搅拌混合物,直到薄层色谱显示反应完成。然后减压除去溶剂,残渣加入乙酸乙酯(50ml),然后搅拌0.5小时后过滤混合物,烘干得到1.727g白色固体,产率为86.4%。1hnmr(dmso-d6)δppm:9.98(s,1h,nh),7.97(d,j=8.0hz,2h,ar-h),7.88(d,j=8.0hz,2h,ar-h),7.48(s,2h,so2nh2),4.57(s,2h,nh2);13cnmr(dmso-d6)δppm:165.20,146.63,136.77,128.17,126.19;esi-msm/z:计算值c7h9n3o3s[m+h]+:216.0398,实测值:216.0436。
第三步:4-(2-(萘-2-亚甲基)肼羰基)苯磺酰胺的制备
将1-萘甲醛(1.248g,2.0mmoll)加入到4(肼基羰基)-苯磺酰胺(1.720g,2mmol)的乙醇(5ml)的混合物中,将混合物在回流下搅拌反应,直到tlc显示反应完成。然后对混合物进行过滤,得到0.632g的白色固体,产率为89.6%。1hnmr(dmso-d6)δppm:12.13(s,1h,nh),9.13(s,1h,ch),8.89(d,j=8.0hz,1h,ar-h),8.16-7.61(m,10h,ar-h),7.58(s,2h,so2nh2);13cnmr(dmso-d6)δppm:1662.60,148.97,147.29,136.84,134.09,131.34,130.75,130.20,129.93,129.40,128.92,128.59,127.98,126.88,126.37,126.15,125.62,124.74;esi-msm/z:计算值c18h15n3o3s[m+h]+:354.0868,实测值:354.0907。
第四步:4-(5-(萘-2-基)-1,3,4-噁二唑-2-基)苯磺酰胺的合成
将4-(2-(萘-2-亚甲基)肼羰基)苯磺酰胺(200mg,0.57mmol)加入naclo(56mg,0.76mmol)和碳酸铯(205mg,0.63mmol)在甲醇(100ml)和丙酮(100ml)中的混合物中,搅拌,室温下用铊灯照射tlc,反应完成。然后,过滤混合物并减压除去溶剂,用二氯甲烷和甲醇(v/v=50:1)硅胶柱层析纯化残渣,得到175mg白色固体,产率88.1%。1hnmr(dmso-d6)δppm:9.21(d,j=8.0hz,1h,ar-h),8.45(m,1h,ar-h),8.40(d,j=8.0hz,2h,ar-h),8.27(d,j=8.0hz,1h,ar-h),8.13(d,j=8.0hz,1h,ar-h),8.09(d,j=8.0hz,2h,ar-h),7.82-7.68(m,4h,ar-h),7.63(s,2h,so2nh2);13cnmr(dmso-d6)δppm:164.97,163.30,147.38,133.98,133.47,129.79,129.60,129.51,128.92,128.06,127.42,127.24,126.69,126.03,125.94,120.02;esi-msm/z:计算值c18h13n3o3s[m+h]+:352.0711,实测值:352.0750。
实施例2:4-(5-(2,4-二甲基苯基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率64.5%。1hnmr(dmso-d6)δppm:8.31(d,j=8.0hz,2h,ar-h),8.05(d,j=8.0hz,2h,ar-h),7.99(d,j=8.0hz,1h,ar-h),7.62(s,2h,so2nh2),7.52(m,2h,ar-h),7.30(s,1h,ar-h),7.27(d,j=8.0hz,1h,ar-h),2.68(s,3h,ch3),2.38(s,3h,ch3);13cnmr(dmso-d6)δppm:165.33,163.00,147.20,142.31,138.26,132.96,129.51,127.84,127.22,126.76,120.03,22.08,21.48;esi-msm/z:计算值c16h15n3o3s[m+h]+:330.0868,实测值:330.0907。
实施例3:4-(5-([1,1'-联苯]-4-基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率81.7%。1hnmr(dmso-d6)δppm:8.37(d,j=8.0hz,2h,ar-h),8.24(d,j=8.0hz,2h,ar-h),8.07(d,j=8.0hz,2h,ar-h),7.97(d,j=8.0hz,2h,ar-h),7.80(m,2h,ar-h),7.64(s,2h,so2nh2),7.54(m,2h,ar-h),7.46(m,1h,ar-h);13cnmr(dmso-d6)δppm:164.89,163.72,147.28,144.13,139.24,129.68,128.98,128.13,128.00,127.93,127.44,127.22,126.71,122.56;esi-msm/z:计算值c20h15n3o3s[m+h]+:378.0868,实测值:378.0907。
实施例4:4-(5-(2-氯苯基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率64.4%。1hnmr(dmso-d6)δppm:8.31(d,j=8.0hz,2h,ar-h),8.18(m,1h,ar-h),8.07(d,j=8.0hz,2h,ar-h),7.78-7.57(m,5h,ar-h,so2nh2);13cnmr(dmso-d6)δppm:164.01,163.16,147.62,133.99,132.44,131.81,128.47,128.01,127.30,126.42,122.78;esi-msm/z:计算值c14h10cln3o3s[m+h]+:336.0102,实测值:336.0205。
实施例5:4-(5-(3-氯苯基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率67.8%。1hnmr(dmso-d6)δppm:8.33(d,j=8.0hz,2h,ar-h),8.20(dd,1h,ar-h),8.09(d,j=8.0hz,2h,ar-h),7.80-7.62(m,5h,ar-h,so2nh2);13cnmr(dmso-d6)δppm:164.01,163.17,147.51,134.00,132.44,132.02,131.80,128.47,128.03,127.31,126.47,122.80;esi-msm/z:计算值c14h10cln3o3s[m+h]+:336.0102,实测值:336.0203。
实施例6:4-(5-(4-(二甲氨基)苯基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率52.5%。1hnmr(dmso-d6)δppm:8.28(d,j=8.0hz,2h,ar-h),8.04(d,j=8.0hz,2h,ar-h),7.93(d,j=8.0hz,2h,ar-h),7.60(s,2h,so2nh2),6.87(d,j=8.0hz,2h,ar-h),3.04(s,6h,ch3);13cnmr(dmso-d6)δppm:165.70,162.49,152.99,146.85,128.65,127.49,127.18,127.00,112.28,109.88;esi-msm/z:计算值c16h16n4o3s[m+h]+:345.0977,实测值:345.1018。
实施例7:4-(5-(2,6-二甲氧基苯基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率62.3%。1hnmr(dmso-d6)δppm:8.25(d,j=8.0hz,2h,ar-h),8.05(d,j=8.0hz,2h,ar-h),7.62(m,3h,ar-h,so2nh2),6.87(d,j=8.0hz,2h,ar-h),3.79(s,6h,ch3);13cnmr(dmso-d6)δppm:164.52,160.66,160.05,147.46,134.86,127.82,126.52,104.87,101.77,56.86;esi-msm/z:计算值c16h15n3o5s[m+h]+:362.0766,实测值:362.0806。
实施例8:4-(5-(2,4,6-三甲氧基苯基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率69.4%。1hnmr(dmso-d6)δppm:8.22(d,j=8.0hz,2h,ar-h),8.03(d,j=8.0hz,2h,ar-h),7.60(s,2h,so2nh2),6.41(s,2h,ar-h),6.87(d,j=8.0hz,2h,ar-h),3.89(s,3h,ch3),3.78(s,6h,ch3);13cnmr(dmso-d6)δppm:164.80,164.05,160.86,147.28,127.73,127.35,126.74,94.40,91.60,56.68;esi-msm/z:计算值c17h17n3o6s[m+h]+:392.0872,实测值:392.0911。
实施例9:4-(5-(吡啶-4-基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率68.5%。1hnmr(dmso-d6)δppm:8.89(d,j=8.0hz,2h,ar-h),8.37(d,j=8.0hz,2h,ar-h),8.09(m,4h,ar-h),7.64(s,2h,so2nh2);13cnmr(dmso-d6)δppm:164.47,163.54,151.53,147.60,130.87,128.17,127.24,126.41,120.91;esi-msm/z:计算值c13h10n4o3s[m+h]+:303.0507,实测值:303.0547。
实施例10:4-(5-(吡啶-3-基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率75.4%。1hnmr(dmso-d6)δppm:9.36(d,j=4.0hz,1h,ar-h),8.87(m,1h,ar-h),8.55(m,1h,ar-h),8.39(d,j=8.0hz,2h,ar-h),8.09(d,j=8.0hz,2h,ar-h),7.72(m,1h,ar-h),7.64(s,2h,so2nh2);13cnmr(dmso-d6)δppm:164.07,163.32,153.25,148.06,147.46,134.94,128.06,127.22,126.52,124.93,120.40;esi-msm/z:计算值c13h10n4o3s[m+h]+:303.0507,实测值:303.0546。
实施例11:4-(5-(5-溴吡啶-2-基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率63.5%。1hnmr(dmso-d6)δppm:8.99(dd,1h,ar-h),8.39(m,1h,ar-h),8.33(d,j=8.0hz,2h,ar-h),8.16(m,1h,ar-h),8.08(d,j=8.0hz,2h,ar-h),7.62(s,2h,so2nh2);13cnmr(dmso-d6)δppm:164.47,163.96,151.78,147.60,141.85,141.15,128.08,127.33,126.39,125.22,123.85;esi-msm/z:计算值c13h9brn4o3s[m+h]+:382.9558,实测值:382.9638。
实施例12:4-(5-(4-甲氧基吡啶-3-基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率62.8%。1hnmr(dmso-d6)δppm:8.97(dd,1h,ar-h),8.40(dd,1h,ar-h),8.34(d,j=8.0hz,2h,ar-h),8.06(d,j=8.0hz,2h,ar-h),7.62(s,2h,so2nh2),7.09(d,j=8.0hz,1h,ar-h),3.97(s,3h,ch3);13cnmr(dmso-d6)δppm:166.17,163.53,163.43,147.28,146.90,137.92,127.88,127.19,126.62,114.11,112.09,54.59;esi-msm/z:计算值c14h12n4o4s[m+h]+:333.0613,实测值:333.0552。
实施例13:4-(5-(2-甲氧基吡啶-3-基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率73.0%。1hnmr(dmso-d6)δppm:8.47(m,2h,ar-h),8.31(d,j=8.0hz,2h,ar-h),8.07(d,j=8.0hz,2h,ar-h),7.62(s,2h,so2nh2),7.28(m,1h,ar-h),4.07(s,3h,ch3);13cnmr(dmso-d6)δppm:163.81,162.51,160.84,151.29,147.37,140.24,127.90,127.27,126.60,117.89,107.35,54.64;esi-msm/z:计算值c14h12n4o4s[m+h]+:333.0613,实测值:333.0552。
实施例14:5-(4-氨磺酰苯基)-1,3,4-噁二唑-2-羧酸乙酯
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率53.9%。1hnmr(dmso-d6)δppm:8.28(d,j=8.0hz,2h,ar-h),8.06(d,j=8.0hz,2h,ar-h),7.64(s,2h,so2nh2),4.47(q,2h,ch2),1.38(t,3h,ch3);13cnmr(dmso-d6)δppm:165.10,157.51,154.56,147.88,146.90,128.66,127.40,125.90,63.59,14.61;esi-msm/z:计算值c11h11n3o5s[m+h]+:333.0613,实测值:298.0493。
实施例15:4-(5-苯乙基-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率82.5%。1hnmr(dmso-d6)δppm:8.15(d,j=8.0hz,2h,ar-h),8.01(d,j=8.0hz,2h,ar-h),7.59(s,2h,so2nh2),7.28(m,4h,ar-h),7.20(m,1h,ar-h),3.28(t,2h,ch2),3.12(t,2h,ch2);13cnmr(dmso-d6)δppm:167.35,163.54,147.15,140.33,128.96,128.92,127.60,1227.27,126.91,126.74,32.06,27.00;esi-msm/z:计算值c16h15n3o3s[m+h]+:330.0868,实测值:330.0907。
实施例16:4-(5-环丙基-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率68.7%。1hnmr(dmso-d6)δppm:8.16(d,j=8.0hz,2h,ar-h),8.01(d,j=8.0hz,2h,ar-h),7.58(s,2h,so2nh2),2.34(m,1h,ch),1.19(m,4h,ch2);13cnmr(dmso-d6)δppm:169.31,162.89,146.98,127.53,127.16,126.82,8.81,6.28;esi-msm/z:计算值c11h11n3o3s[m+h]+:266.0555,实测值:266.0594。
实施例17:4-(5-环戊基-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率76.3%。1hnmr(dmso-d6)δppm:8.18(d,j=8.0hz,2h,ar-h),8.02(d,j=8.0hz,2h,ar-h),7.59(s,2h,so2nh2),3.47(m,1h,ch),2.10(m,2h,ch2),1.93(m,2h,ch2),1.73(m,4h,ch2);13cnmr(dmso-d6)δppm:170.96,163.59,147.09,127.62,127.22,126.91,36.09,31.10,25.60;esi-msm/z:计算值c13h15n3o3s[m+h]+:294.0868,实测值:294.0907。
实施例18:4-(5-环己基-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率81.6%。1hnmr(dmso-d6)δppm:8.19(d,j=8.0hz,2h,ar-h),8.03(d,j=8.0hz,2h,ar-h),7.60(s,2h,so2nh2),3.08(m,1h,ch),2.10-1.28(m,10h,ch2);13cnmr(dmso-d6)δppm:170.67,163.32,147.09,127.62,127.22,126.87,30.08,25.70,25.20;esi-msm/z:计算值c14h17n3o3s[m+h]+:308.1024,实测值:308.1063。
实施例19:4-(5-(4-(二甲氨基)苯基)-1,3,4-噁二唑-2-基)苯磺酰胺甲磺酸盐
将甲磺酸(31mg,0.32mmol)加入4-(5-(4-(二甲氨基)苯基)-1,3,4-噁二唑-2-基)苯磺酰胺(100mg,0.29mmol)的甲醇溶液(5ml)中,50℃下反应2小时,减压蒸除溶剂,残留物中加入二氯甲烷-甲醇(4ml,v/v=50:1),得到红棕色固体100mg,收率71.0%。1hnmr(dmso-d6)δppm:8.19(d,j=8.0hz,2h,ar-h),8.03(d,j=8.0hz,2h,ar-h),7.60(s,2h,so2nh2),3.08(m,1h,ch),2.10-1.28(m,10h,ch2);esi-msm/z:计算值c17h20n4o6s2[m+h]+:345.0977,实测值:345.1017。
实施例20:4-(5-(4-硝基苯基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率74.0%。1hnmr(dmso-d6)δppm:8.50-8.38(m,6h,ar-h),8.09(d,j=8.0hz,2h,ar-h),7.62(s,2h,so2nh2);esi-msm/z:计算值c14h10n4o5s[m+h]+:347.0405,实测值:347.0445。
实施例21:4-(5-(4-丙氧基苯基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率59.4%。1hnmr(dmso-d6)δppm:8.33(d,j=8.0hz,2h,ar-h),8.08(m,4h,ar-h),7.61(s,2h,so2nh2),7.20(d,j=8.0hz,2h,ar-h),4.07(t,2h,och2),1.79(m,2h,ch2ch3),1.03(t,3h,ch2ch3);esi-msm/z:计算值c17h17n3o4s[m+h]+:360.0973,实测值:360.1013。
实施例22:4-(5-(4-异丙氧基苯基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率65.8%。1hnmr(dmso-d6)δppm:8.31(d,j=8.0hz,2h,ar-h),8.05(m,4h,ar-h),7.59(s,2h,so2nh2),7.16(d,j=8.0hz,2h,ar-h),4.78(m,1h,och),1.31(d,6h,j=4.0hz,chch3);esi-msm/z:计算值c17h17n3o4s[m+h]+:360.0973,实测值:360.1013。
实施例23:4-(5-(4-异丁氧基苯基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率71.5%。1hnmr(dmso-d6)δppm:8.32(d,j=8.0hz,2h,ar-h),8.07(m,4h,ar-h),7.57(s,2h,so2nh2),7.19(d,j=8.0hz,2h,ar-h),3.88(d,2h,j=8.0hz,och2),2.07(m,1h,ch),1.02(d,6h,j=8.0hz,chch3);esi-msm/z:计算值c18h19n3o4s[m+h]+:374.1130,实测值:374.1170。
实施例24:4-(5-(4-(甲磺酰基)苯基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率71.5%。1hnmr(dmso-d6)δppm:8.43-8.37(m,4h,ar-h),8.20(d,2h,j=8.0hz,ar-h),8.07(d,2h,j=8.0hz,ar-h),7.63(s,2h,so2nh2),3.35(s,3h,ch3);esi-msm/z:计算值c15h13n3o5s2[m+h]+:380.0330,实测值:380.0399。
实施例25:4-(5-(4-(三氟甲氧基)苯基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率53.8%。1hnmr(dmso-d6)δppm:8.35(d,j=8.0hz,2h,ar-h),8.30(d,j=8.0hz,2h,ar-h),8.07(d,j=8.0hz,2h,ar-h),7.67-7.63(m,4h,ar-h,so2nh2);esi-msm/z:计算值c15h10f3n3o4s[m+h]+:386.0378,实测值:386.0406。
实施例26:4-(5-(4-((3-氟苄基)氧基)苯基)-1,3,4-噁二唑-2-基)苯磺酰胺
除了替换相应的反应起始原料以外,根据实施例1的方法制备目标化合物,白色固体,收率65.1%。1hnmr(dmso-d6)δppm:8.32(d,j=8.0hz,2h,ar-h),8.07(m,4h,ar-h),7.57(s,2h,so2nh2),7.19(d,j=8.0hz,2h,ar-h),3.88(d,2h,j=8.0hz,och2),2.07(m,1h,ch),1.02(d,6h,j=8.0hz,chch3);esi-msm/z:计算值c21h16n3o4s[m+h]+:426.0879,实测值:426.0917。
试验实施例1:化合物对碳酸酐酶的抑制试验
根据碳酸酐酶可催化4-硝基邻苯二甲酸成邻苯二甲酸根离子产生颜色变化的远离,采用分光光度计测定405nm的数值变化。实验中以15mmhepes(ph7.5)为缓冲液,100mmnacl为离子强度调节剂。以乙酰唑胺为对照,每实验重复3次。化合物的测试浓度为30.0000,10.0000,3.3333,1.1111,0.3704,0.1235,0.0412,0.0137,0.0046,0.0015um/l,以及空白对照。hcaⅰ、ⅱ酶溶液与化合物混合液在25℃下孵育15分钟,之后加入邻苯二甲酸反应60分钟,记录吸光度值,并以抑制剂浓度为横坐标绘制曲线,计算ic50,利用chenge-prusoff方程计算ki,结果见表1。实施例1-18所得化合物对hcaⅰ、ⅱ均有抑制作用,特别是对hcaⅰ抑制作用,远强于对照药乙酰唑胺。
表1
试验实施例2:代表化合物抗常压缺氧实验
将实施例2、实施例19所得化合物进行小鼠体内实验,不加药物为空白对照(ck)。雄性小鼠连续给药3天,每天一次,每次400mg。最后一次给药1.5小时后,将小鼠迅速放入280±5ml的广口瓶中(广口瓶预置10g钠石灰),迅速盖紧橡胶塞,倒扣入水中,记录小鼠存活时间。结果见图1,其中*:p≤0.05versusck;**:p≤0.001versusck。结果显示口服乙酰唑胺、实施例2、实施例19化合物的小鼠存活时间均有一定程度延长,特别是口服乙酰唑胺、实施例19化合物的小鼠存活时间相对于空白存在统计学上显著性差异,实施例19的抗缺氧活性强于对照药乙酰唑胺。
- 还没有人留言评论。精彩留言会获得点赞!