一种β-羟基酯类化合物的合成方法与流程
本发明属于医药、有机化工合成技术领域,具体涉及到一种合成β-羟基酯类化合物类化合物的方法。
背景技术:
β-羟基酯类化合物广泛存在于各种天然产物中,是很多天然产物、生物活性分子及药物分子的基本结构单元。在药物化学领域,其具有广泛的用途,如抗精神病药,抗抑郁剂,抗高血压药,抗炎药等(s.ibrayim,x.fang,d.zhang,l.liu,f.wu,chin.j.chem.2011,29,2713–2716;p.p.reddy,k.-f.yen,b.-j.uang,j.org.chem.2002,67,1034–1035;j.i.degraw,p.h.christie,r.l.kisliuk,y.gaumont,f.m.sirotnak,j.med.chem.1990,33,212–215;s.yamakoshi,e.kawanishi,tetrahedronlett.2014,55,1175–1177;p.wu,w.cai,q.-y.chen,s.xu,r.yin,y.li,w.zhang,h.luesch,org.lett.2016,18,5400–5403.)。由于这类化合物具有潜在的药用价值,吸引了世界各国化学家对它们研究的浓厚兴趣(s.reformatsky,ber.dtsch.chem.ges.1887,20,1210–1211;b)s.choppin,l.ferreiro-medeiros,m.barbarotto,f.colobert,chem.soc.rev.2013,42,937–949;c)p.g.cozzi,angew.chem.int.ed.2007,46,2568–2571)。
近年来,化学家们已经发展了一些通过reformatsky反应构建β-羟基酯类化合物的有效方法,主要是通过锌粉或金属锌试剂促进,不同金属催化来实现,具体有以下方法:(1)[rhcl(pph3)3]催化,二甲基锌促进下的reformatsky反应(k.kanai,h.wakabayashi,t.honda,org.lett.2000,2,2549–2551);(2)金属镍催化,二甲基锌促进下醛与胺及溴代酯在手性配体作用下的不对称reformatsky反应(p.g.cozzi,e.rivalta,angew.chem.int.ed.2005,44,3600–3603);(3)碘单质催化,铁粉促进下醛与溴代酯的reformatsky反应合成β-羟基酯类化合物(x.-y.liu,x.-r.li,c.zhang,x.-q.chu,w.rao,t.-p.loh,z.-l.shen,org.lett.2019,21,5873-5878);(4)二甲基锌促进下的醛与溴代酯或碘代酯的自由基不对称reformatsky反应(p.g.cozzi,angew.chem.int.ed.2006,45,2951–2954;p.g.cozzi,a.mignogna,l.zoli,synthesis2007,17,2746–2750;m.a.fernández-
虽然目前对reformatsky反应的研究取得了很大的进步,但还存在很多的不足。如所报道的方法都反应效率不高,反应时间较长,收率较低;底物适用性不够好;对映选择性不够好;使用价格昂贵的过渡金属催化如钯、金、铑等作为催化剂,催化剂用量大,反应成本较高。因此发展原料价廉易得、操作简单、简单高效的reformatsky反应合成β-羟基酯类化合物仍然是具有一定挑战性的课题。
技术实现要素:
本发明克服现有技术的缺陷,提供了一种β-羟基酯类化合物合成方法,该方法原料易得,收率高,价格低廉,原子经济性高,操作安全简单。
本发明的原理是以醛和碘代酯为原料,在镍盐的催化下,锰粉的促进作用下,发生分子间的reformatsky反应生成β-羟基酯类化合物。方法所有原料廉价易得,反应收率高,方法简单易行,操作安全,因而具有潜在的实用价值。
本发明的目的通过以下技术方案实现:
一种β-羟基酯类化合物的合成方法,以醛类化合物和碘代乙酸酯类化合物作为原料,锰粉作为促进剂,金属镍盐作为催化剂,以有机溶剂为反应介质,并加入有机质子酸,在惰性气体保护下搅拌反应,反应结束后冷却至室温,减压蒸馏浓缩得到粗产物,再经柱层析提纯,得到β-羟基酯类化合物;所述醛类化合物为芳香醛、含氧芳杂醛、含硫芳杂醛、含氮芳杂醛或脂肪醛。
上述反应如下式所示:
优选地,所述碘代乙酸酯类化合物为ich2cooet。
优选地,所述催化剂与醛类化合物的摩尔比为0.05~0.2:1。
优选地,所述催化剂为碘化镍,溴化镍,氯化镍,醋酸镍,六氟镍(iv)酸钾,三氟甲磺酸镍(ii)或双(六氟乙基丙酮)合镍(ii)。
优选地,所述锰粉与醛类化合物的摩尔比为2~4:1。
优选地,所述碘代乙酸酯类化合物与醛类化合物的摩尔比为1~2:1;
优选地,所述有机质子酸与醛类化合物的摩尔比为0.1~0.5:1。
优选地,所述有机质子酸为特戊酸,对甲基苯磺酸,三氟乙酸,冰醋酸。
优选地,所述有机溶剂为二甲基亚砜、n,n-二甲基甲酰胺,正已烷,二氯甲烷,甲苯或1,4-二氧六环,乙醚,四氢呋喃,乙腈,n,n-二甲基乙酰胺中的一种。
优选地,所述醛类化合物为苯甲醛、对氯苯甲醛、对氟苯甲醛、对甲基氧基苯甲醛、2,3-二甲基苯甲醛、2,4,6-三甲基苯甲醛、2,6-二氟苯甲醛、2-萘甲醛、2-噻吩甲醛、糠醛、环已基醛、肉桂醛、橙花醛。
优选地,所述反应温度为10~35℃,反应时间为6~36h;
优选地,所述柱层析的洗脱液为纯正已烷或混合溶剂,所述混合溶剂为石油醚和乙酸乙酯的混合溶剂,其中石油醚和乙酸乙酯的体积比为5~50:1。
所述惰性气体包括氮气、氩气、氦气等。
本发明相对于现有的技术,具有以下优点及效果:
(1)本发明方法大大提高了反应效率,所述β-羟基酯类化合物的产率可达到90%以上,甚至高达98%。
(2)本发明β-羟基酯类化合物的合成方法操作安全简单,原料价格低廉、容易得到,对功能团适应性好,对底物适应性广,环境友好,具有良好的工业应用前景。
附图说明
图1是实施例10所得产品的氢谱图;
图2是实施例10所得产品的碳谱图;
图3是实施例11所得产品的氢谱图;
图4是实施例11所得产品的碳谱图;
图5是实施例12所得产品的氢谱图;
图6是实施例12所得产品的碳谱图;
图7是实施例13所得产品的氢谱图;
图8是实施例13所得产品的碳谱图;
图9是实施例14所得产品的氢谱图;
图10是实施例14所得产品的碳谱图;
图11是实施例15所得产品的氢谱图;
图12是实施例15所得产品的碳谱图;
图13是实施例16所得产品的氢谱图;
图14是实施例16所得产品的碳谱图;
图15是实施例17所得产品的氢谱图;
图16是实施例17所得产品的碳谱图;
图17是实施例18所得产品的氢谱图;
图18是实施例18所得产品的碳谱图。
具体实施方式
下面结合具体实施例和附图,对本发明作进一步的详细说明,但本发明的实施方式和适应的底物不限于此。
实施例1
在25ml反应管中加入0.5毫摩尔苯甲醛、0.75毫摩尔碘代乙酸乙酯,22毫克nibr2,83毫克锰粉,15微升cf3cooh,四氢呋喃作溶剂,在n2气保护下,室温下搅拌反应36小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率90%。
1hnmr(400mhz,cdcl3):δ7.41–7.28(m,5h),5.19–5.11(m,1h),4.20(q,j=7.1hz,2h),3.39(d,j=3.4hz,1h),2.77–2.73(m,2h),1.28(t,j=7.1hz,3h).
13cnmr(100mhz,cdcl3):δ172.41,142.60,128.55,127.79,125.70,70.34,60.88,43.40,14.16.
根据以上数据推断所得产物的结构如下所示:
实施例2
在25ml反应管中加入0.5毫摩尔苯甲醛、0.75毫摩尔碘代乙酸乙酯,13毫克nicl2,83毫克锰粉,15微升cf3cooh,四氢呋喃作溶剂,在n2气保护下,室温下搅拌反应36小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率23%。
实施例3
在25ml反应管中加入0.5毫摩尔苯甲醛、0.75毫摩尔碘代乙酸乙酯,31毫克nii2,83毫克锰粉,15微升cf3cooh,四氢呋喃作溶剂,在n2气保护下,室温下搅拌反应36小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率92%。
1hnmr(400mhz,cdcl3):δ7.41–7.28(m,5h),5.19–5.11(m,1h),4.20(q,j=7.1hz,2h),3.39(d,j=3.4hz,1h),2.77–2.73(m,2h),1.28(t,j=7.1hz,3h).
13cnmr(100mhz,cdcl3):δ172.41,142.60,128.55,127.79,125.70,70.34,60.88,43.40,14.16.
根据以上数据推断所得产物的结构如下所示:
实施例4
在25ml反应管中加入0.5毫摩尔苯甲醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,15微升cf3cooh,四氢呋喃作溶剂,在n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率92%。
1hnmr(400mhz,cdcl3):δ7.41–7.28(m,5h),5.19–5.11(m,1h),4.20(q,j=7.1hz,2h),3.39(d,j=3.4hz,1h),2.77–2.73(m,2h),1.28(t,j=7.1hz,3h).
13cnmr(100mhz,cdcl3):δ172.41,142.60,128.55,127.79,125.70,70.34,60.88,43.40,14.16.
根据以上数据推断所得产物的结构如下所示:
实施例5
在25ml反应管中加入0.5毫摩尔苯甲醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,21.5毫克对甲基苯磺酸,四氢呋喃作溶剂,在n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率56%。
实施例6
在25ml反应管中加入0.5毫摩尔苯甲醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,15微升cf3cooh,1,4-二氧六环作溶剂,在n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率90%。
1hnmr(400mhz,cdcl3):δ7.41–7.28(m,5h),5.19–5.11(m,1h),4.20(q,j=7.1hz,2h),3.39(d,j=3.4hz,1h),2.77–2.73(m,2h),1.28(t,j=7.1hz,3h).
13cnmr(100mhz,cdcl3):δ172.41,142.60,128.55,127.79,125.70,70.34,60.88,43.40,14.16.
根据以上数据推断所得产物的结构如下所示:
实施例7
在25ml反应管中加入0.5毫摩尔苯甲醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,15微升cf3cooh,甲苯作溶剂,在n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率78%。
实施例8
在25ml反应管中加入0.5毫摩尔苯甲醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,15微升cf3cooh,二氯甲烷作溶剂,在n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率80%。
实施例9
在25ml反应管中加入0.5毫摩尔苯甲醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,15微升cf3cooh,正已烷作溶剂,在n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率85%。
实施例10
在25ml反应管中加入0.5毫摩尔苯甲醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,15微升cf3cooh,乙腈作溶剂,在n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率98%。
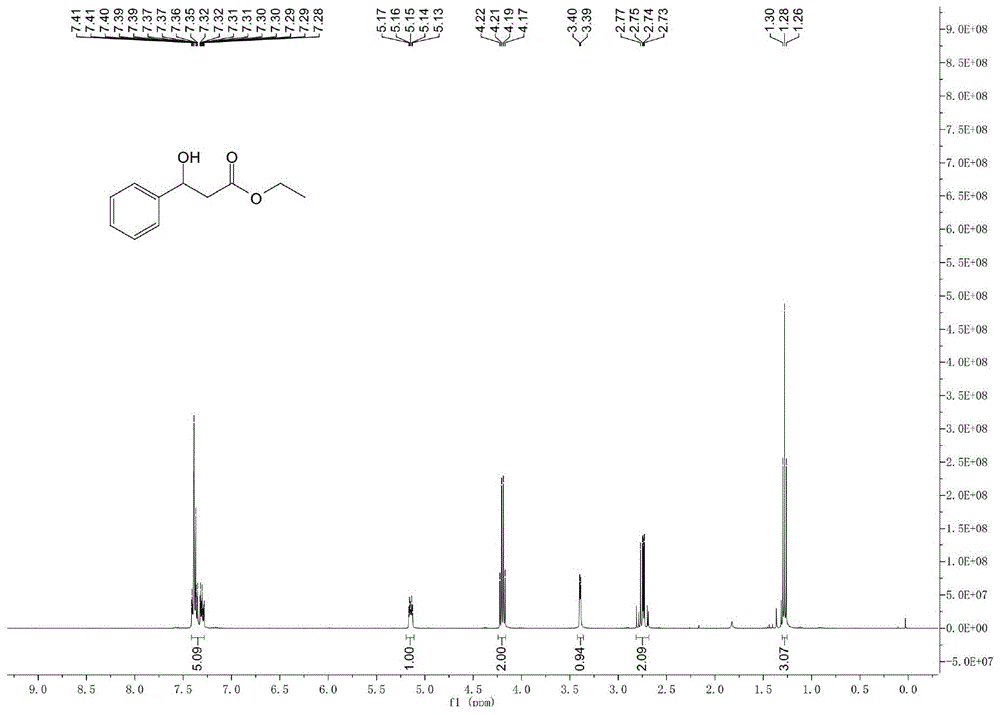
实施例10所得产物的结构表征数据如下所示(如图1和图2所示):
1hnmr(400mhz,cdcl3):δ7.41–7.28(m,5h),5.19–5.11(m,1h),4.20(q,j=7.1hz,2h),3.39(d,j=3.4hz,1h),2.77–2.73(m,2h),1.28(t,j=7.1hz,3h).
13cnmr(100mhz,cdcl3):δ172.41,142.60,128.55,127.79,125.70,70.34,60.88,43.40,14.16.
根据以上数据推断所得产物的结构如下所示:
实施例11
在25ml反应管中加入0.5毫摩尔对氟苯甲醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,15微升cf3cooh,乙腈作为溶剂,在n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率95%。
实施例11所得产物的结构表征数据如下所示(如图3和图4所示):
1hnmr(400mhz,cdcl3):δ7.41–7.33(m,2h),7.09–7.01(m,2h),5.17–5.09(m,1h),4.20(q,j=7.1hz,2h),3.41(d,j=2.6hz,1h),2.78–2.65(m,2h),1.28(t,j=7.1hz,3h).
13cnmr(100mhz,cdcl3):δ172.33,163.52,161.08,138.31,138.28,127.43,127.35,115.49,115.27,69.69,60.97,43.33,14.14.
根据以上数据推断所得产物的结构如下所示:
实施例12
在25ml反应管中加入0.5毫摩尔对甲氧基苯甲醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,15微升cf3cooh,乙腈作为溶剂,在n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为5:1,产率92%。
实施例12所得产物的结构表征数据如下所示(如图5和图6所示):
1hnmr(400mhz,cdcl3):δ7.32(d,j=8.6hz,2h),6.91(d,j=8.7hz,2h),5.11(dt,j=8.8,3.4hz,1h),4.20(q,j=7.1hz,2h),3.82(s,3h),3.22(d,j=3.3hz,1h),2.73(m,2h),1.34(dt,j=14.3,13.6hz,4h).
13cnmr(100mhz,cdcl3):δ172.46,159.22,134.73,126.98,113.92,69.98,60.85,55.30,43.34,14.17.
根据以上数据推断所得产物的结构如下所示:
实施例13
在25ml反应管中加入0.5毫摩尔2-萘甲醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,15微升cf3cooh,在乙腈作为溶剂,n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率96%。
实施例13所得产物的结构表征数据如下所示(如图7和图8所示):
1hnmr(400mhz,cdcl3):δ8.09(d,j=8.2hz,1h),7.92–7.88(m,1h),7.81(d,j=8.2hz,1h),7.73(d,j=7.1hz,1h),7.57–7.47(m,3h),5.95(dd,j=9.2,2.7hz,1h),4.24(q,j=7.1hz,2h),3.63(s,1h),2.89(qd,j=16.4,6.3hz,2h),1.30(t,j=7.2hz,3h).
13cnmr(100mhz,cdcl3):δ172.71,138.19,133.78,130.01,129.02,128.27,126.29,125.63,125.54,123.00,122.85,67.35,61.01,42.83,14.21.
根据以上数据推断所得产物的结构如下所示:
实施例14
在25ml反应管中加入0.5毫摩尔2-呋喃甲醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,15微升cf3cooh,乙腈作为溶剂,在n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率93%。
实施例14所得产物的结构表征数据如下所示(如图9和图10所示):
1hnmr(400mhz,cdcl3):δ7.40(dd,j=1.8,0.8hz,1h),6.36(dd,j=3.2,1.8hz,1h),6.30(d,j=3.3hz,1h),5.16(dt,j=8.6,4.4hz,1h),4.25–4.19(m,2h),3.25(d,j=5.0hz,1h),2.96–2.83(m,2h),1.32–1.30(m,3h).
13cnmr(100mhz,cdcl3):δ171.97,154.72,142.26,110.26,106.32,64.22,60.98,39.77,14.15.
根据以上数据推断所得产物的结构如下所示:
实施例15
在25ml反应管中加入0.5毫摩尔肉桂醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,15微升cf3cooh,乙腈作为溶剂,在n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率94%。
实施例15所得产物的结构表征数据如下所示(如图11和图12所示):
1hnmr(400mhz,cdcl3):δ7.40(d,j=7.4hz,2h),7.34(t,j=7.3hz,2h),7.29–7.25(m,1h),6.68(d,j=15.9hz,1h),6.25(dd,j=15.9,6.0hz,1h),4.75(dd,j=11.4,6.0hz,1h),4.21(q,j=7.1hz,2h),2.71–2.60(m,2h),1.30(t,j=7.1hz,3h).
13cnmr(100mhz,cdcl3):δ172.30,136.44,130.78,129.94,128.61,127.83,126.56,68.90,60.90,41.52,14.21.
根据以上数据推断所得产物的结构如下所示:
实施例16
在25ml反应管中加入0.5毫摩尔环已基甲醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,15微升cf3cooh,乙腈作为溶剂,在n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率90%。
实施例16所得产物的结构表征数据如下所示(如图13和图14所示):
1hnmr(400mhz,cdcl3):δ4.16(q,j=7.1hz,2h),3.76(dd,j=10.3,4.5hz,1h),2.81(s,1h),2.43(dt,j=16.2,12.8hz,2h),1.86(d,j=12.6hz,1h),1.75(d,j=9.3hz,2h),1.66(d,j=12.0hz,2h),1.41–1.32(m,1h),1.29–1.11(m,6h),1.08–0.96(m,2h).
13cnmr(100mhz,cdcl3):δ173.53,77.41,77.09,76.77,72.11,60.63,43.06,38.61,28.77,28.22,26.40,26.14,26.03,14.15.
根据以上数据推断所得产物的结构如下所示:
实施例17
在25ml反应管中加入0.5毫摩尔2,4,6-三甲基苯甲醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,15微升cf3cooh,乙腈作为溶剂,在n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率83%。
实施例17所得产物的结构表征数据如下所示(如图15和图16所示):
1hnmr(400mhz,cdcl3):δ6.85(s,2h),5.63(dd,j=10.6,2.1hz,1h),4.23(q,j=7.1hz,2h),3.08(dd,j=16.5,10.7hz,1h),2.59–2.50(m,1h),2.44(d,j=10.2hz,6h),2.27(s,3h),1.32(t,j=7.2hz,3h).
13cnmr(100mhz,cdcl3):δ172.71,137.00,136.12,134.62,130.18,67.52,60.87,40.08,20.76,20.68,14.21.
根据以上数据推断所得产物的结构如下所示:
实施例18
在25ml反应管中加入0.5毫摩尔橙花醛、0.75毫摩尔碘代乙酸乙酯,15.6毫克nii2,83毫克锰粉,15微升cf3cooh,乙腈作为溶剂,在n2气保护下,室温下搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压蒸馏得到粗产物,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液为石油醚/乙酸乙酯为10:1,产率88%。
实施例18所得产物的结构表征数据如下所示(如图17和图18所示):
1hnmr(400mhz,cdcl3):δ5.21(d,j=8.6hz,1h),5.13–5.03(m,1h),4.77(qd,j=9.0,4.1hz,1h),4.16(q,j=7.1hz,2h),2.94–2.59(m,1h),2.56–2.41(m,2h),2.09(dt,j=13.6,6.0hz,3h),2.02–1.96(m,1h),1.73–1.66(m,6h),1.59(d,j=3.5hz,3h),1.26(t,j=7.0hz,3h).
13cnmr(100mhz,cdcl3):δ172.49,172.45,139.52,139.32,132.37,131.72,126.47,125.49,123.82,123.79,65.13,64.75,60.66,60.63,41.88,41.76,39.43,32.35,26.44,26.31,25.65,23.30,17.68,17.65,16.64,14.18.
根据以上数据推断所得产物的结构如下所示:
- 还没有人留言评论。精彩留言会获得点赞!