一种常温常压下甲烷制备甲醇的方法及实验方法与流程
本发明涉及甲烷处理领域,具体地讲是涉及一种常温常压下由甲烷制备甲醇的方法及实验方法。
背景技术:
天然气是储量十分丰富的资源和能源,其主要成分是甲烷,在常温下是气体,甲烷同时也是主要的温室气体之一,合理地利用天然气不仅关系到未来的资源配置和能源利用,而且也是可持续发展的重要战略发展方向之一。然而,大多数天然气产地远离使用地,远距离运输工艺设备要求高、运输成本高。
从能源的角度看,ch3oh比ch4更易储存、运输,就地把天然气转化成液体的甲醇,将大大降低运输成本。
目前,由甲烷合成甲醇的方法有多相催化氧化法、均相催化氧化法、熔盐氧化法、等离子体转化法、酶催化氧化法和光催化氧化法等。
典型的采用硅基催化剂甲烷直接转化制甲醇的方法,甲烷和空气以二氧化硅为载体在418℃下催化生成甲醇,甲醇选择性为37%,甲烷转化率为仅仅5.1%。当气体流速为390ml/min,甲醇产率仅为15.5mmol/h。
目前技术将ch4氧化成ch3oh通常需要很高的温度和压力,同时还要面临ch4被深度氧化的挑战。ch4氧化的途径主要包括两大类:其一是气相氧化,例如通过金属交换的沸石催化剂和o2,n2o或h2o来循环气相氧化ch4,但这种方式通常需要较高的温度(200至500℃)才能够氧化ch4并使生成ch3oh解吸出来;其二是液相氧化,液相氧化通常需要使用贵金属催化剂或者制备出某种特殊的催化剂,而且还需要使用某些氧化剂,比如h2o2,来断裂c-h键从而使甲烷被氧化,液相氧化的反应条件通常比较温和,但封闭的催化循环常常无法实现,需要使用或者制备的催化剂的成本也比较高。
技术实现要素:
本发明的目的在于克服上述传统技术的不足之处,提供一种常温常压下由甲烷制备甲醇的方法。
本发明的目的是通过以下技术措施来达到的:
一种常温常压下由甲烷制备甲醇的方法,其特征在于:包括以下工艺步骤:
步骤一,常压容器内注入反应用水,所述反应用水为自来水或去离子水;
步骤二,加入铁源,至溶液中铁源浓度为0.01~10g/l;
步骤三,加入金属硫化物,直至溶液中金属硫化物浓度为0.2~10g/l;
步骤四,调节水溶液的ph值至3.8~5.0;
步骤五,通入含甲烷气体;
步骤六,加入双氧水直至或维持h2o2浓度为0.01~1mmol/l。
其中,步骤二中所述铁源是feso4、fe(no3)3、fecl3、fe2(so4)3、fepo4、柠檬酸铁中的任意一种或多种的混合物。
其中,优选铁源是feso4。
其中,步骤三中所述金属硫化物为还原性金属硫化物。
其中,步骤三中所述金属硫化物为mos2、cos2、ws2、cds、cus、cr2s3、ces2、nis、zns、pbs、ins、gas、mns、fes2中的任意一种或多种的混合物。
其中,优选金属硫化物为mos2。
其中,步骤五中所述含甲烷气体为纯甲烷气或者甲烷混合气。所述甲烷混合气为甲烷与空气或其他气体的混合气,所述甲烷混合气中甲烷含量为50%~99.99%。
其中,步骤四中调节水溶液ph值采用硫酸或氢氧化钠。
其中,步骤六中加入的双氧水为30wt.%双氧水。
本发明利用具有还原性的金属硫化物,在常温下温和地促进芬顿反应的进行以及铁离子的循环,从而能够持续产生自由基将ch4氧化为ch3oh。
一种常温常压下由甲烷制备甲醇的实验方法,其特征在于:包括以下实验步骤:
步骤一,常压容器内注入反应用水,所述反应用水为自来水或去离子水;
步骤二,加入铁源或铁源替代物,至溶液中铁源或铁源替代物浓度为0.01~10g/l;
步骤三,加入金属硫化物,直至溶液中金属硫化物浓度为0.2~10g/l;
步骤四,调节水溶液的ph值至3.8~5.0;
步骤五,通入含甲烷气体;
步骤六,加入30wt.%双氧水直至或维持h2o2浓度为0.01~1mmol/l。
步骤七,将反应完成的溶液循环n次,并检测每次反应结束时甲烷转化甲醇情况。n为大于等于2的整数。
其中,步骤二中所述铁源是feso4、fe(no3)3、fecl3、fe2(so4)3、fepo4、柠檬酸铁中的任意一种或多种的混合物,所述铁源替代物为镍化合物、铜化合物或锰化合物中的任意一种或多种的混合物。
本发明公开了一种常温常压下由甲烷制备甲醇的方法,由于采用了上述技术方案,与现有技术相比,本发明的优点是:
1)本发明使用的金属硫化物和铁剂来源广泛,且价格低廉,通过本申请的工艺流程可以跳过催化剂的制备过程,节省了材料的制备、加工等工序,还避免使用贵金属材料,大大降低原材料的成本;
2)本发明在常温常压下就可以达到对甲烷的选择性降解,降低了反应温度和压力要求,有利于技术的广泛推广使用;
3)本发明中使用的助催化剂可以循环使用,进一步降低成本;
4)本发明由甲烷合成甲醇液相氧化的反应条件比较温和,而且可以实现封闭的催化循环,甲醇生成速率显著提高,生成甲醇的选择性高达56.3~62.7%,适宜工业化生产及自产物中提取甲醇。
附图说明
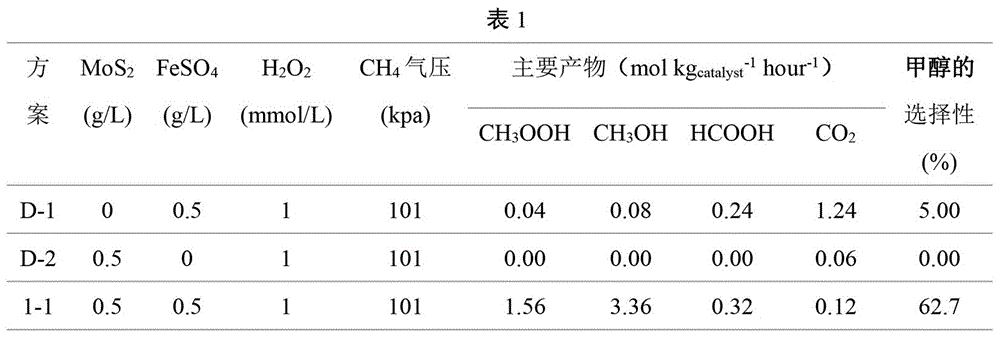
附图1是本发明中的第一组实验数据表。
附图2是本发明中的第二组实验数据表。
附图3是本发明中的第三组实验数据表。
附图4是本发明中的第四组实验数据图表。
具体实施方式
下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1:一种常温常压下由甲烷制备甲醇的方法,包括以下工艺步骤:
步骤一,常压容器内注入反应用水,所述反应用水为自来水或去离子水;
步骤二,加入铁源,至溶液中铁源浓度为0.01~10g/l;
步骤三,加入金属硫化物,直至溶液中金属硫化物浓度为0.2~10g/l;所述金属硫化物为还原性金属硫化物;
步骤四,调节水溶液的ph值至3.8~5.0;调节水溶液ph值采用硫酸或氢氧化钠;
步骤五,通入含甲烷气体;
步骤六,加入30wt.%双氧水直至或维持h2o2浓度为0.01~1mmol/l。
其中,步骤二中所述铁源是feso4、fe(no3)3、fecl3、fe2(so4)3、fepo4、柠檬酸铁中的任意一种或多种的混合物。
其中,本实施例中优选铁源是feso4。
其中,步骤三中所述金属硫化物为mos2、cos2、ws2、cds、cus、cr2s3、ces2、nis、zns、pbs、ins、gas、mns、fes2中的任意一种或多种的混合物。
其中,本实施例中优选金属硫化物为mos2。
其中,步骤五中所述含甲烷气体为纯甲烷气或者甲烷混合气。所述甲烷混合气为甲烷与空气、其他含氧气体或不含氧气体混合构成的混合气,所述甲烷混合气中甲烷含量为50%~99.99%。
本发明利用具有还原性的金属硫化物,在常温下温和地促进芬顿反应的进行以及铁离子的循环,从而能够持续产生自由基将ch4氧化为ch3oh。
实施例2:一种常温常压下由甲烷制备甲醇的实验方法,包括以下实验步骤:
步骤一,常压容器内注入反应用水,所述反应用水为自来水或去离子水;
步骤二,加入铁源或铁源替代物,至溶液中铁源或铁源替代物浓度为0.01~10g/l;
步骤三,加入金属硫化物,直至溶液中金属硫化物浓度为0.2~10g/l;
步骤四,调节水溶液的ph值至3.8~5.0;
步骤五,通入含甲烷气体;
步骤六,加入30wt.%双氧水直至或维持h2o2浓度为0.01~1mmol/l。
其中,步骤二中所述铁源是feso4、fe(no3)3、fecl3、fe2(so4)3、fepo4、柠檬酸铁中的任意一种或多种的混合物,所述铁源替代物为镍化合物、铜化合物或锰化合物中的任意一种或多种的混合物。
其中,步骤三中所述金属硫化物为mos2、cos2、ws2、cds、cus、cr2s3、ces2、nis、zns、pbs、ins、gas、mns、fes2中的任意一种或多种的混合物。
其中,步骤五中所述含甲烷气体为纯甲烷气或者甲烷混合气。所述甲烷混合气为甲烷与空气、其他含氧气体或不含氧气体混合构成的混合气,所述甲烷混合气中甲烷含量为50%~99.99%。
实施例3:一种常温常压下由甲烷制备甲醇的实验方法,其中,步骤七,将反应完成的溶液循环n次,并检测每次反应结束时甲烷转化甲醇情况。n为大于等于2的整数。
本实施例中其余步骤同实施例2。
本发明公开了一种在常温下温和地促进芬顿反应的进行以及铁离子的循环,从而能够持续产生自由基将ch4氧化为ch3oh的实验方法,通过上述实验方法可以验证本发明的有益效果,并且可以从中选取有利于工业化生产的具体催化剂构成。
作为验证,下面列举4组实验,分别采用不同催化剂在相同条件下进行实施例2中的实验、对比实验及其实验结果,实验采取的操作步骤同实施例2。
第一组实验:
实验1-1:采用实施例2中的实验步骤:
步骤一中反应用水为去离子水0.1l;
步骤二中铁源为七水合硫酸亚铁,分子式为feso4,feso4浓度0.5g/l;
步骤三中金属硫化物选用mos2,溶液中金属硫化物浓度为0.5g/l;
步骤四调节水溶液的ph值至3.8~5.0;
步骤五中通入含甲烷气体为99.99%浓度甲烷气0.1l,压力为常压,即101kpa;
步骤六中加入30wt.%双氧水直至h2o2浓度为1mmol/l。
反应结束,检测实验溶液中主要产物、产量,计算甲醇选择性。
对比实验d-1:省略实验1中的步骤三,其余部分同实验1-1。
反应结束,检测实验溶液中主要产物、产量、生成速度,计算甲醇选择性。
对比实验d-2:省略实验1中的步骤二,其余部分同实验1-1。
反应结束,检测实验溶液中主要产物、产量,计算甲醇选择性。
第一组实验结果如附图1中数据表1所示,对比实验d-1中在没有mos2的条件下,甲醇的产量很低,仅为0.08molkgcatalyst-1hour-1,,甲醇的选择性也仅5%。对比实验d-2中在没有feso4的条件下,没有甲醇产生,按照本发明方法进行的实验1-1中加入助催化剂mos2,在常温下温和地促进铁离子的循环,从而能够持续产生自由基将ch4氧化为ch3oh,氧化甲烷生成甲醇的速率得到显著提高,达到了3.36molkgcatalyst-1hour-1,提高了42倍,甲醇的选择性也高达62.7%。具有极高的工业应用前景。
下面按照实施例2中步骤采用不同催化剂在相同条件下进行第二组实验,配合实验结果说明本发明的甲烷转化甲醇效果。
第二组实验:
实验2-1:采用实施例2中的实验步骤:
步骤一中反应用水为去离子水0.1l;
步骤二中:采用铁源替代物,铁源替代物为niso4,niso4浓度0.5g/l;
步骤三中金属硫化物选用mos2,溶液中金属硫化物浓度为0.5g/l;
步骤四调节水溶液的ph值至3.8~5.0;
步骤五中通入含甲烷气体为99.99%浓度甲烷气0.1l,压力为常压,即101kpa;
步骤六中加入30wt.%双氧水直至h2o2浓度为1mmol/l。
反应结束,检测实验溶液中主要产物、产量,计算甲醇选择性。
实验2-2:实验步骤二中铁源替代物为mncl2,mncl2浓度0.5g/l;,其余部分同实验2-1。
实验2-3:实验步骤二中铁源替代物为cucl2,cucl2浓度0.5g/l,其余部分同实验2-1。
第二组实验结果如附图2中的数据表2所示,在均相芬顿体系中加入助催化剂mos2的前提下,将铁元素替换为镍、锰、铜后,虽然能够得到一定的甲醇产量,其中以cucl2效果最好,达到了2.88molkgcatalyst-1hour-1。但是上述实验结果证实,铁源替代物效果差于铁源。
下面按照实施例2中步骤采用不同催化剂在相同条件下进行第三组实验,配合实验结果说明本发明的甲烷转化甲醇效果。
第三组实验:
实验3-1:采用实施例2中的实验步骤:
步骤一中反应用水为去离子水0.1l;
步骤二中:铁源为七水合硫酸亚铁,分子式为feso4,feso4浓度0.5g/l;
步骤三中金属硫化物选用cos2,溶液中cos2浓度为0.5g/l;
步骤四调节水溶液的ph值至3.8~5.0;
步骤五中通入含甲烷气体为99.99%浓度甲烷气0.1l,压力为常压,即101kpa;
步骤六中加入30wt.%双氧水直至h2o2浓度为1mmol/l。
反应结束,检测实验溶液中主要产物、产量,计算甲醇选择性。
实验3-2:实验步骤三中金属硫化物为ws2,ws2浓度0.5g/l,其余部分同实验3-1。
实验3-3:实验步骤三中金属硫化物为cds,cds浓度0.5g/l,其余部分同实验3-1。
实验结果如附图3中的数据表3所示,在均相芬顿体系中加入feso4的前提下,将mos2替换为cos2、ws2、cds后,虽然能够得到较好的甲醇产量,其中以cos2效果最好,达到了3.06molkgcatalyst-1hour-1。但是上述实验结果证实,上述金属硫化物效果差于mos2。
下面按照实施例3中步骤进行第四组实验,配合实验结果说明本发明的甲烷转化甲醇效果。
第四组实验:
实验4:采用实施例3中的实验步骤:
步骤一中反应用水为去离子水0.1l;
步骤二中:铁源为七水合硫酸亚铁,分子式为feso4,feso4浓度0.5g/l;
步骤三中金属硫化物选用mos2,溶液中mos2浓度为0.5g/l;
步骤四调节水溶液的ph值至3.8~5.0;
步骤五中通入含甲烷气体为99.99%浓度甲烷气0.1l,压力为常压,即101kpa;
步骤六中加入30wt.%双氧水直至h2o2浓度为1mmol/l;
步骤七,将反应完成的溶液循环10次,并检测每次反应结束时甲烷转化甲醇情况。反应结束,检测实验溶液中主要产物、产量,计算甲醇选择性。
实验结果如附图4中的图表所示,将助催化剂mos2循环使用10次,甲醇的产率均保持在3.30处上下浮动,因此随着循环次数的增加,助催化剂mos2的效果无显著变化。证实本发明的催化剂具有可持续使用优点,能够节省大量催化剂的支出,有利于工业推广,降低工业生产成本。
对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明内。不应将权利要求中的任何附图标记视为限制所涉及的权利要求。
此外,应当理解,虽然本说明书按照实施方式加以描述,但并非每个实施方式仅包含一个独立的技术方案,说明书的这种叙述方式仅仅是为清楚起见,本领域技术人员应当将说明书作为一个整体,各实施例中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。
- 还没有人留言评论。精彩留言会获得点赞!