对生理性铁过载的治疗的制作方法
1.本发明涉及在患有诸如β-地中海贫血和骨髓增生异常综合征(mds)等病症的患者中降低铁过载的药物。
背景技术:
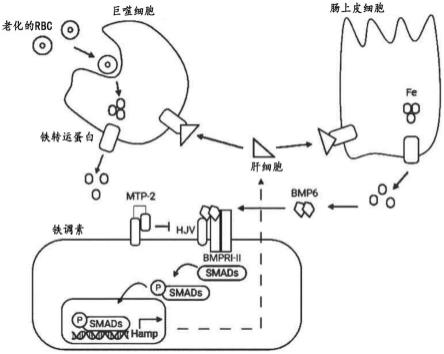
2.铁对于红细胞生成是必需的,红细胞生成即产生将氧从肺转运到身体其他组织的红细胞(erythrocyte/red blood cell)。然而,过量的铁是有毒的,因为其能够产生活性氧类,所以必须严格地调节其被十二指肠的吸收。肝肽激素铁调素在调节铁吸收以适应身体铁需求中起重要作用。铁调素通过促进铁转运蛋白(唯一已知的铁输出物)的降解负调节细胞铁输出。铁转运蛋白在作为铁的主要储存区室的细胞如巨噬细胞和十二指肠肠细胞的基底外侧上表达。因此,铁调素对铁转运蛋白的负调节限制了十二指肠铁吸收和铁从铁储存细胞如巨噬细胞中的释放。已经确定,通过分泌bmp配体(主要是bmp6)对肝细胞中的bmp-smad信号传导途径的激活刺激铁调素表达。蛋白裂解酶-2(mtp-2)(一种由基因tmprss6编码的ii型跨膜胰蛋白酶样丝氨酸蛋白酶)由肝细胞表达并通过潜在地切割bmp共受体如hjv来抑制bmp-smad信号传导(knutson,nutrition reviews67:284-288 2009),从而降低铁调素的表达并引起膳食铁的摄取增加和铁从细胞储存中的释放。mtp-2的表达由bmp6和过量的铁诱导,bmp6对于铁调素的表达是必需的(meynard等人,blood 118:747-756 2011)。因此,尽管bmp6刺激铁调素表达,但它也增加负调节物的表达,维持负反馈机制以防止铁调节异常(wahedi等人,j biol chem 292:18354-18371 2017)。图1。
3.表现为血液中高于正常转铁蛋白铁饱和度的铁过载导致许多包括以下的遗传疾病和其他病症的发病:β-地中海贫血、骨髓增生异常综合征(mds)、blackfan diamond贫血、镰状细胞病、真性红细胞增多症和血色素沉着病。
4.β-地中海贫血是一种由β-珠蛋白基因的遗传缺陷引起的遗传性血红蛋白病。在成人中,血红蛋白通常由四条多肽(珠蛋白)链构成-两个α-珠蛋白亚基和两个β-珠蛋白亚基-每个珠蛋白亚基携带其中中心铁可逆地结合氧的血红素基团。在β-地中海贫血中,血红蛋白的缺陷性产生导致无效的红细胞生成,并因此导致贫血(携氧红细胞的缺乏)。响应于贫血而上调的促红细胞生成素(epo)的过度产生,和/或由异常扩增和无效的红细胞生成导致的成红细胞激素红富铁激素(erythroferrone)的水平升高,对铁调节剂铁调素具有抑制作用,从而导致从肠道吸收铁和从内部储存释放铁增加,引起铁过载。有趣的是,不是贫血本身而是铁过载被认为降低了β-地中海贫血的期望寿命。铁可用性的增加导致转铁蛋白饱和度和血红素产生的增加,这与α-珠蛋白表达的补偿性增加一起,导致高铁血色原形成和活性氧应激及红系祖细胞凋亡增加。这种高度刺激但无效的红细胞生成导致大量成熟的红细胞不能存活,因此导致脾增大或脾肿大,这也是该疾病的特征。
5.有三种类型的β-地中海贫血,根据β-链合成的减少程度分类。纯合型或重度β-地中海贫血是最严重形式的先天性溶血性贫血,其特征在于缺乏或严重抑制功能性β-链合成。患者需要非常频繁的输血(“输血依赖性β-地中海贫血”)。另一方面,中间型β-地中海贫
血患者不需要定期输血并且是遗传杂合的(“不依赖于输血的β-地中海贫血”)。第三种形式的β-地中海贫血称为轻度β-地中海贫血,它是一种轻微的无症状病症,其中β-链合成仅受到中度抑制。
6.输血依赖性患者中输血的一个不利影响是每次输血含有至少200mg铁,因此加剧了铁过载和由非转铁蛋白结合的铁引起的毒性组织损伤的问题,这需要铁螯合疗法。铁螯合剂与循环中的非转铁蛋白结合的铁络合,并且可以改变平衡并从组织释放铁以避免组织损伤。然而,螯合剂不能降低转铁蛋白饱和度,因此不能避免高铁血色原形成增加和细胞凋亡增加。患者仍依赖输血。此外,铁螯合剂可具有副作用如肾衰竭、毒性中性粒细胞减少症和腹泻。尽管输血和铁螯合已经改善了输血依赖性患者的预后,但是现今一些患者经历的铁过载仍然代表未满足的临床需求。
7.类似地,对于治疗被诊断患有其他铁过载贫血和相关障碍的患者存在未满足的临床需求。骨髓增生异常综合征(mds)是一组克隆性干细胞障碍,其特征在于导致一种或多种血细胞减少症的无效和发育异常的血细胞生成,以及发生急性髓样白血病(aml)的不同倾向。几种形式的mds与贫血和红系前体中的毒性铁沉积相关,包括具有5q-染色体缺失的mds(5q-mds)和难治性贫血伴环形铁粒幼细胞(rars)。这些形式的mds通常与铁调素水平降低有关。通常,mds可以通过定期输血来控制,但这可能导致继发性铁过载并降低总存活期,如在β-地中海贫血中如此。因此,当铁过载达到某一阈值时,通常用铁螯合剂治疗mds患者。
8.另一种铁过载疾病是遗传性血色素沉着病。这是高加索人中最常见的遗传疾病,其特征在于由于铁调素缺乏或不敏感而引起过量铁吸收和累积的遗传突变。1型血色素沉着病由hfe基因中的突变引起。2型血色素沉着病由hjv或hamp基因中的突变引起。3型血色素沉着病由tfr2基因中的突变引起。4型血色素沉着病由slc40a1基因中的突变引起。该疾病的症状包括关节疼痛、腹痛、疲劳和虚弱。如果不治疗,该疾病可导致肝硬化、肝癌、心脏病和/或衰竭和糖尿病。目前的治疗是静脉切开术。
9.在动物模型中还显示罕见形式的贫血受益于降铁疗法。这些包括blackfan diamond贫血和镰状细胞贫血。肝脏内的铁沉积(主要在实质细胞中)也被认为会在疾病如血色素沉着病和丙型肝炎感染以及铁负载贫血中促进氧化应激和纤维化。铁代谢的调节也被认为在肝纤维化和肝硬化、非酒精性脂肪肝病(nafdl)和非酒精性脂肪性肝炎(nash)的发展中是重要的。肝纤维化通常转化为肝硬化,伴有肝功能丧失和进展为肝癌。
10.正在为患有如上述那些的病症的患者寻求新的医学治疗。尽管输血和铁螯合可以改善总存活期,但是这些治疗没有解决潜在的疾病病理学并且具有不希望的副作用,如所指出的。
11.研究的一个分支涉及铁过载贫血的生物学研究,其使用患有遗传性β-地中海贫血的小鼠作为人类疾病的模型。hbbth3/+小鼠展现出与人中间型β-地中海贫血相似的特征,包括hb水平在7与9g/dl之间、异常的红细胞形态、增加的网织红细胞计数、
12.无效和髓外红细胞生成、肝脾肿大以及肝脾铁过载(其为随着年龄增长而恶化的复杂表型)(franceschi等人,haematologica 91:1336-134 2006)。
13.缺失tmprss6(mtp2)或降低其表达已显示增加铁调素表达,从而校正hbbth3/+小鼠中的铁过载、脾肿大和贫血(guo等人,journal of clinical investigation 123:1531
–
1541 2013;nai等人,blood 119:5021-5029 2012)。已经显示,通过在β地中海贫血的
hbbth3/+小鼠模型中使用脂质纳米颗粒(lnp)配制的tmprss6 sirna降低tmprss6的基因表达诱导铁调素并降低组织和血清铁水平。此外,hbbth3/+动物的lnp-tmprss6 sirna治疗改善了红细胞存活和红细胞生成,并因此显著减少贫血(schmidt等人,blood 121(7):1200-1208 2013)。
14.guo等人证明,hbbth3/+小鼠在用针对tmprss6的反义寡核苷酸治疗后显示出不溶性膜结合珠蛋白形成、ros和细胞凋亡以及贫血的减少(guo等人,2013,同上)。这些动物还展现出较低的促红细胞生成素水平、无效红细胞生成和脾肿大的显著改善以及总血红蛋白水平的增加。
15.与这些研究一致,与tmprss6+地中海贫血小鼠相比,在地中海贫血小鼠的遗传背景中敲除tmprss6显著降低铁过载和提高血红蛋白水平。
16.基因疗法代表了解决铁过载疾病患者中潜在疾病病理学的可能方法。2019年6月,基因疗法“zynteglo”获得了ema的条件性监管批准,用于治疗12岁以上没有其他治疗选择的患者的输血依赖性β-地中海贫血。基因疗法将校正性β-珠蛋白基因离体添加到患者的骨髓干细胞中,然后将其再移植到患者体内。尽管具有潜在的治愈作用,但这是一种高度侵入性和非常昂贵的程序。截至2019年11月,zynteglo的批准因生产问题而被延迟,并且其尚未被批准用于最严重类型的β-地中海贫血(β0/β0基因型),因为超过一半的用zynteglo进行实验治疗的此类患者不得不又恢复输血。
17.还在临床研究中的是如下融合蛋白,其含有与人igg1的fc部分连接的激活素ii型受体的胞外结构域。这些配体陷阱作用于转化生长因子-β(tgfβ)超家族以增加晚期红细胞生成。索特西普(sotatercept)是激活素iia型受体igg-fc融合蛋白,以及罗特西普(luspatercept)是激活素iib型受体igg-fc融合蛋白。这些蛋白质已经显示出显著减少了在铁过载贫血中对红细胞输血的需要,但是迄今为止它们还没有被证明足以实现不依赖输血(piga等人,blood 133:1279-1289 2019)。
18.主要基于iii期believe试验提供的数据,罗特西普(reblozyl)于2019年11月8日获得fda批准用于治疗β地中海贫血中需要定期输血的成人的贫血。本研究的主要临床终点是实现输血负担从基线减少至少33%的患者比例,从第13周到第24周减少至少2个单位。仅21.4%的患者实现了这一点,仅7.6%至10.3%的患者在相同的时间范围内实现了超过50%的输血减少。因此,对于β地中海贫血的治疗仍然存在持续的医学需求。
19.也许通过治疗干预增加铁调素水平的最简单的概念是铁调素、铁调素衍生物或类似物本身的治疗性使用(casu等人,blood 128:265-276 2016;casu,nemeth&rivella,blood131:1790-1794 2018;preza等人,journal of clinical investigation 121:4880-4888,2011)。尽管是简单的治疗概念,但尚无这样的治疗成功地满足监管批准的标准。最近在临床试验(在用la jolla药物进行的β地中海贫血的ii期试验中的ljpc-401和在用merganser的i期试验后的m-021)后,这些方法中的至少两种已经被终止。此外,仍然存在开发有效的新疗法的医学需求。
技术实现要素:
20.本发明涉及结合并抑制mtp-2的结合多肽,如抗体。mtp-2抑制性结合多肽可用于降低患者的铁过载,所述患者包括患有β-地中海贫血、msd和其他铁过载贫血以及本文所述
020、nori-021、nori-022、nori-023、nori-024、nori-025、nori-026、nori-027、nori-028、nori-029、nori-030、nori-031、nori-032或nori-033的vh结构域和vl结构域,或与所述vh和/或vl结构域共享90%序列同一性的变体vh和/或vl结构域。
28.在第一构型中,抗体包含
29.vh结构域,所述vh结构域包含nori-003hcdr并与nori-003的vh结构域具有至少90%序列同一性,和
30.vl结构域,所述vl结构域包含nori-003lcdr并与nori-003的vl结构域具有至少90%序列同一性。
31.抗体可包含nori-003vh结构域和nori-003vl结构域。任选地,抗体是包含nori-003重链和nori-003轻链的igg。
32.在第二构型中,抗体包含
33.vh结构域,所述vh结构域包含nori-006hcdr并与nori-006的vh结构域具有至少90%序列同一性,和
34.vl结构域,所述vl结构域包含nori-006lcdr并与nori-006的vl结构域具有至少90%序列同一性。
35.抗体可包含nori-006vh结构域和nori-006vl结构域。任选地,抗体是包含nori-006重链和nori-006轻链的igg。
36.在第三构型中,抗体包含
37.vh结构域,所述vh结构域包含nori-008hcdr并与nori-008的vh结构域具有至少90%序列同一性,和
38.vl结构域,所述vl结构域包含nori-008lcdr并与nori-008的vl结构域具有至少90%序列同一性。
39.抗体可包含nori-008vh结构域和nori-008vl结构域。任选地,抗体是包含nori-008重链和nori-008轻链的igg。
40.在第四构型中,抗体包含
41.vh结构域,所述vh结构域包含nori-011hcdr并与nori-011的vh结构域具有至少90%序列同一性,和
42.vl结构域,所述vl结构域包含nori-011lcdr并与nori-011的vl结构域具有至少90%序列同一性。
43.抗体可包含nori-011vh结构域和nori-011vl结构域。任选地,抗体是包含nori-011重链和nori-011轻链的igg。
44.在本发明的各种实施方案中,vh和/或vl结构域共享的序列同一性%任选地高于90%,例如它可以是95%或更高、98%或更高或99%或更高。
45.结合多肽可以包含由如下v、d和j基因区段的重组产生的抗体vh结构域,所述v、d和j基因区段是产生nori-001至nori-033中任一个的vh结构域的v、d和j基因区段。结合多肽可以包含由如下v和j基因区段的重组产生的抗体vl结构域,所述v和j基因区段是产生nori-001至nori-033中任一个的vl结构域的v和j基因区段。例如,结合多肽可以包含由产生nori-001至nori-033中任一个的vh结构域的v、d和j基因区段的重组产生的vh结构域,并且它可以包含由如下v和j基因区段的重组产生的抗体vl结构域,所述v和j基因区段是产生
所述抗体的vl结构域的v和j基因区段。
46.mtp-2酶活性的抑制可以在用于抑制丝氨酸蛋白酶切割mtp-2底物以产生可检测产物的体外测定中确定。这种体外酶测定可包括使多肽与mtp-2或mtp-2胞外结构域接触,并检测可检测产物的产生相对于缺乏所述多肽的对照测定(可包括阴性对照多肽以代替)减少的程度。可以用一定浓度范围的多肽进行酶测定,以产生可以计算ic50值的剂量-反应曲线。因此,根据本发明的抑制剂可以通过其在这种酶测定中的剂量依赖性抑制来鉴定。
47.合适的体外酶测定是使用mtp-2和50μm终浓度荧光mtp-2底物的酶测定。示例性底物是boc-gln-gly-arg-amc,目前可作为baychem 4016429获得。这种测定中的mtp-2可以具有0.075u/μl的活性率。mtp-2可提供为溶液中的纯化蛋白,例如mtp-2胞外结构域。因此,可以在50μm boc-gln-gly-arg-amc荧光底物的存在下,在用具有0.075u/μl活性率的纯化mtp-2胞外结构域的酶测定中测定结合多肽的ic50。结合多肽在这样的测定中可具有小于100nm的ic50。
48.作为纯化ecd的替代方案,可以在基于细胞的测定(例如使用hek293细胞)中用细胞表面表达的mtp-2在体外测定抑制。
49.mtp-2抑制的作用(例如,降低铁调素的表达,可测量为其编码基因hamp的mrna的减少)可进一步在体内检测,确认抑制活性和生物相关性。
50.在各种实施方案中,抑制剂的效力根据其在体外测定(例如,如上所述的测定)中测量的抑制mtp-2酶活性的ic50来定量。优选地,根据本发明的结合多肽在抑制mtp-2酶活性的体外测定中具有小于100nm、小于80nm、小于60nm、小于50nm、小于40nm、小于30nm、小于25nm、小于20nm、小于15nm或小于10nm的ic50。ic50任选地为至少0.01nm、至少0.1nm、至少1nm、至少2nm、至少3nm或至少5nm。
51.可以将效力与本文所述的一种或多种抗mtp-2抗体进行比较以供参考。例如,包含nori-001至nori-033中任一个的vh和vl结构域的抗体可用作参考抗体。参考抗体可作为igg提供。例如,根据本发明的结合多肽的ic50可以在nori-001至nori-033中任一个(例如,nori-003igg、nori-006igg、nori-008igg、nori-009igg、或nori-011igg)的ic50的25%或10%内,或者其ic50可以低于所述参考抗体的ic50。“在x%内”是指测试结合多肽的ic50比参考抗体的ic50大不超过x%且小不超过x%。
52.可以将抑制效力与抑蛋白酶多肽的抑制效力进行比较,抑蛋白酶多肽是一种已知占据丝氨酸蛋白酶活性位点的6500道尔顿泛丝氨酸蛋白酶抑制剂。结合多肽的ic50可类似于或小于抑蛋白酶多肽的ic50。结合多肽的ic50可以在抑蛋白酶多肽的ic50的50%内、25%内或10%内。
53.在一个实施方案中,mtp-2抑制的测定用人mtp-2进行。在另一个实施方案中,mtp-2抑制的测定用非人(例如小鼠、大鼠或食蟹猴)mtp-2进行。在使用不同物种的mtp-2的相同酶测定中比较结合多肽的抑制效力提供了结合多肽的物种交叉反应性的指示。通常,物种交叉反应性是期望的,因为其使得有可能在多物种中在体内测试结合多肽-例如可以在靶物种(例如人)中的临床工作之前在实验室动物(例如小鼠、大鼠或食蟹猴)中进行临床前工作。优选地,根据本发明的结合多肽对于结合和抑制多物种的mtp-2具有交叉反应性。优选地,它结合并抑制人和小鼠mtp-2。更优选地,它结合并抑制人、小鼠、大鼠和食蟹猴mtp-2。
54.结合多肽在抑制非人(例如小鼠、大鼠和/或食蟹猴)mtp-2酶活性的体外测定中的
ic50可以在抑制人mtp-2酶活性的体外测定中的ic50的50%内、25%内或20%内。
55.结合多肽在抑制非人(例如小鼠、大鼠和/或食蟹猴)mtp-2酶活性的体外测定中的ic50可以与其在抑制人mtp-2酶活性的体外测定中的ic50相差小于100倍、小于50倍、小于10倍、小于5倍、或小于2倍、小于50倍、小于10倍、小于5倍、或小于2倍。
56.类似地,通过比较结合多肽对一种物种的mtp-2的亲和力与其对另一物种的mtp-2的亲和力,可提供物种交叉反应性的另一量度。可以比较例如通过表面等离子体共振测定的结合亲和力(kd)。结合非人(例如小鼠、大鼠和/或食蟹猴)mtp-2的结合多肽的kd可与其结合人mtp-2的kd相差小于50倍、小于10倍、小于5倍或小于2倍。
57.结合多肽与参考分子竞争结合mtp-2的能力可在体外测定。关于结合mtp-2的竞争可以在使用全长mtp-2、mtp-2胞外结构域、丝氨酸蛋白酶催化结构域、和/或任选地根据mtp-2中的与参考分子结合的区域选择的其他分离片段或结构域的测定中测定。例如,根据本发明的结合多肽可以是与抑蛋白酶多肽竞争结合mtp-2的结合多肽。根据本发明的结合多肽可以是与本文所述的任何抗mtp-2抗体竞争结合mtp-2的结合多肽。例如,包含nori-001至nori-033中任一个的vh和vl结构域的抗体可用作参考抗体。参考抗体可作为igg提供。例如,在各种实施方案中,结合多肽可以是与nori-003igg、nori-006igg、nori-008igg或nori-011igg竞争结合mtp-2的结合多肽。可替代地,参考抗体可以作为scfv提供。例如,在各种实施方案中,结合多肽可以是与nori-003scfv、nori-006scfv、nori-008scfv或nori-011igg竞争结合mtp-2的结合多肽。
58.可以测定竞争测定中的ic50。例如,结合多肽在与标记的抑蛋白酶多肽结合人mtp-2的竞争测定中可具有小于20nm的ic50。如表s所示,抑蛋白酶多肽的58个氨基酸的成熟序列可用于竞争测定。
59.还提供了编码本文所述的结合多肽的核酸,以及包含所述核酸的细胞。体外宿主细胞可包含核酸,所述核酸任选地整合到其细胞(例如,基因组)dna中或是瞬时转染的(例如,质粒dna)。
60.本发明的这些和其他方面和实施方案,包括产生结合多肽的方法、药物组合物和治疗患者的方法,在下文中更详细地描述。
61.条款
62.提供了针对蛋白裂解酶-2(mtp-2)的抗体。抑制mtp-2减少膳食铁的摄取并减少铁从体内细胞储库中的释放。mtp-2的抑制剂(如针对丝氨酸蛋白酶结构域的抗体)可用于治疗铁过载,铁过载是诸如β-地中海贫血等疾病的特征,且原本会导致铁的毒性累积。mtp-2抑制剂与激活素受体配体陷阱或与促红细胞生成素的组合提供了额外的治疗效果。
63.以下编号的条款代表本发明的实施方案并且是说明书的一部分。
64.1.一种分离的结合多肽,其结合mtp-2并抑制所述mtp-2的酶活性,任选地其中所述结合多肽结合mtp-2的丝氨酸蛋白酶催化结构域。
65.2.根据条款1所述的结合多肽,其包含免疫球蛋白结构域,其中针对mtp-2的结合位点由所述免疫球蛋白结构域的环区形成。
66.3.根据条款2所述的结合多肽,其是抗体,任选地人抗体。
67.4.根据任一前述条款所述的结合多肽,其中所述mtp-2是人mtp-2。
68.5.根据条款4所述的结合多肽,其中所述mtp-2是人mtp-2和小鼠mtp-2。
69.6.根据条款4或条款5所述的结合多肽,其结合包含序列多态性的人mtp-2,其中残基253是k或e且残基736是v或a。
70.7.根据任一前述条款所述的结合多肽,其不结合mtp-1并且任选地不结合ii型跨膜丝氨酸蛋白酶家族的其他成员。
71.8.根据任一前述条款所述的结合多肽,其在使用mtp-2胞外结构域和50μm终浓度荧光mtp-2底物的酶测定中展现出对mtp-2丝氨酸蛋白酶活性的剂量依赖性抑制。
72.9.根据条款8所述的结合多肽,其在针对人mtp-2胞外结构域和50μm终浓度荧光mtp-2底物的酶测定中具有小于100nm的ic50。
73.10.根据条款8或条款9所述的结合多肽,其在针对小鼠mtp-2胞外结构域和50μm终浓度荧光mtp-2底物的酶测定中具有小于100nm的ic50。
74.11.根据条款10所述的结合多肽,其在使用小鼠mtp-2胞外结构域的酶测定中的ic50与其在使用人mtp-2胞外结构域的所述测定中的ic50相差小于100倍。
75.12.根据任一前述条款所述的结合多肽,其在使用hek293细胞表面表达的人mtp-2和50μm终浓度荧光mtp-2底物的酶测定中展现出对mtp-2丝氨酸蛋白酶活性的剂量依赖性抑制。
76.13.根据条款11所述的结合多肽,其在使用hek293细胞表面表达的人mtp-2和50μm终浓度荧光mtp-2底物的酶测定中具有小于100nm的ic50。
77.14.根据任一前述条款所述的结合多肽,其与包含nori-001至nori-033中任一个的vh和vl结构域的igg竞争结合人和/或小鼠mtp-2。
78.15.根据条款14所述的结合多肽,其与包含nori-003、nori-006、nori-008或nori-011的vh和vl结构域的igg竞争结合人和/或小鼠mtp-2的丝氨酸蛋白酶催化结构域。
79.16.根据任一前述条款所述的结合多肽,其与抑蛋白酶多肽竞争结合人和/或小鼠mtp-2的丝氨酸蛋白酶催化结构域。
80.17.根据条款16所述的结合多肽,其在与标记的抑蛋白酶多肽结合人和/或小鼠mtp-2的竞争测定中具有小于100nm的ic50。
81.18.根据条款17所述的结合多肽,其在与标记的抑蛋白酶多肽结合人和/或小鼠mtp-2的竞争测定中具有小于50nm的ic50。
82.19.根据条款18所述的结合多肽,其在与标记的抑蛋白酶多肽结合人mtp-2的竞争测定中具有小于20nm的ic50。
83.20.根据任一前述条款所述的结合多肽,其具有通过表面等离子体共振测定的小于50nm的对人mtp-2的亲和力(kd)。
84.21.根据任一前述条款所述的结合多肽,其具有通过表面等离子体共振测定的小于50nm的对小鼠mtp-2的亲和力(kd)。
85.22.根据条款21所述的结合多肽,其中对小鼠mtp-2的kd在对人mtp-2的kd的50倍内。
86.23.根据任一前述条款所述的结合多肽,其包含通过表g中显示的nori-001至nori-033中任一个的种系vdj基因区段组的重组获得的抗体重链可变(vh)结构域和/或通过表g中显示的nori-001至nori-033中任一个的种系vj基因区段组的重组获得的抗体轻链可变(vl)结构域。
87.24.根据条款23所述的结合多肽,其中所述vh结构域和所述vl结构域各自通过表g中所示的nori-001、nori-002、nori-003、nori-004、nori-005、nori-006、nori-007、nori-008、nori-009、nori-010、nori-011、nori-012、nori-013、nori-014、nori-015、nori-016、nori-017、nori-018、nori-019、nori-020、nori-021、nori-022、nori-023、nori-024、nori-025、nori-026、nori-027、nori-028、nori-029、nori-030、nori-031、nori-032或nori-033的种系基因区段组的重组获得。
88.25.根据任一前述条款所述的结合多肽,其包含通过以下种系vdj基因区段的重组获得的抗体重链可变(vh)结构域:
89.ighv3-9*01、ighd4-17*01和ighj6*02,
90.ighv4-61*01、ighd3-22*01和ighj5*02,
91.ighv3-49*05、ighd3-9*01和ighj4*02,或
92.ighv3-13*01、ighd3-10*01和ighj3*02。
93.26.根据任一前述条款所述的结合多肽,其包含通过以下种系vj基因区段的重组获得的抗体轻链可变(vl)结构域:
94.iglv2-8*01和iglj2*01,
95.igkv1d-33*01和igkj5*01,
96.igkv1d-33*01和igkj4*01,以及
97.igkv3d-7*01和igkj1*01。
98.27.根据任一前述条款所述的结合多肽,其包含vh结构域和vl结构域,所述vh结构域包含一组重链互补决定区(hcdr)hcdr1、hcdr2和hcdr3,以及所述vl结构域包含一组轻链互补决定区(lcdr)lcdr1、lcdr2和lcdr3,其中所述hcdr组是nori-001至nori-033中任一个的hcdr组和/或其中所述lcdr组是nori-001至nori-033中任一个的lcdr组。
99.28.根据条款27所述的结合多肽,其中所述hcdr组是nori-003的cdr组以及所述lcdr组是nori-003的lcdr组。
100.29.根据条款27所述的结合多肽,其中所述hcdr组是nori-006的cdr组以及所述lcdr组是nori-006的lcdr组。
101.30.根据条款27所述的结合多肽,其中所述hcdr组是nori-011的cdr组以及所述lcdr组是nori-011的lcdr组。
102.31.根据条款27所述的结合多肽,其中所述hcdr组是nori-008的cdr组以及所述lcdr组是nori-008的lcdr组。
103.32.根据任一前述条款所述的结合多肽,其包含与nori-001至nori-033中任一个的vh结构域具有至少90%氨基酸序列同一性的vh结构域和/或与nori-001至nori-033中任一个的vl结构域具有至少90%氨基酸序列同一性的vl结构域。
104.33.根据条款32所述的结合多肽,其包含
105.vh结构域,所述vh结构域包含nori-003hcdr并与nori-003的vh结构域具有至少90%氨基酸序列同一性,和
106.vl结构域,所述vl结构域包含nori-003lcdr并与nori-003的vl结构域具有至少90%氨基酸序列同一性。
107.34.根据条款33所述的结合多肽,其包含nori-003抗体vh结构域和nori-003vl结
构域。
108.35.根据条款32所述的结合多肽,其包含
109.vh结构域,所述vh结构域包含nori-006hcdr并与nori-006的vh结构域具有至少90%氨基酸序列同一性,和
110.vl结构域,所述vl结构域包含nori-006lcdr并与nori-006的vl结构域具有至少90%氨基酸序列同一性。
111.36.根据条款32所述的结合多肽,其包含nori-011vh结构域和nori-011vl结构域。
112.37.根据条款36所述的结合多肽,其包含
113.vh结构域,所述vh结构域包含nori-011hcdr并与nori-011的vh结构域具有至少90%氨基酸序列同一性,和
114.vl结构域,所述vl结构域包含nori-011lcdr并与nori-011的vl结构域具有至少90%氨基酸序列同一性。
115.38.根据条款32所述的结合多肽,其包含nori-008vh结构域和nori-008vl结构域。
116.39.根据条款38所述的结合多肽,其包含
117.vh结构域,所述vh结构域包含nori-008hcdr并与nori-008的vh结构域具有至少90%氨基酸序列同一性,和
118.vl结构域,所述vl结构域包含nori-008lcdr并与nori-008的vl结构域具有至少90%氨基酸序列同一性。
119.38.根据条款37所述的结合多肽,其包含nori-008vh结构域和nori-008vl结构域。
120.39.根据条款1至38中任一项所述的结合多肽,其中所述结合多肽包含抗体恒定区。
121.40.根据条款39所述的结合多肽,其中所述结合多肽是igg抗体。
122.41.根据条款40所述的结合多肽,其包含人igg4pe恒定区。
123.42.根据条款41所述的结合多肽,其包含nori-003抗体重链和nori-003抗体轻链。
124.43.根据条款41所述的结合多肽,其包含nori-006抗体重链和nori-006抗体轻链。
125.44.根据条款41所述的结合多肽,其包含nori-011抗体重链和nori-011抗体轻链。
126.45.根据条款41所述的结合多肽,其包含nori-008抗体重链和nori-008抗体轻链。
127.46.一种分离的抗体,其包含根据条款23至38中任一项所定义的vh结构域和vl结构域。
128.47.一种分离的抗体,其包含vh结构域和vl结构域,所述vh结构域和vl结构域是nori-001至nori-033中任一个的vh和vl结构域,
129.或包含其中框架区的一个或多个非种系残基恢复为种系的所述vh和vl结构域。
130.48.根据条款47所述的抗体,其包含nori-003的vh和vl结构域或包含其中框架区的一个或多个非种系残基恢复为种系的所述vh和vl结构域。
131.49.根据条款47所述的抗体,其包含nori-006的vh和vl结构域或包含其中框架区的一个或多个非种系残基恢复为种系的所述vh和vl结构域。
132.50.根据条款47所述的抗体,其包含nori-011的vh和vl结构域或包含其中框架区的一个或多个非种系残基恢复为种系的所述vh和vl结构域。
133.51.根据条款47所述的抗体,其包含nori-008的vh和vl结构域或包含其中框架区
的一个或多个非种系残基恢复为种系的所述vh和vl结构域。
134.52.一种分离的抗体,其包含nori-001至nori-033中任一个的重链和轻链。
135.53.一种单克隆igg抗体,其包含:
136.nori-003抗体重链和nori-003抗体轻链,
137.nori-006抗体重链和nori-006抗体轻链,
138.nori-011抗体重链和nori-011抗体轻链,或
139.nori-008抗体重链和nori-008抗体轻链。
140.54.编码根据条款1至45中任一项所定义的结合多肽或根据条款46或条款53中任一项所定义的抗体的核酸。
141.55.一种体外宿主细胞,其包含根据条款54中所定义的核酸。
142.56.一种组合物,其包含与药学上可接受的赋形剂一起配制的根据条款1至45中任一项所定义的结合多肽或根据条款46至53中任一项所定义的抗体。
143.57.根据条款56所述的组合物,其用于皮下施用。
144.58.一种包含根据条款54所述的核酸的组合物,其用于体内基因疗法。
145.59.根据条款56至58中任一项所述的组合物,其用于通过疗法治疗人体或动物体。
146.60.药物的组合,其包含(i)mtp-2抑制剂和(ii)tgfβ超家族配体拮抗剂。
147.61.根据条款60所述的组合,其用于治疗患者的铁过载和使红细胞生成正常化。
148.62.一种治疗患者的铁过载和使红细胞生成正常化的方法,其包括向所述患者施用(i)mtp-2抑制剂和(ii)tgfβ家族配体拮抗剂,其中将(i)和(ii)同时或依序施用。
149.63.根据条款61所述的组合或根据条款62所述的方法,其中所述患者患有β-地中海贫血(任选地重度β-地中海贫血)、mds、blackfan diamond贫血、1型血色素沉着病或3型血色素沉着病。
150.64.根据条款60至63中任一项所述的组合或方法,其中所述拮抗剂是激活素ii受体配体陷阱。
151.65.根据条款64所述的组合或方法,其中所述拮抗剂是激活素iib受体fc融合蛋白。
152.66.根据条款65所述的组合或方法,其中所述拮抗剂是罗特西普。
153.67.根据条款64所述的组合或方法,其中所述拮抗剂是激活素iia受体fc融合蛋白。
154.68.根据条款67所述的组合或方法,其中所述拮抗剂是索特西普。
155.69.药物的组合,其包含(i)mtp-2抑制剂和(ii)促红细胞生成素。
156.70.根据条款69所述的组合,其用于治疗患者中与铁过载相关的贫血。
157.71.一种治疗患者中与铁过载相关的贫血的方法,其包括向所述患者施用(i)mtp-2抑制剂和(ii)促红细胞生成素,其中将(i)和(ii)同时或依序施用。
158.72.根据任一前述条款所述的组合或方法,其中所述mtp-2抑制剂是根据任一前述条款所定义的结合多肽或抗体。
159.72.一种方法,其在患者中:
160.减少膳食铁的吸收,
161.治疗铁过载,
162.提高肝细胞中铁调素的表达,
163.减少由铁过载引起的贫血,
164.降低血清铁浓度和/或
165.降低转铁蛋白铁饱和度,
166.所述方法包括向所述患者施用根据条款56至58中任一项所述的组合物。
167.73.根据条款72所述的方法,其中所述患者患有β-地中海贫血(例如,重度或中度β-地中海贫血)、5q-mds或rars。
168.74.根据条款72或条款73所述的方法,其中所述方法还包括向所述患者施用tgfβ家族配体的拮抗剂。
169.75.根据条款74所述的方法,其中所述拮抗剂是激活素ii受体配体陷阱。
170.76.根据条款75所述的方法,其中所述拮抗剂是激活素iib受体fc融合蛋白。
171.77.根据条款76所述的方法,其中所述拮抗剂是罗特西普。
172.78.根据条款75所述的方法,其中所述拮抗剂是激活素iia受体fc融合蛋白。
173.79.根据条款76所述的方法,其中所述拮抗剂是索特西普。
174.80.根据条款72或条款73所述的方法,其中所述方法还包括向所述患者施用红细胞生成刺激剂,任选地其中所述红细胞生成刺激剂是促红细胞生成素。
175.81.根据条款72或条款73所述的方法,其中所述方法包括向所述患者施用另外的治疗剂例如罗特西普,以降低铁过载。
176.82.根据条款56至58中任一项所述的组合物,其用于根据条款72至81中任一项所定义的方法中。
177.83.根据条款56至58中任一项所述的组合物在制造用于治疗患者的药物中的用途,所述治疗包括根据条款72至81中任一项所定义的方法。
178.84.一种降低铁过载的治疗剂,其用于以下方法中,所述方法在患者中:
179.减少膳食铁的吸收,
180.治疗铁过载,
181.提高肝细胞中铁调素的表达,
182.减少由铁过载引起的贫血,
183.降低血清铁浓度和/或
184.降低转铁蛋白铁饱和度,
185.所述方法包括向所述患者施用所述治疗剂和根据条款56至58中任一项所述的组合物。
186.85.一种包含促红细胞生成素(epo)的治疗剂,其用于刺激患者的红细胞生成的方法中,所述方法包括向所述患者施用所述药剂和根据条款56至58中任一项所述的组合物。
187.86.一种包含tgfβ家族配体拮抗剂的治疗剂,其用于促进患者的红细胞成熟的方法中,所述方法包括向所述患者施用所述药剂和根据条款56至58中任一项所述的组合物。
188.87.根据条款74至81中任一项所述的方法,根据条款82所述的用于所述用途的组合物,根据条款83所述的组合物的用途,根据条款84至86中任一项所述的用于所述用途的治疗剂,其中所述方法包括将所述治疗剂和所述组合物分开地且依序地施用于所述患者。
189.蛋白裂解酶-2(mtp-2)
190.mtp-2是ii型跨膜胰蛋白酶样丝氨酸蛋白酶,属于ii型跨膜丝氨酸蛋白酶(ttsp)家族。mtp-2的相应基因tmprss6位于22q12.3。
191.mtp-2的典型亚型(亚型1)是分子量为90kda的811个氨基酸的蛋白质。它具有类似于密切相关的ttsp家族成员如蛋白裂解酶-1和肠肽酶的保守结构,其由以下构成:小的n末端胞内信号肽,作为单次跨膜结构域发挥功能的信号锚,随后是由海胆精子蛋白、肠肽酶和突触蛋白聚糖(sea)结构域组成的胞外结构,含有两个补体因子c1r/c1s、海胆胚胎生长因子和骨形态发生蛋白(cub)结构域和三个低密度脂蛋白受体(ldlr)a类重复序列的躯干区,和c末端丝氨酸蛋白酶(sp)结构域。sp结构域具有高度保守的催化氨基酸三联体:组氨酸(617)、天冬氨酸(668)和丝氨酸(762),它们是酶功能所必需的。图2。
192.与其他ttsp成员一样,将mtp-2正确加工成膜结合的酶活性形式是复杂的过程,其中蛋白质内的多个二硫键和其他内源蛋白质的存在起关键作用。mtp-2合成到内质网膜中并作为无活性酶原运输到细胞表面,从而在cub2结构域与丝氨酸蛋白酶之间的高度保守激活基序内的精氨酸残基处进行自切割。mtp-2丝氨酸蛋白酶结构域含有四个必需的二硫键,其中一个关键地将所述结构域连接到膜结合的躯干部。
193.mtp-2的切割形式代表活性形式并且主要保持为膜结合的,在所在处它可以切割细胞表面上的其他膜结合靶标。然而,mtp-2的体外过表达导致发现在培养细胞的上清液中发现的mtp-2的“脱落”活性形式。这种脱落形式是否是具有体内功能的天然mtp-2生物学的一部分或仅仅是在基于细胞的系统中过表达的结果仍然未知。
194.mtp-2的氨基酸序列示于表s中。例如,人mtp-2具有uniprot id q8iu80的氨基酸序列,包括n末端前导序列和胞质结构域、跨膜结构域和胞外结构域(ecd)。ecd包含全长蛋白质的氨基酸84-811。包含ecd(氨基酸78-811)的mtp-2片段可以重组产生并用于本文所述的测定中(例如,以his标记的形式)。用于测定中的mtp-2的产生详述于实施例5中。
195.根据本发明的结合多肽可以结合并抑制在细胞表面上表达的mtp-2、分离的mtp-2ecd和脱落的可溶性mtp-2ecd中的任一种或多种或全部。
196.除非上下文另有说明,否则本文提及的mtp-2可以是人或非人(例如小鼠、大鼠或食蟹猴)的。优选地,mtp-2是人mtp-2。
197.由于涉及大部分蛋白质结构的mtp-2的复杂加工,因此蛋白质中的突变可导致功能丧失。此外,存在已知的tmprss6多态性,如rs855791,其可导致增加的mtp-2活性和对铁调素的更有效抑制。r576a突变使sp结构域切割和完全mtp-2激活所必需的关键精氨酸突变,因此将蛋白质保持为无活性酶原。s762a突变使sp结构域催化三联体中的关键丝氨酸残基突变且完全消除活性。因此,由于自我切割需要自活性,因此蛋白质也保持为无活性酶原。e114k突变体已经在具有非功能性mtp-2表达的患者中描述。该突变存在于sea结构域中,因此最有可能阻止蛋白质正确运输至细胞表面。
198.mtp-2有四种已知的变体,覆盖了大约92%的人群:
199.亚型1(27.4%);
200.rs855791snp,其导致第736位缬氨酸至丙氨酸的单个氨基酸改变(27.2%);
201.具有v736a和另外的k253e变异的变体(25.9%);以及
202.单独k253e的变体(11.4%)。
203.结合多肽将优选结合所有四种这样的变体,因此适于通过抑制大多数人群表达的
mtp-2变体来治疗全部或大多数人群。因此,结合多肽可以结合包含序列多态性的人mtp-2,其中残基253是k或e且残基736是v或a。
204.mtp-2有4种已知的亚型。称为典型亚型的亚型1是全长811个氨基酸,主要在睾丸中表达。亚型2是肝脏的主要亚型,在n末端缺失9个细胞内氨基酸(802个氨基酸)。该n末端区域被认为参与膜结合的mtp-2的内化,因此比亚型1更慢地内化。亚型3也主要与亚型1一起在睾丸中表达。它具有9个n末端氨基酸,但利用外显子10的选择性剪接变体,其驱动缺乏sp结构域的截短形式的表达,并因此在功能上无活性。亚型4显示与亚型2相同的外显子,但在外显子16与17之间还具有另外的22个氨基酸的外显子,其破坏sp结构域功能并且在功能上也无活性。亚型4被认为在亚型2也表达的组织中表达,并且由于它们缺乏功能,因此认为亚型3和4是亚型1和2的显性负调节物。已显示亚型3或4的表达可阻断亚型2介导的hjv切割。
205.结合多肽可以至少结合活性亚型1和2。任选地,它可以结合亚型3。任选地,它可以结合亚型4。结合多肽任选地不结合亚型3。任选地,它不结合亚型4。不与无活性亚型结合可能有益于旨在抑制mtp-2活性的治疗性分子。与亚型1和/亚型2的丝氨酸蛋白酶催化结构域结合,以及不与亚型3和/或亚型4结合是潜在有利的。
206.与mtp-2结合
207.如上所述,mtp-2是一种多结构域蛋白质,已知该蛋白质中的各种突变导致功能丧失。因此,可以产生识别各种结构域中的结合位点并抑制蛋白质的酶活性的结合多肽。
208.结合多肽可以结合mtp-2的丝氨酸蛋白酶催化结构域。它可以结合自激活的mtp-2。它可以结合mtp-2ecd。它可以结合mtp-2酶原。
209.结合丝氨酸蛋白酶催化结构域的结合多肽可以被鉴定为结合包含所述结构域的mtp-2并且不结合缺少所述结构域的mtp-2的结合多肽。可以构建具有c末端截短的mtp-2的“无头”变体,所述c末端截短缺失丝氨酸蛋白酶结构域,但仍包含ecd的剩余部分。结合全长mtp-2ecd和不结合无头mtp-2ecd表明结合多肽识别丝氨酸蛋白酶催化结构域中的表位。可以在htrf测定中或通过表面等离子体共振来测量结合,本文提供了其示例方案。与丝氨酸蛋白酶催化结构域的结合也可以在使用mtp-2ecd和无头mtp-2ecd的酶抑制测定中鉴定。结合丝氨酸蛋白酶催化结构域的结合物可以在这种测定中展现出与mtp-2ecd的剂量依赖性结合,而在所述测定中不展现出与无头mtp-2ecd的剂量依赖性结合。
210.可以通过荧光激活细胞分选仪(facs)检测与细胞表面表达的mtp-2(例如,在hek293细胞上表达)的结合。
211.结合多肽可与抑蛋白酶多肽竞争结合mtp-2(例如mtp-2ecd,例如其丝氨酸蛋白酶催化结构域)。
212.还可以测定结合多肽之间的竞争。例如,结合多肽可以与包含nori-001至nori-033中任一个的vh和vl结构域的抗体(例如igg或scfv)或包含nori-001至nori-033中任一个的完整重链和轻链的igg竞争。它可以例如与nori-003scfv竞争。它可以与nori-006scfv竞争。它可以与nori-011scfv竞争。它可以与nori-008scfv竞争。
213.结合多肽之间的竞争表明它们在mtp-2的相同区域中具有表位,例如两者可以以重叠的结合足迹结合相同的结构域。
214.ic50可以在竞争测定中以结合多肽抑制参考分子(例如抑蛋白酶多肽或nori抗
体)与mtp-2结合的能力的量度来计算。结合多肽在这种测定中可具有小于100nm的ic50。任选地,ic50小于50nm,例如小于20nm。
215.例如,与抑蛋白酶多肽竞争的ic50可以在htrf竞争测定中用浓度为5nm的直接标记的抑蛋白酶多肽(例如抑蛋白酶多肽-647)、浓度为0.3nm的结合多肽和浓度为10nm的人mtp-2抗原或浓度为60nm的小鼠mtp-2抗原来测定。二抗(例如ad0207)可以以1:1000稀释度使用。参见实施例8,其中根据制造商的说明书使用647快速标记试剂盒(innova biosciences-362-0010)直接标记抑蛋白酶多肽。为了测定结合多肽与参考nori抗体竞争的ic50,可以如上直接标记参考抗体(例如,用647标记)并使用相同的方案,用参考抗体替代抑蛋白酶多肽。
216.用于htrf竞争测定的材料和方法
217.将抗体以4x浓度滴定到htrf缓冲液(含有0.1%bsa(sigma-a7906)和氟化钾0.53m(sigma-60240-250g)的dpbs(gibco-14190144))中,起始浓度为200nm。将5μl/w抗体添加至384孔白色板(greiner-784904)中。将humtp-2和momtp-2的纯化蛋白稀释到htrf缓冲液(humtp-2=40nm和momtp-2=240nm)中,4x终浓度并以5μl/w铺板。然后将moigg1骨架中的抗mtp-2mab(nori-037)用在htrf缓冲液中以1:1000稀释度4x终浓度的delfia eu-n1兔抗小鼠igg抗体(ad0207)稀释至1.2nm 4x终浓度。最后,将647标记的抑蛋白酶多肽(sigma-a3428)在htrf缓冲液中稀释至20nm 4x终浓度,并以5μl/w铺板。在黑暗中在室温下将板孵育3小时或更长时间。使用htrf 100闪烁方案在1h、2h和3h下在envision板读取器上读取板。(ex:340nm em1:620nm em2:665nm)。
218.结合亲和力
219.结合多肽对人mtp-2的亲和力(kd)可以小于100nm、小于50nm、小于25nm或小于10nm。结合多肽对小鼠mtp-2的亲和力(kd)可以小于100nm、小于50nm、小于25nm或小于10nm。结合多肽对大鼠mtp-2的亲和力(kd)可以小于100nm、小于50nm、小于25nm或小于10nm。结合多肽对食蟹猴mtp-2的亲和力(kd)可以小于100nm、小于50nm、小于25nm或小于10nm。
220.在一些实施方案中,结合人mtp-2的kd可以小于5nm,例如小于4nm、小于3nm、小于2nm、小于1nm、或小于0.1nm。kd任选地为至少0.001nm,例如至少0.005nm。
221.结合多肽可以展现出在实施例6中(例如在表k或表w中)所示的范围内的亲和力(kd)。结合多肽结合mtp-2的kd可以与nori-001至nori-033igg或scfv(例如,nori-009igg)中任一个的kd相同或更低。任选地,kd等于或小于抑蛋白酶多肽的kd。
222.可根据结合相互作用的平衡解离常数kd,即缔合或结合速率(ka)与解离或分解速率(kd)的比率ka/kd,定量结合多肽对mtp-2的亲和力。可以使用表面等离子体共振(spr)测量抗原结合的kd、ka和kd。示例spr程序和条件在实施例6中阐述。
223.简言之,spr可以在25℃下通过将结合多肽以10μl/min在1μg/ml浓度下在芯片上捕获60秒来进行(可以捕获大约35与50ru之间),并且以30μl/min注射mtp-2(分析物)120秒(缔合时间)并监测解离600秒。可以将分析物以100、25、6.25、1.56和0nm浓度注射。产生结合多肽的传感图,并且可以将数据拟合至1:1相互作用模型(例如,使用具有全局拟合的rmax、ka、kd且ri=0的biacore评价软件)。
224.亲和力的定量可以使用采用单价形式的抗原结合多肽臂的spr进行,例如包含抗
原结合位点的抗体fab或fv,或具有针对所讨论抗原的单个抗原结合臂的异二聚体免疫球蛋白(例如igg)。可替代地,可便利的是测定二价形式的抗原结合多肽臂(例如包含同二聚体抗原结合臂的igg)的亲和力。spr可以包括将抗原结合多肽臂的二聚体包被到生物传感器芯片上(直接或间接),将抗原结合多肽臂暴露于一定浓度范围的缓冲溶液中的抗原,检测结合,并计算结合相互作用的平衡解离常数kd。spr可以在25℃下进行。合适的缓冲溶液是150mm nacl、0.05%去污剂(例如p20)和3mm edta,ph 7.6。含有2.5mm cacl2的hbs-p 1x(10mm hepes ph 7.4,150mm nacl,3mm edta,0.05%聚山梨酸酯20ph 7.6)是示例缓冲液。可以使用标准算法将结合数据拟合到1:1模型,所述标准算法可能是所用仪器固有的。已知多种spr仪器,如biacoretm、proteon xpr36tm和(sapidyne instruments,inc)。
225.如本文别处所述,分离的纯化mtp-2ecd可便利地用于测定,并且是spr的合适分析物。
226.交叉反应性
227.监管机构可能需要候选治疗分子,以在其进入人类临床试验之前已在实验室动物中证明治疗功效。β-地中海贫血的小鼠模型和结合多肽在野生型小鼠中的评估的例子展示于本文中。为了实现在这种动物模型中测试结合多肽,希望结合物与来自一种或多种非人哺乳动物的相应抗原交叉反应。因此,它可以结合非人mtp-2以及人mtp-2。
228.一种定量抗原结合分子(或更精确地,其抗原结合位点)的物种交叉反应程度的方式是以其对一种物种的抗原的亲和力与对另一种物种的抗原的亲和力相比的倍数差异,例如对人抗原与对小鼠抗原的亲和力相比的倍数差异。亲和力可以定量为kd,是指抗原与抗原结合分子结合的平衡解离常数。kd可通过本文别处描述的spr测定。
229.物种交叉反应性结合分子对结合人和非人抗原的亲和力的差异倍数可以是100倍或更小、50倍或更小、30倍或更小、25倍或更小、20倍或更小、15倍或更小、10倍或更小或5倍或更小。换言之,结合人抗原的胞外结构域的kd可以在结合非人抗原的胞外结构域的kd的30倍、25倍、20倍、15倍、10倍或5倍内。
230.优选地,人和非人抗原的结合亲和力在结合非人mtp-2的kd的10倍或更小的范围内,更优选在5倍或2倍内,例如如通过表面等离子体共振测定的,可以比结合人mtp-2的kd高多达10倍(优选多达5倍或多达2倍)或低多达10倍(优选低多达5倍或低多达2倍)。
231.如果结合两种物种的抗原的kd满足阈值,例如,如果结合人抗原的kd和结合非人抗原的kd都是10mm或更小,优选5mm或更小,更优选1mm或更小,则结合分子也可以被认为具有物种交叉反应性。kd可以是100nm或更小、50nm或更小、25nm或更小、10nm或更小、5nm或更小、2nm或更小、或1nm或更小。
232.交叉反应性还可以通过结合多肽识别细胞上表达的多物种的mtp-2的能力来鉴定,例如使用facs。htrf也可用于测定与多物种的mtp-2的结合和交叉反应性。
233.结合多肽可以具有可测量的阻断酶活性的能力,其通过荧光读出使用来自多物种的mtp-2底物(例如,人和小鼠、大鼠和食蟹猴mtp-2中的一种或多种或全部)得出。在使用人和非人(例如,小鼠、大鼠或食蟹猴)mtp-2的本文描述的测定中,它可以展现出对mtp-2催化活性的剂量依赖性抑制。
234.虽然结合不同物种的抗原的物种交叉反应性可能是有利的,但仍然需要结合物对
mtp-2的选择性以避免不希望的副作用。因此,在体内,mtp-2优选是由结合多肽的抗原结合位点结合的唯一抗原。尽管如此,结合多肽可以任选地被工程化以包含另外的结合位点,并且包含抗体恒定区的抗体可以例如任选地结合一种或多种fc受体。
235.结合多肽任选地不结合mtp-1(例如人mtp-1)。任选地,它不结合mtp-3(例如人mtp-3)。任选地,它不结合ii型跨膜丝氨酸蛋白酶家族的其他成员。
236.对mtp-2的抑制
237.mtp-2主要在肝细胞上表达,并且通过调节肝细胞中铁调素的表达而在铁代谢中具有主要作用。现在已经确定铁调素(铁稳态的主要调节剂)表达受骨形态发生蛋白(bmp)生长因子控制,所述骨形态发生蛋白生长因子与肝细胞上存在的i型和ii型bmp受体结合,并针对decapentaplegic(smad)信号传导途径诱导bmp/级联分子。bmp受体下游的smad1、5、8/smad4复合物的磷酸化增加编码铁调素的hamp基因的表达并增加铁调素的分泌。铁调素通过与存在于十二指肠肠细胞、巨噬细胞和肝细胞上的铁转运体铁转运蛋白结合,诱导内化和降解并因此减少进入血液的铁量来降低血液的铁水平。mtp-2被认为通过选择性切割肝细胞表面上的bmpr复合物的成员并因此使bmp/smad信号传导沉默来负调节铁调素表达。一种提出的mtp-2的酶靶标是血幼素(hjv),其为bmpr复合物的辅助受体,它是最大bmp/smad信号传导所必需的。然而,尽管研究已经显示mtp-2能够切割hjv并产生特异性切割产物,但是mtp-2掩蔽小鼠显示膜结合hjv的表达的相矛盾的降低,而tmprss6 ko小鼠显示切割的hjv的水平增加。最近,研究表明mtp-2最有可能切割bmpr复合物的多个成员以抑制铁调素表达。
238.根据对tmprss6 mrna表达的组织范围扫描,在睾丸中也存在低水平的mtp-2表达,然而,这里mtp-2的作用在很大程度上是未知的。由于mtp-2的局部表达,具有功能丧失性mtp-2突变的tmprss6 ko小鼠和人都显示出这样的表型,其中铁水平极大地升高并且没有另外的副作用,表明除铁调节的另外作用是有限的,因此对于抗mtp-2疗法存在的担忧不大。
239.因此,本发明提出抑制mtp-2,从而防止或减少其下游底物的切割,导致mtp-2对铁调素表达的抑制降低。
240.mtp-2的抑制是指mtp-2的酶活性的抑制。mtp-2是丝氨酸蛋白酶,而抑制剂可以是抑制成熟活性mtp-2催化丝氨酸蛋白酶切割其底物和/或抑制通过催化丝氨酸蛋白酶切割所致的mtp-2酶原自激活的抑制剂。
241.在各种实施方案中,结合多肽可以结合mtp-2的丝氨酸蛋白酶催化结构域。丝氨酸蛋白酶催化结构域含有mtp-2的酶活性位点。抑制可由结合mtp-2并部分或完全掩蔽酶活性位点的结合多肽引起的酶-底物相互作用的空间位阻导致,从而减少底物结合。抑制可以可替代地或另外地由在丝氨酸蛋白酶催化结构域中诱导失活性构象变化、或使丝氨酸蛋白酶催化结构域偏向失活构象的结合多肽引起,由此其酶活性降低。不管抑制的分子机制如何,结合多肽抑制mtp-2丝氨酸蛋白酶活性的能力可以在酶测定中进行功能测定。
242.本文描述了用于抑制对mtp-2底物的丝氨酸蛋白酶切割以产生可检测产物的体外测定。这些包括用纯化的mtp-2ecd和荧光底物的酶测定,以及用细胞表面表达的mtp-2和荧光底物的酶测定。这些测定中的每一个测定对mtp-2对其底物的切割的抑制。可以例如以50μm终浓度使用荧光底物boc-gln-gly-arg-amc。作为mtp-2酶活性抑制剂的结合多肽可以通
过在这样的酶测定中对mtp-2丝氨酸蛋白酶活性的剂量依赖性抑制来鉴定。
243.在一个实施方案中,在50μm boc-gln-gly-arg-amc荧光底物的存在下,结合多肽在针对具有0.075u/μl活性率的人mtp-2胞外结构域的酶测定中具有小于100nm的ic50。ic50可以小于80nm、小于60nm、小于50nm、小于40nm、小于30nm、小于25nm、小于20nm、小于15nm或小于10nm。ic50任选地为至少0.01nm、至少0.1nm、至少1nm、至少2nm、至少3nm或至少5nm。
244.在一个实施方案中,在50μm boc-gln-gly-arg-amc荧光底物的存在下,结合多肽在针对具有0.075u/μl活性率的非人(例如,小鼠、大鼠或食蟹猴)mtp-2胞外结构域的酶测定中具有小于100nm的ic50。ic50可以小于80nm、小于60nm、小于50nm、小于40nm、小于30nm、小于25nm、小于20nm、小于15nm或小于10nm。ic50任选地为至少0.01nm、至少0.1nm、至少1nm、至少2nm、至少3nm或至少5nm。
245.如上所述,优选地,结合多肽具有物种交叉反应性并且因此抑制来自多于一种物种的mtp-2,例如抑制人和非人(例如小鼠、大鼠或食蟹猴)mtp-2。在测定中用于定量交叉反应性的参数在本文别处讨论。
246.在一个实施方案中,在使用hek293细胞表面表达的人mtp-2和50μm终浓度荧光mtp-2底物的酶测定中,结合多肽展现出对mtp-2丝氨酸蛋白酶活性的剂量依赖性抑制。它在所述测定中可具有小于100nm的ic50。ic50可以小于80nm、小于60nm、小于50nm、小于40nm、小于30nm、小于25nm、小于20nm、小于15nm或小于10nm。ic50任选地为至少0.01nm、至少0.1nm、至少1nm、至少2nm、至少3nm或至少5nm。
247.还可以在肝细胞中检测对mtp-2酶活性的抑制。例如,抑制mtp-2的结合多肽可增加肝癌细胞系中的铁调素表达(有或无bmp刺激),可测量为hamp mrna相对于对照的增加。
248.可以从体内测定中获得类似的读出。在施用结合多肽的小鼠中,对mtp-2酶活性的抑制可导致hamp mrna的增加、血清铁的减少和转铁蛋白饱和度(tsat)的降低。可以将结合多肽施用于野生型(例如,以10mg/kg)以测量这些作用。其可在给药后24小时内使肝细胞中的hamp mrna增加至少2倍,且此增加可在给药后持续3天且优选21天(例如,在单次10mg/kg剂量的腹膜内施用后)。结合多肽可以降低小鼠的血清铁浓度。这也可以在24小时内检测到,并且优选在给药后持续3天且优选21天。用于测量hamp mrna,定量血清铁和tsat的示例实验和方案在实施例中列出。
249.结合多肽
250.根据本发明的结合多肽是具有特异性抑制并结合mtp-2的能力的多肽分子。
251.许多类别的结合多肽是本领域已知的,包括经典的igg抗体和其他基于免疫球蛋白结构域的结合蛋白(参见binz,amstutz&pluckthun,nature biotechnology 23(10):1257 2005。非免疫球蛋白结合分子也是已知的,并且结合环可以被工程化到其他多肽支架如纤连蛋白中。
252.优选地,本发明的结合多肽包含免疫球蛋白结构域,其中针对mtp-2的结合位点由免疫球蛋白结构域的环区形成。结合多肽的优选实施方案是抗体。
253.根据本发明的抗体是免疫球蛋白或包含免疫球蛋白结构域的分子,无论是天然的还是部分或完全合成产生的。抗体可以是igg、igm、iga、igd或ige分子或其抗原特异性抗体片段(包括但不限于fab、f(ab')2、fv、二硫键连接的fv、scfv、单结构域抗体、闭合构象多特
异性抗体、二硫键连接的scfv、双抗体),无论是源自天然产生抗体的任何物种,还是通过重组dna技术产生;无论分离自血清、b细胞、杂交瘤、转染瘤、酵母还是细菌。可以使用常规技术将抗体人源化。术语抗体涵盖包含抗体抗原结合位点的任何多肽或蛋白质。抗原结合位点(互补位)是抗体与其靶抗原(mtp-2)的表位结合并互补的部分。
254.术语“表位”是指由抗体结合的抗原区域。表位可被定义为结构性的或功能性的。功能性表位通常是结构性表位的子集,并且具有直接促进相互作用的亲和力的那些残基。表位也可以是构象的,也就是由非线性氨基酸构成。在某些实施方案中,表位可以包括决定簇,即分子的化学活性表面基团(如氨基酸、糖侧链、磷酰基或磺酰基),并且在某些实施方案中,可具有特定的三维结构特征,和/或特定的电荷特征。
255.抗原结合位点是包含抗体的一个或多个cdr并且能够结合抗原的多肽或结构域。例如,多肽包含cdr3(例如hcdr3)。例如,多肽包含抗体的可变结构域的cdr1和2(例如hcdr1和2)或cdr1-3(例如hcdr1-3)。
256.抗体抗原结合位点可以由一个或多个抗体可变结构域提供。在一个例子中,抗体结合位点由单个可变结构域提供,例如由重链可变结构域(vh结构域)或轻链可变结构域(vl结构域)提供。在另一个例子中,结合位点包含vh/vl对或两个或更多个这样的对。因此,抗体抗原结合位点可包含vh和vl。
257.抗体可以是完整的免疫球蛋白,包括恒定区,或者可以是抗体片段。抗体片段是完整抗体的一部分,例如包含完整抗体的抗原结合区和/或可变区。抗体片段的例子包括:
258.(i)fab片段,即由vl、vh、cl和ch1结构域组成的单价片段;(ii)f(ab')2片段,即包括在铰链区通过二硫键连接的两个fab片段的二价片段;
259.(iii)由vh和ch1结构域组成的fd片段;
260.(iv)由抗体的单臂的vl和vh结构域组成的fv片段,
261.(v)dab片段(ward等人,(1989)nature 341:544-546;其通过引用以其整体并入本文),其由vh或vl结构域组成;以及
262.(vi)分离的互补决定区(cdr),其保留特异性抗原结合功能。
263.抗体的其他例子为包含重链二聚体(5
’‑
vh-(任选的铰链)-ch2-ch3-3’)且不含轻链的h2抗体。
264.单链抗体(例如scfv)是常用的片段。多特异性抗体可由抗体片段形成。本发明的抗体可以适当地采用任何这样的形式。
265.任选地,结合多肽或其抗体免疫球蛋白结构域可以与另外的多肽序列和/或标记、标签、毒素或其他分子融合或缀合。结合多肽可以与一个或多个不同的抗原结合区融合或缀合,从而提供能够结合除mtp-2外的第二抗原的分子。例如,本发明的抗体可以是多特异性抗体,例如双特异性抗体,其包含(i)针对mtp-2的抗体抗原结合位点和(ii)识别另一抗原的另一抗原结合位点(任选地抗体抗原结合位点,如本文所述)。
266.抗体通常包含抗体vh和/或vl结构域。抗体的分离的vh和vl结构域也是本发明的一部分。抗体可变结构域是如下的抗体轻链和重链的部分,所述部分包括互补决定区(cdr;即cdr1、cdr2、和cdr3)和框架区(fr)的氨基酸序列。因此,在每个vh和vl结构域内是cdr和fr。vh结构域包含一组hcdr,并且vl结构域包含一组lcdr。vh是指重链的可变结构域。vl是指轻链的可变结构域。每个vh和vl通常由三个cdr和四个fr构成,按照以下顺序从氨基末端
到羧基末端排列:fr1、cdr1、fr2、cdr2、fr3、cdr3、fr4。根据本发明使用的方法,指定为cdr和fr的氨基酸位置可以根据kabat(sequences of proteins of immunological interest(national institutes of health,bethesda,md.,1987和1991))或根据imgt命名法定义。
267.抗体可以包含抗体vh结构域,所述抗体vh结构域包含vh cdr1、cdr2和cdr3以及框架。其可替代地或还包含抗体vl结构域,所述抗体vl结构域包含vl cdr1、cdr2和cdr3以及框架。根据本发明的抗体vh和vl结构域和cdr的例子列于表s中。本文公开的所有vh和vl序列、cdr序列、cdr组和hcdr组和lcdr组代表本发明的方面和实施方案。如本文所述,“cdr组”包含cdr1、cdr2和cdr3。因此,hcdr组是指hcdr1、hcdr2和hcdr3,而lcdr组是指lcdr1、lcdr2和lcdr3。除非另有说明,否则“cdr组”包括hcdr和lcdr。
268.如实施例中更详细描述的,我们分离并表征了特别感兴趣的抗体,命名为nori-001、nori-002、nori-003、nori-004、nori-005、nori-006、nori-007、nori-008、nori-009、nori-010、nori-011、nori-012、nori-013、nori-014、nori-015、nori-016、nori-017、nori-018、nori-019、nori-020、nori-021、nori-022、nori-023、nori-024、nori-025、nori-026、nori-027、nori-028、nori-029、nori-030、nori-031、nori-032和nori-033(“nori-001至nori-033”)。
269.在本发明的各个方面,除非上下文另有说明,否则抗体可选自这些抗体中的任一种,或选自nori-003、nori-006、nori-011或nori-008的子集。
270.本发明涵盖具有所附序列表和/或附图中所示的所有抗体的vh和/或vl结构域序列的抗mtp-2抗体,以及包含那些抗体的hcdr和/或lcdr、并且任选地具有本文公开的任何抗mtp-2抗体的全重链和/或全轻链氨基酸序列的抗体。
271.cdr序列可以通过imgt或通过另一种方法如kabat来定义。除非另有说明,否则对可变结构域中的残基或cdr或框架区的提及是指imgt定义。
272.当抗体vh结构域或vl结构域在框架区中包含一个或多个不同于通过重组产生其的种系基因区段的残基时,非种系残基可保留或可突变为不同的残基,例如其可恢复为种系残基。对应的种系基因区段可被鉴定为与可变结构域的序列最紧密比对的基因区段,并且与nori-001至nori-033vh和vl结构域中每一个对应的种系基因区段示于本文表g中。
273.根据本发明的抗体可以包含一个或多个如本文所述的cdr,例如cdr3,以及任选地cdr1和cdr2,以形成一组cdr。cdr或cdr组可以是nori-001至nori-033中任一个的cdr或cdr组。
274.本发明提供包含抗体nori-001至nori-033中任一个的hcdr1、hcdr2和/或hcdr3和/或这些抗体中任一个的lcdr1、lcdr2和/或lcdr3(例如一组cdr)的抗体。抗体可包含这些抗体之一的一组vh cdr。任选地,它还可以包含这些抗体之一的一组vl cdr,并且vl cdr可以来自与vh cdr相同或不同的抗体。
275.本发明还提供了包含公开的一组hcdr的vh结构域和/或包含公开的一组lcdr的vl结构域。
276.通常,vh结构域与vl结构域配对以提供抗体抗原结合位点,但如下文进一步讨论的,单独的vh或vl结构域可用于结合抗原。nori-003vh结构域可以与nori-003vl结构域配对,从而形成包含nori-003vh和vl结构域二者的抗体抗原结合位点。提供了本文公开的其他vh和vl结构域的类似实施方案。在其他实施方案中,nori-003vh与除nori-003vl以外的
vl结构域配对。轻链混杂性在本领域中是已确立的。同样,本发明提供了本文公开的其他vh和vl结构域的类似实施方案。
277.因此,抗体nori-001至nori-033中任一个的vh可以与抗体nori-001至nori-033中任一个的vl配对。
278.抗体可以在抗体框架内包含一个或多个cdr,例如一组cdr。框架区可以具有人种系基因区段序列。因此,抗体可以是具有vh结构域的人抗体,所述vh结构域在人种系框架中包含一组hcdr。通常,抗体还具有vl结构域,所述vl结构域例如在人种系框架中包含一组lcdr。抗体“基因区段”,例如vh基因区段、d基因区段或jh基因区段是指具有衍生抗体的该部分的核酸序列的寡核苷酸,例如vh基因区段是包含与从fr1到cdr3部分的多肽vh结构域对应的核酸序列的寡核苷酸。人v、d和j基因区段重组产生vh结构域,而人v和j区段重组产生vl结构域。d结构域或区域是指抗体链的多样性结构域或区域。j结构域或区域是指抗体链的连接结构域或区域。体细胞超突变可导致抗体vh或vl结构域具有与相应基因区段不精确匹配或比对的框架区,但序列比对可用于鉴定最接近的基因区段,并因此鉴定衍生特定vh或vl结构域的基因区段的特定组合。当将抗体序列与基因区段比对时,可将抗体氨基酸序列与由基因区段编码的氨基酸序列比对,或可直接将抗体核苷酸序列与基因区段的核苷酸序列比对。
279.本发明的抗体可以是人抗体或包含人可变区和非人(例如小鼠)恒定区的嵌合抗体。本发明的抗体例如具有人可变区,并且任选地还具有人恒定区。
280.因此,抗体任选地包括恒定区或其部分,例如人抗体恒定区或其部分。例如,vl结构域可以在其c末端附接至抗体轻链κ或λ恒定结构域。类似地,抗体vh结构域可以在其c末端附接至衍生自任何抗体同种型(例如igg、iga、ige和igm)和同种型亚类中任一个(例如igg1或igg4)的免疫球蛋白重链恒定区的全部或部分(例如ch1结构域或fc区)。人重链恒定区的例子示于表s中。
281.可替代地,本发明抗体的恒定区可以是非人恒定区。例如,当在转基因动物(其例子在本文别处描述)中产生抗体时,可以产生包含人可变区和非人(宿主动物)恒定区的嵌合抗体。一些转基因动物产生完全人抗体。其他已经被工程化以产生包含嵌合重链和完全人轻链的抗体。当抗体包含一个或多个非人恒定区时,这些可以被人恒定区替代以提供更适合作为治疗组合物施用于人的抗体,因为它们的免疫原性由此降低。
282.用木瓜蛋白酶消化抗体产生两个相同的抗原结合片段(也称为“fab”片段)和“fc”片段(不具有抗原结合活性但具有结晶能力)。“fab”当用于本文时指抗体片段,其包括重链和轻链中每一个的一个恒定区和一个可变区。本文的术语“fc区”用于定义免疫球蛋白重链的c末端区,包括天然序列fc区和变体fc区。“fc片段”是指通过二硫键保持在一起的两条h链的羧基末端部分。抗体的效应子功能由fc区中的序列决定,该区域也由在某些类型的细胞上发现的fc受体(fcr)识别。用胃蛋白酶消化抗体产生f(ab')2片段,其中抗体分子的两个臂保持连接并包含两个抗原结合位点。f(ab')2片段具有交联抗原的能力。
283.当在本文中使用时,“fv”是指抗体的保留抗原识别和抗原结合位点两者的最小片段。此区域由紧密非共价或共价缔合的一个重链可变结构域和一个轻链可变结构域的二聚体组成。在此构型中,每个可变结构域的三个cdr相互作用以将抗原结合位点限定在vh-vl二聚体的表面上。这六个cdr共同为抗体赋予抗原结合特异性。然而,即使单个可变结构域
(或仅包含三个对抗原具有特异性的cdr的半个fv)也具有识别和结合抗原的能力,但其亲和力低于整个结合位点。
284.本文公开的抗体可以被修饰为增加或减少血清半衰期。在一个实施方案中,引入以下突变中的一个或多个:t252l、t254s或t256f,以增加抗体的生物半衰期。生物半衰期也可以通过改变重链恒定区ch1结构域或cl区以包含取自igg的fc区的ch2结构域的两个环的补救受体结合表位来增加,如美国专利号5,869,046和6,121,022中所述,其中描述的修饰通过引用并入本文。在另一个实施方案中,将本发明抗体或抗原结合片段的fc铰链区突变以降低抗体或片段的生物半衰期。将一个或多个氨基酸突变引入fc-铰链片段的ch
2-ch3结构域界面区中,使得相对于天然fc-铰链结构域spa结合,抗体或片段具有受损的葡萄球菌蛋白a(spa)结合。增加血清半衰期的其他方法是本领域技术人员已知的。因此,在一个实施方案中,抗体或片段被peg化。在另一个实施方案中,抗体或片段融合至白蛋白结合结构域,例如白蛋白结合单结构域抗体(dab)。在另一个实施方案中,抗体或片段被pas化(即由pas构成的多肽序列的遗传融合(xl-protein gmbh),其形成具有大流体动力学体积的不带电荷的无规卷曲结构)。在另一个实施方案中,抗体或片段被xten化/rpeg化(即非精确重复肽序列(amunix,versartis)与治疗性肽的遗传融合)。在另一个实施方案中,抗体或片段被elp化(即与elp重复序列(phasebio)的遗传融合)。在strohl,biodrugs(2015)29:215-239中更详细地描述了这些各种半衰期延长融合物,所述融合物例如在表2和6中,通过引用并入本文。
285.抗体恒定区
286.如上所讨论,抗体可以以各种同种型和具有不同的恒定区提供。抗体的fc区被fc受体识别并确定抗体介导细胞效应子功能的能力,包括抗体依赖性细胞介导的细胞毒性(adcc)活性、补体依赖性细胞毒性(cdc)活性和抗体依赖性细胞吞噬作用(adcp)活性。这些细胞效应子功能涉及将携带fc受体的细胞募集到靶细胞位点,导致杀伤抗体结合的细胞。
287.在本发明的上下文中,希望避免细胞效应子功能,如adcc、adcp和/或cdc。因此,根据本发明的抗体可能缺乏fc效应子功能,例如它们可含有不介导adcc、adcp和/或cdc的fc区,或者它们可能缺乏fc区或完全缺乏抗体恒定区。抗体可能具有效应子无效的恒定区。
288.抗体可具有结合一种或多种类型的fc受体但不诱导细胞效应子功能(即不介导adcc、cdc或adcp活性)的重链恒定区。这样的恒定区可能不能结合负责触发adcc、cdc或adcp活性的一种或多种特定fc受体。
289.抗体可具有不结合fcγ受体的重链恒定区,例如恒定区可包含leu235glu突变(即,其中野生型亮氨酸残基突变为谷氨酸残基),其可称为“e”突变,例如igg4-e。重链恒定区的另一个任选突变是ser228pro(“p”突变),其通过减少fab臂交换来增加稳定性。重链恒定区可以是包含leu235glu突变和ser228pro突变二者的igg4。该“igg4-pe”重链恒定区是效应子无效的。替代的效应子无效的人恒定区是失能的igg1。
290.igg4pe是本发明优选的抗体同种型。结合多肽可以是包含表s所示igg4pe恒定区序列的igg4pe抗体。
291.抗体恒定区可以被工程化为在体内具有延长的半衰期。例子包括“yte”突变和其他半衰期延长突变(dall’acqua,kiener&wu,jbc 281(33):23514-23524 2006和wo02/060919,通过引用并入本文)。三重突变yte是igg ch2结构域中3个氨基酸的取代,这些突变
提供根据kabat的eu索引编号的残基252处的酪氨酸、残基254处的苏氨酸和残基256处的谷氨酸。如参考出版物中所述,与具有人ch2野生型结构域的相应抗体的半衰期相比,yte修饰增加了抗体的半衰期。为了提供增加的体内效力持续时间,本发明的抗体可以包括抗体恒定区(例如,igg恒定区,例如,igg ch2结构域),其具有与相应的野生型人恒定区(例如,igg,例如,igg ch2结构域)相比增加抗体半衰期的一个或多个突变。半衰期可通过标准方法测定,如wo 02/060919中所述。
292.可根据待治疗患者的基因型选择合适的抗体恒定区。例如,如us 20160319017中所述,增加人患者红细胞生成的方法可包括施用结合由tmprss6核苷酸序列编码的人mtp-2的结合物(例如抗体),所述tmprss6核苷酸序列包含选自以下的snp:
293.rs855791、rs2543519、rs2235324和rs1421312;
294.所述结合物包含选自以下的恒定区:
295.(a)人γ-4重链恒定区,其包含us20160319017的seq id no:73中所示的位置189处的leu或seq id no:73中所示的位置289处的arg;以及
296.(b)人γ-1重链恒定区,其包含对应于us20160319017的seq id no:42的位置204的asp或对应于us20160319017的seq id no:42的位置206的leu;并且其中
297.(i)人受试者包含tmprss6核苷酸序列,所述tmprss6核苷酸序列包含所述选择的snp;以及
298.(ii)人患者包含编码所述选择的恒定区的恒定区基因区段;或人患者表达包含所述选择的恒定区的抗体。
299.可以是us 20160319017中所述的抗体,其包含如所述公开案中所述的恒定区和/或用于治疗包含如所述公开案中所述的tmprss6核苷酸序列多态性的患者。
300.其他示例恒定区示于表s中。
301.产生和修饰结合多肽
302.鉴定和制备结合多肽(包括抗体)的方法是本领域熟知的。
303.例如,可以使用实验室动物产生抗体,所述实验室动物如用mtp-2或其片段(例如重组mtp-2ecd)或它们的编码核酸免疫的小鼠(包括转基因小鼠(例如kymousetm、humab或memo))、大鼠(例如)、骆驼科动物、鲨鱼、兔、鸡或其他非人动物,随后任选地对恒定区和/或可变区进行人源化以产生人或人源化抗体。在一个例子中,可以使用展示技术,如酵母、噬菌体或核糖体展示,这对于技术人员是清楚的。标准亲和力成熟(例如使用展示技术)可以在从转基因动物、噬菌体展示文库或其他文库分离抗体先导物之后的另一步骤中进行。合适技术的代表性例子描述于us 20120093818(amgen,inc)中,其通过引用以其整体并入本文,例如段落[0309]至[0346]中所述的方法。
[0304]
期望产生结合物变体的原因有很多,包括优化多肽序列用于大规模制造、促进纯化、增强稳定性或改善包含在所需药物配制品中的适用性。可以在抗体序列中的一个或多个靶残基处进行蛋白质工程化工作,例如用替代氨基酸取代一个氨基酸(任选地,产生在该位置处含有所有天然存在的氨基酸(可能除了cys和met)的变体),并且监测对功能和表达的影响以确定最佳取代。在一些情况下,不希望用cys或met取代残基或将这些残基引入序列中,因为这样做可能在制造中产生困难-例如通过形成新的分子内或分子间半胱氨酸-半
胱氨酸键。当选择先导候选物并对其优化用于制造和临床开发时,通常希望尽可能少地改变其抗原结合特性,或至少保留亲本分子的亲和力和效力。然而,也可以产生变体以调节关键抗体特征,如亲和力、交叉反应性或中和效力。
[0305]
抗体可以包含任何公开的抗体的一组h和/或l cdr,其中在所公开的h和/或l cdr组内具有一个或多个氨基酸突变。突变可以是氨基酸取代、缺失或插入。因此,例如在所公开的h和/或l cdr组内可以有一个或多个氨基酸取代。例如,在所述h和/或l cdr组内可以有多达12、11、10、9、8、7、6、5、4、3或2个突变,例如取代。例如,在hcdr3中可有至多6、5、4、3或2个突变,例如取代,和/或在lcdr3中可有至多6、5、4、3或2个突变,例如取代。抗体可以包含本文任何nori抗体所示的一组hcdr、lcdr或一组6个(h和l)cdr,或者可以包含具有一个或两个保守取代的该组cdr。
[0306]
可任选地在本文公开的抗体vh或vl结构域的框架区中进行一个或多个氨基酸突变。例如,不同于相应人种系区段序列的一个或多个残基可以恢复为种系。对应于示例抗mtp-2抗体的vh和vl结构域的人种系基因区段序指示于表g中。
[0307]
抗体可包含与所附序列表中所示的任何抗体的vh结构域具有至少60%、70%、80%、85%、90%、95%、98%或99%氨基酸序列同一性的vh结构域,和/或包含与任何那些抗体的vl结构域具有至少60%、70%、80%、85%、90%、95%、98%或99%氨基酸序列同一性的vl结构域。可用于计算两个氨基酸序列的%同一性的算法包括例如blast、fasta或smith-waterman算法,例如采用默认参数。特定变体可包括一个或多个氨基酸序列改变(氨基酸残基的添加、缺失、取代和/或插入)。
[0308]
可以在一个或多个框架区和/或一个或多个cdr中进行改变。任选地通过cdr诱变提供变体。改变通常不会导致功能丧失,因此包含由此改变的氨基酸序列的抗体可以保留结合mtp-2的能力。它可以保留与其中不进行改变的抗体相同的定量结合能力,例如在本文所述的测定中所测量的。包含由此改变的氨基酸序列的抗体可具有改进的结合和/或抑制mtp-2的能力。
309.改变可以包括用非天然存在的或非标准的氨基酸替代一个或多个氨基酸残基,将一个或多个氨基酸残基修饰成非天然存在的或非标准的形式,或将一个或多个非天然存在的或非标准的氨基酸插入序列中。本文别处描述了本发明序列中改变的数目和位置的例子。天然存在的氨基酸包括20种“标准”l-氨基酸,通过它们的标准单字母码标识为g、a、v、l、i、m、p、f、w、s、t、n、q、y、c、k、r、h、d、e。非标准氨基酸包括可并入多肽主链中或由修饰现有氨基酸残基产生的任何其他残基。非标准氨基酸可以是天然存在的或非天然存在的。
[0310]
如本文所用的术语“变体”是指与亲本多肽或核酸相差一个或多个氨基酸或核酸缺失、取代或添加,但保留亲本分子的一种或多种特定功能或生物活性的肽或核酸。氨基酸取代包括其中氨基酸被不同的天然存在的氨基酸残基替代的改变。这样的取代可以被分类为“保守的”,在这种情况下,包含在多肽中的氨基酸残基被另一种天然存在的在极性、侧链功能或大小方面具有相似特征的氨基酸替代。这种保守取代是本领域熟知的。本发明涵盖的取代也可以是“非保守的”,其中肽中存在的氨基酸残基被具有不同特性的氨基酸,如来自不同组的天然存在的氨基酸取代(例如用丙氨酸取代带电荷或疏水性氨基酸),或可替代地,其中天然存在的氨基酸被非常规氨基酸取代。在一些实施方案中,氨基酸取代是保守的。当用于提及多核苷酸或多肽时,术语变体还涵盖指分别与参考多核苷酸或多肽相比(例
如,与野生型多核苷酸或多肽相比)可在一级、二级或三级结构上变化的多核苷酸或多肽。
[0311]
在一些方面,可以使用通过使用本领域熟知的方法分离或产生的“合成变体”、“重组变体”或“化学修饰的”多核苷酸变体或多肽变体。“修饰的变体”可以包括保守的或非保守的氨基酸改变,如下所述。多核苷酸改变可导致由参考序列编码的多肽中的氨基酸取代、添加、缺失、融合和截短。一些方面使用包括插入变体、缺失变体或具有氨基酸取代的取代变体,包括通常不存在于作为变体基础的肽序列中的氨基酸和其他分子的插入和取代,例如但不限于通常不存在于人蛋白质中的鸟氨酸的插入。当描述多肽时,术语“保守取代”是指基本上不改变多肽活性的多肽氨基酸组成的改变。例如,保守取代是指用氨基酸残基取代具有相似化学特性(例如,酸性、碱性、带正电荷或带负电荷、极性或非极性等)的不同氨基酸残基。保守氨基酸取代包括用异亮氨酸或缬氨酸替代亮氨酸、用谷氨酸替代天冬氨酸、或用丝氨酸替代苏氨酸。提供功能相似的氨基酸的保守取代表是本领域熟知的。例如,以下六组各自含有彼此保守取代的氨基酸:1)丙氨酸(a)、丝氨酸(s)、苏氨酸(t);2)天冬氨酸(d)、谷氨酸(e);3)天冬酰胺(n)、谷氨酰胺(q);4)精氨酸(r)、赖氨酸(k);5)异亮氨酸(i)、亮氨酸(l),甲硫氨酸(m)、缬氨酸(v);和6)苯丙氨酸(f)、酪氨酸(y)、色氨酸(w)。(还参见creighton,proteins,w.h.freeman and company(1984),通过引用以其整体并入。)在一些实施方案中,如果改变、添加或缺失单个氨基酸或小百分比的氨基酸的单独取代、缺失或添加不降低肽的活性,则这些变化也可认为是“保守取代”。插入或缺失通常在约1至5个氨基酸的范围内。保守氨基酸的选择可以基于以下来选择:肽中要取代的氨基酸的位置,例如如果氨基酸在肽的外部并且暴露于溶剂,或者在内部并且不暴露于溶剂。
[0312]
可以基于以下来选择将取代现有氨基酸的氨基酸:现有氨基酸的位置,包括其暴露于溶剂(即,如果与未暴露于溶剂的内部定位的氨基酸相比,氨基酸暴露于溶剂或存在于肽或多肽的外表面上)。此类保守氨基酸取代的选择是本领域熟知的,例如dordo等人,j.moi biol,1999,217,721-739和taylor等人,j.theor.biol.119(1986);205-218以及s.french和b.robson,j.mol.evol.19(1983)171中披露的。因此,可以选择适合于在蛋白质或肽外部的氨基酸(即暴露于溶剂的氨基酸)的保守氨基酸取代,例如但不限于,可以使用以下取代:y被f取代,t被s或k取代,p被a取代,e被d或q取代,n被d或g取代,r被k取代,g被n或a取代,t被s或k取代,d被n或e取代,i被l或v取代,f被y取代,s被t或a取代,r被k取代,g被n或a取代,k被r取代,a被s、k或p取代。
[0313]
在替代的实施方案中,还可以选择适合于在蛋白质或肽内部的氨基酸的所涵盖的保守氨基酸取代,例如可以使用适合于在蛋白质或肽内部的氨基酸(即氨基酸不暴露于溶剂)的保守取代,例如但不限于,可以使用以下保守取代:其中y被f取代,t被a或s取代,i被l或v取代,w被y取代,m被l取代,n被d取代,g被a取代,t被a或s取代,d被n取代,i被l或v取代,f被y或l取代,s被a或t取代且a被s、g、t或v取代。在一些实施方案中,非保守氨基酸取代也被涵盖在变体的术语中。
[0314]
本发明包括产生含有表s中所示的抗体vh和/或vl结构域的vh和/或vl结构域变体的抗体的方法。此类抗体可通过包括以下的方法产生:
[0315]
(i)通过在亲本抗体vh结构域的氨基酸序列中添加、缺失、取代或插入一个或多个氨基酸,提供作为亲本抗体vh结构域的氨基酸序列变体的抗体vh结构域,
[0316]
其中亲本抗体vh结构域是nori-001至nori-033中任一个的vh结构域或包含那些
抗体中任一个的重链互补决定区的vh结构域,
[0317]
(ii)任选地将由此提供的vh结构域与vl结构域组合,以提供vh/vl组合,以及
[0318]
(iii)测试由此提供的vh结构域或vh/vl结构域组合以鉴定具有一种或多种所需特征的抗体。
[0319]
vh结构域可以是nori-003的vh结构域。它可以是nori-006的vh结构域。它可以是nori-011的vh结构域。它可以是nori-008的vh结构域。
[0320]
所需特征包括与人和/或非人mtp-2结合。可以鉴定相对于亲本抗体而言对人和/或小鼠mtp-2具有可比或更高亲和力的抗体。其他所需特征包括本文所述的酶测定中的抑制,和血清铁浓度和/或tsat的体内降低,和hamp mrna的增加。鉴定具有所需特征的抗体可包括鉴定具有本文所述的功能属性的抗体,所述功能属性如其亲和力、交叉反应性、特异性或中和效力,其中任一者可在如本文所述的测定中确定。
[0321]
当方法中包括vl结构域时,vl结构域可以是nori-001至nori-033中任一个的vl结构域,或可以是通过在亲本vl结构域的氨基酸序列中添加、缺失、取代或插入一个或多个氨基酸而提供的变体,其中亲本vl结构域是nori-001至nori-033中任一个的vl结构域或包含那些抗体中任一个的轻链互补决定区的vl结构域。vl结构域可以是与vh结构域同属的相同抗体的vl结构域。它可以是nori-003的vl结构域。它可以是nori-006的vl结构域。它可以是nori-011的vl结构域。它可以是nori-008的vl结构域。
[0322]
产生变体抗体的方法可任选地包括产生抗体或vh/vl结构域组合的拷贝。方法可进一步包括表达所得抗体。可以任选地在一个或多个表达载体中产生对应于所需抗体vh和/或vl结构域的核苷酸序列。本文详细描述了合适的在宿主细胞中表达(包括重组表达)的方法。
[0323]
编码核酸和产生方法
[0324]
可以提供分离的核酸,其编码根据本发明的抗体。核酸可以是dna和/或rna。合成来源的基因组dna、cdna、mrna或其他rna或其任何组合可以编码抗体。
[0325]
本发明提供包含至少一种上述多核苷酸的质粒、载体、转录或表达盒形式的构建体。示例性核苷酸序列包括在序列表中。除非上下文另有要求,否则对本文所述的核苷酸序列的提及涵盖具有指定序列的dna分子,并且涵盖具有其中u取代t的指定序列的rna分子。
[0326]
本发明还提供了包含一种或多种编码抗体的核酸的重组宿主细胞。产生所编码抗体的方法可包括从核酸表达,例如通过培养含有核酸的重组宿主细胞。因此可以获得抗体,并且可以使用任何合适的技术分离和/或纯化,然后适当地使用。产生方法可包括将产物配制成包含至少一种额外组分如药学上可接受的赋形剂的组合物。
[0327]
用于在各种不同宿主细胞中克隆和表达多肽的系统是熟知的。合适的宿主细胞包括细菌、哺乳动物细胞、植物细胞、丝状真菌、酵母和杆状病毒系统以及转基因植物和动物。
[0328]
抗体和抗体片段在原核细胞中的表达是本领域已确立的。常见的细菌宿主是大肠杆菌。在培养的真核细胞中的表达也是本领域技术人员可获得的生产选择。本领域可用于表达异源多肽的哺乳动物细胞系包括中国仓鼠卵巢(cho)细胞、hela细胞、幼仓鼠肾细胞、nso小鼠黑色素瘤细胞、yb2/0大鼠骨髓瘤细胞、人胚肾细胞(例如hek293)、人胚视网膜细胞和许多其他细胞。
[0329]
载体可含有适当的调节序列,包括启动子序列、终止子序列、多腺苷酸化序列、增
强子序列、标记基因和其他适当的序列。可以将编码抗体的核酸引入宿主细胞中。本发明的核酸可以整合到宿主细胞的基因组(例如染色体)中。根据标准技术,可以通过包含促进与基因组重组的序列来促进整合。可以通过各种方法将核酸引入真核细胞,所述方法包括磷酸钙转染、deae-葡聚糖、电穿孔、脂质体介导的转染以及使用逆转录病毒或其他病毒(例如痘苗病毒)或对于昆虫细胞而言使用杆状病毒的转导。将核酸引入宿主细胞(特别是真核细胞)可以使用基于病毒或质粒的系统。质粒系统可以以附加体维持,或者可以掺入宿主细胞或人工染色体中。掺入可以通过在单个或多个基因座处随机或靶向整合一个或多个拷贝进行。对于细菌细胞,合适的技术包括氯化钙转化、电穿孔和使用噬菌体的转染。引入后可以表达核酸,例如通过在用于基因表达的条件下培养宿主细胞,然后任选地分离或纯化结合多肽,例如抗体。
[0330]
配制和施用
[0331]
根据本发明的结合多肽及其编码核酸分子通常以分离的形式提供。vh和/或vl结构域和核酸可以从其天然环境或其产生环境中纯化提供。分离的结合多肽和分离的核酸将不含或基本上不含与它们天然缔合的物质,如与它们在体内一起发现的,或当制备它们是通过体外重组dna技术进行的情况下在制备它们的环境(例如细胞培养物)中发现的其他多肽或核酸。任选地,分离的结合多肽或核酸(1)不含通常与其一起被发现的至少一些其他蛋白质,(2)基本上不含来自相同来源(例如,来自相同物种)的其他蛋白质,(3)由来自不同物种的细胞表达,(4)已经从至少约50%的天然缔合的多核苷酸、脂质、碳水化合物或其他物质分离,(5)与不天然缔合的多肽可操作地(通过共价或非共价相互作用)缔合,或(6)天然不存在。
[0332]
结合多肽或其编码核酸可以与稀释剂或佐剂一起配制,并且仍然出于实用目的而被分离,例如,如果用于包被微量滴定板以用于免疫测定,可以将它们与载体混合,而当用于治疗时,可以将它们与药学上可接受的载体或稀释剂混合。如本文别处所述,其他活性成分也可包括在治疗制剂中。结合多肽可以在体内天然地或通过异源真核细胞(如cho细胞)系统被糖基化,或者可不发生糖基化(例如如果通过在原核细胞中表达而产生)。本发明涵盖具有修饰的糖基化模式的抗体。
[0333]
通常,分离的产物构成给定样品的至少约5%、至少约10%、至少约25%或至少约50%。结合多肽可以基本上不含在其天然或产生环境中发现的会干扰其治疗、诊断、预防、研究或其他用途的蛋白质或多肽或其他污染物。
[0334]
本发明提供了包含本文所述的结合多肽的治疗组合物。还提供了包含编码此类结合多肽的核酸的治疗组合物。编码核酸在本文别处更详细地描述,且包括dna和rna,例如mrna。在本文所述的治疗方法中,使用编码结合多肽的核酸和/或含有这种核酸的细胞可用作包含所述结合多肽本身的组合物的替代物(或附加物)。含有编码结合多肽的核酸的细胞(任选地其中所述核酸被稳定地整合到基因组中)因此代表了用于患者治疗用途的药物。可将编码结合多肽的核酸引入源自预期患者的人细胞中并离体修饰。向患者施用含有编码核酸的细胞提供了能够表达结合多肽的细胞储库,这与施用分离的核酸或分离的结合多肽相比,可以在更长的时间内提供治疗益处。还可以将核酸直接施用于患者进行基因疗法。因此,可以提供编码结合多肽的核酸用于基因疗法,包括将编码核酸引入患者体内的细胞中,使得核酸在患者细胞中表达并提供治疗效果,本文公开了所述治疗效果的例子,包括增加
hamp mrna、降低血清铁、降低tsat、和治疗与铁过载相关的疾病和病症。
[0335]
组合物可以含有合适的载体、赋形剂和其他药剂,它们被掺入配制品中以提供改进的转移、递送、耐受性等。在所有药物化学家都知晓的配方中可以找到许多适当的配制品:remington's pharmaceutical sciences,mack publishing company,伊斯顿,宾夕法尼亚州。这些配制品包括例如散剂、糊剂、软膏、凝胶、蜡、油、脂质、含有脂质(阳离子或阴离子)的囊泡(如lipofectint
tm
)、dna缀合物、无水吸收糊剂、水包油和油包水乳剂、乳剂卡波蜡(carbowax)(具有不同分子量的聚乙二醇)、半固体凝胶和含有卡波蜡的半固体混合物。另外参见powell等人"compendium of excipients for parenteral formulations"pda(1998)j pharm sci technol 52:238-311。组合物可包含与医用注射缓冲液和/或佐剂组合的抗体或核酸。
[0336]
可以将结合多肽或其编码核酸配制用于向患者施用的所需途径,例如配制于注射用液体(任选地水溶液)中。
[0337]
各种递送系统是已知的并且可用于施用本发明的药物组合物。引入方法包括但不限于皮内、肌内、腹膜内、静脉内、皮下、鼻内、硬膜外和口服途径。可以将组合物通过任何便利的途径施用,例如通过输注或团注,通过上皮或粘膜皮肤内层(例如,口腔粘膜、直肠和肠粘膜等)吸收,并且可以与其他生物活性剂一起施用。施用可为全身或局部的。优选通过皮下注射施用抗原结合分子。施用可以是患者自我施用,例如自我注射。
[0338]
还可以将药物组合物在囊泡中递送,特别是在脂质体中递送(参见langer(1990)science249:1527-1533;treat等人(1989)liposomes in the therapy of infectious disease and cancer,lopez berestein和fidler(编),liss,纽约州,第353-365页;lopez-berestein,同上,第317-327页;总体上参见同上)。
[0339]
在某些情况下,可以在控释系统中递送所述药物组合物。在一个实施方案中,可以使用泵(参见langer,同上;sefton(1987)crc crit.ref.biomed.eng.14:201)。在另一个实施方案中,可以使用聚合物材料;参见medical applications of controlled release,langer and wise(编),crc pres.,波卡拉顿,佛罗里达州(1974)。在又另一个实施方案中,可以将控释系统放置在组合物的靶标附近,因此仅需要全身剂量的一部分(参见,例如,goodson,medical applications of controlled release,同上,第2卷,第115-138页,1984)。
[0340]
可注射制剂可包括用于静脉内、皮下、皮内和肌内注射、滴注等的剂型。这些可注射制剂可通过公知方法制备。例如,可以通过例如将上述抗体或其盐溶解、悬浮或乳化在常规用于注射的无菌水性介质或油性介质中来制备可注射制剂。作为注射用水性介质,有例如生理盐水,一种含有葡萄糖和其他助剂等的等渗溶液,其可以与适当的增溶剂如醇(例如,乙醇)、多元醇(例如,丙二醇、聚乙二醇)、非离子表面活性剂[例如,聚山梨醇酯80、hco-50(氢化蓖麻油的聚氧乙烯(50mol)加合物)]等组合使用。作为油性介质,采用例如芝麻油、大豆油等,其可以与增溶剂如苯甲酸苄酯、苯甲醇等组合使用。这样制备的注射剂可填充在适当的安瓿中。可以将本发明的药物组合物用标准针和注射筒皮下或静脉内递送。设想治疗将不限于临床使用。因此,使用无针装置进行皮下注射也是有利的。对于皮下递送,笔式递送装置容易地用于递送本发明的药物组合物。这种笔式递送装置可以是可重复使用的或一次性的。可重复使用的笔式递送装置通常利用含有药物组合物的可更换药筒。一旦施用
了药筒内的所有药物组合物并且药筒是空的,就可以容易地弃去空药筒并用含有药物组合物的新药筒替换。然后可以重复使用所述笔式递送装置。在一次性笔式递送装置中,没有可更换的药筒。相反,所述一次性笔式递送装置预装有保持在装置内的储器中的药物组合物。一旦储器内的药物组合物排空,则弃去整个装置。许多可重复使用的笔式和自动注射递送装置已应用于本发明的药物组合物的皮下递送。例子包括但当然不限于autopen
tm
(owen mumford,inc.,伍德斯托克,英国)、disetronic
tm
笔(disetronic medical systems,布格多夫,瑞士)、humalog mix 75/25
tm
笔、humalog
tm
笔、humalin 70/30
tm
笔(eli lilly and co.,indianapolis,ind.)、novopen
tm
i、ii和iii(novo nordisk,哥本哈根,丹麦)、novopen junior
tm
(novo nordisk,哥本哈根,丹麦)、bd
tm
笔(becton dickinson,富兰克林湖,新泽西州)、optipent
tm
、optipen pro
tm
、optipen starlet
tm
、和opticlikt
tm
(sanofi-aventis,法兰克福,德国),仅举几例。用于皮下递送本发明的药物组合物的一次性笔式递送装置的例子包括但当然不限于solostar
tm
笔(sanofi-aventis)、flexpen
tm
(novo nordisk)和kwikpen
tm
(eli lilly)。
[0341]
有利地,将上述的用于口服或肠胃外使用的药物组合物制备成适于配合活性成分剂量的单位剂量的剂型。单位剂量的此类剂型包括例如片剂、丸剂、胶囊剂、注射剂(安瓿)、栓剂等。包含的上述抗体的量通常为每单位剂量的剂型约5至约500mg;尤其是在注射剂形式中,对于其他剂型,可以含有约5至约100mg和约10至约250mg的上述抗体。
[0342]
结合多肽、核酸或包含其的组合物可以包含在医用容器如小药瓶、注射筒、iv容器或注射装置中。在一个例子中,结合多肽、核酸或组合物是体外的,并且可以在无菌容器中。在一个例子中,提供了试剂盒,其包含结合多肽、包装和关于在如本文所述的治疗方法中使用的说明书。
[0343]
本发明的一个方面是包含本发明的结合多肽或核酸和一种或多种药学上可接受的赋形剂的组合物,所述赋形剂的例子在上文中列出。“药学上可接受的”是指由美国联邦政府或州政府的监管机构批准或可批准的或在美国药典或其他普遍认可的药典中列出的,用于在动物体内,包括在人体内使用。可将药学上可接受的载体、赋形剂或佐剂与结合多肽(例如本文所述的任何抗体或多肽分子)一起施用于患者,并且不破坏其药理学活性,并且当以足以递送治疗量的药剂的剂量施用时是无毒的。
[0344]
在一些实施方案中,结合多肽将是根据本发明的组合物中的唯一活性成分。因此,组合物可由抗体组成或其可由结合多肽和一种或多种药学上可接受的赋形剂组成。然而,根据本发明的组合物任选地包括一种或多种另外的活性成分。可能需要与根据本发明的结合多肽或核酸一起施用的其他治疗剂包括用于铁过载的其他治疗剂,其例子在本文中描述。可以将任何这样的药剂或药剂的组合与根据本发明的结合多肽或核酸组合施用,或在组合物中提供,无论是作为组合制剂还是单独制剂。可以将根据本发明的结合多肽或核酸与另一种或多种治疗剂(如所提及的那些)分开地和依序地、或并行地且任选地作为组合制剂施用。
[0345]
可以将多种组合物分开或同时施用。分开施用是指在不同时间施用两种组合物,例如相隔至少10、20、30或10-60分钟,或相隔1、2、3、4、5、6、7、8、9、10、12小时。还可以以24小时间隔,或甚至更长间隔施用组合物。可替代地,可以同时施用两种或更多种组合物,例如间隔小于10或小于5分钟。在一些方面,可以将同时施用的组合物作为混合物施用,各组
分具有或不具有相似或不同的时间释放机制。
[0346]
结合多肽及其编码核酸可用作治疗剂。本文的患者一般是哺乳动物,通常是人。可以将结合多肽或核酸例如通过本文所述的任何施用途径施用于哺乳动物。在优选的实施方案中,通过皮下注射施用结合多肽。
[0347]
施用通常以“治疗有效量”进行,这是产生施用所需效果的足以对患者显示益处的量。确切量将取决于治疗目的并且将可以通过本领域技术人员使用已知技术(参见例如,lloyd(1999),the art,science and technology of pharmaceutical compounding)确定。治疗处方,例如对剂量的决定等,在全科医师和其他医生的责任范围内,并且可以取决于所治疗疾病的症状和/或进展的严重程度。结合多肽或核酸的治疗有效量或合适剂量可以通过比较其在动物模型中的体外活性和体内活性来确定。将小鼠和其他测试动物中的有效剂量外推到人的方法是已知的。
[0348]
在本文所述的治疗方法中,可以施用一个或多个剂量。在一些情况下,单剂量可有效实现长期益处。因此,所述方法可包括施用单剂量的结合多肽、其编码核酸或组合物。可替代地,可以施用多剂量,通常依序施用并间隔数天、数周或数月的时间段。例如,可以每2周、每3周或每4周进行施用。任选地,可以将结合多肽每月一次或以更低频率,例如每两个月或每三个月施用于患者。
[0349]
如本文所用,术语“治疗”(treat、treatment、treating)或“改善”(amelioration)是指治疗性治疗,其中目的是逆转、减轻、改善、抑制、减缓或停止与疾病或障碍相关的病症的进展或严重程度。术语“治疗”包括减少或减轻病症、疾病或障碍的至少一种不良作用或症状。如果一种或多种症状或临床标记降低,则治疗通常是“有效的”。可替代地,如果疾病的进展减少或停止,则治疗是“有效的”。也就是说,“治疗”不仅包括症状或标记的改善,还包括与在没有治疗的情况下预期相比,停止或至少减缓症状的进展或恶化。有益或期望的临床结果包括但不限于一种或多种症状减轻、疾病的程度减小、疾病状态稳定(即,不恶化)、疾病进展延迟或减缓、疾病状态改善或缓和、缓解(无论是部分还是全部)和/或死亡率降低,无论是可检测的还是不可检测的。术语疾病的“治疗”还包括提供疾病的症状或副作用的解除(包括姑息治疗)。对于有效的治疗,没有考虑完全治愈。在某些方面,所述方法还可以包括治愈。在本发明的上下文中,治疗可以是预防性治疗。
[0350]
长半衰期是本发明的结合多肽的期望特征。延长的半衰期转化为较不频繁的施用,这需要更少的注射来维持血流中分子的治疗有效浓度。本发明的抗原结合分子在人中的体内半衰期可以是7、8、9、10、11、12、13、14、15、16、17、18、19,20或21天或更长。抗原结合分子在非人灵长类动物如食蟹猴中的体内半衰期可以是7、8、9、10、11、12、13、14、15、16、17、18、19、20或21天或更长。
[0351]
可以提供结合多肽用于以一周、两周、三周、四周或一个月的规则间隔施用。
[0352]
治疗用途
[0353]
本发明解决的治疗适应证包括治疗对抑制mtp-2活性和/或减少铁摄取是有益的患者。特别的治疗领域是以高铁负载和沉积以及无效红细胞生成为特征的贫血。如前所讨论,几种形式的贫血的特征在于无效红细胞生成,通常伴有原发性铁过载(由高红细胞生成活性引起的不适当的低铁调素水平驱动)和主要由于反复的红细胞输血引起的继发性铁过载。铁过载对器官功能有负面影响,并对红细胞生成有负面影响,从而通过增加成红细胞祖
细胞中的高铁血色原和ros并驱动细胞凋亡导致贫血,从而使功能性红细胞减少。降低铁可减少细胞凋亡并改善α/β珠蛋白失衡,从而允许产生更成熟的红细胞。红系细胞的铁利用率降低导致血红素产生减少,红系前体成熟增加和血红蛋白水平增加。因此,在一些情况下,结合多肽的治疗作用模式可以是抑制mtp-2的酶活性,引起铁调素水平增加,这导致铁限制,使得红细胞生成正常化并改进血红蛋白和红细胞质量。
[0354]
除了解决铁过载的毒性作用之外,贫血的治疗还可以进而改进心脏功能并减轻疲劳。
[0355]
根据本发明的治疗效果可以包括:
[0356]
减少膳食铁的吸收,
[0357]
治疗铁过载,
[0358]
提高肝细胞中铁调素的表达,
[0359]
减少由铁过载引起的贫血,
[0360]
降低血清铁浓度,
[0361]
降低转铁蛋白铁饱和度,
[0362]
减少对输血的需求,
[0363]
减少对铁螯合疗法的需求,
[0364]
延长存活,和/或
[0365]
使红细胞生成正常化。
[0366]
治疗在本文讨论的许多病症中可能是有益的,所述病症包括:
[0367]
低风险骨髓增生异常综合征(mds)伴环形铁粒幼细胞(rars),需要输血
[0368]
5q-mds;
[0369]
输血依赖性β-地中海贫血或重度β-地中海贫血;
[0370]
输血非依赖性β-地中海贫血或中间型β-地中海贫血;
[0371]
血色素沉着病,例如在不携带hjv或铁调素突变的患者中,或在1型或3型血色素沉着病中;
[0372]
肝硬化;
[0373]
肝脂肪变性;
[0374]
肝纤维化,例如在nash(非酒精性脂肪性肝炎)或ash患者中;
[0375]
blackfan diamond贫血;
[0376]
肺动脉高压;
[0377]
镰状细胞病中的贫血(“镰状细胞贫血”);
[0378]
真性红细胞增多症;
[0379]
慢性肾病相关贫血(ckd)。
[0380]
因此,根据本发明治疗的患者可具有上述一种病症。治疗方法可包括向患者施用如本文所述的结合多肽、核酸或组合物。配制品和施用方法的例子在本文别处描述。根据疾病状况,治疗可以在出生后不久开始,在诊断后或在开始输血依赖或血清铁蛋白增加或在原本要开始铁螯合时开始。
[0381]
认为,通过使用抗mtp-2结合多肽治疗,铁调素水平增加,将导致tsat水平降低,伴有β-地中海贫血中血红素和高铁血色原产生的诱导降低或mds中环形铁粒幼细胞的发生减
少。这将导致红系祖细胞凋亡更少和红细胞计数更多。虽然单细胞血红蛋白含量将更低,但由于红细胞数量的增加,总血红蛋白水平将更高。这将减少对红细胞输血的需求。
[0382]
避免毒性组织铁过载或降低其风险应增加患者的总存活期,即延长所治疗患者的存活期。通过避免或减少输血负担,和/或避免或减少对铁螯合和/或静脉切开术的需求,还应当改进患者的生活质量。
[0383]
治疗可减轻疾病负担和病症的症状,如与铁代谢有关的β地中海贫血、mds和血色素沉着病,包括毒性铁过载、心力衰竭、肝衰竭、糖尿病和总存活期降低。
[0384]
有趣的是,tmprss6中的遗传多态性736v(a)-》a(g)与较高的铁调素水平相关,并且已经报道在这些疾病的一些中降低铁过载和改善肝酶,表明增加的铁调素水平对肝再生具有积极影响。小鼠研究已显示tmprss6和/或铁调素增加在小鼠肝纤维化模型中的有益作用。
[0385]
mtp-2的抑制还可用于治疗肥胖症。folgueras等人报道了mtp-2缺乏通过调节铁稳态来防止肥胖症(folgueras等人,nat commun.apr 10;9(1):1350 2018)。
[0386]
期望的是,获得患者的有效治疗而没有严重的副作用。未观察到副作用或仅观察到轻微的副作用。
[0387]
可以将用根据本发明的结合多肽进行的治疗与一种或多种另外的疗法(例如,用于治疗铁过载的另外的治疗剂)组合。可以将结合多肽与激活素ii型受体激动剂融合蛋白例如罗特西普组合。由于mtp-2抑制剂对其他计划的和现有的疗法呈现替代的作用模式,因此其潜在地对红细胞生成提供协同效应。因此,(i)mtp-2抑制剂和(ii)tgfβ超家族配体的拮抗剂(例如基于tgfβ超家族受体的配体清除剂/陷阱)的组合可产生有利的治疗效果。
[0388]
各种配体陷阱作用于tgfβ超家族以增加晚期红细胞生成。tgfβ超家族配体包括激活素、gdf-11和骨形态发生蛋白(bmp)。受体配体陷阱分子可通过提供可溶形式的受体胞外结构域来产生,其中所述受体胞外结构域保留结合其一个或多个配体的能力但不诱导下游信号传导(其原本由正常受体:配体相互作用引起)。受体胞外结构域可以与fc区连接形成融合蛋白。
[0389]
优选地,受体是激活素ii受体,例如actiira或actiirb。拮抗剂可以是包含与fc区融合的激活素ii受体(例如激活素受体iib(actriib))可溶性胞外结构域的多肽。罗特西普是一种这样的分子,其目前用于治疗β-地中海贫血和骨髓增生异常综合征中的贫血。actriia和actriib配体陷阱的例子也可以在acceleron pharma的us 7988973中找到,其通过引用并入本文。suragani rn等人先前描述了“rap-536”,其为与鼠igg2a fc结构域连接的经修饰人actriib胞外结构域(具有l79d取代的天然前体残基24-131),据报道它减轻鼠β-地中海贫血中无效的红细胞生成和疾病并发症(blood 123(25):3864-3872 2014)。索特西普是激活素iia型受体igg-fc融合蛋白的例子。可以类似地产生其他tgfβ家族配体的拮抗剂,例如bmpr-fc融合蛋白。
[0390]
替代的拮抗剂包括针对tgfβ超家族配体的抗体(例如抗激活素抗体)。已经描述了抗激活素a抗体,例如加托索单抗(garetosmab)。
[0391]
tgfβ家族配体的拮抗剂例如actriib-fc、actiiriia-fc或bmpr-fc在红细胞生成期间促进红细胞前体的成熟,而mtp-2抑制剂导致铁降低(使病理学上的高铁水平正常化)并因此减缓红细胞生成。根据本文报道的研究(参见实施例22),我们认为这两种作用的组
合导致更成熟的红细胞的更有效产生。例如,我们证明mtp-2抑制剂(由nori-11-m表示)和激活素受体ii配体陷阱(由actriib-fc表示)的组合比单独的配体陷阱更有效,校正了铁过载和相关的贫血。与mtp-2抑制剂的组合可以通过在患有已经指示用tgfβ超家族配体陷阱的病症的患者(例如,非输血依赖性β-地中海贫血患者)中提供更大的治疗效果来扩展tgfβ超家族配体陷阱的治疗潜力。与mtp-2抑制剂的组合还可扩展配体陷阱治疗其他如患有重度β-地中海贫血的那些的患者群体的治疗潜力,对于这些患者,诸如罗特西普等治疗目前具有有限的益处。
[0392]
罗特西普最近被fda批准用于骨髓增生异常综合征。mds患者在变得依赖输血之前开始发生铁过载,因为无效的红细胞生成抑制肝脏中的铁调素产生,从而导致不受限制的肠道铁摄取。输血进而使铁过载加重。同样的情况发生在输血依赖性β-地中海贫血患者中。在用罗特西普(或其他tgfβ超家族配体陷阱)治疗的此类患者中,通过在治疗方案中包括mtp-2抑制剂将改善治疗益处。组合疗法可用于本文所述的任何治疗适应证或病症,例如blackfan diamond贫血。
[0393]
用于组合疗法的mtp-2抑制剂可以是如本文所述的结合多肽,或其可以是另一种类型的分子,如tmprss6表达的核酸抑制剂(例如靶向tmprss6的反义或sirna分子)或小分子抑制剂(例如3-脒基苯丙氨酸衍生的蛋白裂解酶-1和-2蛋白酶抑制剂和衍生物)。已经描述了此类抑制剂的例子(hammami m,r
ü
hmann e,maurer e,heine a,g
ü
tschow m,klebe g,steinmetzer t(2012)new 3-amidinophenylalanine-derived inhibitors of matriptase.med chem commun 3:807-813;pomothy j,szombath g,rokon
á
l p,m
á
tis g,zs n,steinmetzer t,p
á
szti-gere e(2016)the impact of acute matriptase inhibition in hepatic inflammatory models.biomed res int.https://doi.org/10.1155/2016/6306984)。因此,根据本发明治疗的患者可以是还接受用于降低铁过载的另外的治疗剂治疗的患者。方法可以包括将结合多肽和另外的治疗剂任选地在分开的配制品中共施用于患者。可以依序或同时施用组合物。这同样适用于使用小分子或核酸mtp-2抑制剂代替结合多肽的情况,即,可以同时或依序地用mtp-2抑制剂和另外的治疗剂的组合治疗患者。优选将mtp-2抑制剂和另外的治疗剂在分开的配制品中提供并分开施用。通常,依序施用可以在同一天(任选地间隔几分钟或几小时的时间段)或在不同天进行。
[0394]
可以将用mtp-2抑制剂(例如如本文所述的结合多肽)的治疗与促红细胞生成素(epo)组合。达贝泊汀α(商业上称为aranesp)是与标准epoα和epoβ蛋白相比延长药物半衰期的epo的结构再工程化形式。它用于刺激贫血患者的红细胞生成,以增加血红蛋白水平并减少输血需求。根据贫血的严重程度以不同的剂量施用药物,然而,在慢性肾病相关的贫血(ckd)患者中,推荐的起始剂量为每四周0.45mcg/kg iv/sc,直到血红蛋白水平达到10g/dl之上,此时则可降低剂量。在对中间型β地中海贫血患者进行的一项小型研究中,aranesp已显示出提高血红蛋白水平(singer等人2011),然而,由于rbc细胞凋亡和相关脾肿大的不可接受的增加,通常它不是β-地中海贫血患者的治疗选择。如本文呈现的结果显示,通过用根据本发明的结合多肽和用epo治疗患者可以获得治疗益处。例如,应可以通过每2-4周同时进行的两次分开的皮下注射对人共施用aranesp和抗mtp-2mab疗法。基于在β-地中海贫血小鼠模型中获得的结果(参见实施例20和21),这样的共治疗策略应提供来自aranesp疗法的对贫血的治疗性改善,同时维持脾大小并且同时降低由抗mtp2治疗提供的毒性铁过载。
可以针对人研究和优化精确的组合给药方案,但是通常将涉及向患者施用根据本发明的结合多肽,并且还施用促红细胞生成素(优选重组促红细胞生成素或其医学上批准的变体,例如达贝泊汀α)。任选地,将结合多肽和epo同时施用。可替代地,可以将它们依序施用(在同一天或不同天)。任选地,将结合多肽和epo以分开注射或组合注射皮下施用。在一些实施方案中,本发明提供了用epo和结合多肽对患者进行的治疗,其中结合多肽的施用降低了例如患有本文提及的病症如β-地中海贫血的患者中的红细胞凋亡和与施用epo相关的脾肿大。因此,结合多肽可用于使接受epo治疗的患者的红细胞生成正常化。
附图说明
[0395]
现在将参考附图更详细地描述本发明的实施方案,其中:
[0396]
图1是调节用于红细胞生成和其他细胞功能的铁供应的途径图。膳食铁的吸收和从衰老红细胞(“老化的rbc”)中回收的铁的释放受铁调素调节,所述铁调素下调铁转运蛋白(fpn)(一种在肠道肠细胞(摄取膳食铁)和巨噬细胞(摄取衰老红细胞)的膜中发现的铁输出蛋白)。抑制铁转运蛋白减少了铁从这些细胞的输出,从而限制了可用于身体的新的和再循环的铁的供应。肝细胞中铁调素从hamp基因的表达受bmp/smad途径调节,所述bmp/smad途径由配体bmp6与肝细胞表面上的受体(例如,hjv和bmpr i-ii)的结合启动。来自升高的血清铁浓度的负反馈可上调bmp/smad途径以增加铁调素表达,并由此减少铁通过铁转运蛋白的释放。蛋白裂解酶-2(mtp-2)也存在于肝细胞表面,并下调bmp/smad途径,推测是通过切割共受体如hjv,从而降低铁调素的表达并使铁能够通过铁转运蛋白更多地释放。
[0397]
图2示出mtp-2的结构域结构。
[0398]
图3示出在使用(a)人和(b)小鼠mtp-2进行的基于蛋白质的酶测定中,所选择的抗mtp-2抗体和阴性对照抗体的全剂量反应曲线。所有抗体均为同种型人igg4pe。
[0399]
图4示出从转基因小鼠免疫获得的(a)第一组抗体和(b)第二组抗体在使用人mtp-2ecd的酶测定中抗体的抑制作用%相对于在使用小鼠mtp-2ecd的酶测定中抗体的抑制作用%作图。
[0400]
图5示出在使用人mtp-2ecd的基于细胞的酶测定中所选择的抗mtp-2抗体和阴性对照抗体的全剂量应答曲线。所有抗体均为同种型人igg4pe。
[0401]
图6示出与无头人mtp-2ecd(缺少丝氨酸蛋白酶结构域的重组mtp-2ecd)结合的抗体的htrf测定的结果。ic=同种型对照。所有抗体均为人igg4pe。
[0402]
图7示出与野生型(a)人、(b)小鼠和(c)食蟹猴mtp-2ecd结合的抗体的htrf测定结果。ic=同种型对照。所有抗体均为人igg4pe。
[0403]
图8示出所选择的抗mtp-2抗体或未标记的抑蛋白酶多肽竞争结合(a)人和(b)小鼠mtp-2ecd的htrf竞争测定结果。ic=针对标记的抑蛋白酶多肽-647的同种型对照。所有抗体均为人igg4pe。
[0404]
图9示出用抗mtp-2抗体或对照治疗的野生型小鼠的(a)hamp mrna水平和(b)血清铁水平。
[0405]
图10示出用10mg/kg nori-010治疗24小时、7天和14天或用阴性对照抗体(单一时间点)治疗的野生型小鼠中的(a)hamp mrna水平,(b)血清铁水平,(c)tsat和(d)mcv。
[0406]
图11示出用3mg/kg nori-010治疗24小时、7天和14天或用阴性对照抗体(单一时
间点)治疗的野生型小鼠中的(a)hamp mrna水平,(b)血清铁水平,(c)tsat和(d)mcv。
[0407]
图12示出用人或小鼠抗mtp-2抗体或其同种型对照治疗的小鼠的(a)hamp mrna水平和(b)血清铁水平。
[0408]
图13示出在正常小鼠中以10、3和1mg/kg单次ip注射后nori-008的时程评估结果(a)hamp,(b)血清铁,(c)pk。
[0409]
图14示出在1周时间点(10mg/kg ip剂量)评估igg/κ抗mtp2抗体降低血清铁和转铁蛋白饱和度的结果。
[0410]
图15示出对完全人igg4和小鼠igg1形式的三种抗mtp-2抗体以及它们在皮下注射后降低血清铁浓度的能力的评价结果。
[0411]
图16示出单次10mg/kg sc或ip注射抗体后第7天的(a)血清铁浓度和(b)抗体浓度。在(a)中,黑色圆圈代表huigg4pe同种型对照,以及灰色方块代表nori-010。
[0412]
图17示出第一体内大鼠研究的结果,其中在3只野生型wistar大鼠组中以10mg/kg ip给药nori-008和nori-010。
[0413]
图18示出第二体内大鼠研究的结果,其中在5只野生型han wistar大鼠组中以10mg/kg sq各自给药nori-008、nori-011、nori-003和nori-006。
[0414]
图19示出使用nori-010在中间型地中海贫血的hbbth3/+小鼠模型中进行2周研究的结果。a)通过qpcr从肝脏样品测量的铁调素mrna,b)通过生色测定测量的血清铁水平[μg/dl]和c)计算的转铁蛋白饱和度[%]。
[0415]
图20示出在存在或不存在促红细胞生成素的情况下,使用nori-011-m在中间型地中海贫血的hbbth3/+小鼠模型中进行8周研究的结果。a)通过qpcr从肝样品测量的铁调素mrna,b)红细胞计数,c)每克组织湿重的肝组织铁含量,d)血红蛋白水平,e)血细胞比容,f)平均红细胞体积(mcv),g)红细胞分布宽度(rdw),h)红细胞平均血红蛋白量(mch),i)通过流式细胞术测定的脾脏中红细胞谱系细胞的发育阶段i-v中的细胞数,j)通过流式细胞术测定的骨髓中红细胞谱系细胞的发育阶段i-v中的细胞数和k)脾指数。
[0416]
图21示出在与actriib-fc进行或不进行共同治疗下,使用nori-011-m在中间型地中海贫血的hbbth3/+小鼠模型中进行8周研究的结果。将nori-11-m以10mg/kg每周一次ip施用,将actriib-fc以10mg/kg每周两次ip给予。在8周研究结束时取得用于读出的所有样品。a)通过qpcr从肝样品测量的铁调素mrna,b)每克组织湿重的肝组织铁含量,c)红细胞计数(rbc),d)血红蛋白水平(hb),e)血细胞比容(hct),f)平均红细胞体积(mcv),g)红细胞分布宽度(rdw),h)红细胞平均血红蛋白量(mch),i)通过流式细胞术测定的脾脏中红细胞谱系细胞的发育阶段i-v中的细胞数,j)通过流式细胞术测定的骨髓中红细胞谱系细胞的发育阶段i-v中的细胞数和k)脾指数。
实施例
[0417]
这里我们描述了靶向mtp-2的抗体,用于治疗铁过载疾病。通过对产生具有人可变结构域的抗体的转基因小鼠进行免疫,并在一系列生物相关测定中测试各种抗体,我们能够获得物种交叉反应性mtp-2特异性单克隆抗体(mab),其是mtp-2酶活性的体外和体内交叉反应性中和物。我们表明,所选择的mab在单剂量后提高肝细胞的铁调素表达水平。铁调素的升高通过增加铁转运蛋白的内化和降解而降低血清铁和转铁蛋白饱和度。在代表β-地
中海贫血模型的hbb
th3/+
小鼠中,10mg/kg的单剂量在2周时间点使血清铁和转铁蛋白饱和度分别降低52%和47%。此外,通过重复给药,我们在hbb
th3/+
小鼠中观察到经数周的持续铁限制。这些结果表明,此类mab具有治疗铁过载患者以减少其贫血和减少其输血和铁螯合需求的潜力。
[0418]
实施例1-抗mtp-2抑制性抗体组套的产生
[0419]
使用各种不同的免疫方案和抗原形式,用mtp-2免疫产生具有人可变结构域的抗体的kymab转基因小鼠,并选择抗原特异性b细胞。参见lee等人,nat biotechnol 32(4):356-632014;wo 2011/004192;wo 2011/158009和wo 2013/061098。在基于蛋白质和基于细胞的体外测定中,测试抗体与人mtp-2和小鼠mtp-2的结合以及所述抗体抑制人和小鼠mtp-2的酶活性的能力。
[0420]
均相时间分辨fret(htrf)测定和流式细胞术测定用于初步筛选,以建立回收的抗体与纯化的mtp-2胞外结构域(ecd)的结合,随后确认与细胞表面表达的mtp-2的结合。
[0421]
针对结合人和非人(小鼠和食蟹猴)mtp-2ecd的能力选择交叉反应性抗体。
[0422]
然后在多种功能测定中筛选所选择的抗体,以评估它们抑制溶液中的经纯化人和小鼠mtp-2ecd的酶活性和抑制hek293细胞上表达的人mtp-2的酶活性的能力,如在含有生色mtp-2底物的酶测定中所评估的。
[0423]
虽然获得了许多不同的抗体,包括结合和抑制人mtp-2而非小鼠mtp-2的抗体以及结合和抑制小鼠mtp-2而非人mtp-2的其他抗体的例子,但选择下表g中所列的抗体对于mtp-2活性的交叉反应性抑制剂的潜在开发是特别感兴趣的。
[0424]
[0425][0426]
表g.所选择的抗mtp-2抑制性抗体,示出了通过重组产生这些抗体的vh结构域的人种系v、d和j基因区段和通过重组产生这些抗体的vl结构域的人种系v和j基因区段。
[0427]
实施例2-抗体序列
[0428]
抗体nori-001至nori-033中每一种的hcdr、lcdr、vh结构域和vl结构域的序列示于表s中。示出每种抗体的完整igg4pe重链。还示出每种抗体的完整轻链。除非上下文另有规定,否则“nori-001”是指具有表s中针对nori-001所示的vh和vl结构域的抗体。可以指示抗体的形式,例如“nori-001igg”是具有nori-001vh结构域和nori-001vl结构域的igg,以及“nori-001scfv”是具有nori-001vh结构域和nori-001vl结构域的scfv。
[0429]
确定抗体nori-002在vh结构域中具有高风险的游离半胱氨酸倾向。尽管认为通过结构软件中的分析被掩盖,但该氨基酸被突变以减轻任何潜在的倾向。因此,将c49c突变引入nori-002中,并将包含该突变的新抗体命名为nori-003。
[0430]
通过将p124s突变引入vh结构域中,对抗体nori-010进行序列优化以提高稳定性和表达,从而产生新的抗体nori-011。
[0431]
实施例3-在使用mtp-2ecd的基于蛋白质的酶测定中对mtp-2的抑制
[0432]
在使用人和小鼠mtp-2ecd的酶测定中评估抗体抑制丝氨酸蛋白酶切割经标记的
mtp-2底物以产生可检测产物的能力。
[0433]
在该测定中,抗体nori-001至nori-034均抑制人和小鼠mtp-2二者的酶活性。抑制人mtp-2的ic50值的范围为大约1.5至55nm。抑制小鼠mtp-2的ic50值的范围为大约0.48至40nm。表d。图3。
[0434]
[0435][0436]
表d.抗体nori-001至nori-034在基于蛋白质和细胞的测定中抑制mtp-2酶活性的效力,表示为ic50值。当基于细胞的测定未示出任何值时,在所述测定中没有测试该抗体。
[0437]
通过比较抗体在使用人mtp-2ecd的测定中的抑制与其在使用小鼠mtp-2的测定中的抑制来评估抗体的交叉反应性。通过将两种测定中的抑制百分比值对彼此作图,可以观察到一些抗体对人mtp-2具有特异性而其他抗体对小鼠mtp-2具有特异性,并且对人和小鼠mtp-2二者存在不同程度的抑制。图4。
[0438]
用于基于蛋白质的酶测定的材料和方法
[0439]
对于初始测定,将阳性和阴性对照,即抑蛋白酶多肽(sigma-a3428)和非mtp-2结合性huigg4pe同种型抗体分别在测定缓冲液(200mm tris hcl和1mg/ml bsa,ph 9.0)中以1:3连续稀释,2x终浓度,起始浓度为200nm。在后面的测定中,使用的阳性和阴性对照分别是10nm的nori-008huigg4pe和非mtp-2结合性huigg4pe同种型抗体。
[0440]
将20μl滴定对照和稀释抗体铺板于384孔固体白色板(α板-6005350)中,并将10μl人或小鼠mtp-2ecd蛋白铺板于顶部,由于酶活性的差异,终浓度分别为0.5或2mg/ml。然后将板覆盖并在室温下孵育30分钟。然后将10μl荧光mtp-2肽底物boc-gln-gly-arg-amc(bachem ag-4016429.0050)以在测定缓冲液中50μm的终浓度添加到每个孔中。使酶反应在室温下进行,然后在30分钟、1小时和2小时用360nm的激发波长和460nm的发射波长在板读取器(envision)上读取荧光活性。在通过mtp-2酶的酶活性切割底物肽时,7-酰胺基-4-甲基香豆素(amc、mca或nhmec)部分从c末端释放。amc是在c末端掺入羧肽酶底物中的荧光团。然后可以使用分光荧光计通过在360-380nm下激发并在440-460nm下检测发射来激发释放的香豆素。将阳性和阴性对照分别取为终浓度为200nm的抑蛋白酶多肽/nori-008igg和huigg4pe同种型的16孔的平均值。通过将抑制值输入graphpad软件产生对数曲线,并使用非线性回归参数和对数(抑制剂)与反应-变量斜率(四个参数)方程产生ic50值。
[0441]
抗原试剂的产生细节参见实施例5。
[0442]
实施例4-在使用细胞表面表达的mtp-2的基于细胞的酶测定中对mtp-2的抑制
[0443]
在使用细胞表面表达的人mtp-2的酶测定中评估抗体抑制丝氨酸蛋白酶切割经标记的mtp-2底物以产生可检测产物的能力。
[0444]
在该测定中,抗体nori-008至nori-010、nori-012至nori-014以及nori-017至nori-034均抑制人mtp-2的酶活性。抑制人mtp-2的ic50值的范围为大约0.083nm至17nm。表d。图5。
[0445]
在该基于细胞的测定中,mtp-2由细胞表达并展示在细胞表面上,其中它经历自激活以产生切割其底物的经激活mtp-2。本测定中的抑制剂可通过多种分子机制起作用。例如,在该测定中显示抑制的抑制剂可以结合并抑制mtp-2酶原转化为自激活的mtp-2(图2),
从而防止形成激活形式的mtp-2(其原本在该测定中切割其底物),和/或在该测定中的抑制剂可以结合并抑制激活形式的mtp-2。
[0446]
抗体nori-001至nori-034抑制细胞表面表达的mtp-2的能力证实了它们在基于细胞的环境中对mtp-2的活性,在所述环境中靶抗原在细胞上经历表达和激活,这是体内情况的特征。
[0447]
用于基于细胞的酶测定的材料和方法
[0448]
将用于筛选的所有抗体以及阳性和阴性对照在expi293培养基(a1435101)-无血清培养基(ph 8)中1:3连续稀释,添加高葡萄糖和glutamax-2x终浓度,起始浓度为200nm。将12.5μl抗体(纯化的蛋白a)和对照铺板到96孔固体白色板(corning-cls3917-100ea)中,并在顶部分配25μl在expi293培养基中的细胞(6250个细胞/孔)。然后以在expi293培养基中50μm终浓度向每个孔中添加12.5μl荧光mtp-2肽底物(bachem ag-4016429.0050)。使酶反应在培养箱中在37℃和5%co2下进行过夜。第二天,在360nm激发波长和460nm发射波长下在板读取器(envision)上读取荧光活性。将阳性和阴性对照分别取终浓度为200nm的抑蛋白酶多肽和huigg4pe同种型的4孔的平均值。
[0449]
对于初始测定,阳性对照是抑蛋白酶多肽(sigma-a3428)。对于之后的测定,阳性对照是nori-008huigg4pe。非mtp-2结合性huigg4pe同种型抗体用作阴性对照。
[0450]
抗原试剂的产生细节参见实施例5。
[0451]
实施例5-抗原材料的制备
[0452]
用于蛋白质表达的构建体的产生
[0453]
为了产生用于本文所述测定的纯化蛋白质,我们使用编码以下的dna序列:
[0454]
·
wt人蛋白裂解酶-1(uniprot seq id no:q9y5y6)的胞外结构域(ecd)aa 77-855
[0455]
·
野生型(wt)人mtp-2(uniprot seq id no:q8iu80)aa 78-811
[0456]
·
wt小鼠mtp-2(uniprot seq id no:q9dbi0)aa 80-811
[0457]
·
wt大鼠mtp-2(ncbi seq id:xp006242057.1)aa 80-811
[0458]
·
食蟹猴mtp-2(uniprot seq id no:a0a2k5vap0)aa 73-800
[0459]
上述氨基酸序列也提供在表s中作为参考。
[0460]
这些编码序列与c末端his标签和n末端前导序列融合,进行密码子优化以用于哺乳动物表达,并进行表达。
[0461]
为了产生mtp-2抗原,可以通过与未标记的mohai-2ecd抗原共表达,然后通过镍柱纯化his标记的抗原来大大提高表达。出于此目的,将编码wt小鼠hai-2(uniprot seq id no:q9wu03)aa 28-197的dna与n末端免疫球蛋白前导序列融合,进行密码子优化以用于哺乳动物表达,并进行表达。
[0462]
使用金门和aari限制性位点在cmv启动子的控制下将dna序列克隆到ptt5蛋白表达载体中。使用pei转染试剂将表达质粒转染到cho-3e7细胞中。
[0463]
用于稳定细胞系产生的全长抗原构建体的产生
[0464]
出于筛选mtp-2特异性抗体的目的,产生了表达相关抗原的稳定细胞系。
[0465]
对编码各自与n末端egfp和c末端flag标签(dykddddk)融合的野生型(wt)人mtp-2(uniprot seq id no:q8iu80)氨基酸(aa)1-811、wt小鼠mtp-2(uniprot seq id no:
q9dbi0)aa 1-811的全长dna序列进行密码子优化以用于哺乳动物表达。对未标记的食蟹猴mtp-2(uniprot seq id no:a0a2k5vap0)aa 1-800重复该过程。将dna序列克隆到表达载体中,其处于cmv启动子的控制下且侧翼为3’和5’piggybac特异性末端重复序列,这促进稳定整合到细胞基因组中(参见:“a hyperactive piggybac transposase for mammalian applications”;yusa k.,等人,proc.natl.acad.sci.u s a.,108(4):1531-6,2011年1月25日)。cmv启动子表达载体含有嘌呤霉素选择盒以促进稳定的细胞系产生。
[0466]
亚型2:未标记形式的wt人mtp-2aa 10-811和wt小鼠mtp-2氨基酸13-811通过pcr定向诱变由上述构建体产生,并再克隆到与前述相同的表达载体中。亚型2:未标记形式的k253e、v736a和k253e+v736a人wt mtp-2(uniprot seq id no:q8iu80)序列aa 10-811变体也通过pcr定向诱变产生,并再克隆到与前述相同的表达载体中。
[0467]
对编码具有c末端his标签融合物的wt人蛋白裂解酶-1(mtp-1)(uniprot seq id no:q9y5y6)aa 1-855、具有c末端his标签融合物的wt人蛋白裂解酶-3(mtp-3)(uniprot seq id no:q7rty8)aa 1-854和未标记的wt小鼠hai-2(uniprot seq id no:q9wu03)aa1-252的全长dna序列都进行密码子优化以用于哺乳动物表达,克隆到与前述相同的使用cmv启动子的表达载体中。mtp-1和mtp-3的表达载体含有嘌呤霉素选择盒,而mohai-2的表达载体含有新霉素选择盒以促进双重稳定细胞系产生。
[0468]
表达mtp-1、mtp-2和mtp-3抗原的经稳定转染的hepa 1-6、cho和hek-293细胞的产生
[0469]
为了产生表达wt人mtp-2egfp/flag标记的aa 1-811的人胚肾(hek)-293细胞系,根据制造商的说明书使用freestyle max转染试剂(invitrogen)将cmv启动子表达质粒与编码piggybac转座酶的质粒共转染到人胚肾(hek)-293细胞中。
[0470]
为了产生表达wt人mtp-2egfp/flag标记的aa 1-811的中国仓鼠卵巢(cho)细胞系,根据制造商的说明书使用freestyle max转染试剂(invitrogen)将cmv启动子表达质粒与编码piggybac转座酶的质粒共转染到中国仓鼠卵巢(cho)细胞中。
[0471]
为了产生表达未标记的wt人mtp-2aa 10-811和wt小鼠aa 13-811mtp-2的细胞系,将cmv启动子表达质粒与编码piggybac转座酶的质粒共转染到hek293中。根据制造商的说明书使用freestyle max转染试剂(invitrogen),也将wt人aa 10-811和wt小鼠aa 13-811mtp-2未标记构建体与编码piggybac转座酶的质粒共转染到hepa 1-6细胞系中。
[0472]
为了产生表达his标记的wt人mtp-1aa 10-855和wt人mtp-3aa 1-854的细胞系,根据制造商的说明书使用freestyle max转染试剂(invitrogen)将mtp-1和mtp-3cmv启动子表达质粒与wt mohai-2表达质粒和编码piggybac转座酶的质粒共转染到hek293细胞系中。
[0473]
转染后二十四小时,向培养基中补充嘌呤霉素(2.5μg/ml)或g418(1mg/ml)或嘌呤霉素(2.5μg/ml)和g418(1mg/ml)二者,并生长至少两周以选择稳定的细胞系。每3-4天更换细胞培养基。选择后,将表达wt人mtp-2egfp/flag标记的aa 1-811的hek293细胞系连续稀释成单克隆细胞系以用于最高表达。对表达wt和s762a人mtp-2egfp/flag标记的aa 1-811的cho细胞系进行这种重复。使用抗flag apc缀合的抗体(biolegend-637308)通过流式细胞术评估flag标记的人或小鼠mtp-2构建体在细胞上的表达,而使用未标记的抗his一抗(abcam-ab18184),随后使用山羊抗小鼠647缀合的二抗(citeab-115-605-071)通过流式细胞术评估his标记的人mtp-1、人mtp-3以及人和小鼠mtp-2构建体的表达。选择后,对稳定的
表达未标记的wt人mtp-2和wt小鼠mtp-2的hek293细胞以及稳定的表达未标记的wt人mtp-2和wt小鼠mtp-2的hepa 1-6细胞进行facs分选以用于高表达。使用apc缀合的抗mtp-2抗体,通过流式细胞术评估未标记的人、小鼠和食蟹猴mtp-2构建体在细胞上的表达(包括人和小鼠突变体和人变体构建体)。
[0474]
完全hek293和hepa 1-6培养基由补充有10%v/v胎牛血清(gibco)的杜氏改良伊格尔培养基(gibco)组成。转染期间,使贴壁cho细胞在补充有10%v/v胎牛血清(gibco)的ham's f-12营养混合物(gibco)中培养。转染后,用由补充有8mm glutamax(gibco)的cd-cho培养基组成的完全cho-s培养基悬浮培养表达抗原的cho细胞。此处用于表达的cho-3e7细胞包括ptt5载体系统和可从加拿大国家研究委员会获得的cho ebna 1细胞,但也可使用其他cho细胞系。
[0475]
实施例6-结合亲和力和动力学的表面等离子体共振测定
[0476]
使用biacore 8k系统(ge healthcare),通过表面等离子体共振(spr)进行解离速率筛选。将抗人fc混合物(约1000ru)固定在hbs-p+缓冲液(ge br100671)ph 7.4中的活性物和参考通道中。然后将抗mtp-2huigg4pe抗体仅在活性物通道上以10μl/min在1μg/ml浓度下捕获60秒(大约捕获35和50ru)。然后以30μl/min注射mtp-2ecd蛋白分析物(浓度为100、25、6.25、1.56和0nm)120秒(缔合时间),并监测解离600秒。使用多循环动力学模式,使用所有8个通道。从每种抗体的传感图中减去参考和背景,并使用biacore评价软件中的1:1相互作用模型拟合数据。rmax、ka、kd经全局拟合,ri=0。测试抗体的亲和力(kd)的范围为大约0.012nm至8.5nm。表k.
[0477][0478][0479]
表k.通过表面等离子体共振测定的抗mtp-2抗体的抗体:抗原结合动力学。*表示抗体的kd(解离速率)太慢,且不能用该测定设置测定。真实kd可以《所示的值。
[0480]
还使用上述spr方法用“无头”humtp-2ecd 78-576aa而不是完整ecd评估结合。无头ecd对应于没有丝氨酸蛋白酶结构域的mtp-2ecd。“无头”humtp-2ecd 78-576aa蛋白的氨
基酸序列对应于序列表s中所示的人蛋白裂解酶-2掩蔽ecd蛋白his标签。未检测到7种抗体中的任一种针对无头蛋白的结合,表明所有这些抗体的表位在丝氨酸蛋白酶结构域中。
[0481][0482]
表w.交叉反应性抗mtp-2抗体的抗体:抗原结合动力学
[0483]
发现nori-011、nori-008、nori-003和nori-006与人、小鼠、食蟹猴和大鼠mtp-2ecd蛋白都具有交叉反应性结合。spr中使用的这些蛋白的序列分别由序列表s中的人蛋白裂解酶-2ecd蛋白his标签、小鼠蛋白裂解酶-2ecd蛋白his标签、食蟹猴蛋白裂解酶-2ecd蛋白his标签、大鼠蛋白裂解酶-2ecd蛋白his标签和人蛋白裂解酶-2掩蔽ecd蛋白his标签给出。因为没有检测到这4种抗体中的任一种对人蛋白裂解酶-2掩蔽ecd蛋白his标签的结合,这表明不结合his标签,并且所有抗体的表位都在丝氨酸蛋白酶结构域中。nori-008对于人或小鼠mtp-2的真实kd值由于非常慢的解离速率而不能准确测量。
[0484]
实施例7-与mtp-2丝氨酸蛋白酶结构域的结合
[0485]
对实施例6中的抗体组套进行的spr分析显示,对缺失丝氨酸蛋白酶结构域的截短“无头”humtp-2蛋白没有检测到结合。这表明这些抗体结合mtp-2的丝氨酸蛋白酶结构域。可以预期此类抗体通过阻断或扭曲丝氨酸蛋白酶结构域活性位点来机械地阻断mtp-2,从而防止切割底物。
[0486]
对该无头蛋白进行nori-003、nori-006、nori-008和nori-011的htrf结合测定,并证实没有可检测的结合(图6),而对没有c末端截短的所有人、小鼠和食蟹猴mtp-2蛋白检测到结合(图7)。这再次表明这些抑制性抗体的结合表位在丝氨酸蛋白酶结构域中。另一种抗体nori-036结合无头和完整ecd二者,表明其识别mtp-2上丝氨酸蛋白酶结构域之外的结合位点。
[0487]
实施例8-与抑蛋白酶多肽的竞争
[0488]
抑蛋白酶多肽是一种泛丝氨酸蛋白酶抑制剂,且已知其占据丝氨酸蛋白酶的活性位点。针对标记的抑蛋白酶多肽的htrf竞争测定证实nori-003、nori-006、nori-008和nori-011在该相同位点或其附近结合,并与抑蛋白酶多肽竞争结合人mtp-2蛋白。对于nori-003和nori-006,尽管对humtp-2具有有力的酶抑制ic50值,但这种竞争是弱的,表明这些克隆针对的表位可能接近活性位点,但与抑蛋白酶多肽的结合位点不相同。这通过它们缺乏抑蛋白酶多肽对momtp-2的竞争而证实,而酶测定中的ic50值与nori-011的相似。nori-008在spr和抑蛋白酶多肽竞争测定中分别显示出非常低的kd值和ic50值,表明其结合位点与抑蛋白酶多肽的结合位点相同或紧密重叠。图8。表l.
[0489][0490]
表l.对人和小鼠mtp-2的酶抑制和与抑蛋白酶多肽竞争的抗体ic50值。
[0491]
用于htrf竞争测定的材料和方法
[0492]
将抗体以4x浓度滴定到htrf缓冲液(含有0.1%bsa(sigma-a7906)和氟化钾0.53m(sigma-60240-250g)的dpbs(gibco-14190144))中,起始浓度为200nm。将5μl/w抗体添加至384孔白色板(greiner-784904)中。将humtp-2和momtp-2的纯化蛋白稀释到htrf缓冲液(humtp-2=40nm和momtp-2=240nm)中,4x终浓度并以5μl/w铺板。然后将moigg1骨架中的抗mtp-2mab(nori-037)用在htrf缓冲液中以1:1000稀释度4x终浓度的delfia eu-n1兔抗小鼠igg抗体(ad0207)稀释至1.2nm 4x终浓度。最后,将647标记的抑蛋白酶多肽(sigma-a3428)在htrf缓冲液中稀释至20nm 4x终浓度,并以5μl/w铺板。在黑暗中在室温下将板孵育3小时或更长时间。使用htrf 100闪烁方案在1h、2h和3h下在envision板读取器上读取板。(ex:340nm em1:620nm em2:665nm)。
[0493]
实施例9-进展到体内研究
[0494]
mtp-2已经通过各种模型和概念被验证为通过增加铁调素浓度而成为解决铁过载贫血的靶标。人类遗传学已经表明,在临床前模型和临床干预中,mtp-2活性的缺乏或阻断可以增加铁调素水平并因此降低铁过载。例如,tmprss6敲除小鼠是有活力的,但其特征在于高铁调素水平,因此铁限制导致体毛脱落但不在头部区域周围,产生暂时的所谓“掩蔽”表型。将这些小鼠与具有半合子β珠蛋白链缺失的β地中海贫血小鼠杂交,由于在这些杂交中看到铁调素增加,因此可以改善红细胞计数和血红蛋白(nai等人,2012)。此外,在人中,tmprss6基因的突变引起罕见形式的贫血,其中铁调素水平异常高,使得患者患有不能通过给予更多铁来校正的缺铁(铁难治性缺铁性贫血-irida)(lenoir等人,blood 117:647-650 2011;nai等人,2012同上)。
[0495]
mtp-2活性的抑制表明抗体可能能够增加铁调素表达并因此防止铁过载,铁过载是b-地中海贫血的发病和死亡的主要原因。体内证实了这种活性的抗体由此能够改善β-地中海贫血中的贫血,并且是用于治疗铁过载患者或处于铁过载风险中的那些患者的有价值的治疗剂。
[0496]
体内评估包括评估野生型小鼠中肝细胞中铁调素基因mrna转录的增加和血清铁的减少。该评估的读出可在给药24小时内获得,允许快速确认抗体活性。
[0497]
期望的作用机制是抑制wt mtp-2酶活性和抑制对肝细胞的细胞表面上的下游底物的切割。其直接影响是在施用6小时内可观察到铁调素mrna转录增加2-8倍之间。铁调素表达的增加导致在相似的时间范围内抑制血清铁,并因此抑制转铁蛋白饱和。随着健康动
物中对mtp-2的持续抑制和对血清铁的限制,平均红细胞体积(mcv)和红细胞分布(rdw)降低,这通常在2周后开始表现出来,条件是药物保持存在和活性。
[0498]
被选择用于体内测试的抗体是基于它们对人和小鼠mtp-2蛋白以及细胞表面表达的mtp-2展现出浓度依赖性酶活性抑制而选择的。如果抗体被认为在表达和/或纯化产率方面具有潜在的挑战,造成开发性风险,如果在体外没有观察到针对人或小鼠ecd蛋白的完全酶抑制,或如果产生的ic50值被认为太低,则排除抗体。
[0499]
还在体内测试了在酶测定中示出弱抑制的两种抗体。两者在体内表现非常差,支持抗体必须对mtp-2酶活性具有一定水平的抑制以便在体内表现良好的假设。因此,体外抑制显现是体内功效的必要标准。然而,这可能并不总是足以实现体内效果。对于一些抗体,我们在短期内观察到强的体内性能,但随着时间的推移并没有保持。其他因素,如与小鼠产生的药代动力学或抗药物抗体有关的因素,可影响这些模型中的长期体内性能。
[0500]
实施例10.测定抗mtp-2抗体对野生型小鼠中铁调素mrna和血清铁的影响的方案
[0501]
铁测定方案
[0502]
为了产生图13、14、15、16、17和18中所示的数据,使用quantichrom
tm
铁测定试剂盒(bioassay system,dife-250)进行铁定量。
[0503]
简言之,根据试剂盒方案制备铁标准品。此后,将25μl标准品或样品添加至96孔板上的孔中,随后添加200μl试剂a。然后在微板分光光度计上在595nm处读取该板(读数a)。然后向孔中添加10μl试剂b,接着添加10μl试剂c。然后将板在室温下孵育40分钟,然后在板读取器上在595nm处读取(读数b)。对于所有孔,通过从读数b减去读数a计算吸光度的增加。然后绘制标准曲线,并从标准曲线读取未知的样品铁值。
[0504]
为了产生图9、10、11、12和19中所示的数据,根据试剂盒中提供的方案使用铁直接法测量(f
érè
ne)试剂盒进行血清铁含量分析。
[0505]
简言之,将25μl标准品或来自研究动物的血清与125μl溶液r1和25μl溶液r2一起在96孔中孵育,然后按照600nm clf方案在envision微板读取器上读取板(吸光度a1)。添加2.5μl色原。在室温下孵育20分钟后,按照与先前相同的envision方案读取板(吸光度a2)。结果如下计算:
[0506][0507][0508]
计算为低于0的任何值将报告为0。
[0509]
转铁蛋白饱和度(tsat)的计算
[0510]
根据试剂盒中提供的方案,使用铁固定潜伏期测量试剂盒进行tsat分析。简言之,将25μl标准品或来自研究动物的血清与125μl溶液r1在96孔板中在室温下孵育3min。然后按照600nm clf方案在envision微板读取器上读取板(吸光度a1)。将25μl标准品或来自研究动物的血清与125μl工作溶液(50:1体积的r1:r2)在室温下孵育5min。然后按照与先前相同的envision方案读取板(吸光度a2)。结果如下计算:
[0511][0512]
计算为低于0的任何值将报告为0。
[0513]
血清抗体水平分析
[0514]
使用以下测定确定血清抗体浓度:将96孔板在4℃下用50μl/孔的小鼠抗人igg4 fc(2μg/ml pbs)包被过夜。使用板洗涤器用300μl/孔的pbd-t(pbs加0.1%tween)洗涤板三次。在室温下使用150μl/孔pbs加1%bsa封闭板1小时。稀释样品(使用合并的小鼠血清),制备qc和标准曲线(10点(7.81-2000ng/ml))。然后使用板洗涤器用300μl/孔的pbd-t(pbs加0.1%tween)洗涤板三次。将50μl/孔的标准曲线、样品或qc添加到测定板中,然后将其在室温下以300rpm振荡孵育1小时。然后使用板洗涤器用300μl/孔的pbd-t(pbs加0.1%tween)洗涤板三次。将50μl/孔的以1:12000稀释于pbs加1%bsa中的hrp缀合的小鼠抗人κ添加到板中,然后在室温下在300rpm振荡下孵育1小时。然后使用板洗涤器用300μl/孔的pbd-t(pbs加0.1%tween)洗涤板三次。向每个孔中添加100μl tmb底物。室温下避光孵育10分钟。然后添加100μl/孔的终止溶液(1m硫酸)。使用设定为450nm的微板读取器测量每个孔的光密度,参考读数是在高于540nm处的。从450nm读数减去参考读数。然后将数据导入softmax pro中,并使用标准品的加权因子为1/y的4pl曲线拟合进行回归,从标准曲线读出样品浓度。
[0515]
rna提取
[0516]
使用qiagen rneasy plus mini试剂盒根据试剂盒中的方案从肝样品制备rna。使冷冻样品在湿冰上解冻。然后向样品中添加600μl buffer rlt plus。然后使用塑料杵将样品均质化。然后用1ml注射筒和20g针头将样品氚化。然后离心样品,将上清液置于2ml eppendorf中的gdna消除旋转柱中,弃去沉淀。离心旋转柱和管,保持流动通过并弃去柱。然后将600μl 70%乙醇添加至流过物中。然后将700μl样品置于2ml收集管中的rneasy旋转柱上,然后离心。弃去流过物。然后将旋转柱放回2ml收集管中。并将700μl buffer rw1添加至旋转柱中。然后离心旋转柱并弃去液体流过物。将旋转柱放回到2ml收集管中,并将500μl buffer rpe添加至旋转柱中,并将旋转柱离心。弃去流过物,并如上重复用buffer rpe洗涤柱。以8000x g离心15秒。将旋转柱放入新的2ml收集管中,并充分离心1分钟以干燥膜。将旋转柱置于新的1.5ml收集管中,并将30-50μl无rnase的水直接添加至旋转柱膜中。离心旋转柱1分钟以洗脱rna。使用nanodrop估计流过物中的rna水平(见下文),然后将溶液储存在-20℃或-80℃下。
[0517]
qpcr分析
[0518]
在mrna提取后,通过nanodrop对来自每只小鼠的肝脏的mrna进行定量,并且全部归一化为5ng/μl。简言之,通过qrt-pcr测量小鼠铁调素(hamp)mrna的转录水平,并将其归一化为小鼠次黄嘌呤-鸟嘌呤磷酸核糖基转移酶(hprt)mrna管家基因。然后将5μl mrna提取物(总共25ng)与10μl quantitect probe rt-pcr试剂盒混合,在96孔半裙边qrt-pcr板中与1μl 20x hamp fam探针混合物、1μl 20x hprt vic探针混合物、0.5μl 40x taqman rt酶混合物、2.5μl无rna的h2o以20μl终体积混合。qrt-pcr反应的设置包括48℃下15分钟逆转录步骤,随后是95℃下10分钟激活步骤,然后是95℃下15秒和60℃下1分钟的40个循环。然后通过从hprt减去hamp的ct值来计算-δct值。
[0519]
实施例11.对正常小鼠中4种igg/λ抗mtp2抗体关于在24h时降低血清铁和转铁蛋白饱和度的单剂量评估
[0520]
nori-009、nori-010、nori-012和nori-034作为完全人igg4λmab包括在健康小鼠
中的首次评估中。9周龄c57bl/6雄性小鼠接受一次10mg/kg(150μl/小鼠)的腹膜内注射抗体,每组5只小鼠。注射后24h处死小鼠。作为铁调素诱导的阳性对照,给三只9周龄c57bl/6雄性小鼠注射lps(1μg/g体重),并于4小时后处死。lps(来自大肠杆菌的脂多糖)模拟细菌感染,因此小鼠通过诱导铁调素表达来应答以降低血清铁。lps引起急性炎症反应,并充当已知基于炎症反应引起最大铁调素增加的药剂的阳性对照。对肝组织进行hamp、id1、atho8、smad7、crp和saa3 mrna的实时pcr。还测定了血液学参数。测定红细胞数,并测量血红蛋白。测定所有小鼠的血清铁并计算转铁蛋白饱和度。
[0521]
未见nori-034将铁调素表达增加至高于同种型对照治疗的小鼠中所见的水平。另一方面,nori-009、nori-010和nori-012在给药后24小时均将铁调素表达增加至用同种型对照治疗的组的平均值之上至少1ct值,并且等于在给药后4小时由lps阳性对照诱导的值。结果是,用这些抗体治疗的小鼠中的血清铁含量降低至低于40μg/dl的平均浓度。图9。
[0522]
该实验证实了mtp-2在bmp/smad/铁调素途径中的生物学相关性,并且首次显示了通过抗体定向抑制,正常小鼠中血清铁可以降低。由于nori-034在体内是无活性的,所以没有进一步研究该抗体。
[0523]
实施例12.在正常小鼠中单次腹膜内注射后nori-010的时程评估
[0524]
抗体nori-010是在实施例11中显示出优选特征的抗体之一,因此感兴趣的是确定随时间观察到的效果。c57bl/6雄性小鼠接受一次10mg/kg(150μl/小鼠)的腹膜内注射抗体,每组5只小鼠。各组为在24h、72h、1周和2周终止的5只小鼠。分析与实施例11相同,但还包括血细胞比容(hct)、红细胞平均血红蛋白量(mch)和红细胞分布宽度(rdw)、与红细胞体积有关的细胞直径的量度。
[0525]
施用10mg/kg抗体后,铁调素升高维持2周,在此期间血清铁和tsat降低。mcv值由于一致的铁限制而降低。图10。
[0526]
施用3mg/kg抗体后,由于剂量较低,对铁调素升高的作用在2周时丧失。尽管如此,但血清铁和tsat在2周内保持降低,并且mcv也与10mg/kg剂量的情况下一样降低。图11。
[0527]
实施例13.对两种igg/κ抗mtp2抗体和两种igg/λ抗mtp2抗体关于在24h时降低血清铁和转铁蛋白饱和度的评估
[0528]
评估小鼠igg1(moigg1)形式的nori-008的体内活性。包括nori-010huigg4pe作为体内抗mtp-2活性的阳性对照抗体。包括分别以moigg1和huigg4pe形式的nori-036和nori-037作为阴性对照抗体。后一种对照抗体是与mtp-2的交叉反应性结合物,但在体外不抑制人或小鼠ecd蛋白的酶活性。
[0529]
9周龄c57bl/6雄性小鼠接受一次10mg/kg(150μl/小鼠)的腹膜内注射抗体,每组3-5只小鼠。注射后24h处死小鼠。对肝组织进行hamp、id1、atho8、smad7、crp和saa3 mrna的实时pcr。还测定了血液学参数。测定红细胞数,并测量血红蛋白。测定所有小鼠的血清铁并计算转铁蛋白饱和度。
[0530]
在此,我们发现对人和小鼠mtp-2具有非常强的亲和力的nori-008在体内也是有活性的。与nori-010相比,发现其在24小时时间点在提高铁调素rna表达和降低血清铁含量方面具有相同的活性。图12。
[0531]
这证明两种抗体在体内最大程度地抑制mtp-2活性。nori-036和nori-037是与mtp-2的结合物,但在体内对铁调素表达或血清铁没有影响。这证明体外筛选策略成功地产
生了可成功地在体内阻断mtp-2以诱导生物应答的抗体。
[0532]
实施例14.在正常小鼠中以10、3和1mg/kg单次腹膜内注射后nori-008的时程评估
[0533]
该实验通过血清铁浓度的变化示出腹膜内注射抗mtp-2抗体nori-008后的剂量时间关系。
[0534]
向雄性c57bl6j小鼠(22-28g,n=5/组)以单次2、20或200μg腹膜内注射给予完全人igg4抗mtp-2抗体nori-008。一组接受200μg剂量的人igg4同种型对照抗体并在第1天挑选。另外9组由每剂量nori-008(2、20或200μg)3组组成,对每组在单独剂量下挑选。对用各剂量治疗的一组动物在第1、7和14天取血,并确定血清铁浓度以评估nori-008的功效。
[0535]
然后在第7天对来自每个剂量和时间点的样品分析肝脏中的铁调素表达和血清中的抗体水平(pk分析)。在任何时间点,在2μg组中没有测量到抗体,并且在20μg剂量后24小时,5只动物中仅有三只具有可测量的水平。
[0536]
在200μg剂量下,nori-008作用在体内持续至少1周,然后铁调素表达和血清铁在2周时间点恢复正常。在20μg剂量下,作用持续至少1天,然后在1周时间点恢复正常。使用2μg剂量时,未观察到作用。作用的持续时间与抗体浓度的pk值相关。也就是说,当抗体低于临界浓度时,对mtp-2抑制的作用丧失,并且铁调素表达和血清铁恢复正常。图13。
[0537]
实施例15.对六种igg4/κ抗mtp2抗体关于在正常小鼠中在1周时间点降低血清铁和转铁蛋白饱和度的体内评估
[0538]
该研究评价了六种完全人igg4抗mtp-2抗体在腹膜内注射后降低血清铁浓度的能力。
[0539]
向雄性c57bl6j小鼠(25-32g,n=3-5/组)以单次10mg/kg腹膜内注射给予完全人igg4抗mtp-2抗体。研究中包括八组,每只动物接受单次10mg/kg腹膜内剂量的七种完全人igg4 pe抗mtp2抗体nori-005、nori-004、nori-002、nori-001、nori-007、nori-006和nori-010中的一种或人igg4同种型对照抗体。添加nori-010作为阳性对照和基准抗mtp-2抗体以与本实验中使用的其他抗体比较。除nori-005(n=3)和nori-002(n=4)外,所有组均含有5只动物。在第7天对动物取血并确定血清铁浓度以评估抗mtp-2抗体的铁参数、hamp mrna和igg水平。
[0540]
所有测试的抗体显示铁调素mrna表达增加,因此血清铁水平相应降低。然后在第7天对来自所有测试组的样品分析血清中的抗体水平(pk分析),并在该时间点和剂量下示出不同水平的抗体暴露。图14。
[0541]
实施例16.对huigg4和moigg1主链中的两种igg/κ和一种igg/λ抗mtp2抗体关于在1周时间点降低血清铁的体内评估(10mg/kg腹膜内剂量)
[0542]
本研究评价了三种完全人igg4或小鼠igg1形式的抗mtp-2抗体在皮下注射后降低血清铁浓度的能力。
[0543]
向雄性c57bl6j小鼠(25-32g,n=5/组)以单次10mg/kg皮下注射给予完全人igg4或moigg1抗mtp-2抗体。研究中包括七组,使用三种抗mtp2抗体nori-011、nori-003和nori-006中的一种作为人igg4或鼠igg1,或使用人igg4同种型对照抗体。在第7天对动物取血并确定血清铁浓度以评估抗mtp-2抗体的功效。
[0544]
图15。
[0545]
实施例17.在正常小鼠中单次腹膜内(ip)或皮下(sc)注射nori-010后的体内评
估,在注射后7天读出
[0546]
该实验用于评价完全人igg4抗mtp-2抗体nori-010在皮下注射10mg/kg后是否产生与10mg/kg腹膜内剂量情况下所见相似的血清铁浓度降低。
[0547]
向雄性c57bl6j小鼠(23-29g,n=4-5/组)以单次10mg/kg皮下或腹膜内注射给予完全人igg4抗mtp-2抗体。两组接受单次10mg/kg腹膜内剂量或单次10mg/kg皮下剂量的nori-010(每组n=5)。另外两组腹膜内或皮下接受10mg/kg剂量的人igg4同种型对照抗体。
[0548]
在第7天对动物取血,并确定血清铁浓度和igg水平。图16。
[0549]
该实验的结果显示,对于腹膜内和皮下给药方法,在1周时间点血清中抗体的浓度是相似的。结果是,两种给药方法的血清铁降低也是相似的,并且如前所见,通过mtp-2抑制而降低。
[0550]
实施例18.在正常大鼠中单次腹膜内注射抗mtp-2抗体nori-008和nori-010后的剂量/时间反应的体内评估
[0551]
该实验用于评价腹膜内注射后两种完全人igg4抗mtp-2抗体的剂量-时间关系。
[0552]
向雄性wistar大鼠(260-320g,n=3/组)以单次3或10mg/kg腹膜内注射给予完全人igg4抗mtp-2抗体nori-008和nori-010。通过以10mg/kg腹膜内注射给药higg4同种型对照抗体(标记为“同种型”),作为阴性对照。
[0553]
在第1、3、7、9、14和21天对动物取血。在每个时间点测量血清铁和血清抗体浓度。
[0554]
10mg/kg的nori-010产生药理作用,并使得血清铁降低长达9天,之后恢复正常,而3mg/kg的作用仅持续24小时。10mg/kg的nori-008产生作用,并使得血清铁降低长达9天,之后恢复正常,而3mg/kg的作用仅持续72小时。这些抗体的pd与igg血清水平密切相关,并且当抗体浓度降低时,铁降低作用丧失。图17。
[0555]
实施例19.在正常大鼠中单次皮下注射抗mtp-2抗体nori-003、nori-006、nori-008和nori-010后的剂量/时间反应的体内评估
[0556]
在正常大鼠中单次皮下注射抗mtp-2抗体后进行剂量/时间反应的体内评估。
[0557]
向雄性wistar大鼠(260-320g,n=5/组)以单次10mg/kg皮下注射给予完全人igg4抗mtp-2抗体nori-003、nori-006、nori-008和nori-010。以10mg/kg给药huigg4同种型对照抗体(标记为“同种型”),作为阴性对照。
[0558]
在第1、3、7、9、14和21天对动物取血。在每个时间点测量血清铁和血清抗体浓度。
[0559]
nori-008和nori-010再次显示出类似于实施例18的作用持续时间,降低血清铁的作用持续到第9天,之后恢复正常。nori-003和nori-006都显示出更有利的作用持续时间,血清铁在整个21天的研究中保持受抑制。
[0560]
本研究的pk分析表明四种抗体的cmax的关键差异,其中与nori-008和nori-010相比,nori-003和nori-006在第3天具有高得多的血清抗体浓度。结果是,这两种抗体显示出更有利的pk曲线,并保持高于临界血清抗体浓度,以便以更长时间维持对mtp-2的抑制。因此,维持了抑制血清铁的作用。图18。
[0561]
实施例20.单次腹膜内注射nori-010后在β地中海贫血的小鼠模型中的体内评估
[0562]
在杂合缺失b1和b2珠蛋白基因的中间型β地中海贫血的杂合鼠模型(hbbth3/+)中评估所选择的抗体nori-010。hbbth3/+小鼠展现出与人的中间型β-地中海贫血相似的特征,包括hb水平在7与9g/dl之间、异常的红细胞形态、增加的网织红细胞计数、无效和髓外
红细胞生成、肝脾肿大以及肝脾铁过载(其为随着年龄增长而恶化的复杂表型)。在实施例18-20中观察到nori-010的活性后,以10mg/kg腹膜内注射该抗体,并在该单剂量后2周终止动物(每个时间点n=3)。此外,24h后分析一组动物的铁调素mrna。使用相同剂量的人igg4同种型对照抗体作为阴性对照。
[0563]
记录以下参数的结果:
[0564]-肝脏中的铁调素mrna水平(24h和2周,根据方法实施例10)
[0565]-肝脏中的id1 mrna水平(24h和2周,根据方法实施例10)
[0566]-血清铁浓度(2周,根据方法实施例10)
[0567]-计算的转铁蛋白饱和度(2周,根据方法实施例10)
[0568]-平均红细胞体积(2周)
[0569]
结果显示,在给药nori-010后,在24h时,铁调素水平已经高于同种型对照。这种差异保持两周的时间段。一致地,与同种型对照相比,血清铁水平降低约52%,并且计算的转铁蛋白饱和度在两周时间点比用同种型对照治疗的动物降低47%。图19。
[0570]
实施例21.在有和没有促红细胞生成素共同治疗的β地中海贫血的小鼠模型中用nori-011-m治疗的8周重复剂量评估
[0571]
本研究的目的是观察在比实施例20更长的治疗时间段后对血液学参数的影响。为此,向hbbth3/+小鼠(n=5/组)每周一次腹膜内注射10mg/kg nori-011-m抗体,持续8周。对于该长期重复剂量实验,将nori-011的同种型用鼠恒定区(鼠igg1和鼠λ恒定区)重新格式化,以避免或降低抗mtp2抗体在小鼠中的免疫原性和产生。关于这种重新格式化,还对nori-011vh结构域c末端序列进行了轻微修饰,并将修饰的抗体重新命名为nori-011-m。nori-011-m的序列示于表s中。这里使用的对照是小鼠同种型igg1。
[0572]
此外,该研究试图检查共同施用促红细胞生成素(epo)的影响,已知促红细胞生成素改善一些关键参数,但由于过度细胞死亡而对铁负载和脾大小具有不利影响。这种组合的积极作用已在实验中通过以下方面观察到,其中通过过表达重组成纤维细胞提供epo,以及在hbbth3/+小鼠中通过使用tmprss6反义寡核苷酸治疗降低蛋白裂解酶-2活性(论文#164第60届美国血液学会年会2018)。在该研究中,将临床级epo(达贝泊汀α)与nori-011-m以30μg/kg每周一次在研究的一个组中共同施用。作为对照,还将epo与同种型对照抗体共同施用,这代表单独epo对研究读数的影响。图20示出了肝脏样品中单独血液学参数和铁调素mrna水平的结果。
[0573]
结果显示,在8周的实验历程中,铁调素水平可以始终保持在升高的水平(a)。因此,可以预期,如上述实施例中所见,这将导致铁限制和随后血清铁、肝脏铁含量的降低(b)和mcv的降低(f)。单独使用nori-011-m时,红细胞计数和血红蛋白基本不升高。然而,脾脏中红细胞的成熟得到改善,与任何其他组相比,v期(成熟)的细胞比例大得多(i)。单独给药nori-011-m也使脾脏重量的增加减少约一半,这表明由nori-011-m的阻断引起的铁供应限制对红细胞的成熟具有正常化作用(k)。
[0574]
使用epo(与同种型对照结合)对红细胞计数(c)和血红蛋白(d)具有积极影响,如对红细胞生成的刺激物所预期的。然而,如先前已知的,在β珠蛋白合成缺陷(k)和成熟为功能性和高质量红细胞没有改善(i)的情况下,这种增加的红细胞生成导致细胞死亡增加和相关的脾脏大小(指数)增加。如所预期的,epo不能增加铁调素水平,因此对肝脏铁水平没
有影响(c)。
[0575]
nori-011-m和epo的组合治疗导致积极作用的组合。这表现为与单独的epo相比对红细胞计数(c)和血红蛋白(d)的影响略微降低,但总体上治疗效果更平衡,包括与单独的epo相比肝脏铁过载的持续减少(b)和脾肿大的减少(k)。通过优化蛋白裂解酶抑制和epo刺激的治疗比率,认为这些合作作用可以在临床环境中优化。
[0576]
实施例22.在有和没有actriib-fc融合蛋白共同治疗的β地中海贫血的小鼠模型中用nori-011-m治疗的8周重复剂量评估
[0577]
在该研究中,我们证明与单独用nori-11-m和单独用actriib-fc治疗相比,用nori-11-m和激活素受体iib fc融合蛋白共同治疗可提供有益的治疗效果。这种协同作用可以反映这两种药剂的不同作用模式,其中在红细胞生成过程中,actriib-fc促进红细胞前体的成熟,而nori-11-m导致铁限制和正常化,因此减缓红细胞生成,从而导致更有效地产生更成熟的红细胞。
[0578]
本研究中的工作是使用总体上如以上实施例21中所述的方法和程序经8周多次施用两种药剂进行的。如前,每周一次向hbbth3/+小鼠(n=5/组)腹膜内注射10mg/kg nori-011-m抗体,持续8周。以10mg/kg每周两次腹膜内注射actriib-fc,持续8周。与抗体相比,actriib-fc的施用频率为两倍,这反映了先前公布的相似的激活素受体配体陷阱分子的施用方案(关于actriia-fc,suragani rn,cawley sm,li r,等人modified activin receptor iib ligand trap mitigates ineffective erythropoiesis and disease complications in murineβ-thalassemia.blood.2014;123(25):3864-3872.doi:10.1182/blood-2013-06-511238以及dussiot等人2014)。
[0579]
本实施例中使用的actriib-fc构建体是具有l79d修饰的经修饰人actriib胞外结构域(uniprot-q13705,残基26-131),通过短3x甘氨酸接头与小鼠igg2a-fc结构域(uniprot-p01863,残基99-330)融合,在悬浮cho细胞中表达并通过fc结构域纯化。
[0580]
将治疗组与健康未治疗的野生型小鼠(“wt”)和用小鼠igg1对照(“moigg1”)治疗的hbbth3/+小鼠进行比较。
[0581]
图21示出了肝脏样品中单独血液学参数和铁调素mrna水平的结果。与上述实施例21一致,结果再次表明,使用nori-11-m可使铁调素水平在8周的历程中始终保持在升高的水平(图21a),这证明nori-11-m具有增加铁调素表达水平的作用,从而导致肝脏铁水平降低(图21b)、血清铁降低和平均红细胞体积(mcv)降低(图21f)。对于单独使用actriib-fc的治疗,没有观察到铁调素(hamp)mrna的增加,并且共同治疗与单独使用nori-11-m的结局相同。因此,尽管给药频率较高,但actriib-fc不能直接升高铁调素表达或相应地降低肝脏铁水平。
[0582]
在用nori-11-m治疗的小鼠中红细胞平均血红蛋白量(mch)降低(这反映了铁供应的限制),并且还被actriib-fc降低(图21h),这反映了产生更多数量的细胞(通过总红细胞计数和血红蛋白的增加显示),并因此使得每个细胞可利用更少的血红蛋白。平均红细胞体积(mcv)也降低(图21f)。通常,低mcv表示小红细胞性贫血,但在这种情况下,铁限制(由抗体引起)或血红蛋白缺乏(对于actriib-fc,由更多rbc的成熟增强引起)导致每个细胞的可用性降低,如mch结果已指示。
[0583]
所有治疗组都提高了产生的红细胞的“质量”,如红细胞分布宽度(rdw)的降低(正
常化)所反映的(图21g)。因此改善了红细胞的均匀性。单独使用nori-011-m,红细胞计数略微升高(图21c),但血红蛋白(图21d)和血细胞比容(图21e)均未升高。actriib-fc对所有这些参数具有较大的影响。与单独使用actriib-fc治疗相比,所述组合没有导致进一步增加,这表明对红细胞生成的成熟作用受到actriib-fc而不是nori-11-m驱动。然而,值得注意的是,nori-11-m没有抵消actriib-fc的作用。通过单独用actriib-fc或与nori-11-m组合治疗,红细胞计数恢复到野生型水平,并且血细胞比容和血红蛋白水平均显著升高。这是重要的,因为它表明由nori-11-m引起的铁减少没有逆转由actriib-fc产生的对红细胞生成的有益作用。因此,总体而言,当两种治疗组合使用时,仍然可以实现这两种治疗的优点,以降低铁过载并增加红细胞的产生/成熟。
[0584]
此外,两种药剂一起使用时,实际上导致更大的总体益处,其治疗潜力超过单独使用它们的情况,如例如通过减少脾肿大的作用所见。
[0585]
脾脏中红细胞的成熟得到改善,与任何其他组相比,v期(成熟)的细胞比例大得多(图21i)。与未治疗的对照相比,用两种治疗降低了脾重量的增加,这表明即使由nori-011-m引起的铁供应的限制也对红细胞成熟效率具有正常化作用(图21k)。
[0586]
我们在实施例21中报道了使用epo对红细胞计数(图20c)和总血红蛋白(图20d)具有积极影响,正如对红细胞生成的刺激物所预期的。然而,如医学领域中已知的,在β珠蛋白合成持续缺陷的情况下,这种对红细胞生成的刺激增加也引起细胞死亡和细胞凋亡的增加以及相关的脾脏大小和重量的进一步增加(所谓的脾肿大)(图20k)。在此,在本实施例中,与未治疗的动物相比,使用nori-11-m和actriib-fc都没有导致脾脏重量的增加(图21k)。确实,尽管没有达到健康动物的水平,但是实际上脾脏重量明显降低。通过甚至进一步降低脾脏重量,nori-011-m和actriib-fc的组合治疗显现甚至优于单独的单一疗法。
[0587]
[0588]
[0589]
[0590]
[0591]
[0592]
[0593]
[0594]
[0595]
[0596]
[0597]
[0598]
[0599]
[0600]
[0601]
[0602]
[0603]
[0604]
[0605]
[0606]
[0607]
[0608]
[0609]
[0610]
[0611]
[0612]
[0613]
[0614]
[0615]
[0616]
[0617]
[0618]
[0619]
[0620]
[0621]
[0622]
[0623]
[0624]
[0625]
[0626]
[0627]
[0628]
[0629]
[0630]
[0631]
[0632]
[0633]
[0634]
[0635]
[0636]
[0637]
[0638]
[0639]
[0640]
[0641]
[0642]
[0643]
[0644]
[0645]
[0646]
[0647]
[0648]
[0649]
[0650]
[0651]
[0652]
[0653]
[0654]
[0655]
[0656]
[0657]
[0658]
[0659]
[0660]
[0661]
[0662]
[0663]
[0664]
[0665]
[0666]
[0667]
[0668]
[0669]
[0670]
[0671]
[0672]
[0673]
[0674]
[0675]
[0676]
[0677]
[0678]
[0679]
[0680]
[0681]
[0682]
[0683]
[0684]
[0685]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1