牛源大肠杆菌检测引物探针组合、试剂盒及应用
本发明属于病原菌检测技术领域,具体涉及牛源大肠杆菌检测引物探针组合、试剂盒及应用。
背景技术:
致病性大肠杆菌可引起牛及其他动物的水样腹泻,严重情况甚至导致病畜死亡,造成巨大的经济损失;在致病性大肠杆菌侵染病畜的过程中,菌毛能够黏附牛小肠绒毛特异性受体上,释放肠道毒素,并且可保护致病性大肠杆菌免受肠道消化酶的影响。致病性大肠杆菌具有多种菌毛类型,其中,f5、f41较为流行,鉴定菌毛类型有助于更有针对性地对病畜感染的大肠杆菌进行防治。
目前,研究人员已根据f5、f41研究出利用pcr对大肠杆菌的鉴定方法,然而,针对不同的菌毛类型,需要分别进行pcr检测,并且检测灵敏度低、特异性差。
因此,如何提供一种针对于f5、f41检测灵敏度高、特异性强的牛源大肠杆菌检测产品是本领域亟待解决的问题。
技术实现要素:
本发明公开了牛源大肠杆菌检测引物探针组合、试剂盒及应用。
为了实现上述目的,本发明采用如下技术方案:
牛源大肠杆菌检测引物探针组合,
包括用于检测菌毛抗原f5基因的引物探针和用于检测菌毛抗原f41基因的引物探针;
用于检测菌毛抗原f5基因的引物探针包括:
上游引物forwardf5:5’-ggtcaatggtaatcgtacatcaac-3’,seqidno:1;
下游引物reversef5:5’-actgttcatagaaccagaccag-3’,seqidno:2;
探针probef5:5’cy5-cttgggcaggctgctattagtggtcatg-3’bhq3,seqidno:3;
用于检测菌毛抗原f41基因的引物探针包括:
上游引物forwardf41:5’-tactgagctagggactctt-3’,seqidno:4;
下游引物reversef41:5’-ctggattaacaagcccttca-3’,seqidno:5;
探针probef41:5’rox-tcatttggtgcggcagttgcaactatt-3’bhq2,seqidno:6。
上述牛源大肠杆菌检测引物探针组合在制备检测牛源大肠杆菌的产品中的应用。
牛源大肠杆菌检测试剂盒,包括上述牛源大肠杆菌检测引物探针组合。
上述牛源大肠杆菌检测试剂盒使用时的检测体系为25μl:
premixextaq12.5μl,
10μmforwardf50.2μl,
10μmreversef50.2μl,
10μmprobef50.6μl,
10μmforwardf411μl,
10μmreversef411μl,
10μmprobef410.2μl,
dna模板2μl,
加灭菌水至25μl。
上述牛源大肠杆菌检测试剂盒使用时的检测程序为:
预变性95℃30s;
变性95℃5s,退火延伸56℃30s,44个循环。
上述牛源大肠杆菌检测引物探针组合或上述牛源大肠杆菌检测试剂盒在检测菌毛抗原f5基因或检测菌毛抗原f41基因中的应用。
综上所述,本发明可同时实现大肠杆菌菌毛抗原f5基因和检测菌毛抗原f41基因的检测,检测灵敏度高、特异性强、重复性好,适于推广应用。
附图说明
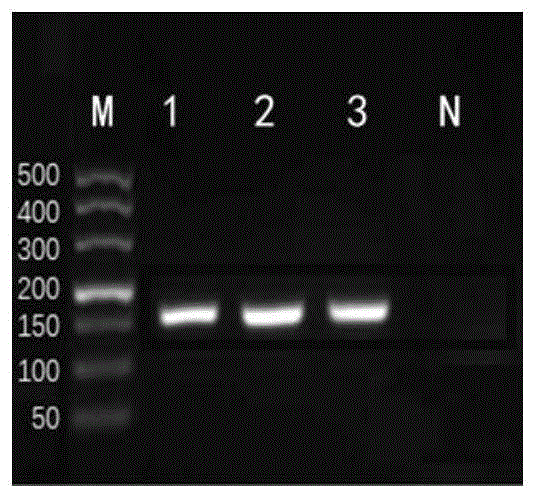
图1所示为菌毛抗原f5基因pcr扩增结果;
其中,m:marker;1-3:f5核酸dna;n:阴性;
图2所示为菌毛抗原f41基因pcr扩增结果;
其中,m:marker;1-3:f41核酸dna;n:阴性;
图3所示为菌毛抗原f5基因克隆菌菌液pcr扩增结果;
其中,m:marker;1-5:f5基因克隆菌菌液;n:阴性;
图4所示为菌毛抗原f41基因克隆菌菌液pcr扩增结果;
其中,m:marker;1-10:f41基因克隆菌菌液;n:阴性;
图5所示为菌毛抗原f5重组质粒pcr扩增结果;
其中,m:marker;1-4:f5重组质粒;n:阴性;
图6所示为菌毛抗原f41重组质粒pcr扩增结果;
其中,m:marker;1-4:f41重组质粒;n:阴性;
图7所示为菌毛抗原f5重组质粒测序结果;
图8所示为菌毛抗原f41重组质粒测序结果;
图9所示为菌毛抗原f5引物探针筛选结果;
图10所示为菌毛抗原f41引物探针筛选结果;
图11所示为菌毛抗原f5引物优化结果;加粗曲线为最优;
图12所示为菌毛抗原f41引物优化结果;加粗曲线为最优;
图13所示为菌毛抗原f5探针优化结果;加粗曲线为最优;
图14所示为菌毛抗原f41探针优化结果;加粗曲线为最优;
图15所示为菌毛抗原f5荧光定量pcr扩增曲线;
1-8:1×108copies/μl~1×101copies/μl;9:阴性;
图16所示为菌毛抗原f5荧光定量pcr标准曲线;
图17所示为菌毛抗原f41荧光定量pcr扩增曲线;
1-7:1×108copies/μl~1×102copies/μl;8:阴性;
图18所示为菌毛抗原f41荧光定量pcr标准曲线;
图19所示为菌毛抗原f5荧光定量pcr敏感性实验结果;
1-9:1×109~1×101copies/μl;10:阴性;
图20所示为菌毛抗原f5常规pcr敏感性实验结果;
1-10:1×109~1×100copies/μl;m:marker;n:阴性;
图21所示为菌毛抗原f41荧光定量pcr敏感性实验结果;
1-9:1×109~1×101copies/μl;10:阴性;
图22所示为菌毛抗原f41常规pcr敏感性实验结果;
1-11:1×1010~1×100copies/μl;m:marker;n:阴性;
图23所示为菌毛抗原f5荧光定量pcr特异性实验结果;
1、2:cvcc209株、阳性质粒;3:阴性对照、cvcc1345株、cvcc216株、cvcc1527株、cvcc2184株、atcc、mh、pma、cpa、cpb、cpd、ibrv、bpiv;
图24所示为菌毛抗原f41荧光定量pcr特异性实验结果;
1:cvcc209株;2:阳性质粒;3:阴性对照、cvcc216株、cvcc1527株、cvcc1345株、cvcc2184株、atcc、mh、pma、cpa、cpb、cpd、ibrv、bpiv;
图25所示为菌毛抗原f5荧光定量pcr重复性实验结果;
1-3:1×106~1×104copies/μl;4:阴性;
图26所示为菌毛抗原f41荧光定量pcr重复性实验结果;
1-3:1×106~1×104copies/μl;4:阴性;
图27所示为菌毛抗原f5双重荧光定量pcr引物浓度优化结果;加粗曲线为最优;
图28所示为菌毛抗原f41双重荧光定量pcr探针浓度优化结果;加粗曲线为最优;
图29所示为双重荧光定量pcr扩增曲线;
1-6:1×107copies/μl~1×102copies/μl;7:阴性;
图30所示为双重荧光定量pcr标准曲线;
图31所示为双重荧光定量pcr敏感性结果;
1-8:1×108~1×101copies/μl;9:阴性;
图32所示为双重荧光定量pcr特异性结果;
1、3:cvcc209;2、4:阳性质粒;5:阴性、mh、pma、pmb、cpa、cpb、cpd、ibrv、bpiv、cvcc216株、cvcc1345株、cvcc1527株、cvcc2184、atcc;
图33所示为双重荧光定量pcr重复性检测结果;
1-3:1×106~104copies/μl;4:阴性;
图34所示为双重荧光定量pcr检测临床样品结果;
1:阳性质粒2:临床样品3:阴性;
图35所示为双重荧光定量pcr检测临床样品结果;
1:阳性质粒2:临床样品3:阴性。
具体实施方式
下面对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1引物和探针的设计与合成
根据genbank上公布的大肠杆菌f5基因序列(登录号m35282.1)、f41基因序列(登录号mf955845.1),设计探针和引物(表1),并由华大基因合成。
表1荧光定量pcr引物与探针
实施例2大肠杆菌菌毛抗原f5、f41单重荧光定量pcr检测
1.细菌dna的提取
用接种环沾取冻干的大肠杆菌参考菌株(表达抗原f5、f41)放于5ml营养肉汤中37℃过夜培养,参考试剂盒说明书,对上述过夜培养的菌液进行dna提取。
2.常规pcr检测
(1)常规pcr反应体系的参数
取步骤1提取的dna作为模板,用实施例1中设计好的引物分别进行扩增。
常规pcr扩增反应体系(25μl)为:premixtaqtm12.5μl、引物(10μmol/l)各1.0μl、模板dna2.0μl、ddh2o8.5μl。
常规pcr扩增反应参数为:94℃3min;94℃20s,58℃20s,72℃20s,30个循环;72℃7min。
(2)琼脂糖凝胶电泳
将琼脂糖和10×tae电泳缓冲液按比例配制成凝胶,将dl500marker和pcr扩增产物分别加入点样孔中进行凝胶电泳,电泳条件为110v60min。电泳结束后观察结果,f5第2组、f41第2组引物电泳结果如图1和图2,电泳条带与目的基因片段大小一致。
3.标准品的构建
(1)胶回收
采用胶回收试剂盒将凝胶电泳后的琼脂糖进行回收:
电泳结束后,在紫外灯下切下含目的片段的凝胶,称取凝胶重量。加入等倍体积buffergdp,55℃水浴8min。准备置备管,把溶胶液转移至吸附柱中,12,000×g离心30s,弃滤液。加入300μlbuffergdp至吸附柱中。静置1min。12,000×g离心30s,弃滤液。加入700μlbuffergw至吸附柱中,12,000×g离心30s,重复一次,12,000×g离心2min。将吸附柱放置在干净的离心管中,加入30μlddh2o,12,000×g离心30~60s,获得回收的大肠杆菌菌毛抗原f5、f41基因回收产物。
(2)目的基因与载体pmd-19t的连接
取大肠杆菌菌毛抗原f5、f41基因回收产物,分别与大小为2692bp的pmdtm19-tvector进行连接。体系(10μl)为pmd19-tvector1μl、胶回收产物4.0μl、solutioni5.0μl;16℃孵育30min,得到连接产物。
(3)克隆质粒的转化
取-80℃环境保存的takaradh5α感受态细胞,随后将连接产物加到100μl感受态细胞中,放入冰中30min后立即转移至入42℃水浴锅中进行45s的热激转化,再次冰内孵化1min。加入890μllb液体培养基,总量1000μl,37℃摇床中培养1h。取出混合液离心3min,吸出700μl上清液弃去,用剩下的300μl上清液反复吹打重悬沉淀,取适量涂布于含amp的lb固体培养基上,随后放入37℃恒温培养箱中静置培养10~12h左右(等到长出适宜大小的单个菌落)。
(4)阳性克隆菌的筛选
从培养的平皿中挑取3~5个单个菌落,转入于lb液体培养基中,37℃、200×g的恒温摇床中培养12~16h。
(5)重组阳性质粒的提取
将培养后的菌液作为模板,进行常规pcr扩增,选取与目的基因片段相同所对应的菌液,参照试剂盒进行质粒提取,步骤如下:
离心管中加入5ml过夜培养的菌液,10,000×g离心1min,留沉淀。加入250μlbufferp1,振荡混匀。加入250μlbufferp2,温和的上下颠倒混匀,使菌体裂解后继续加入350μlbufferp3,13000×g离心10min。准备置备管,取上清13,000×g离心30s,弃滤液。加入600μlbufferpw2至吸附柱中,13,000×g离心30s,弃滤液,重复一次。13,000×g离心1min干燥吸附柱。准备干净的离心管,加入30μlelutionbuffer,室温静置2min,13,000×g离心1min洗脱dna。
(6)重组质粒的鉴定
1)菌液pcr鉴定:
为了验证目的基因是否连接在载体上,以步骤(5)菌液为模板,分别用f5第2组、f41第2组引物进行pcr扩增,观察结果,同时设立阴性对照。
反应体系:12.5μlpremixtaqtm、8.5μl无菌水、上下游引物各1.0μl。
反应程序:95℃3min;95℃20s,58℃20s,72℃20s,30个循环;72℃7min。
结果如图3、4,表明目的基因已克隆到pmd19-t载体。
2)质粒pcr鉴定:
为了鉴定提取的质粒是否与目的基因大小一致,将步骤(5)提出的质粒作为模板,分别用f5第2组、f41第2组引物进行pcr扩增,观察结果,同时设立阴性对照。反应体系、反应程序同上,结果如图5、6所示。
3)测序鉴定:对pcr扩增后与目的片段大小相符的阳性质粒进行测序验证,如图7、8所示,测序结果与genbank上与公布的基因序列进行比对分析,确认与模板基因同源性均为100%。重组质粒置-20℃保存备用。
(7)重组质粒dna拷贝数的计算及稀释
提取质粒后各取1μl,测得f5、f41标准阳性质粒的浓度分别为180.8ng/μl和175.1ng/μl,稀释浓度至100ng/μl,计算质粒拷贝数为3.2×1010copies/μl和3.22×1010copies/μl。制备阳性标准品时使用灭菌水对重组质粒f5、f41进行10倍倍比稀释,得到模板浓度1.0×1010copies/μl~1.0×100copies/μl。
4.大肠杆菌菌毛抗原f5、f41单重荧光定量pcr检测
(1)引物探针组合筛选
利用实施例1引物探针组进行单重荧光定量pcr检测:
单重荧光定量pcr反应程序为预变性95℃30s;变性95℃5s、退火延伸56℃30s,44个循环。
单重荧光定量pcr初始反应体系(25μl)为premixextaq(probeqpcr)12.5μl、pcrforwardprimer(10μm)0.5μl、pcrreverseprimer(10μm)0.5μl、probe0.7μl、dna模板2.0μl、灭菌水8.8μl。
结果如图9、10所示,f5第2组、f41第2组效果最佳,选择f5第2组、f41第2组进行后续实验。
(2)反应参数的优化
为了探索不同反应条件对f5、f41单重荧光定量pcr扩增的影响,需对pcr条件进行摸索优化,来获取最佳的反应条件,并为双重荧光定量pcr各条件的优化提供适当的优化范围。
1)引物浓度优化
阳性质粒dna作为模板,分别吸取0.4μl~1μl,终浓度分别为160nmol/l、200nmol/l、240nmol/l、280nmol/l、320nmol/l、360nmol/l、400nmol/l7个梯度的上下游引物(f5第2组、f41第2组),探针(f5第2组、f41第2组)添加量暂固定为0.7μl。选择荧光值高,ct值最小的为最佳浓度,如果两个条件无法同时满足,则优先考虑ct值。
如图11、12所示,菌毛抗原f5引物浓度0.8μl(320nmol/l)ct值最小,扩增曲线良好;菌毛抗原f41引物浓度0.4μl(160nmol/l)ct值最小,扩增曲线良好;因此本试验菌毛抗原f5的最佳引物浓度选0.8μl(320nmol/l);菌毛抗原f41的最佳引物浓度选0.4μl(160nmol/l)。
2)探针浓度优化
阳性质粒dna作为模板,分别吸取0.4μl~1μl,终浓度分别为160nmol/l、200nmol/l、240nmol/l、280nmol/l、320nmol/l、360nmol/l、400nmol/l7个梯度的探针(f5第2组、f41第2组),引物(f5第2组、f41第2组)添加量参考步骤1)优化结果。
如图13、14所示,菌毛抗原f5探针浓度0.8μl(320nmol/l)ct值最小,扩增曲线良好;菌毛抗原f41探针浓度0.5μl(200nmol/l)ct值最小,扩增曲线良好;因此本试验菌毛抗原f5的最佳探针浓度选0.8μl(320nmol/l);菌毛抗原f41的最佳探针浓度选0.5μl(200nmol/l)。
(3)菌毛抗原f5、f41单重荧光定量pcr标准曲线的建立
模板选用1×101copies/μl~1×108copies/μl共8个浓度的阳性质粒,每个模板作3个重复,设立阴性对照。引物和探针量按照优化结果进行反应,根据软件分析得到相关系数和扩增效率后绘制菌毛抗原f5、f41单重定量pcr标准曲线方程。结果如图15-18所示。
(4)菌毛抗原f5、f41单重荧光定量pcr的敏感性试验
模板为1×100copies/μl~1×109copies/μl共10个标准阳性质粒,作3个重复,设立阴性对照。同时按照步骤2中常规pcr和优化后的荧光定量pcr方法检测,得出常规pcr和定量pcr检测方法的最低检出浓度。
结果如图19-22所示,菌毛抗原f5荧光定量pcr最低能检出浓度为1×101copies/μl的质粒,而常规pcr最低能检出浓度为1×103copies/μl的质粒,两者相差100倍。菌毛抗原f41荧光定量pcr最低能检出浓度为1×101copies/μl的质粒,而常规pcr最低能检出浓度为1×103copies/μl的质粒,两者相差100倍。
(5)菌毛抗原f5、f41单重荧光定量pcr的特异性试验
反应体系、程序不变,分别以牛曼氏杆菌(mh)、多杀性巴氏杆菌a型(pma)、多杀性巴氏杆菌b型(pmb)、牛羊产气荚膜梭菌a型(cpa)、牛羊产气荚膜梭菌b型(cpb)、牛羊产气荚膜梭菌d型(cpd)、牛传染性鼻气管炎病毒(ibrv)、牛副流感病毒(bpiv)、大肠杆菌参考菌株ccvc209、大肠杆菌参考菌株ccvc216、大肠杆菌参考菌株ccvc1345、大肠杆菌参考菌株ccvc1527、沙门氏菌参考菌株ccvc2184、大肠杆菌质控菌株atcc25922的核酸(均为市售菌提取dna)为模板,以1×107copies/μl菌毛抗原f5、f41标准阳性质粒分别作为阳性对照,并设立阴性对照,进行特异性验证,结果如图23、24所示。
(6)菌毛抗原f5、f41单重荧光定量pcr的重复性试验
模板1×104copies/μl~1×106copies/μl阳性质粒,作三次重复,设立阴性对照,对实验数据分析,验证荧光定量pcr方法的稳定性,结果如图25、26所示。
实施例3大肠杆菌菌毛抗原f5、f41双重荧光定量pcr检测
1.引物浓度优化
按照单重荧光定量pcr方法中已优化好的各项反应条件进行扩增(反应体系:25μl),按照表2进行引物浓度优化。
表2引物方阵优化表
结果如图27所示,当菌毛抗原f5引物浓度0.2μl、菌毛抗原f41引物浓度1μl时ct值最小,扩增曲线良好。因此确定菌毛抗原f5、f41的最佳引物浓度分别是0.2μl、1μl。
2.探针浓度优化
菌毛抗原f5、f41引物浓度分别是0.2μl、1μl,按照表3进行探针浓度优化。
表3探针方阵优化表
结果如图28所示,当菌毛抗原f5探针浓度0.6μl、菌毛抗原f41探针浓度0.2μl时ct值最小,扩增曲线良好。因此确定菌毛抗原f5、f41的最佳探针浓度分别是0.6μl、0.2μl。
3.菌毛抗原f5、f41双重荧光定量pcr标准曲线的建立
用于检测菌毛抗原f5基因的引物探针包括:
上游引物forwardf5:5’-ggtcaatggtaatcgtacatcaac-3’,seqidno:1;
下游引物reversef5:5’-actgttcatagaaccagaccag-3’,seqidno:2;
探针probef5:5’cy5-cttgggcaggctgctattagtggtcatg-3’bhq3,seqidno:3;
用于检测菌毛抗原f41基因的引物探针包括:
上游引物forwardf41:5’-tactgagctagggactctt-3’,seqidno:4;
下游引物reversef41:5’-ctggattaacaagcccttca-3’,seqidno:5;
探针probef41:5’rox-tcatttggtgcggcagttgcaactatt-3’bhq2,seqidno:6。
检测体系为25μl:
premixextaq12.5μl,
10μmforwardf50.2μl,
10μmreversef50.2μl,
10μmprobef50.6μl,
10μmforwardf411μl,
10μmreversef411μl,
10μmprobef410.2μl,
dna模板2μl,
加灭菌水至25μl。
检测程序为:
预变性95℃30s;
变性95℃5s,退火延伸56℃30s,44个循环。
模板选用1×102copies/μl~1×107copies/μl阳性质粒,每个模板作3个重复,设立阴性对照,结果如图29、30。
菌毛抗原f5的标准曲线回归方程为y=-3.320x+41.351,相关系数r2达0.999,扩增效率e=100.1%;菌毛抗原f41的标准曲线回归方程为y=-3.243x+43.402,相关系数r2达0.998,扩增效率e=103.4%。
4.菌毛抗原f5、f41双重荧光定量pcr的敏感性试验
扩增体系、程序同双重荧光定量pcr标准曲线建立,模板为1×101copies/μl~1×108copies/μl标准阳性质粒,结果如图31。菌毛抗原f5、f41双重荧光定量pcr最低检出浓度为1×101copies/μl。
5.菌毛抗原f5、f41双重荧光定量pcr的特异性试验
扩增体系、程序同双重荧光定量pcr标准曲线建立,模板同单重荧光定量pcr的特异性试验,结果如图32。只有菌毛抗原f5、f41的阳性质粒和cvcc209出现扩增曲线。
6.菌毛抗原f5、f41双重荧光定量pcr的重复性试验
扩增体系、程序同双重荧光定量pcr标准曲线建立,1×104copies/μl—1×106copies/μl阳性质粒作为模板,结果如图33、表4所示,菌毛抗原f5、菌毛抗原f41同一模板ct值基本一致,扩增曲线也大致相同;组内重复变异系数均低于1%,表明试验重复性高,稳定性良好。
表4重复性试验结果
7.荧光定量pcr方法的应用
用建立的大肠杆菌菌毛抗原f5、f41双重荧光定量pcr检测方法,对109份粪便样品和3份肠内容物中提出的dna样品进行检测。结果如图34、35、表5所示,109份粪便样品中检出菌毛抗原f5阳性43份,菌毛抗原f41阳性28份,双阳性26份;3份肠内容物中检出菌毛抗原f5阳性2份、菌毛抗原f41阳性1份,与测序结果一致。
表5临床样品检测结果
本说明书中各个实施例采用递进的方式描述,每个实施例重点说明的都是与其他实施例的不同之处,各个实施例之间相同相似部分互相参见即可。
对所公开的实施例的上述说明,使本领域专业技术人员能够实现或使用本发明。对上述实施例的多种修改对本领域的专业技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其它实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。
序列表
<110>内蒙古农业大学
内蒙古自治区动物疫病预防控制中心(内蒙古自治区兽药检验中心)
<120>牛源大肠杆菌检测引物探针组合、试剂盒及应用
<160>6
<170>siposequencelisting1.0
<210>1
<211>24
<212>dna
<213>artificial
<400>1
ggtcaatggtaatcgtacatcaac24
<210>2
<211>22
<212>dna
<213>artificial
<400>2
actgttcatagaaccagaccag22
<210>3
<211>28
<212>dna
<213>artificial
<400>3
cttgggcaggctgctattagtggtcatg28
<210>4
<211>19
<212>dna
<213>artificial
<400>4
tactgagctagggactctt19
<210>5
<211>20
<212>dna
<213>artificial
<400>5
ctggattaacaagcccttca20
<210>6
<211>27
<212>dna
<213>artificial
<400>6
tcatttggtgcggcagttgcaactatt27
- 还没有人留言评论。精彩留言会获得点赞!