一种多肽及其制备方法与应用与流程
1.本发明属于生物制药领域,具体涉及一种多肽及其制备方法与应用。
背景技术:
2.glp
‑
1(胰高血糖素样肽
‑
1)是人体内一种肠源性激素,在进食后,该类激素可促进胰岛素分泌(这种“肠促胰素效应”所产生的胰岛素占进食后胰岛素总量的50%以上),发挥葡萄糖浓度依赖性降糖作用,非常智能,只有在血糖高的时候才起作用,所以没有注射型胰岛素的低血糖风险。更让人向往的是glp
‑
1具有保护胰岛β细胞的作用:促进胰岛素基因的转录、胰岛素的合成和分泌,并可刺激胰岛β细胞的增殖和分化,抑制胰岛β细胞凋亡,增加胰岛β细胞数量。glp
‑
1还可作用于胰岛α细胞,强烈地抑制胰高血糖素的释放,并作用于胰岛δ细胞,促进生长抑素的分泌,生长抑素又可作为旁分泌激素参与抑制胰高血糖素的分泌。
3.glp
‑
1的缺点:人体自身产生的glp
‑
1极易被体内的二肽基肽酶ⅳ(dpp
‑
4)降解,其血浆半衰期不足2分钟,必须持续静脉滴注或持续皮下注射才能产生疗效,这大大限制了glp
‑
1的临床应用。
4.索马鲁肽是一种有效的glp
‑
1受体激动剂。索马鲁肽有30多个氨基酸,其在结构上的主要特点包括对dpp
‑
4水解酶催化位点的氨基酸进行了替换aib8(2
‑
氨基异丁酸),在氨基酸lys
26
上通过spacer接枝了十八碳链烷基二酸,以结合白蛋白,延缓肾脏清除。虽然索马鲁肽长效性已得到了提高,但仍不能满足患者对长效性的追求。
技术实现要素:
5.本发明旨在至少解决上述现有技术中存在的技术问题之一。为此,本发明提出一种多肽,能够长效控糖。
6.本发明还提出一种具有上述多肽的制备方法。
7.本发明还提出一种上述多肽的应用。
8.根据本发明的一个方面,提出了一种多肽,所述多肽的氨基酸序列为his
‑
(d
‑
ser)
‑
glu
‑
gly
‑
thr
‑
phe
‑
thr
‑
ser
‑
asp
‑
val
‑
ser
‑
ser
‑
tyr
‑
leu
‑
glu
‑
gly
‑
gln
‑
ala
‑
ala
‑
lys(peg2‑
peg2‑
γ
‑
glu
‑
co(ch2)
18
co2h)
‑
glu
‑
phe
‑
ile
‑
ala
‑
trp
‑
leu
‑
val
‑
arg
‑
gly
‑
arg
‑
gly,简写为:hsegtftsdvssylegqaa
‑
k(peg2‑
peg2‑
γglu
‑
co(ch2)
18
cooh)
‑
efiawlvrgrg;分子量为4171.73。
9.本发明方案的第二方面提出了一种具有上述多肽的制备方法,所述方法包括以下步骤:以固相合成树脂为起始原料,采用fmoc/t
‑
bu固相合成策略依次连接氨基酸,得到带氨基酸保护基的多肽主链;在多肽主链上接枝侧链,进行脱保护基团和切肽;所述侧链为peg2
‑
peg2
‑
γ
‑
glu
‑
co(ch2)
18
cooh;所述多肽主链的氨基酸连接顺序为his
‑
(d
‑
ser)
‑
glu
‑
gly
‑
thr
‑
phe
‑
thr
‑
ser
‑
asp
‑
val
‑
ser
‑
ser
‑
tyr
‑
leu
‑
glu
‑
gly
‑
gln
‑
ala
‑
ala
‑
lys
‑
glu
‑
phe
‑
ile
‑
ala
‑
trp
‑
leu
‑
val
‑
arg
‑
gly
‑
arg
‑
gly。
10.在本发明的一些实施方式中,所述接枝侧链的位置为主链第20位氨基酸赖氨酸处。
11.在本发明的一些实施方式中,所述树脂为wang resin树脂。
12.在本发明的一些实施方式中,采用fmoc/t
‑
bu固相合成策略依次连接氨基酸还包括组装fmoc
‑
gly
‑
wang resin载体。
13.在本发明的一些实施方式中,组装fmoc
‑
gly
‑
wang resin载体时,fmoc
‑
gly
‑
oh与树脂的添加比为(4~8):1。
14.在本发明的一些实施方式中,多肽主链的获得还包括以1
‑
羟基苯并三唑(hobt),n,n
‑
二异丙基碳二亚胺(dic)为偶联剂偶联氨基酸,以n,n
‑
二甲基甲酰胺(dmf)为溶剂,采用10~30%的哌啶(piperidine)/n,n
‑
二甲基甲酰胺(dmf)溶液脱除fmoc保护基团的步骤。
15.在本发明的一些实施方式中,所述脱除fmoc基团为采用10~30%的哌啶/dmf(v/v)溶液洗涤树脂,脱去保护基。
16.在本发明的一些实施方式中,还包括采用水合茚三酮检测偶联氨基酸和脱除fmoc基团的步骤。
17.在本发明的一些实施方式中,氨基酸与dic和hobt的添加比为1:(1~2):(1~3)。
18.在本发明的一些实施方式中,氨基酸保护基为pbf、boc、fmoc、tbu、otbu和trt中的一种或多种。
19.在本发明的一些实施方式中,采用裂解液进行同步脱保护基团和切肽步骤。
20.在本发明的一些实施方式中,所述裂解液的组成包括tfa(三氟乙酸)、phenol(苯酚)、thioanisole(茴香硫醚)和edt(1,2
‑
乙二硫醇),质量比为(80~90):(3~6):(3~6):(2~5)。
21.本发明的第三方面提出了一种上述多肽的应用,所述多肽的应用为在制备治疗或预防糖尿病的药物中的应用。
22.在本发明的一些实施方式中,所述多肽在制备胰高血糖素样肽
‑
1受体激动剂中的应用
23.在本发明的一些实施方式中,所述多肽在制备胰高血糖素受体(gcgr)激动剂中的应用。
24.在本发明的一些实施方式中,所述多肽在制备治疗或预防高血糖引起的肥胖症的药物中的应用。
25.一种治疗糖尿病的药物,所述药物包括上述多肽。
26.在本发明的一些实施方式中,所述治疗糖尿病的药物的制备原料还包括药用载体。
27.在本发明的一些实施方式中,所述药用载体为药学领域常规的药物载体。
28.在本发明的一些实施方式中,所述药用载体包括稀释剂、赋形剂、填充剂、黏合剂、崩解剂、吸收促进剂、表面活性剂、吸附载体、润滑剂、甜味剂和香味剂中的至少一种。
29.在本发明的一些实施方式中,所述赋形剂包括水。
30.在本发明的一些实施方式中,所述填充剂包括淀粉和蔗糖中的至少一种。
31.在本发明的一些实施方式中,所述黏合剂包括纤维素衍生物、藻酸盐、明胶和聚乙烯吡咯烷酮中的至少一种。
32.在本发明的一些实施方式中,所述湿润剂包括甘油。
33.在本发明的一些实施方式中,所述崩解剂包括琼脂、碳酸钙和碳酸氢钠中的至少一种。
34.在本发明的一些实施方式中,所述吸收促进剂包括季铵化合物。
35.在本发明的一些实施方式中,所述表面活性剂包括十六烷醇。
36.在本发明的一些实施方式中,所述吸附载体包括高岭土和皂黏土中的至少一种。
37.在本发明的一些实施方式中,所述润滑剂包括滑石粉、硬脂酸钙、硬脂酸镁和聚乙二醇中的至少一种。
38.在本发明的一些实施方式中,所述多肽在药物中的质量分数为0.01%~99%。
39.根据本发明的一些优选实施方式,所述多肽在药物中的质量分数为0.05%~95%。
40.根据本发明的一些优选实施方式,所述多肽在药物中的质量分数为0.05%~20%。
41.在本发明的一些实施方式中,所述糖尿病药物的给药量标准为:上述多肽化合物0.01mg/天~10mg/天。
42.在本发明的一些实施方式中,所述药物的剂型为本领域常规的各种剂型,优选地为固体、半固体或液体的形式,可以为水溶液、非水溶液或混悬液,更优选地为片剂、胶囊剂、软胶囊剂、颗粒剂、丸剂、口服液、干混悬剂、滴丸剂、干浸膏剂、注射剂或输注剂,透皮剂、透皮微针。
43.在本发明的一些实施方式中,所述药物的给药方式可以为本领域常规的给药方式,包括但不限于注射给药或口服给药。所述注射给药可以为静脉注射、肌肉注射、腹腔注射、皮内注射或皮下注射等途径。
44.本文所述的术语“给药剂量”为能够缓解或延迟疾病、退化性或损伤性病症进展的量。可以随被治疗的具体疾病以及其它因素而定,其它因素包括年龄、体重、健康状况、症状的严重程度、给药途径、治疗的频率和在治疗期间是否伴随其它的药物。
45.根据本发明的实施方式,至少具有以下有益效果:
46.1、肥胖可诱导内质网应激、肝脏脂质堆积和胰岛素抵抗,肥胖诱导的内质网应激通过激活jnk和其下游胰岛素受体的丝氨酸磷酸化水平损伤胰岛素信号通路,内质网应激已经被认为是肥胖时发生胰岛素抵抗的一个新的重要机制。本发明提供的多肽化合物通过将第二序列氨基酸采用d
‑
型丝氨酸替换aib氨基异丁酸,可减弱胰岛素信号通路,降低akt磷酸化水平和irs
‑
1的酪氨酸磷酸化水平。抑制细胞色素p450 4a的表达可减轻肝脏内质网应激和胰岛素抵抗。内质网应激在胰岛素抵抗中发挥重要的作用,它可作为糖尿病的潜在治疗靶点。这一创新设计使得本发明的肽链具有更强活性,靶向性跟强,减重控糖效果也更为明显。
47.2、本发明方案的氨基酸序列通过特定位点的氨基酸替换和在氨基酸序列中第20位lys上连接的“侧臂”短肽链,即:采用位点特异性“侧臂”修饰技术,跟无“侧臂”修饰的阳性药索马鲁肽相比,本发明所设计的多肽药物极大程度延长了其作用半衰期,实现了多肽药物的超长效化,其整体的药物作用效果大大优于阳性药索马鲁肽。另外,本发明制备的多肽利用亲脂性取代基结合血液中的白蛋白,保护其免受酶降解,从而提高半衰期。本发明制
备的多肽通过分子内桥稳定分子的螺旋结构,提高了针对胰高血糖素样肽1受体(glp
‑
1r)的效力和/或选择性。本发明的制备的多肽,稳定性好,易于放大生产,成本低。通过跟索马鲁肽进行比较,其发挥药效的长效性和稳定性远远优于索马鲁肽(半衰期达到索马鲁肽2倍或以上)。
48.3、本技术方案制备的多肽具有比索马鲁肽更佳优异的长效血控糖作用,血药浓度更平稳,同时具有高酶解稳定性、高生物活性、基本无不良发应发生的效果,在制备高血糖引起的肥胖症药物和糖尿病药物中具有重要意义。
附图说明
49.下面结合附图和实施例对本发明做进一步的说明,其中:
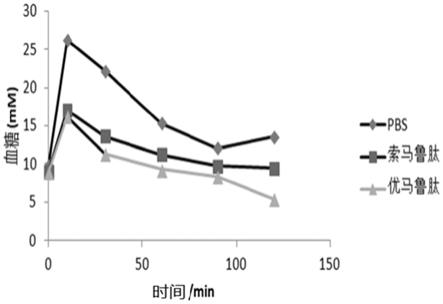
50.图1为本发明测试例中的给药优马鲁肽和索马鲁肽24h后对小鼠进行灌胃葡萄糖,小鼠血糖的变化折线图;
51.图2为本发明测试例中的给药优马鲁肽和索马鲁肽48h后对小鼠进行灌胃葡萄糖,小鼠血糖的变化折线图;
52.图3为本发明测试例中对照组和给药优马鲁肽和索马鲁肽后血糖每分钟的变化率的对比图,其中,****为p<0.00001;
53.图4为本发明测试例中的优马鲁肽和索马鲁肽对血糖的影响auc结果图,其中,*为p<0.005,****为p<0.00001。
具体实施方式
54.以下将结合实施例对本发明的构思及产生的技术效果进行清楚、完整地描述,以充分地理解本发明的目的、特征和效果。显然,所描述的实施例只是本发明的一部分实施例,而不是全部实施例,基于本发明的实施例,本领域的技术人员在不付出创造性劳动的前提下所获得的其他实施例,均属于本发明保护的范围。
55.实施例1多肽的制备
56.本实施例制备了一种多肽,按照fmoc/t
‑
bu策略手工合成,合成规模:0.5mmol,合成如下多肽:boc
‑
his(boc)
‑
d
‑
ser(t
‑
bu)
‑
glu(otbu)
‑
gly
‑
thr(t
‑
bu)
‑
phe
‑
thr(t
‑
bu)
‑
ser(t
‑
bu)
‑
asp(otbu)
‑
val
‑
ser(t
‑
bu)
‑
ser(t
‑
bu)
‑
tyr(t
‑
bu)
‑
leu
‑
glu(otbu)
‑
gly
‑
gln(trt)
‑
ala
‑
ala
‑
lys(peg2
‑
peg2
‑
γ
‑
glu
‑
co(ch2)
18
cooh)
‑
glu(otbu)
‑
phe
‑
ile
‑
ala
‑
trp(boc)
‑
leu
‑
val
‑
arg(pbf)
‑
gly
‑
arg(pbf)
‑
gly
‑
wang resin,具体过程为:
57.1、主肽链组装
58.(1)称取1.47g wang resin(loading 0.47mmol/g,西安蓝晓),加入反应柱中,加入n,n
‑
二甲基甲酰胺(dmf)中溶胀30min,称取fmoc
‑
gly
‑
oh:1.233g(6eq),hobt:0.672g(7.2eq),dmap:0.06g(0.72eq),待用。抽掉dmf,用n,n
‑
二甲基甲酰胺(dmf)充分洗涤树脂2次,把上述称好的物料加入到反应柱中。加入适量的dmf,氮气搅拌均匀,加入n,n
‑
二异丙基碳二亚胺(dic)0.83ml(7.8eq)。反应2h,反应结束。抽掉反应液,用dmf洗涤3次,加入乙酸酐/吡啶(7:6,v/v)封闭4h。抽掉封闭液,dmf洗涤6次,得fmoc
‑
gly
‑
wang resin。
59.(2)以fmoc
‑
gly
‑
wang resin为载体,以1
‑
羟基苯并三唑(hobt),n,n
‑
二异丙基碳二亚胺(dic)为偶联剂,以n,n
‑
二甲基甲酰胺(dmf)为溶剂,以20%的哌啶(piperidine)/n,
n
‑
二甲基甲酰胺(dmf)溶液脱除fmoc基团(两次5min+7min),脱fmoc和偶联过程用水合茚三酮监测去保护和偶联效果。进行手工投料,依次从c端到n端进行缩合反应连接fmoc
‑
arg(pbf)
‑
oh,fmoc
‑
gly
‑
oh,fmoc
‑
arg(pbf)
‑
oh,fmoc
‑
val
‑
oh,fmoc
‑
leu
‑
oh,fmoc
‑
trp(boc)
‑
oh,fmoc
‑
ala
‑
oh,fmoc
‑
ile
‑
oh,fmoc
‑
phe
‑
oh,fmoc
‑
glu(otbu)
‑
oh,fmoc
‑
lys(alloc)
‑
oh,fmoc
‑
ala
‑
oh,fmoc
‑
ala
‑
oh,fmoc
‑
gln(trt)
‑
oh,fmoc
‑
gly
‑
oh,fmoc
‑
glu(otbu)
‑
oh,fmoc
‑
leu
‑
oh,fmoc
‑
tyr(tbu)
‑
oh,fmoc
‑
ser(tbu)
‑
oh,fmoc
‑
ser(tbu)
‑
oh,fmoc
‑
val
‑
oh,fmoc
‑
asp(otbu)
‑
oh,fmoc
‑
ser(tbu)
‑
oh,fmoc
‑
thr(tbu)
‑
oh,fmoc
‑
phe
‑
oh,fmoc
‑
thr(tbu)
‑
oh,fmoc
‑
gly
‑
oh,fmoc
‑
glu(otbu)
‑
oh,fmoc
‑
d
‑
ser(t
‑
bu)
‑
oh,boc
‑
his(trt)
‑
oh以上氨基酸投料(相对于合成规模5eq)得到boc
‑
his
‑
d
‑
ser(t
‑
bu)
‑
glu(otbu)
‑
gly
‑
thr(tbu)
‑
phe
‑
thr(tbu)
‑
ser(tbu)
‑
asp(otbu)
‑
val
‑
ser(tbu)
‑
ser(tbu)
‑
tyr(tbu)
‑
leu
‑
glu(otbu)
‑
gly
‑
gln(trt)
‑
ala
‑
ala
‑
lys(alloc)
‑
glu(otbu)
‑
phe
‑
ile
‑
ala
‑
trp(boc)
‑
leu
‑
val
‑
arg(pbf)
‑
gly
‑
arg(pbf)
‑
gly
‑
wang resin。反应结束用n,n
‑
二甲基甲酰胺(dmf)洗涤6次,二氯甲烷(dcm)洗涤6次。
60.(3)烯丙氧羰基(alloc)的脱除与亲脂取代基的引入
61.用n,n
‑
二甲基甲酰胺(dmf)/二氯甲烷(dcm)=1:1(体积比)的溶液中将树脂洗涤两次,加入四三苯基膦钯(pd(pph3)4)的dcm溶液和吗啉,将该反应混合物在室温下振摇2小时,然后过滤得boc
‑
his(boc)
‑
d
‑
ser(t
‑
bu)
‑
glu(otbu)
‑
gly
‑
thr(t
‑
bu)
‑
phe
‑
thr(t
‑
bu)
‑
ser(t
‑
bu)
‑
asp(otbu)
‑
val
‑
ser(t
‑
bu)
‑
ser(t
‑
bu)
‑
tyr(t
‑
bu)
‑
leu
‑
glu(otbu)
‑
gly
‑
gln
‑
ala
‑
ala
‑
lys
‑
glu(otbu)
‑
phe
‑
ile
‑
ala
‑
trp(boc)
‑
leu
‑
val
‑
arg(pbf)
‑
gly
‑
arg(pbf)
‑
gly
‑
wangresin。此后依次用n,n
‑
二甲基甲酰胺(dmf),二氯甲烷(dcm),二氯甲烷(dcm),n,n
‑
二甲基甲酰胺(dmf)充分洗涤树脂各三次。
62.加入fmocnh
‑
peg2
‑
oh(cas#:872679
‑
70
‑
4,quanta biodesign)相当于合成规模5倍,以1
‑
羟基苯并三唑(hobt),n,n
‑
二异丙基碳二亚胺(dic)为偶联剂,用量分别为氨基酸投料量的1.2倍和1.3倍,振摇2小时后,过滤。得boc
‑
his(boc)
‑
d
‑
ser(t
‑
bu)
‑
glu(otbu)
‑
gly
‑
thr(t
‑
bu)
‑
phe
‑
thr(t
‑
bu)
‑
ser(t
‑
bu)
‑
asp(otbu)
‑
val
‑
ser(t
‑
bu)
‑
ser(t
‑
bu)
‑
tyr(t
‑
bu)
‑
leu
‑
glu(otbu)
‑
gly
‑
gln
‑
ala
‑
ala
‑
lys(fmoc
‑
peg2)
‑
glu(otbu)
‑
phe
‑
ile
‑
ala
‑
trp(boc)
‑
leu
‑
val
‑
arg(pbf)
‑
gly
‑
arg(pbf)
‑
gly
‑
wangresin。此后依次用n,n
‑
二甲基甲酰胺(dmf),二氯甲烷(dcm),二氯甲烷(dcm),n,n
‑
二甲基甲酰胺(dmf)充分洗涤树脂各三次。
63.20%的哌啶(piperidine)/n,n
‑
二甲基甲酰胺(dmf)溶液脱除fmoc基团(两次5min+7min),加fmocnh
‑
peg2
‑
oh(cas#:872679
‑
70
‑
4,quanta biodesign)相当于合成规模5倍,以1
‑
羟基苯并三唑(hobt),n,n
‑
二异丙基碳二亚胺(dic)为偶联剂,用量分别为氨基酸投料量的1.2倍和1.3倍,振摇2小时后,过滤得boc
‑
his(boc)
‑
d
‑
ser(t
‑
bu)
‑
glu(otbu)
‑
gly
‑
thr(t
‑
bu)
‑
phe
‑
thr(t
‑
bu)
‑
ser(t
‑
bu)
‑
asp(otbu)
‑
val
‑
ser(t
‑
bu)
‑
ser(t
‑
bu)
‑
tyr(t
‑
bu)
‑
leu
‑
glu(otbu)
‑
gly
‑
gln
‑
ala
‑
ala
‑
lys(fmoc
‑
peg2
‑
peg2)
‑
glu(otbu)
‑
phe
‑
ile
‑
ala
‑
trp(boc)
‑
leu
‑
val
‑
arg(pbf)
‑
gly
‑
arg(pbf)
‑
gly
‑
wangresin。此后依次用n,n
‑
二甲基甲酰胺(dmf),二氯甲烷(dcm),二氯甲烷(dcm),n,n
‑
二甲基甲酰胺(dmf)充分洗涤树脂各三次。
64.20%的哌啶(piperidine)/n,n
‑
二甲基甲酰胺(dmf)溶液脱除fmoc基团(两次5min+7min),加fmoc
‑
glu
‑
otbu相当于合成规模5倍,以1
‑
羟基苯并三唑(hobt),n,n
‑
二异丙基碳二亚胺(dic)为偶联剂,用量分别为氨基酸投料量的1.2倍和1.3倍,振摇2小时后,过滤得
boc
‑
his(boc)
‑
d
‑
ser(t
‑
bu)
‑
glu(otbu)
‑
gly
‑
thr(t
‑
bu)
‑
phe
‑
thr(t
‑
bu)
‑
ser(t
‑
bu)
‑
asp(otbu)
‑
val
‑
ser(t
‑
bu)
‑
ser(t
‑
bu)
‑
tyr(t
‑
bu)
‑
leu
‑
glu(otbu)
‑
gly
‑
gln
‑
ala
‑
ala
‑
lys(fmoc
‑
peg2
‑
peg2
‑
γ
‑
glu)
‑
glu(otbu)
‑
phe
‑
ile
‑
ala
‑
trp(boc)
‑
leu
‑
val
‑
arg(pbf)
‑
gly
‑
arg(pbf)
‑
gly
‑
wang resin。此后依次用n,n
‑
二甲基甲酰胺(dmf),二氯甲烷(dcm),二氯甲烷(dcm),n,n
‑
二甲基甲酰胺(dmf)充分洗涤树脂各三次。
65.20%的哌啶(piperidine)/n,n
‑
二甲基甲酰胺(dmf)溶液脱除fmoc基团(两次5min+7min),加二十烷酸单叔丁酯相当于合成规模5倍,以1
‑
羟基苯并三唑(hobt),n,n
‑
二异丙基碳二亚胺(dic)为偶联剂,用量分别为氨基酸投料量的1.2倍和1.3倍,振摇2小时后,过滤得boc
‑
his(boc)
‑
d
‑
ser(t
‑
bu)
‑
glu(otbu)
‑
gly
‑
thr(t
‑
bu)
‑
phe
‑
thr(t
‑
bu)
‑
ser(t
‑
bu)
‑
asp(otbu)
‑
val
‑
ser(t
‑
bu)
‑
ser(t
‑
bu)
‑
tyr(t
‑
bu)
‑
leu
‑
glu(otbu)
‑
gly
‑
gln
‑
ala
‑
ala
‑
lys(peg2
‑
peg2
‑
γ
‑
glu
‑
co(ch2)
18
cooh)
‑
glu(otbu)
‑
phe
‑
ile
‑
ala
‑
trp(boc)
‑
leu
‑
val
‑
arg(pbf)
‑
gly
‑
arg(pbf)
‑
gly
‑
wang resin。此后依次用n,n
‑
二甲基甲酰胺(dmf),二氯甲烷(dcm),二氯甲烷(dcm)充分洗涤树脂各三次后,真空抽干。
66.2、多肽全保护的脱除
67.往干燥的boc
‑
his(boc)
‑
d
‑
ser(t
‑
bu)
‑
glu(otbu)
‑
gly
‑
thr(t
‑
bu)
‑
phe
‑
thr(t
‑
bu)
‑
ser(t
‑
bu)
‑
asp(otbu)
‑
val
‑
ser(t
‑
bu)
‑
ser(t
‑
bu)
‑
tyr(t
‑
bu)
‑
leu
‑
glu(otbu)
‑
gly
‑
gln
‑
ala
‑
ala
‑
lys(peg2
‑
peg2
‑
γ
‑
glu
‑
co(ch2)
18
cooh)
‑
glu(otbu)
‑
phe
‑
ile
‑
ala
‑
trp(boc)
‑
leu
‑
val
‑
arg(pbf)
‑
gly
‑
arg(pbf)
‑
gly
‑
wang resin,加入裂解液tfa/phenol/thioanisole/edt/h2o(82.5:5:5:2.5:5,体积比)10倍重量体积,室温反应2.5个小时。过滤,滤饼用少量裂解液洗涤3次,合并滤液。滤液在搅拌下缓慢倒入冰乙醚中。静置0.5个小时以上,待沉淀完全,沉淀离心,用冰乙醚洗涤3次,真空干燥得到粗品化合物h
‑
his
‑
(d
‑
ser)
‑
glu
‑
gly
‑
thr
‑
phe
‑
thr
‑
ser
‑
asp
‑
val
‑
ser
‑
ser
‑
tyr
‑
leu
‑
glu
‑
gly
‑
gln
‑
ala
‑
ala
‑
lys(peg2
‑
peg2
‑
γ
‑
glu
‑
co(ch2)
18
cooh)
‑
glu
‑
phe
‑
ile
‑
ala
‑
trp
‑
leu
‑
val
‑
arg
‑
gly
‑
arg
‑
gly。
68.3、多肽化合物的精制纯化
69.将上步中所得粗品溶于乙腈(acn)/h2o=1:2(体积比)的溶液中,通过10μm反相c18制备柱(20mm x 250mm)进行制备型hplc纯化。用30%乙腈(含0.05%三氟乙酸)/h2o(含0.05%三氟乙酸)为起始,以梯度(1.33%/min的速度增加乙腈的比例),流速为15ml/min将该柱洗脱30分钟,收集含有肽的组分,冷冻抽干,得到hplc纯度大于95%的纯品的多肽,将该多肽命名为优马鲁肽(yomaglutide)(如果纯度没有达到要求,可重复一次hplc纯化)。用液质联用分析分离出的产物,产物纯度大于95%。
70.试验例
71.1、优马鲁肽对glp
‑
1r和gcgr的激动活性的测定
72.本试验例测试了实施例制备的优马鲁肽与索马鲁肽对glp
‑
1r和gcgr的激动活性。
73.实验材料:索马鲁肽购自浙江湃肽生物有限公司(cas no.:910463
‑
68
‑
2)。在glp
‑
1r
‑
luciferase
‑
293t细胞和gcgr
‑
luciferase
‑
293t细胞模型中,对优马鲁肽进行glp
‑
1r和gcgr的激动活性初筛。
74.实验方法:消化细胞铺96孔板(含10%fbs的培养基,glp
‑
1r
‑
luciferase
‑
293t:20000cell/well,gcgr
‑
luciferase
‑
293t:20000cell/well,100μl);36h后,弃96孔板中培养基,加入90μl无血清培养基;6h后,用无血清培养基配制系列浓度(0.01、0.1、1、10、100、
1000、10000、100000、1000000、10000000、100000000pm)的优马鲁肽及索马鲁肽,每孔加入10μl(即稀释10倍),孵育细胞5h;向每孔中加入100μl的细胞裂解液,冰上裂解10min后震荡均匀,取2μl裂解液加入384酶标仪白板中,先加入10μl的萤火虫荧光素酶反应液,读数,再加入10μl的海肾荧光素酶反应液,读数;数据处理,用萤火虫荧光素酶的读数除以海肾荧光素酶的读数,再扣除空白组的数值可得到不同浓度下的激动倍数。
75.实验结果:索马鲁肽glp
‑
1的ec
50
为265.2pm和gcgr的ec
50
为8600875pm;本发明的优马鲁肽多肽化合物glp
‑
1的ec
50
为315.2pm和gcgr的ec
50
为26008755pm。结果表明本技术方案制备的优马鲁肽多肽化合物对glp
‑
1r和gcgr同样与索马鲁肽具有较显著的激动活性,同时对glp
‑
1r受体的激活具有一定的特异性。
76.2、优马鲁肽和索马鲁肽对口服葡萄糖耐量(ogtt)的作用
77.实验方法:将8周龄的雄性c57bl/6j小鼠(南京大学模式动物研究中心)按照相似的血糖(从尾尖获取的血液样品评估)随机分组,每组8只。禁食(6小时)后对动物给药,本发明中优马鲁肽多肽化合物、阳性对照多索马鲁肽均按照100ug/kg的剂量,皮下进行给药,对照组给予pbs。灌胃葡萄糖用ddh2o配成浓度为0.5g/ml的贮备液,常温保存。灌胃前将小鼠禁食8h,分别在给药24h和48h按照2.5g/kg的剂量灌胃葡萄糖,灌胃葡萄糖用ddh2o配成浓度为0.5g/ml的贮备液,常温保存。灌胃前将小鼠禁食8h,分别在给药24h和48h时按照2.5g/kg的剂量灌胃葡萄糖,并且分别在t=0分钟、t=15分钟、t=30分钟、t=60分钟、t=90分钟和t=120分钟时测量血糖。检测血糖变化,跟踪血糖直到48小时。使用软件graphpadprism处理数据作出血糖变化折线图(如图1和图2所示),并计算曲线下面积得到auc图(如图3和图4所示)。
78.实验结果:结果如图1
‑
4所示,图1为给药优马鲁肽和索马鲁肽24h后对小鼠进行灌胃葡萄糖,小鼠血糖的变化折线图;图2为给药优马鲁肽和索马鲁肽48h后对小鼠进行灌胃葡萄糖,小鼠血糖的变化折线图;图3为对照组和给药优马鲁肽和索马鲁肽后血糖每分钟的变化率的对比图;图4为优马鲁肽和索马鲁肽对血糖的影响auc结果图;从图中可以看出,与载剂(pbs)相比,索马鲁肽和优马鲁肽在给药24h后,第一个ogtt曲线时段(0
‑
120min)其auc均可显著降低(p<0.05),而在随后的ogtt曲线时段48h,其auc开始不同程度的提升。在48h的ogtt曲线时段下的auc,索马鲁肽已失去药效活性。
79.综上所述,本发明方案制备的优马鲁肽和索马鲁肽的活性相当,但是优马鲁肽对于长效降糖的效果明显优于索马鲁肽。与载剂(pbs)相比,本发明的优马鲁肽多肽化合物能改善小鼠糖耐受的效果,展现了更为优秀和显著地改善葡萄糖耐受效果,同时结果也说明本发明的优马鲁肽具有更为优秀和显著的长效降糖效果。
80.上面结合附图对本发明实施例作了详细说明,但是本发明不限于上述实施例,在所属技术领域普通技术人员所具备的知识范围内,还可以在不脱离本发明宗旨的前提下作出各种变化。此外,在不冲突的情况下,本发明的实施例及实施例中的特征可以相互组合。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1