一种吡唑衍生物及其作为PDE10抑制剂的用途的制作方法
一种吡唑衍生物及其作为pde10抑制剂的用途
技术领域
1.本发明涉及一种吡唑衍生物及其作为pde10抑制剂的用途。
背景技术:
2.磷酸二酯酶(pde)是一类细胞内酶,其参与核苷酸环腺苷酸单磷酸酯(camp)和环鸟苷酸单磷酸酯(cgmp)到它们各自的核苷酸单磷酸酯的水解过程。环核苷酸camp和cgmp分别通过腺苷酰基和鸟苷酰基环化酶来合成,并且在多个细胞通道中充当二级信使。camp和cgmp充当调节众多细胞内过程的细胞内二级信使,特别是在中枢神经系统的神经细胞中。在神经细胞中,其包括camp和cgmp-依赖性激酶的活化,以及随后在突触传递的急性调节中及在神经元分化和存活中涉及的蛋白质磷酸化作用。环核苷酸信号的复杂性表现为camp和cgmp合成和降解中涉及的酶的分子多样性。至少存在十个腺苷酰基环化酶家族、两个鸟苷酰基环化酶家族和十一个磷酸二酯酶家族。此外,已知不同类型的神经细胞能表达这些类型中每一类的多种同功酶,并且对于不同同功酶在给定神经细胞内的区分和功能特异性有充分的证据。
3.调节环核苷酸信号的主要机理是通过磷酸二酯酶催化的环核苷酸分解代谢。已有由21种不同基因编码的11个已知的pde家族。每种基因通常产生多种拼接变体,从而进一步增加了同功酶的多样性。通常根据环核苷酸底物特异性、调节机理和对抑制剂的敏感性来从功能性上区分pde家族。此外,pde在整个生物体中(包括在中枢神经系统中)的表达是有差别的。由于这些不同的酶活性和区域分布,不同pde的同功酶可能具有不同的生理功能。此外,能够选择性地抑制不同pde家族或同功酶的化合物可能提供特定的治疗作用和/或更少的副作用。
4.根据主要的氨基酸序列和截然不同的酶活性,pde10被鉴定为一个独特的家家族。pde10对camp(km=0.05μm)的亲和性高于对cgmp(km=3μm)的亲和性。然而,其对cgmp的vmax比对camp高约5倍。与之前鉴定的pde家族相比,多肽的pde10家族显示出较低的序列同源程度,并且显示出对某些已知对其它pde家族具有特异性的抑制剂不敏感。pde10主要在人的脑、睾丸、甲状腺等中表达。特别是在脑内的纹状体的中型多刺神经元(msn、medium-sized spiny neuron)中高度表达,在丘脑、海马、额皮质和嗅结节中中度表达。而且,pde10也在小鼠和大鼠的脑、睾丸中高表达。这些表达pde10的脑部位在精神疾病的病理学机制中显示出重要的作用,因此暗示pde10与精神障碍、神经变性疾病等病理学机制相关。
5.pde10抑制剂的潜在的抗精神病作用已得到大量文献的证实。us2003/0032579中报道了作为具有中度的选择性的pde10抑制剂的罂粟碱,降低了作为精神病动物模型的大鼠中的阿朴吗啡诱导性刻板症,大鼠中的氟哌啶醇诱导性僵直症增加,另一方面,大鼠脑中的多巴胺浓度同时降低,显示出具有以往的抗精神病药作用。而且,由对患者的适用也得到证实,确认罂粟碱作为处置精神病用的pde10抑制剂。在wo2005/082883号公报和ep1250923中,公开了作为pde10抑制剂的罂粟碱和各种的芳香族杂环化合物(喹唑啉和异喹唑啉化合物等)。而且,公开了pde10抑制剂对精神障碍、焦虑症、运动障碍、药物依赖症、伴随认知障
碍症状的疾病、情绪障碍、或情绪症状等疾病或症状的治疗或预防有用。而且,也公开了pde10抑制剂对神经变性疾病(例如,帕金森病和亨廷顿氏病等)的治疗或预防有用。
6.现有技术中报道了大量以吡唑和三氮唑作为母核结构的pde10抑制剂:持田制药株式会社公开了一类新型的吡唑衍生物(cn107011343a,cn106957317a),其可用于pde10相关的各种疾病;霍夫曼-拉罗奇有限公司公开了一系列三氮唑化合物(cn104364249a)作为pde10抑制剂;辉瑞公司(cn101611029a)公开了一类吡唑衍生物,可作为pde10抑制剂。
7.由此可见,开发新的pde10抑制剂仍然具有巨大的市场前景和社会效益。
技术实现要素:
8.本发明所要解决的技术问题是:提供了一种吡唑衍生物,其能够作为pde10抑制剂。
9.本发明的第一个方面,是提供一种式i所示化合物及其药学上可接受的盐,其具有如下结构:
[0010][0011]
优选地,所述药学上可接受的盐选自:盐酸盐、氢溴酸盐、磷酸盐、硫酸盐、乙酸盐、草酸盐、酒石酸盐、柠檬酸盐、三氟乙酸盐、甲烷磺酸盐、乙烷磺酸盐、对甲苯磺酸盐或水杨酸盐;
[0012]
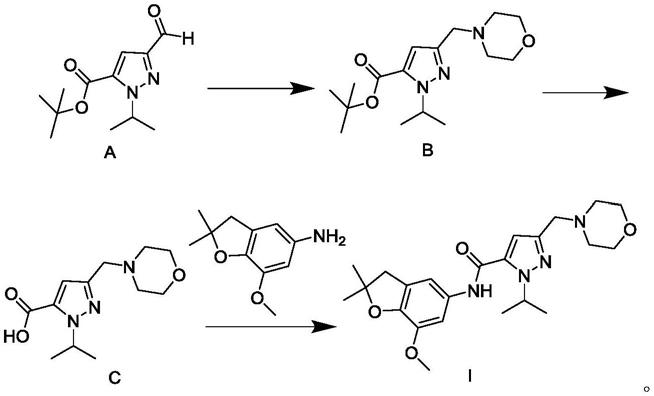
本发明的另一方面提供一种制备式i化合物的方法,其合成路线如下:
[0013][0014]
具体反应步骤如下:
[0015]
步骤1):将1,1-二甲基乙基-3-甲酰基-1-(1-甲基乙基)-1h-吡唑-5-羧酸酯,即原料a,溶解在无水dcm中,通氮气保护,然后加入吗啉,室温下反应2.5小时,再加入三乙酰氧基硼氢化钠,并将反应混合物在室温搅拌24小时,反应完毕后,经后处理得到1,1-二甲基乙
基-1-(1-甲基乙基)-3-(4-吗啉基甲基)-1h-吡唑-5-羧酸酯,即中间体b;
[0016]
步骤2):将中间体b溶解在1,4-二氧六烷中,然后加入含有4m氯化氢的1,4-二氧六烷溶液,并将混合物在室温下搅拌,24小时后,再加入4m氯化氢的1,4-二氧六烷溶液并将混合物在室温下搅拌48小时,加入一滴水并将混合物在室温搅拌24小时,经后处理得到1-(1-甲基乙基)-3-(4-吗啉基甲基)-1h-吡唑-5-羧酸,即中间体c;
[0017]
步骤3):在搅拌下,将中间体c和7-甲氧基-2,2-二甲基-2,3-二氢苯并呋喃-5-胺溶解于dcm中,然后加入dcc和dmap,室温搅拌反应,tlc检测反应完全,经后处理得到式i化合物。
[0018]
优选地,所述反应步骤具体操作如下:
[0019]
步骤1):将2.38g 1,1-二甲基乙基-3-甲酰基-1-(1-甲基乙基)-1h-吡唑-5-羧酸酯,即原料a,溶解在无水dcm 80ml中,通氮气保护,然后加入吗啉1ml,室温下反应2.5小时,再加入三乙酰氧基硼氢化钠4.5g,并将反应混合物在室温搅拌24小时,反应完毕后,加入碳酸氢钠溶液150ml和dcm 150ml,收集有机相;水相用dcm萃取三次,合并有机相,真空除去溶剂,残余物通过硅胶快速色谱法纯化,得到1,1-二甲基乙基-1-(1-甲基乙基)-3-(4-吗啉基甲基)-1h-吡唑-5-羧酸酯,即中间体b;
[0020]
步骤2):将1.55g 1,1-二甲基乙基-1-(1-甲基乙基)-3-(4-吗啉基甲基)-1h-吡唑-5-羧酸酯,即中间体b,溶解在1,4-二氧六烷10ml中,然后加入含有4m氯化氢的1,4-二氧六烷20ml溶液,并将混合物在室温下搅拌,24小时后,再加入4m氯化氢的1,4-二氧六烷15ml溶液并将混合物在室温下搅拌48小时,加入一滴水并将混合物在室温搅拌24小时,真空除去溶剂,加入甲苯50ml,并不断研磨,有白色固体析出,过滤,滤饼在真空烘箱中干燥过夜,得到1-(1-甲基乙基)-3-(4-吗啉基甲基)-1h-吡唑-5-羧酸,即中间体c;
[0021]
步骤3):在搅拌下,将0.51g中间体c和0.46g 7-甲氧基-2,2-二甲基-2,3-二氢苯并呋喃-5-胺溶解于20ml dcm中,然后加入0.70g dcc和0.10g dmap,室温搅拌反应,tlc检测反应完全,抽滤,滤饼用无水乙醇重结晶,得式i化合物。
[0022]
本发明的另一方面提供一种药物组合物,其包含式i所示的化合物或其药学上可接受的盐,以及药学上可接受的载体、赋形剂。
[0023]
本发明另一方面涉及一种式i化合物及其药学上可接受的盐或包含其药物组合物在制备pde10抑制剂中的用途。同时该化合物可治疗由pde10介导的疾病;所述疾病选自精神分裂症,例如错乱型、紧张性、未分类或残余型精神分裂症;精神分裂症样病症;情感性精神分裂症,例如妄想症或抑郁型;妄想症;物质-诱发的精神失常,例如由酒精、安非他命、大麻、可卡因、迷幻剂、吸入剂、鸦片样物质或苯西克定诱发的精神失常;妄想型人格障碍;以及精神分裂型人格障碍。
[0024]
定义:
[0025]
在某些实施方案中,药学上可接受的形式是药学上可接受的盐,药学上可接受的盐在本领域中是熟知的。药学上可接受的盐的实例是诸如盐酸、氢溴酸、磷酸、硫酸、高氯酸、乙酸、草酸、顺丁烯二酸、酒石酸、柠檬酸、丁二酸或丙二酸、乙酸、丙酸、乙醇酸、丙酮酸、草酸、乳酸、三氟乙酸、甲烷磺酸、乙烷磺酸、对甲苯磺酸、水杨酸等与化合物形成盐的形式。
[0026]“药学上可接受的载体”或“药学上可接受的赋形剂”包括任何和所有溶剂、分散介质、包覆剂、等张剂和吸收延迟剂等。药学上可接受的载体或赋形剂不破坏公开的化合物的
药理学活性,并且在以足以递送治疗量的化合物的剂量施用时是无毒的。药物活性物质的所述介质和试剂的使用在本领域中是熟知的。
[0027]
与现有技术相比,本发明的有益效果是:
[0028]
(1)本发明提供了一类新的pde10抑制剂,拓宽了现有的具有mao抑制活性的化合物,可作为先导化合物继续优化;
[0029]
(2)本发明化合物相对于现有的pde10抑制剂,具有更好的抑制效果。
[0030]
(3)本发明的化合物制备方法简单,工艺流程短,易于实现工业化。
具体实施方式
[0031]
下面通过实施例来具体说明本发明的内容。在本发明中,以下实施例是为了更好地阐述本发明,并不是用来限制本发明的范围。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
[0032]
实施例1
[0033][0034]
步骤1):将1,1-二甲基乙基-3-甲酰基-1-(1-甲基乙基)-1h-吡唑-5-羧酸酯(原料a,2.38g)溶解在无水dcm(80ml)中,通氮气保护,然后加入吗啉(1ml),室温下反应2.5小时。再加入三乙酰氧基硼氢化钠(4.5g),并将反应混合物在室温搅拌24小时。反应完毕后,加入碳酸氢钠溶液(150ml)和dcm(150ml),收集有机相;水相用dcm萃取三次,合并有机相。真空除去溶剂,残余物通过硅胶快速色谱法纯化,得到1,1-二甲基乙基-1-(1-甲基乙基)-3-(4-吗啉基甲基)-1h-吡唑-5-羧酸酯(中间体b,2.84g),为无色油。
[0035]1hnmr(400mhz,cdcl3)δ(ppm):6.74(s,1h),3.88-3.94(m,1h),3.61-3.72(m,4h),2.55-2.70(m,4h),3.55(s,2h),1.47(s,9h),1.36(s,6h).
[0036]
elemental analysis:c,62.11;h,8.80;n,13.58;o,15.51。
[0037]
步骤2):将1,1-二甲基乙基-1-(1-甲基乙基)-3-(4-吗啉基甲基)-1h-吡唑-5-羧酸酯(1.55g)溶解在1,4-二氧六烷(10ml)中。然后加入含有4m氯化氢的1,4-二氧六烷(20ml)溶液,并将混合物在室温下搅拌。24小时后,再加入4m氯化氢的1,4-二氧六烷(15ml)溶液并将混合物在室温下搅拌48小时。加入一滴水并将混合物在室温搅拌24小时。真空除去溶剂,加入甲苯(50ml),并不断研磨,有白色固体析出。过滤,滤饼在真空烘箱中干燥过夜,得到1-(1-甲基乙基)-3-(4-吗啉基甲基)-1h-吡唑-5-羧酸(中间体c,1.15g),为白色固
体;
[0038]
步骤3):在搅拌下,将中间体c(0.51g)和7-甲氧基-2,2-二甲基-2,3-二氢苯并呋喃-5-胺(0.46g)溶解于20ml dcm中,然后加入0.70g dcc,0.10g dmap。室温搅拌反应,tlc检测反应完全,抽滤,滤饼用无水乙醇重结晶,得白色固体0.43g,即为式i化合物。
[0039]1hnmr(400mhz,cdcl3)δ(ppm):9.91(s,1h),7.49(s,1h),7.21(s,1h),6.53(s,1h),3.90-3.97(m,1h),3.88(s,3h),3.63-3.74(m,4h),3.53(s,2h),2.90(s,2h),2.41-2.53(m,4h),1.49(s,6h),1.36(s,6h).
[0040]
实施例2化合物(i)体外化合物评价(酶抑制活性评价:人pde10抑制作用)
[0041]
使用imap tr-fret磷酸二酯酶检测试剂盒(molecular device)进行测定。向384孔板(corning)中加入稀释了的各浓度的试验化合物10μl和用1
×
imap包含0.1%bsa的反应缓冲液(由试剂盒所带的5
×
制作,10mm tris-hcl、ph=7.2、10mm mgcl2、0.05%nan3、和0.1%bsa)稀释为2ng/ml的pde10酶5μl,在室温下预温浴5分钟。加入用1
×
imap包含0.1%bsa的反应缓冲液稀释为400nm的试剂盒所带的camp基质5μl,在室温下反应60分钟。再添加试剂盒所带的imap tr-fret结合溶液60μl并放置3小时以上,然后用arvo sx(perkinelmer)在激发波长340nm下测定铽的荧光强度(emission=490nm)和tr-fret(emission=520nm),计算产生的5
’‑
amp的量。将代替试验化合物添加了溶剂的孔的数值计为0%、将未添加pde10酶的孔的数值记作100%,算出各试验化合物的抑制活性。
[0042]
测定结果表明,本发明实施例中所公开的化合物(i)的pde10抑制活性的ic
50
值为87
±
22.5nmol/l,表明本发明化合物具有良好的pde10抑制活性。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1