靶向SARS-CoV-2的纳米抗体及制备方法和应用与流程
靶向sars-cov-2的纳米抗体及制备方法和应用
技术领域
1.本发明涉及生物技术领域,尤其涉及一种靶向sars-cov-2的纳米抗体及制备方法和应用。
背景技术:
2.新型冠状病毒肺炎(corona virus disease 2019,covid-19)可通过飞沫传播、接触呼吸道分泌物、气溶胶传播等途径传播,带来的后果十分严重。引起covid-19的急性呼吸系统综合症冠状病毒2(severe acute respiratory syndrome coronavirus 2,sars-cov-2) 主要表达4种结构蛋白,分别为刺突蛋白(spike,s)、包膜蛋白(envelope)、膜蛋白(membrane)和核衣壳蛋白(nucleocapsid)。其中s蛋白包括n 端的s1亚基和 c 末端的s2亚基,s1亚基包含大约200个氨基酸的受体结合域 (receptor binding domain,rbd)负责病毒与宿主受体结合,s2亚基负责病毒与宿主细胞膜融合。s蛋白在病毒附着、感染和传播中发挥至关重要的作用,通过与宿主细胞的血管紧张素转化酶2(angiotensin converting enzyme2,ace2)结合进而感染细胞,是抗sars-cov-2药物研发的重要靶点。
3.中和抗体是对抗covid-19的重要疗法。已有研究发现通过给重症covid-19 患者输送康复者的血清能够显著改善临床结果,表明中和抗体疗法对新冠重症患者也有较好的缓解作用。其作用机理为中和抗体与新冠病毒表面的刺突糖蛋白结合进而影响sars-cov-2与宿主细胞的表面受体结合,从而使病毒无法感染靶细胞。目前已有多个中和抗体获批上市用于covid-19的治疗,这些单抗靶点主要集中在s蛋白的rbd结构域。然而,面对不断突变的sars-cov-2,已有中和抗体很难靶向新的新冠变异株。最近的一项研究表明,omicron亚型ba.2可逃避几乎所有的中和抗体治疗。因此,迫切需要开发出新的可以同时靶向不同新冠变异株特别是omicron及其亚型ba.2的中和抗体。
技术实现要素:
4.本技术的目的在于提供一种靶向sars-cov-2的纳米抗体及制备方法和应用,旨在解决现有技术中缺乏新冠变异株omicron及其亚型ba.2的中和抗体的问题。
5.为实现上述申请目的,本技术采用的技术方案如下:第一方面,本技术公开了一种靶向sars-cov-2的纳米抗体,纳米抗体包括纳米抗体nbf2、纳米抗体nbg4、纳米抗体nbg1、纳米抗体nbd2、纳米抗体nbe8中的至少一种,其中,纳米抗体nbf2的氨基酸序列如seq.id no.1所示,纳米抗体nbg4的氨基酸序列如seq.id no.2所示,纳米抗体nbg1的氨基酸序列如seq.id no.3所示,纳米抗体nbd2的氨基酸序列如seq.id no.4所示,纳米抗体nbe8的氨基酸序列如seq.id no.5所示。
6.第二方面,本技术公开了一种靶向sars-cov-2的纳米抗体的制备方法,包括如下步骤:提供目的蛋白,将目的蛋白包被在免疫管上进行富集筛选,得到噬菌体文库;在噬菌体文库中选取克隆子进行验证,得到阳性克隆子;
将阳性克隆子进行测序并根据测序结果合成纳米抗体的基因序列;将纳米抗体的基因序列克隆至表达载体中得到重组质粒,将重组质粒转入宿主细胞中诱导表达并进行纯化,得到靶向sars-cov-2的纳米抗体。
7.第三方面,本技术公开了靶向sars-cov-2的纳米抗体在制备预防和/或治疗新型冠状病毒肺炎的药物中的应用。
8.第四方面,本技术公开了靶向sars-cov-2的纳米抗体在制备检测新型冠状病毒的检测试剂或检测试剂盒中的应用。
9.本技术第一方面提供的靶向sars-cov-2的纳米抗体,包括纳米抗体nbf2、纳米抗体nbg4、纳米抗体nbg1、纳米抗体nbd2、纳米抗体nbe8中的至少一种,提供的纳米抗体对新冠病毒野生株、新冠病毒变异株阿尔法(alpha)、新冠病毒贝塔(beta)、新冠病毒德尔塔(delta)、新冠病毒omicron及其亚型ba.2 的rbd结构域具有较高的亲和力,能够快速且特异性地中和不同的新冠病毒,有效抑制其活性;同时,提供的纳米抗体具有更长的cdr3序列,有利于纳米抗体进行灵活调节其构象,提高与病毒的结合作用,且制备成本较低,有利于广泛应用。
10.本技术第二方面提供的一种靶向sars-cov-2的纳米抗体的制备方法,该制备方法基于噬菌体展示筛选技术,以sars-cov-2的变异株奥密克戎(omicron) rbd蛋白为靶标构建了纳米抗体库以筛选阳性克隆子,并进行测序、克隆、表达、纯化,得到靶向sars-cov-2的纳米抗体;该制备方法利用噬菌体在宿主菌中快速复制的生物特性,能够快速、高通量地筛选与特定变异株奥密克戎(omicron) rbd蛋白结合的纳米抗体,制备方法快速、简便,有利于大量筛选,提高了筛选效率。
11.本技术第三方面提供的靶向sars-cov-2的纳米抗体在制备预防和/或治疗新型冠状病毒肺炎的药物中的应用,由于筛选得到的靶向sars-cov-2的纳米抗体包括纳米抗体nbf2、纳米抗体nbg4、纳米抗体nbg1、纳米抗体nbd2、纳米抗体nbe8中的至少一种,对新冠病毒野生株及各变异株的病毒具有较好的中和活性能力和抑制活性能力,适用于制备预防和/或治疗新型冠状病毒肺炎的相关药物。
12.本技术第四方面提供的靶向sars-cov-2的纳米抗体在制备检测新型冠状病毒的检测试剂或检测试剂盒中的应用,提供的靶向sars-cov-2的纳米抗体包括纳米抗体nbf2、纳米抗体nbg4、纳米抗体nbg1、纳米抗体nbd2、纳米抗体nbe8中的至少一种,对新冠病毒野生株及各变异株的病毒具有较高得结合能力,适用于制备检测新型冠状病毒的检测试剂或检测试剂盒。
附图说明
13.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
14.其中:图1为omicron rbd蛋白纳米抗体筛选图。
15.图2为omicron rbd噬菌体elisa验证示意图。
16.图3为omicron rbd纳米抗体表达纯化结果图。
17.图4为omicron rbd纳米抗体免疫印迹检测结果图。
18.图5为omicron rbd纳米抗体elisa验证图。
19.图6为sars-cov-2 野生株(wild type,wt) rbd纳米抗体elisa验证图。
20.图7为delta rbd纳米抗体elisa验证图。
21.图8为纳米抗体与阴性对照蛋白牛血清白蛋白(bovine serum albumin,bsa)elisa验证图。
22.图9为 biacore检测纳米抗体d2与wt rbd蛋白的亲和常数图。
23.图10为biacore检测纳米抗体d2与alpha rbd蛋白的亲和常数图。
24.图11为biacore检测纳米抗体d2与beta rbd蛋白的亲和常数图。
25.图12为biacore检测纳米抗体d2与delta rbd蛋白的亲和常数图。
26.图13为biacore检测纳米抗体d2与omicron rbd蛋白的亲和常数图。
27.图14为biacore检测纳米抗体d2与omicron ba.2 rbd蛋白的亲和常数图。
28.图15为biacore检测纳米抗体e8与wt rbd蛋白的亲和常数图。
29.图16为biacore检测纳米抗体e8与alpha rbd蛋白的亲和常数图。
30.图17为biacore检测纳米抗体e8与beta rbd蛋白的亲和常数图。
31.图18为 biacore检测纳米抗体e8与delta rbd蛋白的亲和常数图。
32.图19为biacore检测纳米抗体e8与omicron rbd蛋白的亲和常数图。
33.图20为biacore检测纳米抗体e8与omicron ba.2 rbd蛋白的亲和常数图。
34.图21为biacore检测纳米抗体f2与wt rbd蛋白的亲和常数图。
35.图22为biacore检测纳米抗体f2与alpha rbd蛋白的亲和常数图。
36.图23为biacore检测纳米抗体f2与beta rbd蛋白的亲和常数图。
37.图24为biacore检测纳米抗体f2与delta rbd蛋白的亲和常数图。
38.图25为biacore检测纳米抗体f2与omicron rbd蛋白的亲和常数图。
39.图26为biacore检测纳米抗体f2与omicron ba.2 rbd蛋白的亲和常数图。
40.图27为biacore检测纳米抗体g1与wt rbd蛋白的亲和常数图。
41.图28为biacore检测纳米抗体g1与alpha rbd蛋白的亲和常数图。
42.图29为biacore检测纳米抗体g1与beta rbd蛋白的亲和常数图。
43.图30为biacore检测纳米抗体g1与delta rbd蛋白的亲和常数图。
44.图31为biacore检测纳米抗体g1与omicron rbd蛋白的亲和常数图。
45.图32为biacore检测纳米抗体g1与omicron ba.2 rbd蛋白的亲和常数图。
46.图33为biacore检测纳米抗体g4与wt rbd蛋白的亲和常数图。
47.图34为biacore检测纳米抗体g4与alpha rbd蛋白的亲和常数图。
48.图35为biacore检测纳米抗体g4与beta rbd蛋白的亲和常数图。
49.图36为biacore检测纳米抗体g4与delta rbd蛋白的亲和常数图。
50.图37为biacore检测纳米抗体g4与omicron rbd蛋白的亲和常数图。
51.图38为biacore检测纳米抗体g4与omicron ba.2 rbd蛋白的亲和常数图。
52.图39为纳米抗体与ace2竞争性 elisa图。
具体实施方式
53.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
54.本技术实施例第一方面提供的一种靶向sars-cov-2的纳米抗体,纳米抗体包括纳米抗体nbf2、纳米抗体nbg4、纳米抗体nbg1、纳米抗体nbd2、纳米抗体nbe8中的至少一种,其中,纳米抗体nbf2的氨基酸序列如seq.id no.1所示,纳米抗体nbg4的氨基酸序列如seq.id no.2所示,纳米抗体nbg1的氨基酸序列如seq.id no.3所示,纳米抗体nbd2的氨基酸序列如seq.id no.4所示,纳米抗体nbe8的氨基酸序列如seq.id no.5所示。
55.本技术实施例第一方面提供的靶向sars-cov-2的纳米抗体,包括纳米抗体nbf2、纳米抗体nbg4、纳米抗体nbg1、纳米抗体nbd2、纳米抗体nbe8中的至少一种,提供的纳米抗体对新冠病毒野生株、新冠病毒变异株阿尔法(alpha)、新冠病毒贝塔(beta)、新冠病毒德尔塔(delta)、新冠病毒omicron及其亚型ba.2 的rbd结构域具有较高的亲和力,能够快速且特异性地中和不同的新冠病毒,有效抑制其活性;同时,提供的纳米抗体具有更长的cdr3序列,有利于纳米抗体进行灵活调节其构象,提高与病毒的结合作用,且制备成本较低,有利于广泛应用。
56.纳米抗体nbf2的氨基酸序列如seq.id no.1所示,seq.id no.1如下:mavqlvesggglvqaggslrlscaaagltftgyvmawfrqapgknrefvaavsrsgvvtryadsvkgrftvsrdnakgtvnlqmnslkpedtavyycaagrtyatssynrdydywgqgtqvtvss。
57.纳米抗体nbf2的碱基序列如seq.id no.17所示,seq.id no.17如下:atggcggtgcagctggtggagtctgggggaggattggtgcaggctgggggctctctgagactctcctgtgcagccgctggactcaccttcactggttatgtaatggcctggttccgccaggctccagggaagaaccgtgagtttgtagcggccgttagccggagtggtgttgttacacgctatgcagactccgtgaagggccgattcaccgtctccagagacaacgccaagggcacggtcaatttgcaaatgaacagcctgaaacctgaggacacggccgtttattactgtgcagcaggccgaacatacgctactagtagttacaaccgtgactatgactactggggccaggggacccaggtcaccgtctcctca。
58.纳米抗体nbg4的氨基酸序列如seq.id no.2所示,seq.id no.2如下:mavqlvesggglvlaggslrlscaatgltftgyvmawfrqapgknrefvaavsrsgvvtryadsvkgrftvsrdnakgtvnlqmnslkpedtavyycaagrtyatssynhdydywgqgtqvtvss。
59.纳米抗体nbg4的碱基序列如seq.id no.18所示,seq.id no.18如下:atggcggttcagctggttgaaagcggcggcggtctggttctggcgggtggtagcctgcgtctgagctgcgcggcgaccggcctgacctttaccggctatgtgatggcgtggtttcgccaagcgccgggcaaaaaccgcgaatttgtggcggcggtgagccgcagcggcgtggtgacccgctatgcggatagcgtgaaaggccgctttaccgtgagccgcgataacgcgaaaggcaccgtgaacctgcagatgaacagcctgaaaccggaagataccgcggtgtattattgcgcggcgggccgcacctatgcgacgagcagctataaccatgattatgattattggggccaaggcacccaagtgaccgtgagcagc。
60.纳米抗体nbg1的氨基酸序列如seq.id no.3所示,seq.id no.3如下:mavqlvesggglvqaggslrlscaatglaftgyvmawfrqapgknrefvaavsrsgvvtryadsvkgrftvsrdnakgtvnlqmnslkpedtavyycaagrtyatssynhdydywgqgtqvtvss。
61.纳米抗体nbg1的碱基序列如seq.id no.19所示,seq.id no.19如下:atggcggtgc
agctggtggagtctgggggaggattggtgcaggctgggggctctctgagactctcctgtgcagccactggactcgccttcactggttatgtaatggcctggttccgccaggctccagggaagaaccgtgagtttgtagcggccgttagccggagtggtgttgttacacgctatgcagactccgtgaagggccgattcaccgtctccagagacaacgccaagggcacggtcaatttgcaaatgaacagcctgaaacctgaggacacggccgtttattactgtgcagcaggccgaacatacgctactagtagttacaaccatgactatgactactggggccaggggacccaggtcaccgtctcctca。
62.纳米抗体nbd2的氨基酸序列如seq.id no.4所示,seq.id no.4如下:mavqlvesggglvqaggslrlscaatgltftgyvmawfrqapgknrefvaavsrsgvvtryadsvkgrftvsrdnakgtvnlqmnslkpedtavyycaagrtyatssynhdydywgqgtqvtvss。
63.纳米抗体nbd2的碱基序列如seq.id no.20所示,seq.id no.20如下:atggcggtgcagctggtggagtctgggggaggattggtgcaggctgggggctctctgagactctcctgtgcagccactggactcaccttcactggttatgtaatggcctggttccgccaggctccagggaagaaccgtgagtttgtagcggccgttagccggagtggtgttgttacacgctatgcagactccgtgaagggccgattcaccgtctccagagacaacgccaagggcacggtcaatttgcaaatgaacagcctgaaacctgaggacacggccgtttattactgtgcagcaggccgaacatacgctactagtagttacaaccatgactatgactactggggccaggggacccaggtcaccgtctcctca。
64.纳米抗体nbe8的氨基酸序列如seq.id no.5所示,seq.id no.5如下:mavqlvesggglvqaggslrlscaatgltftgyvmawfrqapgrnrefvaavsrsgvvtryadsvkgrftvsrdnakgtvnlqmnslkpedtavyycaagrtyatssynhdydywgqgtqvtvss。
65.纳米抗体nbe8的碱基序列如seq.id no.21所示,seq.id no.21如下:atggcggtgcagctggtggagtctgggggaggattggtgcaggctgggggctctctgagactctcctgtgcagccactggactcaccttcactggttatgtaatggcctggttccgccaggctccagggaggaaccgtgagtttgtagcggccgttagccggagtggtgttgttacacgctatgcagactccgtgaagggccgattcaccgtctccagagacaacgccaagggcacggtcaatttgcaaatgaacagcctgaaacctgaggacacggccgtttattactgtgcagcaggccgaacatacgctactagtagttacaaccatgactatgactactggggccaggggacccaggtcaccgtctcctca。
66.在一些实施例中,提供的纳米抗体包括4个框架区fr1、fr2、fr3、fr4和3个互补决定区cdr1、cdr2、cdr3;各个区域氨基酸序列的不同会影响纳米抗体与病毒的结合能力。
67.纳米抗体nbf2中,fr1的氨基酸序列如seq id no.6所示,具体为:avqlvesggglvqaggslrlscaaagltft;fr2的氨基酸序列如seq id no.7所示,具体为:wfrqapgknrefva;fr3的氨基酸序列如seq id no.8所示,具体为:rftvsrdnakgtvnlqmnslkpedtavyycaa;fr4的氨基酸序列如seq id no.9所示,具体为:wgqgtqvtvss;cdr1的氨基酸序列如seq id no.10所示,具体为:gyvma;cdr2的氨基酸序列如seq id no.11所示,具体为:avsrsgvvtryadsvkg;cdr3的氨基酸序列如seq id no.12所示,具体为:grtyatssynrdydy。
68.纳米抗体nbg4中,fr1的氨基酸序列如seq id no.13所示,具体为:avqlvesggglvlaggslrlscaatgltft;fr2的氨基酸序列如seq id no.7所示,fr3的氨基酸序列如seq id no.8所示,fr4的氨基酸序列如seq id no.9所示,cdr1的氨基酸序列如seq id no.10所示,cdr2的氨基酸序列如seq id no.11所示,cdr3的氨基酸序列如seq id no.14所示,具体为:grtyatssynhdydy;纳米抗体nbg4中,fr2、fr3、fr4、cdr1、cdr2的氨基酸序列与纳米抗体nbf2的一致。
69.纳米抗体nbg1中,fr1的氨基酸序列如seq id no.15所示,具体为:
avqlvesggglvqaggslrlscaatglaft;fr2的氨基酸序列如seq id no.7所示,fr3的氨基酸序列如seq id no.8所示,fr4的氨基酸序列如seq id no.9所示,cdr1的氨基酸序列如seq id no.10所示,cdr2的氨基酸序列如seq id no.11所示,cdr3的氨基酸序列如seq id no.14所示;纳米抗体nbg1中,fr2、fr3、fr4、cdr1、cdr2的氨基酸序列与纳米抗体nbf2的一致,cdr3的氨基酸序列与纳米抗体nbg4的一致。
70.纳米抗体nbd2中,fr1的氨基酸序列如seq id no.6所示,fr2的氨基酸序列如seq id no.7所示,fr3的氨基酸序列如seq id no.8所示,fr4的氨基酸序列如seq id no.9所示,cdr1的氨基酸序列如seq id no.10所示,cdr2的氨基酸序列如seq id no.11所示,cdr3的氨基酸序列如seq id no.14所示;纳米抗体nbd2中,fr1、fr2、fr3、fr4、cdr1、cdr2的氨基酸序列与纳米抗体nbf2的一致,cdr3的氨基酸序列与纳米抗体nbg4的一致。
71.纳米抗体nbe8中,fr1的氨基酸序列如seq id no.6所示,fr2的氨基酸序列如seq id no.16所示,具体为:wfrqapgrnrefva;fr3的氨基酸序列如seq id no.8所示,fr4的氨基酸序列如seq id no.9所示,cdr1的氨基酸序列如seq id no.10所示,cdr2的氨基酸序列如seq id no.11所示,cdr3的氨基酸序列如seq id no.14所示;纳米抗体nbe8中,fr1、fr3、fr4、cdr1、cdr2的氨基酸序列与纳米抗体nbf2的一致,cdr3的氨基酸序列与纳米抗体nbg4的一致。
72.本技术实施例第二方面提供了一种靶向sars-cov-2的纳米抗体的制备方法,包括如下步骤:s01. 提供目的蛋白,将目的蛋白包被在免疫管上进行富集筛选,得到噬菌体文库;s02. 在噬菌体文库中选取克隆子进行验证,得到阳性克隆子;s03. 将阳性克隆子进行测序并根据测序结果合成纳米抗体的基因序列;s04. 将纳米抗体的基因序列克隆至表达载体中得到重组质粒,将重组质粒转入宿主细胞中诱导表达并进行纯化,得到靶向sars-cov-2的纳米抗体。
73.本技术实施例第二方面提供的一种靶向sars-cov-2的纳米抗体的制备方法,该制备方法基于噬菌体展示筛选技术,以sars-cov-2的变异株奥密克戎(omicron) rbd蛋白为靶标构建了纳米抗体库以筛选阳性克隆子,并进行测序、克隆、表达、纯化,得到靶向sars-cov-2的纳米抗体;该制备方法利用噬菌体在宿主菌中快速复制的生物特性,能够快速、高通量地筛选与特定变异株奥密克戎(omicron)的棘突蛋白rbd结构域结合的纳米抗体,制备方法快速、简便,有利于大量筛选,提高了筛选效率。
74.步骤s01中,提供目的蛋白,将目的蛋白包被在免疫管上进行富集筛选,得到噬菌体文库。
75.在一些实施例中,提供的目的蛋白为变异株奥密克戎(omicron)的棘突蛋白rbd结构域,并且提供的目的蛋白的浓度为10~12 μg/ml。在具体实施例中,将目的蛋白按10 μg/ml的浓度包被在免疫管上。
76.在一些实施例中,富集筛选的步骤中,进行2~3轮富集筛选。经过多轮富集,确保得到的文库容量大,更有利于进行阳性克隆子的筛选。
77.步骤s02中,在噬菌体文库中选取克隆子进行验证,得到阳性克隆子。
78.在一些实施例中,在噬菌体文库中选取克隆子进行验证的步骤中,采用酶联免疫
吸附剂测定法进行验证,其中,验证的阳性标准为酶联免疫吸附剂测定的数值大于对应牛血清白蛋白的数值3倍且数值大于0.5。
79.进一步的,对选取的克隆子进行2次噬菌体elisa鉴定,鉴定结构均符合验证的阳性标准的,确定为得到的阳性克隆子。
80.步骤s03中,将阳性克隆子进行测序并根据测序结果合成纳米抗体的基因序列。
81.步骤s04中,将纳米抗体的基因序列克隆至表达载体中得到重组质粒,将重组质粒转入宿主细胞中诱导表达并进行纯化,得到靶向sars-cov-2的纳米抗体。
82.在一些实施例中,表达载体选自pcoldii载体,将纳米抗体的基因序列克隆至pcoldii载体中得到重组质粒;进一步的,在克隆过程中同时融合表达血凝素标签(hemagglutinin ha tag)用于后续检测。
83.在一些实施例中,宿主细胞选自大肠杆菌,将重组质粒转入大肠杆菌细胞中诱导表达并进行纯化。
84.在一些实施例中,将重组质粒转入大肠杆菌细胞中诱导表达并进行纯化,步骤如下:(1)使用0.2mm浓度的iptg在16℃低温进行诱导表达,能够防止形成包涵体和蛋白降解;(2)根据预实验诱导条件进行大量诱导表达,高压破菌仪工作条件1000 w进行破菌;(3)于转速为17000 g,4℃离心30 min,取上清与ni填料4℃共孵育1小时,再进行洗脱纯化;(4)ni柱纯化后进行分子筛分离,akata参数设置0.5 ml流速/分钟,每1 ml收集一次,得到靶向sars-cov-2的纳米抗体。
85.本技术实施例第三方面提供靶向sars-cov-2的纳米抗体在制备预防和/或治疗新型冠状病毒肺炎的药物中的应用。
86.本技术实施例第三方面提供的靶向sars-cov-2的纳米抗体在制备预防和/或治疗新型冠状病毒肺炎的药物中的应用,由于筛选得到的靶向sars-cov-2的纳米抗体包括纳米抗体nbf2、纳米抗体nbg4、纳米抗体nbg1、纳米抗体nbd2、纳米抗体nbe8中的至少一种,对新冠病毒野生株及各变异株的病毒具有较好的中和活性能力和抑制活性能力,适用于制备预防和/或治疗新型冠状病毒肺炎的相关药物。
87.本技术实施例第四方面提供靶向sars-cov-2的纳米抗体在制备检测新型冠状病毒的检测试剂或检测试剂盒中的应用本技术实施例第四方面提供的靶向sars-cov-2的纳米抗体在制备检测新型冠状病毒的检测试剂或检测试剂盒中的应用,提供的靶向sars-cov-2的纳米抗体包括纳米抗体nbf2、纳米抗体nbg4、纳米抗体nbg1、纳米抗体nbd2、纳米抗体nbe8中的至少一种,对新冠病毒野生株及各变异株的病毒具有较高得结合能力,适用于制备检测新型冠状病毒的检测试剂或检测试剂盒。
88.下面结合具体实施例进行说明。
89.实施例1(一)靶向sars-cov-2的纳米抗体及其制备方法试验步骤:(1)将目的蛋白omicron rbd按10 μg/ml浓度包被在免疫管上,进行3轮富集筛选;(2)使用第三轮噬菌体洗脱液铺板,随机挑取96个单克隆进行elisa验证,以elisa读数大于对应bsa读数3倍且读数大于0.5为阳性标准;(3)经过2次噬菌体elisa鉴定的阳性单克隆送
公司测序确定序列信息;(4)根据测序信息设计并合成筛选到的纳米抗体,将纳米抗体基因序列克隆入pcoldii载体,同时融合表达血凝素标签(hemagglutinin ha tag),得到重组质粒;(5)将重组质粒转入大肠杆菌细胞中进行表达,用0.2mm浓度的iptg在16℃低温进行诱导;(6)根据预实验诱导条件进行大量诱导表达,高压破菌仪工作条件1000 w进行破菌;(7)于转速17000 g,4℃离心30 min,取上清与ni填料4℃共孵育1小时;(8)ni柱纯化后进行分子筛分离,akata参数设置0.5 ml流速/分钟,每1 ml收集一次,得到靶向sars-cov-2的纳米抗体。
90.结果分析:omicron rbd纳米抗体的筛选鉴定对omicron rbd进行了噬菌体纳米抗体文库的筛选,三轮筛选之后,如图1所示,文库富集将近3000倍。从第三轮所得文库挑取约200个克隆进行两次噬菌体elisa作初步验证,如图2所示,初步鉴定出10个阳性克隆,分别为nba7、nba11、nbb3、nbc3、nbd2、nbe5、nbe8、nbf2、nbg1、nbg4。
91.进一步进行表达纯化这10个纳米抗体,纯化得到的10个纳米抗体的蛋白结果如图3所示,并用anti-ha免疫印迹(western blot,wb)检测证实蛋白的正确性,如图4所示,筛选得到的10个克隆子均表达正确。
92.(二)elisa初步鉴定纳米抗体与sars-cov-2各变异株rbd结合试验步骤:将ha标签融合到纳米抗体基因编码序列里,表达具有ha标签的10个纳米抗体nba7、nba11、nbb3、nbc3、nbd2、nbe5、nbe8、nbf2、nbg1、nbg4;分别用elisa板包被omicron rbd蛋白,封闭,之后加入各种浓度的纳米抗体在室温孵育1小时,pbs漂洗3次,anti-ha抗体室温孵育1小时后,辣根过氧化物酶标记的抗ha抗体放大信号,tmb显色,同时做无关纳米抗体的对照和无关蛋白抗原的空白对照。
93.结果分析:将上步纯化表达验证正确的10个纳米抗体与sars-cov-2 wt、delta (b.1.617.2)、omicron (b.1.1.529) rbd蛋白和阴性对照蛋白牛血清白蛋白(bovine serum albumin,bsa)进行elisa验证。
94.与omicron rbd蛋白结合的分析结果如图5所示,可以看出,其中,nb d2、nbe8、nbf2、nbg1和nbg4五条纳米抗体与omicron rbd显示结合活性。
95.与sars-cov-2 野生株(wild type,wt) rbd蛋白结合的分析结果如图6所示,可以看出,其中,nb d2、nbe8、nbf2、nbg1和nbg4五条纳米抗体与sars-cov-2 野生株(wild type,wt) rbd显示结合活性。
96.与delta rbd蛋白结合的分析结果如图7所示,可以看出,其中,nb d2、nbe8、nbf2、nbg1和nbg4五条纳米抗体与delta rbd显示结合活性。
97.与阴性对照蛋白牛血清白蛋白结合的分析结果如图8所示,可以看出,其中,10个纳米抗体与bsa蛋白的结合,发现均无结合活性。
98.因此,可以确认了5个阳性纳米抗体nb d2、nbe8、nbf2、nbg1和nbg4与sars-cov-2各变异株rbd具有结合活性,而与阴性对照蛋白bsa无结合(三)5个阳性纳米抗体与sars-cov-2 各变异株rbd蛋白的亲和力
试验步骤:提供5个阳性纳米抗体nb d2、nbe8、nbf2、nbg1和nbg4(各附图中,5个阳性纳米抗体分别简称为:d2、e8、f2、g1和g4),基于分子互相作用分析平台biacore,分析检测纳米抗体与sars-cov-2 各变异株(wt、alpha、beta、delta、omicron和omicron ba.2) rbd蛋白的亲和力。
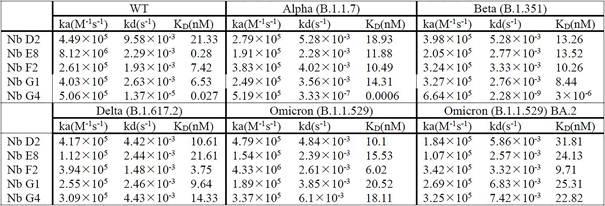
99.结果分析:5个阳性纳米抗体nb d2、nbe8、nbf2、nbg1和nbg4分别与sars-cov-2 各变异株(wt、alpha、beta、delta、omicron和omicron ba.2) rbd蛋白的亲和力如表1所示,可以看出,亲和力均在纳摩尔水平,具有较高的亲和力。
100.表1(四)5个阳性纳米抗体与表面等离子共振(surface plasmon resonance,spr)分析试验步骤:实验用来验证在体外表达纯化的纳米抗体与体外纯化的抗原蛋白直接相互作用,并计算二者的平衡常数。在 biacore s200上运行多循环动力学以研究纳米抗体和omicron rbd蛋白的结合动力学。提供5个阳性纳米抗体nb d2、nbe8、nbf2、nbg1和nbg4,分别在运行温度25℃下,新冠冠野生株(wt)、变异株阿尔法(alpha)、贝塔(beta)、德尔塔(delta)和奥密克戎(omicron)及其亚型ba.2 rbd蛋白被固定在cm5 series s 传感器芯片表面,倍比稀释的纳米抗体以 30 μl/分钟的速度流过芯片表面,持续 120秒,然后是 240秒的解离,制作动力学曲线,计算各相关参数。
101.结果分析:(1) nb d2纳米抗体表面等离子共振(surface plasmon resonance,spr)分析spr结果显示nb d2纳米抗体与sars-cov-2 各变异株(wt、alpha、beta、delta、omicron和omicron ba.2) rbd蛋白均有结合,如图9所示,nb d2与wt rbd蛋白的亲和力为21.33 nm;如图10所示,nb d2与alpha rbd蛋白的亲和力为18.93 nm;如图11所示,nb d2与beta rbd蛋白的亲和力为13.26 nm;如图12所示,nb d2与delta rbd蛋白的亲和力为10.61 nm;如图13所示,nb d2与omicron rbd蛋白的亲和力为10.1 nm;如图14所示,nb d2与omicron ba.2 rbd蛋白的亲和力为31.81 nm。
102.(2)nb e8纳米抗体表面等离子共振(surface plasmon resonance,spr)分析spr结果显示nb e8纳米抗体与sars-cov-2 各变异株(wt、alpha、beta、delta、omicron和omicron ba.2) rbd蛋白均有结合,如图15所示,nb e8与wt rbd蛋白的亲和力为
0.28 nm;如图16所示,nb e8与alpha rbd蛋白的亲和力为11.88 nm;如图17所示,nb e8与beta rbd蛋白的亲和力为13.52 nm;如图18所示,nb e8与delta rbd蛋白的亲和力为21.61 nm;如图19所示,nb e8与omicron rbd蛋白的亲和力为15.53 nm;如图20所示,nb e8与omicron ba.2 rbd蛋白的亲和力为24.13 nm。
103.(3)nb f2纳米抗体表面等离子共振(surface plasmon resonance,spr)分析spr结果显示nb f2纳米抗体与sars-cov-2 各变异株(wt、alpha、beta、delta、omicron和omicron ba.2) rbd蛋白均有结合,如图21所示,nb f2与wt rbd蛋白的亲和力为7.42 nm;如图22所示,nb f2与alpha rbd蛋白的亲和力为10.49 nm;如图23所示,nb f2与beta rbd蛋白的亲和力为10.26 nm;如图24所示,nb f2与delta rbd蛋白的亲和力为3.75 nm;如图25所示,nb f2与omicron rbd蛋白的亲和力为6.02 nm;如图26所示,nb f2与omicron ba.2 rbd蛋白的亲和力为9.71 nm。
104.(4)nb g1纳米抗体表面等离子共振(surface plasmon resonance,spr)分析spr结果显示nb g1纳米抗体与sars-cov-2 各变异株(wt、alpha、beta、delta、omicron和omicron ba.2) rbd蛋白均有结合,如图27所示,nb g1与wt rbd蛋白的亲和力为6.53 nm;如图28所示,nb g1与alpha rbd蛋白的亲和力为14.31 nm;如图29所示,nb g1与beta rbd蛋白的亲和力为8.44 nm;如图30所示,nb g1与delta rbd蛋白的亲和力为9.64 nm;如图31所示,nb g1与omicron rbd蛋白的亲和力为20.52 nm;如图32所示,nb g1与omicron ba.2 rbd蛋白的亲和力为25.31 nm。
105.(5)nb g4纳米抗体表面等离子共振(surface plasmon resonance,spr)分析spr结果显示nb g4纳米抗体与sars-cov-2 各变异株(wt、alpha、beta、delta、omicron和omicron ba.2) rbd蛋白均有结合,如图33所示,nb g4与wt rbd蛋白的亲和力为27.15 pm;如图34所示,nb g4与alpha rbd蛋白的亲和力为0.64 pm;如图35所示,nb g4与beta rbd蛋白的亲和力为0.003 pm;如图36所示,nb g4与delta rbd蛋白的亲和力为14.33 nm;如图37所示,nb g4与omicron rbd蛋白的亲和力为18.11 nm;如图38所示,nb g4与omicron ba.2 rbd蛋白的亲和力为22.82 nm。
106.(五)5个阳性纳米抗体与ace2竞争性 elisa实验试验步骤:根据spr结果,选择亲和力较好的纳米抗体进行竞争性 elisa实验验证。将omicron rbd蛋白以0.5μg/ml的浓度包被在elisa板上4℃过夜。次日用pbs清洗一次,用3%的bsa进行室温封闭2小时。根据ace2的最低饱和浓度进行纳米抗体倍比稀释,即稀释液为含0.5μg/ml ace2的0.1%pbst溶液,室温孵育2.5小时。0.1%pbst漂洗。
107.结果分析:检测了这5个纳米抗体是否与ace2竞争结合omicron rbd蛋白,用含ace2最低饱和浓度的0.1%pbst溶液进行纳米抗体稀释,与提前包被有omicron rbd蛋白的elisa板室温孵育2.5小时。0.1%pbst漂洗3次,用anti-ace2抗体检测ace2的含量,同时做无纳米抗体和无ace2蛋白的空白对照。如图39所示,结果显示nb f2可明显竞争性抑制ace2与omicron rbd蛋白的结合,半抑制浓度(half maximum inhibitory concentration,ic50) 为0.06 μm。
108.因此,提供的纳米抗体nbf2、纳米抗体nbg4、纳米抗体nbg1、纳米抗体nbd2、纳米抗体nbe8对新冠病毒野生株、新冠病毒变异株阿尔法(alpha)、新冠病毒贝塔(beta)、新冠病
毒德尔塔(delta)、新冠病毒omicron及其亚型ba.2 的rbd结构域具有较高的亲和力,能够快速且特异性地中和不同的新冠病毒,有效抑制其活性;同时,提供的纳米抗体具有更长的cdr3序列,有利于纳米抗体进行灵活调节其构象,提高与病毒的结合作用,且制备成本较低,有利于广泛应用。
109.以上所揭露的仅为本发明较佳实施例而已,当然不能以此来限定本发明之权利范围,因此依本发明权利要求所作的等同变化,仍属本发明所涵盖的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1