舒更葡糖钠有关物质及基于其的舒更葡糖钠或其游离酸纯度检测方法与流程
1.本发明涉及舒更葡糖钠杂质分析技术领域,尤其是舒更葡糖钠有关物质及基于其的舒更葡糖钠或其游离酸纯度检测方法。
背景技术:
2.舒更葡糖钠(sugammadex sodium),化学名为6a,6b,6c,6d,6e,6f,6g,6
h-八联-s-(2-羧乙基)-6a,6b,6c,6d,6e,6f,6g,6
h-八硫代-γ-环糊精八钠盐(1:8),结构式如下式(1):
[0003][0004]
舒更葡糖钠发挥作用在于其γ-环糊精的分子结构,它是20年来开发成功的首个也是唯一的选择性肌肉松弛拮抗剂,可以与罗库溴铵形成复合物,降低血液中游离的药物浓度,从而逆转罗库溴铵的神经肌肉阻滞作用,且副作用较小。
[0005]
舒更葡糖钠或其游离酸有关物质是指舒更葡糖钠在生产过程中带入的起始原料、中间体、聚合物、副反应产物以及贮藏过程中的降解产物等。目前,国内外尚未有文献报道采用高效液相法能将舒更葡糖钠或其游离酸中共洗脱组分达到有效的分离,本发明主要研究共洗脱组分有rrt0.35a、rrt0.35b、rrt1.44a、rrt1.44b、rrt1.59a与rrt1.59b。
[0006]
舒更葡糖钠或其游离酸有关物质的存在直接关系到药品的质量和安全性,需要进行结构确证、来源分析、杂质限定确认和纯度检测等,其前提是获得舒更葡糖钠有关物质,以及含有该有关物质的舒更葡糖钠或其游离酸。因此,合成舒更葡糖钠有关物质,以及含有该有关物质的舒更葡糖钠或其游离酸并进行纯度检测,对舒更葡糖钠中间体、原料药及其制剂的质量控制具有重要的意义。
[0007]
舒更葡糖钠有关物质,以及含有该有关物质的舒更葡糖钠或其游离酸的结构信息及其来源参见下表1。
[0008]
[0009]
[0010][0011]
表1
[0012]
现有技术中,舒更葡糖钠中含有的杂质(rrt0.35a与rrt0.35b、rrt1.44a与rrt1.44b、rrt1.59a与rrt1.59b)相互之间不能实现基线分离,无法进行准确定量。杂质之间的分离度不符合ich q3a中对于有关物质方法学验证项下对专属性的要求,即杂质之间的分离度小于1.5。
[0013]
现有技术尚未披露能够分离rrt0.35a、rrt0.35b、rrt1.44a、rrt1.44b、rrt1.59a、rrt1.59b这些杂质的定量、定性检测方法。总而言之,现有技术得到的舒更葡糖钠检测结果并不能真实反应药物质量。
技术实现要素:
[0014]
为更好地进行舒更葡糖钠的质量控制,本发明提供舒更葡糖钠有关物质及基于其的舒更葡糖钠或其游离酸纯度检测方法,包括含有舒更葡糖钠或其游离酸的药物为固体/液体组合物的纯度检测,固体/液体组合物指的是包含舒更葡糖钠或其游离酸的原料药以及一种或多种药学上可接受的赋形剂或溶剂。
[0015]
本发明提供的舒更葡糖钠有关物质包括杂质rrt0.35a、rrt0.35b、rrt1.44a、rrt1.44b、rrt1.59a、rrt1.59b中的一种或多种;
[0016]
rrt0.35a具有以下结构:
[0017][0018]
rrt0.35b具有以下结构:
[0019][0020]
rrt1.44a具有以下结构:
[0021]
[0022]
rrt1.44b具有以下结构:
[0023][0024]
rrt1.59a具有以下结构:
[0025][0026]
rrt1.59b具有以下结构:
[0027][0028]
下面对上述六种杂质的产生途径进行分析。
[0029]
1、杂质rrt0.35a的产生途径如下:
[0030][0031]
反应溶剂dmf在碱性加热条件下分解形成游离的二甲胺,二甲胺可能在反应过程中与单碘代杂质(中间体碘代伽马环糊精未完全反应形成)的碘基发生取代反应,产生叔胺基化合物杂质rrt0.35a。
[0032]
2、杂质rrt0.35b的产生途径如下:
[0033][0034]
舒更葡糖钠侧链上的硫醚易被氧化降解,生成具有相近亚砜结构的两种非对映异
构体杂质;这两种杂质在光照条件下继续被氧化,生成光降解杂质rrt0.35b。
[0035]
3、杂质rrt1.44a的产生途径如下:
[0036][0037]
单羟基舒更葡糖钠的单个侧链断裂,形成单巯基单羟基舒更葡糖钠;在有氧气参与反应时,单巯基杂质上的巯基与相邻糖环6位羟基,加热条件下可能发生脱水反应,形成跨相邻两个糖环的硫醚键,生成杂质rrt1.44a。
[0038]
4、杂质rrt1.44b的产生途径如下:
[0039][0040]
中间体碘代环糊精中的杂质七碘代伽马环糊精,未被碘代的葡萄糖单元上,在反应生成的氢碘酸催化下发生pinnacle重排,使得己糖环缩环,6-位羟甲基在重排同时脱水形成丙环并环,从而生成杂质rrt1.44b。
[0041]
5、杂质rrt1.59a的产生途径如下:
[0042][0043]
起始物料3-巯基丙酸中若含有2-巯基丙酸,可能会在合成过程中,与单碘代舒更葡糖钠反应,产生杂质rrt1.59a。
[0044]
6、杂质rrt1.59b的产生途径如下:
[0045][0046]
单碘代舒更葡糖钠中的碘基在碱性加热条件下,可能发生e2消除反应,失去一分子的hi,生成具有烯键结构的杂质rrt1.59b。
[0047]
通过上述六种杂质的产生途径可以看出,均为舒更葡糖钠及其游离酸合成过程中的副产物或降解杂质,因此,适用于作为参比标准或对照品,用于舒更葡糖钠及其游离酸的质量控制。
[0048]
也就是说,本发明可以提供一种舒更葡糖钠或其游离酸样品纯度检测方法,通过hplc分析来测定样品中杂质rrt0.35a、rrt0.35b、rrt1.44a、rrt1.44b、rrt1.59a、rrt1.59b中的一种或多种的存在,再与参照参比标准溶液中或对照品溶液存在的已知杂质rrt0.35a、rrt0.35b、rrt1.44a、rrt1.44b、rrt1.59a、rrt1.59b中的一种或多种进行对比,进而判定舒更葡糖钠或其游离酸样品纯度检测。
[0049]
以上为六种杂质在舒更葡糖钠及其游离酸合成过程中的产生途径。为了便于试验,需从舒更葡糖钠粗品中提取出上述杂质,下面对具体提取过程进行介绍。
[0050]
杂质rrt0.35a的制备:取舒更葡糖钠粗品进行柱层析纯化,固定相为adme,洗脱溶剂为磷酸二氢钠-水-乙腈体系,洗脱比例为磷酸二氢钠水溶液:乙腈=83:20;弃前洗脱液10ml,收集后洗脱液10ml,或脱盐,真空浓缩干燥,得杂质rrt0.35a。
[0051]
杂质rrt0.35b的制备:取舒更葡糖钠粗品进行柱层析纯化,固定相为adme,洗脱溶剂为磷酸二氢钠-水-乙腈体系;洗脱比例为磷酸二氢钠水溶液:乙腈=83:20,收集洗脱液15ml,或脱盐,真空浓缩干燥,得杂质rrt0.35b。
[0052]
杂质rrt1.44a的制备:取舒更葡糖钠粗品进行柱层析纯化,固定相为adme,洗脱溶剂为磷酸二氢钠-水-乙腈体系,洗脱比例为磷酸二氢钠水-乙腈溶液:乙腈=10:90,磷酸二氢钠水-乙腈溶液中磷酸二氢钠水溶液:乙腈=83:20,弃前洗脱液30ml,收集后洗脱液15ml,或脱盐,真空浓缩干燥,得杂质rrt1.44a。
[0053]
杂质rrt1.44b的制备:取舒更葡糖钠粗品进行柱层析纯化,固定相为adme,洗脱溶剂为磷酸二氢钠-水-乙腈体系,洗脱比例为磷酸二氢钠水-乙腈溶液:乙腈=10:90,磷酸二氢钠水-乙腈溶液中磷酸二氢钠水溶液:乙腈=83:20,弃前洗脱液20ml,收集后洗脱液10ml,或脱盐,真空浓缩干燥,得杂质rrt1.44b。
[0054]
杂质rrt1.59a的制备:取舒更葡糖钠粗品进行柱层析纯化,固定相为adme,洗脱溶剂为磷酸二氢钠-水-乙腈体系,洗脱比例为磷酸二氢钠水-乙腈溶液:乙腈=1:99,磷酸二氢钠水-乙腈溶液中磷酸二氢钠水溶液:乙腈=83:20,弃前洗脱液45ml,收集后洗脱液15ml,或脱盐,真空浓缩干燥,得杂质rrt1.59a。
[0055]
杂质rrt1.59b的制备:取舒更葡糖钠粗品进行柱层析纯化,固定相为adme,洗脱溶剂为磷酸二氢钠-水-乙腈体系,洗脱比例为磷酸二氢钠水-乙腈溶液:乙腈=1:99,磷酸二
氢钠水-乙腈溶液中磷酸二氢钠水溶液:乙腈=83:20,弃前洗脱液30ml,收集后洗脱液15ml,或脱盐,真空浓缩干燥,得杂质rrt1.59b。
[0056]
为表征上述六种杂质rrt0.35a、rrt0.35b、rrt1.44a、rrt1.59a、rrt1.59b,对其进行hplc分析,包括以下步骤:
[0057]
步骤1,制备1mg/ml~10mg/ml舒更葡糖钠样品溶液;
[0058]
步骤2,利用杂质rrt0.35a、rrt0.35b、rrt1.44a、rrt1.44b、rrt1.59a、rrt1.59b中的任意一种或多种制备0.5μg/ml~50μg/ml参比标准溶液/对照品溶液;
[0059]
步骤3,对样品溶液和参比标准溶液/对照品溶液进行hplc分析,色谱柱采用以有机硅聚合物包膜硅基材键合金刚烷基的adme柱,流动相a为0.01~0.10mol/l(优选0.025mol/l)、ph 2~4(优选ph=3.0)的磷酸二氢钠水溶液/乙酸-乙酸铵水溶液/甲酸水溶液/甲酸-甲酸铵水溶液/醋酸-醋酸钠水溶液:乙腈=70~95:5~30(优选83:20),流动相b为乙腈,梯度洗脱时间与流动相比例如下:
[0060]
时间(min)流动相a(%)流动相b(%)0100021100035982509285575256050506530708030708510001051000
[0061]
色谱柱柱温35~45℃,优选40℃;四元泵流速0.15ml/min~0.35ml/min,优选0.27ml/min;紫外检测器检测波长190~210nm,优选200nm;
[0062]
步骤4,对比样品溶液和参比标准溶液/对照品溶液的典型色谱图,得出舒更葡糖钠或其游离酸纯度。
[0063]
优选的,adme柱用两根色谱柱串联,在四元泵与进样器之间的流路中串联鬼峰捕集小柱;鬼峰捕集柱型号(2mm~5mm)
×
(100mm~300mm),填料粒径1~5μm,其中填充材料与adme柱一致或极性相当。
[0064]
本发明有益效果:1、提供可以用于进行舒更葡糖钠定性、定量分析的六种舒更葡糖钠有关物质;2、色谱柱采用以有机硅聚合物包膜硅基材键合金刚烷基的adme柱,较以往c18官能团建合为主的传统反相保留机理色谱柱相比,adme柱既保持了疏水性又提高了表面极性,可以很好地分离舒更葡糖钠有关物质,不仅分离效果显著,实用性强,对仪器要求低,仪器损耗小,成本低廉,并且操作方便,分离基线平稳,灵敏度高,分析结果可靠,具有广泛的应用前景。
附图说明
[0065]
图1为杂质rrt0.35a 1h-nmr图;
[0066]
图2为杂质rrt0.35a 13c-nmr图;
[0067]
图3为杂质rrt0.35ams图;
[0068]
图4为杂质rrt0.35b 1h-nmr图;
[0069]
图5为杂质rrt0.35b 13c-nmr图;
[0070]
图6为杂质rrt0.35b ms图(1/2);
[0071]
图7为杂质rrt0.35b ms图(2/2);
[0072]
图8为杂质rrt1.44a 1h-nmr图;
[0073]
图9为杂质rrt1.44a 13c-nmr图;
[0074]
图10为杂质rrt1.44a ms图(1/2);
[0075]
图11为杂质rrt1.44a ms图(2/2);
[0076]
图12为杂质rrt1.59b 1h-nmr图;
[0077]
图13为杂质rrt1.59b 13c-nmr图;
[0078]
图14为杂质rrt1.59b ms图;
[0079]
图15为杂质rrt1.59a 1h-nmr图;
[0080]
图16为杂质rrt1.59a 13c-nmr图;
[0081]
图17为杂质rrt1.59a ms图;
[0082]
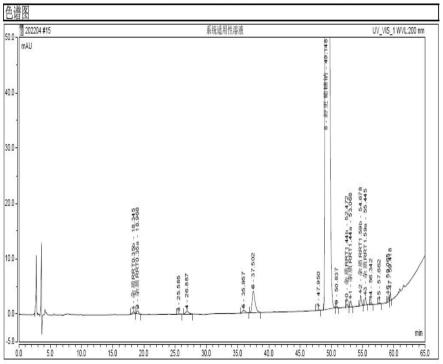
图18为系统适用性溶液典型色谱图;
[0083]
图19为rrt0.35b、rrt0.35a、舒更葡糖钠、rrt1.44b、rrt1.44a、rrt1.59b、rrt1.59a的混合对照品典型色谱图(紫外);
[0084]
图20为rrt0.35b、rrt0.35a、舒更葡糖钠、rrt1.44b、rrt1.44a、rrt1.59b、rrt1.59a的混合对照品典型色谱图(cad);
[0085]
图21为rrt0.35b、rrt0.35a、舒更葡糖钠、rrt1.44b、rrt1.44a、rrt1.59b、rrt1.59a的混合对照品典型色谱图(elsd)。
具体实施方式
[0086]
下面结合附图和具体实施方式对本发明作进一步详细的说明。本发明的实施例是为了示例和描述起见而给出的,而并不是无遗漏的或者将本发明限于所公开的形式。很多修改和变化对于本领域的普通技术人员而言是显而易见的。选择和描述实施例是为了更好说明本发明的原理和实际应用,并且使本领域的普通技术人员能够理解本发明从而设计适于特定用途的带有各种修改的各种实施例。
[0087]
实施例1舒更葡糖钠有关杂质的制备
[0088]
1、原材料如下:
[0089]
⑴
乙腈:hplc级别,由simark公司提供,批号lot:s62105ac01h,含量≥99.9%;
[0090]
⑵
二水合磷酸二氢钠:ar级别,由国药集团化学试剂有限公司提供,批号lot:20210806;
[0091]
⑶
磷酸:ar级别,由成都市科隆化学品有限公司提供,批号lot:2021110801,含量≥85.0%;
[0092]
⑷
舒更葡糖钠:由合肥博思科创医药科技有限公司提供,批号分别为:a003-22001、a003-22002、a003-22003,含量分别为98.8%、99.1%、99.5%。
[0093]
2、舒更葡糖钠粗品制备:
[0094]
⑴
向10l反应釜中加入2.1kg dmso,搅拌下加入3-巯基丙酸300g;
[0095]
⑵
将600g碘代环糊精溶于4.8kg dmso中,235g氢氧化钠溶于500g水中待用;
[0096]
⑶
氮气保护下,向反应釜中缓缓滴加氢氧化钠水溶液,滴毕在10-20℃温度下滴加溶解有碘代环糊精的dmso溶液,滴毕升温反应14-16h;
[0097]
⑷
反应结束降温至10-30℃,缓缓向反应釜中加入3kg无水甲醇进行淬灭反应,离心收集固料,即得舒更葡糖钠粗品。
[0098]
3、杂质rrt0.35a对照品的制备:取舒更葡糖钠粗品进行柱层析纯化,固定相为adme,洗脱溶剂为磷酸二氢钠-水-乙腈体系,洗脱比例为磷酸二氢钠水溶液:乙腈=83:20;弃前洗脱液10ml,收集后洗脱液10ml,或脱盐,真空浓缩干燥,得杂质rrt0.35a。
[0099]
批号lot:0.35a-20201116,含量99.82%。
[0100]1h-nmr(500m hz,dmso)核磁如图1所示,
13
c-nmr(500m hz,dmso)核磁如图2所示。高分辨质谱显示其分子离子峰m/z=1940.4552[m+h]
+
,结果与理论计算相符,具体如图3所示。
[0101]
4、杂质rrt0.35b对照品的制备:取舒更葡糖钠粗品进行柱层析纯化,固定相为adme,洗脱溶剂为磷酸二氢钠-水-乙腈体系;洗脱比例为磷酸二氢钠水溶液:乙腈=83:20,收集洗脱液15ml,或脱盐,真空浓缩干燥,得杂质rrt0.35b。
[0102]
批号lot:sug-b-20210617,含量98.9%。
[0103]1h-nmr(400m hz,dmso)核磁如图4所示,
13
c-nmr(400m hz,dmso)核磁如图5所示。高分辨质谱显示其分子离子峰m/z=1015.1910[m+h]
+
,结果与理论计算相符,具体如图6-7所示。
[0104]
5、杂质rrt1.44a对照品的制备:取舒更葡糖钠粗品进行柱层析纯化,固定相为adme,洗脱溶剂为磷酸二氢钠-水-乙腈体系,洗脱比例为磷酸二氢钠水-乙腈溶液:乙腈=10:90,磷酸二氢钠水-乙腈溶液中磷酸二氢钠水溶液:乙腈=83:20,弃前洗脱液30ml,收集后洗脱液15ml,或脱盐,真空浓缩干燥,得杂质rrt1.44a。
[0105]
批号lot:sg-rrt1.44-20190718,含量97.47%。
[0106]1h-nmr(500m hz,dmso)核磁如图8所示,
13
c-nmr(500m hz,dmso)核磁如图9所示。高分辨质谱显示其分子离子峰m/z=1846.3678[m+na]
+
,结果与理论计算相符,具体如图10-11所示。
[0107]
6、杂质rrt1.44b对照品的制备:取舒更葡糖钠粗品进行柱层析纯化,固定相为adme,洗脱溶剂为磷酸二氢钠-水-乙腈体系,洗脱比例为磷酸二氢钠水-乙腈溶液:乙腈=10:90,磷酸二氢钠水-乙腈溶液中磷酸二氢钠水溶液:乙腈=83:20,弃前洗脱液20ml,收集后洗脱液10ml,或脱盐,真空浓缩干燥,得杂质rrt1.44b。
[0108]
7、杂质rrt1.59b对照品的制备:取舒更葡糖钠粗品进行柱层析纯化,固定相为adme,洗脱溶剂为磷酸二氢钠-水-乙腈体系,洗脱比例为磷酸二氢钠水-乙腈溶液:乙腈=1:99,磷酸二氢钠水-乙腈溶液中磷酸二氢钠水溶液:乙腈=83:20,弃前洗脱液30ml,收集后洗脱液15ml,或脱盐,真空浓缩干燥,得杂质rrt1.59b。
[0109]
批号lot:sg-1.59-20190130,含量99.12%。
[0110]1h-nmr(500m hz,dmso)核磁如图12所示,
13
c-nmr(500m hz,dmso)核磁如图13所
示。高分辨质谱显示其分子离子峰m/z=1894.39018[m+h]
+
,结果与理论计算相符,具体如图14所示。
[0111]
8、杂质rrt1.59a对照品的制备:取舒更葡糖钠粗品进行柱层析纯化,固定相为adme,洗脱溶剂为磷酸二氢钠-水-乙腈体系,洗脱比例为磷酸二氢钠水-乙腈溶液:乙腈=1:99,磷酸二氢钠水-乙腈溶液中磷酸二氢钠水溶液:乙腈=83:20,弃前洗脱液45ml,收集后洗脱液15ml,或脱盐,真空浓缩干燥,得杂质rrt1.59a。
[0112]
批号lot:sg-1.59a-20190325,含量96.95%。
[0113]1h-nmr(500m hz,dmso)核磁如图15所示,
13
c-nmr(500m hz,dmso)核磁如图16所示。高分辨质谱显示其分子离子峰m/z=2001.41841[m+h]
+
,结果与理论计算相符,具体如图17所示。
[0114]
9、舒更葡糖钠供试品:由合肥博思科创医药科技有限公司提供,批号lot:ws20001-2,含量91.8%。
[0115]
10、系统适用性溶液制备:配制成每1ml中约含杂质rrt0.35a、rrt0.35b、rrt1.44a、rrt1.44b、rrt1.59a、rrt1.59b对照品各5μg、舒更葡糖钠供试品5mg的溶液。
[0116]
11、混合对照品溶液制备:
[0117]
混合对照品贮备液
①
:精密称定rrt0.35b对照品、rrt0.35a对照品、舒更葡糖钠供试品、rrt1.44a对照品、rrt1.59b对照品、rrt1.59a对照品各2mg置入20ml量瓶中,加溶剂1(0.05mol/l磷酸二氢钠溶液(ph3.0):乙腈=1:1)使溶解并稀释至刻度,摇匀,即得。
[0118]
混合对照品溶液:精密移取混合对照品贮备液
①
1ml置20ml量瓶中,并用溶剂2稀释至刻度,摇匀,即得。
[0119]
实施例2样品检测
[0120]
1、仪器与hplc色谱条件如下:
[0121]
⑴
高效液相色谱仪(赛默飞u3000);
[0122]
⑵
紫外检测器、cad检测器或elsd检测器;
[0123]
⑶
万分之一电子天平(上海良平仪器仪表有限公司,fa2004);
[0124]
⑷
十万分之一电子天平(赛多利斯科学仪器(北京)有限公司,bt25s);
[0125]
⑸
百万分之一电子天平(mettlertoledo,xp6);
[0126]
⑹
实验室用ph计(mettlertoledo,fe20);
[0127]
⑺
色谱柱:capcellpakadme type hr 3μm,2.1mm
×
150mm,coi.no.v44h2b 01095、coi.no.v44h2b 01096两支串联;
[0128]
⑻
杂质捕集小柱:welchghost-buster column 4.6
×
50mm 06100-3100061900953 g160027-05;
[0129]
⑼
流动相a:0.025mol/l磷酸二氢钠水溶液(ph3.0):乙腈=83:20,
[0130]
或0.1%甲酸水溶液(ph3.0):乙腈=83:20;
[0131]
⑽
流动相b:乙腈。
[0132]
梯度洗脱时间与流动相比例如下表2所示。
[0133][0134][0135]
表2
[0136]
⑾
舒更葡糖钠供试品溶液:精密称定并配制成每1ml中约含舒更葡糖钠供试品5mg的溶液。
[0137]
2、对系统适用性溶液和混合对照品溶液进行hplc分析,得到图19-图21所示色谱图。
[0138]
3、舒更葡糖钠有关物质检测
[0139]
⑴
分别取批号为a003-22001、a003-22002、a003-22003的舒更葡糖钠溶液2.5μl注入液相色谱仪中,记录色谱图,将测得的峰面积带入,用校正因子法计算含量,结果见表3。
[0140][0141]
表3
[0142]
⑵
方法学验证(分析验证杂质能有效检出)
[0143]
①
线性
[0144]
杂质rrt0.35b浓度在0.4349~6.5237μg/ml范围内,y=0.0459x-0.0001,r=0.9997;
[0145]
杂质rrt0.35a浓度在0.5153~7.7298μg/ml范围内,y=0.0467x-0.0010,r=
0.9997;
[0146]
舒更葡糖钠浓度在0.4714~7.0709μg/ml范围内,y=0.0502x+0.0006,r=0.9991;
[0147]
杂质rrt1.44a浓度在0.4925~7.3870μg/ml范围内,y=0.0484x+0.0004,r=0.9999;
[0148]
杂质rrt1.59b浓度在0.5826~8.7387μg/ml范围内,y=0.0543x-0.0082,r=0.9998;
[0149]
杂质rrt1.59a浓度在0.5027~7.5403μg/ml范围内,y=0.0549x-0.0069,r=0.9999。
[0150]
由此可以看得出,相关系数r均不小于0.990,峰面积与其浓度线性关系良好。
[0151]
②
进样重复性
[0152]
杂质rrt0.35b保留时间rsd为0.23%,峰面积rsd为4.97%;
[0153]
杂质rrt0.35a保留时间rsd为0.24%,峰面积rsd为4.50%;
[0154]
舒更葡糖钠保留时间rsd为0.07%,峰面积rsd为0.37%;
[0155]
杂质rrt1.44a保留时间rsd为0.04%,峰面积rsd为1.66%;
[0156]
杂质rrt1.59b保留时间rsd为0.04%,峰面积rsd为0.53%;
[0157]
杂质rrt1.59a保留时间rsd为0.04%,峰面积rsd为0.71%。
[0158]
由此可以看得出,各组分保留时间的rsd均小于20.0%,峰面积的rsd均小于20.0%,进样重复性良好。
[0159]
③
稳定性
[0160]
混合对照品溶液在48小时内,
[0161]
杂质rrt0.35b峰面积rsd为3.81%;
[0162]
杂质rrt0.35a峰面积rsd为2.82%;
[0163]
舒更葡糖钠峰面积rsd为4.70%;
[0164]
杂质rrt1.44a峰面积rsd为3.70%;
[0165]
杂质rrt1.59b峰面积rsd为4.87%;
[0166]
杂质rrt1.59a峰面积rsd为2.61%。
[0167]
舒更葡糖钠供试品溶液在48小时内,
[0168]
杂质rrt0.35b峰面积rsd为1.77%;
[0169]
杂质rrt0.35a峰面积rsd为3.00%;
[0170]
舒更葡糖钠峰面积rsd为0.16%;
[0171]
杂质rrt1.44a峰面积rsd为1.70%;
[0172]
杂质rrt1.59b峰面积rsd为1.61%;
[0173]
杂质rrt1.59a峰面积rsd为0.43%。
[0174]
由此可以看得出,各组分峰面积的rsd均小于5.0%,溶液稳定性良好。
[0175]
④
回收率
[0176]
混合对照品贮备液
②
:精密移取混合对照品贮备液
①
5ml置50ml量瓶中,并加溶剂2(0.05mol/l磷酸二氢钠溶液(ph3.0))稀释至刻度,摇匀,即得。
[0177]
取舒更葡糖钠粗品100mg,精密称定,置20ml量瓶中,再精密移取混合对照品贮备
液
②
1ml,加溶剂2使溶解并稀释至刻度,摇匀,即得回收率loq溶液,配制3份。
[0178]
取舒更葡糖钠粗品50mg,精密称定,置10ml量瓶中,再精密移取混合对照品贮备液
②
5ml,加溶剂2使溶解并稀释至刻度,即得回收率100%溶液,配制3份。
[0179]
取舒更葡糖钠粗品50mg,精密称定,置10ml量瓶中,再精密移取混合对照品贮备液
②
6ml,加溶剂2使溶解并稀释至刻度,即得回收率120%溶液,配制3份。
[0180]
舒更葡糖钠有关物质中杂质rrt0.35a回收率试验结果如表4所示。
[0181][0182]
表4舒更葡糖钠有关物质中杂质rrt0.35b回收率试验结果如表5所示。
[0183][0184][0185]
表5舒更葡糖钠有关物质中杂质rrt1.44a回收率试验结果如表6所示。
[0186][0187]
表6舒更葡糖钠有关物质中杂质rrt1.59a回收率试验结果如表7所示。
[0188][0189]
表7
[0190]
⑤
定量限
[0191]
注入液相色谱仪,色谱峰信噪比为10:1,得到各杂质的定量限(loq),结果见下表8。
[0192]
名称定量限μg/ml定量限相当于供试液的百分量%杂质rrt0.35b0.50880.0102杂质rrt0.35a0.51530.0103舒更葡糖钠0.47140.0094杂质rrt1.44a0.49250.0098杂质rrt1.59b0.50600.0101杂质rrt1.59a0.50270.0101
[0193]
表8
[0194]
⑥
重复性与中间精密度
[0195]
杂质rrt0.35b含量为0.0730%,rsd为2.37%;
[0196]
杂质rrt0.35a含量为0.1190%,rsd为2.31%;
[0197]
杂质rrt1.44a含量为0.1125%,rsd为2.29%;
[0198]
杂质rrt1.59b含量为0.0288%,rsd为6.97%;
[0199]
杂质rrt1.59a含量为0.0057%,rsd为4.86%。
[0200]
重复性与中间精密度共12份供试品加标溶液相比,
[0201]
杂质rrt0.35b含量为0.0831%,rsd为12.93%;
[0202]
杂质rrt0.35a含量为0.1162%,rsd为3.64%;
[0203]
杂质rrt1.44a含量为0.1128%,rsd为1.75%;
[0204]
杂质rrt1.59b含量为0.0275%,rsd为7.30%;
[0205]
杂质rrt1.59a含量为0.0055%,rsd为7.70%,
[0206]
由此可以看得出,各杂质含量的rsd均小于10.0%,重复性与中间精密度结果良好。
[0207]
显然,所描述的实施例仅仅是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域及相关领域的普通技术人员在没有作出创造性劳动的前提下所获得的所有其他实施例,都应属于本发明保护的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1