细胞球体制备装置及制备方法
1.本发明涉及类器官制备技术领域,尤其涉及一种细胞球体制备装置及制备方法。
背景技术:
2.类器官球体可以通过细胞球体培养而成。简单来说,可以先制备细胞悬液,然后将细胞悬液与油相材料在t型通道中混合,细胞悬液被油相材料剪切从而形成液滴,液滴固化后形成细胞球体,细胞球体后续经培养后可以形成类器官球体。
3.然而,现有技术中,细胞球体的制备效率较低,且由于细胞悬液的进液量的控制精度低,细胞球体的质量和质量稳定性较差。
技术实现要素:
4.本发明旨在至少解决现有技术中存在的技术问题之一。为此,本发明提出一种细胞球体制备装置,制备细胞球体的效率较高,制备的细胞球体的质量和质量稳定性均较高。
5.本发明还提出一种细胞球体制备方法。
6.根据本发明的第一方面实施例的细胞球体制备装置,包括:机架,以及安装于所述机架的供料模块、微流控芯片和固化模块;所述供料模块包括上位机、切换阀,以及连接于所述切换阀的水相储液器、油相储液器、第一泵、第二泵以及储液管,其中,所述水相储液器用于储存细胞悬液,所述油相储液器用于储存油相材料,所述第一泵、所述第二泵和所述切换阀均与所述上位机通讯连接,以使所述上位机能够驱动所述第一泵、所述第二泵和所述切换阀的运行;所述微流控芯片具有三通流道,所述三通流道具有第一入口、第二入口和出口,所述出口与所述固化模块连接,所述出口供所述细胞悬液的液滴流出,所述油相储液器与所述第二入口连接,以使所述油相储液器中的所述油相材料能够流向所述第二入口;所述固化模块用于使所述细胞悬液的液滴固化;所述切换阀具有进样状态和制备状态;当所述切换阀处于进样状态:所述水相储液器、所述储液管和所述第一泵依次连通,所述第一泵能够吸取所述水相储液器中的所述细胞悬液,以使所述储液管内部具有所述细胞悬液;当所述切换阀处于制备状态:所述第二泵、所述储液管和所述第一入口依次连通,所述第二泵能够将所述储液管中的所述细胞悬液输送至所述第一入口。
7.根据本发明实施例的细胞球体制备装置,至少具有如下有益效果:本发明的制备装置通过上位机驱动第一泵、第二泵和切换阀,实现细胞悬液和油相材料的自动进样,进样过程无需使用者手动驱动泵或调节阀门的状态,这有利于提高进样效率,从而提高细胞球体的制备效率。此外,调整切换阀的状态切换时间间隔、第一泵的运行时间和第二泵的运行时间,可以精确控制储液管中的细胞悬液的液体量,从而控制制备状态下进入微流控芯片的细胞悬液的液体量,从而保证微流控芯片的细胞悬液进液量的精确性,提高细胞球体的质量以及提高细胞球体的质量稳定性。
8.根据本发明的一些实施例,所述切换阀具有第一接口、第二接口、第三接口、第四接口、第五接口和第六接口;所述水相储液器与所述第一接口连接,所述第一泵与所述第二
接口连接,所述储液管的两端分别与所述第三接口和所述第六接口连接,所述第二泵与所述第四接口连接,所述微流控芯片的第一入口与所述第五接口连接;当所述切换阀处于进样状态:所述第一接口和所述第六接口连通,所述第二接口和所述第三接口连通,所述第四接口和所述第五接口连通;当所述切换阀处于制备状态:所述第一接口和所述第二接口连通,所述第三接口和所述第四接口连通,所述第五接口和所述第六接口连通。
9.根据本发明的一些实施例,所述第二泵与所述油相储液器连接;当所述切换阀处于制备状态,所述第二泵能够将所述油相储液器中的所述油相材料注入所述储液管,以使所述油相材料将所述储液管中的所述细胞悬液推向所述第一入口。
10.根据本发明的一些实施例,还包括打印模块,所述打印模块包括:打印头,与所述固化模块连接,用于将所述细胞球体喷出;多轴位移机构,安装于所述机架的顶部,所述打印头安装于所述多轴位移机构,所述多轴位移机构能够驱动所述打印头运动。
11.根据本发明的一些实施例,所述机架包括相互间隔设置的制备腔和固化腔,所述供料模块和所述微流控芯片均设置于所述制备腔中,所述固化模块设置于所述固化腔中。
12.根据本发明的一些实施例,还包括温度调节模块,温度调节模块安装于所述机架的内部,所述温度调节模块用于调节所述制备腔的温度。
13.根据本发明的第二方面实施例的细胞球体制备方法,包括:使水相储液器、储液管和第一泵依次连通,所述第一泵吸取所述水相储液器中的所述细胞悬液,以使所述储液管的内部具有所述细胞悬液;使第二泵、所述储液管和微流控芯片的第一入口依次连通,所述第二泵将所述储液管内部的所述细胞悬液输送至所述第一入口;使油相储液器中的油相材料流向所述微流控芯片的第二入口,使所述油相材料在所述微流控芯片中剪切所述细胞悬液,并形成所述细胞悬液的液滴;使所述液滴固化形成细胞球体。
14.根据本发明实施例的细胞球体制备方法,至少具有如下有益效果:可以提高微流控芯片的进样效率,提高细胞球体的制备效率;而且,使用该方法可以精确控制微流控芯片的细胞悬液进液量,保证细胞球体的质量以及提高细胞球体的质量稳定性。
15.根据本发明的一些实施例,通过穿刺取样获得细胞样本,并利用所述细胞样本制备所述细胞悬液。
16.根据本发明实施例的细胞球体制备方法,至少具有如下有益效果:取样方便,且样本量的需求量较小,这有利于降低细胞微球或类器官球体的材料成本。
17.本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
附图说明
18.下面结合附图和实施例对本发明做进一步的说明,其中:
19.图1为本发明实施例的细胞球体制备装置的结构示意图;
20.图2为本发明实施例的细胞球体制备装置的系统示意图;
21.图3为本发明的细胞球体制备装置的微流控芯片的流道的示意图;
22.图4为本发明的细胞球体制备装置的切换阀处于进样状态时的示意图;
23.图5为本发明的细胞球体制备装置的切换阀处于制备状态时的示意图;
24.图6为本发明实施例的细胞球体制备方法的示意图。
25.附图标记:100-制备装置,101-机架,102-细胞培养板,103-多轴位移机构,104-制备腔, 201-供料模块,202-水相储液器,203-油相储液器,204-储液管,205-第二泵,206-切换阀, 207-第一泵,208-微流控芯片,209-固化模块,210-打印模块,211-上位机,300-三通流道, 301-第一入口,302-第二入口,303-出口,401-第一接口,402-第二接口,403-第三接口,404
‑ꢀ
第四接口,405-第五接口,406-第六接口。
具体实施方式
26.下面详细描述本发明的实施例,所述实施例的示例在附图中示出,其中自始至终相同或类似的标号表示相同或类似的元件或具有相同或类似功能的元件。下面通过参考附图描述的实施例是示例性的,仅用于解释本发明,而不能理解为对本发明的限制。
27.在本发明的描述中,需要理解的是,涉及到方位描述,例如上、下、前、后、左、右等指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本发明和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本发明的限制。
28.在本发明的描述中,若干的含义是一个以上,多个的含义是两个以上,大于、小于、超过等理解为不包括本数,以上、以下、以内等理解为包括本数。如果有描述到第一、第二只是用于区分技术特征为目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量或者隐含指明所指示的技术特征的先后关系。
29.本发明的描述中,除非另有明确的限定,设置、安装、连接等词语应做广义理解,所属技术领域技术人员可以结合技术方案的具体内容合理确定上述词语在本发明中的具体含义。
30.本发明的描述中,参考术语“一个实施例”、“一些实施例”、“示意性实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不一定指的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任何的一个或多个实施例或示例中以合适的方式结合。
31.本发明提供了一种细胞球体制备装置(下文简称装置,对应附图标记“100”),该制备装置100可以利用油相材料对细胞悬液(细胞悬液相当于水相材料)的剪切力,制备细胞悬液的液滴,然后使液滴固化形成细胞球体。细胞悬液中含有的细胞种类取决于所需要制备的类器官种类,细胞具体可以是肌肉细胞、肝脏细胞等。使用者获取细胞样本后,可以将细胞加入到基质胶、水凝胶等溶液中而获得细胞悬液。油相材料可以是氟油。
32.制备装置100包括机架101、供料模块201、微流控芯片208和固化模块209,其中,供料模块201、微流控芯片208和固化模块209均安装在机架101中。
33.参照图3,微流控芯片208具有三通流道300,三通流道300具有第一入口301、第二入口302和出口303。若油相材料通过第二入口302进入三通流道300,且细胞悬液通过第一入口301进入三通流道300,细胞悬液和油相材料在三通处汇合后,细胞悬液将会被分散为均一的包裹细胞的微小液滴。细胞悬液的液滴会从出口303离开微流控通道,油相材料也会从出口303离开微流控芯片208。
34.结合图2,微流控芯片208的出口303与固化模块209连接,离开微流控芯片208的液
滴会进入固化模块209,固化模块209可以使液滴固化,并形成包括细胞的细胞球体。细胞球体包括凝固的水凝胶或基质胶,以及被包裹在水凝胶或基质胶中的细胞。具体地,固化模块209能够加热液滴,使液滴在某一温度范围下固化;例如,固化模块209包括固化管道(未具体示出),离开微流控芯片208的液滴会进入固化管道中,固化模块209通加热固化管道中的液滴,进而使液滴固化形成细胞球体。
35.固化模块209对固化管道的加热方式,可以是水浴加热。相应地,固化模块209还可以包括能够容纳水的水浴容器以及用于加热水浴容器中的水的加热件(例如电加热丝),固化管道可以浸泡在水浴容器中的水里面。又或者,固化模块209包括电加热丝,电加热丝直接在布设在供液滴流动的固化管道的外部,电加热丝直接加热固化管道。固化模块209的具体结构设置方式还有多种,只要能够实现对液滴的加热即可,此处不一一列举。
36.下面再对供料模块201进行介绍。
37.参照图2,供料模块201包括上位机211、切换阀206,以及与切换阀206连接的水相储液器202、油相储液器203、第一泵207、第二泵205以及储液管204。水相储液器202用于储存细胞悬液,油相储液器203则用于储存油相材料。上位机211可以是能够发出操控命令的计算机,第一泵207、第二泵205均与上位机211通讯连接。第一泵207、第二泵205和切换阀206均可以根据上位机211发出的指令动作,从而实现进样;本发明中的进样是指指将细胞悬液和油相材料输入微流控芯片208中。
38.需要说明的是,在一些实施例中,固化模块209、打印模块210也可以与上位机211通讯连接,固化模块209、打印模块210的运行均可以通过上位机211进行控制。
39.切换阀206具有进样状态和制备状态。参照图4,当切换阀206处于进样状态时,水相储液器202、储液管204和第一泵207依次连通,第一泵207吸取水相储液器202中的细胞悬液,相应地,细胞悬液会进入储液管204的内部。参照图5,当切换阀206处于制备状态时,第二泵205、储液管204和第一入口301依次连通,第二泵205将储液管204中的细胞悬液输送至第一入口301。
40.结合图2,油相储液器203可以与微流控芯片208的第二入口302连接(可以通过管路连接),从而使油相储液器203中的油相材料可以从第二入口302流入微流控芯片208内部。而且,可以是在切换阀206处于制备状态时,使油相材料从油相储液器203流向第二入口302。从第一入口301进入的细胞悬液和从第二入口302进入的油相材料汇合后,细胞悬液便被分散成液滴。
41.在一些实施例中,可以是供料模块201还包括第三泵(未示出),第三泵用于驱动油相储液器203中的油相材料流向第二入口302。当然,第三泵并不是必须的,在另一些实施例中,也可以将油相储液器203设置在较高的位置,利用油相材料的重力使油相材料流向第二入口302;相应地,在油相储液器203与第二入口302之间的管路上安装控制油相材料流动的阀门即可。
42.本发明的制备装置100通过上位机211驱动第一泵207、第二泵205和切换阀206,实现细胞悬液和油相材料的自动进样,进样过程无需使用者手动驱动泵或调节阀门的状态,这有利于提高进样效率,从而提高细胞球体的制备效率。此外,调整切换阀206的状态切换时间间隔、第一泵207的运行时间和第二泵205的运行时间,可以精确控制储液管204中的细胞悬液的液体量,从而控制制备状态下进入微流控芯片208的细胞悬液的液体量,从而保证
微流控芯片208的细胞悬液进液量的精确性,提高细胞球体的质量以及提高细胞球体的质量稳定性。
43.参照图2,在一些实施例中,制备装置100还包括打印模块210,打印模块210与固化模块209连接,打印模块210用于将细胞球体喷出。打印模块210包括打印头(打印头未示出)和多轴位移机构103,参照图1,多轴位移机构103安装于机架101的顶部,多轴位移机构103用于驱动打印头运动。打印头的入口端与固化模块209的出口端连接,从固化模块 209的出口303端流出的细胞球体,会进入打印头,打印头通过气压将细胞球体喷出。参照图1,从打印头喷出的细胞球体可以被喷到细胞培养板102或培养皿中。多轴位移机构103 用于驱动打印头运动,从而将多个细胞球体喷到细胞培养板102的不同的孔中。需要说明的是,在打印头将细胞球体喷出时,油相材料也会从打印头中喷出并挥发。
44.在一些实施例中,切换阀206设置为六通道切换阀。参照图4或图5,具体地,切换阀 206包括第一接口401、第二接口402、第三接口403、第四接口404、第五接口405和第六接口406。水相储液器202与第一接口401连接,第一泵207与第二接口402连接,储液管 204的两端分别与第三接口403和第六接口406连接,第二泵205与第四接口404连接,微流控芯片208的第一入口301与第五接口405连接。
45.参照图4,当切换阀206处于进样状态时,第一接口401和第六接口406连通,第二接口402和第三接口403连通,第四接口404和第五接口405连通。此状态下,启动第一泵207 运行,水相储液器202中的细胞悬液可以流向第一泵207处,在该流动过程中,细胞悬液会进入储液管204中。
46.参照图5,当切换阀206处于制备状态时,所述第一接口401和所述第二接口402连通,所述第三接口403和所述第四接口404连通,所述第五接口405和所述第六接口406连通。此状态下,启动第二泵205运行,第二泵205便可以将储液管204中的细胞悬液泵送至第一入口301。
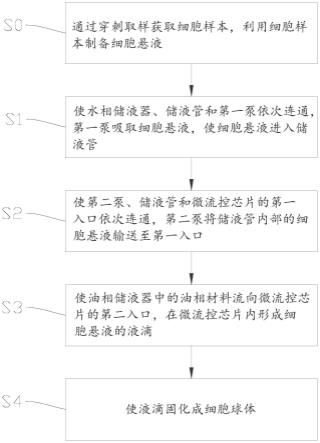
47.由于气体不易将细胞悬液推动至第一入口301,为了使第二泵205能够将储液管204中的细胞悬液泵送至第一入口301,在一些实施例中,第二泵205可以设置为用于输送油相材料,并利用油相材料将储液管204中的细胞悬液推到第一入口301处。
48.具体地,结合图2和图5,第二泵205与油相储液器203连接,当切换阀206处于制备状态下,第二泵205能够将油相储液器203中的油相材料注入储液管204,并使后进入储液管204的油相材料将之前存在于储液管204中的细胞悬液推向第一入口301。油相储液器203 中可以具有两个相互分隔的储油腔体,其中一个储油腔体中的油相材料用于流向第二入口302,另一个储油腔体中的油相材料则在第二泵205的驱动下流向储液管204(两个储油腔体中的油相材料相同)。当然,油相储液器203中也可以仅具有一个储油腔体,但油相储液器 203仍然需要具有两个供油相材料流出的出口303。
49.需要说明的是,油相材料进入储液管204后,油相材料和细胞悬液并非在具有三通形状的流道中汇合,油相材料并不会对细胞悬液产生足以使细胞悬液分散成液滴的剪切力,细胞悬液不会在储液管204中被分散成液滴,细胞悬液的液滴还是在微流控芯片208的三通流道 300中形成。此外,细胞悬液和油相材料不相溶。
50.在细胞球体的制备过程中,需要保证细胞悬液在合适的温度下储存,以及保证细胞悬液和油相材料在合适的温度下汇合,从而保证细胞球体的制备质量。例如,某些细胞悬
液需要在4℃下储存。
51.为保持细胞悬液处于合适的温度,机架101包括制备腔104和固化腔,制备腔104和固化腔相互间隔设置。固化腔未具体示出,在保证制备腔104和固化腔相互间隔设置的情况下,固化腔的位置选择较为灵活。
52.固化模块209安装在固化腔中,供料模块201和微流控芯片208则安装在制备腔104中。由于液滴的固化需要较高的温度(例如,液滴需要在37℃下固化),将固化模块209安装在另外的腔体(固化腔)中可以减少固化模块209对供料模块201和微流控芯片208处的温度的影响。
53.此外,在一些实施例中,制备装置100还包括温度调节模块,温度调节模块安装于机架 101的内部(未示出),并用于调节制备腔104中的温度,从而调节供料模块201和微流控芯片208中的细胞悬液的温度。
54.温度调节模块可以设置为蒸汽压缩式制冷机组,即,温度调节模块包括依次连接的压缩机、冷凝器、节流阀、蒸发器以及循环流经前述部件的制冷剂。其中,蒸发器可以布置于制备腔104的壁面的内部,制冷剂在蒸发器内蒸发后,制冷剂吸收制备腔104中的空气和模块的热量,从而对制备腔104进行降温。又或者,温度调节模块还包括风机,风机用于驱动空气依次流经蒸发器和制备腔104,空气流经蒸发器的表面后温度降低,低温空气吹入制备腔 104中,从而对制备腔104中的模块进行降温。
55.需要说明的是,温度调节模块也可以与上位机211通讯连接,温度调节模块的运行也可以通过上位机211进行控制。
56.参照图6,基于上述发明构思,本发明还提供了一种细胞球体制备方法(下文简称制备方法),制备方法包括以下步骤:
57.s1:使水相储液器202、储液管204和第一泵207依次连通,第一泵207吸取水相储液器202中的细胞悬液,以使储液管204的内部具有细胞悬液;
58.s2:使第二泵205、储液管204和微流控芯片208的第一入口301依次连通,第二泵205 将储液管204内部的细胞悬液输送至第一入口301;
59.s3:使油相储液器203中的油相材料流向微流控芯片208的第二入口302,使细胞悬液在微流控芯片208中的三通流道300中形成液滴;
60.s4:使液滴固化形成细胞球体。
61.使用该方法,可以提高微流控芯片208的进样效率,提高细胞球体的制备效率;而且,使用该方法可以精确控制微流控芯片208的细胞悬液进液量,保证细胞球体的质量以及提高细胞球体的质量稳定性。在获得细胞球体后,可以对细胞球体进行培养,并获得类器官球体。
62.此外,参照图6,在一些实施例中,制备方法还包括以下步骤s0:通过穿刺活检取样获得细胞样本,并利用该细胞样本制备细胞悬液。现有技术大多利用手术切除样本进行类器官建模,取样不便,且样本量需要较多。而本发明可以利用穿刺活检的样本进行细胞球体的制备和类器官的建模,取样方便,且样本量的需求量较小,这有利于降低细胞微球或类器官球体的材料成本。
63.上面结合附图对本发明实施例作了详细说明,但是本发明不限于上述实施例,在所属技术领域普通技术人员所具备的知识范围内,还可以在不脱离本发明宗旨的前提下作
出各种变化。此外,在不冲突的情况下,本发明的实施例及实施例中的特征可以相互组合。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1