多能干细胞衍生内皮细胞外泌体的制备方法和应用
1.本发明属于分子生物学及生物医药、医学保健领域,涉及一种外泌体,具体涉及一种人诱导多能干细胞(hipsc)衍生内皮细胞(hipsc-ecs)外泌体(hipsc-ec-exo)的制备方法及其在治疗心梗中的应用。
背景技术:
2.心血管疾病是全球的头号死因,而其中的心肌梗死由于发病率和死亡率不断上升,已经成为严重危害我国居民健康的疾病之一,并且给社会带来了沉重的经济负担。因此,急需发展安全有效的心肌梗死治疗手段。干细胞治疗,例如多能干细胞衍生内皮细胞(hipsc-ecs),被看作一种修复梗死心肌的潜在方法。有研究表明,hipsc-ecs具有促进血管新生和减少心肌细胞凋亡来保护缺血性心肌的疗效。然而,较低的细胞移植效率和存活率限制了hipsc-ecs的治疗前景,并提示旁分泌作用可能是干细胞发挥作用的主要机制。
3.外泌体是一种直径在30-150nm之间具有脂质双分子层结构的碗碟状囊泡,被看作是移植细胞旁分泌作用分泌所释放的重要可溶性因子。外泌体作为一种治疗性载体,其中存在丰富的多功能蛋白、磷脂、和核酸(包括mrna和microrna),这也是外泌体行使多种生物功能如免疫调节,肿瘤的生长与迁移,血管新生,组织损伤修复尤其是心肌修复的重要媒介。与干细胞移植治疗心梗相比,外泌体作为一种脱细胞疗法存在着能够避免移植细胞引起的异常分化、同时减少宿主的免疫排斥反应、增加修复梗死心肌效率等诸多优点。因而脱细胞的外泌体疗法有望成为促进梗死心肌修复的新策略,但hipsc-ec分泌的外泌体是否也具有保护缺血心肌的疗效未知。
4.钙离子作为细胞内一种独一无二的第二信使,在多种生物途径中都发挥着重要作用,例如肌肉收缩,能量代谢和细胞凋亡。ca
2+
稳态的紊乱是心脏衰竭的一个重要标志,因为心肌细胞收缩功能依赖于细胞内ca
2+
循环的同步运动,这有助于心律的产生和兴奋-收缩耦合。大量的证据表明心肌梗死会导致ca
2+
循环的紊乱。进一步的,细胞内过高的钙离子浓度会进一步影响细胞的能量代谢,因为过高的钙离子水平需要被线粒体所摄取从而增加了线粒体的负担,这种能量供给和利用的平衡的打破进一步导致了凋亡信号通路的激活;同时细胞内过高的钙离子浓度会进一步激活钙依赖水解酶的激活,这种钙依赖水解酶的过度磷酸化则会导致心肌肌丝的降解,影响收缩功能同时激活凋亡信号通路。因此,通过维持细胞内钙稳态来减轻心肌的缺血性损伤就显得尤为重要。hipsc-ec-exo能否通过调控钙稳态来起缺血心肌保护作用有待研究。
5.探究hipsc-ec-exo是否可以作为一种新型的修复梗死心肌策略将变得十分有趣。但是目前的研究存在着重大的不足:1)如何建立高效的提取hipsc-ec-exo体系;2)hipsc-ec-exo是否在体内、体外对缺血心肌具有保护作用;3)hipsc-ec-exo是否能通过对钙稳态的调控从而发挥对缺血心肌发挥保护作用。回答这些问题将有助于开发一种可以高效提取且在治疗心梗疾病具有优秀应用价值的干细胞衍生产品。
技术实现要素:
6.本发明要解决目前缺乏高效的多能干细胞衍生内皮细胞外泌体(hipsc-ec-exo)的制备方法的技术问题,提供一种多能干细胞衍生内皮细胞外泌体(hipsc-ec-exo)的制备方法,该方法可高效分离提取hipsc-ec-exo,并进一步确定hipsc-ec-exo对心梗后缺血心肌具有治疗保护作用。
7.为了解决上述技术问题,本发明通过如下技术方案实现:
8.在本发明的一个方面,提供了一种多能干细胞衍生内皮细胞外泌体hipsc-ec-exo的制备方法,包括以下步骤:
9.将人诱导多能干细胞hipscs分化为内皮细胞ecs,再通过流式细胞术细胞分选收集同时表达血小板-内皮细胞粘附分子cd31和血管内皮钙粘蛋白cd144的细胞,获得纯化的hipsc-ecs;
10.将hipsc-ecs在无血清培养基中培养46~50小时后收集细胞上清,并将该收集的细胞上清于250~350g转速下离心8~12分钟后去除残存的细胞;
11.收集上清于1500~2500g转速条件下离心8~12分钟去除死细胞;
12.收集上清于8000~12000g转速条件下离心25~35分钟去除细胞碎片;
13.收集上清于95000~105000g转速条件下离心1.8~2.5小时后弃去上清,所得沉淀即为多能干细胞衍生内皮细胞外泌体hipsc-ec-exo。
14.优选的,所述将人诱导多能干细胞hipscs分化为内皮细胞ecs的步骤包括:用含y27632mtesr的培养基传代hipscs,再用含chir99021、骨形态发生蛋白4和b27的培养基诱导分化,然后用含血管内皮生长因子和forskolin stem-pro34的培养基处理hipscs,可将hipscs分化为ecs。
15.所述获得纯化的hipsc-ecs,在无血清培养基中维持。
16.所述多能干细胞衍生内皮细胞外泌体沉淀,用pbs重悬后于-80℃保存或用于实验。
17.在本发明的另一方面,还提供了一种由上述制备方法制得的多能干细胞衍生内皮细胞外泌体hipsc-ec-exo。
18.在本发明的另一方面,还提供了多能干细胞衍生内皮细胞外泌体hipsc-ec-exo在制备治疗或预防缺血性心脏病的干细胞衍生产品中的应用。
19.所述缺血性心脏病包括:心绞痛、心肌梗死、缺血性心肌病、无症状性的心肌缺血。
20.优选的,所述hipsc-ec-exo可通过直接心肌注射给药。
21.所述hipsc-ec-exo通过增加心肌细胞atp和钙瞬变、减少乳酸脱氢酶的释放保护心肌细胞免受糖氧剥夺损伤。
22.所述hipsc-ec-exo直接心肌注射可改善心梗后心脏收缩功能、血流动力学、和限制心脏的不良重构。进一步探究机制发现,hipsc-ec-exo可通过调节心肌中相关钙调蛋白serca-2a、ryr-2、p-ser16-plb的表达,改善心肌细胞的收缩和钙瞬变从而维持钙稳态。
23.本发明多能干细胞衍生内皮细胞外泌体(hipsc-ec-exo)的制备方法,能高效分离提取hipsc-ec-exo,并首次证明了hipsc-ec-exo心肌注射可以显著改善心梗小鼠的心肌收缩功能、血流动力学,还可以减轻心梗后有害的左室重构,具有治疗缺血性心脏病的作用,可作为细胞治疗的替代方法。
附图说明
24.下面结合附图和具体实施方式对本发明作进一步详细的说明。
25.图1是本发明实施例1的人诱导多能干细胞衍生内皮细胞(hipsc-ecs)的鉴定结果图;
26.图2是本发明实施例1的人诱导多能干细胞衍生内皮细胞外泌体(hipsc-ec-exo)的分离提取与鉴定结果图;
27.图3是本发明实施例2的hipsc-ec-exo体外对缺血心肌的保护作用实验结果图;
28.图4是本发明实施例3的hipsc-ec-exo可改善小鼠心梗后的心功能持续恶化的实验结果图;
29.图5是本发明实施例3的hipsc-ec-exo抑制小鼠心梗后心脏的不良重构的实验结果图;
30.图6是本发明实施例3的hipsc-ec-exo可改善小鼠心梗后心肌细胞收缩与钙瞬变的检测结果图;
31.图7是本发明实施例3的hipsc-ec-exo可调节钙调相关蛋白的表达结果图。
具体实施方式
32.下列实施例中,未注明具体条件的实验方法,通常按常规条件,如《精编分子生物学实验指南》(f.m.奥斯伯,r.e.金斯顿,j.g.塞德曼等主编,马学军,舒跃龙的译.北京:科学出版社,2004)中所述的方法进行。
33.为了建立高效的提取hipsc-ec-exo体系,本发明研制出了一种多能干细胞衍生内皮细胞外泌体hipsc-ec-exo的制备方法,包括以下步骤:
34.将人诱导多能干细胞hipscs分化为内皮细胞ecs,再通过流式细胞术细胞分选收集同时表达血小板-内皮细胞粘附分子cd31和血管内皮钙粘蛋白cd144的细胞,获得纯化的hipsc-ecs;
35.将hipsc-ecs在无血清培养基中培养46~50小时后收集细胞上清,并将该收集的细胞上清于250~350g转速下离心8~12分钟后去除残存的细胞;
36.收集上清于1500~2500g转速条件下离心8~12分钟去除死细胞;
37.收集上清于8000~12000g转速条件下离心25~35分钟去除细胞碎片;
38.收集上清于95000~105000g转速条件下离心1.8~2.5小时后弃去上清,所得沉淀即为多能干细胞衍生内皮细胞外泌体hipsc-ec-exo。
39.实施例1 hipsc-ec-exo的分离提取与鉴定方法
40.1.1hipsc-ecs的分化与鉴定
41.本发明采用由人脐带血单个核细胞经oct4、sox2、klf4和cmyc转录重编程获得的hipscs。将hipscs分化为内皮细胞(ecs),简单地说,用含10μm y27632 mtesr培养基按照1:10传代hipscs,随后用含8μm chir99021和25ng/ml骨形态发生蛋白4(bmp4)的1%b27+培养基诱导分化,再用含200ng/ml血管内皮生长因子(vegf)和2μm forskolin stempro34培养基处理hipscs,可分化为ecs。通过流式细胞术细胞分选(facs)收集同时表达血小板-内皮细胞粘附分子(cd31)和血管内皮钙粘蛋白(cd144)的细胞,从而获得纯化的hipsc-ecs,并在无血清培养基(egm-2mv)中维持。纯化的hipsc-ecs通过成管实验和低密度脂蛋白摄取实
cms钙瞬变的代表图和统计图。糖氧剥夺损伤+生理盐水为对照组;糖氧剥夺损伤+外泌体为治疗组。
51.实施例3 hipsc-ec-exo对心梗小鼠心肌的保护作用
52.3.1小鼠心肌梗死模型的建立
53.选用8-12周龄nod-prkdc
scid il2rg
em1
/smoc(m-nsg)小鼠作为实验对象,通过永久结扎左前降支(lad)冠状动脉导致心肌梗死制造心梗模型。心梗+外泌体组动物直接心肌内注射hipsc-ec-exo(20μg/20μl pbs)至左室前壁3个部位;心梗组心肌内注射20μl pbs至左室前壁3个部位;假手术组仅穿过lad下方不打结,其余均进行正常手术过程,术后恢复正常,不进行任何实验治疗。结扎后肉眼可见结扎处至心尖变白,证明心梗模型建立成功。
54.3.2心脏超声检测小鼠心功能
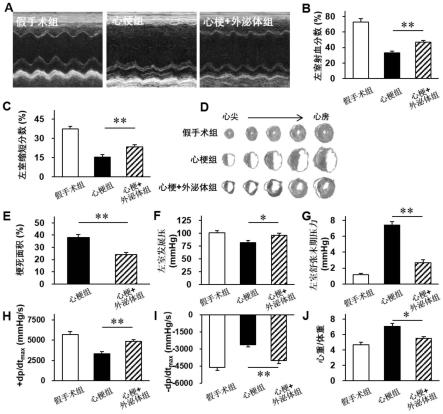
55.小鼠心梗模型建立当天视为第0天,则分别于第0天、第28天进行心动超声检测。待小鼠于异氟烷诱导麻醉后置于检测台上固定四肢,使用异氟烷于口鼻处持续麻醉并使用脱毛膏脱去小鼠胸前的皮毛。小鼠胸前区域涂抹适量的耦合剂后使用心脏超声诊断仪探头记录心脏长轴和左室短轴运动图像。根据m型超声图像数据分析,计算心脏左室射血分数(lvef)和心脏左室缩短分数(lvfs)。图4是小鼠心梗后28天心功能检测的代表图和统计数据,结果显示hipsc-ec-exo可以显著减轻小鼠心梗后28天的心功能持续恶化。图4中,图4a心超检测小鼠心梗后28天心功能的代表图;图4b是心超检测小鼠心梗后28天左室射血分数指标的统计图;图4c是心超检测小鼠心梗后28天左室缩短分数指标的统计图。
56.3.3masson评估小鼠心脏纤维疤痕面积
57.小鼠心梗后第28天处死小鼠后心脏收样,制作心脏的冰冻切片用于后续的各种病理染色分析,使用改良版的masson染色试剂盒(索莱宝,中国)染色并用image j软件分析心脏纤维疤痕的面积。图4d-4e是masson染色检测小鼠心梗后28天心脏纤维疤痕面积的代表图和统计图,结果显示hipsc-ec-exo可以显著减少小鼠心梗后28天的心脏纤维疤痕的面积。
58.3.4血流动力学
59.小鼠的麻醉固定如前所述,将小鼠颈部气管暴露出来后将小鼠右颈总动脉分离出来,然后用线将右颈总动脉的近头端结扎后将导管缓慢插入到动脉中。缓慢的将导管推入左室中,待图像稳定后开始记录实验数据。利用powerlab系统(ad instrument,澳大利亚)连续监测左室压力。测定左室发展压(lvdp)、左室舒张末期压力(lvedp)、左室压力最大上升速率(+dp/dtmax)和左室压力最大下降速率(-dp/dtmax)。图4f-4i是小鼠心梗后28天心脏血流动力学检测结果统计图,结果显示hipsc-ec-exo可以显著改善小鼠心梗后28天的血流动力学。
60.图4j是小鼠心梗后28天心脏重量与体重的比值,由图4j可知,心梗+外泌体组与心梗组相比显著减少了心重与体重的比值,说明外hipsc-ec-exo可以改善心梗后的心肌肥厚。图4j中,心梗组为对照组,心梗+外泌体组为治疗组。
61.3.5免疫荧光
62.小鼠心脏的冰冻切片的制备如上所述。对于对心梗后第28天的冰冻切片使用fitc标记的wga染料(sigma-aldrich)染色检测心肌细胞的横截面积的大小。使用原位细胞死亡检测试剂盒进行tunel染色以评估心肌细胞的凋亡。图5是小鼠心梗后28天wga染色和心梗
后3天tunel染色的代表图和统计数据,结果显示hipsc-ec-exo可以显著减少小鼠心梗后28天的心肌细胞的肥大和心梗后3天的心肌细胞的凋亡。
63.在图5中,图5a-5b是wga染色检测小鼠心梗后28天心脏心肌细胞的横截面积大小的代表图和统计图;图5c-5d是tunel染色检测小鼠心梗后3天心脏心肌细胞的凋亡情况的代表图和统计图。其中心梗组为对照组,心梗+外泌体组为治疗组。
64.3.6心肌细胞收缩和钙瞬变检测
65.于小鼠心梗第28天使用langendroff体外灌流的方法分离小鼠心脏左室的心肌细胞。之后将心肌细胞于室温下避光孵育钙离子荧光探针(fura-2 am)20分钟,再用不含荧光探针的含钙台氏液(1.8mmol/l)洗涤细胞3次,每次10分钟。将几滴负载了fura-2的心肌细胞加入到荧光倒置显微镜上的灌流槽中,并加入约300μl含钙台氏液(1.8mmol/l),温度控制在25℃,贴壁10分钟。使用电子刺激器按照0.5hz、1hz、和2hz频率刺激心肌细胞后通过ionoptix检测系统记录心肌细胞的收缩和钙瞬变的变化情况。图6是小鼠心梗后28天心肌细胞的收缩和钙瞬变的代表图和统计数据。结果显示hipsc-ec-exo可以显著增强小鼠心梗后28天的心肌细胞收缩能力和钙瞬变的幅度。
66.在图6中,图6a是小鼠心梗后28天分离的心肌细胞在0.5hz,1hz,和2hz电刺激频率下的细胞收缩的代表图;图6b-6c是心肌细胞收缩的指标包括细胞收缩幅度和细胞最大收缩速率与细胞静息时的长度的比值的统计图;图6d是小鼠心梗后28天心肌细胞在0.5hz,1hz,和2hz电刺激频率下的钙瞬变的代表图;图6e-6f是钙瞬变指标包括钙瞬变振幅和细胞钙瞬变上升的最大速率与静息钙瞬变比值的统计图。其中心梗组为对照组,心梗+外泌体组为治疗组。
67.3.7聚丙烯酰胺凝胶电泳
68.在电泳仪(biorad,usa)上对蛋白样本进行聚丙烯酰胺凝胶电泳,随后将一抗ryr-2(sigma-aldrich)、serca-2a(sigma-aldrich)、plb(abcam)、p-ser16-plb(abcam)抗体与膜孵育过夜,并用甘油醛酸-3-磷酸脱氢酶(gapdh)(proteintech)或β-微管蛋白(β-tublin)(abcam)抗体标记内参。图7是小鼠心梗后28天心脏组织中相关的钙调蛋白的表达情况,结果显示hipsc-ec-exo可以显著改善心梗28天后的serca-2a、ryr-2、p-ser16-plb蛋白的表达情况。
69.在图7中,图7a-7b是聚丙烯酰氨凝胶电泳检测心梗后28天心脏组织样本中钙调蛋白包括serca-2a和ryr-2的表达的代表图和统计图;图c-d是聚丙烯酰氨凝胶电泳检测心梗后28天心脏组织样本中plb和p-ser16-plb表达的代表图和统计图。其中心梗组为对照组,心梗+外泌体组为治疗组。
70.以上所述实施例仅表达了本发明的实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1