血清组分和单克隆抗体制备的纳米粒在制备药物中的用途的制作方法
1.本技术涉及生物领域,更具体的涉及血清组分和单克隆抗体制备的纳米粒在制备药物中的用途。
背景技术:
2.血清,指血液凝固后,在血浆中除去纤维蛋白原及某些凝血因子后分离出的淡黄色透明液体或指纤维蛋白原已被除去的血浆。其主要作用是提供基本营养物质、提供激素和各种生长因子、提供结合蛋白、提供促接触和生长因子使细胞贴壁免受机械损伤、对培养中的细胞起到某些保护作用。每100ml人血清含有蛋白质6-8g,其中主要是白蛋白和球蛋白。血清不会凝固。有免疫,维持酸碱平衡和渗透压的作用,血清蛋白质亦可储备供给机体蛋白质不足时的应用。
3.临床上也有注射血清用于疾病的治疗。比如首先注射血清的功效,主要是改善大脑血液循环,预防脑血栓形成,及时调节脑代谢产物,疏通和保护血管内膜和内皮细胞,防止内膜损伤,以及内皮细胞衰老的作用。其次血清注射的作用,主要是治疗,或辅助治疗脑血栓形成、脑出血、常见心脑血管疾病和脑梗死,尤其是辅助治疗脑出血,它能及时修复损伤和脑血管,进一步预防疾病,促进脑细胞恢复、脑血管重建,防止脑损伤再次发生。在癌症患者的治疗中,通过也会使用血清或者血清中的人血白蛋白进行治疗,提高癌症患者的治疗效果。在癌症晚期,由于营养不良以及肿瘤引起的全身性慢性炎症抑制血清白蛋白合成,导致患者低白蛋白血症的发生。合并低白蛋白血症的恶性肿瘤患者化疗前补充白蛋白不仅能降低化疗毒副作用,同时减轻化疗后全身炎性反应,使化疗患者明显获益。
4.血清中,最主要起到活性作用的是人血白蛋白。白蛋白是指在人体内含量最高(通常占血浆蛋白总含量的50%以上),且含有585种氨基酸残基的一种单链多肽。它是血浆中存在的最小蛋白质之一,分子量约为66458。同时,白蛋白也是一种通用的大分子载体,有利于帮助溶解度有限的各种内源性化合物(包括脂肪酸和胆红素),在全身循环中的运输。白蛋白还可与紫杉烷类、磺胺类、青霉素类和苯并二氮杂类等治疗剂结合,来影响药物的生物分布、生物活性和代谢。由于具备上述功能,在临床上白蛋白已被广泛证明是一种安全的生物材料,可用于设计药物输送系统。白蛋白作为药物载体,能够避免难溶性药物被血液清除,从而发挥靶向作用;还可减少抗肿瘤药物所产生的不良反应和毒副作用;同时,还能增加患者的顺从性,具有广阔的应用前景。
5.人血白蛋白作为抗肿瘤药物的载体与其他载体相比,具有如下优势:(1)生物相容性好。白蛋白是人体的内源性物质,不会给机体带来毒性反应,也不会引发自身免疫反应,或使机体产生变性、降解等一些不良反应。(2)稳定性好。白蛋白是具有特殊结构和独特性质的蛋白质,在一定的温度和ph范围内,会保持良好的稳定性。因此,对于大多数的外源性物质来说,白蛋白是一种理想的载体,可以提高外源性物质的稳定性。(3)载药性能好。白蛋白具有独特的空间结构,能够以物理包裹或化学键偶联的方式将药物包载。研究发现,白蛋白可以增加疏水性药物在血浆中的溶解度,并且对于易氧化药物具有较好的保护作用。(4)
具有靶向性。药代动力学研究表明,白蛋白不仅可以躲避网状内皮系统的识别与吞噬,被动靶向于肝、肾、骨髓等器官;还可以在白蛋白表面,通过以非共价键结合的方式,修饰各类具有靶向功能的物质(例如,对白蛋白表面具有活性赖氨酸中的氨基进行化学修饰)。因为在血管的内皮细胞和大部分的肿瘤细胞表面都有白蛋白受体,这些受体可以提高白蛋白药物在肿瘤细胞中的富集,进而实现白蛋白在体内主动靶向的目的。(5)体内半衰期时间较长。由于白蛋白在血液中带有负电荷,使其不易被巨噬细胞清除,这个特点为实现药物的长效循环提供了可能。因此,人血白蛋白所具备的这些优点,为其成为一种良好的药物载体奠定了一定的基础。
6.x连锁凋亡抑制蛋白(x-linked inhibitor ofapoptosis protein,xiap)是新发现的一个iap家族中的主要成员,是iap家族中最强的凋亡抑制因子,它可直接抑制caspases并可多途径调节细胞凋亡。xiap基因在大多数的肿瘤细胞株中过表达,其表达与肿瘤的进展、复发、预后以及肿瘤化疗的耐药密切相关。近年研究发现x染色体连锁的凋亡抑制基因(xiap)能够选择性抑制癌细胞凋亡的上游启动分子caspase-9和下游效应分子caspase-3,caspase-7,使癌细胞抵抗凋亡并对化疗产生耐药。蒽贝素是从紫金牛科植物中提取的多酚类化合物,是一种xiap的小分子抑制剂,能与xiap蛋白分子中bir3结构域结合,阻止xiap分子与caspase-9结合而诱导细胞凋亡。
7.基于xiap在调控凋亡中的重要作用以及与肿瘤发生发展的密切关系,靶向xiap已作为了抗癌治疗的一项策略。靶向xiap抑制的细胞试验以及定向敲除xiap的小鼠并没表现出有意义的病理变化,对小鼠以xiap抑制剂处理其并未表现出毒性反应,从这些可见靶向xiap成为了一项有吸引力的研究。而xiap作为iap家族的重要成员,已作为这方面研究的重点。对xiap的抑制方法有反义rna、sirna和人工合成xiap的小分子抑制剂。通过反义寡核苷酸和sirna方法降解xiap的mrna,进而消除xiap的表达,使得许多肿瘤细胞恢复了对化疗的敏感性。但是目前,针对xiap抑制剂的研究还不够多,可用的xiap抑制剂的类型也不够多,值得进一步的研究。
技术实现要素:
8.本发明克服现有技术的缺陷,提供了一种特异性的xiap抑制剂。
9.所述的xiap抑制剂为特异性针对xiap的单克隆抗体。
10.具体的,所述抗体的轻链可变区序列如seq id no:1所示,其重链可变区的序列如seq id no:2所示。
11.进一步的,本发明还提供了xiap的单克隆抗体介导的阿霉素白蛋白纳米粒。
12.进一步的,所述的纳米颗粒是通过如下方法制备获得:阿霉素与人血清白蛋白溶解到蒸馏水中,在室温下搅拌;调节ph值至9;乙醇以0.5ml/min的速度滴至已经孵化好的药物与白蛋白混合溶液中继续搅拌,向纳米粒溶液中滴加8%戊二醛溶液室温磁力搅拌,使纳米粒交联固化,制得固化纳米粒的溶液。将纳米粒溶液以15000r/min的转速高速离心倾去上清液加水至原体积,超声分散。洗涤3次,以去除制备中加入的有机溶剂,得到阿霉素白蛋白纳米粒。取阿霉素白蛋白纳米粒,加入nhs-peg3500-mal溶液(44mg溶于500μl ph8.0的磷酸盐缓冲液中)中,恒温磁力搅拌。18000离心10min弃去上清液后,再用双蒸水重新分散。取单抗缓冲液(适量单抗溶于ph8.0的磷酸盐缓冲液,单抗终浓度为1mg/ml)加入2-亚氨基硫
烷盐酸缓冲液(6.9mg溶于50mlph8.0的磷酸盐缓冲液中)中,恒温磁力搅拌。取前述制备的巯基化的阿霉素白蛋白纳米粒,加入到硫醇化的单抗缓冲液中,恒温磁力搅拌,采用离心超滤法纯化,制备获得纳米粒。
13.进一步的,xiap的单克隆抗体介导的阿霉素白蛋白纳米粒的制备方法也可以采用本领域常规的纳米粒制备方法制备获得,只要能够制备得到相应的纳米粒即可。
14.进一步的,本发明还提供了人血白蛋白,所述人血白蛋白可以是本发明分离制备的,也可以是商业购买的人血白蛋白。
15.进一步的,本发明还提供了xiap的单克隆抗体在制备用于治疗胃癌的药物组合物中的用途。
16.进一步的,本发明还提供了xiap的单克隆抗体介导的阿霉素白蛋白纳米粒在制备用于治疗胃癌的药物组合物中的用途。
17.进一步的,本发明的药物组合物还含有药学上可接受的载体。
18.本文所用的术语“药学上可接受的”是指当分子本体和组合物适当地给予动物或人时,它们不会产生不利的、过敏的或其它不良反应。本文所用的“药学上可接受的载体”应当与本发明的突变蛋白相容,即能与其共混而不会在通常情况下大幅度降低药物组合物的效果。可作为药学上可接受的载体或其组分的一些物质的具体例子是糖类,如乳糖、葡萄糖和蔗糖;淀粉,如玉米淀粉和土豆淀粉;纤维素及其衍生物,如羧甲基纤维素钠、乙基纤维素和甲基纤维素;西黄蓍胶粉末;麦芽;明胶;滑石;固体润滑剂,如硬脂酸和硬脂酸镁;硫酸钙;植物油,如花生油、棉籽油、芝麻油、橄榄油、玉米油和可可油;多元醇,如丙二醇、甘油、山梨糖醇、甘露糖醇和聚乙二醇;海藻酸;乳化剂,如tween;润湿剂,如月桂基硫酸钠;着色剂;调味剂;压片剂、稳定剂;抗氧化剂;防腐剂;等渗盐溶液;和磷酸盐缓冲液等。
19.术语
″
药学上可接受载体
″
是指一种或多种有机或无机成分,它可以是天然的或合成的,与抗体组合后可促进其应用。可接受的载体包括无菌的生理盐水或是其它药学上可获得的且为本领域所熟知的水或非水的等渗溶液和灭菌混悬剂。“有效剂量”是指能够改善或延缓病态的、退变的或损坏的状况的进程的剂量。
20.用于本发明的单克隆抗体也可用杂交瘤方法制得,因为编码本发明人源化抗体的dna序列可用本领域技术人员熟知的常规手段,如根据本发明公开的氨基酸序列人工合成或用pcr法扩增得到,因而也可用重组dna方法,可用本领域熟知的各种方法将该序列连入合适的表达载体中。最后,在适合本发明抗体表达的条件下,培养转化所得的宿主细胞,然后本领域技术人员应用熟知的常规分离纯化手段纯化得到本发明的单克隆抗体。
21.有益效果
22.本发明以xiap蛋白作为免疫原,通过免疫小鼠制备并获得了xiap单克隆抗体,所述抗体本身具有较好的抑制癌细胞增殖的效果,并且将所述的抗体与本发明从血清中制备得到的人血白蛋白一起制备可xiap的单克隆抗体介导的阿霉素白蛋白纳米粒,所述纳米粒具有较好的抑制肿瘤生长的效果。
附图说明
23.图1单抗生物活性鉴定结果
24.图2单抗对xiap蛋白表达的影响
具体实施方式
25.本发明可通过后续对于本发明一些实施方案描述以及其中所包括的实施例的详细内容而更容易被了解。在进一步叙述本发明之前,应明了本发明不会被局限于所述特定实施方案中,因为这些实施方案必然是多样的。亦应明了本说明书中所使用的用语仅是为了阐述特定实施方案,而非作为限制,因为本发明的范围将会被仅仅界定在所附的权利要求中。
26.实施例1xiap单克隆抗体的制备
27.抗原xiap重组蛋白,禾午生物,货号a00961与弗氏完全佐剂按1∶1的比例混合乳化,腹部皮下途径接种7周龄雌性balb/c小鼠,抗原蛋白量约为120μg/只,初次免疫后2周,抗原与弗氏不完全佐剂混合乳化,同法免疫。以后免疫不再加佐剂,分别在4周、6周后各加强免疫1次,融合前3d腹腔及尾静脉途径再加强免疫1次。
28.细胞融合按常规方法,取免疫小鼠的脾细胞与sp2/0混合于融合管内,1000r/min,离心12min,弃去上清,轻振融合管底,使沉淀细胞松散均匀,置37℃水浴中预热。然后在48s内缓慢滴加预热的peg4000溶液1ml,边加边轻转搅拌,然后在90s内缓慢加入不完全dmem培养基,终止融合。静置10min后,1000r/min,离心12min,弃上清,加入hat培养基,使细胞悬浮并混匀。加入适量饲养细胞分装至96孔细胞培养板,放于co2培养箱内培养。第5天各孔补加1滴hat培养液,第10天用ht培养液换出全部hat培养液,并可开始检测筛选。融合后待杂交瘤细胞长满孔底1/3~1/2时换液,3~4d后即可取细胞培养上清进行检测筛选获得阳性杂交瘤细胞株14株,将阳性孔中的细胞扩大培养并及时冻存,同时按有限稀释法进行亚克隆,至阳性率为100%时,即可定株,共筛选获得2株阳性最强、稳定性最好的杂交瘤细胞株,分别是xiap-11a6和xiap-14d8。采取体内诱生法制备大量腹水,采用辛酸-饱和硫酸铵沉淀法纯化,分别获得纯化后的xiap-11a6和xiap-14d8用于后续研究。
29.实施例2xiap-11a6单抗特性鉴定
30.以重组蛋白xiap包板,包板浓度为5μg/ml,每孔100μl,同时设空白孔和阴性对照孔,4℃过夜。用1
‰
pbst液洗板后,每孔加入单克隆抗体,按1:1000倍比稀释,每孔100μl,振荡摇匀后,37℃置1h,洗板,加入hrp标记的羊抗鼠抗体1∶3000稀释,每孔100μl,37℃孵育40min后用1
‰
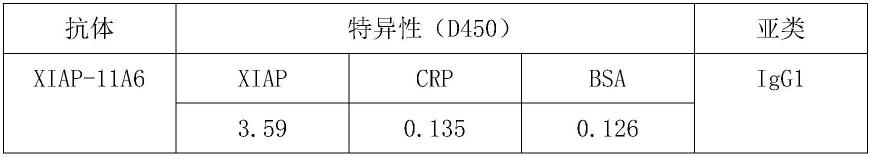
pbst洗板,再以tmb显色系统显色,用酶标仪于450nm处测定各孔光密度值[d(450)]。单克隆抗体用间接elisa法鉴定其特异性,包被无关蛋白crp及bsa作为对照。进行特异性鉴定。单克隆抗体亚类鉴定按照试剂盒提供的方法进行。结果如表1所示。
[0031]
表1xiap-11a6特性鉴定结果
[0032][0033]
从表1的结果可以看出,单克隆抗体xiap-11a6具有较好的特异性,并且其亚型为igg1。
[0034]
实施例3xiap-11a6单抗亲和力鉴定及序列鉴定
[0035]
抗体的亲和力测定采用间接elisa法。以重组蛋白xiap包板,包板浓度分别为1、
0.5、0.25、0.125μg/ml,同时设空白孔和阴性对照孔,4℃过夜。1
‰
pbst液洗板后用1%bsa封闭,37℃1h。洗板后每孔加入单克隆抗体(1μg/ml),振荡摇匀后37℃置1h,洗板后加入hrp标记的羊抗鼠抗体1∶3000稀释,每孔100μl,37℃孵育40min后,用1
‰
pbst洗板,利用tmb显色系统显色后,用酶标仪于450nm处测定各孔光密度值[d(450)]。然后根据公式kd=(n-1)/2(n[ab']-[ab])(式中:n=[ag]/[ag'];[ab]或[ab']代表间接elisa法中达到最大光密度值一半时的抗体浓度),计算获得单抗相对亲和力为3.82
×
109l/mol。
[0036]
利用序列鉴定试剂盒,提取并鉴定抗体的轻链可变区和重链可变区序列分别如seq id no:1和seq id no:2所示。
[0037]
实施例4xiap-11a6单抗生物活性鉴定
[0038]
分别取对数生长期的sgc7901胃癌细胞悬浮于含10%胎牛血清的dmem高糖培养液中,将细胞悬液浓度调整为1.0
×
105/ml,并接种于96孔板,每组设置3个复孔,每孔1
×
104个/l,于5%c02、37℃恒温培养箱中培养24h后加药。对照组加入培养液,,药物处理组浓度分别为0,5,10,50,100,200μg/ml,继续培养72h。阳性对照组:阿帕替尼100μg/ml;每孔分别加入10μl cck-8溶液,继续培养4h。每孔分别加入10μl的dmso,摇床孵育10min,充分溶解结晶。用酶标仪在450nm下测定各孔的吸光度值。细胞活力(%)=[a(加药)-a(空白)]/[a(0加药)-a(空白)]
×
100%。其中,a(加药):具有细胞、cck-8溶液和embelin溶液的孔的吸光度;a(空白):具有培养基和cck-8溶液而没有细胞的孔的吸光度;a(0加药):具有细胞、cck-8溶液而没有单抗溶液的孔的吸光度。抑制率=100(%)-细胞活力(%)。结果如图1所示。
[0039]
从图1的结果可以看出,本发明的xiap-11a6单抗具有较好的剂量依赖性,随着浓度的增加,对细胞的抑制率逐渐增加,特别是在200μg/ml是,细胞抑制率达到了(86.3
±
1.9)%,与空白对照相比差异显著(p《0.05),与阳性对照相比,相同药物用量条件下,本发明的单抗对于细胞的抑制率也有提高的优势。
[0040]
制备各组细胞总蛋白质,并用bca法测定蛋白浓度,上样,电泳,电转,封闭,结合一抗,二抗,显色,用密度扫描仪全自动扫描图像分析仪,数据分析测定条带的面积和灰度值,得出积分灰度值以代表蛋白表达量,以内参蛋白β-action作为对照基础,计算xiap/β-action相对表达量,结果如图2所示。
[0041]
结果显示,实验组的xiap蛋白表达量明显减弱,与未加药的对照组相比差异具有统计学意义(p《0.05)。在200μg/ml时,xiap/β-action相对表达量达到了(0.06
±
0.02),而空白对照组和阳性对照组基本一致都在0.63左右,这也说明阳性对照组不能显著抑制xiap蛋白的表达。其靶点与本发明的靶点并不相同。
[0042]
实施例5人血白蛋白的制备
[0043]
取血浆5l,加入体积份数为95%的-15℃药用乙醇至最终乙醇浓度至20%,同时用ph4.0缓冲液调节ph6.2,血浆蛋白含量5.0%,调控温度至-5℃,搅拌2小时,静置5小时,往混合液中按20g/l加入硅藻土和珍珠岩二者组合作为助滤剂,采用加压过滤分离,收集压滤上清液用ph4.0缓冲液调节ph6.0,加入体积份数为95%的-15℃药用乙醇至最终乙醇的体积达到上一步收集的压滤上清液和药用乙醇混合液总体积的40%,调控温度至-5℃,搅拌3小时,静置6小时,往反应混悬液中按15g/l加入硅藻土或珍珠岩或二者组合作为助滤剂,采用加压过滤分离,收集压滤上清液用1~2mol/l醋酸溶液调节ph4.7,加入体积份数为95%的-15℃药用乙醇至最终乙醇的体积达到上一步收集的压滤上清液和药用乙醇混合液总体
积的40%,调控温度至-8℃,搅拌2小时,静置8小时,采用加压过滤分离,压滤上清液废弃或回收乙醇,收集压滤分离组分v沉淀进入下一步工序。将上一工序收集的组分v沉淀用4%乙醇溶液溶解,用1mol/l醋酸溶液调节ph4.5,调控温度至-2℃,静置4小时,深层过滤,收集过滤液用1mol/l醋酸溶液调节ph4.0,浓缩使制品溶液蛋白质含量8%,往制品溶液中添加质量分数为10%的氯化钠溶液,至氯化钠溶液的体积达到制品溶液和氯化钠混合液总体积的1.0%,先用5倍浓缩液体积的0.9%氯化钠溶液连续透析,接着用1倍浓缩液体积的0.5%氯化钠溶液透析至乙醇含量≤0.25%,再浓缩制品溶液至蛋白质含量≥22%以上,收集浓缩液调ph6.8,添加辛酸钠,至每克蛋白质中添加0.14克辛酸钠,60℃水浴保温10小时。用装配有0.2微米滤膜的除菌滤器将上一步巴氏灭活后蛋白溶液进行除菌过滤,保存备用。
[0044]
根据《中国药典》2015年版三部,抽样进行检测,通过免疫电泳法发现主要沉淀线为白蛋白,通过蛋白含量检测,蛋白含量达到98.7%,制备成功。
[0045]
实施例6xiap-11a6单抗介导的阿霉素白蛋白纳米粒的制备
[0046]
2mg阿霉素与15mg实施例5制备的人血清白蛋白溶解到1ml的蒸馏水中,为了使药物有效吸附到人血清白蛋白上,在室温下搅拌3h;调节ph值至9;4ml乙醇以0.5ml/min的速度滴至已经孵化好的药物与白蛋白混合溶液中继续搅拌,向纳米粒溶液中滴加10μl 8%戊二醛溶液室温磁力搅拌20h,使纳米粒交联固化,制得固化纳米粒的溶液。将纳米粒溶液以15000r/min的转速高速离心倾去上清液加水至原体积,超声分散。洗涤3次,以去除制备中加入的有机溶剂,得到阿霉素白蛋白纳米粒。
[0047]
取阿霉素白蛋白纳米粒1ml,加入250μl nhs-peg3500-mal溶液(44mg溶于500μl ph8.0的磷酸盐缓冲液中)中,20℃恒温磁力搅拌1.5h。18000离心10min弃去上清液后,再用1ml双蒸水重新分散。取1.5ml单抗缓冲液(适量单抗溶于ph8.0的磷酸盐缓冲液,单抗终浓度为1mg/ml)加入5.0μl的2-亚氨基硫烷盐酸缓冲液(6.9mg溶于50mlph8.0的磷酸盐缓冲液中)中,20℃恒温磁力搅拌1h。取前述制备的1ml巯基化的阿霉素白蛋白纳米粒,加入到1.5ml硫醇化的单抗缓冲液中,20℃恒温磁力搅拌12h,采用离心超滤法纯化。
[0048]
利用动态光散射粒度测定仪测定纳米粒的粒径大小在大约238nm左右,zeta电位为26.45mv,并且与同浓度未偶联单抗的活性相比,偶联物的抗体活性保存率》88%,表明偶联物较好地保留了原抗体的活性。
[0049]
实施例7xiap-11a6单抗介导的阿霉素白蛋白纳米粒的活性鉴定
[0050]
取babl/c裸鼠,5周龄左右,裸鼠在spf饲养,并用灭菌食物和水喂养。实验分为如下几组:
[0051]
空白对照组:注射生理盐水,不给药;
[0052]
低剂量给药组:实施例6制备的xiap-11a6单抗介导的阿霉素白蛋白纳米粒50mg/kg;
[0053]
高剂量给药组:实施例6制备的xiap-11a6单抗介导的阿霉素白蛋白纳米粒250mg/kg;
[0054]
阳性对照组:阿帕替尼50mg/kg;
[0055]
将sgc7901胃癌细胞悬浮液以5
×
106个/ml皮下接种建模,与模型建立24h后开始给药,每组10只。7d间隔给药,共给药3周。四周后将所有裸鼠脱臼处死,取出肿瘤称重。结果如表2所示。
[0056]
表2各组平均瘤重
[0057][0058]
从表2可以看出,与空白对照组相比,给药组和阳性对照组具有显著的肿瘤重量下降的趋势(**p《0.01)。采用高剂量给药,肿瘤重量只有0.016
±
0.002,抑制效果显著。
[0059]
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,但本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1