一种含硫代苯酰胺结构的喹唑啉酮类衍生物、组合物及其防治猕猴桃溃疡病的应用
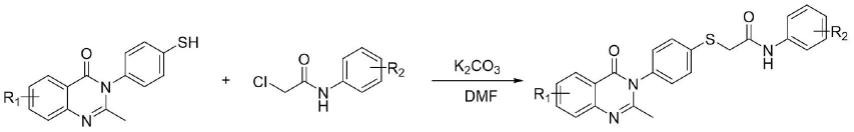
1.本发明涉及化学技术领域,具体来说涉及含硫代苯酰胺结构的喹唑啉酮类衍生物的制备方法及其组合物对猕猴桃溃疡病菌、水稻白叶枯病菌、柑橘溃疡病菌、黄瓜灰霉病菌、小麦赤霉病菌、辣椒枯萎病菌具有抑制作用的用途。
背景技术:
2.猕猴桃种植产业发展前景良好,就经济效益而言,是农民增收致富,带动农村产业发展的一个重要举措,但由于可引起猕猴桃溃疡病的丁香假单胞杆菌猕猴桃致病变种(pseudomonassyringaepv.actinidiae,psa)的存在,猕猴桃无法健康的生长,阻碍了我国乃至全世界的猕猴桃产业的发展。由于psa引起的猕猴桃溃疡病具有传播十分迅速、传播途径多、传播过程不易被发现的特点,在植株感病早期,植株一般不出现症状,等种植区出现溃疡病病症时,病情可能已经到难以控制的程度,此外,由水稻白叶枯病菌、柑橘溃疡病菌、黄瓜灰霉病菌、小麦赤霉病菌、辣椒枯萎病菌等引起的植物细菌性病害和真菌病害都是造成农业损失的主要原因,随着保护地的继续发展和高附加值作物的连年栽培,植物细菌性病害和真菌病害呈现出越来越难以控制的趋势,目前,市面上常用的抗菌剂不仅有田间防效不佳,不利于环境的可持续发展的缺点,更使细菌的耐药性不断增强,因此,研发一种高效、低毒、对环境友好的抗病毒剂和抗菌剂已刻不容缓。
3.吲哚乙酸是一种植物生长调节剂,植物生长调节剂的基本作用在于调节植物的生长,一般而言,植物生长调节的化合物在植物体内的含量极少,很难大量提取,一般通过人工合成。
4.在杂环化合物中,含氮杂环化合物占据着重要的位置,由于其存在着独特的生物活性,得到许多化学家的青睐,由于喹唑啉类杂环具有的良好生物活性和环境相容性,成为国内外研究的热点。酰胺类化合物的抑菌活性也成为农药研究者们的热点。近年来,发现含有喹唑啉酰胺类化合物具有较好的抗植物细菌性活性。
5.2022年,王琴等(王琴,张燕,饶念,等.酰胺类喹唑啉酮衍生物的合成及抗菌活性[j].化学研究与应用,2022,34(3):493~503.)设计合成了系列含酰胺结构单元的新型喹唑啉酮类化合物并进行了抑菌活性的初步筛选,通过筛选发现该类化合物具有较好的抗真菌活性。
[0006]
2007年,徐广芳等(徐广芳.新型喹唑啉类化合物的抑菌活性筛选及作用机理初步研究[d].贵州大学,2007.)采用室内生长速率法对合成的数十个喹唑啉类化合物进行了抑菌活性的初步筛选,通过筛选发现含喹唑啉母环结构的化合物具有较好的抗真菌活性,化合物6-氟-4-乙硫基喹唑啉抑菌效果最好,对小麦赤霉病原菌(g.zeae)、辣椒枯萎病原菌(f.oxysporum)、苹果腐烂病原菌(c.mandshurica)、半夏立枯病原菌(r.solani)、水稻纹枯病原菌(t.cucumeris)、马铃薯晚疫病原菌(p.infestans)、油菜菌核病原菌(s.sclerotiorum)、黄瓜灰霉病原菌(b.cinerea)、苹果炭疽病原菌(c.gloeosporioides)
九种植物病原真菌都有较好的生物活性,生物活性甚至超过了商品药剂恶霉灵。
[0007]
2020年,张贵强等(张贵强,郭晴晴,易君明,等.新型含2,4-二氯苯基的1,2,4-三唑喹唑啉衍生物的合成及抑菌活性[j].合成化学,2020(6):491-499.)合成了含2,4-二氯苯基1,2,4-三唑1,3,4-噻二嗪喹唑啉类化合物,采用浊度法测试目标化合物对柑橘溃疡病菌(xac),烟草青枯病菌(rs),水稻百叶枯病菌(xoo)的抑制活性.结果表明,部分化合物具有较好的抑菌活性,和对照药剂噻菌酮和叶枯唑的抑制率相当。
[0008]
综上所述,喹唑啉类衍生物表现出了一定的杀菌活性。为创制新型高效的抗病毒剂和杀菌剂,本发明在前期工作的基础上,设计合成了系列含硫代苯酰胺结构的喹唑啉酮类衍生物化合物,期望筛选出高活性的抗菌药物。
技术实现要素:
[0009]
本发明的一种含硫代苯酰胺结构的喹唑啉酮类衍生物及其组合物的制备方法及其防治猕猴桃溃疡病的应用。
[0010]
本发明的另一目的在于对猕猴桃溃疡病、水稻白叶枯病、柑橘溃疡病、黄瓜灰霉病、小麦赤霉病、辣椒枯萎病具有抑制作用的用途。
[0011]
本发明技术方案:一种含硫代苯酰胺结构的喹唑啉酮类衍生物,其通式为下式(i):
[0012][0013]
其中:r1为卤素、甲基、甲氧基或上述取代基团任意组合的二取代或三取代,r2为卤素的单取代或二取代。
[0014]
优选的,r1为3-甲基,3-氯,4-氯,3-甲氧基,6-甲氧基,3,4-二甲基,4-甲基,3-氟,5-氟,5-甲基,6-甲基,6-氯,5-甲氧基,4-氟,3,5-二氟,6-氟,3-甲基-5-氯;r2为4-氯,3-溴-4-氯,2-氟-4-氯,2-溴-4-氯,3-溴-4-氟。
[0015]
一种含硫代苯酰胺结构的喹唑啉酮衍生物的制备方法,包括以下步骤:
[0016]
(1)按摩尔比取代苯甲酸:原乙酸三乙酯=1:20~50投料,加热回流4-6h,待反应结束,温度降到室温后,过滤收集固体,得到取代2-甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0017][0018]
(2)按摩尔比取代2-甲基-4h-苯并[d][1,3]噁嗪-4-酮:对氨基苯硫酚:冰乙酸=1:1:20~50投料,加热回流4-6h,待反应结束,将反应体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度降到室温后,过滤收集固体,得到取代3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮。
氯-3-(4-巯基苯基)-2,8-二甲基喹唑啉-4(3h)-酮。
[0030]
(3)将6-氯-3-(4-巯基苯基)-2,8-二甲基喹唑啉-4(3h)-酮(1.00mmol),2-氯-n-(4-氯苯基)乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到2-((4-(6-氯-2,8-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)-n-(4-氯苯基)乙酰胺,收率为48.3%,熔点为175.1-176.6℃。
[0031]
实施例2:n-(3-溴-4-氯苯基)-2-((4-(5-氯-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-2),包括以下步骤:
[0032]
(1)将2-氨基-6-氯-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体5-氯-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0033]
(2)将5-氯-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到5-氯-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮。
[0034]
(3)将5-氯-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(3-溴-4-氯苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(3-溴-4-氯苯基)-2-((4-(5-氯-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为85.1%,熔点为185.3-186.5℃。
[0035]
实施例3:n-(4-氯苯基)-2-((4-(2,8-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-3),包括以下步骤:
[0036]
(1)将2-氨基-3-甲基-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体2,8-二甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0037]
(2)将2,8-二甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到3-(4-巯基苯基)-2,8-二甲基喹唑啉-4(3h)-酮。
[0038]
(3)将3-(4-巯基苯基)-2,8-二甲基喹唑啉-4(3h)-酮(1.00mmol),2-氯-n-(4-氯苯基)乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(4-氯苯基)-2-((4-(2,8-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为58.7%,熔点为266.5-267.1℃。
[0039]
实施例4:n-(3-溴-4-氯苯基)-2-((4-(5-氟-2-甲基)-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-4),包括以下步骤:
[0040]
(1)将2-氨基-6-氟-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体5-氟-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0041]
(2)将5-氟-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到5-氟-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮。
[0042]
(3)将5-氟-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(3-溴-4-氯苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(3-溴-4-氯苯基)-2-((4-(5-氟-2-甲基)-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为54.9%,216.2-217.1℃。
[0043]
实施例5:n-(4-氯-2-氟苯基)-2-((4-(5-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-5),包括以下步骤:
[0044]
(1)将2-氨基-6-甲氧基-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体5-甲氧基-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0045]
(2)将5-甲氧基-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到3-(4-巯基苯基)-5-甲氧基-2-甲基喹唑啉-4(3h)-酮。
[0046]
(3)将3-(4-巯基苯基)-5-甲氧基-2-甲基喹唑啉-4(3h)-酮(1.00mmol),2-氯-n-(4-氯-2-氟苯基)乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(4-氯-2-氟苯基)-2-((4-(5-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为24.7%,熔点为172.3-173.5℃。
[0047]
实施例6:n-(4-氯-2-氟苯基)-2-((4-(2,7,8-三甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-6),包括以下步骤:
[0048]
(1)将2-氨基-3,4-二甲基-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体2,7,8-三甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0049]
(2)将2,7,8-三甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到3-(4-巯基苯基)-2,7,8-三甲基喹唑啉-4(3h)-酮。
[0050]
(3)将3-(4-巯基苯基)-2,7,8-三甲基喹唑啉-4(3h)-酮(1.00mmol),2-氯-n-(4-氯-2-氟苯基)乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(4-氯-2-氟苯基)-2-((4-(2,7,8-三甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为24.6%,熔点为162.7-163.9℃。
[0051]
实施例7:n-(4-氯苯基)-2-((4-(2,6-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-7),包括以下步骤:
[0052]
(1)将2-氨基-5-甲基-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体2,6-二甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0053]
(2)将2,6-二甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到3-(4-巯基苯基)-2,6-二甲基喹唑啉-4(3h)-酮,收率为33.1%,熔点为187.1-188.7℃。
[0054]
(3)将3-(4-巯基苯基)-2,6-二甲基喹唑啉-4(3h)-酮(1.00mmol),2-氯-n-(4-氯苯基)乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(4-氯苯基)-2-((4-(2,6-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为85.1%,208.5-209.1℃。
[0055]
实施例8:n-(4-氯-2-氟苯基)-2-((4-(8-氟-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-8),包括以下步骤:
[0056]
(1)将2-氨基-3-氟-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体8-氟-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0057]
(2)将8-氟-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到8-氟-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮。
[0058]
(3)将8-氟-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮(1.00mmol),2-氯-n-(4-氯苯基)乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(4-氯-2-氟苯基)-2-((4-(8-氟-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为55.4%,熔点为163.1-164.5℃。
[0059]
实施例9:n-(2-溴-4-氯苯基)-2-((4-(2,6-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-9),包括以下步骤:
[0060]
(1)将2-氨基-5-甲基-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体2,6-二甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0061]
(2)将2,6-二甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到3-(4-巯基苯基)-2,6-二甲基喹唑啉-4(3h)-酮。
[0062]
(3)将3-(4-巯基苯基)-2,6-二甲基喹唑啉-4(3h)-酮(1.00mmol),n-(2-溴-4-氯苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(2-溴-4-氯苯基)-2-((4-(2,6-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)
乙酰胺,收率为47.5%,187.3-188.6℃。
[0063]
实施例10:n-(2-溴-4-氯苯基)-2-((4-(5-氟-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-10),包括以下步骤:
[0064]
(1)同实施例4(1)步;(2)同实施例4(2)步;
[0065]
(3)将5-氟-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(2-溴-4-氯苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(2-溴-4-氯苯基)-2-((4-(5-氟-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为66.9%,熔点为210.1-211.7℃。
[0066]
实施例11:n-(3-溴-4-氟苯基)-2-((4-(8-氯-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-11),包括以下步骤:
[0067]
(1)将2-氨基-3-氯-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体8-氯-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0068]
(2)将8-氯-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到8-氯-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮。
[0069]
(3)将8-氯-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(3-溴-4-氟苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(3-溴-4-氟苯基)-2-((4-(8-氯-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为55.6%,熔点为229.0-230.3℃。
[0070]
实施例12:n-(3-溴-4-氟苯基)-2-((4-(5-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-12),包括以下步骤:
[0071]
(1)将2-氨基-6-甲氧基-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体5-甲氧基-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0072]
(2)将5-甲氧基-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到3-(4-巯基苯基)-5-甲氧基-2-甲基喹唑啉-4(3h)-酮。
[0073]
(3)将3-(4-巯基苯基)-5-甲氧基-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(3-溴-4-氟苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(3-溴-4-氟苯基)-2-((4-(5-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为51.6%,熔点为159.5-160.5℃。
[0074]
实施例13:n-(3-溴-4-氟苯基)-2-((4-(6-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-13),包括以下步骤:
[0075]
(1)将2-氨基-5-甲氧基-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体6-甲氧基-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0076]
(2)将6-甲氧基-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到3-(4-巯基苯基)-6-甲氧基-2-甲基喹唑啉-4(3h)-酮。
[0077]
(3)将3-(4-巯基苯基)-6-甲氧基-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(3-溴-4-氟苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(3-溴-4-氟苯基)-2-((4-(6-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为57.7%,熔点为198.4-199.9℃。
[0078]
实施例14:n-(3-溴-4-氟苯基)-2-((4-(6-氟-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-14),包括以下步骤:
[0079]
(1)将2-氨基-5-氟-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体6-氟-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0080]
(2)将6-氟-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到6-氟-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮。
[0081]
(3)将6-氟-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(3-溴-4-氟苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(3-溴-4-氟苯基)-2-((4-(6-氟-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为40.9%,熔点为189.3-190.5℃。
[0082]
实施例15:n-(3-溴-4-氟苯基)-2-((4-(6,8-二氟-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-15),包括以下步骤:
[0083]
(1)将2-氨基-3,5-二氟-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体6,8-二氟-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0084]
(2)将6,8-二氟-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到6,8-二氟-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮。
[0085]
(3)将6,8-二氟-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(3-溴-4-氟苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(3-溴-4-氟苯基)-2-((4-(6,8-二氟-2-甲基-4-氧代喹唑啉-3(4h)-基)
苯基)硫代)乙酰胺,收率为69.3%,熔点为153.8-154.9℃。
[0086]
实施例16:n-(3-溴-4-氟苯基)-2-((4-(5-氟-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-16),包括以下步骤:
[0087]
(1)同实施例4(1)步;(2)同实施例4(2)步;
[0088]
(3)将5-氟-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(3-溴-4-氟苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(3-溴-4-氟苯基)-2-((4-(5-氟-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为64.1%,熔点为192.1-193.8℃。
[0089]
实施例17:n-(2-溴-4-氯苯基)-2-((4-(8-氯-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-17),包括以下步骤:
[0090]
(1)同实施例11(1)步;(2)同实施例11(2)步;
[0091]
(3)将8-氯-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(2-溴-4-氯苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(2-溴-4-氯苯基)-2-((4-(8-氯-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为44.1%,熔点为169.9-170.6℃。
[0092]
实施例18:n-(2-溴-4-氯苯基)-2-((4-(8-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-18),包括以下步骤:
[0093]
(1)将2-氨基-3-甲氧基-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体2,6-二甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0094]
(2)将8-甲氧基-2-甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到3-(4-巯基苯基)-8-甲氧基-2-甲基喹唑啉-4(3h)-酮。
[0095]
(3)将3-(4-巯基苯基)-8-甲氧基-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(2-溴-4-氯苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(2-溴-4-氯苯基)-2-((4-(8-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为52.3%,189.5-190.7℃。
[0096]
实施例19:n-(3-溴-4-氯苯基)-2-((4-(2,6-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-19),包括以下步骤:
[0097]
(1)同实施例9(1)步;(2)同实施例9(2)步;
[0098]
(3)将3-(4-巯基苯基)-2,6-二甲基喹唑啉-4(3h)-酮(1.00mmol),n-(3-溴-4-氯苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(3-溴-4-氯苯基)-2-((4-(2,6-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,47.5%,熔点为191.0-192.2℃。
[0099]
实施例20:n-(2-溴-4-氯苯基)-2-((4-(6-氯-2,8-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-20),包括以下步骤:
[0100]
(1)同实施例1(1)步;(2)同实施例1(2)步;
[0101]
(3)将6-氯-3-(4-巯基苯基)-2,8-二甲基喹唑啉-4(3h)-酮(1.00mmol),n-(2-溴-4-氯苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(2-溴-4-氯苯基)-2-((4-(6-氯-2,8-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为51.2%,熔点为158.5-159.4℃。
[0102]
实施例21:n-(3-溴-4-氟苯基)-2-((4-(8-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-21),包括以下步骤:
[0103]
(1)同实施例18(1)步;(2)同实施例18(1)步;
[0104]
(3)将3-(4-巯基苯基)-8-甲氧基-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(3-溴-4-氟苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(3-溴-4-氟苯基)-2-((4-(8-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为75.3%,熔点为262.3-263.1℃。
[0105]
实施例22:n-(2-溴-4-氯苯基)-2-((4-(2,8-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-22),包括以下步骤:
[0106]
(1)同实施例3(1)步;(2)同实施例3(1)步;
[0107]
(3)将3-(4-巯基苯基)-2,8-二甲基喹唑啉-4(3h)-酮(1.00mmol),n-(2-溴-4-氯苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(2-溴-4-氯苯基)-2-((4-(2,8-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为60.5%,熔点为155.2-156.6℃。
[0108]
实施例23:n-(3-溴-4-氟苯基)-2-((4-(2,8-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-23),包括以下步骤:
[0109]
(1)同实施例3(1)步;(2)同实施例3(1)步;
[0110]
(3)将3-(4-巯基苯基)-2,8-二甲基喹唑啉-4(3h)-酮(1.00mmol),n-(3-溴-4-氟苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(3-溴-4-氟苯基)-2-((4-(2,8-二甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为55.1%,熔点为230.3-231.5℃。
[0111]
实施例24:n-(2-溴-4-氯苯基)-2-((4-(5-氯-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-24),包括以下步骤:
[0112]
(1)同实施例2(1)步;(2)同实施例2(2)步;
[0113]
(3)将5-氯-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(2-溴-4-氯苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(2-溴-4-氯苯基)-2-((4-(5-氯-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫
代)乙酰胺,收率为80.9%,熔点为201.1-202.3℃。
[0114]
实施例25:n-(4-氯苯基)-2-((4-(8-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-25),包括以下步骤:
[0115]
(1)同实施例18(1)步;(2)同实施例18(1)步;
[0116]
(3)将3-(4-巯基苯基)-8-甲氧基-2-甲基喹唑啉-4(3h)-酮(1.00mmol),2-氯-n-(4-氯苯基)乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(4-氯苯基)-2-((4-(8-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为85.4%,熔点为253.7-254.9℃。
[0117]
实施例26:n-(3-溴-4-氯苯基)-2-((4-(8-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-26),包括以下步骤:
[0118]
(1)同实施例18(1)步;(2)同实施例18(1)步;
[0119]
(3)将3-(4-巯基苯基)-8-甲氧基-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(3-溴-4-氯苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(3-溴-4-氯苯基)-2-((4-(8-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为73.0%,熔点为232.1-233.3℃。
[0120]
实施例27:n-(3-溴-4-氯苯基)-2-((4-(5-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-27),包括以下步骤:
[0121]
(1)同实施例5(1)步;(2)同实施例5(1)步;
[0122]
(3)将3-(4-巯基苯基)-5-甲氧基-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(3-溴-4-氯苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(3-溴-4-氯苯基)-2-((4-(5-甲氧基-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为65.3%,熔点为204.3-205.1℃。
[0123]
实施例28:n-(4-氯苯基)-2-((4-(2,7,8-三甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-28),包括以下步骤:
[0124]
(1)将2-氨基-3,4-二甲基-苯甲酸(10.0mmol),以原乙酸三乙酯50ml为溶剂,加入到100ml三口烧瓶中回流反应4-5h,待反应结束,冷却至室温后,过滤收集固体,得到中间体2,7,8-三甲基-4h-苯并[d][1,3]噁嗪-4-酮。
[0125]
(2)将2,7,8-三甲基-4h-苯并[d][1,3]噁嗪-4-酮(1.0mmol),对氨基苯硫酚(1.0mmol),以冰乙酸30ml为溶剂,加热回流4-6h,经tlc跟踪监测反应进程,反应完毕后,将体系倒入带有磁力搅拌器的冰水中,充分搅拌。待温度将至室温后,过滤收集固体,得到3-(4-巯基苯基)-2,7,8-三甲基喹唑啉-4(3h)-酮。
[0126]
(3)将3-(4-巯基苯基)-2,7,8-三甲基喹唑啉-4(3h)-酮(1.00mmol),2-氯-n-(4-氯苯基)乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(4-氯苯基)-2-((4-(2,7,8-三甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为42.6%,熔点为186.9-187.5℃。
[0127]
实施例29:n-(3-溴-4-氯苯基)-2-((4-(8-氯-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺的合成(化合物编号为t-29),包括以下步骤:
[0128]
(1)同实施例11(1)步;(2)同实施例11(2)步;
[0129]
(3)将8-氯-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮(1.00mmol),n-(3-溴-4-氯苯基)-2-氯乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到n-(3-溴-4-氯苯基)-2-((4-(8-氯-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)乙酰胺,收率为82.3%,熔点为237.2-238.7℃。
[0130]
实施例30:2-((4-(5-氯-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)-n-(4-氯苯基)乙酰胺的合成(化合物编号为t-30),包括以下步骤:
[0131]
(1)同实施例2(1)步;(2)同实施例2(2)步;
[0132]
(3)将5-氯-3-(4-巯基苯基)-2-甲基喹唑啉-4(3h)-酮(1.00mmol),2-氯-n-(4-氯苯基)乙酰胺(1.1mmol),碳酸钾(1.5mmol),以n,n-二甲基甲酰胺20ml为溶剂,室温搅拌,tlc跟踪监测反应,待反应完成后,倒入带有磁力搅拌器的冰水中,充分搅拌,过滤收集固体,得到2-((4-(5-氯-2-甲基-4-氧代喹唑啉-3(4h)-基)苯基)硫代)-n-(4-氯苯基)乙酰胺,收率为64.4%,熔点为192.6-193.8℃。
[0133]
对上述实施例t-1~t-30合成的含硫代苯酰胺结构的喹唑啉酮类衍生物的核磁共振氢谱(1hnmr)、碳谱(
13
cnmr)和高分辨质谱(hrms)数据如表1所示。
[0134]
表1.实施例t-1~t-30化合物的波谱数据
[0135]
[0136]
[0137]
[0138]
[0139]
[0140]
[0141]
[0142]
[0143]
[0144]
[0145][0146]
实施例31:目标化合物对猕猴桃溃疡病菌、水稻白叶枯病菌、柑橘溃疡病菌的抑制活性
[0147]
(1)测试方法
[0148]
采用浊度法(yangl.;etal.,2017)测定化合物的杀菌活性。制备浓度为100μg/ml的被测化合物。配制nb培养基(3.0g牛肉提取物,5.0g蛋白胨,1.0g酵母粉,10.0g葡萄糖,1000ml蒸馏水,ph7.0-7.2),分别用接菌环划一小块含有烟草青枯病菌、魔芋软腐病菌的培养基放入两个nb培养基中,塞好塞子,在28℃,180rpm恒温摇床振荡培养到生长对数期(od=0.6-0.8)备用。取40μl的菌液、4ml水-吐温(1%吐温20)、1ml配制好的化合物溶液,将试管28
±
1℃下培养,并以180rpm连续摇动1-3天。通过测量600nm(od600)处的光密度来监测细菌的生长,但含有同样浓度的溶剂和0.1%tween20作为空白对照,叶枯唑作为对照药剂,每处理重复三次。通过以下公式计算药剂对细菌的抑制率:
[0149]
i=(ctur-ttur)/ctur
×
100%
[0150]
其中i为抑制率,ctur代表未经药物处理的试管中细菌生长的校正的浊度值(空白对照),ttur代表经化合物处理的试管中细菌生长的校正的浊度值。
[0151]
(2)生物测试结果
[0152]
表2目标化合物在100μg/ml下对猕猴桃溃疡病菌、水稻白叶枯病菌、柑橘溃疡病菌的抑制活性
[0153][0154]
在浓度为100μg/ml,以叶枯唑为对照药剂测试了目标化合物的抑菌活性,从表2生物活性测定结果可以看出含硫代苯酰胺结构的喹唑啉酮类衍生物对对猕猴桃溃疡病菌、水稻白叶枯病菌、柑橘溃疡病菌具有较好的抑制活性,其中t-11的活性最好,抑制率分别为83.5%、82.4%、78.4%,优于对照药剂叶枯唑。
[0155]
实施例32:目标化合物对黄瓜灰霉病菌、小麦赤霉病菌、辣椒枯萎病菌的抑制活性
[0156]
(1)测试方法
[0157]
采用离体生长速率法(tarun,k.c.;etal.,2006)测定化合物的抑菌活性。加热马铃薯葡萄糖琼脂培养基(pda培养基:马铃薯200g、琼脂20g、葡萄糖20g、蒸馏水1000ml)至溶融状态(40~60℃),将10ml药液(10倍终浓度的药液)倒入90mlpda培养基中,充分摇匀,均匀倒入直径9cm的培养皿内,水平放置,待冷却凝固。在已经培养4d的新鲜病原菌菌落边缘用打孔器打取直径为4mm的菌碟,将菌碟倒置于含药剂pda平板中央,然后置于27℃恒温恒湿培养箱中倒置培养,待空白对照菌落生长至接近平皿三分之二处时开始观测,十字交叉法测量菌落直径,取平均值(宋素琴,等,2004)。空白对照不加药剂,但含有同样浓度的溶剂和0.5%tween20,每处理重复三次。通过以下公式计算药剂对菌丝生长的抑制率:
[0158]
i(%)=(c-t)/(c-0.4)
×
100%
[0159]
其中i为抑制率,c为空白对照直径(cm),t为处理直径(cm)。
[0160]
(2)生物测试结果
[0161]
表3目标化合物在100μg/ml下对黄瓜灰霉病菌、小麦赤霉病菌、辣椒枯萎病菌的抑制活性
[0162]
[0163][0164]
采用离体生长速率法,在浓度为100μg/ml,以恶霉灵为对照药剂测试了目标化合物的抑菌活性,从表3生物活性测定结果可以看出含硫代苯酰胺结构的喹唑啉酮类衍生物对黄瓜灰霉病菌、小麦赤霉病菌、辣椒枯萎病菌都具有较好的抑制活性,其中t-11的活性最好,抑制率为85.6%、76.9%、72.6%,优于对照药剂叶枯唑。
[0165]
实施例33:目标化合物t-11组合物的制备
[0166]
下述所用的部分制剂通过市场购买的制剂进行浓度调节制备得到。以下实施例是对本发明的进一步说明,但本发明不局限于本实施例中的比例、制剂类型和用途。下面实施例中,目标化合物t-11和吲哚乙酸的可湿性粉剂制备复配组合物,各组合物中,目标化合物t-11和吲哚乙酸比例按照质量配比计算。根据需要制备如下目标化合物t-11和吲哚乙酸的制剂。
[0167]
组合物1:t-11:吲哚乙酸可湿性粉剂=1:1
[0168]
组合物2:t-11:吲哚乙酸可湿性粉剂=1:2
[0169]
组合物3:t-11:吲哚乙酸可湿性粉剂=2:1
[0170]
实施例34:目标化合物t-11的组合物的抗猕猴桃溃疡病活性
[0171]
按照实施例33中提到的抑菌活性测试方法对目标化合物t-11与吲哚乙酸的组合物进行抗猕猴桃溃疡病菌活性测试。
[0172]
表4药物对猕猴桃溃疡病菌的抑制活性
[0173]
[0174][0175]
采用离体生长速率法,在浓度为100μg/ml,测试了组合物的抗猕猴桃溃疡病菌活性,从表4生物活性测定结果可以看出复配组合物的抗猕猴桃溃疡病菌活性相对比复配前的化合物有所提高,组合物3(t-11:吲哚乙酸可湿性粉剂=2:1)对猕猴桃溃疡病菌的抑制活性达100.0%。因此,t-11与吲哚乙酸的复配组合物对猕猴桃溃疡病有协同增效的效果。
[0176]
本发明实施例辅以说明本发明的技术方案。本发明效果是合成路线简单、产率较高,得到新型、高效的防治猕猴桃溃疡病的新药剂。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1